{{ Ток в различных средах Работу выполнили ученики





























































montaghnik.ppt
- Размер: 6.5 Мб
- Автор:
- Количество слайдов: 67
Описание презентации {{ Ток в различных средах Работу выполнили ученики по слайдам
 {{ Ток в различных средах Работу выполнили ученики 10 класса
{{ Ток в различных средах Работу выполнили ученики 10 класса

 Прохождение электрического тока через газ называется разрядом. • Разряд, существующий при действии внешнего ионизатора, — несамостоятельный. • Если действие внешнего ионизатора продолжается, то через определенное время в газе устанавливается внутренняя ионизация (ионизация электронным ударом) и разряд становится самостоятельным.
Прохождение электрического тока через газ называется разрядом. • Разряд, существующий при действии внешнего ионизатора, — несамостоятельный. • Если действие внешнего ионизатора продолжается, то через определенное время в газе устанавливается внутренняя ионизация (ионизация электронным ударом) и разряд становится самостоятельным.
 Газы в нормальном состоянии являются диэлектриками , так как состоят из электрически нейтральных атомов и молекул и поэтому не проводят электричества. Электрический ток в газах
Газы в нормальном состоянии являются диэлектриками , так как состоят из электрически нейтральных атомов и молекул и поэтому не проводят электричества. Электрический ток в газах
 • При этом возможны два случая: • либо эти заряженные частицы создаются действием какого-нибудь внешнего фактора или вводятся в газ извне – несамостоятельная проводимость , , • либо они создаются в газе действием самого электрического поля, существующего между электродами – самостоятельная проводимость. Для того, чтобы сделать газ проводящим, нужно тем или иным способом внести в него или создать в нем свободные носители заряда – заряженные частицы.
• При этом возможны два случая: • либо эти заряженные частицы создаются действием какого-нибудь внешнего фактора или вводятся в газ извне – несамостоятельная проводимость , , • либо они создаются в газе действием самого электрического поля, существующего между электродами – самостоятельная проводимость. Для того, чтобы сделать газ проводящим, нужно тем или иным способом внести в него или создать в нем свободные носители заряда – заряженные частицы.
 • Электронный удар • Термическая ионизация • Фотоионизация • Радиоактивность Проводниками могут быть только ионизированные газы, в которых содержатся электроны, положительные и отрицательные ионы. Ионизацией называется процесс отделения электронов от атомов и молекул. Ионизация возникает под действием высоких температур и различных излучений (рентгеновских, радиоактивных, ультрафиолетовых, космических лучей), вследствие столкновения быстрых частиц или атомов с атомами и молекулами газов. Образовавшиеся электроны и ионы делают газ проводником электричества. Процессы ионизации: Электрический ток в газах
• Электронный удар • Термическая ионизация • Фотоионизация • Радиоактивность Проводниками могут быть только ионизированные газы, в которых содержатся электроны, положительные и отрицательные ионы. Ионизацией называется процесс отделения электронов от атомов и молекул. Ионизация возникает под действием высоких температур и различных излучений (рентгеновских, радиоактивных, ультрафиолетовых, космических лучей), вследствие столкновения быстрых частиц или атомов с атомами и молекулами газов. Образовавшиеся электроны и ионы делают газ проводником электричества. Процессы ионизации: Электрический ток в газах
 В зависимости от процессов образования ионов в разряде при различных давлениях газа и напряжениях, приложенных к электродам, различают несколько типов самостоятельных разрядов: тлеющий искровой коронный дуговой. Типы самостоятельных разрядов Электрический ток в газах
В зависимости от процессов образования ионов в разряде при различных давлениях газа и напряжениях, приложенных к электродам, различают несколько типов самостоятельных разрядов: тлеющий искровой коронный дуговой. Типы самостоятельных разрядов Электрический ток в газах
 Тлеющий разряд Электрический ток в газах Тлеющий разряд возникает, если давление газа низкое (от сотых долей до нескольких мм. рт. ст. ) и напряжение на электродах порядка нескольких сотен вольт. Он представляет собой слабое свечение газа, заметное только в тёмном помещении или в тёмное время суток.
Тлеющий разряд Электрический ток в газах Тлеющий разряд возникает, если давление газа низкое (от сотых долей до нескольких мм. рт. ст. ) и напряжение на электродах порядка нескольких сотен вольт. Он представляет собой слабое свечение газа, заметное только в тёмном помещении или в тёмное время суток.
 Тлеющий разряд • Его можно наблюдать в стеклянной трубке с впаянными у концов плоскими металлическими электродами. • Вблизи катода располагается тонкий светящийся слой, называемый катодной светящейся пленкой Электрический ток в газах
Тлеющий разряд • Его можно наблюдать в стеклянной трубке с впаянными у концов плоскими металлическими электродами. • Вблизи катода располагается тонкий светящийся слой, называемый катодной светящейся пленкой Электрический ток в газах
 Тлеющий разряд Электрический ток в газах применяется в светящихся трубках рекламы, заполненных неоном, аргоном, в лампах дневного света. Важнейшее современное применение тлеющий разряд получил в сравнительно недавно созданных квантовых источниках света – газовых лазерах.
Тлеющий разряд Электрический ток в газах применяется в светящихся трубках рекламы, заполненных неоном, аргоном, в лампах дневного света. Важнейшее современное применение тлеющий разряд получил в сравнительно недавно созданных квантовых источниках света – газовых лазерах.
 {{ Искровой разряд возникает в газе обычно при давлениях порядка атмосферного Р атат. . Электрический ток в газах
{{ Искровой разряд возникает в газе обычно при давлениях порядка атмосферного Р атат. . Электрический ток в газах
 Если после получения искрового разряда от мощного источника постепенно уменьшать расстояние между электродами, то разряд из прерывистого становится непрерывным возникает новая форма газового разряда, называемая дуговым разрядом. . РР атат UU =50 -100 В I = 100 АА Дуговой разряд. Электрический ток в газах
Если после получения искрового разряда от мощного источника постепенно уменьшать расстояние между электродами, то разряд из прерывистого становится непрерывным возникает новая форма газового разряда, называемая дуговым разрядом. . РР атат UU =50 -100 В I = 100 АА Дуговой разряд. Электрический ток в газах
 Электрическая дуга (дуговой разряд) В 1802 году русский физик В. В. Петров (1761 -1834) установил, что если присоединить к полюсам большой электрической батареи два кусочка древесного угля и, приведя угли в соприкосновение, слегка их раздвинуть, то между концами углей образуется яркое пламя, а сами концы углей раскалятся добела, испуская ослепительный свет.
Электрическая дуга (дуговой разряд) В 1802 году русский физик В. В. Петров (1761 -1834) установил, что если присоединить к полюсам большой электрической батареи два кусочка древесного угля и, приведя угли в соприкосновение, слегка их раздвинуть, то между концами углей образуется яркое пламя, а сами концы углей раскалятся добела, испуская ослепительный свет.
 Дуговой разряд применяется для сварки металлических деталей, для выплавки сталей и сплавов. При этом лицо сварщика или рабочего сталелитейного производства должно быть закрыто толстым тёмным стеклом, чтобы ультрафиолетовое излучение, испускаемое дугой, не повредило глаза и кожу. В мировой промышленности около 90% инструментальной стали выплавляется именно в дуговых электропечах.
Дуговой разряд применяется для сварки металлических деталей, для выплавки сталей и сплавов. При этом лицо сварщика или рабочего сталелитейного производства должно быть закрыто толстым тёмным стеклом, чтобы ультрафиолетовое излучение, испускаемое дугой, не повредило глаза и кожу. В мировой промышленности около 90% инструментальной стали выплавляется именно в дуговых электропечах.
 {{Коронный разряд возникает, если давление газа близко к атмосферному, и есть сильное неоднородное электрическое поле. Оно существует вблизи заострённых частей проводников, подключенных к высоковольтным источникам тока, а также находящихся во влажном атмосферном воздухе во время грозы. На фотографии показан коронный разряд вокруг листа растения, находящегося в высокочастотном электромагнитном поле. Электрический ток в газах
{{Коронный разряд возникает, если давление газа близко к атмосферному, и есть сильное неоднородное электрическое поле. Оно существует вблизи заострённых частей проводников, подключенных к высоковольтным источникам тока, а также находящихся во влажном атмосферном воздухе во время грозы. На фотографии показан коронный разряд вокруг листа растения, находящегося в высокочастотном электромагнитном поле. Электрический ток в газах
 {{Коронный разряд сопровождается слабым свечением и небольшим шумом. Такое свечение иногда появляется на концах корабельных мачт, и известно как «огни святого Эльма» . Особенно нежелательно возникновение этого разряда вокруг проводов высоковольтных ЛЭП, так как он приводит к потерям электрической энергии. Для предотвращения этого применяют расщепление проводов ЛЭП (на 2, 3, 5, 8 параллельно идущих проводов, разнесённых друг от друга на 40 -50 см и удерживаемых изоляционными распорками). Электрический ток в газах
{{Коронный разряд сопровождается слабым свечением и небольшим шумом. Такое свечение иногда появляется на концах корабельных мачт, и известно как «огни святого Эльма» . Особенно нежелательно возникновение этого разряда вокруг проводов высоковольтных ЛЭП, так как он приводит к потерям электрической энергии. Для предотвращения этого применяют расщепление проводов ЛЭП (на 2, 3, 5, 8 параллельно идущих проводов, разнесённых друг от друга на 40 -50 см и удерживаемых изоляционными распорками). Электрический ток в газах
 {{В некоторых случаях коронный разряд с громоотвода бывает настолько сильным, что у острия возникает явно видимое свечение. Такое свечение иногда появляется и возле других заостренных предметов, например, на концах корабельных мачт, острых верхушек деревьев, и т. д. Это явление было замечено еще несколько веков тому назад и вызывало суеверный ужас мореплавателей, не понимавших истинной его сущности «Огни святого Эльма» Электрический ток в газах
{{В некоторых случаях коронный разряд с громоотвода бывает настолько сильным, что у острия возникает явно видимое свечение. Такое свечение иногда появляется и возле других заостренных предметов, например, на концах корабельных мачт, острых верхушек деревьев, и т. д. Это явление было замечено еще несколько веков тому назад и вызывало суеверный ужас мореплавателей, не понимавших истинной его сущности «Огни святого Эльма» Электрический ток в газах
 {{ Электрический ток в газах Коронный разряд применяется в электрофильтрах для очистки газов. Трубка, заполненная дымом, внезапно делается совершенно прозрачной, если внести в неё острые металлические электроды, соединенные с высоковольтным источником тока. Если продувать через трубку струю дыма или пыли, выходящая струя воздуха станет совершенно чистой, а все мелкие частицы, содержащиеся в газе, будут осаждаться на электродах.
{{ Электрический ток в газах Коронный разряд применяется в электрофильтрах для очистки газов. Трубка, заполненная дымом, внезапно делается совершенно прозрачной, если внести в неё острые металлические электроды, соединенные с высоковольтным источником тока. Если продувать через трубку струю дыма или пыли, выходящая струя воздуха станет совершенно чистой, а все мелкие частицы, содержащиеся в газе, будут осаждаться на электродах.
 {{Электрический ток в жидкостях
{{Электрический ток в жидкостях
 Упорядоченное движение заряженных частиц называется электрическим током. В металлах заряженные частицы – электроны. Но если мы проведем опыт – то через раствор идет ток. Ещё в 1877 году шведский ученый Сванте Аррениус, изучая электропроводность растворов различных веществ, пришел к выводу, что её причиной являются ионы, которые образуются при растворении соли в воде. При растворении в воде молекула Cu. SO 44 распадается(диссоцирует) на два разнозаряженных иона – Cu (2+) и SO 44 (2 -). Электроток в растворе. Электролиты
Упорядоченное движение заряженных частиц называется электрическим током. В металлах заряженные частицы – электроны. Но если мы проведем опыт – то через раствор идет ток. Ещё в 1877 году шведский ученый Сванте Аррениус, изучая электропроводность растворов различных веществ, пришел к выводу, что её причиной являются ионы, которые образуются при растворении соли в воде. При растворении в воде молекула Cu. SO 44 распадается(диссоцирует) на два разнозаряженных иона – Cu (2+) и SO 44 (2 -). Электроток в растворе. Электролиты
 Проводят электрический ток растворы солей, щелочей, кислот. Вещества, растворы которых проводят электрический ток, называются электролитами. Растворы сахара, спирта, глюкозы и некоторых других веществ не проводят электрический ток. Вещества, растворы которых не проводят электрический ток, называются неэлектролитами.
Проводят электрический ток растворы солей, щелочей, кислот. Вещества, растворы которых проводят электрический ток, называются электролитами. Растворы сахара, спирта, глюкозы и некоторых других веществ не проводят электрический ток. Вещества, растворы которых не проводят электрический ток, называются неэлектролитами.
 Процесс распада электролита на ионы называется электролитической диссоциацией. С. Аррениус, который придерживался физической теории растворов, не учитывал взаимодействия электролита с водой и считал, что в растворах находятся свободные ионы. В отличие от него русские химики И. А. Каблуков и В. А. Кистяковский применили к объяснению электролитической диссоциации химическую теорию Д. И. Менделеева и доказали, что при растворении электролита происходит химическое взаимодействие растворённого вещества с водой, которое приводит к образованию гидратов, а затем они диссоциируют на ионы. Они считали, что в растворах находятся не свободные ионы, а гидратированные, то есть окруженные молекулами воды. Электролитическая диссоциация
Процесс распада электролита на ионы называется электролитической диссоциацией. С. Аррениус, который придерживался физической теории растворов, не учитывал взаимодействия электролита с водой и считал, что в растворах находятся свободные ионы. В отличие от него русские химики И. А. Каблуков и В. А. Кистяковский применили к объяснению электролитической диссоциации химическую теорию Д. И. Менделеева и доказали, что при растворении электролита происходит химическое взаимодействие растворённого вещества с водой, которое приводит к образованию гидратов, а затем они диссоциируют на ионы. Они считали, что в растворах находятся не свободные ионы, а гидратированные, то есть окруженные молекулами воды. Электролитическая диссоциация
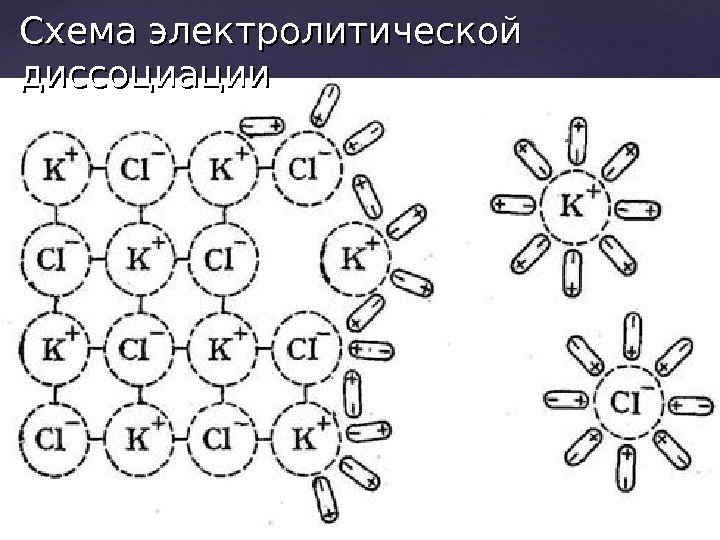
 Следовательно, диссоциация молекул электролитов происходит в следующей последовательности: а) ориентация молекул воды вокруг полюсов молекулы электролита ; ; б) гидратация молекулы электролита ; ; в) распад её на гидратированные ионы. .
Следовательно, диссоциация молекул электролитов происходит в следующей последовательности: а) ориентация молекул воды вокруг полюсов молекулы электролита ; ; б) гидратация молекулы электролита ; ; в) распад её на гидратированные ионы. .
 Схема электролитической диссоциации
Схема электролитической диссоциации
 По отношению к степени электролитической диссоциации электролиты делятся на сильные и слабые. Сильные электролиты – такие, которые при растворении практически полностью диссоциируют. У них значение степени диссоциации стремится к единице. Слабые электролиты – такие, которые при растворении почти не диссоциируют. Их степень диссоциации стремится к нулю.
По отношению к степени электролитической диссоциации электролиты делятся на сильные и слабые. Сильные электролиты – такие, которые при растворении практически полностью диссоциируют. У них значение степени диссоциации стремится к единице. Слабые электролиты – такие, которые при растворении почти не диссоциируют. Их степень диссоциации стремится к нулю.
 Из этого делаем вывод, что электрический ток в жидкостях представляет собой направленное движение не электронов, как в металлах, а гидратированных ионов, что показано на схеме. Следовательно, если в жидкости нет ионов, то и электрический ток не будет проводится. Но с появлением ионов ток будет проходить через жидкостях. Продемонстрируем это опытом. + + + — —
Из этого делаем вывод, что электрический ток в жидкостях представляет собой направленное движение не электронов, как в металлах, а гидратированных ионов, что показано на схеме. Следовательно, если в жидкости нет ионов, то и электрический ток не будет проводится. Но с появлением ионов ток будет проходить через жидкостях. Продемонстрируем это опытом. + + + — —
 Электролиз— физико-химическое явление, состоящее в выделении нана электродах составных частей растворённых веществ, являющихся результатом окислительно-восстановительных наэлектродах, которое возникает при прохожденииэлектрического токачерез раствор либо расплав электролита. . Электролиз
Электролиз— физико-химическое явление, состоящее в выделении нана электродах составных частей растворённых веществ, являющихся результатом окислительно-восстановительных наэлектродах, которое возникает при прохожденииэлектрического токачерез раствор либо расплав электролита. . Электролиз
 Упорядоченное движениеионовв проводящих жидкостях происходит в электрическом поле, которое создается электродами — проводниками, соединёнными с полюсами источника электрической энергии. Анодом называется положительный электрод, катодом — отрицательный. Положительныеионы катионы (ионыметаллов)движутся к катоду, отрицательныеионы анионы кислотных остатков и гидроксильной группы— движутся к аноду. ++ −−+ − +−+ − ++ −−
Упорядоченное движениеионовв проводящих жидкостях происходит в электрическом поле, которое создается электродами — проводниками, соединёнными с полюсами источника электрической энергии. Анодом называется положительный электрод, катодом — отрицательный. Положительныеионы катионы (ионыметаллов)движутся к катоду, отрицательныеионы анионы кислотных остатков и гидроксильной группы— движутся к аноду. ++ −−+ − +−+ − ++ −−
 Катионы активных металлов Катионы менее активных металлов Катионы неактивных металлов Li. Li ++ , Cs ++ , K, K ++ , Ca 2+2+ , , Na. Na ++ , Mg 2+2+ , Al 3+3+ Zn. Zn 2+2+ , Cr 3+3+ , Fe 2+2+ , Cd 2+2+ , , Co. Co 2+2+ , Ni 2+2+ , Sn 2+2+ , Pb 2+2+ Cu. Cu 2+2+ , , Ag. Ag ++ , Hg 2+2+ , Au 33 Тяжело разряжаются (только с расплавов) В водном растворе восстанавливаются только металл и водород Легко разряжаются и восстанавливается только металл Ряд активности металлов
Катионы активных металлов Катионы менее активных металлов Катионы неактивных металлов Li. Li ++ , Cs ++ , K, K ++ , Ca 2+2+ , , Na. Na ++ , Mg 2+2+ , Al 3+3+ Zn. Zn 2+2+ , Cr 3+3+ , Fe 2+2+ , Cd 2+2+ , , Co. Co 2+2+ , Ni 2+2+ , Sn 2+2+ , Pb 2+2+ Cu. Cu 2+2+ , , Ag. Ag ++ , Hg 2+2+ , Au 33 Тяжело разряжаются (только с расплавов) В водном растворе восстанавливаются только металл и водород Легко разряжаются и восстанавливается только металл Ряд активности металлов
 Физик Майкл Фарадей подробно изучил явление электролиза и пришел к выводу, что масса выделяющегося на электроде вещества прямо пропорциональна силе тока ( II ) и времени ( t)t). Этот закон был назван первым законом Фарадея. Закон Фарадея
Физик Майкл Фарадей подробно изучил явление электролиза и пришел к выводу, что масса выделяющегося на электроде вещества прямо пропорциональна силе тока ( II ) и времени ( t)t). Этот закон был назван первым законом Фарадея. Закон Фарадея
 Формула этого закона – m=k I I tt Где k – электрохимический эквивалент вещества. kk равно массе вещества, которая выделяется на электроде за 1 с при силе тока 1 А. Это постоянное табличное значение отличное для каждого вещества. Первый закон Фарадея
Формула этого закона – m=k I I tt Где k – электрохимический эквивалент вещества. kk равно массе вещества, которая выделяется на электроде за 1 с при силе тока 1 А. Это постоянное табличное значение отличное для каждого вещества. Первый закон Фарадея
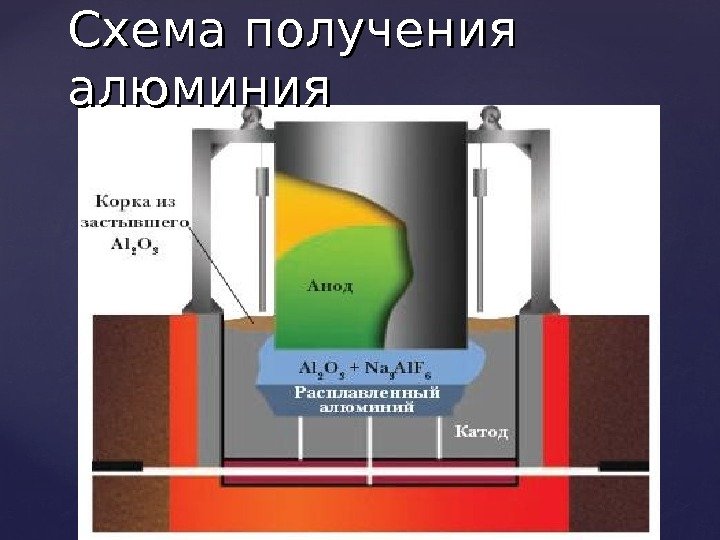
 Электролитический метод используется для получения чистых металлов. Хорошим примером является электролитическое промышленное получение алюминия. Для этого в качестве электролита используют Al. Al 22 OO 33 растворенный в расплавленном криолите (Na(Na 33 Al. F 66 ) ) при температуре 950 С. Раствор помещают в специальные электролитические ванны, где стенки и дно, выложенные графитом, используются в качестве катода, а погруженные в электролит угольные блоки. В процессе пропускания тока на катоде выделяется чистый алюминий. Аналогично (аффинаж) очищают и драгоценные металлы (золото Au Au , серебро Ag). Применение электролиза
Электролитический метод используется для получения чистых металлов. Хорошим примером является электролитическое промышленное получение алюминия. Для этого в качестве электролита используют Al. Al 22 OO 33 растворенный в расплавленном криолите (Na(Na 33 Al. F 66 ) ) при температуре 950 С. Раствор помещают в специальные электролитические ванны, где стенки и дно, выложенные графитом, используются в качестве катода, а погруженные в электролит угольные блоки. В процессе пропускания тока на катоде выделяется чистый алюминий. Аналогично (аффинаж) очищают и драгоценные металлы (золото Au Au , серебро Ag). Применение электролиза
 Схема получения алюминия
Схема получения алюминия
 Посредством электролиза можно покрыть предметы слоем того или иного металла. Этот процесс называется гальваностегией. Изделие, которое хотят покрыть слоем металла, опускают в ванну в качестве катода. В ванне раствор электролита, который содержит нужный металл. Пластина из этого же металла – анод. В процессе пропускания тока через раствор нужный металл выделяется на аноде (изделии), а пластинка (анод) постепенно растворяется. Гальваностегия
Посредством электролиза можно покрыть предметы слоем того или иного металла. Этот процесс называется гальваностегией. Изделие, которое хотят покрыть слоем металла, опускают в ванну в качестве катода. В ванне раствор электролита, который содержит нужный металл. Пластина из этого же металла – анод. В процессе пропускания тока через раствор нужный металл выделяется на аноде (изделии), а пластинка (анод) постепенно растворяется. Гальваностегия
 Гальваностегия используется для защиты металлических изделий коррозии. Гальваностегию активно используют вв ювелирном деле, ведь именно с помощью этой технологии наводят позолоту на изделия. На схеме раствор Ag. NO 3 , , катод – изделие, анод – серебренная пластина. Под действием электролиза серебро оседает на поверхности изделия.
Гальваностегия используется для защиты металлических изделий коррозии. Гальваностегию активно используют вв ювелирном деле, ведь именно с помощью этой технологии наводят позолоту на изделия. На схеме раствор Ag. NO 3 , , катод – изделие, анод – серебренная пластина. Под действием электролиза серебро оседает на поверхности изделия.
 Также с помощью электролиза можно изготовить рельефные металлические копии изделий (например, монет, медалей). Этот процесс был изобретен русским физиком и электротехником Борисом Семеновичем Якоби (1801 1874) в сороковых годах\ XIX века и называется гальванопластикой. Для изготовления рельефной копии предмета сначала делают слепок из какого-либо пластичного материала, например из = воска. Этот слепок натирают графитом и погружают в электролитическую ванну в качестве катода, где нана нём и осаждается слой металла. Это применяется вв полиграфии при изготовлении печатных форм. Гальванопластика
Также с помощью электролиза можно изготовить рельефные металлические копии изделий (например, монет, медалей). Этот процесс был изобретен русским физиком и электротехником Борисом Семеновичем Якоби (1801 1874) в сороковых годах\ XIX века и называется гальванопластикой. Для изготовления рельефной копии предмета сначала делают слепок из какого-либо пластичного материала, например из = воска. Этот слепок натирают графитом и погружают в электролитическую ванну в качестве катода, где нана нём и осаждается слой металла. Это применяется вв полиграфии при изготовлении печатных форм. Гальванопластика
 Кроме указанных выше , электролиз нашел применение и в других областях: получение оксидных защитных пленок на металлах (анодирование); электрохимическая обработка поверхности металлического изделия (полировка); электрохимическое окрашивание металлов (например, меди, латуни, цинка, хрома и др. ); очистка воды – удаление из нее растворимых примесей. В результате получается так называемая мягкая вода (по своим свойствам приближающаяся к дистиллированной); электрохимическая заточка режущих инструментов (например, хирургических ножей, бритв и т. д. ).
Кроме указанных выше , электролиз нашел применение и в других областях: получение оксидных защитных пленок на металлах (анодирование); электрохимическая обработка поверхности металлического изделия (полировка); электрохимическое окрашивание металлов (например, меди, латуни, цинка, хрома и др. ); очистка воды – удаление из нее растворимых примесей. В результате получается так называемая мягкая вода (по своим свойствам приближающаяся к дистиллированной); электрохимическая заточка режущих инструментов (например, хирургических ножей, бритв и т. д. ).
 {{ Презентация на тему: ““ Электрический ток в жидкостях ””
{{ Презентация на тему: ““ Электрический ток в жидкостях ””
 Электролитическая диссоциация По электрическим свойствам все жидкости можно разделить на 2 группы: ЖИДКОСТИ ПРОВОДЯЩИЕ НЕПРОВОДЯЩИЕ Содержащие свободные заряженные частицы (диссоциирующие) — электролиты Не содержащие свободные заряженные частицы (недиссоциирующие) К ним относятся растворы (чаще всего водные) и расплавы солей, кислот и оснований К ним относятся дистилированная вода, спирт, минеральное масло…
Электролитическая диссоциация По электрическим свойствам все жидкости можно разделить на 2 группы: ЖИДКОСТИ ПРОВОДЯЩИЕ НЕПРОВОДЯЩИЕ Содержащие свободные заряженные частицы (диссоциирующие) — электролиты Не содержащие свободные заряженные частицы (недиссоциирующие) К ним относятся растворы (чаще всего водные) и расплавы солей, кислот и оснований К ним относятся дистилированная вода, спирт, минеральное масло…
 Электролиты – растворы солей, кислот и щелочей. Электролитическая диссоциация -распад нейтральных молекул вещества в растворителе на положительные и отрицательные ионы. Степень диссоциации – отношение числа молекул, диссоциировавших на ионы, к общему количеству молекул данного вещества. Рекомбинация – процесс объединения ионов разных знаков в нейтральные молекулы. Электролиты обладают ионной проводимостью. При ионной проводимости прохождение тока сопровождается переносом вещества.
Электролиты – растворы солей, кислот и щелочей. Электролитическая диссоциация -распад нейтральных молекул вещества в растворителе на положительные и отрицательные ионы. Степень диссоциации – отношение числа молекул, диссоциировавших на ионы, к общему количеству молекул данного вещества. Рекомбинация – процесс объединения ионов разных знаков в нейтральные молекулы. Электролиты обладают ионной проводимостью. При ионной проводимости прохождение тока сопровождается переносом вещества.
 По отношению к степени электролитической диссоциации электролиты делятся на сильные и слабые. Сильные электролиты – такие, которые при растворении практически полностью диссоциируют. У них значение степени диссоциации стремится к единице. Слабые электролиты – такие, которые при растворении почти не диссоциируют. Их степень диссоциации стремится к нулю.
По отношению к степени электролитической диссоциации электролиты делятся на сильные и слабые. Сильные электролиты – такие, которые при растворении практически полностью диссоциируют. У них значение степени диссоциации стремится к единице. Слабые электролиты – такие, которые при растворении почти не диссоциируют. Их степень диссоциации стремится к нулю.
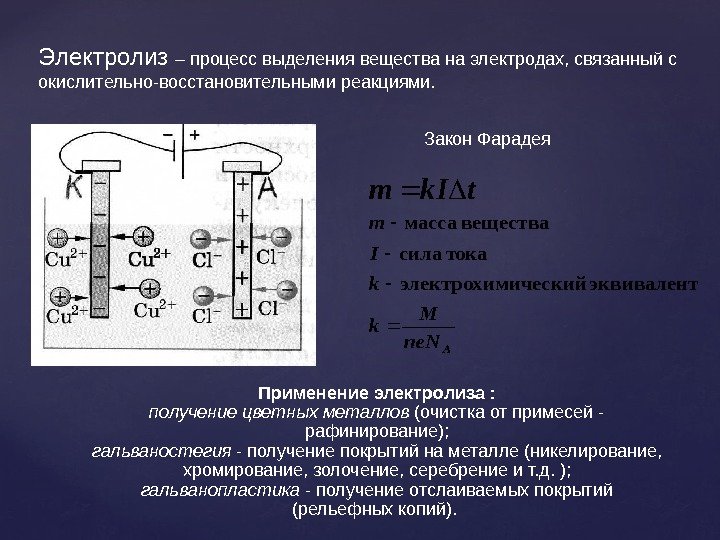
 Электролиз – процесс выделения вещества на электродах, связанный с окислительно-восстановительными реакциями. Закон Фарадея. Ane. N M k k I m tk. Im эквивалент ическийэлектрохим тока сила вещества масса Применение электролиза : получение цветных металлов (очистка от примесей — рафинирование); гальваностегия — получение покрытий на металле (никелирование, хромирование, золочение, серебрение и т. д. ); гальванопластика — получение отслаиваемых покрытий (рельефных копий).
Электролиз – процесс выделения вещества на электродах, связанный с окислительно-восстановительными реакциями. Закон Фарадея. Ane. N M k k I m tk. Im эквивалент ическийэлектрохим тока сила вещества масса Применение электролиза : получение цветных металлов (очистка от примесей — рафинирование); гальваностегия — получение покрытий на металле (никелирование, хромирование, золочение, серебрение и т. д. ); гальванопластика — получение отслаиваемых покрытий (рельефных копий).
 {{Ток в вакууме
{{Ток в вакууме
 Что такое вакуум? — это такая степень разрежения газа, при которой соударений молекул практически нет. — электрический ток невозможен, т. к. возможное количество ионизированных молекул не может обеспечить электропроводность; — создать эл. ток в вакууме можно, если использовать источник заряженных частиц; — действие источника заряженных частиц может быть основано на явлении термоэлектронной эмиссии.
Что такое вакуум? — это такая степень разрежения газа, при которой соударений молекул практически нет. — электрический ток невозможен, т. к. возможное количество ионизированных молекул не может обеспечить электропроводность; — создать эл. ток в вакууме можно, если использовать источник заряженных частиц; — действие источника заряженных частиц может быть основано на явлении термоэлектронной эмиссии.
 Термоэлектронная эмиссия — это испускание электронов твердыми или жидкими телами при их нагревании до температур, соответствующих видимому свечению раскаленного металла. Нагретый металлический электрод непрерывно испускает электроны, образуя вокруг себя электронное облако. В равновесном состоянии число электронов, покинувших электрод, равно числу электронов, возвратившихся на него ( т. к. электрод при потере электронов заряжается положительно). Чем выше температура металла, тем выше плотность электронного облака.
Термоэлектронная эмиссия — это испускание электронов твердыми или жидкими телами при их нагревании до температур, соответствующих видимому свечению раскаленного металла. Нагретый металлический электрод непрерывно испускает электроны, образуя вокруг себя электронное облако. В равновесном состоянии число электронов, покинувших электрод, равно числу электронов, возвратившихся на него ( т. к. электрод при потере электронов заряжается положительно). Чем выше температура металла, тем выше плотность электронного облака.
 {{ Электрический ток в вакууме возможен в электронных лампах. Электронная лампа — это устройство, в котором применяется явление термоэлектронной эмиссии. Вакуумный диод — это двухэлектродная ( А- анод и К — катод ) электронная лампа. Внутри стеклянного баллона создается очень низкое давление Н — нить накала, помещенная внутрь катода для его нагревания. Поверхность нагретого катода испускает электроны. Если анод соединен с + источника тока, а катод с -, то в цепи протекает постоянный термоэлектронный ток. Вакуумный диод обладает односторонней проводимостью. Т. е. ток в аноде возможен, если потенциал анода выше потенциала катода. В этом случае электроны из электронного облака притягиваются к аноду, создавая эл. ток в вакууме. Вакуумны й диод
{{ Электрический ток в вакууме возможен в электронных лампах. Электронная лампа — это устройство, в котором применяется явление термоэлектронной эмиссии. Вакуумный диод — это двухэлектродная ( А- анод и К — катод ) электронная лампа. Внутри стеклянного баллона создается очень низкое давление Н — нить накала, помещенная внутрь катода для его нагревания. Поверхность нагретого катода испускает электроны. Если анод соединен с + источника тока, а катод с -, то в цепи протекает постоянный термоэлектронный ток. Вакуумный диод обладает односторонней проводимостью. Т. е. ток в аноде возможен, если потенциал анода выше потенциала катода. В этом случае электроны из электронного облака притягиваются к аноду, создавая эл. ток в вакууме. Вакуумны й диод
 Вольтамперная характеристика вакуумного диода. При малых напряжениях на аноде не все электроны, испускаемые катодом, достигают анода, и электрический ток небольшой. При больших напряжениях ток достигает насыщения, т. е. максимального значения.
Вольтамперная характеристика вакуумного диода. При малых напряжениях на аноде не все электроны, испускаемые катодом, достигают анода, и электрический ток небольшой. При больших напряжениях ток достигает насыщения, т. е. максимального значения.
 Электронные пучки — это поток быстро летящих электронов в электронных лампах и газоразрядных устройствах. Свойства электронных пучков: — отклоняются в электрических полях; — отклоняются в магнитных полях под действием силы Лоренца; — при торможении пучка, попадающего на вещество возникает рентгеновское излучение; — вызывает свечение ( люминесценцию ) некоторых твердых и жидких тел ( люминофоров ); — нагревают вещество, попадая на него. Устройство для формирования электронного пучка
Электронные пучки — это поток быстро летящих электронов в электронных лампах и газоразрядных устройствах. Свойства электронных пучков: — отклоняются в электрических полях; — отклоняются в магнитных полях под действием силы Лоренца; — при торможении пучка, попадающего на вещество возникает рентгеновское излучение; — вызывает свечение ( люминесценцию ) некоторых твердых и жидких тел ( люминофоров ); — нагревают вещество, попадая на него. Устройство для формирования электронного пучка
 — используются явления термоэлектронной эмиссии и свойства электронных пучков. -ЭЛТ состоит из электронной пушки, горизонтальных и вертикальных отклоняющих пластин-электродов и экрана. -В электронной пушке электроны, испускаемые подогревным катодом, проходят через управляющий электрод-сетку и ускоряются анодами. Электронная пушка фокусирует электронный пучок в точку и изменяет яркость свечения на экране. Отклоняющие горизонтальные и вертикальные пластины позволяют перемещать электронный пучок на экране в любую точку экрана. Экран трубки покрыт люминофором, который начинает светиться при бомбардировке его электронами. Электронно — лучевая трубка ( ЭЛТ )
— используются явления термоэлектронной эмиссии и свойства электронных пучков. -ЭЛТ состоит из электронной пушки, горизонтальных и вертикальных отклоняющих пластин-электродов и экрана. -В электронной пушке электроны, испускаемые подогревным катодом, проходят через управляющий электрод-сетку и ускоряются анодами. Электронная пушка фокусирует электронный пучок в точку и изменяет яркость свечения на экране. Отклоняющие горизонтальные и вертикальные пластины позволяют перемещать электронный пучок на экране в любую точку экрана. Экран трубки покрыт люминофором, который начинает светиться при бомбардировке его электронами. Электронно — лучевая трубка ( ЭЛТ )
 {{ {{ Основное применение ЭЛТ: кинескопы в телеаппаратуре; дисплеи ЭВМ; электронные осциллографы в измерительной технике. с электростатическим управлением электронного пучка (отклонение эл. пучка только лишь эл. полем) с электромагнитным управлением (добавляются магнитные отклоняющие катушки ). Существуют два вида трубок
{{ {{ Основное применение ЭЛТ: кинескопы в телеаппаратуре; дисплеи ЭВМ; электронные осциллографы в измерительной технике. с электростатическим управлением электронного пучка (отклонение эл. пучка только лишь эл. полем) с электромагнитным управлением (добавляются магнитные отклоняющие катушки ). Существуют два вида трубок
 Полупроводники
Полупроводники
 Полупроводники Непроводники (диэлектрики) Проводники Прежде всего поясним само понятие – полупроводник. По способности проводить электрические заряды вещества условно делятся на проводники и непроводники электричества. Тела и вещества, в которых можно создавать электрический ток, называют проводниками. Тела и вещества, в которых нельзя создавать электрический ток , называют непроводниками тока. Металлы , уголь, кислоты, растворы солей, щелочи, живые организмы и многие другие тела и вещества. Воздух, стекло, парафин, слюда, лаки, фарфор, резина, пластмассы, различные смолы, маслянистые жидкости, сухое дерево, сухая ткань, бумага и другие вещества. Проводники Непроводники (диэлектрики) Полупроводники по электропроводности занимают промежуточное место между проводниками и непроводниками.
Полупроводники Непроводники (диэлектрики) Проводники Прежде всего поясним само понятие – полупроводник. По способности проводить электрические заряды вещества условно делятся на проводники и непроводники электричества. Тела и вещества, в которых можно создавать электрический ток, называют проводниками. Тела и вещества, в которых нельзя создавать электрический ток , называют непроводниками тока. Металлы , уголь, кислоты, растворы солей, щелочи, живые организмы и многие другие тела и вещества. Воздух, стекло, парафин, слюда, лаки, фарфор, резина, пластмассы, различные смолы, маслянистые жидкости, сухое дерево, сухая ткань, бумага и другие вещества. Проводники Непроводники (диэлектрики) Полупроводники по электропроводности занимают промежуточное место между проводниками и непроводниками.
 Период Группа III IV Y VI VII 1 2 B C N O F 3 Al Si P S Cl 4 Ga Ge As Se Br 5 In Sn Sb Te I 6 Tl Pb Bi Po Al Бор B, углерод C, кремний Si фосфор Р, сера S, германий Ge, мышьяк As , селен Se, олово Sn , сурьма Sb, теллур Te и йод I. Полупроводники — это ряд элементов таблицы Менделеева, большинство минералов, различные окислы, сульфиды, теллуриды и другие химические соединения. Полупроводники
Период Группа III IV Y VI VII 1 2 B C N O F 3 Al Si P S Cl 4 Ga Ge As Se Br 5 In Sn Sb Te I 6 Tl Pb Bi Po Al Бор B, углерод C, кремний Si фосфор Р, сера S, германий Ge, мышьяк As , селен Se, олово Sn , сурьма Sb, теллур Te и йод I. Полупроводники — это ряд элементов таблицы Менделеева, большинство минералов, различные окислы, сульфиды, теллуриды и другие химические соединения. Полупроводники
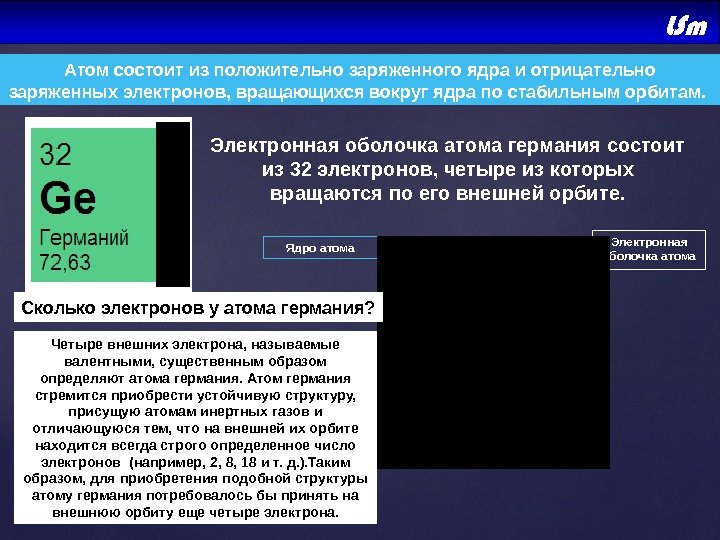
 Атом состоит из положительно заряженного ядра и отрицательно заряженных электронов, вращающихся вокруг ядра по стабильным орбитам. Электронная оболочка атома германия состоит из 32 электронов, четыре из которых вращаются по его внешней орбите. Ge Электронная оболочка атома. Ядро атома Сколько электронов у атома германия? Четыре внешних электрона, называемые валентными, существенным образом определяют атома германия. Атом германия стремится приобрести устойчивую структуру, присущую атомам инертных газов и отличающуюся тем, что на внешней их орбите находится всегда строго определенное число электронов (например, 2, 8, 18 и т. д. ). Таким образом, для приобретения подобной структуры атому германия потребовалось бы принять на внешнюю орбиту еще четыре электрона.
Атом состоит из положительно заряженного ядра и отрицательно заряженных электронов, вращающихся вокруг ядра по стабильным орбитам. Электронная оболочка атома германия состоит из 32 электронов, четыре из которых вращаются по его внешней орбите. Ge Электронная оболочка атома. Ядро атома Сколько электронов у атома германия? Четыре внешних электрона, называемые валентными, существенным образом определяют атома германия. Атом германия стремится приобрести устойчивую структуру, присущую атомам инертных газов и отличающуюся тем, что на внешней их орбите находится всегда строго определенное число электронов (например, 2, 8, 18 и т. д. ). Таким образом, для приобретения подобной структуры атому германия потребовалось бы принять на внешнюю орбиту еще четыре электрона.
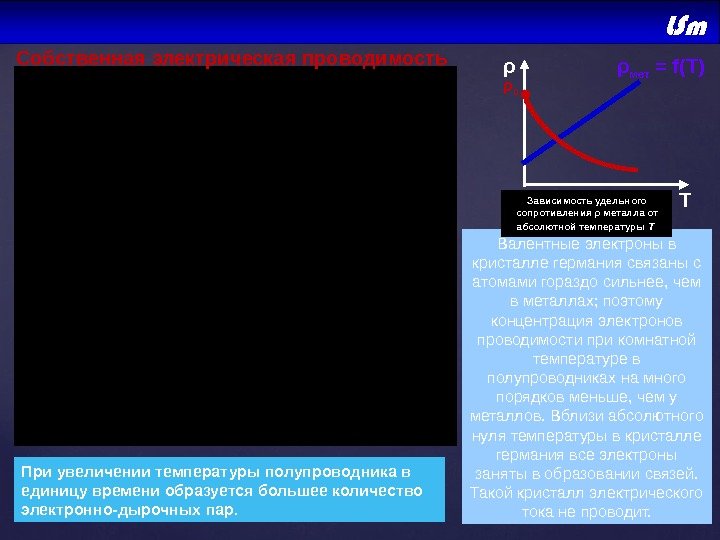
 Тρ ρ 0 • При повышении температуры некоторая часть валентных электронов может получить энергию, достаточную для разрыва ковалентных связей. Тогда в кристалле возникнут свободные электроны (электроны проводимости). Одновременно в местах разрыва связей образуются вакансии, которые не заняты электронами. Эти вакансии получили название дырок. ρ мет = f( Т ) ρ полуп = f( Т ) Повысим температуру полупроводника. Валентные электроны в кристалле германия связаны с атомами гораздо сильнее, чем в металлах; поэтому концентрация электронов проводимости при комнатной температуре в полупроводниках на много порядков меньше, чем у металлов. Вблизи абсолютного нуля температуры в кристалле германия все электроны заняты в образовании связей. Такой кристалл электрического тока не проводит. При увеличении температуры полупроводника в единицу времени образуется большее количество электронно-дырочных пар. ? Зависимость удельного сопротивления ρ металла от абсолютной температуры T Собственная электрическая проводимость
Тρ ρ 0 • При повышении температуры некоторая часть валентных электронов может получить энергию, достаточную для разрыва ковалентных связей. Тогда в кристалле возникнут свободные электроны (электроны проводимости). Одновременно в местах разрыва связей образуются вакансии, которые не заняты электронами. Эти вакансии получили название дырок. ρ мет = f( Т ) ρ полуп = f( Т ) Повысим температуру полупроводника. Валентные электроны в кристалле германия связаны с атомами гораздо сильнее, чем в металлах; поэтому концентрация электронов проводимости при комнатной температуре в полупроводниках на много порядков меньше, чем у металлов. Вблизи абсолютного нуля температуры в кристалле германия все электроны заняты в образовании связей. Такой кристалл электрического тока не проводит. При увеличении температуры полупроводника в единицу времени образуется большее количество электронно-дырочных пар. ? Зависимость удельного сопротивления ρ металла от абсолютной температуры T Собственная электрическая проводимость
 Электронно-дырочный механизм проводимости проявляется только у чистых (т. е. без примесей) полупроводников и поэтому называется собственной электрической проводимостью. Собственная (электронно-дырочная) электрическая проводимость. Примесная (электронно-дырочная) электрическая проводимость. Проводимость полупроводников при наличии примесей называется примесной проводимостью. Примесная (электронная) электрическая проводимость. Примесная (дырочная) электрическая проводимость. Изменяя концентрацию примесей, можно значительно увеличивать число носителей зарядов того или иного знака и создавать полупроводники с преимущественной концентрацией либо отрицательно, либо положительно заряженных носителей. Примесными центрами могут быть: атомы или ионы химических элементов, внедренные в решетку полупроводника; избыточные атомы или ионы, внедренные в междоузлия решетки; различного рода другие дефекты и искажения в кристаллической решетке: пустые узлы, трещины, сдвиги, возникающие при деформациях кристаллов, и др.
Электронно-дырочный механизм проводимости проявляется только у чистых (т. е. без примесей) полупроводников и поэтому называется собственной электрической проводимостью. Собственная (электронно-дырочная) электрическая проводимость. Примесная (электронно-дырочная) электрическая проводимость. Проводимость полупроводников при наличии примесей называется примесной проводимостью. Примесная (электронная) электрическая проводимость. Примесная (дырочная) электрическая проводимость. Изменяя концентрацию примесей, можно значительно увеличивать число носителей зарядов того или иного знака и создавать полупроводники с преимущественной концентрацией либо отрицательно, либо положительно заряженных носителей. Примесными центрами могут быть: атомы или ионы химических элементов, внедренные в решетку полупроводника; избыточные атомы или ионы, внедренные в междоузлия решетки; различного рода другие дефекты и искажения в кристаллической решетке: пустые узлы, трещины, сдвиги, возникающие при деформациях кристаллов, и др.
 Электронная проводимость возникает, когда в кристалл германия с четырехвалентными атомами введены пятивалентные атомы (например, атомы мышьяка, As). Дальнейшее содержание слайда в полной версии презентации.
Электронная проводимость возникает, когда в кристалл германия с четырехвалентными атомами введены пятивалентные атомы (например, атомы мышьяка, As). Дальнейшее содержание слайда в полной версии презентации.
 Полупроводник с избыточными электронами проводимости называют полупроводником n-типа , с избыточными дырками полупроводником р-типа.
Полупроводник с избыточными электронами проводимости называют полупроводником n-типа , с избыточными дырками полупроводником р-типа.
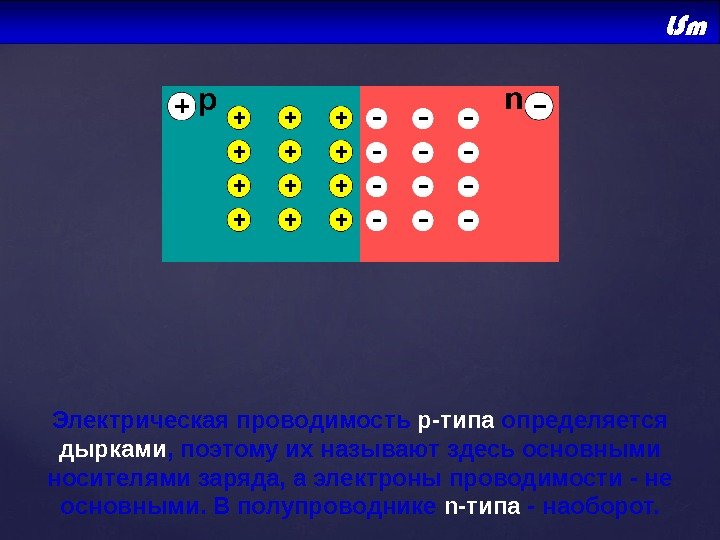
 Электрическая проводимость р-типа определяется дырками , поэтому их называют здесь основными носителями заряда, а электроны проводимости — не основными. В полупроводнике n-типа — наоборот.
Электрическая проводимость р-типа определяется дырками , поэтому их называют здесь основными носителями заряда, а электроны проводимости — не основными. В полупроводнике n-типа — наоборот.
 Дальнейшее содержание слайда в полной версии презентации.
Дальнейшее содержание слайда в полной версии презентации.
 Дальнейшее содержание слайда в полной версии презентации.
Дальнейшее содержание слайда в полной версии презентации.
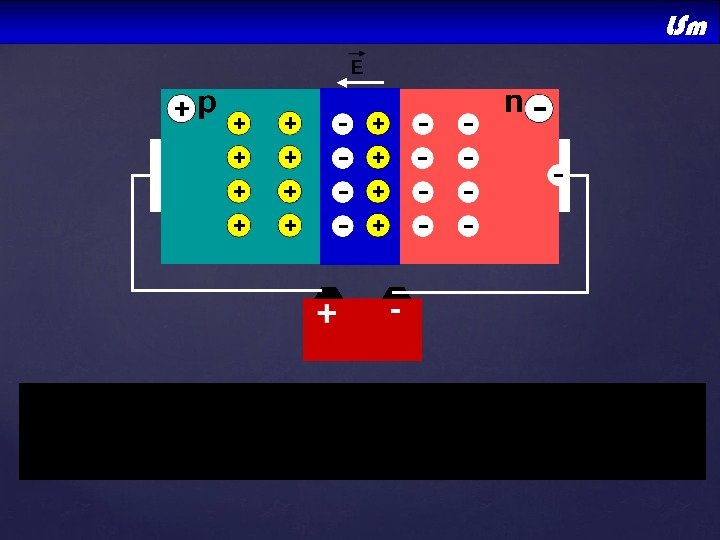
 Способность n–p-перехода пропускать ток практически только в одном направлении используется в приборах, которые называются полупроводниковыми диодами. Полупроводниковые диоды изготавливают из кристаллов кремния или германия. При их изготовлении в кристалл c каким-либо типом проводимости вплавляют примесь, обеспечивающую другой тип проводимости. Изображают полупроводниковые диоды на электрических схемах в виде треугольника и отрезка, проведенного через одну из его вершин параллельно противолежащей стороне. В зависимости от назначения диода его обозначение может содержать дополнительные символы. В любом случае острая вершина треугольника указывает на направление протекания прямого тока через диод. Треугольник соответствует р-области и называется иногда анодом, или эмиттером, а прямолинейный отрезок — n-области и называется катодом, или базой. База Б Эмиттер Э
Способность n–p-перехода пропускать ток практически только в одном направлении используется в приборах, которые называются полупроводниковыми диодами. Полупроводниковые диоды изготавливают из кристаллов кремния или германия. При их изготовлении в кристалл c каким-либо типом проводимости вплавляют примесь, обеспечивающую другой тип проводимости. Изображают полупроводниковые диоды на электрических схемах в виде треугольника и отрезка, проведенного через одну из его вершин параллельно противолежащей стороне. В зависимости от назначения диода его обозначение может содержать дополнительные символы. В любом случае острая вершина треугольника указывает на направление протекания прямого тока через диод. Треугольник соответствует р-области и называется иногда анодом, или эмиттером, а прямолинейный отрезок — n-области и называется катодом, или базой. База Б Эмиттер Э
 По конструкции полупроводниковые диоды могут быть плоскостными или точечными. Как правило, диоды изготавливают из кристалла германия или кремния, с проводимостью n-типа. В одну из поверхностей кристалла вплавляют каплю индия. Вследствие диффузии атомов индия в глубь второго кристалла, в нём образуется область p-типа. Остальная часть кристалла по-прежнему имеет проводимость n-типа. Между ними и возникает p-n — переход. Для предотвращения воздействия влаги и света, а также для прочности кристалл заключают в корпус, снабжая контактами. Германиевые и кремниевые диоды могут работать в разных интервалах температур и с токами различной силы и напряжения.
По конструкции полупроводниковые диоды могут быть плоскостными или точечными. Как правило, диоды изготавливают из кристалла германия или кремния, с проводимостью n-типа. В одну из поверхностей кристалла вплавляют каплю индия. Вследствие диффузии атомов индия в глубь второго кристалла, в нём образуется область p-типа. Остальная часть кристалла по-прежнему имеет проводимость n-типа. Между ними и возникает p-n — переход. Для предотвращения воздействия влаги и света, а также для прочности кристалл заключают в корпус, снабжая контактами. Германиевые и кремниевые диоды могут работать в разных интервалах температур и с токами различной силы и напряжения.
 Прямой ток Обратный ток Пробой U , ВI , м AОбъясняется это тем, что электроны приобретают большую скорость и, ударяясь об атомы, выбивают их них электроны. Если напряжение не увеличивать, диод останется исправным. Если же продолжать увеличивать напряжение, то электрический пробой переходит в тепловой пробой. Это значит, что диод нагревается, и ток резко увеличивается за счет выхода электронов из своих атомов при повышении температуры. Тепловой пробой разрушает полупроводник, диод неисправен. Обратный ток очень мал и почти не зависит от величины обратного напряжения, т. к. он образован дрейфовым током (не основными носителями зарядов). Но при определенном напряжении обратный ток резко возрастает. Это явление называется электрическим пробоем.
Прямой ток Обратный ток Пробой U , ВI , м AОбъясняется это тем, что электроны приобретают большую скорость и, ударяясь об атомы, выбивают их них электроны. Если напряжение не увеличивать, диод останется исправным. Если же продолжать увеличивать напряжение, то электрический пробой переходит в тепловой пробой. Это значит, что диод нагревается, и ток резко увеличивается за счет выхода электронов из своих атомов при повышении температуры. Тепловой пробой разрушает полупроводник, диод неисправен. Обратный ток очень мал и почти не зависит от величины обратного напряжения, т. к. он образован дрейфовым током (не основными носителями зарядов). Но при определенном напряжении обратный ток резко возрастает. Это явление называется электрическим пробоем.
 Переменный ток Рассмотрим понятие «переменный ток» на самом простом уровне. Перем нный ток ее — электрический ток, который периодически изменяется по модулю и направлению. Чем быстрее вращается рамка, тем больше частота переменного тока. В электроэнергетических системах России и большинства стран мира принята стандартная частота f = 50 Гц, в США 60 Гц . В технике связи применяются переменный ток высокой частоты (от 100 к. Гц до 30 ГГц). Для специальных целей в промышленности, медицине и др. отраслях науки и техники используют переменный ток самых различных частот. I I t t. T Синусоидальный характер Т – период переменного тока. Это наименьший промежуток времени (выраженный в секундах ) , через который изменения силы тока (и напряжения) повторяются
Переменный ток Рассмотрим понятие «переменный ток» на самом простом уровне. Перем нный ток ее — электрический ток, который периодически изменяется по модулю и направлению. Чем быстрее вращается рамка, тем больше частота переменного тока. В электроэнергетических системах России и большинства стран мира принята стандартная частота f = 50 Гц, в США 60 Гц . В технике связи применяются переменный ток высокой частоты (от 100 к. Гц до 30 ГГц). Для специальных целей в промышленности, медицине и др. отраслях науки и техники используют переменный ток самых различных частот. I I t t. T Синусоидальный характер Т – период переменного тока. Это наименьший промежуток времени (выраженный в секундах ) , через который изменения силы тока (и напряжения) повторяются
 Выпрямление переменного тока
Выпрямление переменного тока
 + — ~ R н + — I I t t. T/2 Далее процесс повторяется… Переменный ток
+ — ~ R н + — I I t t. T/2 Далее процесс повторяется… Переменный ток

