Thermus thermophilis 70 S (Yusupov et. al,















57-2.pptx
- Размер: 6.0 Мб
- Автор:
- Количество слайдов: 44
Описание презентации Thermus thermophilis 70 S (Yusupov et. al, по слайдам
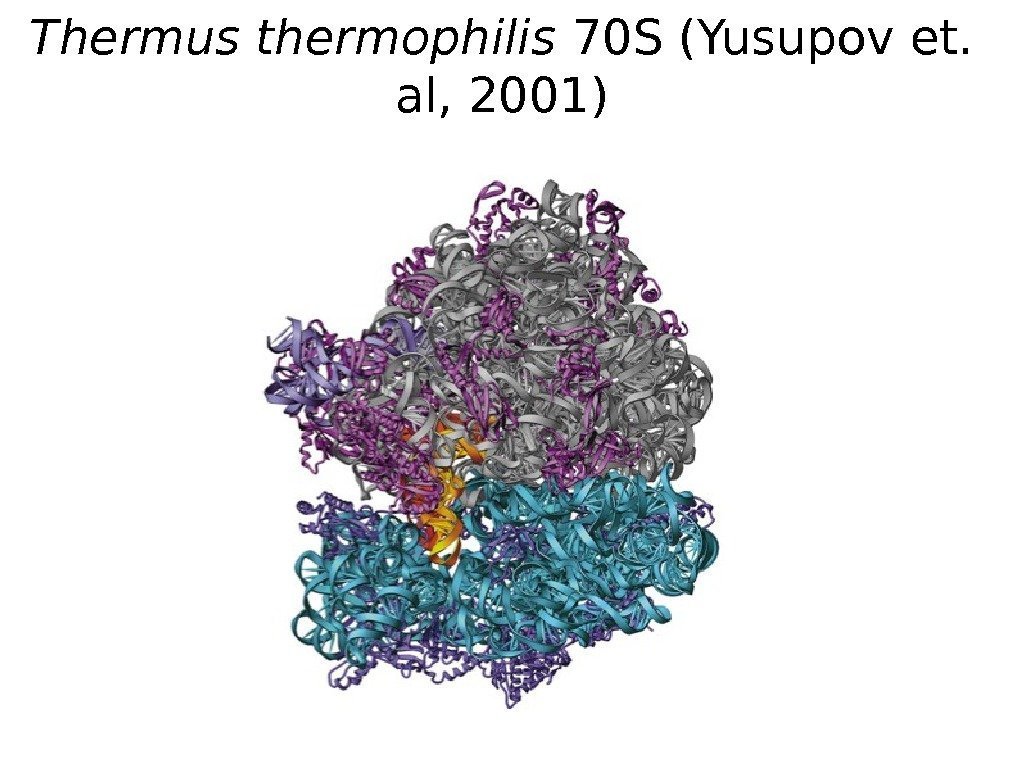
 Thermus thermophilis 70 S (Yusupov et. al, 2001)
Thermus thermophilis 70 S (Yusupov et. al, 2001)
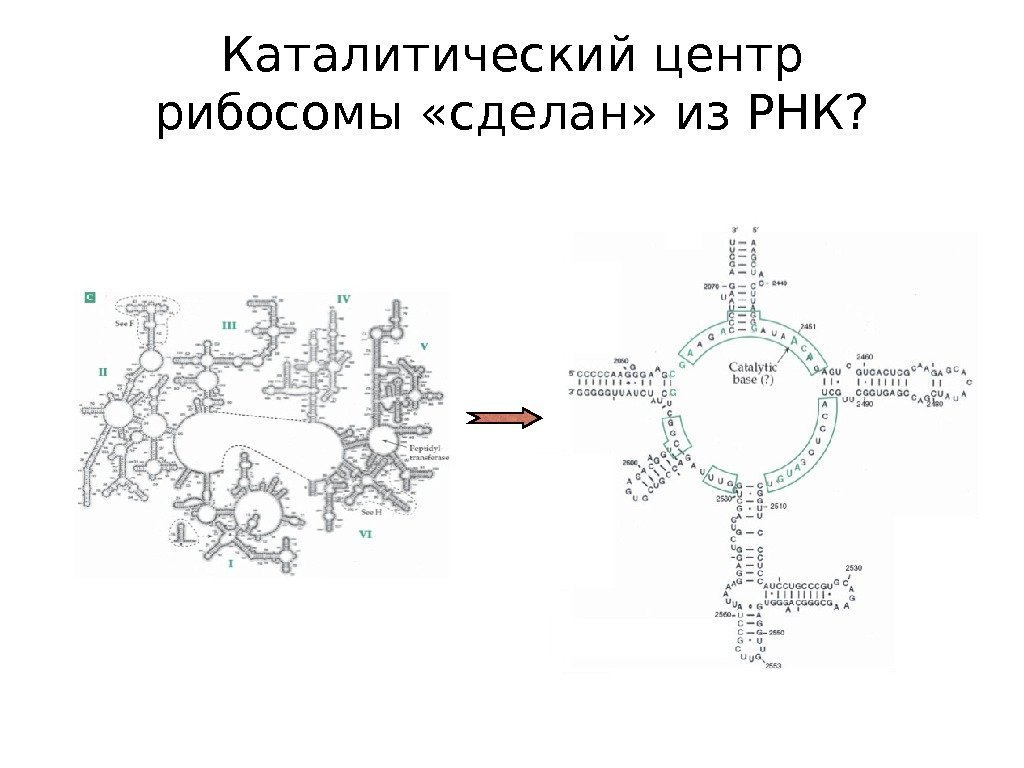
 Каталитический центр рибосомы «сделан» из РНК?
Каталитический центр рибосомы «сделан» из РНК?
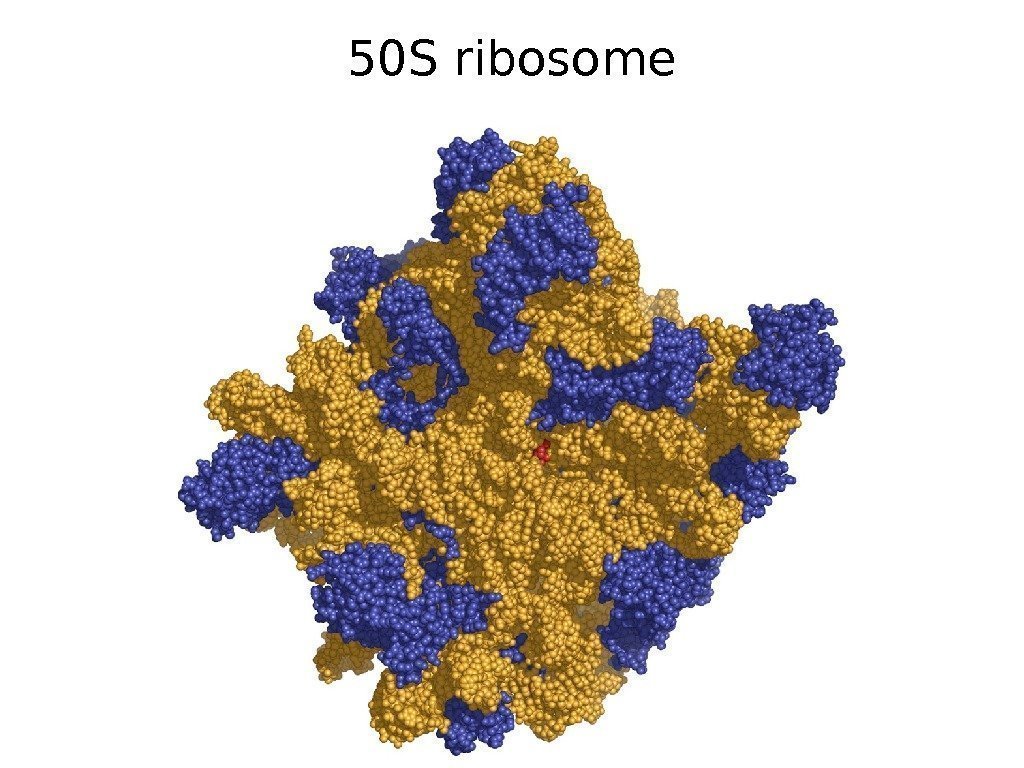
 50 S ribosome
50 S ribosome
 Вопрос • В м. РНК всегда есть много триплетов, кодирующих метионин, — как понять, с которого надо начинать синтез белка?
Вопрос • В м. РНК всегда есть много триплетов, кодирующих метионин, — как понять, с которого надо начинать синтез белка?
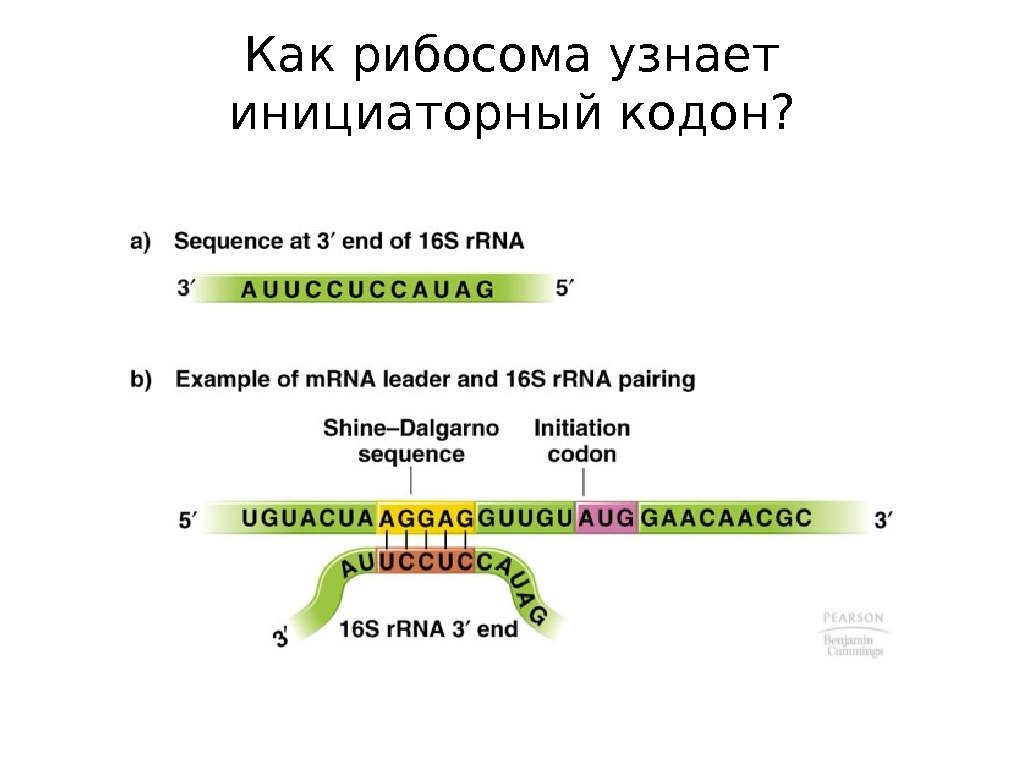
 Как рибосома узнает инициаторный кодон?
Как рибосома узнает инициаторный кодон?
 Вопрос • Что будет, если удалить последовательность анти-ШД из 16 S r. RNA?
Вопрос • Что будет, если удалить последовательность анти-ШД из 16 S r. RNA?
 Ответ: • Грамм-отрицательные бактерии ничего не заметят и будут жить как ни в чем не бывало!
Ответ: • Грамм-отрицательные бактерии ничего не заметят и будут жить как ни в чем не бывало!
 Рибосомный белок S 1 • Связывается с AU-богатыми участками, расположенными upstream от AUG-кодона • Способен привлекать рибосому без участия ШД
Рибосомный белок S 1 • Связывается с AU-богатыми участками, расположенными upstream от AUG-кодона • Способен привлекать рибосому без участия ШД
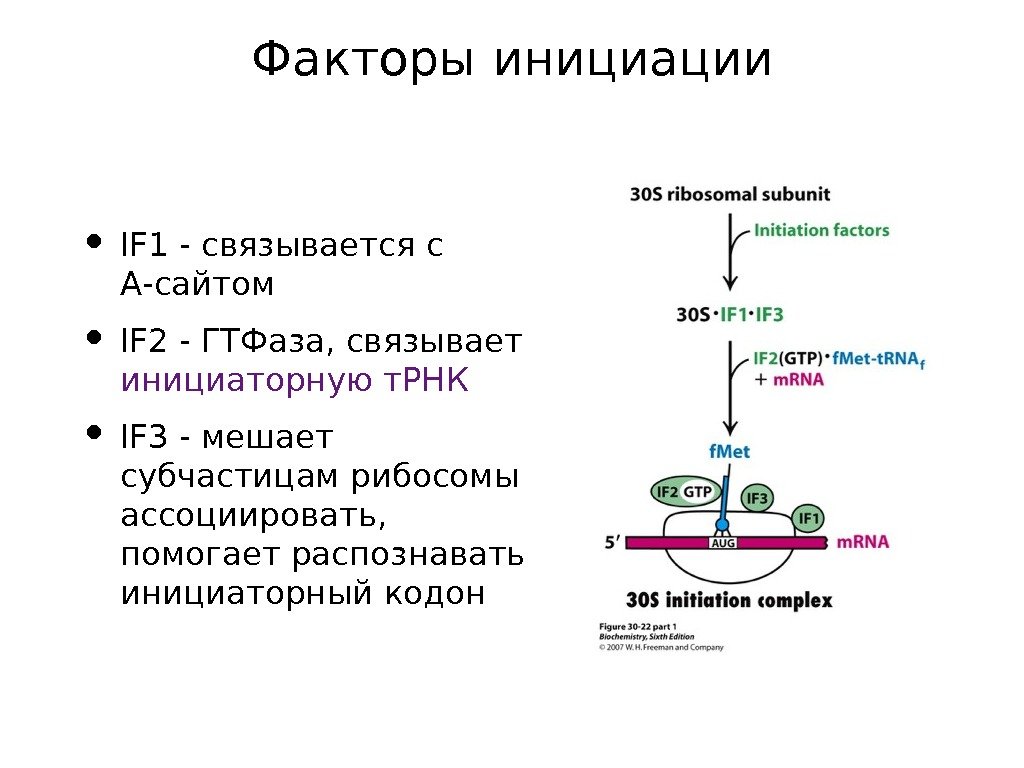
 Факторы инициации • IF 1 — связывается с А-сайтом • IF 2 — ГТФаза, связывает инициаторную т. РНК • IF 3 — мешает субчастицам рибосомы ассоциировать, помогает распознавать инициаторный кодон
Факторы инициации • IF 1 — связывается с А-сайтом • IF 2 — ГТФаза, связывает инициаторную т. РНК • IF 3 — мешает субчастицам рибосомы ассоциировать, помогает распознавать инициаторный кодон
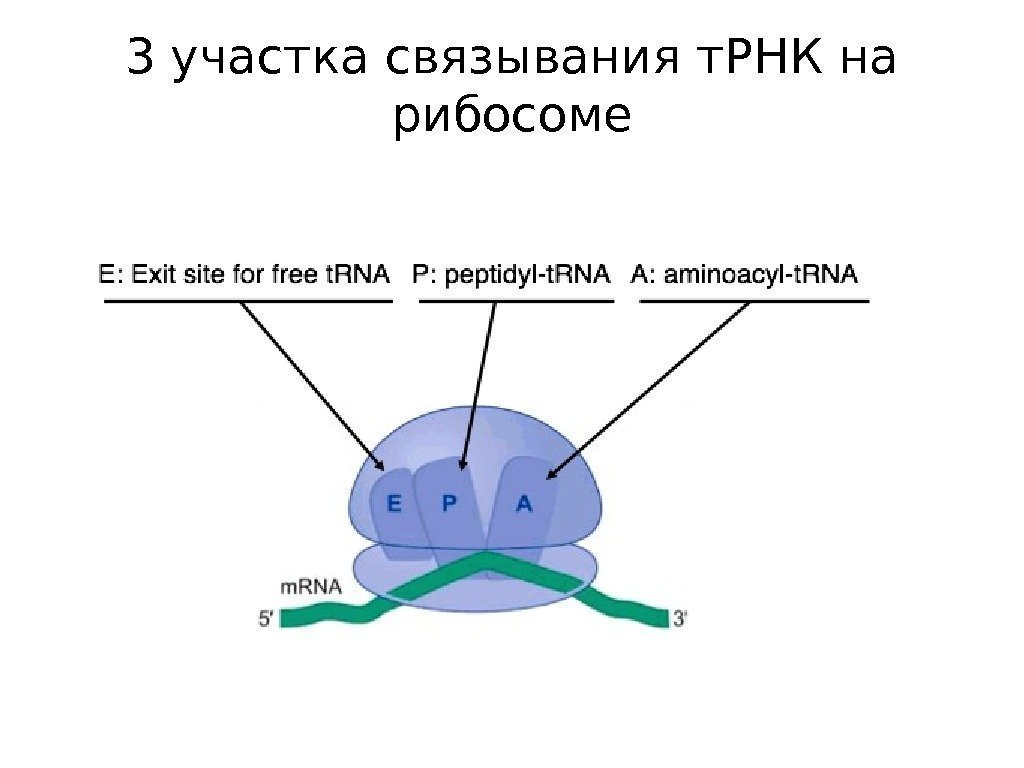
 3 участка связывания т. РНК на рибосоме
3 участка связывания т. РНК на рибосоме
 • Инициация: т. РНК связывается с Р-сайтом • Элонгация: т. РНК связывается с А-сайтом
• Инициация: т. РНК связывается с Р-сайтом • Элонгация: т. РНК связывается с А-сайтом
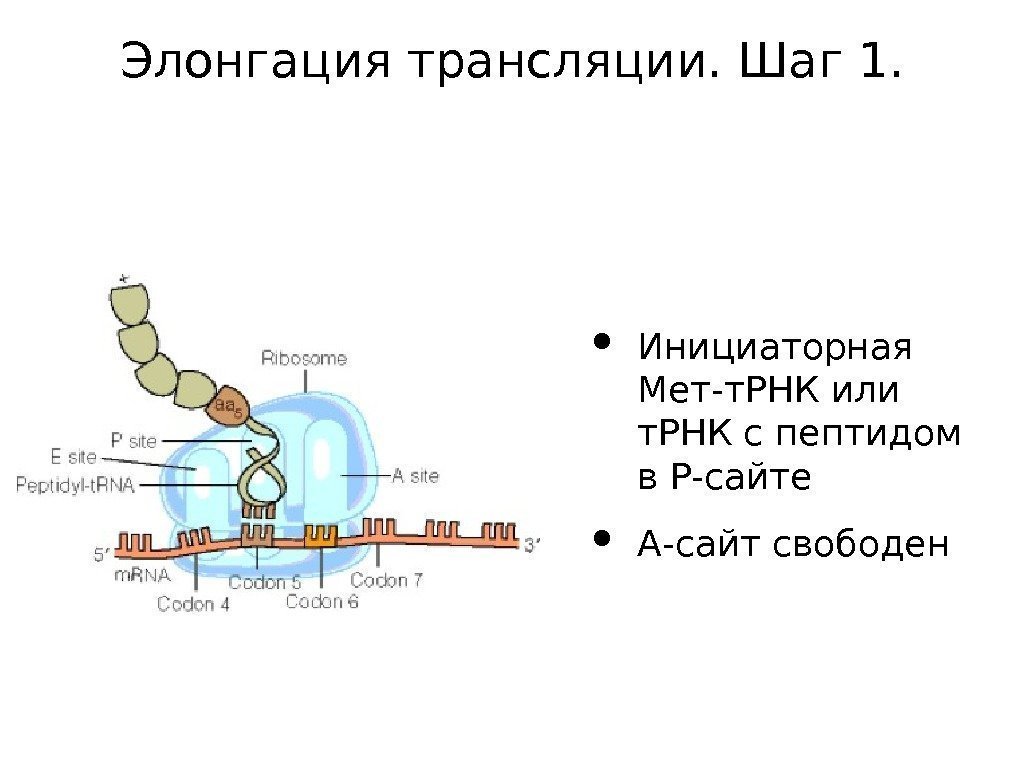
 Элонгация трансляции. Шаг 1. • Инициаторная Мет-т. РНК или т. РНК с пептидом в Р-сайте • А-сайт свободен
Элонгация трансляции. Шаг 1. • Инициаторная Мет-т. РНК или т. РНК с пептидом в Р-сайте • А-сайт свободен
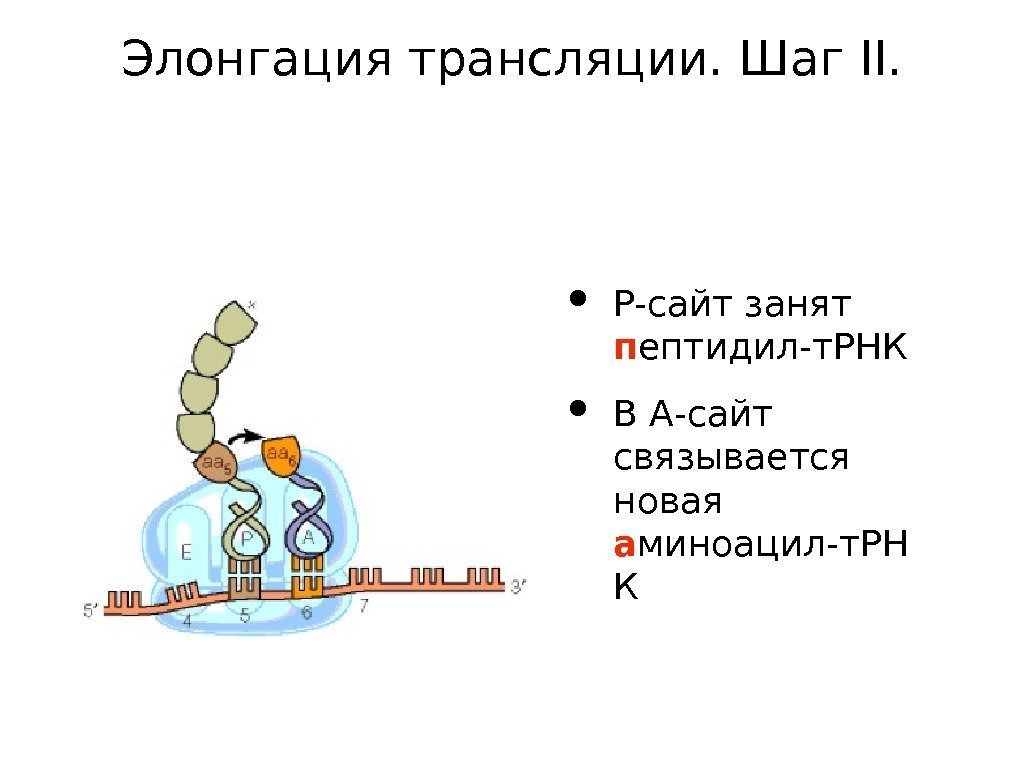
 Элонгация трансляции. Шаг II. • P-сайт занят п ептидил-т. РНК • В А-сайт связывается новая а миноацил-т. РН К
Элонгация трансляции. Шаг II. • P-сайт занят п ептидил-т. РНК • В А-сайт связывается новая а миноацил-т. РН К
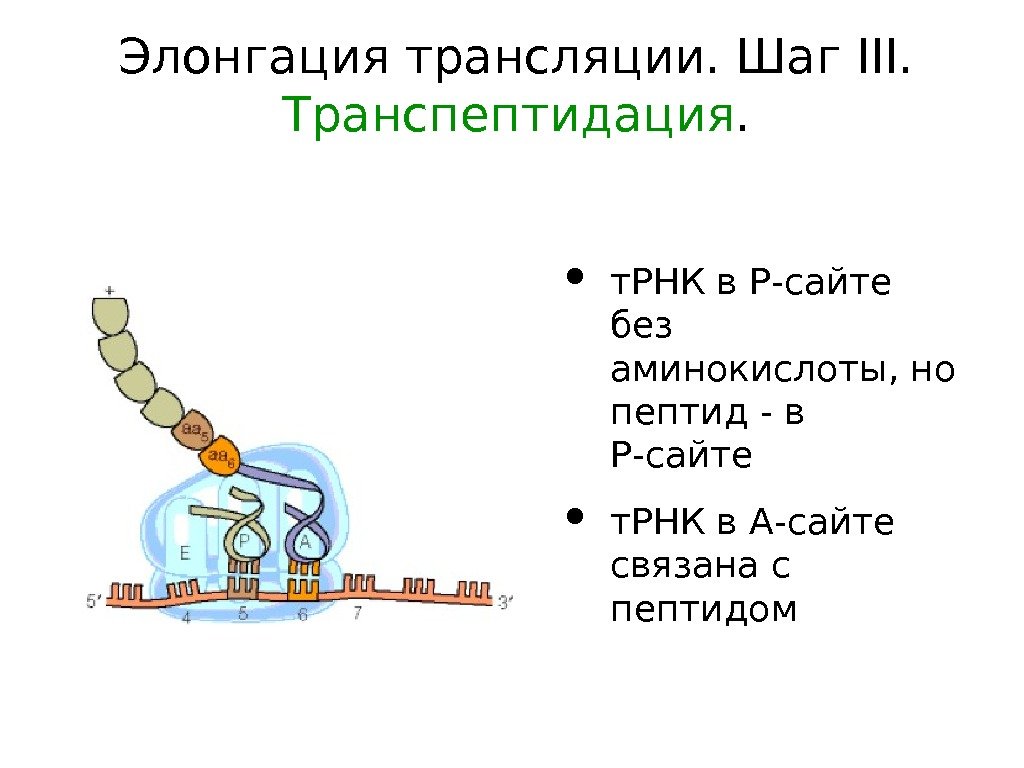
 Элонгация трансляции. Шаг III. Транспептидация. • т. РНК в Р-сайте без аминокислоты, но пептид — в Р-сайте • т. РНК в А-сайте связана с пептидом
Элонгация трансляции. Шаг III. Транспептидация. • т. РНК в Р-сайте без аминокислоты, но пептид — в Р-сайте • т. РНК в А-сайте связана с пептидом
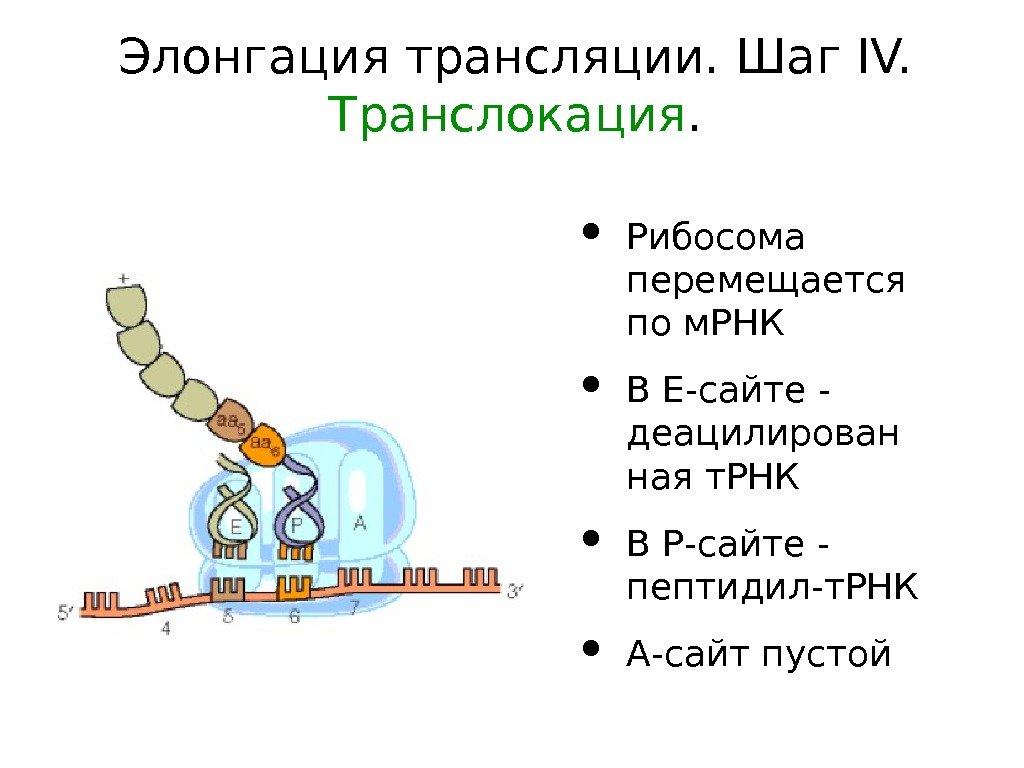
 Элонгация трансляции. Шаг IV. Транслокация. • Рибосома перемещается по м. РНК • В Е-сайте — деацилирован ная т. РНК • В Р-сайте — пептидил-т. РНК • А-сайт пустой
Элонгация трансляции. Шаг IV. Транслокация. • Рибосома перемещается по м. РНК • В Е-сайте — деацилирован ная т. РНК • В Р-сайте — пептидил-т. РНК • А-сайт пустой
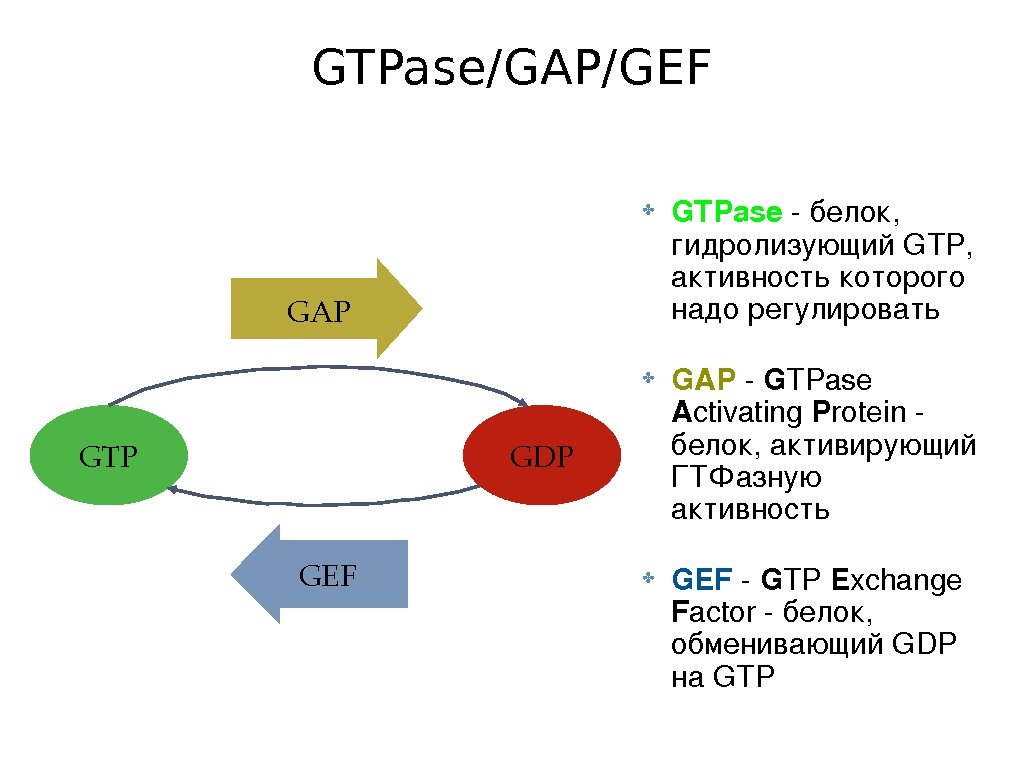
 GTPase/GAP/GEF ✤ GTPase белок, гидролизующий GTP, активность которого надо регулировать ✤ GAP G TPase A ctivating P rotein белок , активирующий ГТФазную активность ✤ GEF G TP E xchange F actor белок, обменивающий GDP на GTPGTP GDP GEFGAP
GTPase/GAP/GEF ✤ GTPase белок, гидролизующий GTP, активность которого надо регулировать ✤ GAP G TPase A ctivating P rotein белок , активирующий ГТФазную активность ✤ GEF G TP E xchange F actor белок, обменивающий GDP на GTPGTP GDP GEFGAP
 Кто «работает» GAP’ом для IF 2?
Кто «работает» GAP’ом для IF 2?
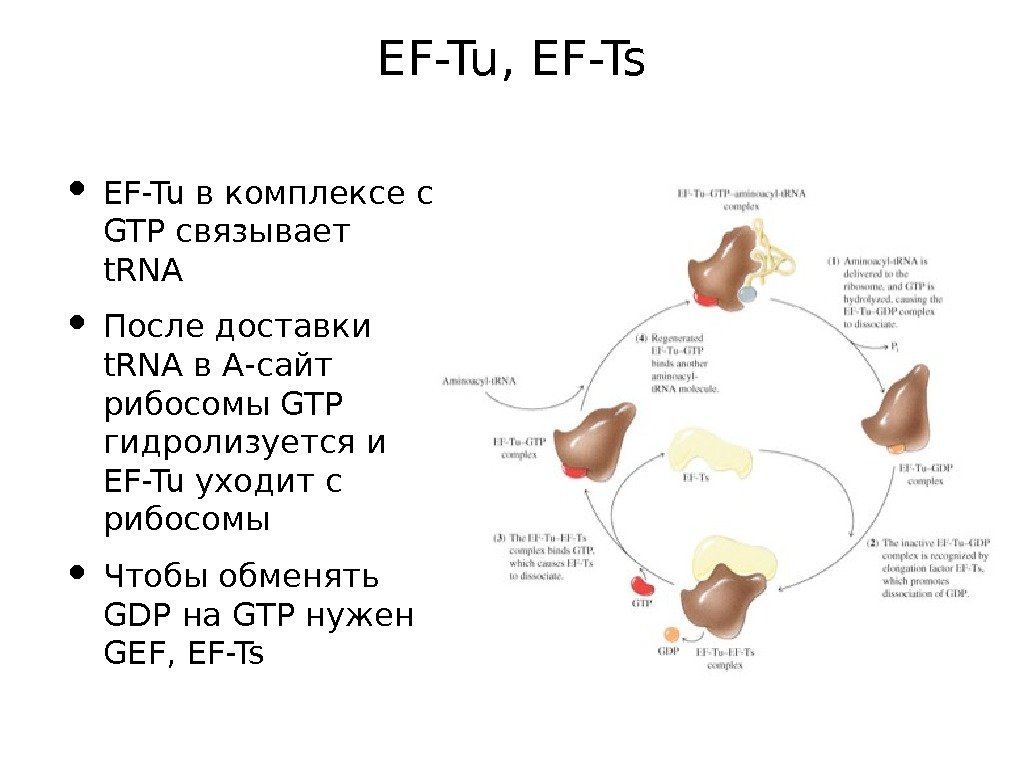
 EF-Tu, EF-Ts • EF-Tu в комплексе с GTP связывает t. RNA • После доставки t. RNA в А-сайт рибосомы GTP гидролизуется и EF-Tu уходит с рибосомы • Чтобы обменять GDP на GTP нужен GEF, EF-Ts
EF-Tu, EF-Ts • EF-Tu в комплексе с GTP связывает t. RNA • После доставки t. RNA в А-сайт рибосомы GTP гидролизуется и EF-Tu уходит с рибосомы • Чтобы обменять GDP на GTP нужен GEF, EF-Ts
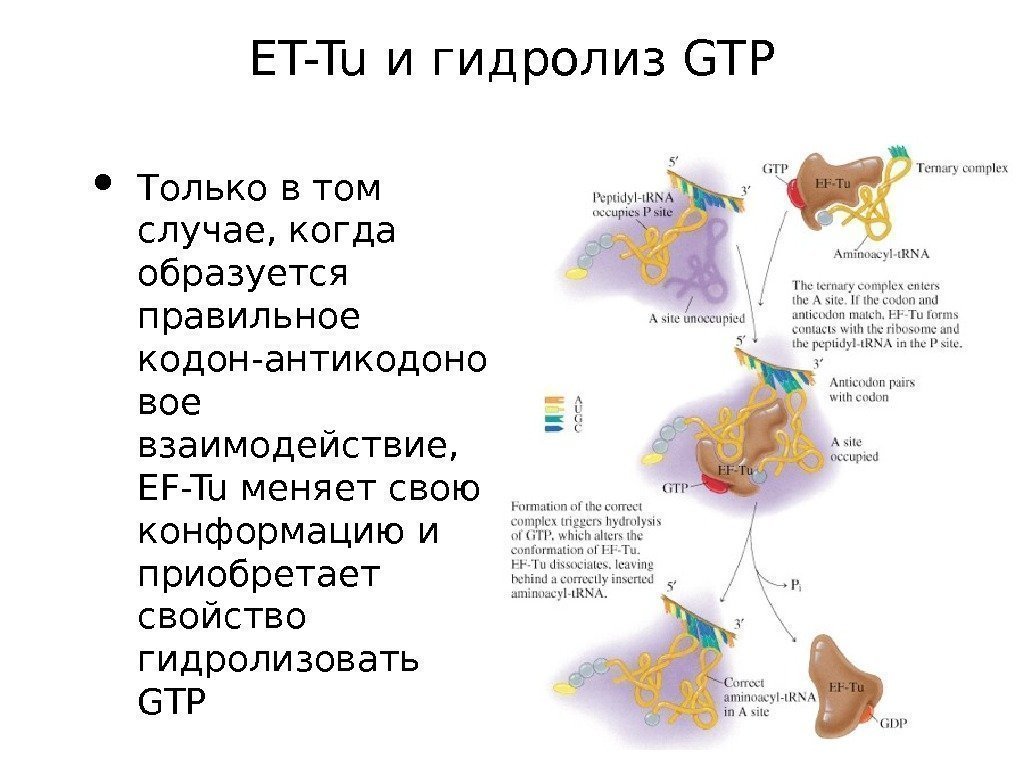
 ET-Tu и гидролиз GTP • Только в том случае, когда образуется правильное кодон-антикодоно вое взаимодействие, EF-Tu меняет свою конформацию и приобретает свойство гидролизовать GTP
ET-Tu и гидролиз GTP • Только в том случае, когда образуется правильное кодон-антикодоно вое взаимодействие, EF-Tu меняет свою конформацию и приобретает свойство гидролизовать GTP
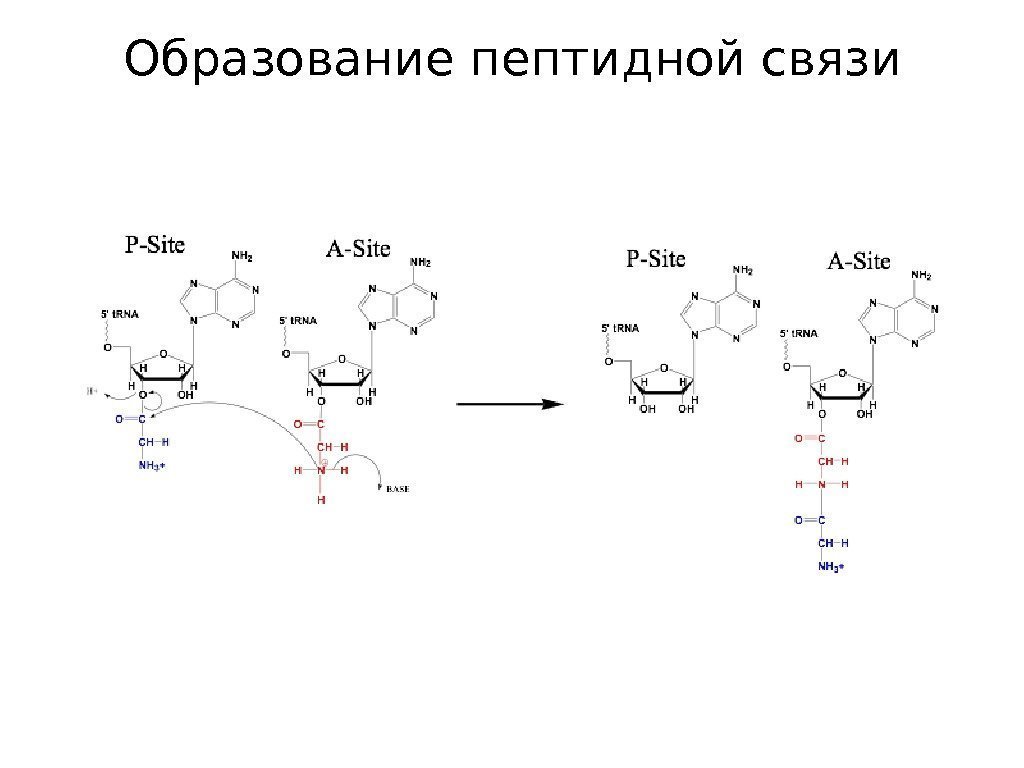
 Образование пептидной связи
Образование пептидной связи
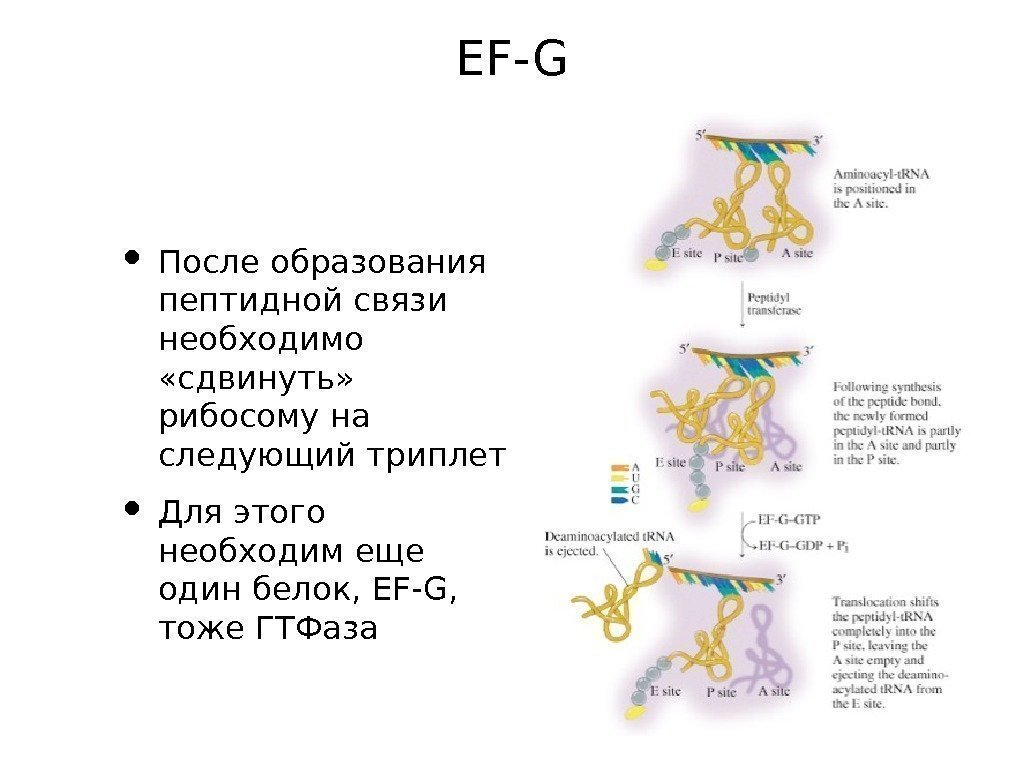
 EF-G • После образования пептидной связи необходимо «сдвинуть» рибосому на следующий триплет • Для этого необходим еще один белок, EF-G, тоже ГТФаза
EF-G • После образования пептидной связи необходимо «сдвинуть» рибосому на следующий триплет • Для этого необходим еще один белок, EF-G, тоже ГТФаза
 Элонгация трансляции у эукариот • e. EF-1 A — сажает т. РНК в А-сайт (EF-Tu) • e. EF-1 B — обменивает GDP на GTP (EF-Ts) • e. EF 2 — транслоцирует рибосому (EF-G)
Элонгация трансляции у эукариот • e. EF-1 A — сажает т. РНК в А-сайт (EF-Tu) • e. EF-1 B — обменивает GDP на GTP (EF-Ts) • e. EF 2 — транслоцирует рибосому (EF-G)
 Терминация трансляции • У бактерий 3 фактора терминации • RF 1 — узнает UAA и UAG • RF 2 — узнает UAA и UGA • RF 3 — помогает работать RF 1/2, GTPase • RRF — разрушает пост-терминационную рибосому • У эукариот e. RF 1 узнает все три кодона • e. RF 3 — аналог RF 3, встречается только у грибов
Терминация трансляции • У бактерий 3 фактора терминации • RF 1 — узнает UAA и UAG • RF 2 — узнает UAA и UGA • RF 3 — помогает работать RF 1/2, GTPase • RRF — разрушает пост-терминационную рибосому • У эукариот e. RF 1 узнает все три кодона • e. RF 3 — аналог RF 3, встречается только у грибов
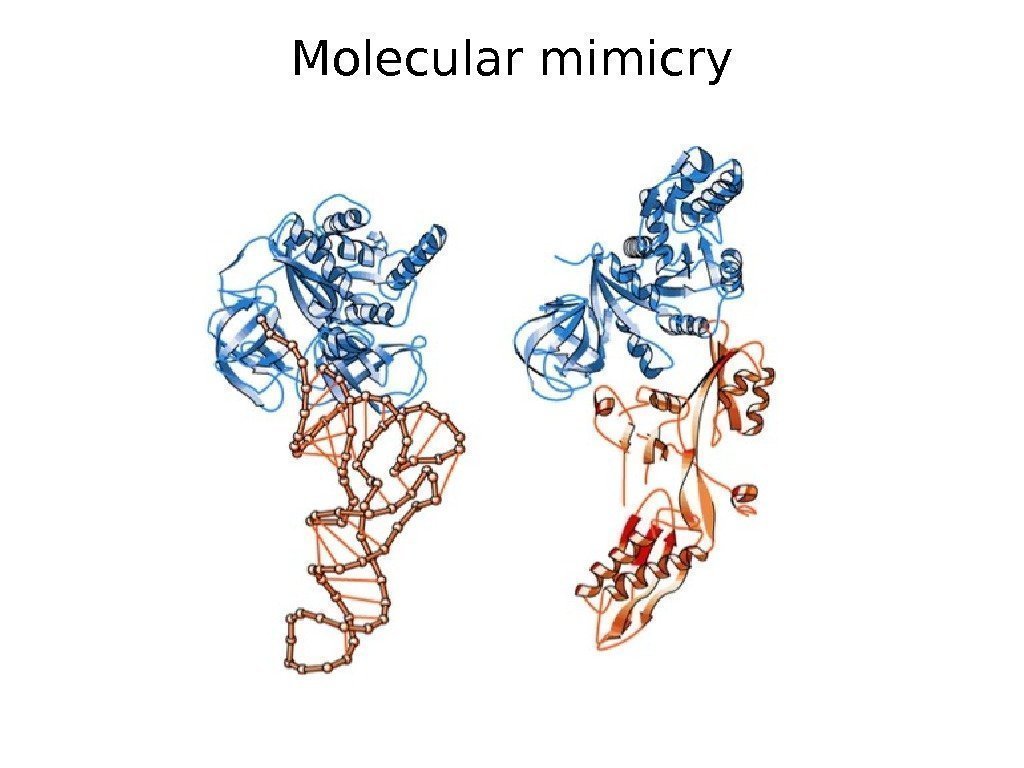
 Molecular mimicry
Molecular mimicry
 Рибосомаиантибиотики • Тетрациклин — мешает посадки т. РНК в А-сайт • Хлорамфеникол — ингибирует пептидил-трансферазную активность рибосомы • Эритромицин — «забивает» рибосомный туннель • Тобрамицин — связывается с А-сайтом, но что делает конкретно не до конца ясно
Рибосомаиантибиотики • Тетрациклин — мешает посадки т. РНК в А-сайт • Хлорамфеникол — ингибирует пептидил-трансферазную активность рибосомы • Эритромицин — «забивает» рибосомный туннель • Тобрамицин — связывается с А-сайтом, но что делает конкретно не до конца ясно
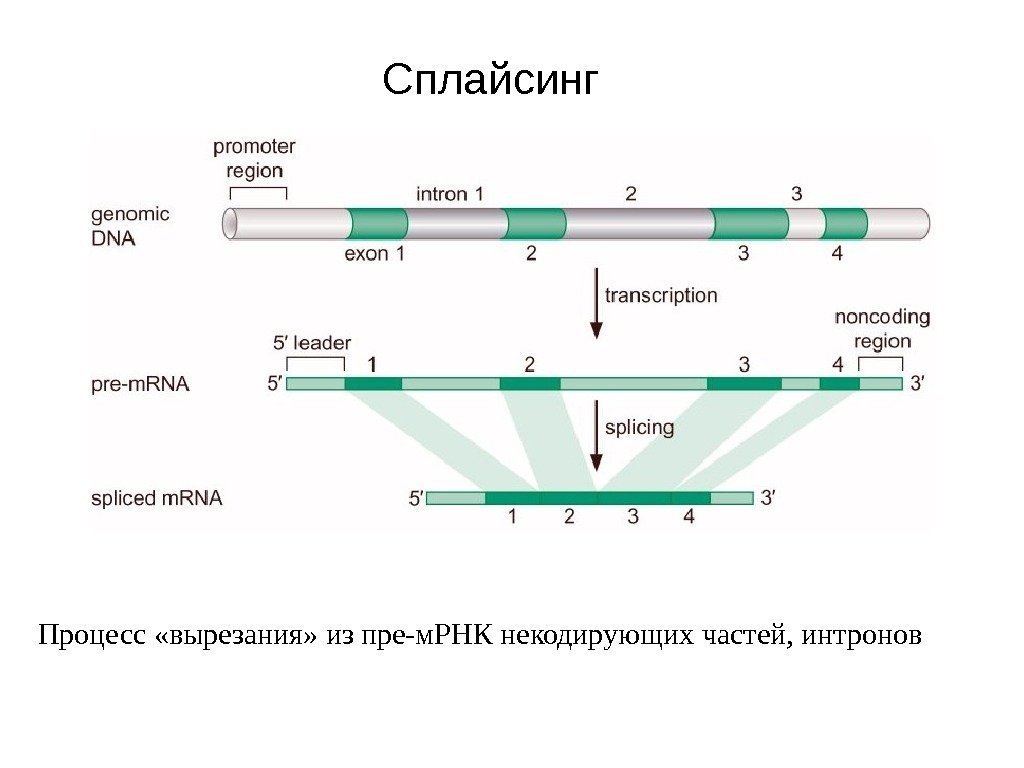
 Сплайсинг Процесс «вырезания» из пре-м. РНК некодирующих частей, интронов
Сплайсинг Процесс «вырезания» из пре-м. РНК некодирующих частей, интронов
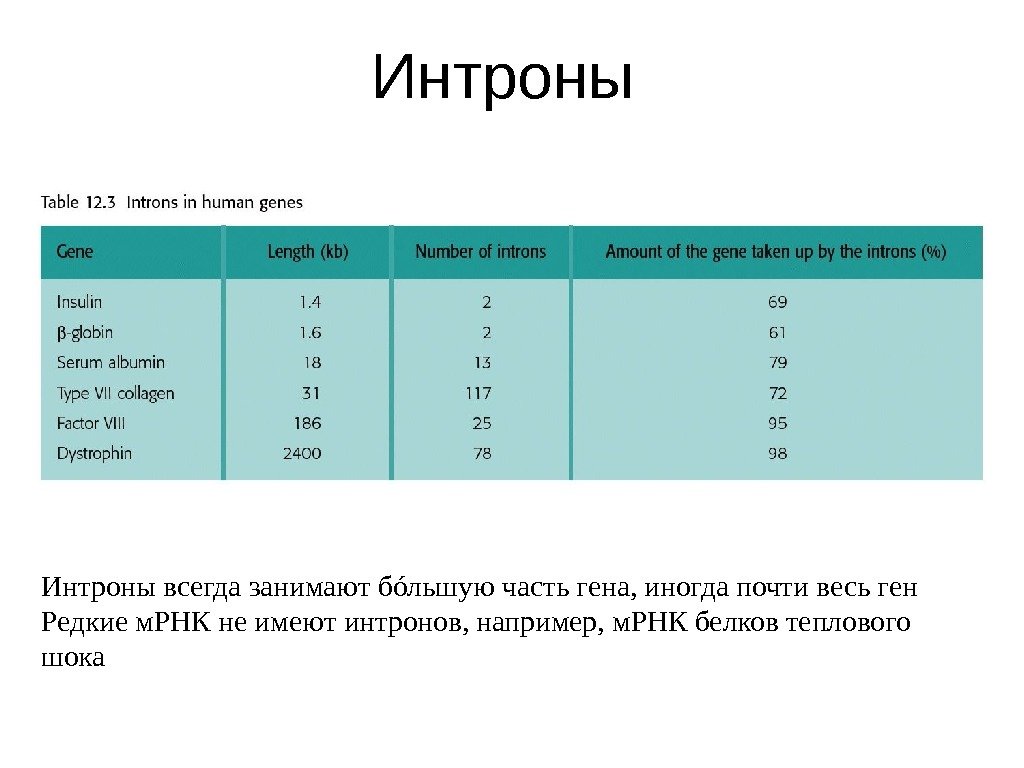
 Интроны всегда занимают бóльшую часть гена, иногда почти весь ген Редкие м. РНК не имеют интронов, например, м. РНК белков теплового шока
Интроны всегда занимают бóльшую часть гена, иногда почти весь ген Редкие м. РНК не имеют интронов, например, м. РНК белков теплового шока
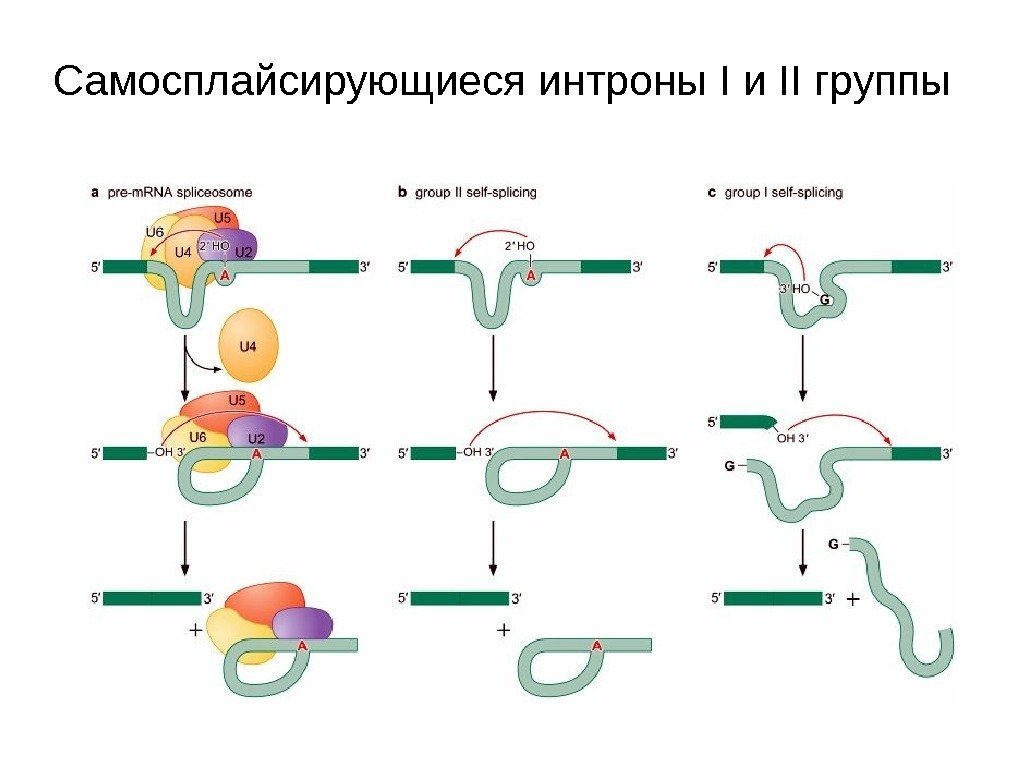
 Самосплайсирующиеся интроны I и II группы
Самосплайсирующиеся интроны I и II группы
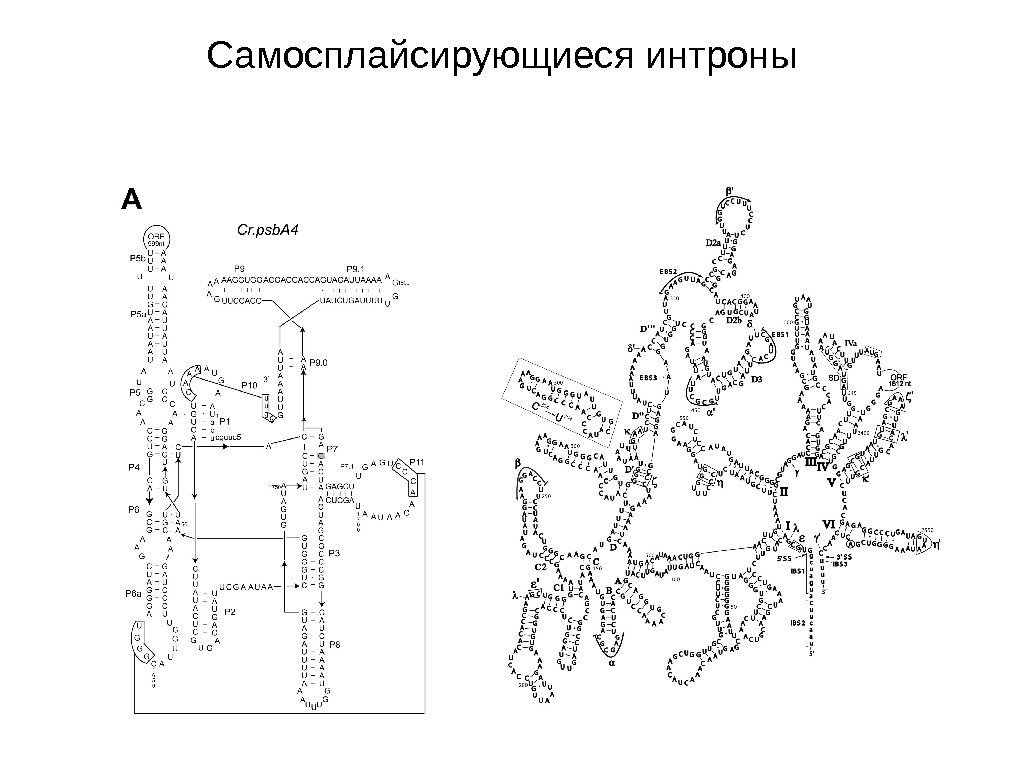
 Самосплайсирующиеся интроны
Самосплайсирующиеся интроны
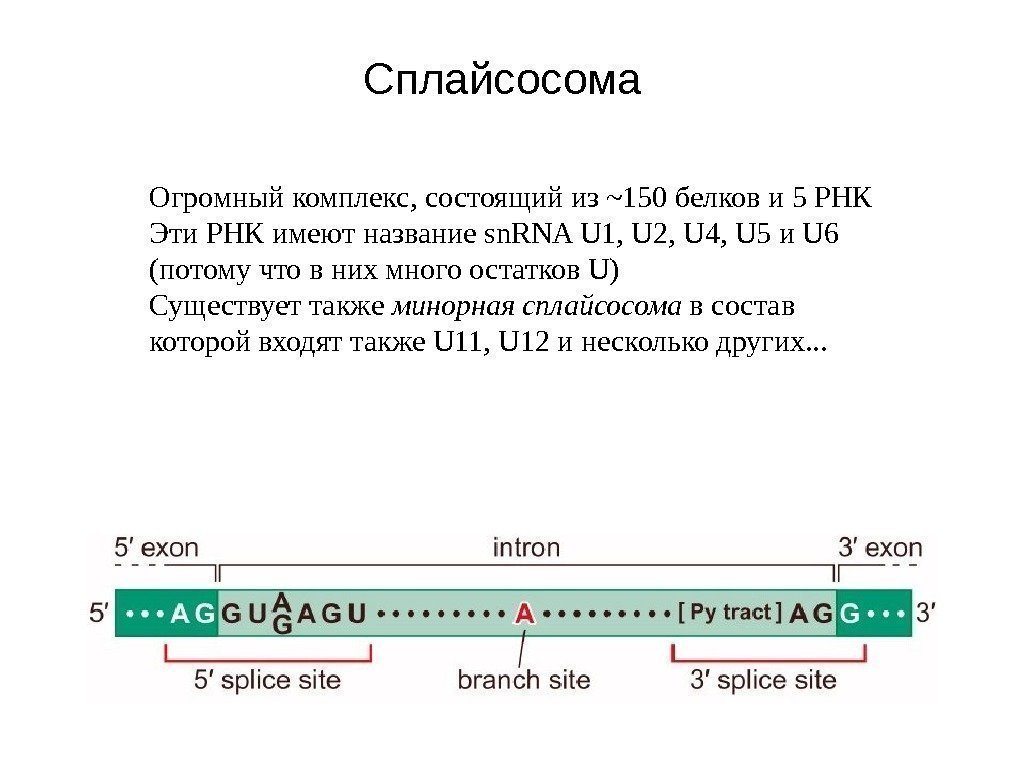
 Сплайсосома Огромный комплекс, состоящий из ~150 белков и 5 РНК Эти РНК имеют название sn. RNA U 1, U 2, U 4, U 5 и U 6 (потому что в них много остатков U) Существует также минорная сплайсосома в состав которой входят также U 11, U 12 и несколько других. . .
Сплайсосома Огромный комплекс, состоящий из ~150 белков и 5 РНК Эти РНК имеют название sn. RNA U 1, U 2, U 4, U 5 и U 6 (потому что в них много остатков U) Существует также минорная сплайсосома в состав которой входят также U 11, U 12 и несколько других. . .
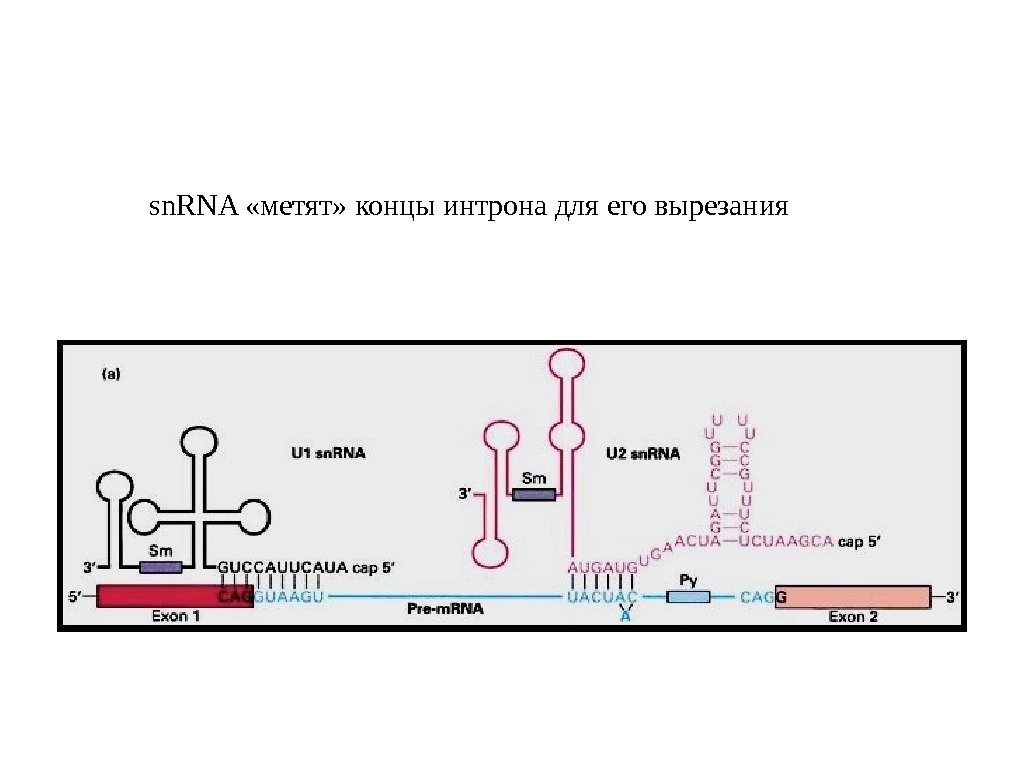
 sn. RNA «метят» концы интрона для его вырезания
sn. RNA «метят» концы интрона для его вырезания
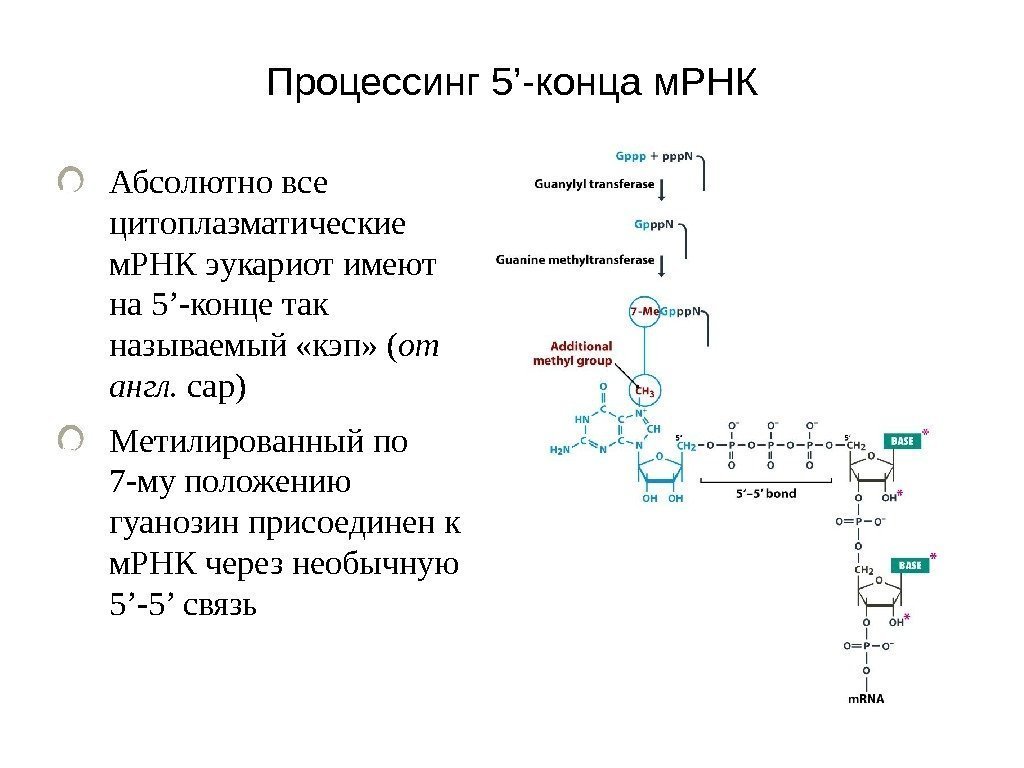
 Процессинг 5’-конца м. РНК Абсолютно все цитоплазматические м. РНК эукариот имеют на 5’-конце так называемый «кэп» ( от англ. cap) Метилированный по 7 -му положению гуанозин присоединен к м. РНК через необычную 5’-5’ связь
Процессинг 5’-конца м. РНК Абсолютно все цитоплазматические м. РНК эукариот имеют на 5’-конце так называемый «кэп» ( от англ. cap) Метилированный по 7 -му положению гуанозин присоединен к м. РНК через необычную 5’-5’ связь
 Альтернативный сплайсинг По различным оценкам, от 40% до 75% генов человека могут иметь альтернативно сплайсированные транскрипты Также известны случаи альтернативного полиаденилирования
Альтернативный сплайсинг По различным оценкам, от 40% до 75% генов человека могут иметь альтернативно сплайсированные транскрипты Также известны случаи альтернативного полиаденилирования
 м. РНКэукариот «зациклены» Wells SE et al Circularization of m. RNA by eukaryotic translation initiation factors. Mol Cell. 1998 2: 135 -40. ✴ e. IF 4 F связывается на 5’ концем. РНК ✴ PABP связывается на 3’ концем. РНК ✴ e. IF 4 F связывается с PABP
м. РНКэукариот «зациклены» Wells SE et al Circularization of m. RNA by eukaryotic translation initiation factors. Mol Cell. 1998 2: 135 -40. ✴ e. IF 4 F связывается на 5’ концем. РНК ✴ PABP связывается на 3’ концем. РНК ✴ e. IF 4 F связывается с PABP
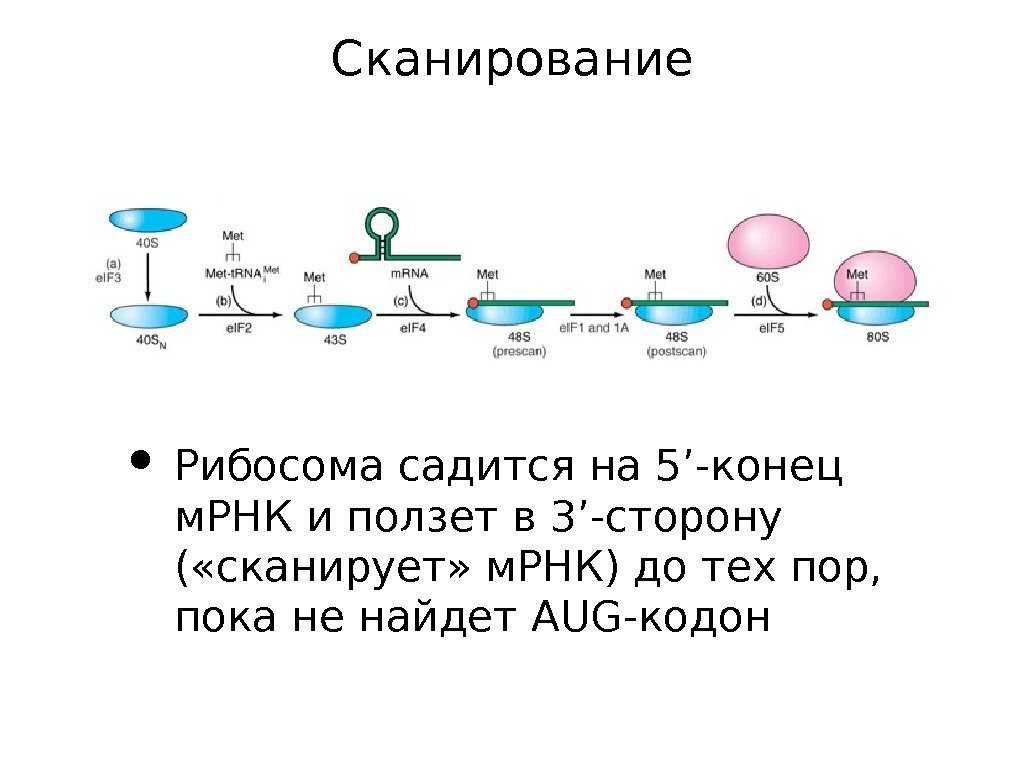
 Сканирование • Рибосома садится на 5’-конец м. РНК и ползет в 3’-сторону ( «сканирует» м. РНК) до тех пор, пока не найдет AUG-кодон
Сканирование • Рибосома садится на 5’-конец м. РНК и ползет в 3’-сторону ( «сканирует» м. РНК) до тех пор, пока не найдет AUG-кодон
 Kozak context/Kozak sequence • Не каждый первый AUG-кодон узнается рибосомой • Самый хороший AUG-кодон окружен хорошим контекстом: A/G CC AUG A/G • Еще лучше, если в 10 -15 нуклеотидах после AUG есть шпилька
Kozak context/Kozak sequence • Не каждый первый AUG-кодон узнается рибосомой • Самый хороший AUG-кодон окружен хорошим контекстом: A/G CC AUG A/G • Еще лучше, если в 10 -15 нуклеотидах после AUG есть шпилька
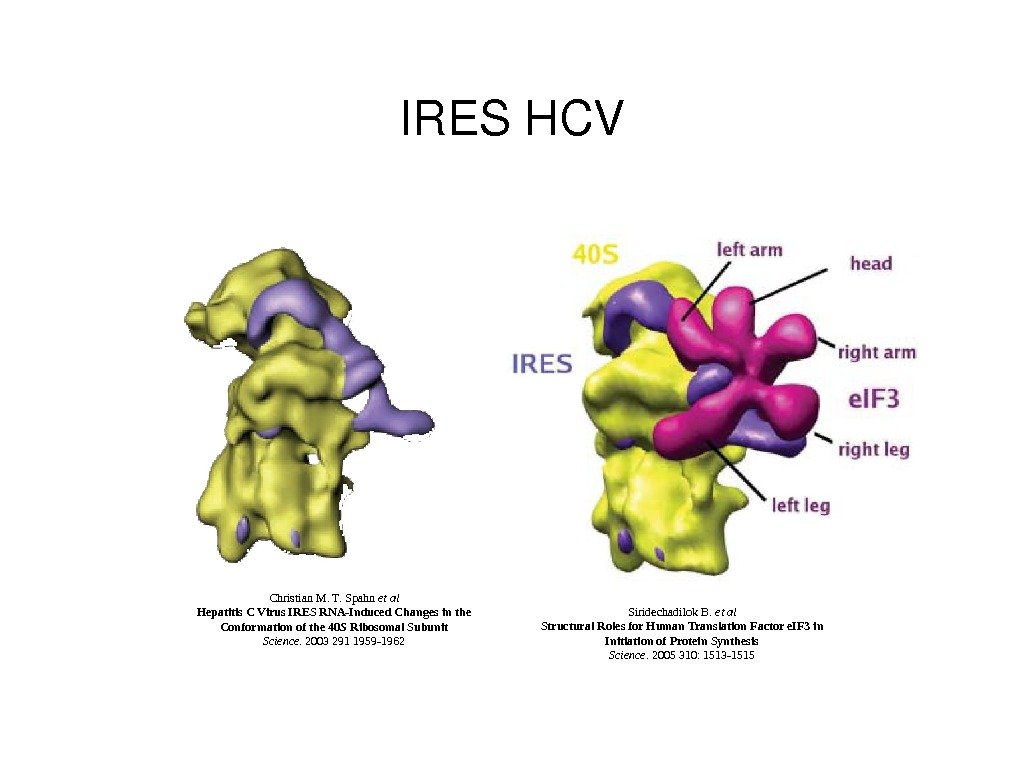
 IRESHCV Siridechadilok B. et al Structural Roles for Human Translation Factor e. IF 3 in Initiation of Protein Synthesis Science. 2005 310: 1513 -1515 Christian M. T. Spahn et al Hepatitis C Virus IRES RNA-Induced Changes in the Conformation of the 40 S Ribosomal Subunit Science. 2003 291 1959 —
IRESHCV Siridechadilok B. et al Structural Roles for Human Translation Factor e. IF 3 in Initiation of Protein Synthesis Science. 2005 310: 1513 -1515 Christian M. T. Spahn et al Hepatitis C Virus IRES RNA-Induced Changes in the Conformation of the 40 S Ribosomal Subunit Science. 2003 291 1959 —
 Frameshift — сдвиг рамки считывания • На повторяющихся последовательностях типа AAAAAA • Структуры в м. РНК могут регулировать сдвиг
Frameshift — сдвиг рамки считывания • На повторяющихся последовательностях типа AAAAAA • Структуры в м. РНК могут регулировать сдвиг
 Как трансляция может регулировать другие процессы в клетке
Как трансляция может регулировать другие процессы в клетке
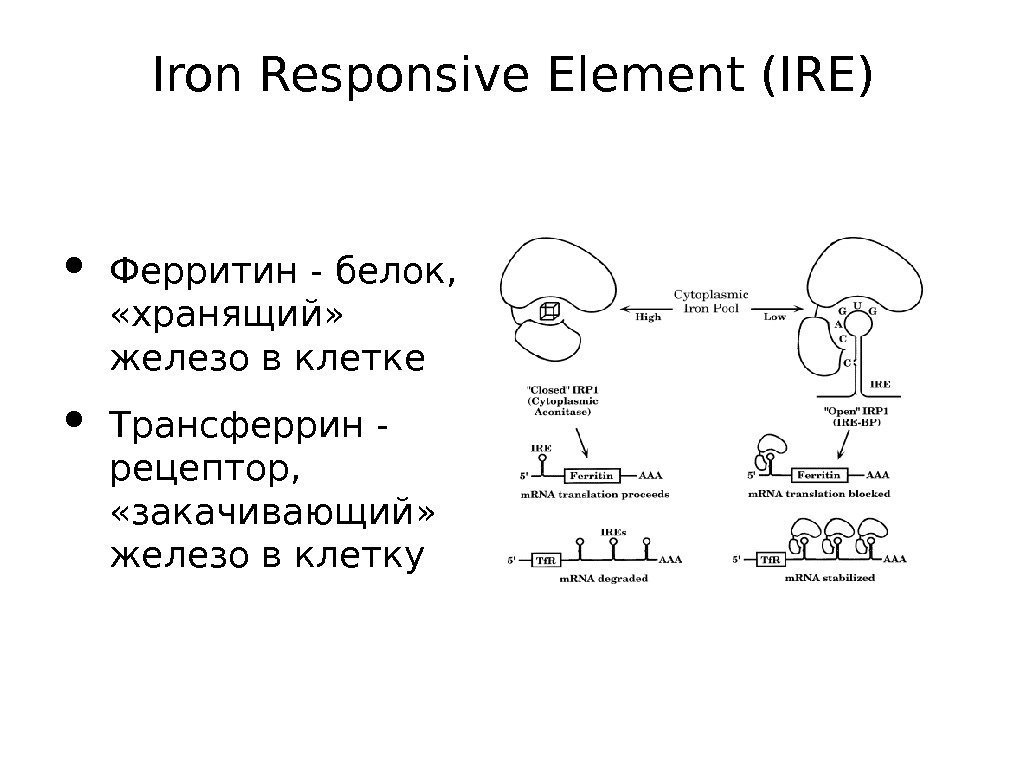
 Iron Responsive Element (IRE) • Ферритин — белок, «хранящий» железо в клетке • Трансферрин — рецептор, «закачивающий» железо в клетку
Iron Responsive Element (IRE) • Ферритин — белок, «хранящий» железо в клетке • Трансферрин — рецептор, «закачивающий» железо в клетку
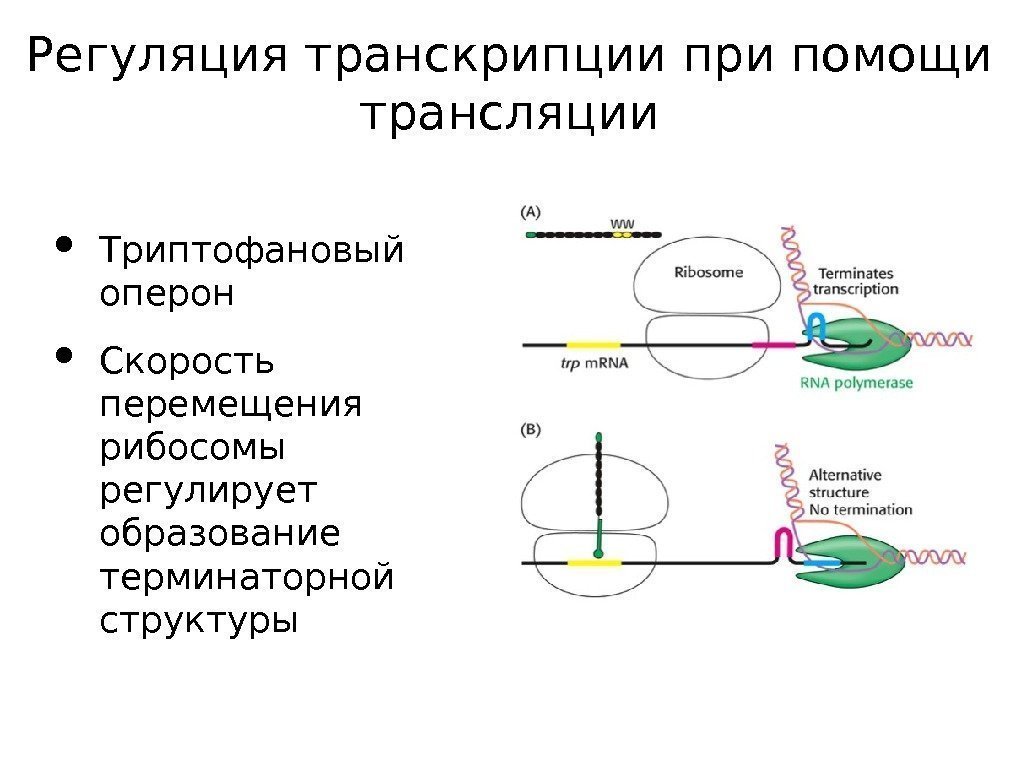
 Регуляция транскрипции при помощи трансляции • Триптофановый оперон • Скорость перемещения рибосомы регулирует образование терминаторной структуры
Регуляция транскрипции при помощи трансляции • Триптофановый оперон • Скорость перемещения рибосомы регулирует образование терминаторной структуры
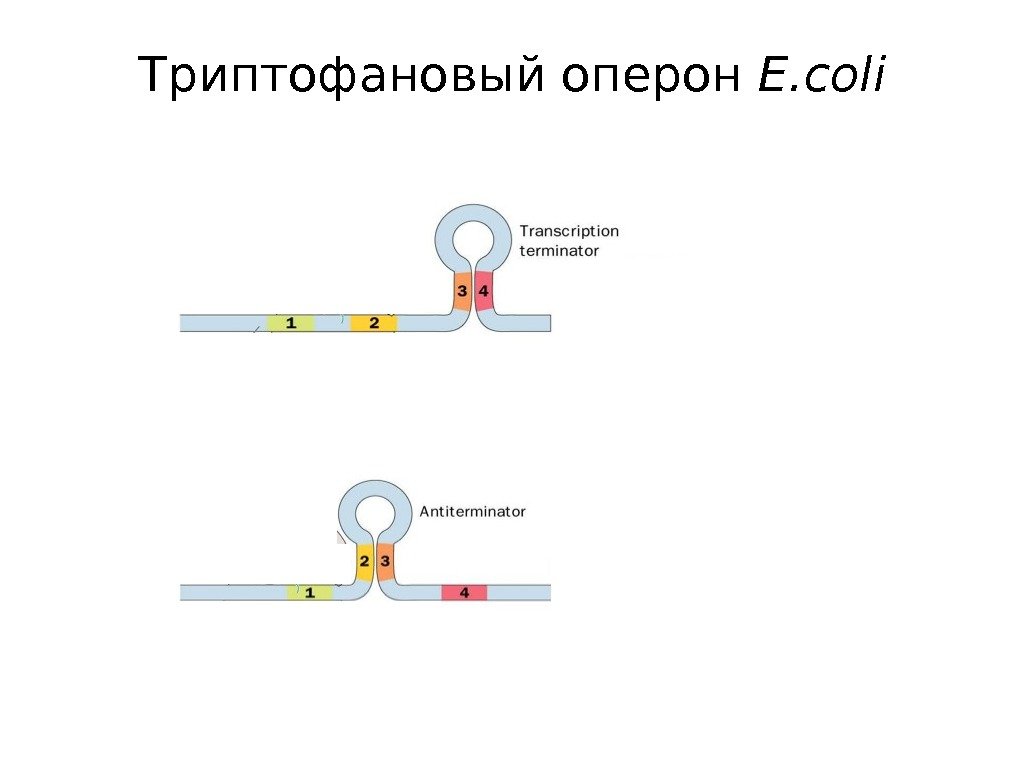
 Триптофановый оперон E. coli
Триптофановый оперон E. coli
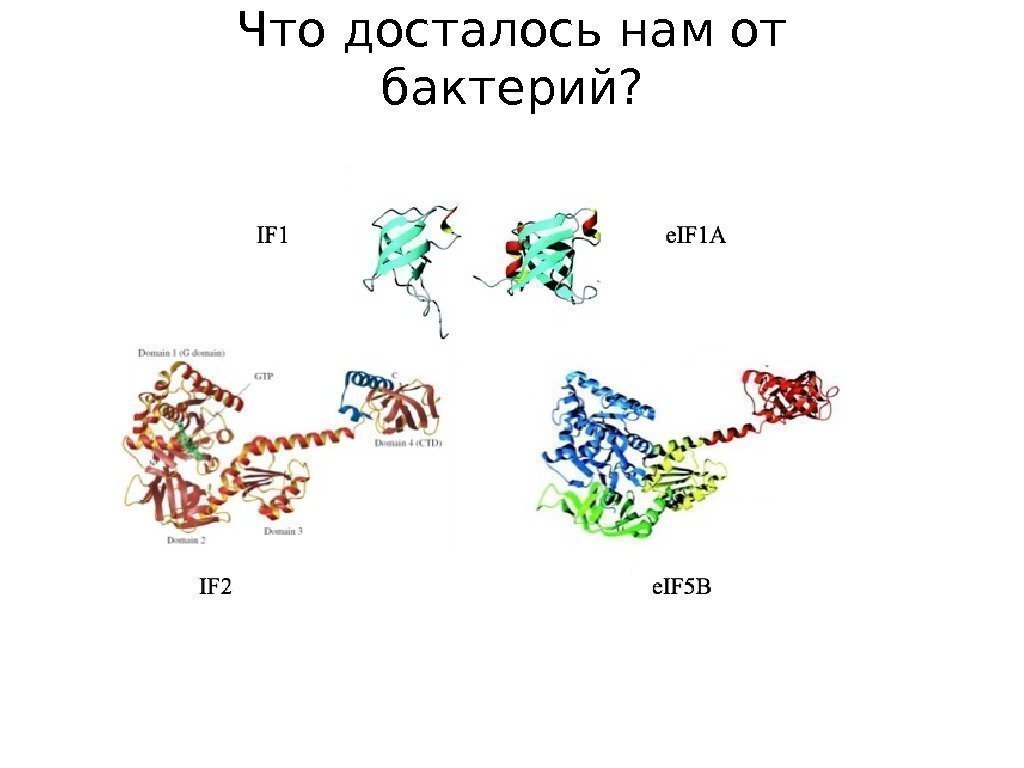
 Что досталось нам от бактерий?
Что досталось нам от бактерий?
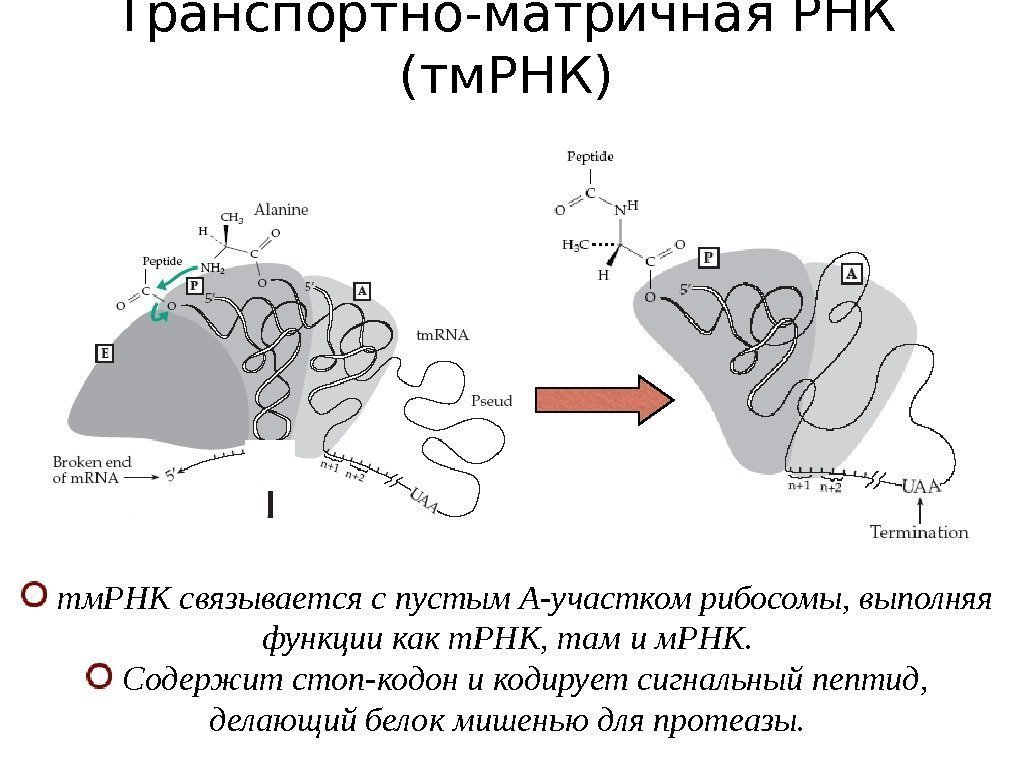
 Транспортно-матричная РНК (тм. РНК) тм. РНК связывается с пустым А-участком рибосомы, выполняя функции как т. РНК, там и м. РНК. Содержит стоп-кодон и кодирует сигнальный пептид, делающий белок мишенью для протеазы.
Транспортно-матричная РНК (тм. РНК) тм. РНК связывается с пустым А-участком рибосомы, выполняя функции как т. РНК, там и м. РНК. Содержит стоп-кодон и кодирует сигнальный пептид, делающий белок мишенью для протеазы.

