 Теория электролитической диссоциации ЭЛЕКТРОЛИТЫ И НЕЭЛЕКТРОЛИТЫ. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ
Теория электролитической диссоциации ЭЛЕКТРОЛИТЫ И НЕЭЛЕКТРОЛИТЫ. ЭЛЕКТРОЛИТИЧЕСКАЯ ДИССОЦИАЦИЯ
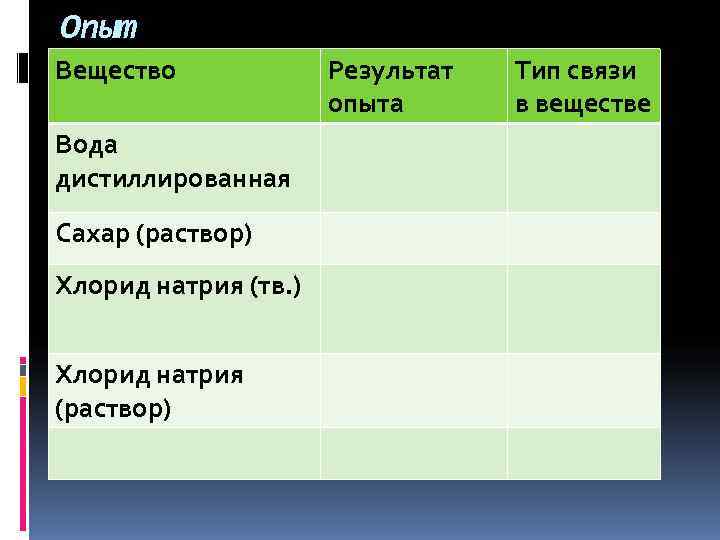 Опыт Вещество Результат Тип связи опыта в веществе Вода дистиллированная Сахар (раствор) Хлорид натрия (тв. ) Хлорид натрия (раствор)
Опыт Вещество Результат Тип связи опыта в веществе Вода дистиллированная Сахар (раствор) Хлорид натрия (тв. ) Хлорид натрия (раствор)
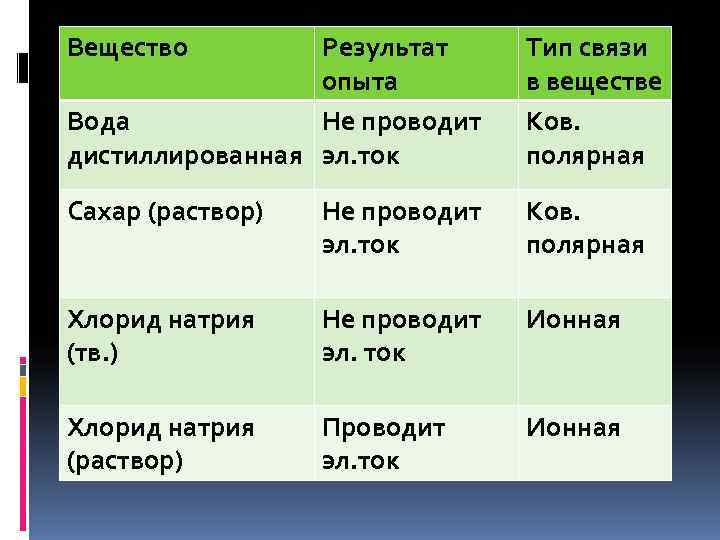 Вещество Результат Тип связи опыта в веществе Вода Не проводит Ков. дистиллированная эл. ток полярная Сахар (раствор) Не проводит Ков. эл. ток полярная Хлорид натрия Не проводит Ионная (тв. ) эл. ток Хлорид натрия Проводит Ионная (раствор) эл. ток
Вещество Результат Тип связи опыта в веществе Вода Не проводит Ков. дистиллированная эл. ток полярная Сахар (раствор) Не проводит Ков. эл. ток полярная Хлорид натрия Не проводит Ионная (тв. ) эл. ток Хлорид натрия Проводит Ионная (раствор) эл. ток
 Вывод: Раствор соли, в отличии от чистой воды и твердой соли, проводит эл. ток, так как содержит свободно перемещающиеся ионы.
Вывод: Раствор соли, в отличии от чистой воды и твердой соли, проводит эл. ток, так как содержит свободно перемещающиеся ионы.
 Вещества Электролиты Неэлектролиты
Вещества Электролиты Неэлектролиты
 Электролиты Это вещества, растворы и расплавы которых проводят электрический ток К электролитам относятся : кислоты, соли, щелочи Это вещества с ионной или ковалентной сильнополярной связью
Электролиты Это вещества, растворы и расплавы которых проводят электрический ток К электролитам относятся : кислоты, соли, щелочи Это вещества с ионной или ковалентной сильнополярной связью
 Неэлектролиты Это вещества, растворы которых не проводят электрический ток Например: вода, сахар, кислород, азот и др. Это вещества с ковалентной неполярной или ковалентной малополярной связью
Неэлектролиты Это вещества, растворы которых не проводят электрический ток Например: вода, сахар, кислород, азот и др. Это вещества с ковалентной неполярной или ковалентной малополярной связью
 Сделайте в тетради рисунки Механизм диссоциации веществ с ионной связью на примере хлорида натрия (рисунок 9 стр. 24 в учебнике) Механизм диссоциации веществ с ковалентной полярной связью на примере хлороводорода (рисунок 12 страница 29 в учебнике)
Сделайте в тетради рисунки Механизм диссоциации веществ с ионной связью на примере хлорида натрия (рисунок 9 стр. 24 в учебнике) Механизм диссоциации веществ с ковалентной полярной связью на примере хлороводорода (рисунок 12 страница 29 в учебнике)
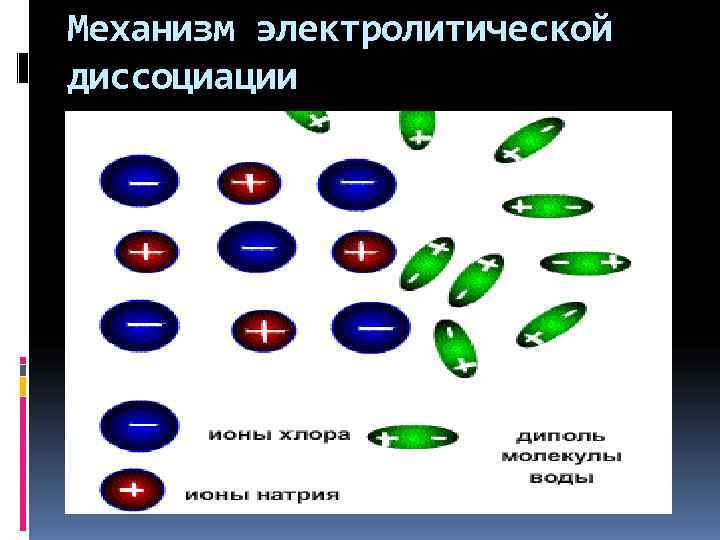 Механизм электролитической диссоциации
Механизм электролитической диссоциации
 Процесс распада электролита на ионы при растворении в воде или расплавлении называется электролитической диссоциацией (ЭД)
Процесс распада электролита на ионы при растворении в воде или расплавлении называется электролитической диссоциацией (ЭД)
 Основная причина диссоциации - образование гидратированных ионов (то есть ионов, связанных с молекулами воды)
Основная причина диссоциации - образование гидратированных ионов (то есть ионов, связанных с молекулами воды)
 Заряды ионов металлов I-III групп главных подгрупп всегда положительны и равны номеру группы: Na + Mg 2+ Al 3+ Для металлов побочных подгрупп – запомните: Cu + Cu 2+ Fe 3+
Заряды ионов металлов I-III групп главных подгрупп всегда положительны и равны номеру группы: Na + Mg 2+ Al 3+ Для металлов побочных подгрупп – запомните: Cu + Cu 2+ Fe 3+
 Заряд гидроксогруппы всегда -1 OH - Заряды кислотных остатков всегда отрицательны и равны их валентности Cl - SO 2 - 4 PO 3 - 4
Заряд гидроксогруппы всегда -1 OH - Заряды кислотных остатков всегда отрицательны и равны их валентности Cl - SO 2 - 4 PO 3 - 4
 Домашнее задание конспект учить (параграф 7, 9 )
Домашнее задание конспект учить (параграф 7, 9 )





























