ТЕМА 2 МАТЕРІАЛЬНИЙ І ТЕПЛОВИЙ БАЛАНС






















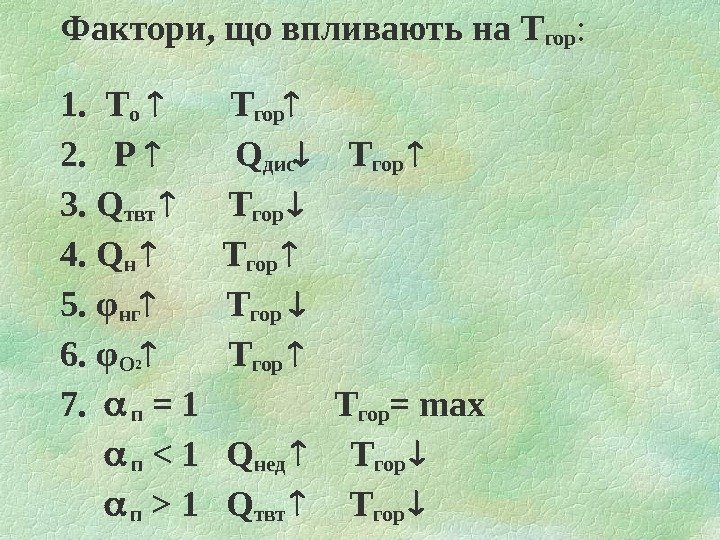

tgv_3_tepl_balans.ppt
- Размер: 285.0 Кб
- Автор:
- Количество слайдов: 28
Описание презентации ТЕМА 2 МАТЕРІАЛЬНИЙ І ТЕПЛОВИЙ БАЛАНС по слайдам
 ТЕМА 2 МАТЕРІАЛЬНИЙ І ТЕПЛОВИЙ БАЛАНС ПРОЦЕСУ ГОРІННЯ Лекція 5 ТЕПЛОТА ЗГОРЯННЯ. ТЕМПЕРАТУРА ГОРІННЯ.
ТЕМА 2 МАТЕРІАЛЬНИЙ І ТЕПЛОВИЙ БАЛАНС ПРОЦЕСУ ГОРІННЯ Лекція 5 ТЕПЛОТА ЗГОРЯННЯ. ТЕМПЕРАТУРА ГОРІННЯ.
 План лекції 1. Тепловий ефект хімічної реакції. 2. Теплота згоряння. Види теплоти згоряння. Розрахункове визначення теплоти згоряння 3. Поняття та види температури горіння речовин. 4. Визначення температури горіння речовин та матеріалів.
План лекції 1. Тепловий ефект хімічної реакції. 2. Теплота згоряння. Види теплоти згоряння. Розрахункове визначення теплоти згоряння 3. Поняття та види температури горіння речовин. 4. Визначення температури горіння речовин та матеріалів.
 1. ТЕПЛОВИЙ ЕФЕКТ ХІМІЧНОЇ РЕАКЦІЇ Тепловий ефект реакції — кількість теплоти, що виділяється чи поглинається системою при протіканні в ній необоротної хімічної реакції за умови сталості температури й об’єму ( Т, V = const ) чи температури і тиску ( Т, P = const ). Хімічна енергія перетворюється в теплову. Початковий і кінцевий рівні енергії системи різняться між собою на величину теплоти реакції Q. E кін – E поч = Q
1. ТЕПЛОВИЙ ЕФЕКТ ХІМІЧНОЇ РЕАКЦІЇ Тепловий ефект реакції — кількість теплоти, що виділяється чи поглинається системою при протіканні в ній необоротної хімічної реакції за умови сталості температури й об’єму ( Т, V = const ) чи температури і тиску ( Т, P = const ). Хімічна енергія перетворюється в теплову. Початковий і кінцевий рівні енергії системи різняться між собою на величину теплоти реакції Q. E кін – E поч = Q
 Якщо E кін 0 , реакція супроводжу-ється виділенням тепла і зветься екзотермічною. Якщо E кін > E поч , то Q < 0 , реакція супроводжу-ється поглинанням тепла і зветься ендотермічною Для визначення теплоти реакції застосовують перший закон термодинаміки: — d. Q = d. U + Pd. V = d. H – Vd. P Якщо горіння відбувається при P =const ( d. P=0) , теплота реакції дорівнює різниці повних ентальпій системи в початковому і кінцевому стані: Q р = — d. H = — H Якщо горіння відбувається при V =const ( d. V=0) , теплота реакції дорівнює різниці між внутрішньою енергією системи в початковому і кінцевому стані: Q v = — d. U = — U
Якщо E кін 0 , реакція супроводжу-ється виділенням тепла і зветься екзотермічною. Якщо E кін > E поч , то Q < 0 , реакція супроводжу-ється поглинанням тепла і зветься ендотермічною Для визначення теплоти реакції застосовують перший закон термодинаміки: — d. Q = d. U + Pd. V = d. H – Vd. P Якщо горіння відбувається при P =const ( d. P=0) , теплота реакції дорівнює різниці повних ентальпій системи в початковому і кінцевому стані: Q р = — d. H = — H Якщо горіння відбувається при V =const ( d. V=0) , теплота реакції дорівнює різниці між внутрішньою енергією системи в початковому і кінцевому стані: Q v = — d. U = — U
 Стандартна теплота реакції — різниця між стандартними теплотами утворення продуктів реакції і вихідних речовин. Qр = — Нхр = — ( nкін Н о f кін — nпоч Н о f поч ) , Стандартна теплота утворення речовини Но f — теплота реакції, в якій утворюється один моль речовини зі складових його елементів за стандартних умов (Р=101, 3 к. Па, Т = 298 К).
Стандартна теплота реакції — різниця між стандартними теплотами утворення продуктів реакції і вихідних речовин. Qр = — Нхр = — ( nкін Н о f кін — nпоч Н о f поч ) , Стандартна теплота утворення речовини Но f — теплота реакції, в якій утворюється один моль речовини зі складових його елементів за стандартних умов (Р=101, 3 к. Па, Т = 298 К).
 2. ТЕПЛОТА ЗГОРЯННЯ Теплота згоряння — кількість тепла, що виділяється під час повного згоряння одиниці кількості ГР за умови, що вихідна суміш та кінцеві ПГ знаходяться за стандартних умов. Оскільки ГР 1 моль, а теплота утворення О 2 та N 2 дорівнює 0 , тепловий ефект реакції горіння становить: гс о fгс і пг о fпггорΔHnΔHnΔÍ іі і гр о fпггорΔHΔHnΔÍ іі
2. ТЕПЛОТА ЗГОРЯННЯ Теплота згоряння — кількість тепла, що виділяється під час повного згоряння одиниці кількості ГР за умови, що вихідна суміш та кінцеві ПГ знаходяться за стандартних умов. Оскільки ГР 1 моль, а теплота утворення О 2 та N 2 дорівнює 0 , тепловий ефект реакції горіння становить: гс о fгс і пг о fпггорΔHnΔHnΔÍ іі і гр о fпггорΔHΔHnΔÍ іі
 2. 1. Види теплоти згоряння Залежно від того, як визначають одиницю кількості ГР, розрізняють теплоти згоряння: молярну Q — кількість тепла, що виділяється при згорянні 1 молю ГР (к. Дж/моль), масову Q / — кількість тепла, що виділяється при згорянні 1 кг ГР (к. Дж/кг), об’ємну Q // — кількість тепла, що виділяється при згорянні 1 м 3 ГР (к. Дж/м 3 ).
2. 1. Види теплоти згоряння Залежно від того, як визначають одиницю кількості ГР, розрізняють теплоти згоряння: молярну Q — кількість тепла, що виділяється при згорянні 1 молю ГР (к. Дж/моль), масову Q / — кількість тепла, що виділяється при згорянні 1 кг ГР (к. Дж/кг), об’ємну Q // — кількість тепла, що виділяється при згорянні 1 м 3 ГР (к. Дж/м 3 ).
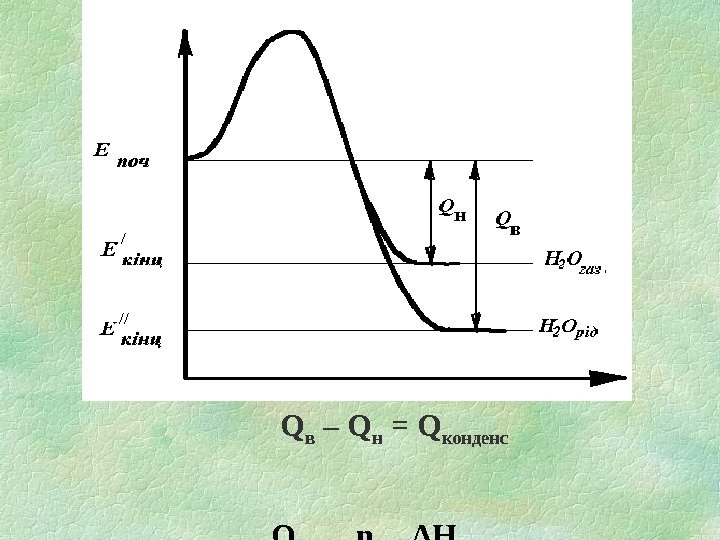
 Залежно від агрегатного стану Н 2 О , яка утворилася під час горіння і знаходиться в ПГ, розрізняють вищу та нижчу теплоту згоряння. Вища теплота згоряння Q в — кількість тепла, що виділяється при повному згорянні одиниці кількості ГР за умови, що вода в ПГ знаходиться у рідкому стані. Нижча теплота згоряння Q н — кількість тепла, що виділяється при повному згорянні одиниці кількості ГР за умови, що вода в ПГ знаходяться в газоподібному стані.
Залежно від агрегатного стану Н 2 О , яка утворилася під час горіння і знаходиться в ПГ, розрізняють вищу та нижчу теплоту згоряння. Вища теплота згоряння Q в — кількість тепла, що виділяється при повному згорянні одиниці кількості ГР за умови, що вода в ПГ знаходиться у рідкому стані. Нижча теплота згоряння Q н — кількість тепла, що виділяється при повному згорянні одиниці кількості ГР за умови, що вода в ПГ знаходяться в газоподібному стані.
 Q в – Q н = Q конденс Q конд = n H 2 O ΔH вип
Q в – Q н = Q конденс Q конд = n H 2 O ΔH вип
 При урахуванні хімічного недопалу, вологості матеріалу, втрати на теплове випромінювання, визначають практичну або робочу теплоту згоряння матеріалу Q н р.
При урахуванні хімічного недопалу, вологості матеріалу, втрати на теплове випромінювання, визначають практичну або робочу теплоту згоряння матеріалу Q н р.
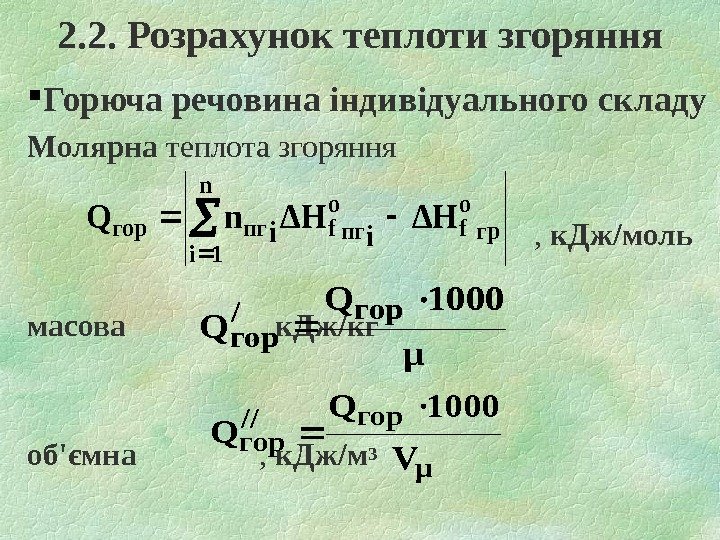
 2. 2. Розрахунок теплоти згоряння Горюча речовина індивідуального складу Молярна теплота згоряння , к. Дж / моль масова , к. Дж/кг об’ємна , к. Дж/м 3μ 1000 Q Q гор/ гор μ гор// гор V 1000 Q Q n 1 i гр о fпггорΔHΔHn. Q іі
2. 2. Розрахунок теплоти згоряння Горюча речовина індивідуального складу Молярна теплота згоряння , к. Дж / моль масова , к. Дж/кг об’ємна , к. Дж/м 3μ 1000 Q Q гор/ гор μ гор// гор V 1000 Q Q n 1 i гр о fпггорΔHΔHn. Q іі
 Горючі матеріали складного хімічного складу суміш газів тверді або рідкі складні матеріали Q скл = Q i g i С тв + (О 2 + 3, 76 N 2 ) = CO 2 + 3, 76 N 2 Q в(Н) =285, 83 к. Дж/моль; Q в(S) = 297, 09 к. Дж/моль к. Джo грf o пгifiв 78, 393078, 393 HHn. Q 100 Qr. QQ n 1 i » iвн n 1 i i » iвн » сумвн i
Горючі матеріали складного хімічного складу суміш газів тверді або рідкі складні матеріали Q скл = Q i g i С тв + (О 2 + 3, 76 N 2 ) = CO 2 + 3, 76 N 2 Q в(Н) =285, 83 к. Дж/моль; Q в(S) = 297, 09 к. Дж/моль к. Джo грf o пгifiв 78, 393078, 393 HHn. Q 100 Qr. QQ n 1 i » iвн n 1 i i » iвн » сумвн i
 Внесок кожного елементу в масову теплоту згоряння: Q в ’ = 327, 6 С + 1429, 2 Н + 92, 8 S ; к. Дж/ кгi iвi i в i / в ‘ в φQ 10 100 φ1000 Q g. Qq μμ С : C C’ вφ327, 6 12 φ393, 0810 q к Д ж / к г ; Н : H H’ вφ1429, 1 2 φ285, 8310 q к Д ж / к г ; S : S S’ вφ92, 8 32 φ297, 0910 q к Д ж / к г.
Внесок кожного елементу в масову теплоту згоряння: Q в ’ = 327, 6 С + 1429, 2 Н + 92, 8 S ; к. Дж/ кгi iвi i в i / в ‘ в φQ 10 100 φ1000 Q g. Qq μμ С : C C’ вφ327, 6 12 φ393, 0810 q к Д ж / к г ; Н : H H’ вφ1429, 1 2 φ285, 8310 q к Д ж / к г ; S : S S’ вφ92, 8 32 φ297, 0910 q к Д ж / к г.
 ФОРМУЛА МЕНДЄЛЄЄВА Враховує наявність в ГР оксигену, нітрогену та вологи. Вища теплота згоряння : Q ′ в = 339, 4 С +1256, 8 Н +108, 9( S – O – N ) , к. Дж/кг Нижча теплота згоряння : Q н / = Q в / -Q конд Q н / = 39, 4 С + 1256, 8 Н + 108, 9 ( S — O — N ) – – 25, 1(9 Н + W ) , к. Дж/ кг де W – мас. відсоток вологи в ГР)W 9(1, 252510 100 W 2 18 ΔHg. QH H вип. OHконд
ФОРМУЛА МЕНДЄЛЄЄВА Враховує наявність в ГР оксигену, нітрогену та вологи. Вища теплота згоряння : Q ′ в = 339, 4 С +1256, 8 Н +108, 9( S – O – N ) , к. Дж/кг Нижча теплота згоряння : Q н / = Q в / -Q конд Q н / = 39, 4 С + 1256, 8 Н + 108, 9 ( S — O — N ) – – 25, 1(9 Н + W ) , к. Дж/ кг де W – мас. відсоток вологи в ГР)W 9(1, 252510 100 W 2 18 ΔHg. QH H вип. OHконд
 ПРАКТИЧНЕ ЗНАЧЕННЯ ТЕПЛОТИ ЗГОРЯННЯ 1) Використовують для розрахунку пожежної навантаги , що є характеристикою теплового впливу пожежі на будівельні конструкції. Пожежна навантага Р — кількість тепла, що може виділитися при згорянні речовин з одиниці поверхні підлоги приміщення. Розрізняють постійну і тимчасову пожежну навантагу. підл n 1 i / нi S Qm Р і
ПРАКТИЧНЕ ЗНАЧЕННЯ ТЕПЛОТИ ЗГОРЯННЯ 1) Використовують для розрахунку пожежної навантаги , що є характеристикою теплового впливу пожежі на будівельні конструкції. Пожежна навантага Р — кількість тепла, що може виділитися при згорянні речовин з одиниці поверхні підлоги приміщення. Розрізняють постійну і тимчасову пожежну навантагу. підл n 1 i / нi S Qm Р і
 2) Використовують для визначення горючості речовини. Речовини є негорючими, якщо вони не відносяться до вибухонебезпечних та їх Qн / менша за 2100 к. Дж/кг або 1830 к. Дж/м 3. 3) Використовують при розрахунку параметрів пожежної небезпеки речовин, таких як температура горіння, температура вибуху, максимальний тиск вибуху, нижча концентраційна межа поширення полум’я.
2) Використовують для визначення горючості речовини. Речовини є негорючими, якщо вони не відносяться до вибухонебезпечних та їх Qн / менша за 2100 к. Дж/кг або 1830 к. Дж/м 3. 3) Використовують при розрахунку параметрів пожежної небезпеки речовин, таких як температура горіння, температура вибуху, максимальний тиск вибуху, нижча концентраційна межа поширення полум’я.
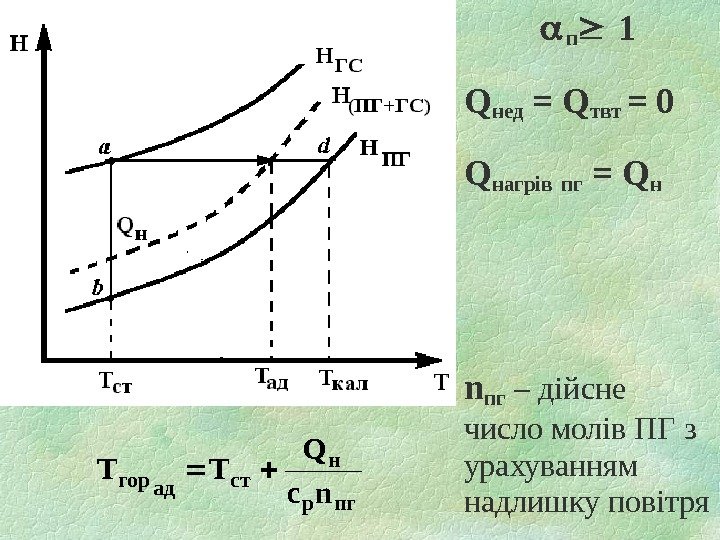
 3. ПОНЯТТЯ ТА ВИДИ ТЕМПЕРАТУРИ ГОРІННЯ РЕЧОВИН Температура горіння — температура, до якої нагріваються продукти горіння в зоні реакції. Розрахувати температуру горіння можна знаючи величину теплоти згоряння. Рівняння теплового балансу під час горіння має вигляд: Q гор – Q нед = Q нагр. пг + Q твт , Залежно від умов, в яких протікає процес горіння, розрізняють температури горіння калориметричну , теоретичну , адіабатичну , дійсну.
3. ПОНЯТТЯ ТА ВИДИ ТЕМПЕРАТУРИ ГОРІННЯ РЕЧОВИН Температура горіння — температура, до якої нагріваються продукти горіння в зоні реакції. Розрахувати температуру горіння можна знаючи величину теплоти згоряння. Рівняння теплового балансу під час горіння має вигляд: Q гор – Q нед = Q нагр. пг + Q твт , Залежно від умов, в яких протікає процес горіння, розрізняють температури горіння калориметричну , теоретичну , адіабатичну , дійсну.
 Калориметрична температура горіння — температура, до якої нагріваються ПГ, якщо виконуються наступні умови: 1) вихідна система знаходиться за стандартних умов (Т о =298 К, Р о =101, 3 к. Па); 2) відбувається повне згоряння ГР, при цьому повітря для горіння надходить у стехіометричному співвідношенні; 3) в процесі утворення ПГ не відбувається їх дисоціація; 4) немає тепловтрат від системи в навколишнє середовище.
Калориметрична температура горіння — температура, до якої нагріваються ПГ, якщо виконуються наступні умови: 1) вихідна система знаходиться за стандартних умов (Т о =298 К, Р о =101, 3 к. Па); 2) відбувається повне згоряння ГР, при цьому повітря для горіння надходить у стехіометричному співвідношенні; 3) в процесі утворення ПГ не відбувається їх дисоціація; 4) немає тепловтрат від системи в навколишнє середовище.
 Через відсутність тепловтрат і недопалу вважаємо, що все тепло, що виділилося під час реакції, іде на нагрівання ПГ. ПГ в зоні реакції мають високу температуру, отже вода в ПГ залишається в газоподібному стані, тому в розрахунках використовують нижчу теплоту згоряння. Qнед = Qтвт = 0 , Qнагрів пг = Qн i iпгpiпг н сткалгор cn Q ТТ )ТТ(cn. Qстгор i iпгpiпгнагр. ПГ
Через відсутність тепловтрат і недопалу вважаємо, що все тепло, що виділилося під час реакції, іде на нагрівання ПГ. ПГ в зоні реакції мають високу температуру, отже вода в ПГ залишається в газоподібному стані, тому в розрахунках використовують нижчу теплоту згоряння. Qнед = Qтвт = 0 , Qнагрів пг = Qн i iпгpiпг н сткалгор cn Q ТТ )ТТ(cn. Qстгор i iпгpiпгнагр. ПГ
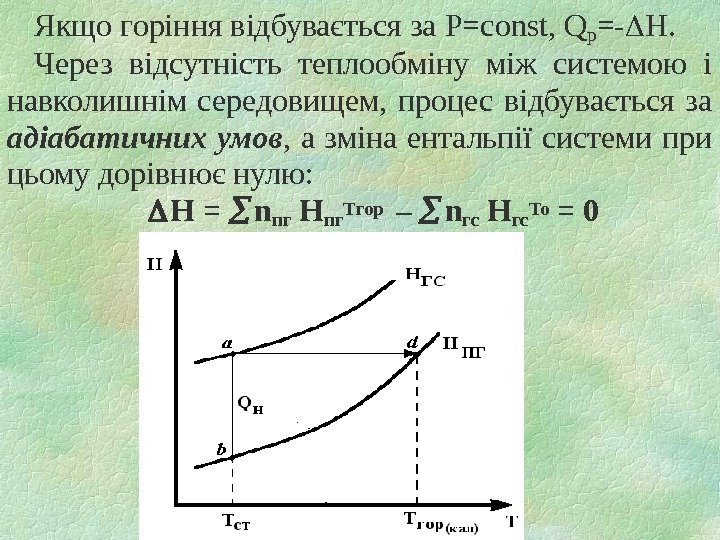
 Якщо горіння відбувається за P=const , Qр =- H. Через відсутність теплообміну між системою і навколишнім середовищем, процес відбувається за адіабатичних умов , а зміна ентальпії системи при цьому дорівнює нулю: Н = n пг Hпг Тгор – n гс Hгс То =
Якщо горіння відбувається за P=const , Qр =- H. Через відсутність теплообміну між системою і навколишнім середовищем, процес відбувається за адіабатичних умов , а зміна ентальпії системи при цьому дорівнює нулю: Н = n пг Hпг Тгор – n гс Hгс То =
 Якщо Тгор достатньо висока, то ПГ можуть дисоціювати з витратою значної кількості тепла. 2 СО 2 = 2 СО + О 2 – 566 к. Дж 2 Н 2 О = 2 Н 2 + О 2 – 478 к. Дж Теоретична температура горіння — ступінь нагрітості продуктів горіння з урахуванням їх дисоціації, якщо виконуються наступні умови: 1) вихідна ГС знаходиться за стандартних умов; 2) відбувається повне згоряння горючої суміші стехіометричного складу; 3) відбувається суттєва дисоціація ПГ; 4) немає тепловтрат від системи в навколишнє середовище.
Якщо Тгор достатньо висока, то ПГ можуть дисоціювати з витратою значної кількості тепла. 2 СО 2 = 2 СО + О 2 – 566 к. Дж 2 Н 2 О = 2 Н 2 + О 2 – 478 к. Дж Теоретична температура горіння — ступінь нагрітості продуктів горіння з урахуванням їх дисоціації, якщо виконуються наступні умови: 1) вихідна ГС знаходиться за стандартних умов; 2) відбувається повне згоряння горючої суміші стехіометричного складу; 3) відбувається суттєва дисоціація ПГ; 4) немає тепловтрат від системи в навколишнє середовище.
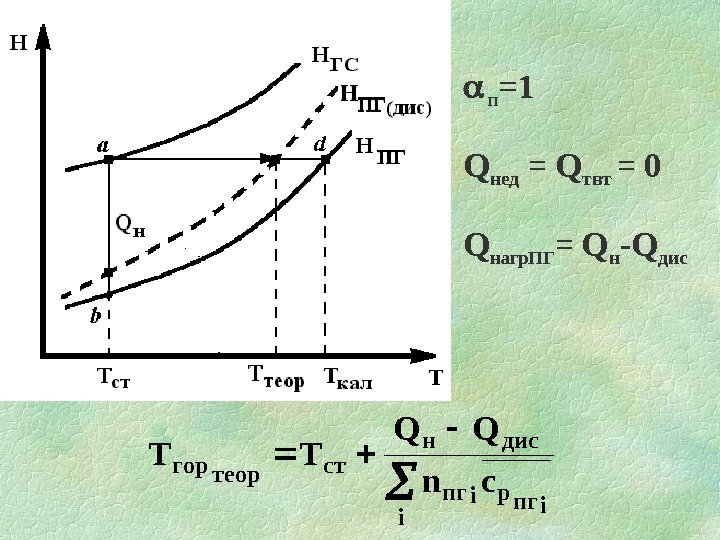
 п = 1 Q нед = Q твт = 0 Q нагр. ПГ = Q н — Q дис i iпгp iпг дисн ст теоргор cn QQ ТТ
п = 1 Q нед = Q твт = 0 Q нагр. ПГ = Q н — Q дис i iпгp iпг дисн ст теоргор cn QQ ТТ
 Адіабатична температура горіння — температура, до якої нагріваються продукти горіння за умов: 1) вихідна ГС знаходиться за стандартних умов; 2) горіння відбувається з надлишком чи нестачею повітря; 3) дисоціація ПГ не відбувається; 4) немає тепловтрат від системи в навколишнє середовище.
Адіабатична температура горіння — температура, до якої нагріваються продукти горіння за умов: 1) вихідна ГС знаходиться за стандартних умов; 2) горіння відбувається з надлишком чи нестачею повітря; 3) дисоціація ПГ не відбувається; 4) немає тепловтрат від системи в навколишнє середовище.
 п 1 Q нед = Qтвт = 0 Q нагрів пг = Qн n пг – дійсне число молів ПГ з урахуванням надлишку повітря пгp н стадгор nc Q ТТ
п 1 Q нед = Qтвт = 0 Q нагрів пг = Qн n пг – дійсне число молів ПГ з урахуванням надлишку повітря пгp н стадгор nc Q ТТ
 Дійсна температура горіння – температура, до якої нагріваються продукти горіння за реальних умов, при цьому враховується: 1) горіння може проходити з надлишком або нестачею повітря, 2) значні тепловтрати у навколишнє середовище, 3) початкові умови, в яких знаходиться вихідна горюча суміш, можуть відрізнятися від стандартних. .
Дійсна температура горіння – температура, до якої нагріваються продукти горіння за реальних умов, при цьому враховується: 1) горіння може проходити з надлишком або нестачею повітря, 2) значні тепловтрати у навколишнє середовище, 3) початкові умови, в яких знаходиться вихідна горюча суміш, можуть відрізнятися від стандартних. .
 де Q недоп — кількість тепла, яка не реалізується в зоні горіння внаслідок хімічного або фізичного недопалу. Q нед = (1 — ) Q н , — коефіцієнт повноти згоряння = 0, 9 0, 75 Q твт — кількість тепла, що втрачається в навколишнє середовище. о пгp недоптвтн гор Т nс QQQ Т дійсн
де Q недоп — кількість тепла, яка не реалізується в зоні горіння внаслідок хімічного або фізичного недопалу. Q нед = (1 — ) Q н , — коефіцієнт повноти згоряння = 0, 9 0, 75 Q твт — кількість тепла, що втрачається в навколишнє середовище. о пгp недоптвтн гор Т nс QQQ Т дійсн
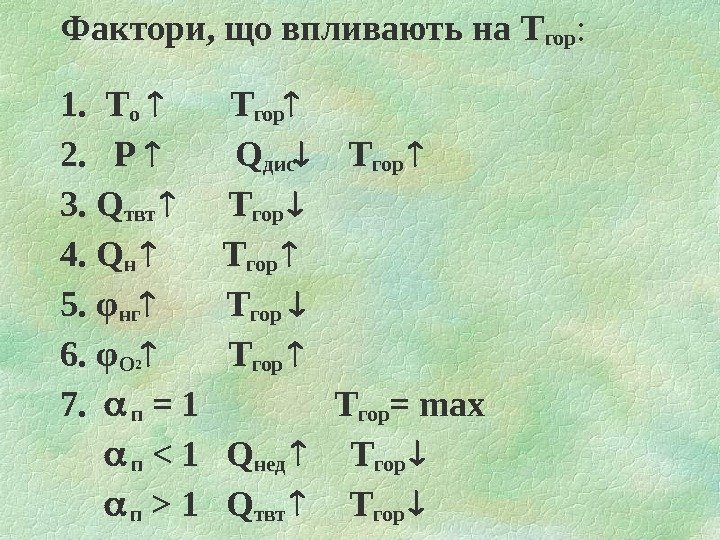 Фактори, що впливають на Тгор : 1. Т о Тгор 2. Р Q дис Тгор 3. Q твт Тгор 4. Q н Тгор 5. φ нг Тгор 6. φ О 2 Тгор 7. п = 1 Тгор = max п 1 Qтвт Тгор
Фактори, що впливають на Тгор : 1. Т о Тгор 2. Р Q дис Тгор 3. Q твт Тгор 4. Q н Тгор 5. φ нг Тгор 6. φ О 2 Тгор 7. п = 1 Тгор = max п 1 Qтвт Тгор
 Завдання на самопідготовку 1. Вивчити матеріал Демидов, Шанд ы ба, Щеглов, Горение и свойства горючих веществ, стор. 29 – 33. Демидов, Саушев. Горение и свойства горючих веществ, стор. 24 -42.
Завдання на самопідготовку 1. Вивчити матеріал Демидов, Шанд ы ба, Щеглов, Горение и свойства горючих веществ, стор. 29 – 33. Демидов, Саушев. Горение и свойства горючих веществ, стор. 24 -42.

