+Программа 151 и 152 Тема 1.1.pptx
- Количество слайдов: 18
 ТЕМА 1. 1 Строение атома и атомного ядра. Явление радиоактивности
ТЕМА 1. 1 Строение атома и атомного ядра. Явление радиоактивности
 2 Изучаемые вопросы • Понятия: материал, вещество, молекула, атом. • Строение атома. Периодическая система химических элементов. • Строение ядер атомов. Изотопы. • Явление радиоактивности. Виды радиоактивного распада и радиоактивного излучения. • Понятие о самоподдерживающейся цепной реакции деления ядер.
2 Изучаемые вопросы • Понятия: материал, вещество, молекула, атом. • Строение атома. Периодическая система химических элементов. • Строение ядер атомов. Изотопы. • Явление радиоактивности. Виды радиоактивного распада и радиоактивного излучения. • Понятие о самоподдерживающейся цепной реакции деления ядер.
 3 Материал и вещество • Материал (от лат. materialis – вещественный) – вещество, предметы, идущие на изготовление чегонибудь. • Вещество – то, из чего состоит физическое тело; вид материи, элементы которой – атомы, молекулы и т. п. – обладают массой покоя.
3 Материал и вещество • Материал (от лат. materialis – вещественный) – вещество, предметы, идущие на изготовление чегонибудь. • Вещество – то, из чего состоит физическое тело; вид материи, элементы которой – атомы, молекулы и т. п. – обладают массой покоя.
 4 Молекула и атом • Молекула (от лат. moles – масса) – мельчайшая частица вещества, способная существовать самостоятельно и обладающая всеми химическими свойствами данного вещества. • Атом (от греч. atomos – неделимый) – мельчайшая частица химического элемента, сохраняющая его свойства.
4 Молекула и атом • Молекула (от лат. moles – масса) – мельчайшая частица вещества, способная существовать самостоятельно и обладающая всеми химическими свойствами данного вещества. • Атом (от греч. atomos – неделимый) – мельчайшая частица химического элемента, сохраняющая его свойства.
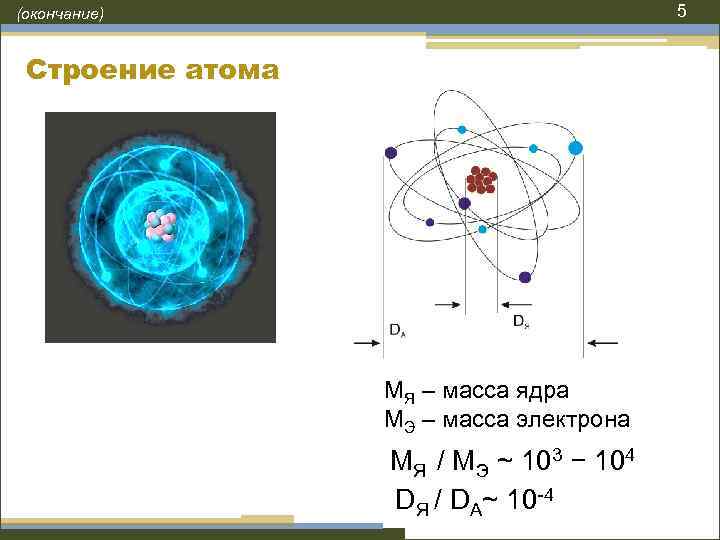 5 (окончание) Строение атома МЯ – масса ядра МЭ – масса электрона МЯ / МЭ ~ 103 − 104 DЯ / DA~ 10 -4
5 (окончание) Строение атома МЯ – масса ядра МЭ – масса электрона МЯ / МЭ ~ 103 − 104 DЯ / DA~ 10 -4
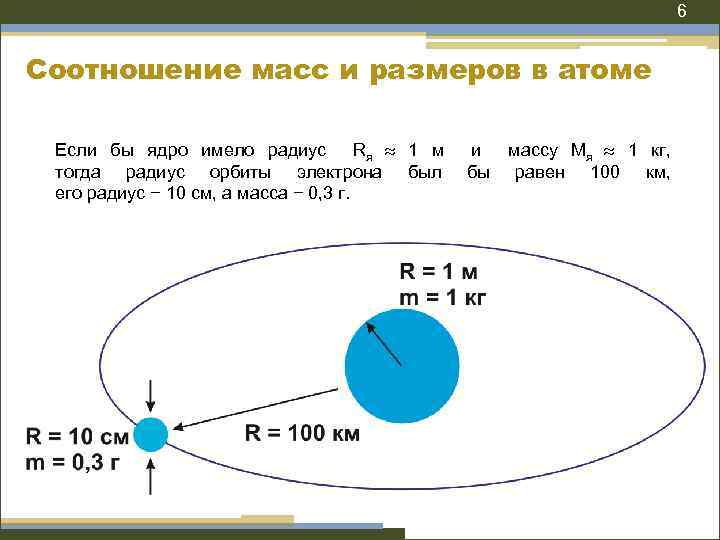 6 Соотношение масс и размеров в атоме Если бы ядро имело радиус Rя 1 м тогда радиус орбиты электрона был его радиус − 10 см, а масса − 0, 3 г. и бы массу Мя 1 кг, равен 100 км,
6 Соотношение масс и размеров в атоме Если бы ядро имело радиус Rя 1 м тогда радиус орбиты электрона был его радиус − 10 см, а масса − 0, 3 г. и бы массу Мя 1 кг, равен 100 км,
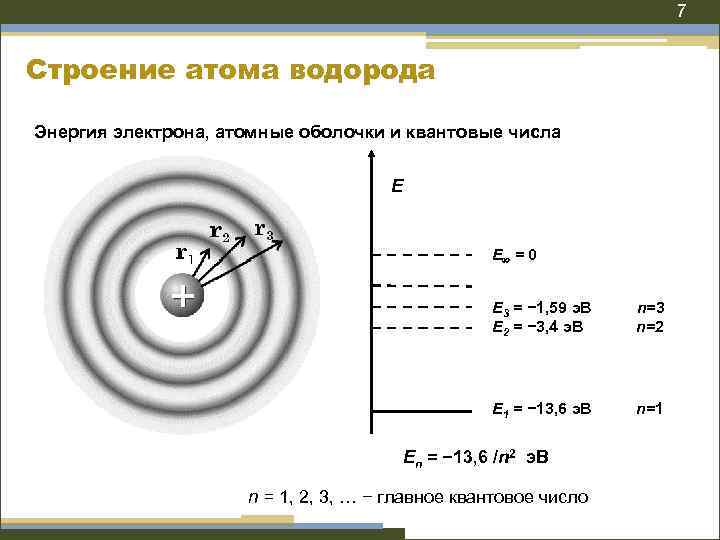 7 Строение атома водорода Энергия электрона, атомные оболочки и квантовые числа Е E = 0 E 3 = − 1, 59 э. В E 2 = − 3, 4 э. В n=3 n=2 E 1 = − 13, 6 э. В n=1 Еn = − 13, 6 /n 2 э. В n = 1, 2, 3, … − главное квантовое число
7 Строение атома водорода Энергия электрона, атомные оболочки и квантовые числа Е E = 0 E 3 = − 1, 59 э. В E 2 = − 3, 4 э. В n=3 n=2 E 1 = − 13, 6 э. В n=1 Еn = − 13, 6 /n 2 э. В n = 1, 2, 3, … − главное квантовое число
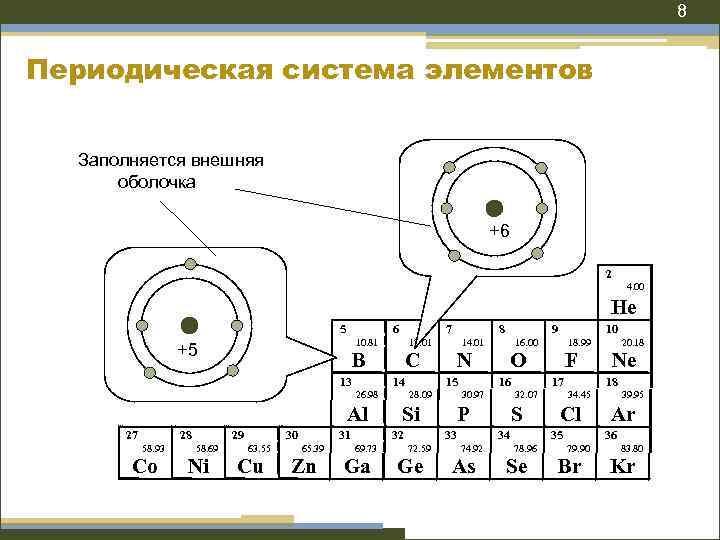 8 Периодическая система элементов Заполняется внешняя оболочка +6 2 4. 00 He 5 6 7 10. 81 +5 B 13 14 27 28 58. 93 Co 29 58. 69 Ni 30 63. 55 Cu 31 65. 39 Zn Ga N 15 28. 09 Ge 17 S 34 As F 32. 07 P 74. 92 18. 99 O 16 33 72. 59 10 16. 00 30. 97 Si 32 69. 73 9 14. 01 C 26. 98 Al 8 12. 01 Se Ne 18 34. 45 Cl 35 78. 96 20. 18 39. 95 Ar 36 79. 90 Br 83. 80 Kr
8 Периодическая система элементов Заполняется внешняя оболочка +6 2 4. 00 He 5 6 7 10. 81 +5 B 13 14 27 28 58. 93 Co 29 58. 69 Ni 30 63. 55 Cu 31 65. 39 Zn Ga N 15 28. 09 Ge 17 S 34 As F 32. 07 P 74. 92 18. 99 O 16 33 72. 59 10 16. 00 30. 97 Si 32 69. 73 9 14. 01 C 26. 98 Al 8 12. 01 Se Ne 18 34. 45 Cl 35 78. 96 20. 18 39. 95 Ar 36 79. 90 Br 83. 80 Kr
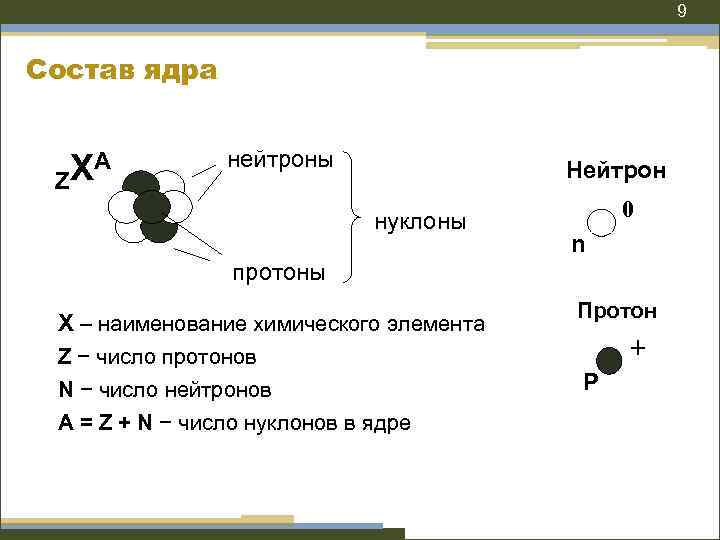 9 Состав ядра XA Z нейтроны Нейтрон нуклоны 0 n протоны Х – наименование химического элемента Z − число протонов N − число нейтронов A = Z + N − число нуклонов в ядре Протон + Р
9 Состав ядра XA Z нейтроны Нейтрон нуклоны 0 n протоны Х – наименование химического элемента Z − число протонов N − число нейтронов A = Z + N − число нуклонов в ядре Протон + Р
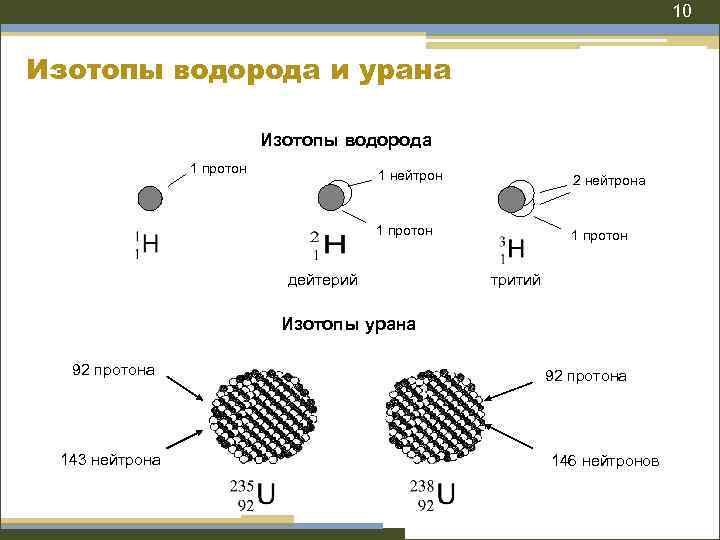 10 Изотопы водорода и урана Изотопы водорода 1 протон 1 нейтрон 2 нейтрона 1 протон дейтерий тритий Изотопы урана 92 протона 143 нейтрона 92 протона 146 нейтронов
10 Изотопы водорода и урана Изотопы водорода 1 протон 1 нейтрон 2 нейтрона 1 протон дейтерий тритий Изотопы урана 92 протона 143 нейтрона 92 протона 146 нейтронов
 11 Открытие радиоактивности А. Беккерель, 1896 г. Пьер и Мария Кюри, соли урана 1898 г. урановая руда
11 Открытие радиоактивности А. Беккерель, 1896 г. Пьер и Мария Кюри, соли урана 1898 г. урановая руда
 12 Свойства радиоактивных излучений Радиоактивное излучение: • действует на фотопленку; • ионизирует воздух; • вызывает люминесценцию некоторых веществ; • проникает сквозь металл.
12 Свойства радиоактивных излучений Радиоактивное излучение: • действует на фотопленку; • ионизирует воздух; • вызывает люминесценцию некоторых веществ; • проникает сквозь металл.
 13 Состав радиоактивных излучений Э. Резерфорд, 1898 г. Виды радиоактивных излучений
13 Состав радиоактивных излучений Э. Резерфорд, 1898 г. Виды радиоактивных излучений
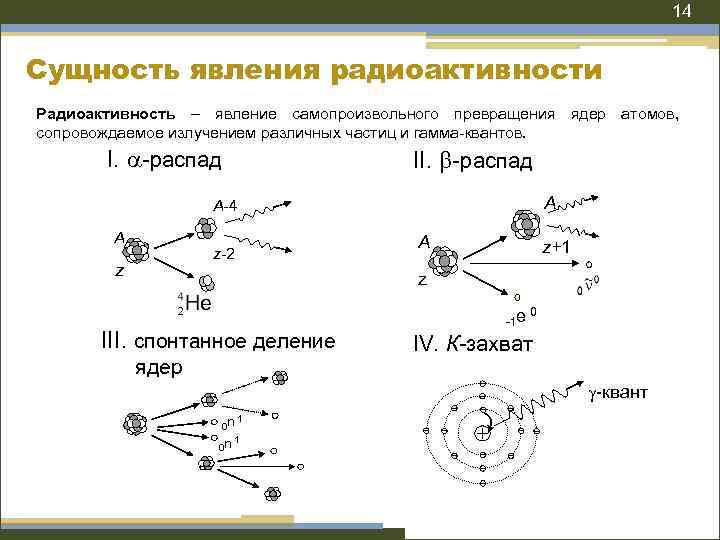 14 Сущность явления радиоактивности Радиоактивность – явление самопроизвольного превращения ядер атомов, сопровождаемое излучением различных частиц и гамма-квантов. I. -распад II. -распад A A-4 А z-2 z A z+1 z III. спонтанное деление ядер -1 e 0 IV. К-захват -квант 1 0 n + Z
14 Сущность явления радиоактивности Радиоактивность – явление самопроизвольного превращения ядер атомов, сопровождаемое излучением различных частиц и гамма-квантов. I. -распад II. -распад A A-4 А z-2 z A z+1 z III. спонтанное деление ядер -1 e 0 IV. К-захват -квант 1 0 n + Z
 15 Основной закон радиоактивного распада дочернее ядро материнское ядро N(t) = N 0 exp(- t) Количество радиоактивных ядер с течением времени уменьшается t
15 Основной закон радиоактивного распада дочернее ядро материнское ядро N(t) = N 0 exp(- t) Количество радиоактивных ядер с течением времени уменьшается t
 16 Период полураспада N(t) = N 0 exp(- t) – период полураспада
16 Период полураспада N(t) = N 0 exp(- t) – период полураспада
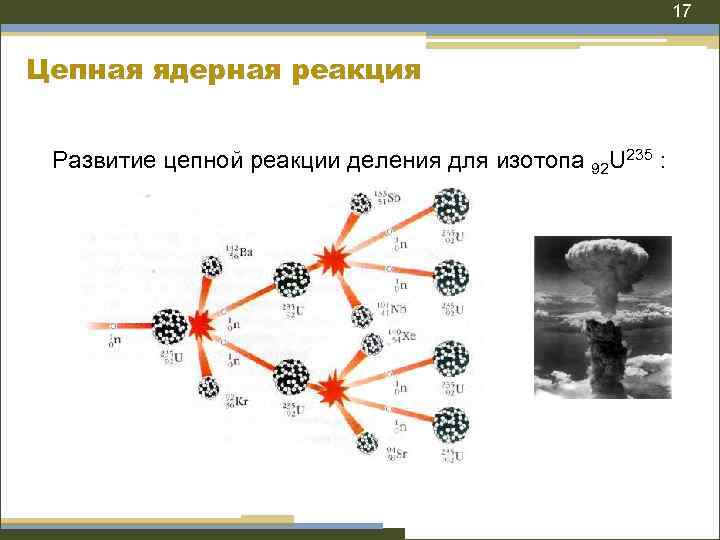 17 Цепная ядерная реакция Развитие цепной реакции деления для изотопа 92 U 235 :
17 Цепная ядерная реакция Развитие цепной реакции деления для изотопа 92 U 235 :
 18 Контрольные вопросы 1. Как устроен атом? 2. Сколько электронов в нейтральном атоме? 3. Сколько электронов может располагаться на электронных оболочках? 4. Из каких частиц состоит ядро атома? 5. Какие ядра называются изотопами? 6. Что называется явлением радиоактивности? 7. Что описывает основной закон радиоактивного распада? 8. Что называется периодом полураспада? 9. Что представляет собой цепная ядерная реакция?
18 Контрольные вопросы 1. Как устроен атом? 2. Сколько электронов в нейтральном атоме? 3. Сколько электронов может располагаться на электронных оболочках? 4. Из каких частиц состоит ядро атома? 5. Какие ядра называются изотопами? 6. Что называется явлением радиоактивности? 7. Что описывает основной закон радиоактивного распада? 8. Что называется периодом полураспада? 9. Что представляет собой цепная ядерная реакция?


