Описание презентации Свойства газов 19. 11. 2016 г. Внутренняя по слайдам
 Свойства газов 19. 11. 2016 г.
Свойства газов 19. 11. 2016 г.
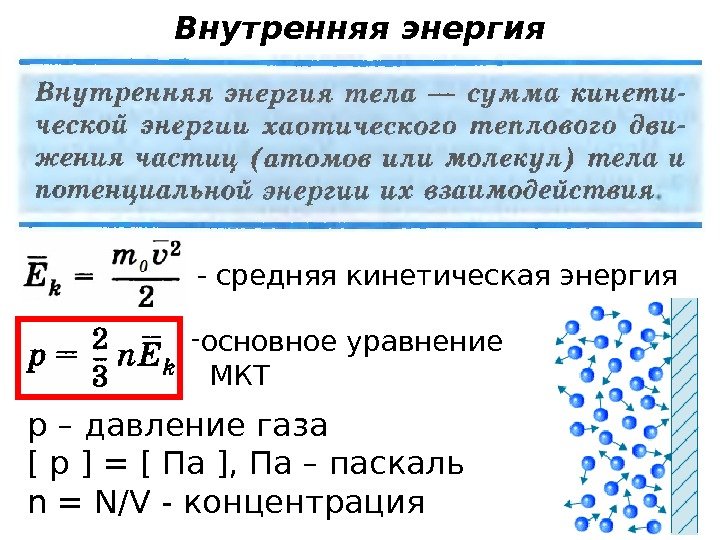 Внутренняя энергия — средняя кинетическая энергия — основное уравнение МКТ р – давление газа [ р ] = [ Па ], Па – паскаль n = N/V — концентрация
Внутренняя энергия — средняя кинетическая энергия — основное уравнение МКТ р – давление газа [ р ] = [ Па ], Па – паскаль n = N/V — концентрация
![- средняя кинетическая энергия движения молекул вещества. Т – обозначение температуры [ Т ] - средняя кинетическая энергия движения молекул вещества. Т – обозначение температуры [ Т ]](//present5.com/presentforday2/20170306/svoystva_gazov_images/svoystva_gazov_2.jpg) — средняя кинетическая энергия движения молекул вещества. Т – обозначение температуры [ Т ] = [К ], К – градус кельвина [ t ] = [ 0 С ] – бытовая единица измерения 0 С – градус Цельсия — постоянная Больцмана
— средняя кинетическая энергия движения молекул вещества. Т – обозначение температуры [ Т ] = [К ], К – градус кельвина [ t ] = [ 0 С ] – бытовая единица измерения 0 С – градус Цельсия — постоянная Больцмана
 — постоянная Больцмана- основное уравнение МКТ n = N/V — концентрация Людвиг Больцман
— постоянная Больцмана- основное уравнение МКТ n = N/V — концентрация Людвиг Больцман
 Уравнение состояния газа — газовая постоянная
Уравнение состояния газа — газовая постоянная
 Изопроцессы
Изопроцессы
 Изопроцессы
Изопроцессы
 Изопроцессы
Изопроцессы
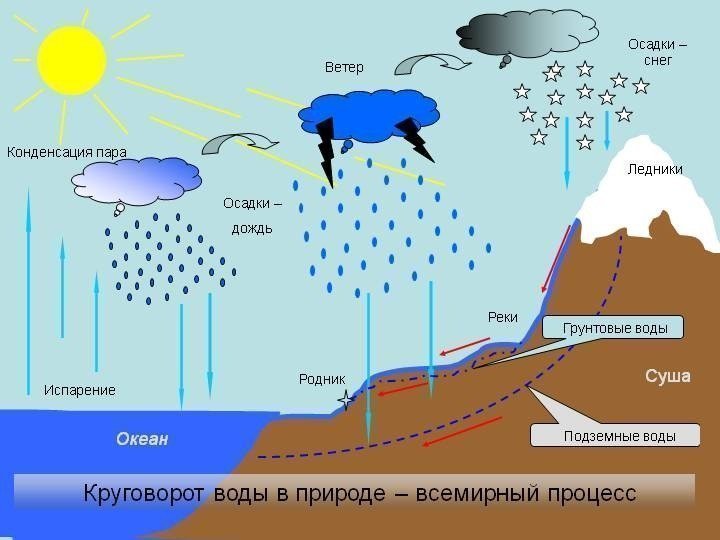
 Парообразование и конденсация
Парообразование и конденсация
 — кол-во теплоты для парообразования — кол-во теплоты при конденсации — удельная теплота парообразования (конденсации), Дж/кг. Парообразование и конденсация
— кол-во теплоты для парообразования — кол-во теплоты при конденсации — удельная теплота парообразования (конденсации), Дж/кг. Парообразование и конденсация
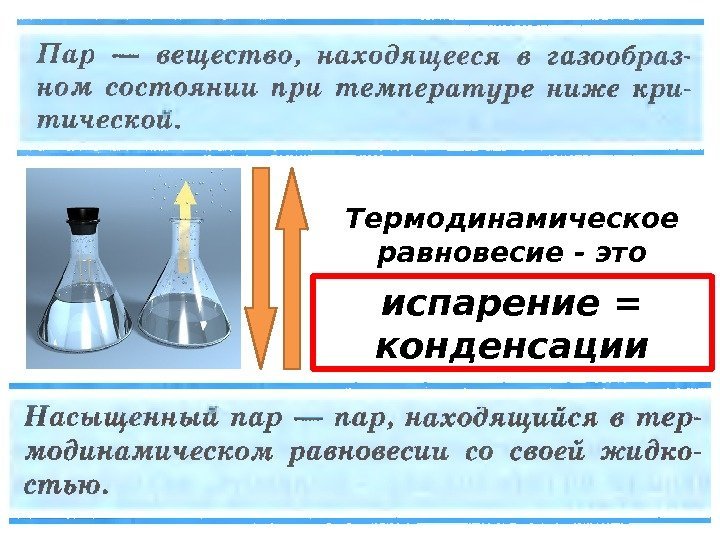 испарение = конденсации. Термодинамическое равновесие — это
испарение = конденсации. Термодинамическое равновесие — это
 Спасибо за внимание!
Спасибо за внимание!



![- средняя кинетическая энергия движения молекул вещества. Т – обозначение температуры [ Т ] - средняя кинетическая энергия движения молекул вещества. Т – обозначение температуры [ Т ]](http://present5.com/presentforday2/20170306/svoystva_gazov_images/svoystva_gazov_2.jpg)