Старение и апоптоз, 2014.ppt
- Количество слайдов: 20
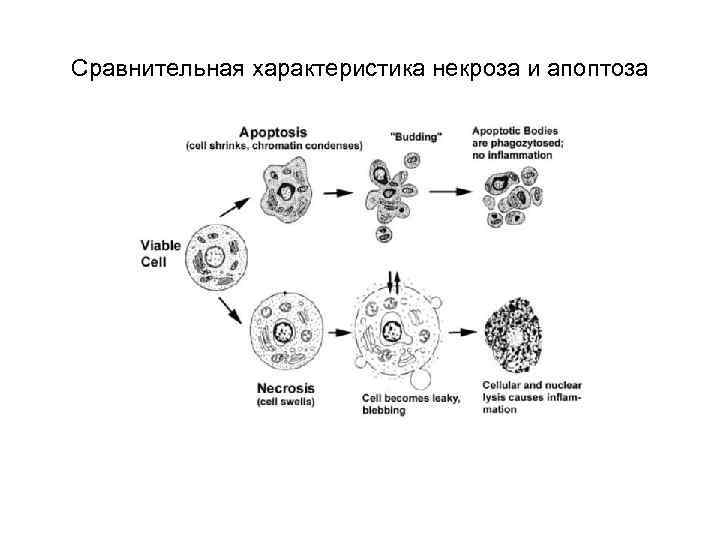 Сравнительная характеристика некроза и апоптоза
Сравнительная характеристика некроза и апоптоза
 Признак Апоптоз Некроз Индукция Активируется физиологическими или патологическими стимулами Различная в зависимости от повреждающего фактора Распространенно сть Одиночная клетка Группа клеток Биохимические изменения Энергозависимая фрагментация ДНК эндогенными эндонуклеазами. Лизосомы интактные. Нарушение или прекращение ионного обмена. Из лизосом высвобождаются ферменты. Распад ДНК Внутриядерная конденсация с расщеплением на фрагменты Диффузная локализация в некротизированной клетке Целостность клеточной мембраны Сохранена Нарушена Морфология Сморщивание клеток и фрагментация с формированием апоптотических телец с уплотненным хроматином Набухание и лизис клеток Воспалительный ответ Нет Обычно есть Удаление погибших клеток Поглощение (фагоцитоз) соседними клетками Поглощение (фагоцитоз) нейтрофилами и макрофагами
Признак Апоптоз Некроз Индукция Активируется физиологическими или патологическими стимулами Различная в зависимости от повреждающего фактора Распространенно сть Одиночная клетка Группа клеток Биохимические изменения Энергозависимая фрагментация ДНК эндогенными эндонуклеазами. Лизосомы интактные. Нарушение или прекращение ионного обмена. Из лизосом высвобождаются ферменты. Распад ДНК Внутриядерная конденсация с расщеплением на фрагменты Диффузная локализация в некротизированной клетке Целостность клеточной мембраны Сохранена Нарушена Морфология Сморщивание клеток и фрагментация с формированием апоптотических телец с уплотненным хроматином Набухание и лизис клеток Воспалительный ответ Нет Обычно есть Удаление погибших клеток Поглощение (фагоцитоз) соседними клетками Поглощение (фагоцитоз) нейтрофилами и макрофагами
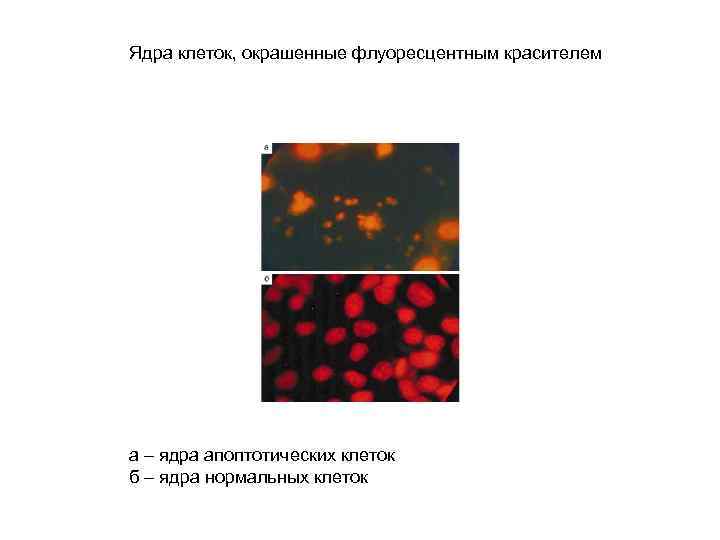 Ядра клеток, окрашенные флуоресцентным красителем а – ядра апоптотических клеток б – ядра нормальных клеток
Ядра клеток, окрашенные флуоресцентным красителем а – ядра апоптотических клеток б – ядра нормальных клеток
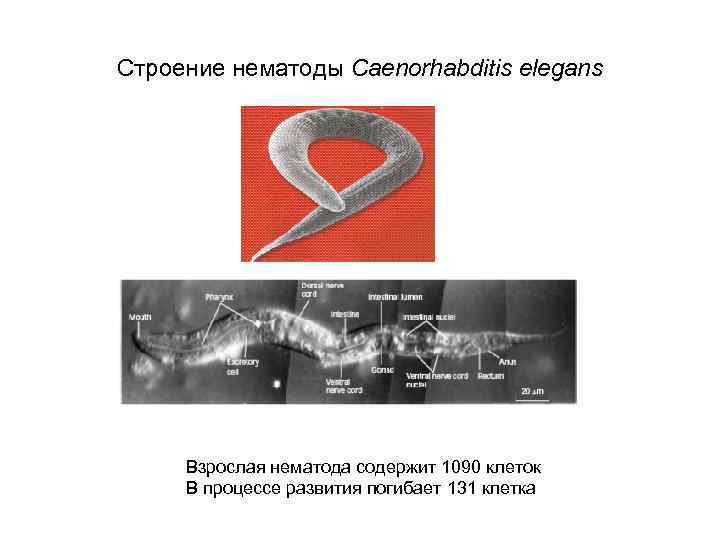 Строение нематоды Caenorhabditis elegans Взрослая нематода содержит 1090 клеток В процессе развития погибает 131 клетка
Строение нематоды Caenorhabditis elegans Взрослая нематода содержит 1090 клеток В процессе развития погибает 131 клетка
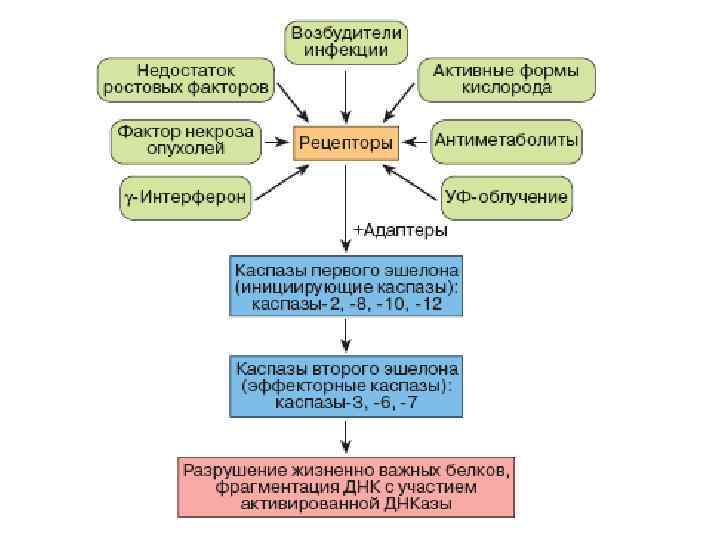 Основные факторы, вызывающие апоптоз и последовательность событий при апоптозе
Основные факторы, вызывающие апоптоз и последовательность событий при апоптозе
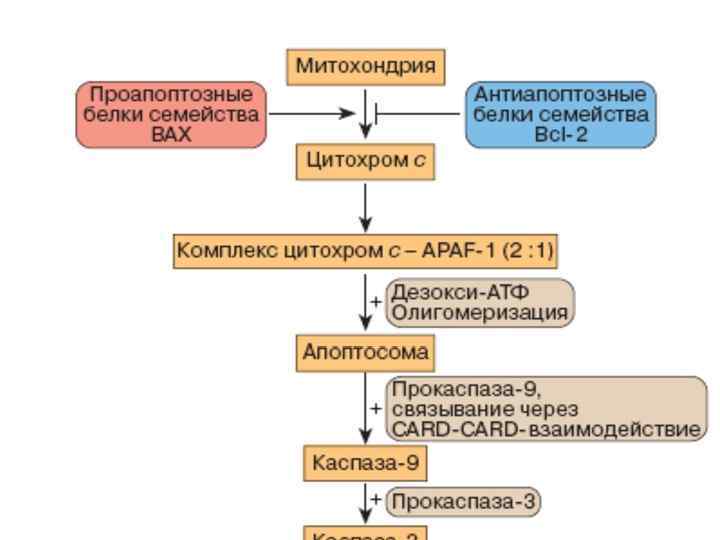 Схема активации каспаз в митохондриях
Схема активации каспаз в митохондриях
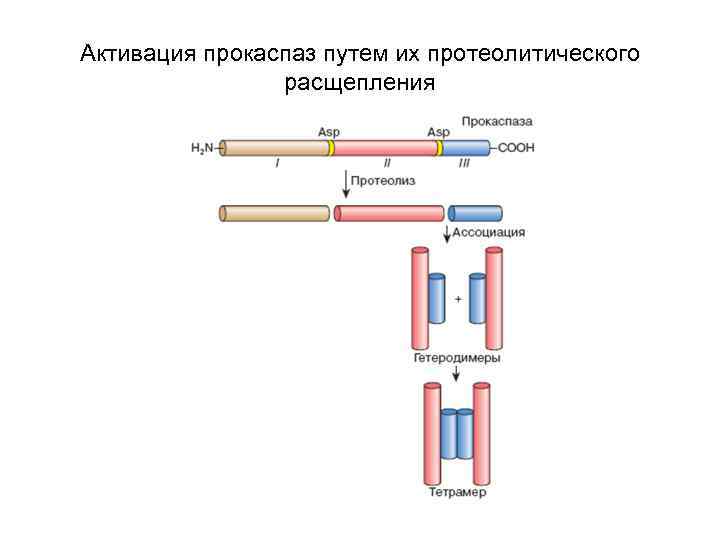 Активация прокаспаз путем их протеолитического расщепления
Активация прокаспаз путем их протеолитического расщепления
 Роль регуляторных белков Bax и Bcl-2 в регуляции апоптоза
Роль регуляторных белков Bax и Bcl-2 в регуляции апоптоза
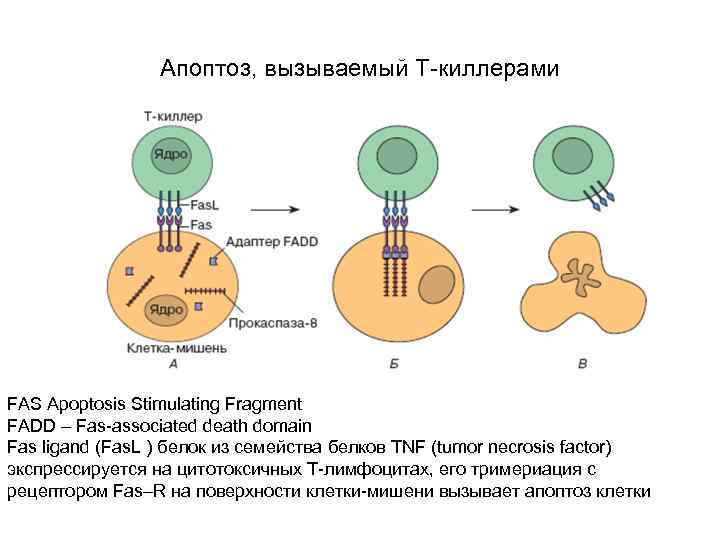 Апоптоз, вызываемый Т-киллерами FAS Apoptosis Stimulating Fragment FADD – Fas-associated death domain Fas ligand (Fas. L ) белок из семейства белков TNF (tumor necrosis factor) экспрессируется на цитотоксичных Т-лимфоцитах, его тримериация с рецептором Fas–R на поверхности клетки-мишени вызывает апоптоз клетки
Апоптоз, вызываемый Т-киллерами FAS Apoptosis Stimulating Fragment FADD – Fas-associated death domain Fas ligand (Fas. L ) белок из семейства белков TNF (tumor necrosis factor) экспрессируется на цитотоксичных Т-лимфоцитах, его тримериация с рецептором Fas–R на поверхности клетки-мишени вызывает апоптоз клетки
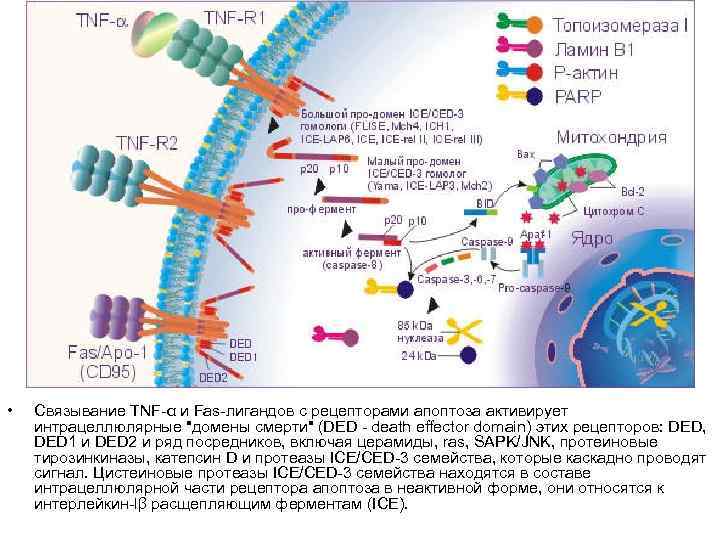 • Связывание TNF-α и Fas-лигандов с рецепторами апоптоза активирует интрацеллюлярные "домены смерти" (DED - death effector domain) этих рецепторов: DED, DED 1 и DED 2 и ряд посредников, включая церамиды, ras, SAPK/JNK, протеиновые тирозинкиназы, катепсин D и протеазы ICE/CED-3 семейства, которые каскадно проводят сигнал. Цистеиновые протеазы ICE/CED-3 семейства находятся в составе интрацеллюлярной части рецептора апоптоза в неактивной форме, они относятся к интерлейкин-lβ расщепляющим ферментам (ICE).
• Связывание TNF-α и Fas-лигандов с рецепторами апоптоза активирует интрацеллюлярные "домены смерти" (DED - death effector domain) этих рецепторов: DED, DED 1 и DED 2 и ряд посредников, включая церамиды, ras, SAPK/JNK, протеиновые тирозинкиназы, катепсин D и протеазы ICE/CED-3 семейства, которые каскадно проводят сигнал. Цистеиновые протеазы ICE/CED-3 семейства находятся в составе интрацеллюлярной части рецептора апоптоза в неактивной форме, они относятся к интерлейкин-lβ расщепляющим ферментам (ICE).
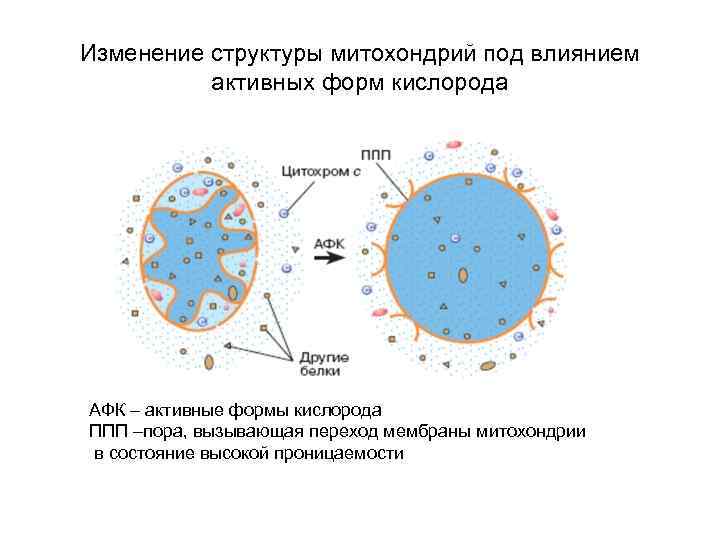 Изменение структуры митохондрий под влиянием активных форм кислорода АФК – активные формы кислорода ППП –пора, вызывающая переход мембраны митохондрии в состояние высокой проницаемости
Изменение структуры митохондрий под влиянием активных форм кислорода АФК – активные формы кислорода ППП –пора, вызывающая переход мембраны митохондрии в состояние высокой проницаемости
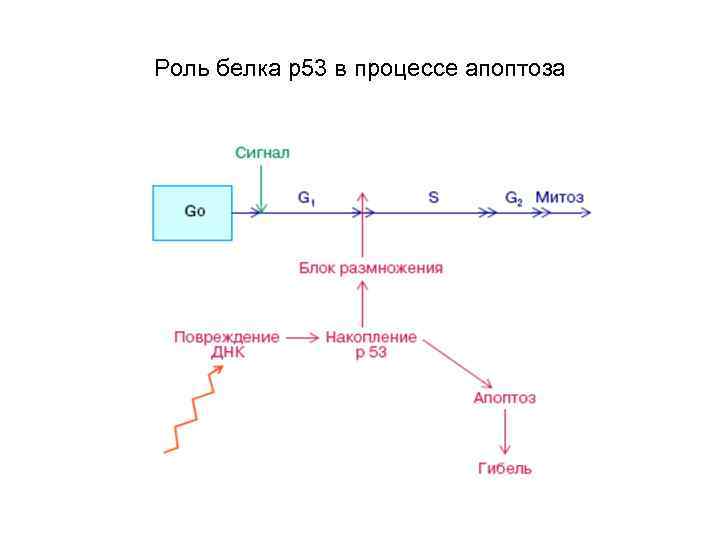 Роль белка р53 в процессе апоптоза
Роль белка р53 в процессе апоптоза
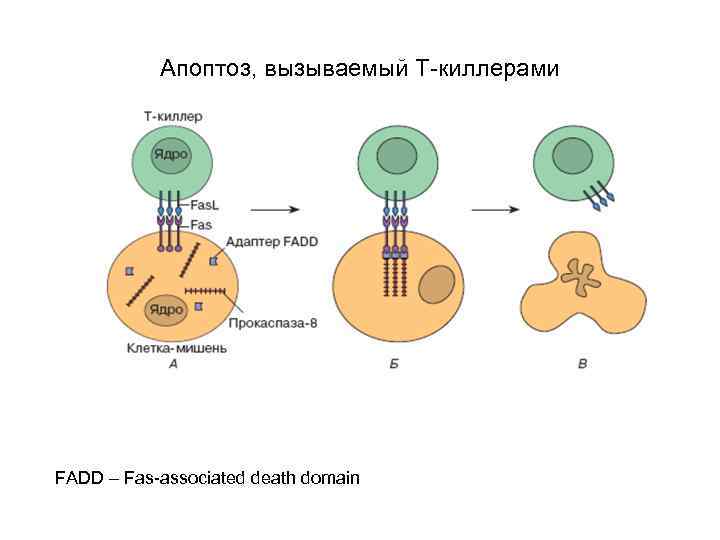 Апоптоз, вызываемый Т-киллерами FADD – Fas-associated death domain
Апоптоз, вызываемый Т-киллерами FADD – Fas-associated death domain
 • «Старение – изменение физиологических функций, чувствительности и энергии с возрастом, которое постепенно увеличивает вероятность смерти индивидуума от привходящих, случайных причин» • П. Медавар, 1952 Теории старения: 1. Накопление в клетках инертных веществ, замедляющих процессы метаболизма 2. Теория затухающего обновления протоплазмы (А. В. Нагорный, 1940) 3. Накопление соматических мутаций (Л. Сцилард, 1959) 4. Свободнорадикальная теория старения (Д. Харман, 1957, Н. М. Эмануэль, 1958) 5. Снижение уровня метилирования ДНК (Б. Ф. Ванюшин, 1973, Villeponteau, 1997) 6. Инактивация многочисленных повторов генов (Ж. А. Медведев, 1980) 7. Теория маргинотомии (теломеразная теория) (А. М. Оловников, 1973) 8. Теории терминальной дифференцировки
• «Старение – изменение физиологических функций, чувствительности и энергии с возрастом, которое постепенно увеличивает вероятность смерти индивидуума от привходящих, случайных причин» • П. Медавар, 1952 Теории старения: 1. Накопление в клетках инертных веществ, замедляющих процессы метаболизма 2. Теория затухающего обновления протоплазмы (А. В. Нагорный, 1940) 3. Накопление соматических мутаций (Л. Сцилард, 1959) 4. Свободнорадикальная теория старения (Д. Харман, 1957, Н. М. Эмануэль, 1958) 5. Снижение уровня метилирования ДНК (Б. Ф. Ванюшин, 1973, Villeponteau, 1997) 6. Инактивация многочисленных повторов генов (Ж. А. Медведев, 1980) 7. Теория маргинотомии (теломеразная теория) (А. М. Оловников, 1973) 8. Теории терминальной дифференцировки
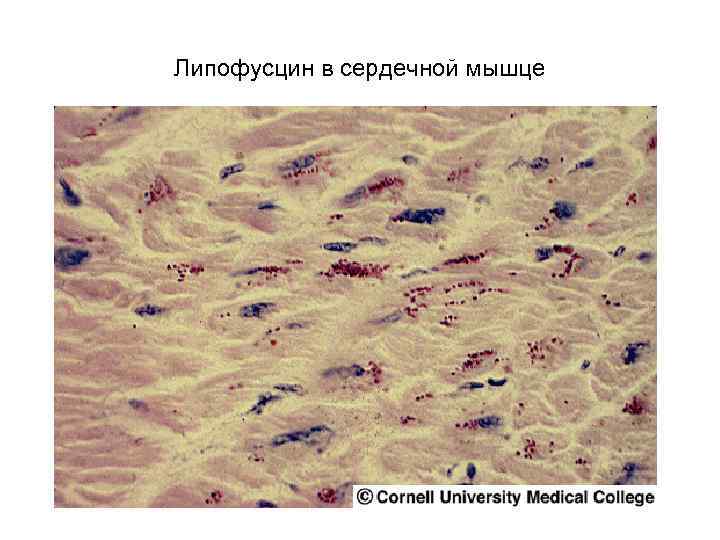 Липофусцин в сердечной мышце
Липофусцин в сердечной мышце
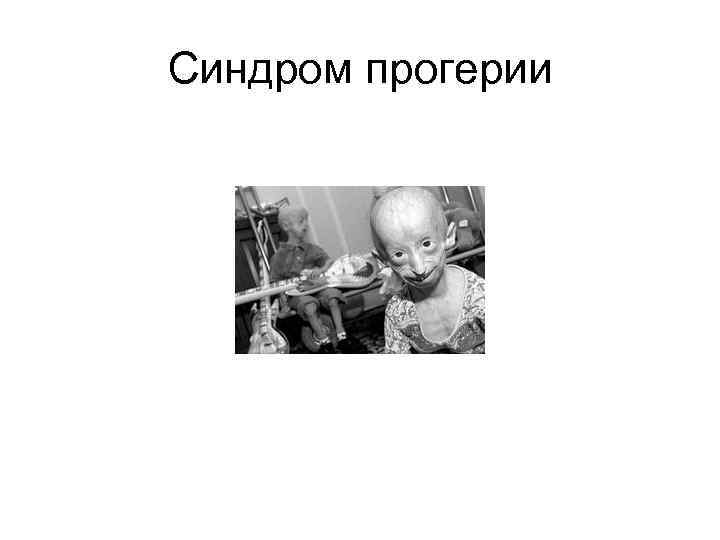 Синдром прогерии
Синдром прогерии
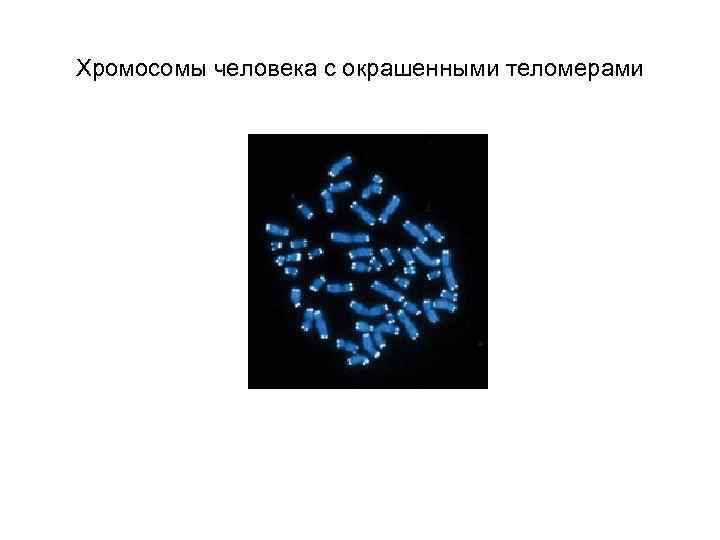 Хромосомы человека с окрашенными теломерами
Хромосомы человека с окрашенными теломерами
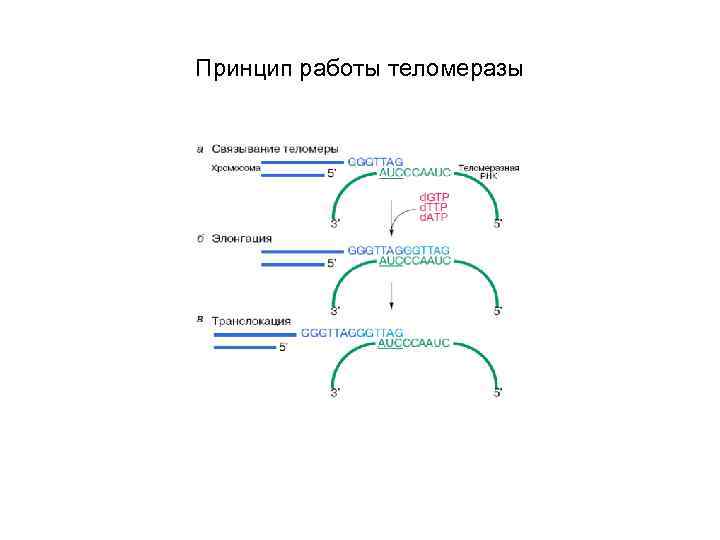 Принцип работы теломеразы
Принцип работы теломеразы
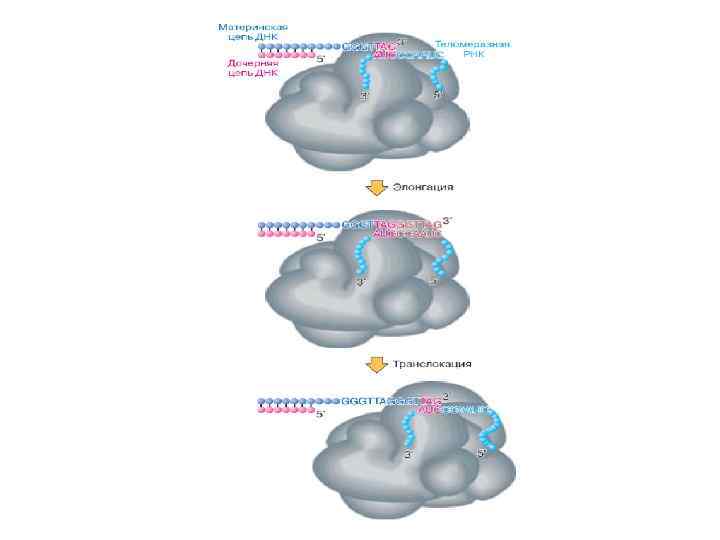
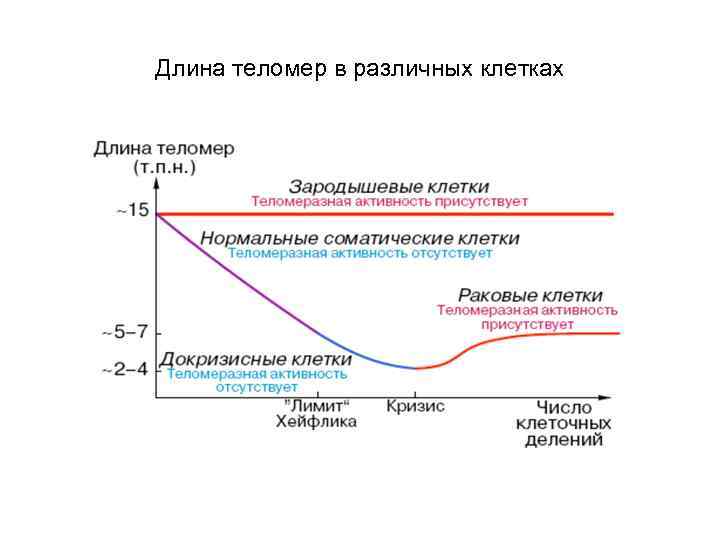 Длина теломер в различных клетках
Длина теломер в различных клетках


