4.2_Спирты одноатомные.pptx
- Количество слайдов: 29
 СПИРТЫ ОДНОАТОМНЫЕ ЛЕКЦИЯ 4
СПИРТЫ ОДНОАТОМНЫЕ ЛЕКЦИЯ 4
 СПИРТЫ Спиртами называют производные алифатических углеводородов, в которых один или несколько атомов водорода замещены на гидроксильную группу –OH.
СПИРТЫ Спиртами называют производные алифатических углеводородов, в которых один или несколько атомов водорода замещены на гидроксильную группу –OH.
 КЛАССИФИКАЦИЯ • По количеству гидроксильных групп, связанных с углеводородным радикалом • • одноатомные, двухатомные, трехатомные, в общем случае – многоатомные • В зависимости от количества углеводородных радикалов, связанных с гидроксилсодержащим атомом углерода, различают • первичные, • вторичные. • Третичные.
КЛАССИФИКАЦИЯ • По количеству гидроксильных групп, связанных с углеводородным радикалом • • одноатомные, двухатомные, трехатомные, в общем случае – многоатомные • В зависимости от количества углеводородных радикалов, связанных с гидроксилсодержащим атомом углерода, различают • первичные, • вторичные. • Третичные.
 СТРОЕНИЕ • Кислород гидроксила как более электроотрицательный атом оттягивает на себя электронную плотность от атома водорода и от атома углерода, связанных с ним: • Поэтому спирты в определенных условиях могут проявлять либо слабые кислотные, либо основные свойства, т. е. являются амфотерными соединениями
СТРОЕНИЕ • Кислород гидроксила как более электроотрицательный атом оттягивает на себя электронную плотность от атома водорода и от атома углерода, связанных с ним: • Поэтому спирты в определенных условиях могут проявлять либо слабые кислотные, либо основные свойства, т. е. являются амфотерными соединениями
 АМФОТЕРНОСТЬ СВОЙСТВ • Кислотность спиртов (легкость отрыва протона Н) уменьшается в ряду: • При переходе от метилового спирта к первичным, вторичным и третичным спиртам основные свойства (легкость отрыва ОН) повышаются:
АМФОТЕРНОСТЬ СВОЙСТВ • Кислотность спиртов (легкость отрыва протона Н) уменьшается в ряду: • При переходе от метилового спирта к первичным, вторичным и третичным спиртам основные свойства (легкость отрыва ОН) повышаются:
 СПОСОБЫ ПОЛУЧЕНИЯ • Гидратация алкенов (по правилу Марковникова) • Гидролиз галогенопроизводных • Восстановление карбонил– и карбоксилсодержащих соединений
СПОСОБЫ ПОЛУЧЕНИЯ • Гидратация алкенов (по правилу Марковникова) • Гидролиз галогенопроизводных • Восстановление карбонил– и карбоксилсодержащих соединений
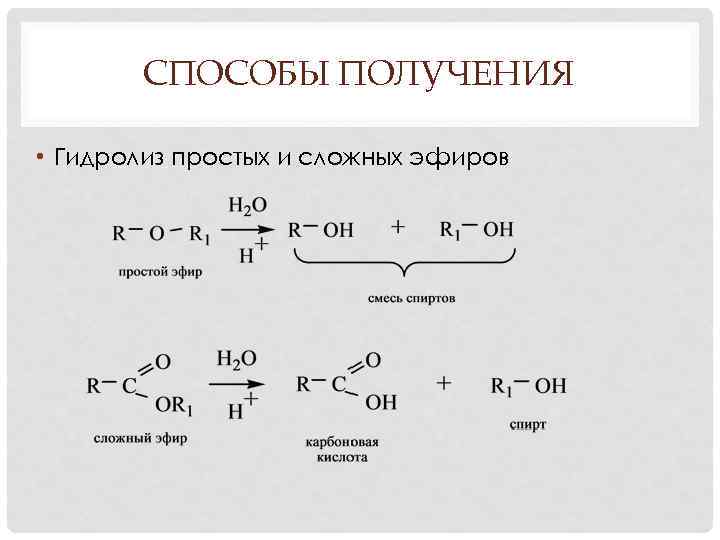 СПОСОБЫ ПОЛУЧЕНИЯ • Гидролиз простых и сложных эфиров
СПОСОБЫ ПОЛУЧЕНИЯ • Гидролиз простых и сложных эфиров
 СПОСОБЫ ПОЛУЧЕНИЯ • Оксосинтез • Ферментативное сбраживание углеводов
СПОСОБЫ ПОЛУЧЕНИЯ • Оксосинтез • Ферментативное сбраживание углеводов
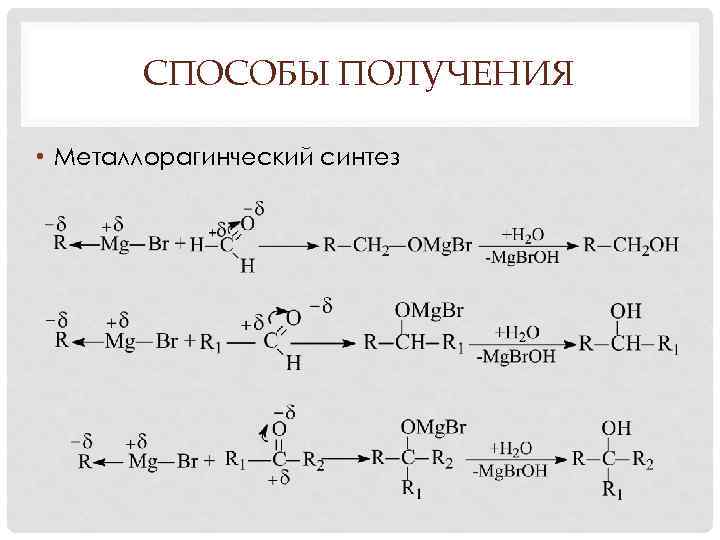 СПОСОБЫ ПОЛУЧЕНИЯ • Металлорагинческий синтез
СПОСОБЫ ПОЛУЧЕНИЯ • Металлорагинческий синтез
 ФИЗИЧЕСКИЕ СВОЙСТВА • Спирты с длиной углеродной цепочки до С 11 – жидкости с характерным запахом, содержащие более 11 атомов углерода – твердые вещества без запаха. • Спирты легче воды, многие ядовиты (10 см 3 метанола вызывает слепоту, большее количество – смерть), все – токсичны. • Зависимость tкип и tпл от строения молекул спиртов имеет обычные, ранее наблюдавшиеся в других гомологических рядах закономерности.
ФИЗИЧЕСКИЕ СВОЙСТВА • Спирты с длиной углеродной цепочки до С 11 – жидкости с характерным запахом, содержащие более 11 атомов углерода – твердые вещества без запаха. • Спирты легче воды, многие ядовиты (10 см 3 метанола вызывает слепоту, большее количество – смерть), все – токсичны. • Зависимость tкип и tпл от строения молекул спиртов имеет обычные, ранее наблюдавшиеся в других гомологических рядах закономерности.
 ФИЗИЧЕСКИЕ СВОЙСТВА • Из-за ассоциации молекул за счет водородных связей спирты имеют более высокие tкип по сравнению с ранее изученными классами органических соединений. • Из-за способности гидроксильной группы образовывать водородные связи с молекулами воды низшие спирты хорошо в ней растворяются. Растворимость спиртов с C 4 и большим числом атомов углерода в молекуле в воде уменьшается, а увеличивается в неполярных растворителях
ФИЗИЧЕСКИЕ СВОЙСТВА • Из-за ассоциации молекул за счет водородных связей спирты имеют более высокие tкип по сравнению с ранее изученными классами органических соединений. • Из-за способности гидроксильной группы образовывать водородные связи с молекулами воды низшие спирты хорошо в ней растворяются. Растворимость спиртов с C 4 и большим числом атомов углерода в молекуле в воде уменьшается, а увеличивается в неполярных растворителях
 ХИМИЧЕСКИЕ СВОЙСТВА • Химическое поведение спиртов, в первую очередь, определяется наличием в их молекуле функциональной гидроксильной группы. • В их разнообразных химических превращениях особое место принадлежит двум типам реакций замещения, протекающим с разрывом связи C-OH и O-H. • В то же время для спиртов характерны реакции элиминирования (дегидратации), приводящие к образованию двойной углерод–углеродной связи; реакции окисления и дегидрирования.
ХИМИЧЕСКИЕ СВОЙСТВА • Химическое поведение спиртов, в первую очередь, определяется наличием в их молекуле функциональной гидроксильной группы. • В их разнообразных химических превращениях особое место принадлежит двум типам реакций замещения, протекающим с разрывом связи C-OH и O-H. • В то же время для спиртов характерны реакции элиминирования (дегидратации), приводящие к образованию двойной углерод–углеродной связи; реакции окисления и дегидрирования.
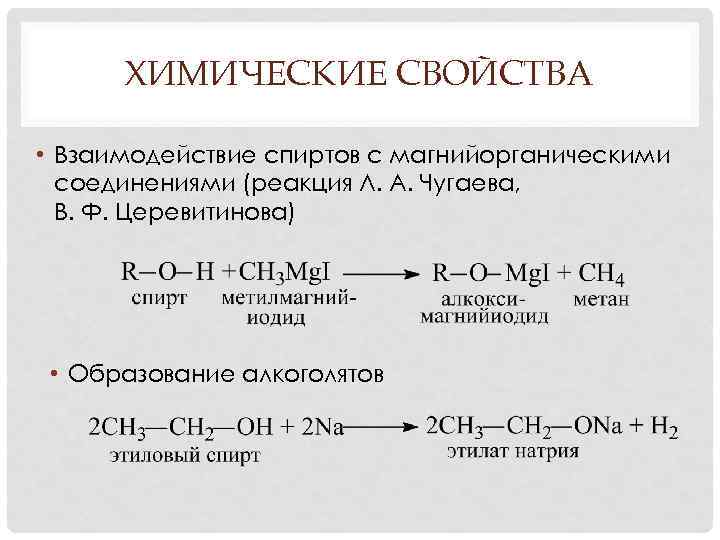 ХИМИЧЕСКИЕ СВОЙСТВА • Взаимодействие спиртов с магнийорганическими соединениями (реакция Л. А. Чугаева, В. Ф. Церевитинова) • Образование алкоголятов
ХИМИЧЕСКИЕ СВОЙСТВА • Взаимодействие спиртов с магнийорганическими соединениями (реакция Л. А. Чугаева, В. Ф. Церевитинова) • Образование алкоголятов

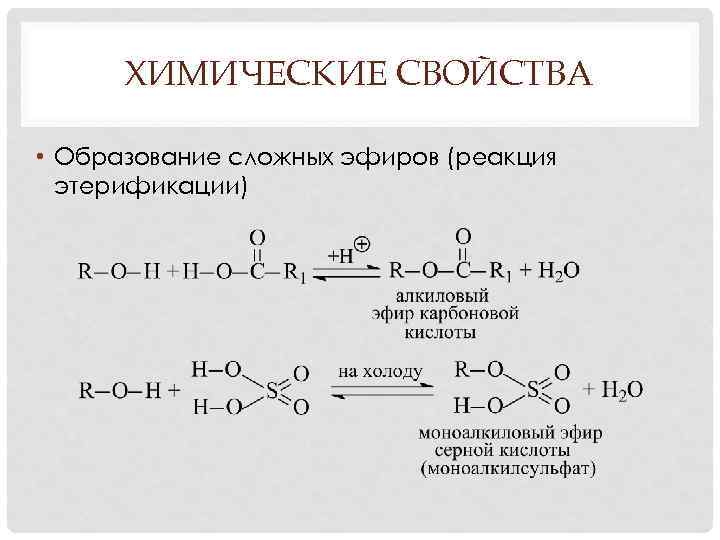 ХИМИЧЕСКИЕ СВОЙСТВА • Образование сложных эфиров (реакция этерификации)
ХИМИЧЕСКИЕ СВОЙСТВА • Образование сложных эфиров (реакция этерификации)
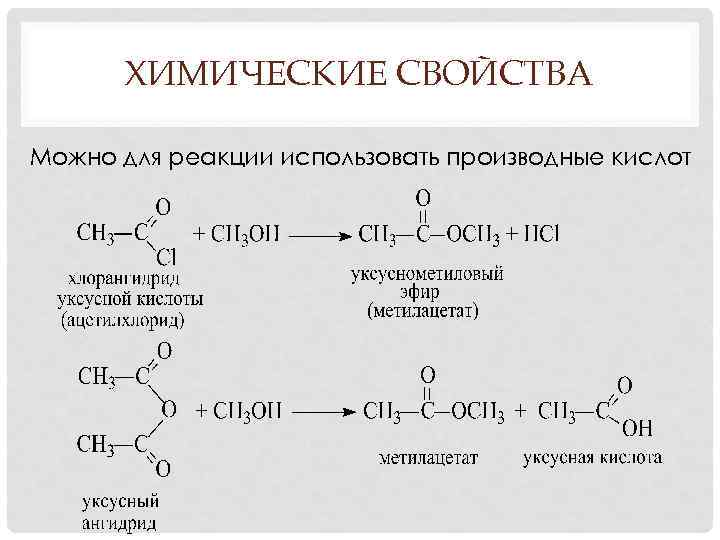 ХИМИЧЕСКИЕ СВОЙСТВА Можно для реакции использовать производные кислот
ХИМИЧЕСКИЕ СВОЙСТВА Можно для реакции использовать производные кислот
 ХИМИЧЕСКИЕ СВОЙСТВА • Образование простых эфиров Механизм реакции:
ХИМИЧЕСКИЕ СВОЙСТВА • Образование простых эфиров Механизм реакции:
 ХИМИЧЕСКИЕ СВОЙСТВА • Замещение гидроксильной группы на галоген Спирты по реакционной способности при взаимодействии с галогеноводородами располагаются в следующий ряд: аллиловый > бензиловый > третичный > вторичный > первичный > CH 3 OH. Реакционная способность кислот снижается при переходе от HI к HCl: HI > HBr > HCl.
ХИМИЧЕСКИЕ СВОЙСТВА • Замещение гидроксильной группы на галоген Спирты по реакционной способности при взаимодействии с галогеноводородами располагаются в следующий ряд: аллиловый > бензиловый > третичный > вторичный > первичный > CH 3 OH. Реакционная способность кислот снижается при переходе от HI к HCl: HI > HBr > HCl.
 МЕХАНИЗМ РЕАКЦИИ Механизм реакции аналогичен механизму нуклеофильного замещения у галогенуглеводородов Спирты вступают в эту реакцию в протонированной форме
МЕХАНИЗМ РЕАКЦИИ Механизм реакции аналогичен механизму нуклеофильного замещения у галогенуглеводородов Спирты вступают в эту реакцию в протонированной форме
 ХИМИЧЕСКИЕ СВОЙСТВА • Внутримолекулярная дегидратация (отщепление воды по правилу Зайцева с образованием алкенов) Реакционная способность падает в ряду: третичный спирт > вторичный > первичный Дегидратация протекает по механизмам Е 1 и Е 2. • Мономолекулярное отщепление воды (Е 1) наблюдается для третичных и вторичных спиртов:
ХИМИЧЕСКИЕ СВОЙСТВА • Внутримолекулярная дегидратация (отщепление воды по правилу Зайцева с образованием алкенов) Реакционная способность падает в ряду: третичный спирт > вторичный > первичный Дегидратация протекает по механизмам Е 1 и Е 2. • Мономолекулярное отщепление воды (Е 1) наблюдается для третичных и вторичных спиртов:
 МЕХАНИЗМ РЕАКЦИИ • Первичные спирты дегидратируются по механизму Е 2:
МЕХАНИЗМ РЕАКЦИИ • Первичные спирты дегидратируются по механизму Е 2:
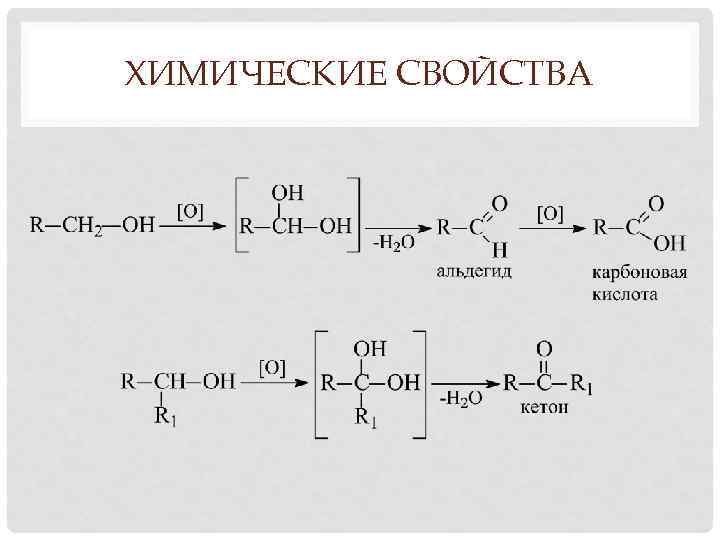
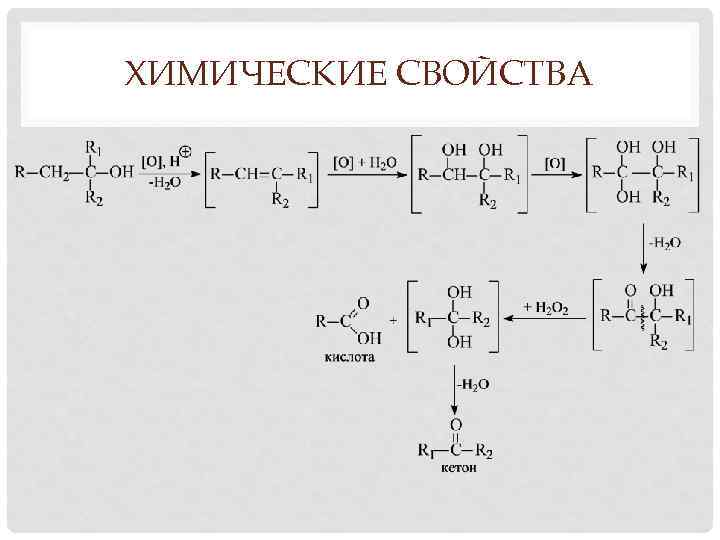
 ХИМИЧЕСКИЕ СВОЙСТВА • Окисление Происходит под действием на спирты KMn. O 4 конц при нагревании, хромовой смеси (H 2 SO 4 + K 2 Cr 2 O 7), О 2 в присутствии катализатора (Сu). Легче окисляются первичные, труднее – вторичные, еще труднее – третичные спирты Первичные спирты окисляются до альдегидов, вторичные – до кетонов, третичные – с разрывом углеродной цепочки (по правилу Попова – рядом с гидроксилом) до смеси карбонильных соединений:
ХИМИЧЕСКИЕ СВОЙСТВА • Окисление Происходит под действием на спирты KMn. O 4 конц при нагревании, хромовой смеси (H 2 SO 4 + K 2 Cr 2 O 7), О 2 в присутствии катализатора (Сu). Легче окисляются первичные, труднее – вторичные, еще труднее – третичные спирты Первичные спирты окисляются до альдегидов, вторичные – до кетонов, третичные – с разрывом углеродной цепочки (по правилу Попова – рядом с гидроксилом) до смеси карбонильных соединений:
 ХИМИЧЕСКИЕ СВОЙСТВА
ХИМИЧЕСКИЕ СВОЙСТВА
 ХИМИЧЕСКИЕ СВОЙСТВА
ХИМИЧЕСКИЕ СВОЙСТВА


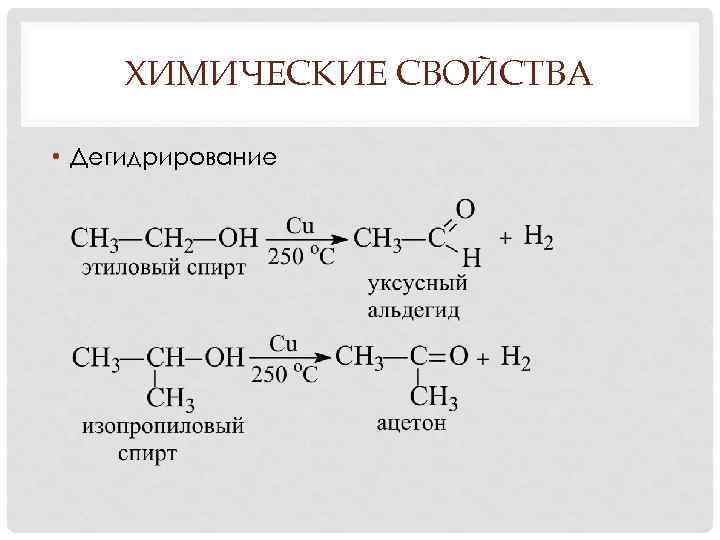 ХИМИЧЕСКИЕ СВОЙСТВА • Дегидрирование
ХИМИЧЕСКИЕ СВОЙСТВА • Дегидрирование
 ПРИМЕНЕНИЕ • Метиловый спирт широко применяется в качестве растворителя и полупродукта при синтезе многих органических соединений. Большие количества метанола расходуются для производства формальдегида и в реакциях метилирования. • Этанол используется в производстве синтетического каучука, этилацетата, диэтилового эфира, хлораля и в качестве растворителя. Большие количества этанола, образующегося при брожении пищевого сырья, идут в пищевую промышленность для получения спиртных напитков (водки, ликеров и т. д. ), парфюмерную для изготовления духов, одеколона и медицинскую промышленность.
ПРИМЕНЕНИЕ • Метиловый спирт широко применяется в качестве растворителя и полупродукта при синтезе многих органических соединений. Большие количества метанола расходуются для производства формальдегида и в реакциях метилирования. • Этанол используется в производстве синтетического каучука, этилацетата, диэтилового эфира, хлораля и в качестве растворителя. Большие количества этанола, образующегося при брожении пищевого сырья, идут в пищевую промышленность для получения спиртных напитков (водки, ликеров и т. д. ), парфюмерную для изготовления духов, одеколона и медицинскую промышленность.
 ПРИМЕНЕНИЕ • Пропиловые, бутиловые и амиловые спирты применяются для разнообразных синтезов и в качестве растворителей. • Поливиниловый спирт применяют в производстве синтетических волокон и лекарственных препаратов. • Аллиловый спирт применяется для получения глицерина, в производстве смол, парфюмерной промышленности • Бензиловый спирт применяется в парфюмерной промышленности
ПРИМЕНЕНИЕ • Пропиловые, бутиловые и амиловые спирты применяются для разнообразных синтезов и в качестве растворителей. • Поливиниловый спирт применяют в производстве синтетических волокон и лекарственных препаратов. • Аллиловый спирт применяется для получения глицерина, в производстве смол, парфюмерной промышленности • Бензиловый спирт применяется в парфюмерной промышленности


