СОВРЕМЕННЫЙ ВЗГЛЯД НА ОСНОВНЫЕ ПАТОГЕНЕТИЧЕСКИЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ
















































гипотезы шизофрении++.ppt
- Количество слайдов: 66
 СОВРЕМЕННЫЙ ВЗГЛЯД НА ОСНОВНЫЕ ПАТОГЕНЕТИЧЕСКИЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ Березовская М. А. Крас. ГМУ, кафедра психиатрии и наркологии с курсом ПО
СОВРЕМЕННЫЙ ВЗГЛЯД НА ОСНОВНЫЕ ПАТОГЕНЕТИЧЕСКИЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ Березовская М. А. Крас. ГМУ, кафедра психиатрии и наркологии с курсом ПО
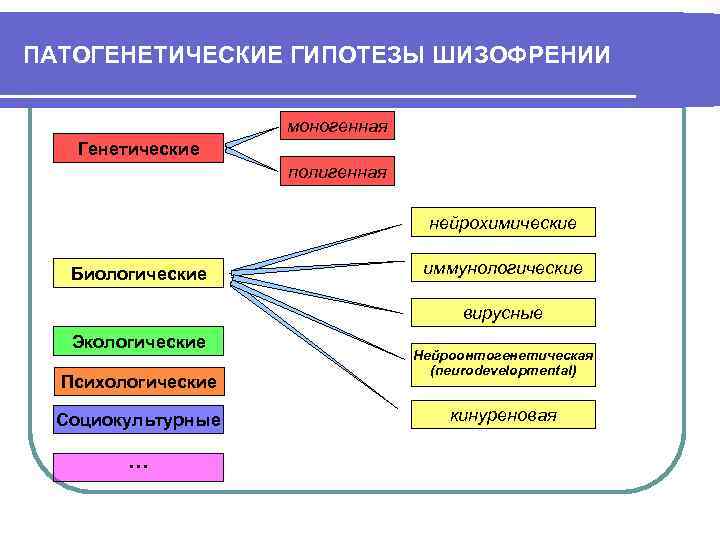
 ПАТОГЕНЕТИЧЕСКИЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ моногенная Генетические полигенная нейрохимические Биологические иммунологические вирусные Экологические Нейроонтогенетическая (neurodevelopmental) Психологические Социокультурные кинуреновая …
ПАТОГЕНЕТИЧЕСКИЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ моногенная Генетические полигенная нейрохимические Биологические иммунологические вирусные Экологические Нейроонтогенетическая (neurodevelopmental) Психологические Социокультурные кинуреновая …
 РОЛЬ НАСЛЕДСТВЕННЫХ ФАКТОРОВ В РАЗВИТИИ ШИЗОФРЕНИИ (Шахматова-Павлова, 1972, Москаленко 1980, Гиндилис, Вартанян 1982, Gershon et al. , 1982; Gottesman and Shields, 1982; Torgensen et al. , 1986; Kendler et al. , 1993). ь Высокая частота встречаемости шизофрении среди членов семей больных (вероятность заболевания для родственников -10%, в популяции -1, 5%). ь Степень конкордантности (совпадения) у монозиготных близнецов выше, чем у дизиготных (50% и 10%, соответственно). ь Большая частота встречаемости шизофрении у биологических родственников усыновленных людей с шизофренией, чем у их приемных родителей. ь Дети, родившиеся от больных родителей и усыновленные здоровыми, сохраняют повышенную вероятность заболевания (10%).
РОЛЬ НАСЛЕДСТВЕННЫХ ФАКТОРОВ В РАЗВИТИИ ШИЗОФРЕНИИ (Шахматова-Павлова, 1972, Москаленко 1980, Гиндилис, Вартанян 1982, Gershon et al. , 1982; Gottesman and Shields, 1982; Torgensen et al. , 1986; Kendler et al. , 1993). ь Высокая частота встречаемости шизофрении среди членов семей больных (вероятность заболевания для родственников -10%, в популяции -1, 5%). ь Степень конкордантности (совпадения) у монозиготных близнецов выше, чем у дизиготных (50% и 10%, соответственно). ь Большая частота встречаемости шизофрении у биологических родственников усыновленных людей с шизофренией, чем у их приемных родителей. ь Дети, родившиеся от больных родителей и усыновленные здоровыми, сохраняют повышенную вероятность заболевания (10%).
 РОЛЬ СРЕДОВЫХ ФАКТОРОВ В РАЗВИТИИ ШИЗОФРЕНИИ Коэффициент наследуемости (вклад генетических факторов) – 80%. Современные генетические представления: Шизофрения – заболевание, имеющее наследственную предрасположенность, которая реализуется при взаимодействии генетических факторов с влиянием окружающей среды.
РОЛЬ СРЕДОВЫХ ФАКТОРОВ В РАЗВИТИИ ШИЗОФРЕНИИ Коэффициент наследуемости (вклад генетических факторов) – 80%. Современные генетические представления: Шизофрения – заболевание, имеющее наследственную предрасположенность, которая реализуется при взаимодействии генетических факторов с влиянием окружающей среды.
 МОНОГЕННАЯ ГИПОТЕЗА (Т. J. Crow, 90 -е годы ХХ века - Am. J Psychiatry, 2007) Аргументы «за» : ь частота возникновения шизофрении постоянна во всех популяциях (по основным симптомам); ь структурные изменения в головном мозге встречаются с одинаковой частотой во всех популяциях; ь возраст манифестации заболевания определяет специфические особенности клинических проявлений; ь отмечены гендерные различия в течении и исходе болезни – у мужчин шизофрения начинается раньше и имеет более неблагоприятный исход; ь основные симптомы психоза связаны с речевыми процессами (бред, расстройства мышления, вербальный галлюциноз), т. е. специфичны только для человека. Ген – на псевдоаутосомном участке Х и Y хромосом
МОНОГЕННАЯ ГИПОТЕЗА (Т. J. Crow, 90 -е годы ХХ века - Am. J Psychiatry, 2007) Аргументы «за» : ь частота возникновения шизофрении постоянна во всех популяциях (по основным симптомам); ь структурные изменения в головном мозге встречаются с одинаковой частотой во всех популяциях; ь возраст манифестации заболевания определяет специфические особенности клинических проявлений; ь отмечены гендерные различия в течении и исходе болезни – у мужчин шизофрения начинается раньше и имеет более неблагоприятный исход; ь основные симптомы психоза связаны с речевыми процессами (бред, расстройства мышления, вербальный галлюциноз), т. е. специфичны только для человека. Ген – на псевдоаутосомном участке Х и Y хромосом
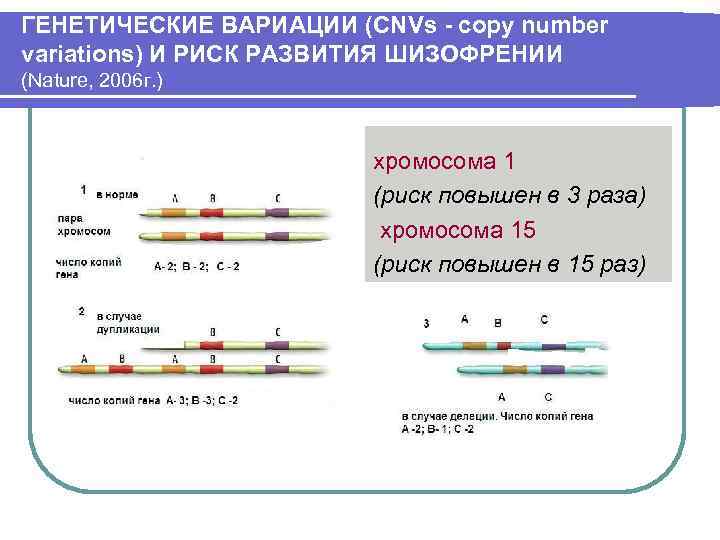
 ГЕНЕТИЧЕСКИЕ ВАРИАЦИИ (CNVs - copy number variations) И РИСК РАЗВИТИЯ ШИЗОФРЕНИИ (Nature, 2006 г. ) хромосома 1 (риск повышен в 3 раза) хромосома 15 (риск повышен в 15 раз)
ГЕНЕТИЧЕСКИЕ ВАРИАЦИИ (CNVs - copy number variations) И РИСК РАЗВИТИЯ ШИЗОФРЕНИИ (Nature, 2006 г. ) хромосома 1 (риск повышен в 3 раза) хромосома 15 (риск повышен в 15 раз)
 ГЕНЫ, СВЯЗАННЫЕ С ШИЗОФРЕНИЕЙ (гены-кандидаты) Ген Связь с шизофренией Катехол-О- Участвует в разрушении дофамина – нейромедиатора, который играет существенную роль в метилтрансфераза мозговых процессах. Нарушения в работе дофаминергической системы рассматриваются в (СОМТ) качестве одной из причин развития шизофрении. Дофаминовый рецептор DRD 4 являются основной мишенью антипсихотических препаратов (атипичных D 4 (DRD 4) нейролептиков). Дофаминовый рецептор Повышение плотности рецепторов в мозге больных шизофренией. Сродство к D 2 (DRD 2) антипсихотическим препаратам. Дофаминовый рецептор Сродство к рецепторам DRD 2, связывание с которыми обеспечивает терапевтический эффект D 3 (DRD 3) антипсихотических средств. Нейрегулин Имеет отношение к функционированию глутаматной системы и пластичности нейронов. Серотониновый рецептор Снижение экспрессии в аутопсийном мозге больных шизофренией. Способность связывать типа 2 А некоторые антипсихотические препараты. (5 -НТR 2 A) Активатор оксидазы D- Влияние на глутаматные рецепторы типа NMDA. Нарушение в работе глутаматергической аминокислот и оксидаза D системы также рассматриваются в качестве одной из причин развития шизофрении. -аминокислот (DAOA/ G 30 и DAAO) BDNF от англ. brain Играет важную роль в нейрогенезе и синаптической пластичности мозга. В префронтальной derived neurotrophic factor коре больных шизофренией было обнаружено снижение экспрессии м-РНК гена BDNF и количества белкового продукта. Дисбиндин (DTNBP 1) Экспрессия в участках, являющихся критическими для развития и патогенеза шизофрении (гиппокамп, префронтальная кора).
ГЕНЫ, СВЯЗАННЫЕ С ШИЗОФРЕНИЕЙ (гены-кандидаты) Ген Связь с шизофренией Катехол-О- Участвует в разрушении дофамина – нейромедиатора, который играет существенную роль в метилтрансфераза мозговых процессах. Нарушения в работе дофаминергической системы рассматриваются в (СОМТ) качестве одной из причин развития шизофрении. Дофаминовый рецептор DRD 4 являются основной мишенью антипсихотических препаратов (атипичных D 4 (DRD 4) нейролептиков). Дофаминовый рецептор Повышение плотности рецепторов в мозге больных шизофренией. Сродство к D 2 (DRD 2) антипсихотическим препаратам. Дофаминовый рецептор Сродство к рецепторам DRD 2, связывание с которыми обеспечивает терапевтический эффект D 3 (DRD 3) антипсихотических средств. Нейрегулин Имеет отношение к функционированию глутаматной системы и пластичности нейронов. Серотониновый рецептор Снижение экспрессии в аутопсийном мозге больных шизофренией. Способность связывать типа 2 А некоторые антипсихотические препараты. (5 -НТR 2 A) Активатор оксидазы D- Влияние на глутаматные рецепторы типа NMDA. Нарушение в работе глутаматергической аминокислот и оксидаза D системы также рассматриваются в качестве одной из причин развития шизофрении. -аминокислот (DAOA/ G 30 и DAAO) BDNF от англ. brain Играет важную роль в нейрогенезе и синаптической пластичности мозга. В префронтальной derived neurotrophic factor коре больных шизофренией было обнаружено снижение экспрессии м-РНК гена BDNF и количества белкового продукта. Дисбиндин (DTNBP 1) Экспрессия в участках, являющихся критическими для развития и патогенеза шизофрении (гиппокамп, префронтальная кора).
 ГЕНЕТИЧЕСКИЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ Болезнь – результат структурных изменений генома на различных уровнях: Ш нуклеотидные замены в генах, Ш изменение числа копий генов, Ш изменение количества хромосом.
ГЕНЕТИЧЕСКИЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ Болезнь – результат структурных изменений генома на различных уровнях: Ш нуклеотидные замены в генах, Ш изменение числа копий генов, Ш изменение количества хромосом.
 ГЕНЕТИЧЕСКИЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ В настоящее время невозможно с определенностью утверждать, что какая- либо модификация гена увеличивает риск развития шизофрении. ШИЗОФРЕНИЯ – разнородное, полигенно- мультифакторное заболевание с множественными распространенными генетическими полиморфизмами, каждый из которых вносит небольшой вклад в подверженность заболеванию.
ГЕНЕТИЧЕСКИЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ В настоящее время невозможно с определенностью утверждать, что какая- либо модификация гена увеличивает риск развития шизофрении. ШИЗОФРЕНИЯ – разнородное, полигенно- мультифакторное заболевание с множественными распространенными генетическими полиморфизмами, каждый из которых вносит небольшой вклад в подверженность заболеванию.
 ВИРУСНАЯ ГИПОТЕЗА РАЗВИТИЯ ШИЗОФРЕНИИ (Fuller Torrey, 80 -е годы ХХ века) Болезнь – следствие вирусного заражения во внутриутробный период развития Конкретного вируса не обнаружено!
ВИРУСНАЯ ГИПОТЕЗА РАЗВИТИЯ ШИЗОФРЕНИИ (Fuller Torrey, 80 -е годы ХХ века) Болезнь – следствие вирусного заражения во внутриутробный период развития Конкретного вируса не обнаружено!
 СВОЙСТВА ВИРУСОВ, ВАЖНЫЕ С ТОЧКИ ЗРЕНИЯ ВИРУСНЫХ ТЕОРИЙ ШИЗОФРЕНИИ Ш Способность поражать узко ограниченные участки мозга. Ш Способность влиять на функционирование клеток без изменения их структуры. Ш Длительный латентный период (медленные вирусы). Ш Возможность передачи вируса вместе с геном. Важное условие – попадание вируса в мозг развивающегося плода в критические периоды его развития
СВОЙСТВА ВИРУСОВ, ВАЖНЫЕ С ТОЧКИ ЗРЕНИЯ ВИРУСНЫХ ТЕОРИЙ ШИЗОФРЕНИИ Ш Способность поражать узко ограниченные участки мозга. Ш Способность влиять на функционирование клеток без изменения их структуры. Ш Длительный латентный период (медленные вирусы). Ш Возможность передачи вируса вместе с геном. Важное условие – попадание вируса в мозг развивающегося плода в критические периоды его развития
 ВИРУСНЫЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ Аргументы «ЗА» : Ш У матерей, перенесших грипп в течение первых трех месяцев беременности, большая вероятность родить больного шизофренией ребенка. Ш Существование группы вирусов, способных поражать нервную систему. Ш Сезонность рождения будущих больных. Ш Существование наследственной предрасположенности к вирусным инфекциям. Ш Возможность передачи вируса вместе с геном.
ВИРУСНЫЕ ГИПОТЕЗЫ ШИЗОФРЕНИИ Аргументы «ЗА» : Ш У матерей, перенесших грипп в течение первых трех месяцев беременности, большая вероятность родить больного шизофренией ребенка. Ш Существование группы вирусов, способных поражать нервную систему. Ш Сезонность рождения будущих больных. Ш Существование наследственной предрасположенности к вирусным инфекциям. Ш Возможность передачи вируса вместе с геном.
 ФАКТОРЫ РИСКА ОКРУЖАЮЩЕЙ СРЕДЫ БИОЛОГИЧЕСКИЕ СОЦИАЛЬНЫЕ l Инфекционные l Миграция заболевания у матери в l Урбанизация период беременности l Осложнения беременности и родов l Месяц рождения (зима- начало весны) l Пожилой возраст отца к моменту рождения ребенка
ФАКТОРЫ РИСКА ОКРУЖАЮЩЕЙ СРЕДЫ БИОЛОГИЧЕСКИЕ СОЦИАЛЬНЫЕ l Инфекционные l Миграция заболевания у матери в l Урбанизация период беременности l Осложнения беременности и родов l Месяц рождения (зима- начало весны) l Пожилой возраст отца к моменту рождения ребенка
 НЕЙРООНТОГЕНЕТИЧЕСКАЯ ГИПОТЕЗА ШИЗОФРЕНИИ, ОСНОВЫВАЮЩАЯСЯ НА ДЕФЕКТАХ РАЗВИТИЯ НЕРВНОЙ СИСТЕМЫ (neurodevelopmental hypothesis) (Weinberger D. R. , 80 -е годы ХХ века) Шизофрения – заболевание, вызванное дефектами развития мозга Причины нарушения развития нервной системы: Ш наследственные факторы, Ш вирусы, Ш токсины, Ш алиментарные факторы, Ш осложнения при беременности
НЕЙРООНТОГЕНЕТИЧЕСКАЯ ГИПОТЕЗА ШИЗОФРЕНИИ, ОСНОВЫВАЮЩАЯСЯ НА ДЕФЕКТАХ РАЗВИТИЯ НЕРВНОЙ СИСТЕМЫ (neurodevelopmental hypothesis) (Weinberger D. R. , 80 -е годы ХХ века) Шизофрения – заболевание, вызванное дефектами развития мозга Причины нарушения развития нервной системы: Ш наследственные факторы, Ш вирусы, Ш токсины, Ш алиментарные факторы, Ш осложнения при беременности
 НЕЙРООНТОГЕНЕТИЧЕСКАЯ ГИПОТЕЗА ШИЗОФРЕНИИ Аргументы «за» : 1. МРТ-исследования + постмортальные исследования: - сокращение объема мозга - сокращение объема височной коры - сокращение объема гиппокампально-амигдалярного комплекса - расширение боковых желудочков - изменение пропорции серого и белого вещества 2. Нарушение цитоархитектоники нейронов в коре мозга 3. Отсутствие чрезмерного глиоза в мозге 4. Отсутствие нормальной мозговой асимметрии
НЕЙРООНТОГЕНЕТИЧЕСКАЯ ГИПОТЕЗА ШИЗОФРЕНИИ Аргументы «за» : 1. МРТ-исследования + постмортальные исследования: - сокращение объема мозга - сокращение объема височной коры - сокращение объема гиппокампально-амигдалярного комплекса - расширение боковых желудочков - изменение пропорции серого и белого вещества 2. Нарушение цитоархитектоники нейронов в коре мозга 3. Отсутствие чрезмерного глиоза в мозге 4. Отсутствие нормальной мозговой асимметрии
 НЕЙРООНТОГЕНЕТИЧЕСКАЯ ГИПОТЕЗА ШИЗОФРЕНИИ (продолжение) Аргументы «за» : 5. Измененная активность ряда маркеров развития мозга (NCAM- молекула нейрональной адгезии, GAP 3 -протеин, ассоциированный с ростом). 6. Нарушение формирования извилин (гирификация). 7. «Мягкие» неврологические знаки и поведенческие особенности в детстве у людей, впоследствии заболевших шизофренией. 8. Более высокий уровень незначительных физических аномалий (дерматоглифика, посадка ушных раковин, высокое сводчатое небо и т. д. ). 9. Экспериментальные свидетельства возможности «отставленности» последствий внутриутробных нарушений развития мозга.
НЕЙРООНТОГЕНЕТИЧЕСКАЯ ГИПОТЕЗА ШИЗОФРЕНИИ (продолжение) Аргументы «за» : 5. Измененная активность ряда маркеров развития мозга (NCAM- молекула нейрональной адгезии, GAP 3 -протеин, ассоциированный с ростом). 6. Нарушение формирования извилин (гирификация). 7. «Мягкие» неврологические знаки и поведенческие особенности в детстве у людей, впоследствии заболевших шизофренией. 8. Более высокий уровень незначительных физических аномалий (дерматоглифика, посадка ушных раковин, высокое сводчатое небо и т. д. ). 9. Экспериментальные свидетельства возможности «отставленности» последствий внутриутробных нарушений развития мозга.
 ОБОБЩЕННАЯ МОДЕЛЬ РАЗВИТИЯ ШИЗОФРЕНИИ (в соответствии с нейроонтогенетической гипотезой) Этиология: совокупность различных экзогенных и эндогенных факторов (генетитческие, вирусы, токсины, алиментарные факторы, родовая травма и т. д. ) Патофизиология: нарушение процессов развития мозга (миграция клеток, прунинг и спрутинг, синаптогенез, апоптоз) Анатомические и функциональные нарушения в формировании нейронных сетей Ухудшение фундаментальных нервных процессов, лежащих в основе когнитивных функций. Феноменология: ухудшение вторичных когнитивных процессов (внимание, память, язык, эмоции) Феноменология: симптомы шизофрении (позитивные, негативные, речевые нарушения и т. д. )
ОБОБЩЕННАЯ МОДЕЛЬ РАЗВИТИЯ ШИЗОФРЕНИИ (в соответствии с нейроонтогенетической гипотезой) Этиология: совокупность различных экзогенных и эндогенных факторов (генетитческие, вирусы, токсины, алиментарные факторы, родовая травма и т. д. ) Патофизиология: нарушение процессов развития мозга (миграция клеток, прунинг и спрутинг, синаптогенез, апоптоз) Анатомические и функциональные нарушения в формировании нейронных сетей Ухудшение фундаментальных нервных процессов, лежащих в основе когнитивных функций. Феноменология: ухудшение вторичных когнитивных процессов (внимание, память, язык, эмоции) Феноменология: симптомы шизофрении (позитивные, негативные, речевые нарушения и т. д. )
 ТАКИМ ОБРАЗОМ: Одним из основных патофизиологических механизмов развития шизофрении и расстройств шизофренического спектра, возможно, является структурно-функциональная рассогласованность различных отделов головного мозга. На феноменологическом уровне эти нарушения проявляются в виде расстройств комплексного восприятия окружающей обстановки, начиная от элементарных обстоятельств (напр. , снижение реакции на боль), вплоть до сложного синтетического анализа социального контекста (эмоций окружающих людей, оценки их поведения и пр. ).
ТАКИМ ОБРАЗОМ: Одним из основных патофизиологических механизмов развития шизофрении и расстройств шизофренического спектра, возможно, является структурно-функциональная рассогласованность различных отделов головного мозга. На феноменологическом уровне эти нарушения проявляются в виде расстройств комплексного восприятия окружающей обстановки, начиная от элементарных обстоятельств (напр. , снижение реакции на боль), вплоть до сложного синтетического анализа социального контекста (эмоций окружающих людей, оценки их поведения и пр. ).
 ПЕРВАЯ ФОРМУЛИРОВКА DA-ГИПОТЕЗЫ ШИЗОФРЕНИИ (Carlsson and Lindqvist, 1963) Болезнь – результат гиперактивной DA- трансмиссии Основание: Шактивация психостимуляторами D-R. Шнерезерпиновые нейролептики – антагонисты DA. Шкорреляция между дозой антипсихотиков и способностью блокировать D 2 - R.
ПЕРВАЯ ФОРМУЛИРОВКА DA-ГИПОТЕЗЫ ШИЗОФРЕНИИ (Carlsson and Lindqvist, 1963) Болезнь – результат гиперактивной DA- трансмиссии Основание: Шактивация психостимуляторами D-R. Шнерезерпиновые нейролептики – антагонисты DA. Шкорреляция между дозой антипсихотиков и способностью блокировать D 2 - R.
 ОСНОВНЫЕ ДОФАМИНЕРГИЧЕСКИЕ ПУТИ ГОЛОВНОГО МОЗГА Структуры мозга Клинические последствия блокады I. Средний мозг нигростриарная система НИГРОСТРИАРНЫЙ ПУТЬ экстрапирамидные побочные эффекты II. Средний мозг мезолимбическая система (гиппокамп, амигдала, чечевидное тело, височная доля) антипсихотический эффект (дофаминергическая гиперфункция) МЕЗОЛИМБИЧЕСКИЙ ПУТЬ III. Гипоталамус средний мозг увеличение выработки гормона пролактина (тубероинфундибулярная система) (нейроэндокринные побочные ТУБЕРОИНФУНДИБУЛЯРНЫЙ ПУТЬ эффекты) IV Средний мозг мезокортикальная уменьшение выраженности негативной система (дофаминергическая симптоматики и когнитивных гипофункция) нарушений применении МЕЗОКОРТИКАЛЬНЫЙ ПУТЬ атипичных антипсихотиков
ОСНОВНЫЕ ДОФАМИНЕРГИЧЕСКИЕ ПУТИ ГОЛОВНОГО МОЗГА Структуры мозга Клинические последствия блокады I. Средний мозг нигростриарная система НИГРОСТРИАРНЫЙ ПУТЬ экстрапирамидные побочные эффекты II. Средний мозг мезолимбическая система (гиппокамп, амигдала, чечевидное тело, височная доля) антипсихотический эффект (дофаминергическая гиперфункция) МЕЗОЛИМБИЧЕСКИЙ ПУТЬ III. Гипоталамус средний мозг увеличение выработки гормона пролактина (тубероинфундибулярная система) (нейроэндокринные побочные ТУБЕРОИНФУНДИБУЛЯРНЫЙ ПУТЬ эффекты) IV Средний мозг мезокортикальная уменьшение выраженности негативной система (дофаминергическая симптоматики и когнитивных гипофункция) нарушений применении МЕЗОКОРТИКАЛЬНЫЙ ПУТЬ атипичных антипсихотиков
 СОВРЕМЕННАЯ DA-ГИПОТЕЗА (Knable and Weinberger, 1997; Goldman-Rakic et al. , 2000) Шизофрения – результат дисбаланса DA -системы в различных отделах мозга: гиперактивация мезолимбических проекций (приводит к гиперстимуляции D 2 -рецепторов и позитивным симптомам) гипоактивность мезокортикальных проекций (приводит к гипостимуляции D 1 -рецепторов, негативным симптомам и когнитивным нарушениям, феномен гипофронтальности).
СОВРЕМЕННАЯ DA-ГИПОТЕЗА (Knable and Weinberger, 1997; Goldman-Rakic et al. , 2000) Шизофрения – результат дисбаланса DA -системы в различных отделах мозга: гиперактивация мезолимбических проекций (приводит к гиперстимуляции D 2 -рецепторов и позитивным симптомам) гипоактивность мезокортикальных проекций (приводит к гипостимуляции D 1 -рецепторов, негативным симптомам и когнитивным нарушениям, феномен гипофронтальности).
 ДОФАМИНО-СЕРОТОНИНОВАЯ ГИПОТЕЗА ШИЗОФРЕНИИ В формирование DA-дисбаланса вовлечена серотониновая система ОСНОВАНИЕ: ШАнтипсихотический эффект атипичных нейролептиков связан не столько с действием на D 2 -R, но с их способностью ингибировать 5 - НТ 2. ШРеципрокные отношения ДА и 5 НТ в дофаминэргических системах мозга.
ДОФАМИНО-СЕРОТОНИНОВАЯ ГИПОТЕЗА ШИЗОФРЕНИИ В формирование DA-дисбаланса вовлечена серотониновая система ОСНОВАНИЕ: ШАнтипсихотический эффект атипичных нейролептиков связан не столько с действием на D 2 -R, но с их способностью ингибировать 5 - НТ 2. ШРеципрокные отношения ДА и 5 НТ в дофаминэргических системах мозга.
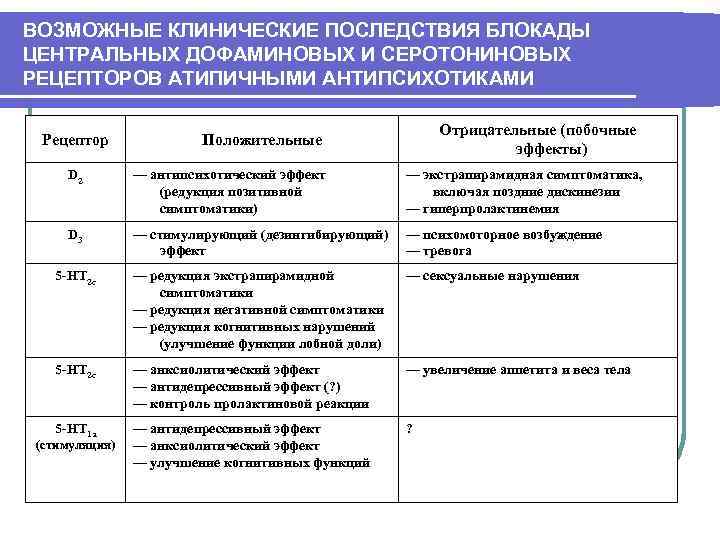
 ВОЗМОЖНЫЕ КЛИНИЧЕСКИЕ ПОСЛЕДСТВИЯ БЛОКАДЫ ЦЕНТРАЛЬНЫХ ДОФАМИНОВЫХ И СЕРОТОНИНОВЫХ РЕЦЕПТОРОВ АТИПИЧНЫМИ АНТИПСИХОТИКАМИ Отрицательные (побочные Рецептор Положительные эффекты) D 2 — антипсихотический эффект — экстрапирамидная симптоматика, (редукция позитивной включая поздние дискинезии симптоматики) — гиперпролактинемия D 3 — стимулирующий (дезингибирующий) — психомоторное возбуждение эффект — тревога 5 -НТ 2 с — редукция экстрапирамидной — сексуальные нарушения симптоматики — редукция негативной симптоматики — редукция когнитивных нарушений (улучшение функции лобной доли) 5 -НТ 2 с — анксиолитический эффект — увеличение аппетита и веса тела — антидепрессивный эффект (? ) — контроль пролактиновой реакции 5 -НТ 1 а — антидепрессивный эффект ? (стимуляция) — анксиолитический эффект — улучшение когнитивных функций
ВОЗМОЖНЫЕ КЛИНИЧЕСКИЕ ПОСЛЕДСТВИЯ БЛОКАДЫ ЦЕНТРАЛЬНЫХ ДОФАМИНОВЫХ И СЕРОТОНИНОВЫХ РЕЦЕПТОРОВ АТИПИЧНЫМИ АНТИПСИХОТИКАМИ Отрицательные (побочные Рецептор Положительные эффекты) D 2 — антипсихотический эффект — экстрапирамидная симптоматика, (редукция позитивной включая поздние дискинезии симптоматики) — гиперпролактинемия D 3 — стимулирующий (дезингибирующий) — психомоторное возбуждение эффект — тревога 5 -НТ 2 с — редукция экстрапирамидной — сексуальные нарушения симптоматики — редукция негативной симптоматики — редукция когнитивных нарушений (улучшение функции лобной доли) 5 -НТ 2 с — анксиолитический эффект — увеличение аппетита и веса тела — антидепрессивный эффект (? ) — контроль пролактиновой реакции 5 -НТ 1 а — антидепрессивный эффект ? (стимуляция) — анксиолитический эффект — улучшение когнитивных функций
 ГЛУТАМАТНАЯ ГИПОТЕЗА ШИЗОФРЕНИИ (J. Kim, 1980, C. Tamminga. , J. Crystal. , 2000 г. ) Болезнь – результат снижения активности ГЛУ- зависимого проведения нервных импульсов из- за недостаточной активности (ингибирования) ГЛУ-рецепторов NMDA типа. Основание : пониженное содержание глутамата в ликворе больных шизофренией
ГЛУТАМАТНАЯ ГИПОТЕЗА ШИЗОФРЕНИИ (J. Kim, 1980, C. Tamminga. , J. Crystal. , 2000 г. ) Болезнь – результат снижения активности ГЛУ- зависимого проведения нервных импульсов из- за недостаточной активности (ингибирования) ГЛУ-рецепторов NMDA типа. Основание : пониженное содержание глутамата в ликворе больных шизофренией
 СОВРЕМЕННАЯ ТРАКТОВКА глу-ГИПОТЕЗЫ ШИЗОФРЕНИИ (Г. Бурбаева, И. Бокша, V. Haroutunyan, C. Tamminga, C. Beasley, S. Tsai 2000 -2008 гг. ) Болезнь – результат нарушений в любом из многочисленных механизмов, воздействующих на Глу-рецепторы разных типов: Ш Модификация активности рецепторов. Ш Изменение активности ферментов, участвующих в метаболизме ГЛУ. Ш Изменение активности глу-транспортера и др.
СОВРЕМЕННАЯ ТРАКТОВКА глу-ГИПОТЕЗЫ ШИЗОФРЕНИИ (Г. Бурбаева, И. Бокша, V. Haroutunyan, C. Tamminga, C. Beasley, S. Tsai 2000 -2008 гг. ) Болезнь – результат нарушений в любом из многочисленных механизмов, воздействующих на Глу-рецепторы разных типов: Ш Модификация активности рецепторов. Ш Изменение активности ферментов, участвующих в метаболизме ГЛУ. Ш Изменение активности глу-транспортера и др.
 СЕРОТОНИН-ГЛУТАМАТНАЯ ГИПОТЕЗА ШИЗОФРЕНИИ В формирование нарушений глутаматной системы вовлечена серотониновая система (формирование серотонин-глутаматных рецепторных комплексов в коре мозга 5 -HT 2 - m. Glu. R 2) При шизофрении наблюдается повышение активности 5 -HT 2 и снижение активности m. Glu. R 2, что может явится дополнительной причиной гипофункции Глу-системы.
СЕРОТОНИН-ГЛУТАМАТНАЯ ГИПОТЕЗА ШИЗОФРЕНИИ В формирование нарушений глутаматной системы вовлечена серотониновая система (формирование серотонин-глутаматных рецепторных комплексов в коре мозга 5 -HT 2 - m. Glu. R 2) При шизофрении наблюдается повышение активности 5 -HT 2 и снижение активности m. Glu. R 2, что может явится дополнительной причиной гипофункции Глу-системы.
 АУТОИММУННАЯ ГИПОТЕЗА ШИЗОФРЕНИИ (Вартанян М. Е. , Коляскина Г. И. , Семенов С. Ф. Yancovich J. , 60 -70 е годы ХХ века) Циркулирующие в крови больных аутоантитела (ААТ) к нейроантигенам, проникая в мозг, нарушают функционирование нейронных сетей и/или синаптическую передачу Экспериментальные подтверждения гипотезы: Швыявление иммунопозитивных клеток на срезах мозга ШИзменение электрической активности нейронов при аппликации ААТ ШНегативное влияние ААТ на процессы нейроонтогенеза ШСпособность ААТ проникать через ГЭБ
АУТОИММУННАЯ ГИПОТЕЗА ШИЗОФРЕНИИ (Вартанян М. Е. , Коляскина Г. И. , Семенов С. Ф. Yancovich J. , 60 -70 е годы ХХ века) Циркулирующие в крови больных аутоантитела (ААТ) к нейроантигенам, проникая в мозг, нарушают функционирование нейронных сетей и/или синаптическую передачу Экспериментальные подтверждения гипотезы: Швыявление иммунопозитивных клеток на срезах мозга ШИзменение электрической активности нейронов при аппликации ААТ ШНегативное влияние ААТ на процессы нейроонтогенеза ШСпособность ААТ проникать через ГЭБ
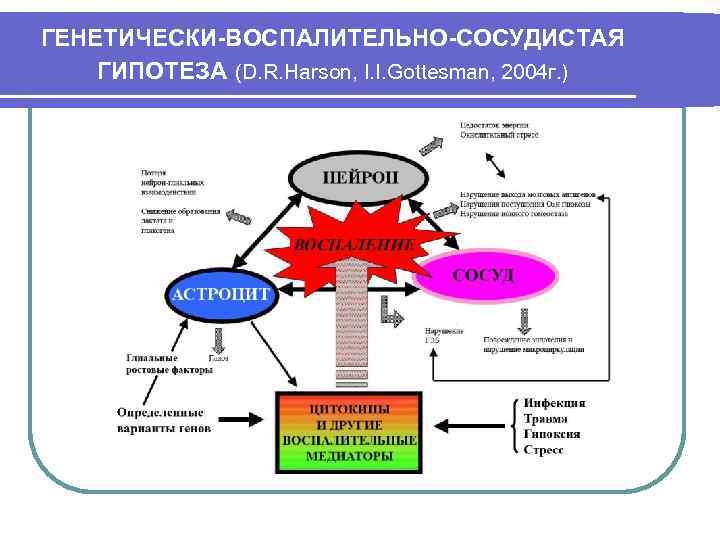
 данные литературы (2003 -2009 гг) АКТИВАЦИЯ ВРОЖДЕННОГО ИММУНИТЕТА ПРИ ШИЗОФРЕНИИ (Воспалительные реакции при шизофрении) ШУвеличение концентрации провоспалительных цитокинов в сыворотке крови (ИЛ-6, ИЛ-8, TNF alpha, гамма-интерферона). ШПрисутствие в крови маркеров воспаления (увеличение концентрации СРБ, молекул адгезии (s. ICAM), Ig. G, фосфолипазной активности и т. д). ШАктивация иммунных клеток в сыворотке (моноциты, Т-лимфоциты, натуральные киллеры). ШУвеличение продукции свободных радикалов NO. ШАктивация микроглии в мозге. ШНарушения микрососудистого русла (мозгового кровотока).
данные литературы (2003 -2009 гг) АКТИВАЦИЯ ВРОЖДЕННОГО ИММУНИТЕТА ПРИ ШИЗОФРЕНИИ (Воспалительные реакции при шизофрении) ШУвеличение концентрации провоспалительных цитокинов в сыворотке крови (ИЛ-6, ИЛ-8, TNF alpha, гамма-интерферона). ШПрисутствие в крови маркеров воспаления (увеличение концентрации СРБ, молекул адгезии (s. ICAM), Ig. G, фосфолипазной активности и т. д). ШАктивация иммунных клеток в сыворотке (моноциты, Т-лимфоциты, натуральные киллеры). ШУвеличение продукции свободных радикалов NO. ШАктивация микроглии в мозге. ШНарушения микрососудистого русла (мозгового кровотока).
 ГЕНЕТИЧЕСКИ-ВОСПАЛИТЕЛЬНО-СОСУДИСТАЯ ГИПОТЕЗА (D. R. Harson, I. I. Gottesman, 2004 г. )
ГЕНЕТИЧЕСКИ-ВОСПАЛИТЕЛЬНО-СОСУДИСТАЯ ГИПОТЕЗА (D. R. Harson, I. I. Gottesman, 2004 г. )
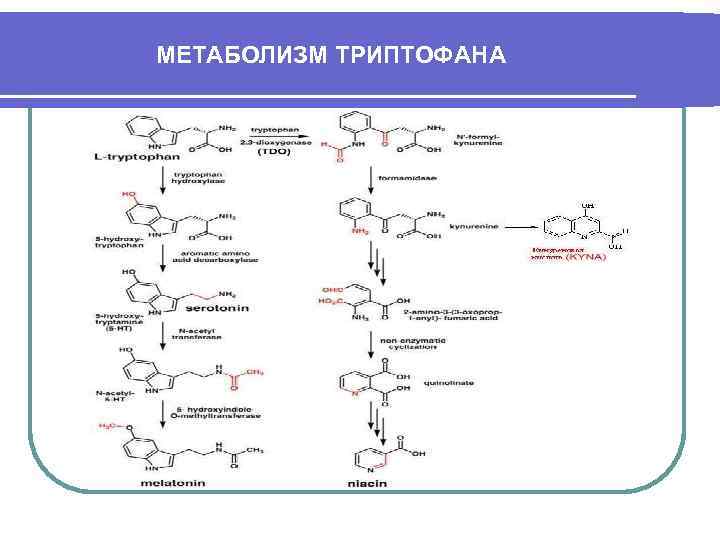
 МЕТАБОЛИЗМ ТРИПТОФАНА
МЕТАБОЛИЗМ ТРИПТОФАНА
 ПСИХОТРОПНЫЕ СВОЙСТВА КИНУРЕНОВОЙ КИСЛОТЫ (KYNA) KYNA: ШЕдинственный эндогенный антагонист NMDA- рецепторов (вызывает гипофункцию глу-системы и реципрокно активирует DA-систему). ШФункциональный антагонист серотонина (вызывает депрессивную симптоматику при шизофрении). ШСнижает проницаемость ГЭБ для триптофана. ШНарушает природные циркадные ритмы (за счет снижения синтеза мелатонина).
ПСИХОТРОПНЫЕ СВОЙСТВА КИНУРЕНОВОЙ КИСЛОТЫ (KYNA) KYNA: ШЕдинственный эндогенный антагонист NMDA- рецепторов (вызывает гипофункцию глу-системы и реципрокно активирует DA-систему). ШФункциональный антагонист серотонина (вызывает депрессивную симптоматику при шизофрении). ШСнижает проницаемость ГЭБ для триптофана. ШНарушает природные циркадные ритмы (за счет снижения синтеза мелатонина).
 КИНУРЕНОВАЯ ГИПОТЕЗА ШИЗОФРЕНИИ Erhardt S. , Schwieler L. , Nilsson L. , Lindholm K. , Engberg G. (2004 г) l Болезнь – результат дизрегуляции метаболизма триптофана, связанный с активацией факторами неспецифического иммунитета триптофан-2, 3 - диоксигеназы – фермента, направляющего метаболизм триптофана в сторону избытка кинуреновой кислоты и реципрокно снижающий синтез серотонина и мелатонина l Ингибиторы триптофан-2, 3 -диоксигеназы – перспективная мишень для создания новых типов антипсихотиков и антидепрессантов
КИНУРЕНОВАЯ ГИПОТЕЗА ШИЗОФРЕНИИ Erhardt S. , Schwieler L. , Nilsson L. , Lindholm K. , Engberg G. (2004 г) l Болезнь – результат дизрегуляции метаболизма триптофана, связанный с активацией факторами неспецифического иммунитета триптофан-2, 3 - диоксигеназы – фермента, направляющего метаболизм триптофана в сторону избытка кинуреновой кислоты и реципрокно снижающий синтез серотонина и мелатонина l Ингибиторы триптофан-2, 3 -диоксигеназы – перспективная мишень для создания новых типов антипсихотиков и антидепрессантов
 ЗАКЛЮЧЕНИЕ (биологические гипотезы): ШПри шизофрении наблюдаются нарушения иммунной системы, различных нейромедиаторных систем (DA, 5 HT, Glu), метаболизма триптофана. ШЭти нарушения формируют сложно организованный паттерн изменений, характерных для шизофрении. ШИсследование взаимосвязей внутри этого паттерна – ключевая задача биологической психиатрии в области исследований шизофрении.
ЗАКЛЮЧЕНИЕ (биологические гипотезы): ШПри шизофрении наблюдаются нарушения иммунной системы, различных нейромедиаторных систем (DA, 5 HT, Glu), метаболизма триптофана. ШЭти нарушения формируют сложно организованный паттерн изменений, характерных для шизофрении. ШИсследование взаимосвязей внутри этого паттерна – ключевая задача биологической психиатрии в области исследований шизофрении.
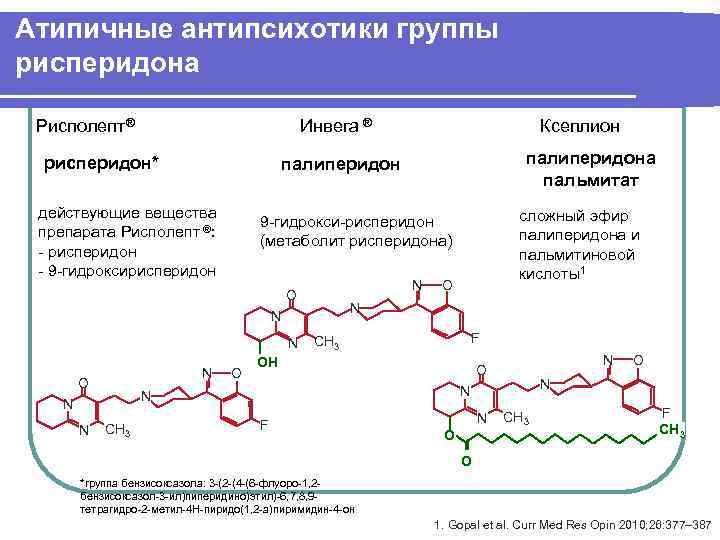
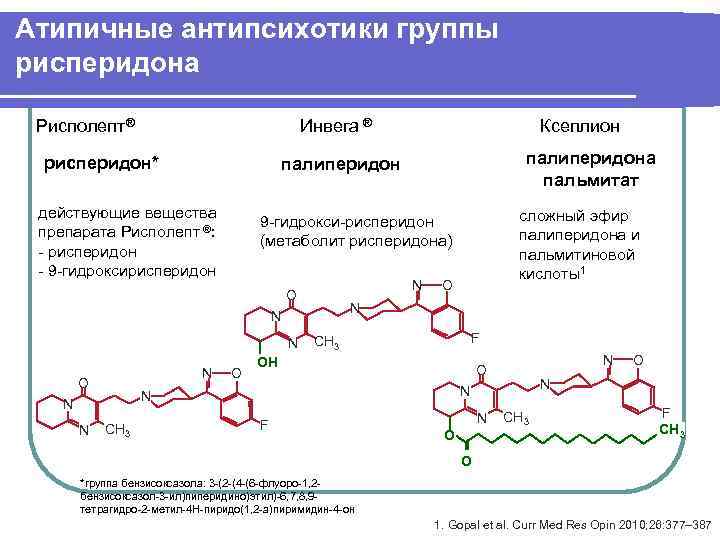
 Атипичные антипсихотики группы рисперидона Рисполепт® Инвега ® Ксеплион рисперидон* палиперидона пальмитат действующие вещества сложный эфир 9 -гидрокси-рисперидон препарата Рисполепт ®: палиперидона и (метаболит рисперидона) - рисперидон пальмитиновой - 9 -гидроксирисперидон кислоты1 N O N N CH 3 F OН N O N O O O N N N CH 3 F N CH 3 F CH 3 O *группа бензисоксазола: 3 -(2 -(4 -(6 -флуоро-1, 2 - бензисоксазол-3 -ил)пиперидино)этил)-6, 7, 8, 9 - тетрагидро-2 -метил-4 H-пиридо(1, 2 -a)пиримидин-4 -он 1. Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
Атипичные антипсихотики группы рисперидона Рисполепт® Инвега ® Ксеплион рисперидон* палиперидона пальмитат действующие вещества сложный эфир 9 -гидрокси-рисперидон препарата Рисполепт ®: палиперидона и (метаболит рисперидона) - рисперидон пальмитиновой - 9 -гидроксирисперидон кислоты1 N O N N CH 3 F OН N O N O O O N N N CH 3 F N CH 3 F CH 3 O *группа бензисоксазола: 3 -(2 -(4 -(6 -флуоро-1, 2 - бензисоксазол-3 -ил)пиперидино)этил)-6, 7, 8, 9 - тетрагидро-2 -метил-4 H-пиридо(1, 2 -a)пиримидин-4 -он 1. Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
 Инвега l Антипсихотический препарат для лечения шизофрении l Целенаправленно объединяет: l Мощный антипсихотический эффект с низкой вероятностью лекарственных взаимодействий l Инновативную систему осмотически контролируемого высвобождения препарата 5 1. Kane et al. Schizophr Res 2007; 90: 147– 61; 2. Marder et al. Biol Psychiatry in press 3. Davidson et al. 2007 Schizophr Res 2007; 93: 117– 30 4. Kramer et al. J Clin Pyschopharmacology 2007; 27: 6– 14 5. Conley et al. Curr Med Res Opin 2006; 22: 1879– 92
Инвега l Антипсихотический препарат для лечения шизофрении l Целенаправленно объединяет: l Мощный антипсихотический эффект с низкой вероятностью лекарственных взаимодействий l Инновативную систему осмотически контролируемого высвобождения препарата 5 1. Kane et al. Schizophr Res 2007; 90: 147– 61; 2. Marder et al. Biol Psychiatry in press 3. Davidson et al. 2007 Schizophr Res 2007; 93: 117– 30 4. Kramer et al. J Clin Pyschopharmacology 2007; 27: 6– 14 5. Conley et al. Curr Med Res Opin 2006; 22: 1879– 92
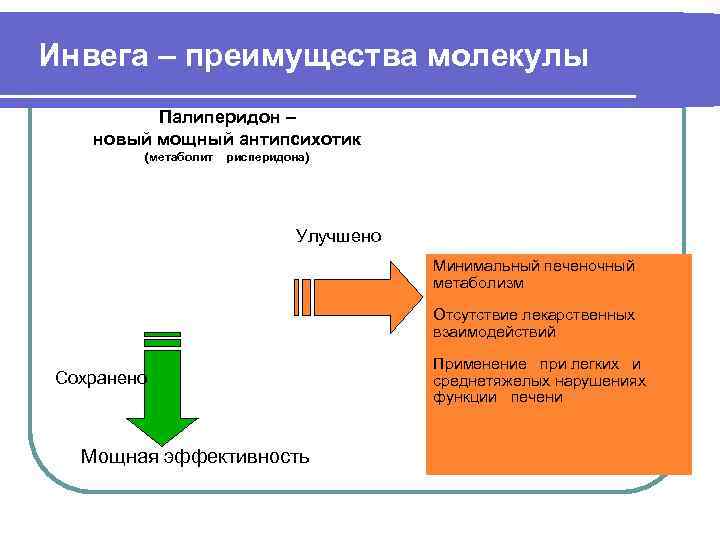
 Инвега – преимущества молекулы Палиперидон – новый мощный антипсихотик (метаболит рисперидона) Улучшено Минимальный печеночный метаболизм Отсутствие лекарственных взаимодействий Применение при легких и Сохранено среднетяжелых нарушениях функции печени Мощная эффективность
Инвега – преимущества молекулы Палиперидон – новый мощный антипсихотик (метаболит рисперидона) Улучшено Минимальный печеночный метаболизм Отсутствие лекарственных взаимодействий Применение при легких и Сохранено среднетяжелых нарушениях функции печени Мощная эффективность
 Палиперидон l Высокая аффинность к D 2 -, 5 HT 2 A-, α 1 and α 2 адренергическим рецепторам 1 палиперидон l Выделяется преимущественно почками l 59% выделяется с мочой в неизменном виде 2 (не подвергается интенсивному метаболизму в печени) l Не вызывает клинически значимых взаимодействий с лекарственными препаратами, метаболизирующимися через CYP 450 l Не требуется коррекции дозы у пациентов с легкими и среднетяжелыми нарушениями функции печени и у курильщиков 3 1. Karlsson et al. ASCPT, Baltimore 8– 11 March 2006. Poster PIII-57 2. Vermeir et al. ECNP, Amsterdam, 21– 25 October 2005. Poster P. 8. 097 3. Invega® (paliperidone) prolonged-release tablets Sm. PC, 2007
Палиперидон l Высокая аффинность к D 2 -, 5 HT 2 A-, α 1 and α 2 адренергическим рецепторам 1 палиперидон l Выделяется преимущественно почками l 59% выделяется с мочой в неизменном виде 2 (не подвергается интенсивному метаболизму в печени) l Не вызывает клинически значимых взаимодействий с лекарственными препаратами, метаболизирующимися через CYP 450 l Не требуется коррекции дозы у пациентов с легкими и среднетяжелыми нарушениями функции печени и у курильщиков 3 1. Karlsson et al. ASCPT, Baltimore 8– 11 March 2006. Poster PIII-57 2. Vermeir et al. ECNP, Amsterdam, 21– 25 October 2005. Poster P. 8. 097 3. Invega® (paliperidone) prolonged-release tablets Sm. PC, 2007
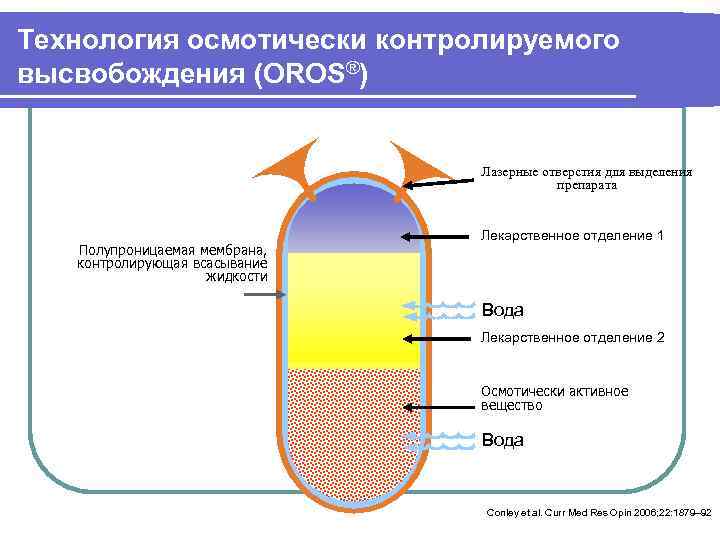
 Технология осмотически контролируемого высвобождения (OROS®) Лазерные отверстия для выделения препарата Лекарственное отделение 1 Полупроницаемая мембрана, контролирующая всасывание жидкости Вода Лекарственное отделение 2 Осмотически активное вещество Вода Conley et al. Curr Med Res Opin 2006; 22: 1879– 92
Технология осмотически контролируемого высвобождения (OROS®) Лазерные отверстия для выделения препарата Лекарственное отделение 1 Полупроницаемая мембрана, контролирующая всасывание жидкости Вода Лекарственное отделение 2 Осмотически активное вещество Вода Conley et al. Curr Med Res Opin 2006; 22: 1879– 92
 Палиперидон: система доставки OROS® l Обеспечивает контролируемое высвобождение палиперидона на протяжении 24 часов 1 l Минимальные колебания концентрации в плазме без пиков и падений 2– 4 (меньше побочных эффектов) l Отсутствие падений концентрации (стабильность эффекта) l Дает возможность однократного дозирования 2– 4 l Не требует титрования дозы: стартовая доза равна терапевтической 3, 4 1. Karlsson et al. Eur Neuropsychopharmacol 2005; 15(Suppl 3): S 386 2. Keith. Prog Neuropsychopharmacol Biol Psychiatry 2006; 30: 996– 1008 3. Conley et al. Curr Med Res Opin 2006; 22: 1879– 92 4. Kane et al. Schizophr Res 2007; 90: 147– 61
Палиперидон: система доставки OROS® l Обеспечивает контролируемое высвобождение палиперидона на протяжении 24 часов 1 l Минимальные колебания концентрации в плазме без пиков и падений 2– 4 (меньше побочных эффектов) l Отсутствие падений концентрации (стабильность эффекта) l Дает возможность однократного дозирования 2– 4 l Не требует титрования дозы: стартовая доза равна терапевтической 3, 4 1. Karlsson et al. Eur Neuropsychopharmacol 2005; 15(Suppl 3): S 386 2. Keith. Prog Neuropsychopharmacol Biol Psychiatry 2006; 30: 996– 1008 3. Conley et al. Curr Med Res Opin 2006; 22: 1879– 92 4. Kane et al. Schizophr Res 2007; 90: 147– 61
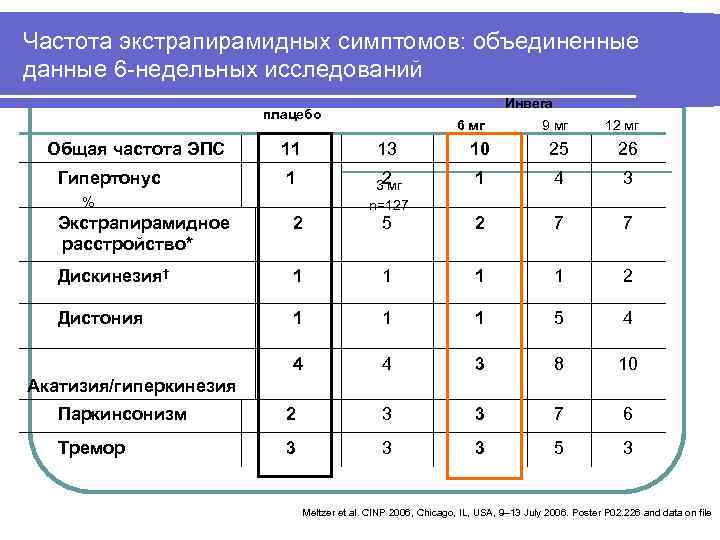
 Частота экстрапирамидных симптомов: объединенные данные 6 -недельных исследований Инвега плацебо 6 мг 9 мг 12 мг Общая частота ЭПС 11 13 10 25 26 Гипертонус 1 32 мг 1 4 3 % n=127 Экстрапирамидное 2 5 2 7 расстройство* Дискинезия† 1 2 Дистония 1 5 4 3 8 10 Акатизия/гиперкинезия Паркинсонизм 2 3 7 6 Тремор 3 5 3 Meltzer et al. CINP 2006, Chicago, IL, USA, 9– 13 July 2006. Poster P 02. 226 and data on file
Частота экстрапирамидных симптомов: объединенные данные 6 -недельных исследований Инвега плацебо 6 мг 9 мг 12 мг Общая частота ЭПС 11 13 10 25 26 Гипертонус 1 32 мг 1 4 3 % n=127 Экстрапирамидное 2 5 2 7 расстройство* Дискинезия† 1 2 Дистония 1 5 4 3 8 10 Акатизия/гиперкинезия Паркинсонизм 2 3 7 6 Тремор 3 5 3 Meltzer et al. CINP 2006, Chicago, IL, USA, 9– 13 July 2006. Poster P 02. 226 and data on file
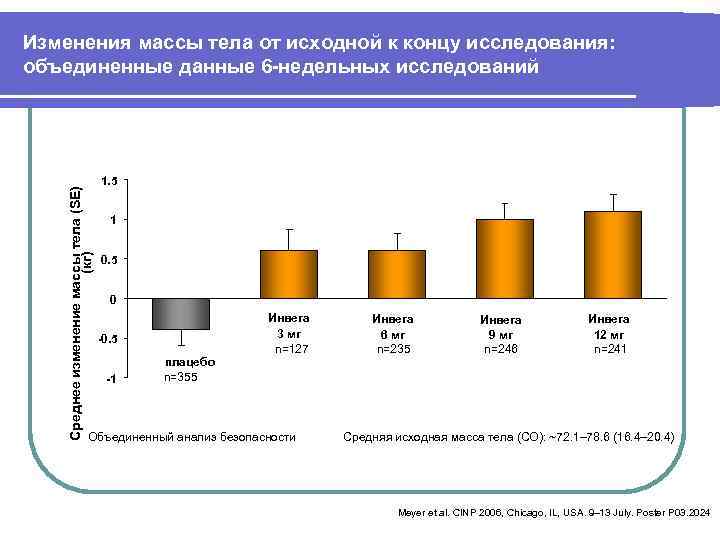
 Изменения массы тела от исходной к концу исследования: объединенные данные 6 -недельных исследований 1. 5 Среднее изменение массы тела (SE) 1 (кг) 0. 5 0 Инвега -0. 5 3 мг 6 мг 9 мг 12 мг n=127 n=235 n=246 n=241 плацебо -1 n=355 Объединенный анализ безопасности Средняя исходная масса тела (СО): ~72. 1– 78. 6 (16. 4– 20. 4) Meyer et al. CINP 2006, Chicago, IL, USA. 9– 13 July. Poster P 03. 2024
Изменения массы тела от исходной к концу исследования: объединенные данные 6 -недельных исследований 1. 5 Среднее изменение массы тела (SE) 1 (кг) 0. 5 0 Инвега -0. 5 3 мг 6 мг 9 мг 12 мг n=127 n=235 n=246 n=241 плацебо -1 n=355 Объединенный анализ безопасности Средняя исходная масса тела (СО): ~72. 1– 78. 6 (16. 4– 20. 4) Meyer et al. CINP 2006, Chicago, IL, USA. 9– 13 July. Poster P 03. 2024
 Переносимость и безопасность: пролактин l Срединное повышение сывороточного пролактина отмечалось у 67% пациентов 1 l Побочные эффекты, потенциально связанные с пролактином (аменорея, галакторея, гинекомастия), зафиксированы у 2% пациентов (vs. 1% в группе плацебо). Связь между повышением пролактина и развитием ПЯ полностью не установлена 2– 5 l Максимальное среднее повышение концентрации сывороточного пролактина обычно наблюдалось на 15 день лечения и сохранялось выше исходных уровней к концу исследования 1. Data on file; 2. Hamner. Ann Clin Psychiatry 2002; 14: 163– 73; 3. Lean and De Smedt. Int Clin Psychopharmacol 2004; 19: 31– 35 4. Hummer and Huber. Curr Med Res Opin 2004; 20: 189– 97; 5. Kleinberg et al. J Clin Psychopharmacol 1999; 19: 57– 61
Переносимость и безопасность: пролактин l Срединное повышение сывороточного пролактина отмечалось у 67% пациентов 1 l Побочные эффекты, потенциально связанные с пролактином (аменорея, галакторея, гинекомастия), зафиксированы у 2% пациентов (vs. 1% в группе плацебо). Связь между повышением пролактина и развитием ПЯ полностью не установлена 2– 5 l Максимальное среднее повышение концентрации сывороточного пролактина обычно наблюдалось на 15 день лечения и сохранялось выше исходных уровней к концу исследования 1. Data on file; 2. Hamner. Ann Clin Psychiatry 2002; 14: 163– 73; 3. Lean and De Smedt. Int Clin Psychopharmacol 2004; 19: 31– 35 4. Hummer and Huber. Curr Med Res Opin 2004; 20: 189– 97; 5. Kleinberg et al. J Clin Psychopharmacol 1999; 19: 57– 61
 Режим дозирования l Инвега продемонстрировала достоверное улучшение общего балла PANSS в дозе 6 мг 1 l 3 мг: Более высокая частота прекращения терапии из-за недостаточной эффективности и частота 30%-клинического ответа ниже* в сравнении с 6 мг 2 l Побочные явления, включая ЭПС и изменения массы тела, применении 6 мг были сравнимыми с плацебо 1 l Дозой 6 мг достигается оптимальная занятость рецепторов 2 l 6 мг – рекомендованная доза; отдельные пациенты могут нуждаться в более низкой или более высокой дозе 1. Meltzer et al. CINP 2006, Chicago, IL, USA, 9– 13 July 2006. Poster P 02. 226 2. Karlsson et al. ASCPT; March 8– 11, 2006; Baltimore, MD, USA. Poster PIII– 57
Режим дозирования l Инвега продемонстрировала достоверное улучшение общего балла PANSS в дозе 6 мг 1 l 3 мг: Более высокая частота прекращения терапии из-за недостаточной эффективности и частота 30%-клинического ответа ниже* в сравнении с 6 мг 2 l Побочные явления, включая ЭПС и изменения массы тела, применении 6 мг были сравнимыми с плацебо 1 l Дозой 6 мг достигается оптимальная занятость рецепторов 2 l 6 мг – рекомендованная доза; отдельные пациенты могут нуждаться в более низкой или более высокой дозе 1. Meltzer et al. CINP 2006, Chicago, IL, USA, 9– 13 July 2006. Poster P 02. 226 2. Karlsson et al. ASCPT; March 8– 11, 2006; Baltimore, MD, USA. Poster PIII– 57
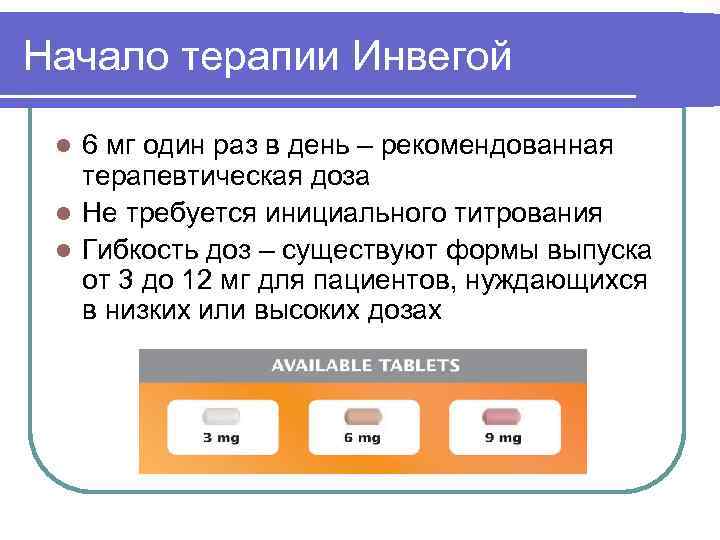
 Начало терапии Инвегой l 6 мг один раз в день – рекомендованная терапевтическая доза l Не требуется инициального титрования l Гибкость доз – существуют формы выпуска от 3 до 12 мг для пациентов, нуждающихся в низких или высоких дозах
Начало терапии Инвегой l 6 мг один раз в день – рекомендованная терапевтическая доза l Не требуется инициального титрования l Гибкость доз – существуют формы выпуска от 3 до 12 мг для пациентов, нуждающихся в низких или высоких дозах
 Заключение l Инвега разработана целенаправленно с целью объединения эффективности антипсихотика с осмотической системой доставки в течение 24 часов 1 l В основных исследованиях продемонстрирована стабильная эффективность l Достоверное улучшение широкого спектра симптомов шизофрении 2 l Раннее начало действия l Эффективность в предотвращении обострений 3 l Достоверное улучшение повседневного и социального функционирования 2 l Доказанная безопасность и переносимость l ЭПС и изменения массы тела в рекомендованной дозе 6 мг сравнимы с плацебо 2 l Отсутствие клинически значимых изменений липидов и глюкозы как в 6 -недельных, так и в длительных исследованиях4 1. Conley et al. Curr Med Res Opin 2006; 22: 1879– 92; 2. Meltzer H et al. CINP 2006, Chicago, IL, USA, 9– 13 July 2006. Poster P 02. 226 3. Kramer et al. J Clin Psychopharm 2007; 27: 6– 14; 4. Kramer et al. APA 2007, San Diego, CA, May 19– 24. Poster NR 498
Заключение l Инвега разработана целенаправленно с целью объединения эффективности антипсихотика с осмотической системой доставки в течение 24 часов 1 l В основных исследованиях продемонстрирована стабильная эффективность l Достоверное улучшение широкого спектра симптомов шизофрении 2 l Раннее начало действия l Эффективность в предотвращении обострений 3 l Достоверное улучшение повседневного и социального функционирования 2 l Доказанная безопасность и переносимость l ЭПС и изменения массы тела в рекомендованной дозе 6 мг сравнимы с плацебо 2 l Отсутствие клинически значимых изменений липидов и глюкозы как в 6 -недельных, так и в длительных исследованиях4 1. Conley et al. Curr Med Res Opin 2006; 22: 1879– 92; 2. Meltzer H et al. CINP 2006, Chicago, IL, USA, 9– 13 July 2006. Poster P 02. 226 3. Kramer et al. J Clin Psychopharm 2007; 27: 6– 14; 4. Kramer et al. APA 2007, San Diego, CA, May 19– 24. Poster NR 498
 Инструкция по применению Инвега – таблетки пролонгированного действия Активное вещество: 3 мг, 6 мг или 9 мг палиперидона l Дети и подростки: не рекомендовано. l Пожилые пациенты: с осторожностью у пожилых пациентов с факторами риска развития инсульта. l Пациенты с нарушением функции почек: при легкой и средней степени нарушения функции почек рекомендовано начинать терапию с 3 мг один раз в сутки. Для пациентов с тяжелыми нарушениями функции почек рекомендована терапевтическая доза 3 мг через день. l Пациенты с нарушениями функции печени: при легкой или средней степени нарушения функции печени не требуется коррекции дозы. Назначать с осторожностью пациентам с тяжелыми нарушениями печеночной функции.
Инструкция по применению Инвега – таблетки пролонгированного действия Активное вещество: 3 мг, 6 мг или 9 мг палиперидона l Дети и подростки: не рекомендовано. l Пожилые пациенты: с осторожностью у пожилых пациентов с факторами риска развития инсульта. l Пациенты с нарушением функции почек: при легкой и средней степени нарушения функции почек рекомендовано начинать терапию с 3 мг один раз в сутки. Для пациентов с тяжелыми нарушениями функции почек рекомендована терапевтическая доза 3 мг через день. l Пациенты с нарушениями функции печени: при легкой или средней степени нарушения функции печени не требуется коррекции дозы. Назначать с осторожностью пациентам с тяжелыми нарушениями печеночной функции.
 Инструкция по применению Предупреждения: С осторожностью назначать пациентам с сердечно- сосудистыми заболеваниями или с семейным анамнезом удлинения интервала QT. С осторожностью назначать пациентам с цереброваскулярными нарушениями или предрасположенностью к гипотензии. С осторожностью назначать пациентам с судорожным синдромом в анамнезе, т. к. потенциально может понижать порог судорожной готовности.
Инструкция по применению Предупреждения: С осторожностью назначать пациентам с сердечно- сосудистыми заболеваниями или с семейным анамнезом удлинения интервала QT. С осторожностью назначать пациентам с цереброваскулярными нарушениями или предрасположенностью к гипотензии. С осторожностью назначать пациентам с судорожным синдромом в анамнезе, т. к. потенциально может понижать порог судорожной готовности.
 КСЕПЛИОН новый препарат для лечения шизофрении
КСЕПЛИОН новый препарат для лечения шизофрении
 Атипичные антипсихотики группы рисперидона Рисполепт® Инвега ® Ксеплион рисперидон* палиперидона пальмитат действующие вещества сложный эфир 9 -гидрокси-рисперидон препарата Рисполепт ®: палиперидона и (метаболит рисперидона) - рисперидон пальмитиновой - 9 -гидроксирисперидон кислоты1 N O N N CH 3 F OН N O N O O O N N N CH 3 F N CH 3 F CH 3 O *группа бензисоксазола: 3 -(2 -(4 -(6 -флуоро-1, 2 - бензисоксазол-3 -ил)пиперидино)этил)-6, 7, 8, 9 - тетрагидро-2 -метил-4 H-пиридо(1, 2 -a)пиримидин-4 -он 1. Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
Атипичные антипсихотики группы рисперидона Рисполепт® Инвега ® Ксеплион рисперидон* палиперидона пальмитат действующие вещества сложный эфир 9 -гидрокси-рисперидон препарата Рисполепт ®: палиперидона и (метаболит рисперидона) - рисперидон пальмитиновой - 9 -гидроксирисперидон кислоты1 N O N N CH 3 F OН N O N O O O N N N CH 3 F N CH 3 F CH 3 O *группа бензисоксазола: 3 -(2 -(4 -(6 -флуоро-1, 2 - бензисоксазол-3 -ил)пиперидино)этил)-6, 7, 8, 9 - тетрагидро-2 -метил-4 H-пиридо(1, 2 -a)пиримидин-4 -он 1. Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
 Показания к применению КСЕПЛИОН показан для лечения шизофрении и профилактики рецидивов шизофрении. На КСЕПЛИОН удобно переводить взрослых пациентов, состояние которых было стабилизировано палиперидоном или рисперидоном. У некоторых взрослых пациентов с шизофренией, ранее реагировавших на пероральные палиперидон или рисперидон, КСЕПЛИОН может применяться без предварительной стабилизации пероральными средствами, если психотические симптомы имеют легкую/среднюю степень тяжести и требуется терапия инъекционными средствами длительного действия
Показания к применению КСЕПЛИОН показан для лечения шизофрении и профилактики рецидивов шизофрении. На КСЕПЛИОН удобно переводить взрослых пациентов, состояние которых было стабилизировано палиперидоном или рисперидоном. У некоторых взрослых пациентов с шизофренией, ранее реагировавших на пероральные палиперидон или рисперидон, КСЕПЛИОН может применяться без предварительной стабилизации пероральными средствами, если психотические симптомы имеют легкую/среднюю степень тяжести и требуется терапия инъекционными средствами длительного действия
 Обзор препарата КСЕПЛИОН Молекула l Действующее вещество: палиперидон l Химико-физическая структура: пальмитат (сложный эфир пальмитиновой кислоты) палиперидона. l Форма: водная суспензия для внутримышечного ведения пролонгированного действия. l Хранение: при комнатной температуре в виде готовой суспензии l Механизм действия: антагонист D 2 и серотониновых 5 -HT 2 A рецепторов, антагонист α 1 - и α 2 - адренергических и H 1 -гистаминергических рецепторов. Отсутствие блокады холинергических, мускариновых, ß 1 - и ß 2 - адренергических рецепторов (способствует хорошей переносимости) l Метаболизм: выводится преимущественно почками (80% выводится с мочой), слабо метаболизируется печенью (отсутствие клинически значимых взаимодействий с препаратами, метаболизиуемыми CYP 450), не требует коррекции дозы у пациентов с низкой или средней степенью печеночной недостаточности 1. Invega® (paliperidone ER) prolonged-release tablets Sm. PC, December 2010; 2. Vermeir et al. Drug Metab Dispos 2008; 36: 769– 779
Обзор препарата КСЕПЛИОН Молекула l Действующее вещество: палиперидон l Химико-физическая структура: пальмитат (сложный эфир пальмитиновой кислоты) палиперидона. l Форма: водная суспензия для внутримышечного ведения пролонгированного действия. l Хранение: при комнатной температуре в виде готовой суспензии l Механизм действия: антагонист D 2 и серотониновых 5 -HT 2 A рецепторов, антагонист α 1 - и α 2 - адренергических и H 1 -гистаминергических рецепторов. Отсутствие блокады холинергических, мускариновых, ß 1 - и ß 2 - адренергических рецепторов (способствует хорошей переносимости) l Метаболизм: выводится преимущественно почками (80% выводится с мочой), слабо метаболизируется печенью (отсутствие клинически значимых взаимодействий с препаратами, метаболизиуемыми CYP 450), не требует коррекции дозы у пациентов с низкой или средней степенью печеночной недостаточности 1. Invega® (paliperidone ER) prolonged-release tablets Sm. PC, December 2010; 2. Vermeir et al. Drug Metab Dispos 2008; 36: 769– 779
 Обзор препарата КСЕПЛИОН Фармакокинетика и фармакодинамика l Максимальная концентрация препарата в плазме крови (tmax) достигается к 13 -14 дню для дельтовидного введения и к 13 -17 дню при введении в ягодичную мышцу l Высвобождение препарата начинается в первый день после инъекции l Максимальная концентрация препарата в плазме крови (Cmax) после однократного введения в дельтовидную мышцу на 28% выше, чем при введении в ягодичную мышцу l Стабильная концентрация при рекомендованной схеме инициирующей терапии достигалась в течение 1 недели l Средний период полувыведения – 25– 49 дней (выше при высоких дозах) 1. Proposed Xeplion® EU Sm. PC; 2. Samtani et al. Poster presented at APA, May 16– 21 2009, San Francisco, CA, USA
Обзор препарата КСЕПЛИОН Фармакокинетика и фармакодинамика l Максимальная концентрация препарата в плазме крови (tmax) достигается к 13 -14 дню для дельтовидного введения и к 13 -17 дню при введении в ягодичную мышцу l Высвобождение препарата начинается в первый день после инъекции l Максимальная концентрация препарата в плазме крови (Cmax) после однократного введения в дельтовидную мышцу на 28% выше, чем при введении в ягодичную мышцу l Стабильная концентрация при рекомендованной схеме инициирующей терапии достигалась в течение 1 недели l Средний период полувыведения – 25– 49 дней (выше при высоких дозах) 1. Proposed Xeplion® EU Sm. PC; 2. Samtani et al. Poster presented at APA, May 16– 21 2009, San Francisco, CA, USA
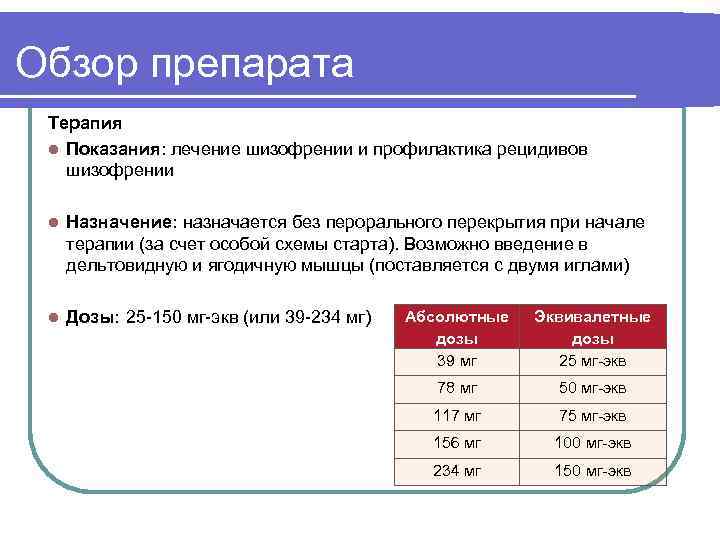
 Обзор препарата Терапия l Показания: лечение шизофрении и профилактика рецидивов шизофрении l Назначение: назначается без перорального перекрытия при начале терапии (за счет особой схемы старта). Возможно введение в дельтовидную и ягодичную мышцы (поставляется с двумя иглами) l Дозы: 25 -150 мг-экв (или 39 -234 мг) Абсолютные Эквивалетные дозы 39 мг 25 мг-экв 78 мг 50 мг-экв 117 мг 75 мг-экв 156 мг 100 мг-экв 234 мг 150 мг-экв
Обзор препарата Терапия l Показания: лечение шизофрении и профилактика рецидивов шизофрении l Назначение: назначается без перорального перекрытия при начале терапии (за счет особой схемы старта). Возможно введение в дельтовидную и ягодичную мышцы (поставляется с двумя иглами) l Дозы: 25 -150 мг-экв (или 39 -234 мг) Абсолютные Эквивалетные дозы 39 мг 25 мг-экв 78 мг 50 мг-экв 117 мг 75 мг-экв 156 мг 100 мг-экв 234 мг 150 мг-экв
 Обзор препарата Результаты l Эффективность и безопасность по сравнению с плацебо: доказаны в 4 краткосрочных и долгосрочном КИ 3 фазы (значительно и статистически достоверно более высокие баллы PANSS и более длительное время до прогрессирования заболевания) l Эффективность и безопасность относительно РК: сопоставимы (отсутствие преимущества) l Хорошая переносимость. Низкий уровень набора веса и ЭПС. Отсутствие сообщений о постинъекционном синдроме. Низкая степень влияния на печень
Обзор препарата Результаты l Эффективность и безопасность по сравнению с плацебо: доказаны в 4 краткосрочных и долгосрочном КИ 3 фазы (значительно и статистически достоверно более высокие баллы PANSS и более длительное время до прогрессирования заболевания) l Эффективность и безопасность относительно РК: сопоставимы (отсутствие преимущества) l Хорошая переносимость. Низкий уровень набора веса и ЭПС. Отсутствие сообщений о постинъекционном синдроме. Низкая степень влияния на печень
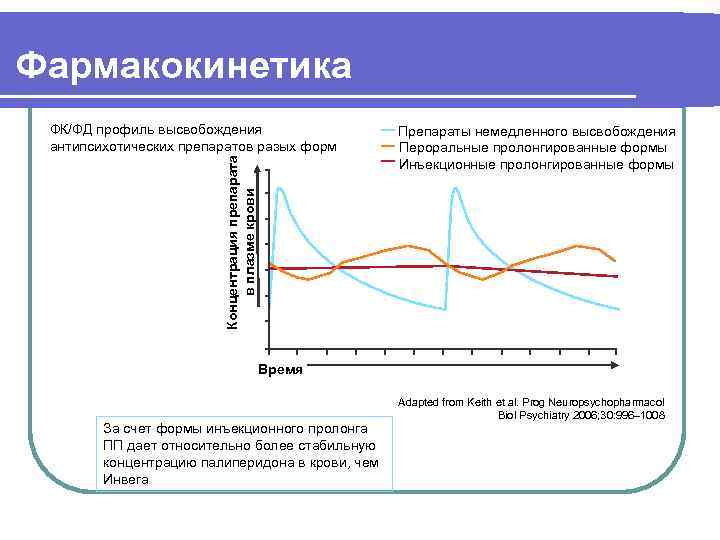
 Фармакокинетика ФК/ФД профиль высвобождения Препараты немедленного высвобождения антипсихотических препаратов разых форм Пероральные пролонгированные формы Концентрация препарата Инъекционные пролонгированные формы в плазме крови Время Adapted from Keith et al. Prog Neuropsychopharmacol Biol Psychiatry 2006; 30: 996– 1008 За счет формы инъекционного пролонга ПП дает относительно более стабильную концентрацию палиперидона в крови, чем Инвега
Фармакокинетика ФК/ФД профиль высвобождения Препараты немедленного высвобождения антипсихотических препаратов разых форм Пероральные пролонгированные формы Концентрация препарата Инъекционные пролонгированные формы в плазме крови Время Adapted from Keith et al. Prog Neuropsychopharmacol Biol Psychiatry 2006; 30: 996– 1008 За счет формы инъекционного пролонга ПП дает относительно более стабильную концентрацию палиперидона в крови, чем Инвега
 Пациенты особых категорий: рекомендации по дозировке l Почечная недостаточность: l Легкая (клиренс креатинина 50–<80 мл/мин): l Доза в интервале 25– 100 мг исходя из особенностей переносимости и/или эффективности терапии у конкретного пациента l Средней/серьезной степени тяжести: применение не рекомендуется l Печеночная недостаточность: l Легкой/средней степени тяжести: корректировка дозы не требуется l Серьезной степени тяжести: применение палиперидона не исследовалось l Пациенты пожилого возраста: l Дозировка аналогична молодым взрослым; корректируйте дозу с учетом состояния почечной функции 1. Инструкция по применению препарата Ксеплион от 28. 02. 11, ЛСР-009014/10 2. Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
Пациенты особых категорий: рекомендации по дозировке l Почечная недостаточность: l Легкая (клиренс креатинина 50–<80 мл/мин): l Доза в интервале 25– 100 мг исходя из особенностей переносимости и/или эффективности терапии у конкретного пациента l Средней/серьезной степени тяжести: применение не рекомендуется l Печеночная недостаточность: l Легкой/средней степени тяжести: корректировка дозы не требуется l Серьезной степени тяжести: применение палиперидона не исследовалось l Пациенты пожилого возраста: l Дозировка аналогична молодым взрослым; корректируйте дозу с учетом состояния почечной функции 1. Инструкция по применению препарата Ксеплион от 28. 02. 11, ЛСР-009014/10 2. Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
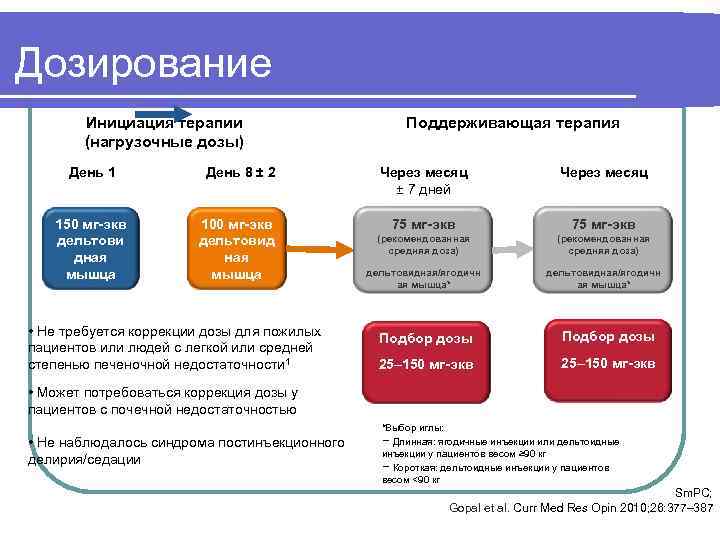
 Дозирование Инициация терапии Поддерживающая терапия (нагрузочные дозы) День 1 День 8 ± 2 Через месяц ± 7 дней 150 мг-экв 100 мг-экв 75 мг-экв дельтовид (рекомендованная средняя доза) дная ная мышца дельтовидная/ягодичн ая мышца* • Не требуется коррекции дозы для пожилых Подбор дозы пациентов или людей с легкой или средней степенью печеночной недостаточности 1 25– 150 мг-экв • Может потребоваться коррекция дозы у пациентов с почечной недостаточностью *Выбор иглы: • Не наблюдалось синдрома постинъекционного – Длинная: ягодичные инъекции или дельтоидные инъекции у пациентов весом ≥ 90 кг делирия/седации – Короткая: дельтоидные инъекции у пациентов весом <90 кг Sm. PC; Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
Дозирование Инициация терапии Поддерживающая терапия (нагрузочные дозы) День 1 День 8 ± 2 Через месяц ± 7 дней 150 мг-экв 100 мг-экв 75 мг-экв дельтовид (рекомендованная средняя доза) дная ная мышца дельтовидная/ягодичн ая мышца* • Не требуется коррекции дозы для пожилых Подбор дозы пациентов или людей с легкой или средней степенью печеночной недостаточности 1 25– 150 мг-экв • Может потребоваться коррекция дозы у пациентов с почечной недостаточностью *Выбор иглы: • Не наблюдалось синдрома постинъекционного – Длинная: ягодичные инъекции или дельтоидные инъекции у пациентов весом ≥ 90 кг делирия/седации – Короткая: дельтоидные инъекции у пациентов весом <90 кг Sm. PC; Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
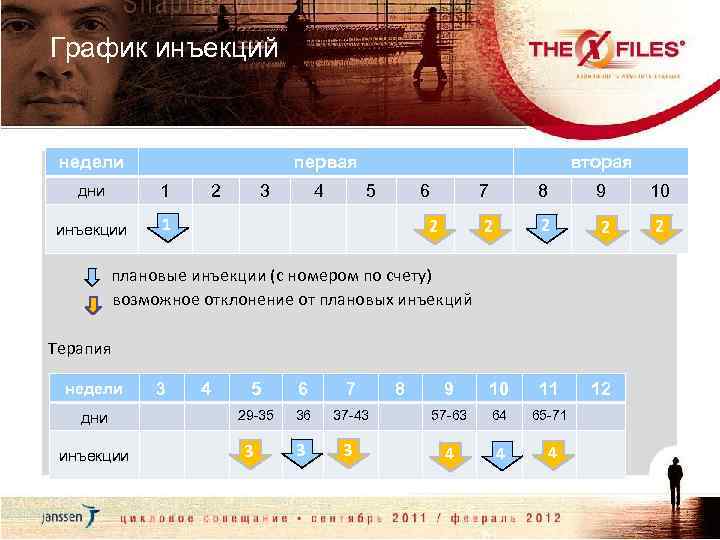
 График инъекций недели первая вторая дни 1 2 3 4 5 6 7 8 9 10 инъекции 1 2 2 2 2 плановые инъекции (с номером по счету) возможное отклонение от плановых инъекций Терапия недели 3 4 5 6 7 8 9 10 11 12 дни 29 -35 36 37 -43 57 -63 64 65 -71 инъекции 3 3 4 4
График инъекций недели первая вторая дни 1 2 3 4 5 6 7 8 9 10 инъекции 1 2 2 2 2 плановые инъекции (с номером по счету) возможное отклонение от плановых инъекций Терапия недели 3 4 5 6 7 8 9 10 11 12 дни 29 -35 36 37 -43 57 -63 64 65 -71 инъекции 3 3 4 4
 Пропуск инъекций при поддерживающей терапии (с третьей инъекции) Временной интервал с Режим введения Доза палиперидона пальмитата и место момента последней инъекции До 1 недели Допустимый интервал Ранее применявшаяся поддерживающая ± 7 дней доза (25 -150 мг экв) в ягодичную или дельтовидную мышцу 1 -6 недель Возобновить инъекции Ранее применявшаяся поддерживающая как можно скорее доза в дельтовидную мышцу >6 недель и <6 месяцев Две инъекции, через 1 Ранее применявшаяся поддерживающая неделю доза в дельтовидную мышцу* >6 месяцев De novo с применением 150/100 мг экв в Дни 1/8 с момента начального режима возобновления терапии в дельтовидную введений мыщцу с последующими ежемесячными поддерживающими дозами *Кроме случаев, когда состояние пациента было стабилизировано на терапии дозой 150 мг экв – в этом случае две первые инъекции должны быть по 100 мг экв Gopal et al, 2010
Пропуск инъекций при поддерживающей терапии (с третьей инъекции) Временной интервал с Режим введения Доза палиперидона пальмитата и место момента последней инъекции До 1 недели Допустимый интервал Ранее применявшаяся поддерживающая ± 7 дней доза (25 -150 мг экв) в ягодичную или дельтовидную мышцу 1 -6 недель Возобновить инъекции Ранее применявшаяся поддерживающая как можно скорее доза в дельтовидную мышцу >6 недель и <6 месяцев Две инъекции, через 1 Ранее применявшаяся поддерживающая неделю доза в дельтовидную мышцу* >6 месяцев De novo с применением 150/100 мг экв в Дни 1/8 с момента начального режима возобновления терапии в дельтовидную введений мыщцу с последующими ежемесячными поддерживающими дозами *Кроме случаев, когда состояние пациента было стабилизировано на терапии дозой 150 мг экв – в этом случае две первые инъекции должны быть по 100 мг экв Gopal et al, 2010
 Необходимость инициирующих доз • При начале терапии с дозы 75 мг экв концентрация палиперидона в плазме крови стабилизировалась до 3 мес • Все это время сохранялся риск субоптимального терапевтического ответа или отсутствия эффективности • После начального введения 150 мг экв у 84% пациентов уже через 1 неделю достигается терапевтическая концентрация палиперидона в плазме крови (7, 5 нг/мл и выше) • Концентрация палиперидона в плазме крови 7. 5 нг/мл – пороговое значение терапевтической концентрации (соответствует занятости центральных D 2 -рецепторов около 60%). На основании данных позитронно-эмиссионной томографии предполагается, что требуется занятость D 2 -рецепторов в диапазоне 60 -80% для достижения удовлетворительного антипсихотического ответа • Рекомендованная начальная доза палиперидона пальмитата не просто является суммой рекомендованных суточных доз орального палиперидона ER (6 мг) для 1 месяца терапии, но вычислена на основании результатов клинических исследований и всестороннего популяционного фармакокинетического моделирования
Необходимость инициирующих доз • При начале терапии с дозы 75 мг экв концентрация палиперидона в плазме крови стабилизировалась до 3 мес • Все это время сохранялся риск субоптимального терапевтического ответа или отсутствия эффективности • После начального введения 150 мг экв у 84% пациентов уже через 1 неделю достигается терапевтическая концентрация палиперидона в плазме крови (7, 5 нг/мл и выше) • Концентрация палиперидона в плазме крови 7. 5 нг/мл – пороговое значение терапевтической концентрации (соответствует занятости центральных D 2 -рецепторов около 60%). На основании данных позитронно-эмиссионной томографии предполагается, что требуется занятость D 2 -рецепторов в диапазоне 60 -80% для достижения удовлетворительного антипсихотического ответа • Рекомендованная начальная доза палиперидона пальмитата не просто является суммой рекомендованных суточных доз орального палиперидона ER (6 мг) для 1 месяца терапии, но вычислена на основании результатов клинических исследований и всестороннего популяционного фармакокинетического моделирования
 Молекула l Сложный эфир палиперидона 3 N O N N CH 3 F O CH 3 l Для создания водной. Oсуспензии для внутримышечных инъекций используется технология Nanocrystal® (патент Elan Pharma International Limited)1, 2 l После инъекции ПП медленно диффундирует из места введения, гидролизуясь до палиперидона 2 1. http: //www. elandrugtechnologies. com/nanocrystal technology; accessed 18 June 2010; 2. Citrome. Int J Clin Pract 2010; 64: 216– 239; 3. Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
Молекула l Сложный эфир палиперидона 3 N O N N CH 3 F O CH 3 l Для создания водной. Oсуспензии для внутримышечных инъекций используется технология Nanocrystal® (патент Elan Pharma International Limited)1, 2 l После инъекции ПП медленно диффундирует из места введения, гидролизуясь до палиперидона 2 1. http: //www. elandrugtechnologies. com/nanocrystal technology; accessed 18 June 2010; 2. Citrome. Int J Clin Pract 2010; 64: 216– 239; 3. Gopal et al. Curr Med Res Opin 2010; 26: 377– 387
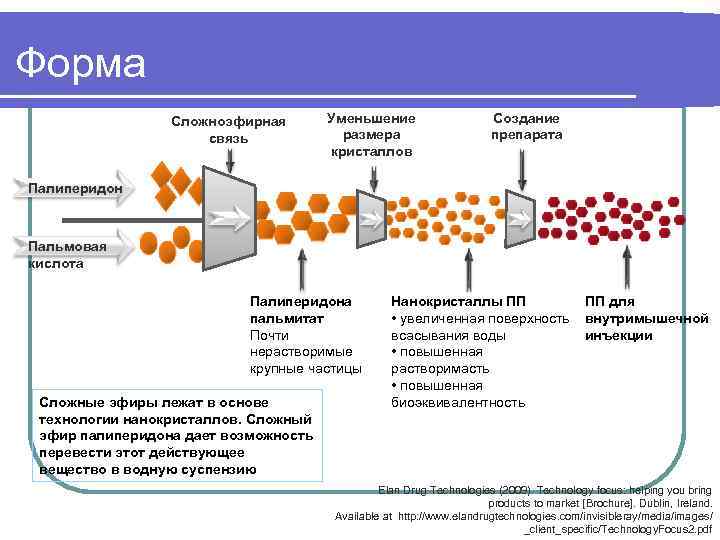
 Форма Сложноэфирная Уменьшение Создание связь размера препарата кристаллов Палиперидон Пальмовая кислота Палиперидона Нанокристаллы ПП ПП для пальмитат • увеличенная поверхность внутримышечной Почти всасывания воды инъекции нерастворимые • повышенная крупные частицы растворимасть • повышенная Сложные эфиры лежат в основе биоэквивалентность технологии нанокристаллов. Сложный эфир палиперидона дает возможность перевести этот действующее вещество в водную суспензию Elan Drug Technologies (2009). Technology focus: helping you bring products to market [Brochure]. Dublin, Ireland. Available at http: //www. elandrugtechnologies. com/invisibleray/media/images/ _client_specific/Technology. Focus 2. pdf
Форма Сложноэфирная Уменьшение Создание связь размера препарата кристаллов Палиперидон Пальмовая кислота Палиперидона Нанокристаллы ПП ПП для пальмитат • увеличенная поверхность внутримышечной Почти всасывания воды инъекции нерастворимые • повышенная крупные частицы растворимасть • повышенная Сложные эфиры лежат в основе биоэквивалентность технологии нанокристаллов. Сложный эфир палиперидона дает возможность перевести этот действующее вещество в водную суспензию Elan Drug Technologies (2009). Technology focus: helping you bring products to market [Brochure]. Dublin, Ireland. Available at http: //www. elandrugtechnologies. com/invisibleray/media/images/ _client_specific/Technology. Focus 2. pdf
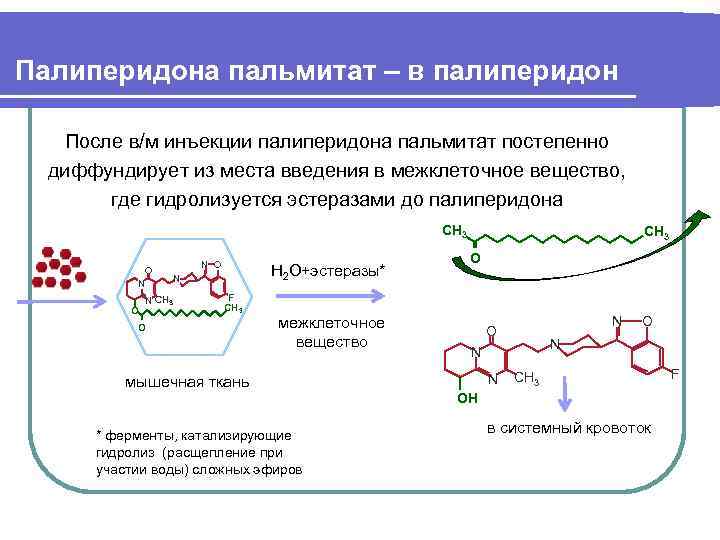
 Палиперидона пальмитат – в палиперидон После в/м инъекции палиперидона пальмитат постепенно диффундирует из места введения в межклеточное вещество, где гидролизуется эстеразами до палиперидона CH 3 N O N H 2 O+эстеразы* N CH 3 F O CH 3 O межклеточное N O вещество N N CH 3 F мышечная ткань OН * ферменты, катализирующие в системный кровоток гидролиз (расщепление при участии воды) сложных эфиров
Палиперидона пальмитат – в палиперидон После в/м инъекции палиперидона пальмитат постепенно диффундирует из места введения в межклеточное вещество, где гидролизуется эстеразами до палиперидона CH 3 N O N H 2 O+эстеразы* N CH 3 F O CH 3 O межклеточное N O вещество N N CH 3 F мышечная ткань OН * ферменты, катализирующие в системный кровоток гидролиз (расщепление при участии воды) сложных эфиров
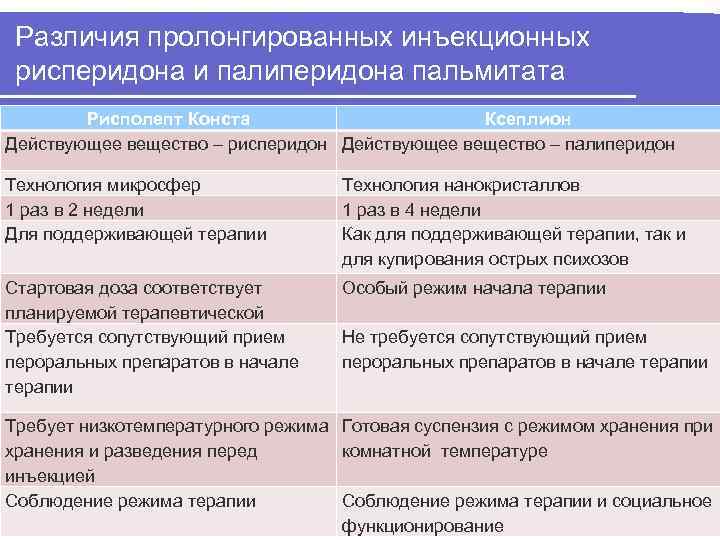
 Различия пролонгированных инъекционных рисперидона и палиперидона пальмитата Рисполепт Конста Ксеплион Действующее вещество – рисперидон Действующее вещество – палиперидон Технология микросфер Технология нанокристаллов 1 раз в 2 недели 1 раз в 4 недели Для поддерживающей терапии Как для поддерживающей терапии, так и для купирования острых психозов Стартовая доза соответствует Особый режим начала терапии планируемой терапевтической Требуется сопутствующий прием Не требуется сопутствующий прием пероральных препаратов в начале терапии Требует низкотемпературного режима Готовая суспензия с режимом хранения при хранения и разведения перед комнатной температуре инъекцией Соблюдение режима терапии и социальное функционирование
Различия пролонгированных инъекционных рисперидона и палиперидона пальмитата Рисполепт Конста Ксеплион Действующее вещество – рисперидон Действующее вещество – палиперидон Технология микросфер Технология нанокристаллов 1 раз в 2 недели 1 раз в 4 недели Для поддерживающей терапии Как для поддерживающей терапии, так и для купирования острых психозов Стартовая доза соответствует Особый режим начала терапии планируемой терапевтической Требуется сопутствующий прием Не требуется сопутствующий прием пероральных препаратов в начале терапии Требует низкотемпературного режима Готовая суспензия с режимом хранения при хранения и разведения перед комнатной температуре инъекцией Соблюдение режима терапии и социальное функционирование
 Выводы l Программа клинической разработки палиперидона пальмитата позволила оптимизировать стратегию инициирующей терапии и выбора места инъекции l Отмечается достоверное улучшение балла по шкале PANSS после 8 дней терапии у пациентов, получавших палиперидона пальмитат, по сравнению с группой плацебо 1 l Переносимость при инъекции препарата в дельтовидную и ягодичную мышцу сходна 2 l Инъекции в дельтовидную мышцу были несколько более болезненными по сравнению с аналогичными инъекциями в ягодичную мышцу l Каких-либо предпочтений в выборе места инъекции для различных доз выявлено не было 2 1. Kramer et al. Int J Neuropsychopharmacol 2010; 13: 635– 647; 2. Hough et al. Prog Neuropsychopharmacol Biol Psychiatry 2009; 33: 1022– 1031
Выводы l Программа клинической разработки палиперидона пальмитата позволила оптимизировать стратегию инициирующей терапии и выбора места инъекции l Отмечается достоверное улучшение балла по шкале PANSS после 8 дней терапии у пациентов, получавших палиперидона пальмитат, по сравнению с группой плацебо 1 l Переносимость при инъекции препарата в дельтовидную и ягодичную мышцу сходна 2 l Инъекции в дельтовидную мышцу были несколько более болезненными по сравнению с аналогичными инъекциями в ягодичную мышцу l Каких-либо предпочтений в выборе места инъекции для различных доз выявлено не было 2 1. Kramer et al. Int J Neuropsychopharmacol 2010; 13: 635– 647; 2. Hough et al. Prog Neuropsychopharmacol Biol Psychiatry 2009; 33: 1022– 1031
 Выводы l Палиперидона пальмитат (25– 100 мг-экв) значимо увеличивал время до развития симптомов рецидива в сравнении с плацебо у пациентов со стабильной шизофренией. l Заключительный анализ подтвердил, что назначение палиперидона пальмитата один раз в месяц снижает тяжесть симптоматики и поддерживает стабильность эффекта. . l Клинически значимое улучшение средней оценки по шкале PSP во время переходной/поддерживающей фазы сохранялось у больных, продолжавших принимать палиперидона пальмитат в фазе двойного слепого лечения. l Данные по общей безопасности соответствуют результатам предшествующих кратковременных исследований с палиперидоном пальмитатом у пациентов с симптоматикой. Hough et al. Schizophr Res 2010; 116: 107– 117; Gopal et al. J Psychopharmacol 2010 [Epub ahead of print]
Выводы l Палиперидона пальмитат (25– 100 мг-экв) значимо увеличивал время до развития симптомов рецидива в сравнении с плацебо у пациентов со стабильной шизофренией. l Заключительный анализ подтвердил, что назначение палиперидона пальмитата один раз в месяц снижает тяжесть симптоматики и поддерживает стабильность эффекта. . l Клинически значимое улучшение средней оценки по шкале PSP во время переходной/поддерживающей фазы сохранялось у больных, продолжавших принимать палиперидона пальмитат в фазе двойного слепого лечения. l Данные по общей безопасности соответствуют результатам предшествующих кратковременных исследований с палиперидоном пальмитатом у пациентов с симптоматикой. Hough et al. Schizophr Res 2010; 116: 107– 117; Gopal et al. J Psychopharmacol 2010 [Epub ahead of print]

