СИНТЕЗ ГЛЮКОЗЫ В ПЕЧЕНИ.ppt
- Количество слайдов: 32
 СИНТЕЗ ГЛЮКОЗЫ В ПЕЧЕНИ (ГЛЮКОНЕОГЕНЕЗ)
СИНТЕЗ ГЛЮКОЗЫ В ПЕЧЕНИ (ГЛЮКОНЕОГЕНЕЗ)
 Некоторые ткани, например мозг, нуждаются в постоянном поступлении глюкозы. Когда поступление углеводов в составе пищи недостаточно, содержание глюкозы в крови некоторое время поддерживается в пределах нормы за счёт расщепления гликогена в печени. Однако запасы гликогена в печени невелики. Они значительно уменьшаются к 6 -10 ч голодания и практически полностью исчерпываются после суточного голодания. В этом случае в печени начинается синтез глюкозы de novo - глюконеогенез.
Некоторые ткани, например мозг, нуждаются в постоянном поступлении глюкозы. Когда поступление углеводов в составе пищи недостаточно, содержание глюкозы в крови некоторое время поддерживается в пределах нормы за счёт расщепления гликогена в печени. Однако запасы гликогена в печени невелики. Они значительно уменьшаются к 6 -10 ч голодания и практически полностью исчерпываются после суточного голодания. В этом случае в печени начинается синтез глюкозы de novo - глюконеогенез.
 Глюконеогенез - процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Процесс протекает в основном в печени (90% глюкозы) и менее интенсивно в корковом веществе почек, а также в слизистой оболочке кишечника (10% глюкозы). Эти ткани могут обеспечивать синтез 80 -100 г глюкозы в сутки. На долю мозга при голодании приходится большая часть потребности организма в глюкозе. Это объясняется тем, что клетки мозга не способны, в отличие от других тканей, обеспечивать потребности в энергии за счёт окисления жирных кислот.
Глюконеогенез - процесс синтеза глюкозы из веществ неуглеводной природы. Его основной функцией является поддержание уровня глюкозы в крови в период длительного голодания и интенсивных физических нагрузок. Процесс протекает в основном в печени (90% глюкозы) и менее интенсивно в корковом веществе почек, а также в слизистой оболочке кишечника (10% глюкозы). Эти ткани могут обеспечивать синтез 80 -100 г глюкозы в сутки. На долю мозга при голодании приходится большая часть потребности организма в глюкозе. Это объясняется тем, что клетки мозга не способны, в отличие от других тканей, обеспечивать потребности в энергии за счёт окисления жирных кислот.
 В глюконеогенезе обратимые реакции катализируют те же ферменты, что и обратимые реакции гликолиза, но в обратном направлении. Однако 3 реакции гликолиза являются необратимыми, поэтому в глюконеогенезе образование фосфоенолпирувата из пирувата, фруктозо-6 -фосфата из фруктозо-1, 6 бифосфата и глюкозы из глюкозо-6 фосфата осуществляют другие ферменты. Необходимо отметить, что гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях.
В глюконеогенезе обратимые реакции катализируют те же ферменты, что и обратимые реакции гликолиза, но в обратном направлении. Однако 3 реакции гликолиза являются необратимыми, поэтому в глюконеогенезе образование фосфоенолпирувата из пирувата, фруктозо-6 -фосфата из фруктозо-1, 6 бифосфата и глюкозы из глюкозо-6 фосфата осуществляют другие ферменты. Необходимо отметить, что гликолиз протекает в цитозоле, а часть реакций глюконеогенеза происходит в митохондриях.
 Первичные субстраты глюконеогенеза - лактат, аминокислоты и глицерол. Включение этих субстратов в глюконеогенез зависит от физиологического состояния организма. Лактат - продукт анаэробного гликолиза. Он образуется при любых состояниях организма в эритроцитах и работающих мышцах. Таким образом, лактат используется в глюконеогенезе постоянно. Глицерол высвобождается при гидролизе жиров в жировой ткани в период голодания или при длительной физической нагрузке. Аминокислоты образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе.
Первичные субстраты глюконеогенеза - лактат, аминокислоты и глицерол. Включение этих субстратов в глюконеогенез зависит от физиологического состояния организма. Лактат - продукт анаэробного гликолиза. Он образуется при любых состояниях организма в эритроцитах и работающих мышцах. Таким образом, лактат используется в глюконеогенезе постоянно. Глицерол высвобождается при гидролизе жиров в жировой ткани в период голодания или при длительной физической нагрузке. Аминокислоты образуются в результате распада мышечных белков и включаются в глюконеогенез при длительном голодании или продолжительной мышечной работе.
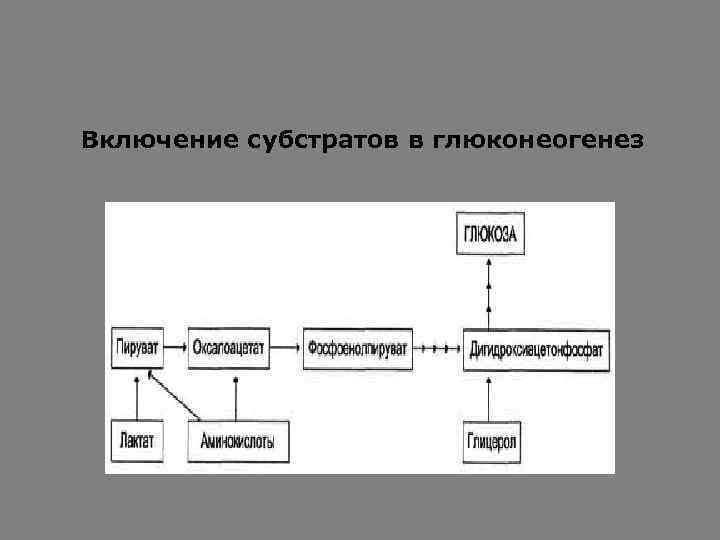 Включение субстратов в глюконеогенез
Включение субстратов в глюконеогенез
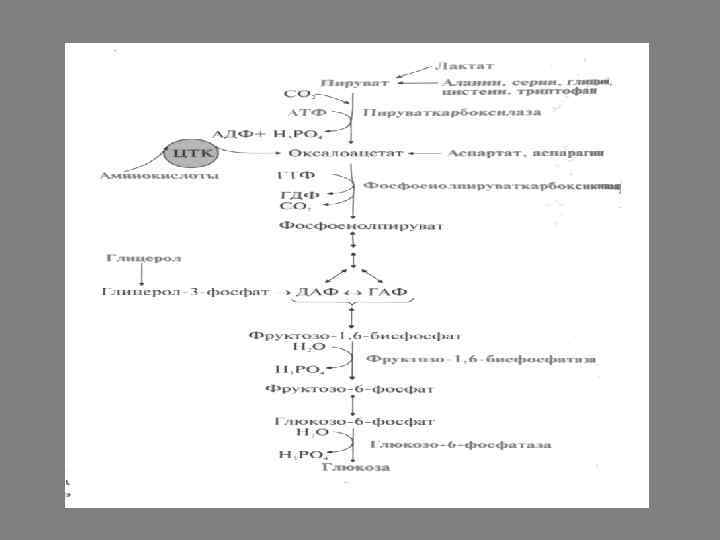
 Синтез глюкозы из лактата. Глюкозолактатный цикл или "цикл Кори". Лактат, образующийся при анаэробном гликолизе в мышцах и эритроцитах, поступает в кровь, а затем в печень. В печени лактат под действием лактатдегидрогеназы превращается в пируват, который может окисляться до СО 2 и Н 2 О или включаться в глюконеогенез. Лактат как источник пирувата важен не столько при голодании, сколько при нормальной жизнедеятельности организма.
Синтез глюкозы из лактата. Глюкозолактатный цикл или "цикл Кори". Лактат, образующийся при анаэробном гликолизе в мышцах и эритроцитах, поступает в кровь, а затем в печень. В печени лактат под действием лактатдегидрогеназы превращается в пируват, который может окисляться до СО 2 и Н 2 О или включаться в глюконеогенез. Лактат как источник пирувата важен не столько при голодании, сколько при нормальной жизнедеятельности организма.
 В печени отношение NADH/NAD+ ниже, чем в сокращающейся мышце, поэтому лактатдегидрогеназная реакция протекает в обратном направлении, т. е. в сторону образования пирувата из лактата. Далее пируват включается в глюконеогенез, а образовавшаяся глюкоза поступает в кровь и поглощается скелетными мышцами. Эту последовательность событий называют "глюкозолактатным циклом", или "циклом Кори".
В печени отношение NADH/NAD+ ниже, чем в сокращающейся мышце, поэтому лактатдегидрогеназная реакция протекает в обратном направлении, т. е. в сторону образования пирувата из лактата. Далее пируват включается в глюконеогенез, а образовавшаяся глюкоза поступает в кровь и поглощается скелетными мышцами. Эту последовательность событий называют "глюкозолактатным циклом", или "циклом Кори".
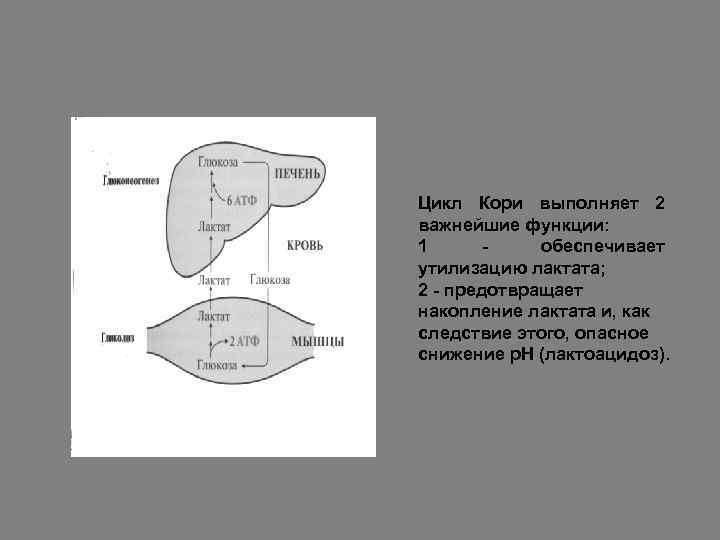 Цикл Кори выполняет 2 важнейшие функции: 1 обеспечивает утилизацию лактата; 2 - предотвращает накопление лактата и, как следствие этого, опасное снижение р. Н (лактоацидоз).
Цикл Кори выполняет 2 важнейшие функции: 1 обеспечивает утилизацию лактата; 2 - предотвращает накопление лактата и, как следствие этого, опасное снижение р. Н (лактоацидоз).
 Лактоацидоз Термин "ацидоз" обозначает увеличение кислотности среды организма (снижение р. Н) до значений, выходящих за пределы нормы. При ацидозе либо увеличивается продукция протонов, либо и то и другое). Метаболический ацидоз возникает при увеличении концентрации промежуточных продуктов обмена (кислотного характера) вследствие увеличения их синтеза или уменьшения скорости распада или выведения. При нарушении кислотно-основного состояния организма быстро включаются буферные системы компенсации (через 10 -15 мин). Лёгочная компенсация обеспечивает стабилизацию соотношения НСО 3 -/Н 2 СО 3, которая в норме соответствует 1: 20, а при ацидозе уменьшается. Лёгочная компенсация достигается увеличением объёма вентиляции и, следовательно, ускорением выведения СО 2 из организма.
Лактоацидоз Термин "ацидоз" обозначает увеличение кислотности среды организма (снижение р. Н) до значений, выходящих за пределы нормы. При ацидозе либо увеличивается продукция протонов, либо и то и другое). Метаболический ацидоз возникает при увеличении концентрации промежуточных продуктов обмена (кислотного характера) вследствие увеличения их синтеза или уменьшения скорости распада или выведения. При нарушении кислотно-основного состояния организма быстро включаются буферные системы компенсации (через 10 -15 мин). Лёгочная компенсация обеспечивает стабилизацию соотношения НСО 3 -/Н 2 СО 3, которая в норме соответствует 1: 20, а при ацидозе уменьшается. Лёгочная компенсация достигается увеличением объёма вентиляции и, следовательно, ускорением выведения СО 2 из организма.
 Одной из причин метаболического ацидоза может быть накопление молочной кислоты. В норме лактат в печени превращается обратно в глюкозу путём глюконеогенеза либо окисляется. Кроме печени, другим потребителем лактата служат почки и сердечная мышца, где лактат может окисляться до СО 2 и Н 2 О и использоваться как источник энергии, особенно при физической работе. Уровень лактата в крови - результат равновесия между процессами его образования и утилизации. Кратковременный компенсированный лактоацидоз встречается довольно часто даже у здоровых людей при интенсивной мышечной работе. У нетренированных людей лактоацидоз при физической работе возникает как следствие относительного недостатка кислорода в мышцах и развивается достаточно быстро. Компенсация осуществляется путём гипервентиляции.
Одной из причин метаболического ацидоза может быть накопление молочной кислоты. В норме лактат в печени превращается обратно в глюкозу путём глюконеогенеза либо окисляется. Кроме печени, другим потребителем лактата служат почки и сердечная мышца, где лактат может окисляться до СО 2 и Н 2 О и использоваться как источник энергии, особенно при физической работе. Уровень лактата в крови - результат равновесия между процессами его образования и утилизации. Кратковременный компенсированный лактоацидоз встречается довольно часто даже у здоровых людей при интенсивной мышечной работе. У нетренированных людей лактоацидоз при физической работе возникает как следствие относительного недостатка кислорода в мышцах и развивается достаточно быстро. Компенсация осуществляется путём гипервентиляции.
 При некомпенсированном лактоацидозе содержание лактата в крови увеличивается до 5 ммоль/л (в норме до 2 ммоль/л). При этом р. Н крови может составлять 7, 25 и менее (в норме 7, 36 -7, 44). Повышение содержания лактата в крови может быть следствием нарушения метаболизма пирувата. Нарушения метаболизма пирувата при лактоацидозе 1 - нарушение использования пирувата в глюконеогенезе; 2 - нарушение окисления пирувата.
При некомпенсированном лактоацидозе содержание лактата в крови увеличивается до 5 ммоль/л (в норме до 2 ммоль/л). При этом р. Н крови может составлять 7, 25 и менее (в норме 7, 36 -7, 44). Повышение содержания лактата в крови может быть следствием нарушения метаболизма пирувата. Нарушения метаболизма пирувата при лактоацидозе 1 - нарушение использования пирувата в глюконеогенезе; 2 - нарушение окисления пирувата.
 Так, при гипоксии, возникающей вследствие нарушения снабжения тканей кислородом или кровью, уменьшается активность пируватдегидрогеназного комплекса и снижается окислительное декарбоксилирование пирувата. В этих условиях равновесие реакции пируват ↔ лактат сдвинуто в сторону образования лактата. Кроме того, при гипоксии уменьшается синтез АТФ, что следовательно, ведёт к снижению скорости глюконеогенеза другого пути утилизации лактата. Повышение концентрации лактата и снижение внутриклеточного р. Н отрицательно влияют на активность всех ферментов, в том числе и пируваткарбоксилазы, катализирующей начальную реакцию глюконеогенеза.
Так, при гипоксии, возникающей вследствие нарушения снабжения тканей кислородом или кровью, уменьшается активность пируватдегидрогеназного комплекса и снижается окислительное декарбоксилирование пирувата. В этих условиях равновесие реакции пируват ↔ лактат сдвинуто в сторону образования лактата. Кроме того, при гипоксии уменьшается синтез АТФ, что следовательно, ведёт к снижению скорости глюконеогенеза другого пути утилизации лактата. Повышение концентрации лактата и снижение внутриклеточного р. Н отрицательно влияют на активность всех ферментов, в том числе и пируваткарбоксилазы, катализирующей начальную реакцию глюконеогенеза.
 Возникновению лактоацидоза также способствуют нарушения глюконеогенеза при печёночной недостаточности различного происхождения. Кроме того, лактоацидозом может сопровождаться гиповитаминоз В 1, так как производное этого витамина (тиаминдифосфат) выполняет коферментную функцию в составе ПДК при окислительном декарбоксилировании пирувата. Дефицит тиамина может возникать, например, алкоголиков с нарушенным режимом питания. у
Возникновению лактоацидоза также способствуют нарушения глюконеогенеза при печёночной недостаточности различного происхождения. Кроме того, лактоацидозом может сопровождаться гиповитаминоз В 1, так как производное этого витамина (тиаминдифосфат) выполняет коферментную функцию в составе ПДК при окислительном декарбоксилировании пирувата. Дефицит тиамина может возникать, например, алкоголиков с нарушенным режимом питания. у
 Итак, причинами накопления молочной кислоты и развития лактоацидоза могут быть: • активация анаэробного гликолиза вследствие тканевой гипоксии различного происхождения; • поражения печени (токсические дистрофии, цирроз и др. ); нарушение использования лактата вследствие наследственных дефектов ферментов глюконеогенеза, недостаточности глюкозо-6 -фосфатазы; • нарушение работы ПДК вследствие дефектов ферментов или гиповитаминозов; • применение ряда лекарственных препаратов, например бигуанидов (блокаторы глюконеогенеза, используемые при лечении сахарного диабета).
Итак, причинами накопления молочной кислоты и развития лактоацидоза могут быть: • активация анаэробного гликолиза вследствие тканевой гипоксии различного происхождения; • поражения печени (токсические дистрофии, цирроз и др. ); нарушение использования лактата вследствие наследственных дефектов ферментов глюконеогенеза, недостаточности глюкозо-6 -фосфатазы; • нарушение работы ПДК вследствие дефектов ферментов или гиповитаминозов; • применение ряда лекарственных препаратов, например бигуанидов (блокаторы глюконеогенеза, используемые при лечении сахарного диабета).
 Синтез глюкозы из аминокислот В условиях голодания часть белков мышечной ткани распадается до аминокислот, которые далее включаются в процесс катаболизма. Аминокислоты, которые при катаболизме превращаются в пируват или метаболиты цитратного цикла, могут рассматриваться как потенциальные предшественники глюкозы и гликогена и носят название гликогенных. Например, оксалоацетат, образующийся из аспарагиновой кислоты, является промежуточным продуктом как цитратногр цикла, так и глюконеогенеза.
Синтез глюкозы из аминокислот В условиях голодания часть белков мышечной ткани распадается до аминокислот, которые далее включаются в процесс катаболизма. Аминокислоты, которые при катаболизме превращаются в пируват или метаболиты цитратного цикла, могут рассматриваться как потенциальные предшественники глюкозы и гликогена и носят название гликогенных. Например, оксалоацетат, образующийся из аспарагиновой кислоты, является промежуточным продуктом как цитратногр цикла, так и глюконеогенеза.
 Синтез глюкозы из аминокислот Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюкозонеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах → пируват в мышцах → аланин в печени → глюкоза в мышцах.
Синтез глюкозы из аминокислот Из всех аминокислот, поступающих в печень, примерно 30% приходится на долю аланина. Это объясняется тем, что при расщеплении мышечных белков образуются аминокислоты, многие из которых превращаются сразу в пируват или сначала в оксалоацетат, а затем в пируват. Последний превращается в аланин, приобретая аминогруппу от других аминокислот. Аланин из мышц переносится кровью в печень, где снова преобразуется в пируват, который частично окисляется и частично включается в глюкозонеогенез. Следовательно, существует следующая последовательность событий (глюкозо-аланиновый цикл): глюкоза в мышцах → пируват в мышцах → аланин в печени → глюкоза в мышцах.
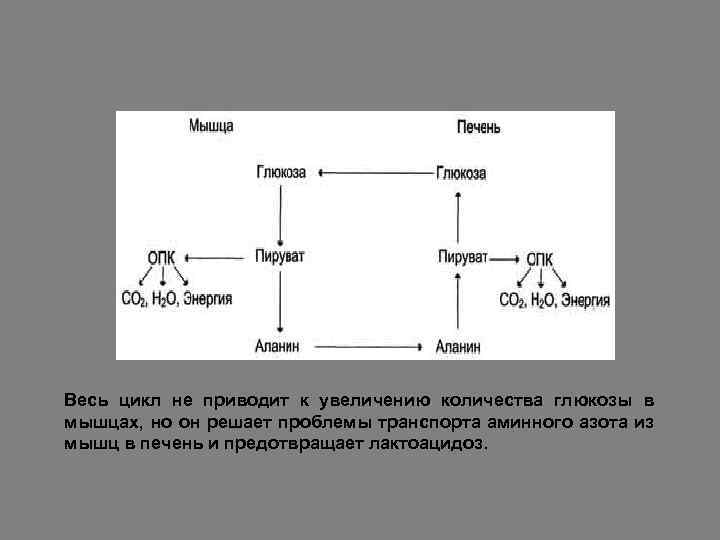 Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень и предотвращает лактоацидоз.
Весь цикл не приводит к увеличению количества глюкозы в мышцах, но он решает проблемы транспорта аминного азота из мышц в печень и предотвращает лактоацидоз.
 Синтез глюкозы из глицерола Глицерол образуется при гидролизе триацилглицеролов, главным образом в жировой ткани. Использовать его могут только те ткани, в которых имеется фермент глицеролкиназа, например печень, почки. Этот АТФ-зависимый фермент катализирует превращение глицерола в глицерол-3 -фосфат. При включении глицерол-3 -фосфата в глюконеогенез происходит его дегидрирование NAD-зависимой дегидрогеназой с образованием дигидроксиацетонфосфата, который далее превращается в глюкозу.
Синтез глюкозы из глицерола Глицерол образуется при гидролизе триацилглицеролов, главным образом в жировой ткани. Использовать его могут только те ткани, в которых имеется фермент глицеролкиназа, например печень, почки. Этот АТФ-зависимый фермент катализирует превращение глицерола в глицерол-3 -фосфат. При включении глицерол-3 -фосфата в глюконеогенез происходит его дегидрирование NAD-зависимой дегидрогеназой с образованием дигидроксиацетонфосфата, который далее превращается в глюкозу.


 Биосинтез глюкозы (реакции глюконеогенеза) В реакции глюконеогенеза может вступать пируват, образующийся при катаболизме аминокислот или в результате окисления лактата. Синтез глюкозы из 2 молекул пирувата включает 4 необратимые реакции и требует затрат энергии.
Биосинтез глюкозы (реакции глюконеогенеза) В реакции глюконеогенеза может вступать пируват, образующийся при катаболизме аминокислот или в результате окисления лактата. Синтез глюкозы из 2 молекул пирувата включает 4 необратимые реакции и требует затрат энергии.
 Образование фосфоенолпирувата из пирувата происходит в ходе двух реакций, первая из которых протекает в митохондриях. Пируват, образующийся из лактата или из некоторых аминокислот, транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалоацетата. Образование оксалоацетата из пирувата. Пируваткарбоксилаза, катализирующая данную реакцию, - митохондриальный фермент, коферментом которого является биотин. Реакция протекает с использованием 1 молекулы АТФ.
Образование фосфоенолпирувата из пирувата происходит в ходе двух реакций, первая из которых протекает в митохондриях. Пируват, образующийся из лактата или из некоторых аминокислот, транспортируется в матрикс митохондрий и там карбоксилируется с образованием оксалоацетата. Образование оксалоацетата из пирувата. Пируваткарбоксилаза, катализирующая данную реакцию, - митохондриальный фермент, коферментом которого является биотин. Реакция протекает с использованием 1 молекулы АТФ.
 Дальнейшие превращения оксалоацетата протекают в цитозоле. Следовательно, на этом этапе должна существовать система транспорта оксалоацетата через митохондриальную мембрану, которая для него непроницаема. Оксалоацетат в митохондриальном матриксе восстанавливается с образованием малата при участии NADH (обратная реакция цитратного цикла). Превращение оксалоацетата в малат
Дальнейшие превращения оксалоацетата протекают в цитозоле. Следовательно, на этом этапе должна существовать система транспорта оксалоацетата через митохондриальную мембрану, которая для него непроницаема. Оксалоацетат в митохондриальном матриксе восстанавливается с образованием малата при участии NADH (обратная реакция цитратного цикла). Превращение оксалоацетата в малат
 Образовавшийся малат затем проходит через митохондриальную мембрану с помощью специальных переносчиков. Кроме того, оксалоацетат способен транспортироваться из митохондрий в цитозоль в виде аспартата в ходе малат-аспартатного челночного механизма. В цитозоле малат вновь превращается в оксалоацетат в ходе реакции окисления с участием кофермента NAD+. Обе реакции: восстановление оксалоацетата и окисление малага катализируют малатдегидрогеназа, но в первом случае это митохондриальный фермент, а во втором - цитозольный. Образованный в цитозоле из малата оксалоацетат затем превращается в фосфоенолпируват в ходе реакции, катализируемой фосфоенолпируваткарбоксикиназой ГТФ-зависимым ферментом. Превращение оксалоацетата в фосфоенолпируват осуществляется с затратой 1 молекулы ГТФ.
Образовавшийся малат затем проходит через митохондриальную мембрану с помощью специальных переносчиков. Кроме того, оксалоацетат способен транспортироваться из митохондрий в цитозоль в виде аспартата в ходе малат-аспартатного челночного механизма. В цитозоле малат вновь превращается в оксалоацетат в ходе реакции окисления с участием кофермента NAD+. Обе реакции: восстановление оксалоацетата и окисление малага катализируют малатдегидрогеназа, но в первом случае это митохондриальный фермент, а во втором - цитозольный. Образованный в цитозоле из малата оксалоацетат затем превращается в фосфоенолпируват в ходе реакции, катализируемой фосфоенолпируваткарбоксикиназой ГТФ-зависимым ферментом. Превращение оксалоацетата в фосфоенолпируват осуществляется с затратой 1 молекулы ГТФ.
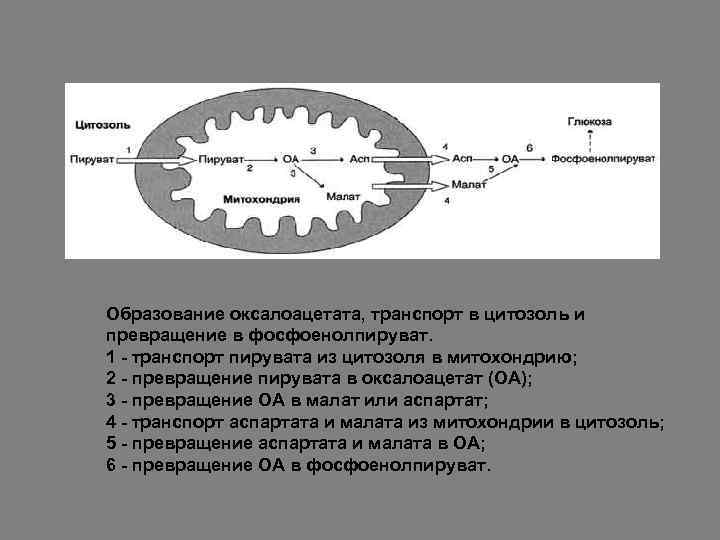 Образование оксалоацетата, транспорт в цитозоль и превращение в фосфоенолпируват. 1 - транспорт пирувата из цитозоля в митохондрию; 2 - превращение пирувата в оксалоацетат (ОА); 3 - превращение ОА в малат или аспартат; 4 - транспорт аспартата и малата из митохондрии в цитозоль; 5 - превращение аспартата и малата в ОА; 6 - превращение ОА в фосфоенолпируват.
Образование оксалоацетата, транспорт в цитозоль и превращение в фосфоенолпируват. 1 - транспорт пирувата из цитозоля в митохондрию; 2 - превращение пирувата в оксалоацетат (ОА); 3 - превращение ОА в малат или аспартат; 4 - транспорт аспартата и малата из митохондрии в цитозоль; 5 - превращение аспартата и малата в ОА; 6 - превращение ОА в фосфоенолпируват.
 Следует отметить, что этот обходной участок глюконеогенеза требует расхода двух молекул с макроэргическими связями (АТФ и ГТФ) в расчёте на одну молекулу исходного вещества - пирувата. В пересчёте на синтез одной молекулы глюкозы из двух молекул пирувата расход составляет 2 моль АТФ и 2 моль ГТФ или 4 моль АТФ
Следует отметить, что этот обходной участок глюконеогенеза требует расхода двух молекул с макроэргическими связями (АТФ и ГТФ) в расчёте на одну молекулу исходного вещества - пирувата. В пересчёте на синтез одной молекулы глюкозы из двух молекул пирувата расход составляет 2 моль АТФ и 2 моль ГТФ или 4 моль АТФ
 Фосфоенолпируват в ходе двух последовательных обратимых реакций, которые фосфоглицеромутаза, катализируют превращается енолаза и в фосфоглицерат. 3 -фосфоглицераткиназой бифосфоглицерата, 3 - фосфорилируется с образованием 1, 3 - при этом донором фосфата является АТФ. В результате 3 обратимых реакций, которые последовательно катализируют глицеральдегид 3 фосфатдегидрогеназа, триозофосфатизомераза и альдолаза, 2 молекулы 1, 3 -бифосфоглицерата превращаются в фруктозо-1, 6 -бисфосфат. Дефосфосфорилирование фруктозо-1, 6 -бисфосфата и глюкозо-6 -фосфата также необратимые реакции глюконеогенеза и их катализируют фруктозо-1, 6 бисфосфатаза и глюкозо-6 -фосфатаза. Эти ферменты относят к гидролазам и отщепляют от субстратов фосфатную группу с участием воды.
Фосфоенолпируват в ходе двух последовательных обратимых реакций, которые фосфоглицеромутаза, катализируют превращается енолаза и в фосфоглицерат. 3 -фосфоглицераткиназой бифосфоглицерата, 3 - фосфорилируется с образованием 1, 3 - при этом донором фосфата является АТФ. В результате 3 обратимых реакций, которые последовательно катализируют глицеральдегид 3 фосфатдегидрогеназа, триозофосфатизомераза и альдолаза, 2 молекулы 1, 3 -бифосфоглицерата превращаются в фруктозо-1, 6 -бисфосфат. Дефосфосфорилирование фруктозо-1, 6 -бисфосфата и глюкозо-6 -фосфата также необратимые реакции глюконеогенеза и их катализируют фруктозо-1, 6 бисфосфатаза и глюкозо-6 -фосфатаза. Эти ферменты относят к гидролазам и отщепляют от субстратов фосфатную группу с участием воды.

 Итак, в печени существуют 4 фермента, которые принимают участие только в глюконеогенезе и катализируют обходные реакции необратимых стадий гликолиза. Пируваткарбоксилаза Фосфоенолпируваткарбоксикиназа фруктозо-1, 6 -бисфосфатаза Глюкозо-6 -фосфатаза.
Итак, в печени существуют 4 фермента, которые принимают участие только в глюконеогенезе и катализируют обходные реакции необратимых стадий гликолиза. Пируваткарбоксилаза Фосфоенолпируваткарбоксикиназа фруктозо-1, 6 -бисфосфатаза Глюкозо-6 -фосфатаза.
 Энергетический баланс глюконеогенеза из пирувата Три реакции глюконеогенеза идут с затратой энергии. При превращении пирувата в оксалоацетат и 3 -фосфоглицерата в 1, 3 -бифосфоглицерат расходуется по 1 молекуле АТФ. Кроме того, 1 молекула ГТФ необходима для образования фосфоенолпирувата из оксалоацетата. Учитывая, что стехиометрический коэффициент этого этапа глюконеогенеза равен 2, для синтеза 1 молекулы глюкозы из 2 молекул пирувата необходимо 4 АТФ и 2 ГТФ ( всего 6 АТФ). Суммарный результат глюконеогенеза из пирувата выражается следующим уравнением: 2 Пируват + 4 АТФ + 2 ГТФ + 2 (NADH + Н+)+ 4 Н 20 → Глюкоза + 4 АДФ + 2 ГДФ + 6 H 3 PO 4 + 2 NAD+
Энергетический баланс глюконеогенеза из пирувата Три реакции глюконеогенеза идут с затратой энергии. При превращении пирувата в оксалоацетат и 3 -фосфоглицерата в 1, 3 -бифосфоглицерат расходуется по 1 молекуле АТФ. Кроме того, 1 молекула ГТФ необходима для образования фосфоенолпирувата из оксалоацетата. Учитывая, что стехиометрический коэффициент этого этапа глюконеогенеза равен 2, для синтеза 1 молекулы глюкозы из 2 молекул пирувата необходимо 4 АТФ и 2 ГТФ ( всего 6 АТФ). Суммарный результат глюконеогенеза из пирувата выражается следующим уравнением: 2 Пируват + 4 АТФ + 2 ГТФ + 2 (NADH + Н+)+ 4 Н 20 → Глюкоза + 4 АДФ + 2 ГДФ + 6 H 3 PO 4 + 2 NAD+


