с.диабет.ppt
- Количество слайдов: 64

Сахарный диабет (лат. diabetes mellītus - "проходить сквозь…") – хроническое эндокринное заболевание, обусловленное абсолютной (дефицит) или относительной (нарушение взаимодействия с клетками-мишенями) недостаточностью инсулина. Характеризуется: • гипергликемией (стойкое ↑ содержания глюкозы в крови), • тяжелым нарушением всех видов обмена веществ (углеводного, жирового, белкового, минерального и водно-солевого) и • расстройством функции органов и систем (особенно НС, ССС, почек и органов зрения).
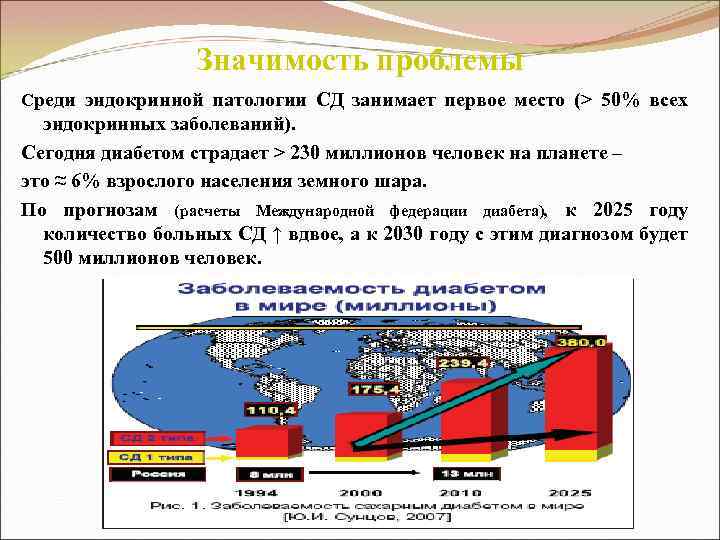
Значимость проблемы Среди эндокринной патологии СД занимает первое место (> 50% всех эндокринных заболеваний). Сегодня диабетом страдает > 230 миллионов человек на планете – это ≈ 6% взрослого населения земного шара. По прогнозам (расчеты Международной федерации диабета), к 2025 году количество больных СД ↑ вдвое, а к 2030 году с этим диагнозом будет 500 миллионов человек.

Значимость проблемы (продолжение) Каждые 10 секунд в мире: - становится на 2 больных больше - ≈ 7 миллионов в год, - 1 человек умирает - 4 миллиона в год (по причине диабета и его осложнений). В России - > 3, 3 миллиона человек с СД (около 300 тысяч – СД 1, около 3 миллионов – СД 2. В 2011 году было 25764 ребенка и подростка с СД 1 и 562 – с СД 2). Среди причин смерти СД занимает четвертое место. У больных СД: - смертность от болезней сердца и инсульта выше в 2 -3 раза (ежегодно умирает 3, 8 миллиона человек), - слепота - в 10 раз, - нефропатия - в 12 -15 раз, - гангрена нижних конечностей - почти в 20 раз, чем среди населения в целом. СД в связи с большой распространенностью и ↑ заболеваемости относят к социальным болезням.

Классификация СД по тяжести течения I. Лёгкое течение: - невысокий уровень гликемии (не > 8 ммоль/л натощак), - незначительная суточная глюкозурия (до 20 г/л). Состояние компенсации поддерживается с помощью диетотерапии. II. Средней степени тяжести: - гликемия натощак ↑ до 14 ммоль/л, - суточная глюкозурия не > 40 г/л, - эпизодически развивается кетоз или кетоацидоз. Компенсация - диета и приём сахароснижающих пероральных средств или введение инсулина. III. Тяжёлое течение - высокие уровни гликемии (натощак > 14 ммоль/л), - высокий уровень глюкозурии (> 40 -50 г/л). Необходима постоянная инсулинотерапия (в дозе 60 ОД и >).
Классификация СД по степени компенсации 1. Компенсированная форма: - нормальные показатели глюкозы в крови и - ее полное отсутствие в моче - достигаются лечением. 2. Субкомпенсированная: - уровень глюкозы в крови не > 13, 9 ммоль/л, - суточная потеря глюкозы с мочой - не > 50 г, - ацетон в моче отсутствует. 3. Декомпенсированная: - уровень глюкозы > 13, 9 ммоль/л, - глюкозурия > 50 г, - в моче - ацетон, - возможна гипергликемическая кома.

Классификация СД (этиопатогенетическая) I. СД 1 -го типа. II. СД 2 -го типа. III. Другие специфические формы СД. IV. Гестационный СД.

СД 1 -го типа Заболевание, которое развивается вследствие прогрессирующего разрушения β-клеток островков Лангерганса поджелудочной железы, сопровождающееся дефицитом синтеза инсулина. Абсолютный дефицит инсулина возникает, когда погибает 80 -95% β-клеток.

Этиология СД 1 Основной этиологический фактор – изменение АГ состава β-клеток островкового аппарата поджелудочной железы, возникающее в результате: 1) генетических причин (дефект генов системы HLA; у представителей негроидной расы риск заболеть СД 1 типа в 4 -5 раз выше, чем у людей европеоидной расы), 2) вирусных атак (тропными к клеткам pancreas вирусами), 3) известны токсические вещества, избирательно поражающие β-клетки и индуцирующие аутоиммунную реакцию.

Этиология СД 1 (продолжение) Генетическая предрасположенность обусловлена несколькими генами, в том числе дефектом генов системы HLA (главный комплекс тканевой (гисто-) совместимости, находится на коротком плече 6 -й хромосомы) – наличие диабетогенных аллелей (известно > 10). • В локусе D – это: - АГ - DR 3, DR 4, DQ, или - генотип DR 3/DR 4 (Локусы DW 3/DRW 3 - ↑ риск по СД 1 в 3, 7 раза, DW 4/DRW 4 - в 4, 9 раза, a DW 3/DRW 4 - в 9, 4 раза), • в локусе В - В 8, В 15.

Этиология СД 1 (продолжение) Аллели генов HLA могут обусловливать: • предрасположенность: - аллели HLA-DR 3, -DR 4 либо -DR 3/DR 4 имеют > 95% больных; - HLA В 8 -АГ и HLA В 15 -АГ ↑ риск по СД 1 ≈ в 2 -3 раза, а сочетание этих АГ - в 10 раз, или • резистентность к СД 1: - аллели HLA-DR 2 и -DR 5 - редко выявляются при СД 1; - АГ В 7 ↓ риск по СД 1 в 14, 5 раза, у лиц с HLA B 2 риск также меньше.

Этиология СД 1 (продолжение) Наличие наследственной предрасположенности свидетельствует о большей вероятности развития СД 1, чем у тех, кто не имеет таковую. Разрешающий фактор - вирусная инфекция (индуцирует аутоиммунную реакцию против β-клеток у лиц с генетической предрасположенностью). Роль вирусной инфекции подтверждается: - сезонностью (чаще заболевают зимой и ранней весной, когда больше вирусных инфекций (британские ученые выяснили, что среди европейцев, больных диабетом, подавляющее большинство людей, который родились в весенние месяцы), - связью с перенесенной инфекцией, - повышением титра противовирусных АТ в крови больных, - обнаружением вирусного АГ в островках, - выделением вируса (например, Коксаки В) из поджелудочной железы умерших, - у умерших от СД 1 типа в начале его развития, находят характерные гистологические изменения в островках (инфильтрация их лимфоцитами, дегенерация β-клеток) - «инсулит» при вирусных и аутоиммунных процессах, - воспроизведением вирусной модели СД у экспериментальных животных.

Этиология СД 1 (продолжение) Особое значение имеют β-цитотропные вирусы: • краснухи (имеет тропизм к островкам pancreas, накапливается и может реплицироваться в них. Частота СД при врожденной краснухе достигает 20% и >. В крови обнаруживают высокий титр АТ к АГ вируса краснухи), • Коксаки В 4 (выделен диабетогенный штамм; инокуляция вируса Коксаки B 4, выделенного из островков поджелудочной железы ребенка, умершего от внезапного диабетического кетоацидоза, вызвала у мышей гипергликемию, воспаление и некроз островков поджелудочной железы, а также ↑ титра нейтрализующих АТ к этому вирусу), • эпидемического паротита, • ветряной оспы, • инфекционного мононуклеоза, • инфекционного гепатита (вирус гепатита В может реплицироваться в инсулярном аппарате), • цитомегаловирус.
Патогенез СД 1 Главное звено патогенеза - разрушение β-клеток. Имеет аутоиммунную природу. Участвуют Гуморальное звено Клеточное звено имм-та (АТ) (цитотоксические л. , макрофаги)
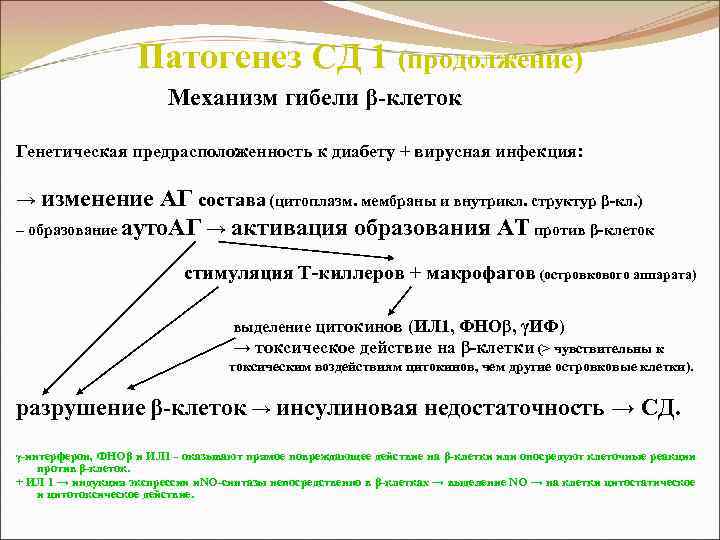
Патогенез СД 1 (продолжение) Механизм гибели β-клеток Генетическая предрасположенность к диабету + вирусная инфекция: → изменение АГ состава (цитоплазм. мембраны и внутрикл. структур β-кл. ) – образование ауто. АГ → активация образования АТ против β-клеток стимуляция Т-киллеров + макрофагов (островкового аппарата) выделение цитокинов (ИЛ 1, ФНОβ, γИФ) → токсическое действие на β-клетки (> чувствительны к токсическим воздействиям цитокинов, чем другие островковые клетки). разрушение β-клеток → инсулиновая недостаточность → СД. γ-интерферон, ФНОβ и ИЛ 1 - оказывают прямое повреждающее действие на β-клетки или опосредуют клеточные реакции против β-клеток. + ИЛ 1 → индукция экспрессии и. NO-синтазы непосредственно в β-клетках → выделение NO → на клетки цитостатическое и цитотоксическое действие.
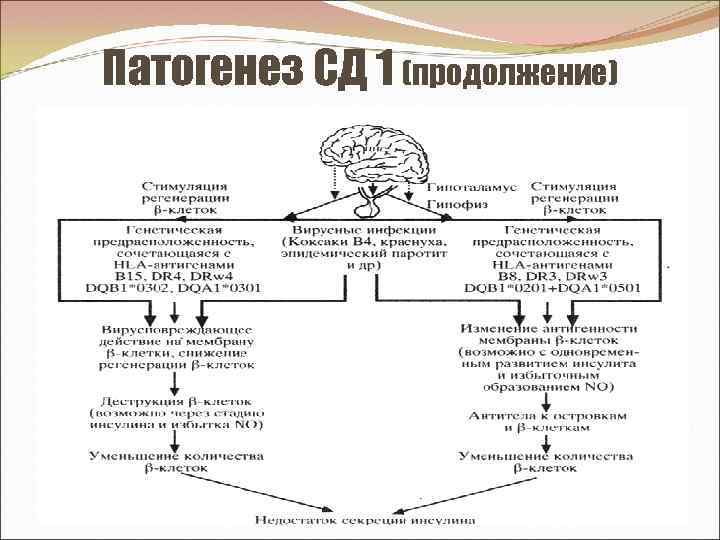
Патогенез СД 1 (продолжение)
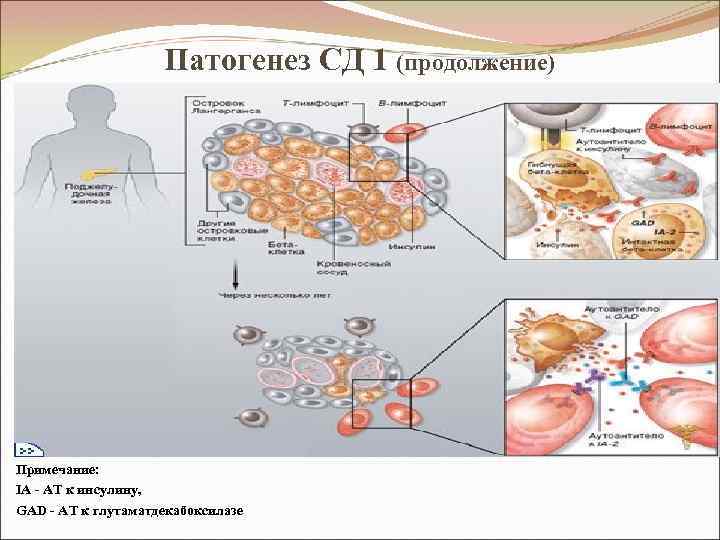
Патогенез СД 1 (продолжение) Примечание: IA - АТ к инсулину, GAD - АТ к глутаматдекабоксилазе

Характеристика СД 1 типа 1. Начало болезни – в молодом, или – чаще – в детском возрасте. 2. Начало острое, внезапное, часто – с осложнения (кетоацидоза или комы). 3. Течение тяжелое, часто осложняется кетозом. 4. Масса тела у большинства больных снижена. 5. Имеется тесная связь с системой HLA, в крови обнаруживаются АТ к островкам. 6. В крови резко снижен уровень инсулина.

Роль инсулина в организме исключительна. Основное действие инсулина: ● на углеводный обмен: - активирует гликогенсинтетазу (способствует синтезу гликогена), - активирует гексокиназу, - тормозит глюконеогенез, - способствует транспорту глюкозы через мембрану клеток; ● на жировой обмен: - угнетает липолиз в жировых депо, - активирует переход углеводов в жир, - тормозит образование кетоновых тел, - стимулирует расщепление кетоновых тел в печени, - в жировых клетках под действием инсулина синтезируется ДНК; ● на белковый обмен: - усиливает транспорт аминокислот в клетку, - обеспечивает энергией синтез белка, усиливая его, - тормозит окисление аминокислот, - тормозит распад белка; ● на водно-солевой обмен: - усиливает поглощение печенью и мышцами калия, - обеспечивает реабсорбцию натрия в канальцах почек, - способствует задержке воды в организме.

Лечение СД 1 типа I. Консервативная терапия. 1. Пожизненная заместительная инсулинотерапия - подбор базового уровня продлённых инсулинов и купирование подъёмов глюкозы крови после приема пищи с помощью инсулинов короткого и ультракороткого действия. 2. Методы лечения, направленные на замедление процесса разрушения β-клеток (что может отсрочить начало болезни или даже предотвратить ее развитие) – например, препараты, подавляющие выработку АТ к β-клеткам (так называемая иммуносупрессивная терапия). II. Хирургическая терапия 1. Трансплантация: - целой поджелудочной железы (обычно производится сочетанная пересадка почки и поджелудочной железы, поэтому операции проводятся у пациентов с диабетической нефропатией. В случае успеха обеспечивает полное излечение от СД), - клеток островкового аппарата (новейшее направление в кардинальном лечении СД I типа. Пересадка островков Лангерганса осуществляется от трупного донора и также, как и в случае с трансплантацией поджелудочной железы, требует тщательного подбора донора и мощной иммуносупрессии).

Этиология СД 2 типа СД 2 – самая частая форма СД - ≈ 90% всех случаев. СД 2 - заболевание с наследственной предрасположенностью. Доказательства генетической природы СД 2 -го типа: • семейное «накопление» заболевания - риск у прямых родственников больного - 40% (если болен отец, риск у детей - 50%, если мать - 35%) (при СД 1 не превышает 10%); • ≈ 90% конкордантность в заболеваемости СД 2 -го типа у монозиготных близнецов; • найдены изолированные популяции, среди которых заболеваемость СД 2 -го типа чрезвычайно высока - > 50%; • в некоторых этнических группах распространенность чрезвычайно высока, например, среди жителей острова Науру (Микронезия) она составляет 40%, а среди индейцев Пима (Аризона, США) превышает 50%; • существуют этнические группы с очень низкой распространенностью, например, деревенские жители Папуа - Новой Гвинеи им не болеют. Предполагают, что в таких популяциях отсутствуют гены предрасположенности к СД 2.

Этиология СД 2 типа (продолжение) Определенные сочетания генов обусловливают предрасположенность к болезни, а ее развитие и клиническое проявление определяются такими факторами, как ожирение, неправильный режим питания, малоподвижный образ жизни и стресс. Разрешающий фактор развития СД 2 - ожирение. Среди лиц с нормальной массой тела частота СД 2 составляет 7, 8%. При избытке массы тела на 20 -29% - 25, 6%, а на 40 -49% - 58, 8%. Особенно опасна абдоминальная форма О. с преимущественным отложением жира на животе. Считается, что инсулинорезистентность при ожирении может быть связана с продукцией жировой тканью ряда активных метаболитов, в том числе лептина, ФНОα, СЖК (могут модулировать секрецию инсулина и ↑ периферическую инсулинорезистентность. Периферическая инсулинорезистентность и ожирение входят в метаболический синдром). Ø 80% больных страдают О. , а Ø ↓ веса приводит к полному исчезновению заболевания. Каждый килограмм лишнего веса ↑ риск развития диабета на 5%: - при О. 1 ст. , риск ↑ в 2 раза, - при 3 ст. – в 10 раз.

Патогенез СД 2 типа У больных СД 2 типа нет ↓ числа β-клеток. Патология не связана с HLA системой, в основе лежат 2 других генетических дефекта. I. Инсулинорезистентность - ↓ чувствительности клеток-мишеней (мышечной, жировой и в < степени – печеночной) к действию инсулина. Отмечается дисбаланс инсулиновой секреции и чувствительности к инсулину - секреция инсулина нормальная или повышенная, но нарушается механизм взаимодействия инсулина с клетками. Выделяют два механизма ИР: 1. Рецепторная инсулинорезистентность – наследственные (мутации гена-рецептора; известно > 30 генов – их повреждение → нарушение связывания инсулина с рецептором): - ↓ количества или - изменение структуры специфических рецепторов (на поверхности клетки) для инсулина.

Патогенез СД 2 (продолжение) 2. Пострецепторная ИР - нарушение пострецепторных механизмов, опосредующих эффекты инсулина. Пострецепторные трансдукторов, дефекты включают изменения активности • участвующих в передаче инсулинового сигнала внутри клетки (нарушение внутриклеточных механизмов передачи сигнала от рецепторов органеллам клетки). Чаще всего - наследственное ↓ основного транспортера глюкозы в мышечных и жировых клетках - GLUT-4 (содержание у лиц с СД 2 снижено на 80%) и • принимающих участие также в: - синтезе белка, - митогенезе, - синтезе гликогена.
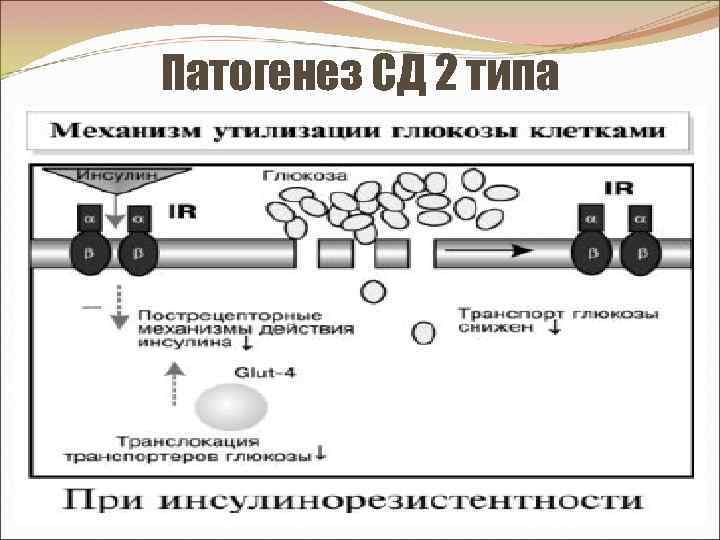
Патогенез СД 2 типа

Патогенез СД 2 (продолжение) II. Наследственное нарушение ранней секреции инсулина βклетками - ↓ первая фаза секреции на пищевую нагрузку (и фактически отсутствует вторая - медленная фаза, в процессе которой секреция инсулина характеризуется монотонностью, что обусловливает чрезмерную постпрандиальную гипергликемию, несмотря на избыточную секрецию инсулина. Развивается состояние несоответствия временной продукции инсулина с диссоциацией гликемии и инсулинемии). В норме поджелудочная железа отвечает на подъем гликемии выбросом инсулина - ранний пик. При патологии - ↓ способность β-клеток секретировать инсулин в 1 -е мин. после приема пищи. Секреторная дисфункция β-клеток заключается в замедлении «раннего» секреторного выброса инсулина в ответ на увеличение уровня глюкозы в крови. При этом 1 -я (быстрая) фаза секреции (заключается в опорожнении везикул с накопленным инсулином) фактически отсутствует; 2 -я (медленная) фаза секреции осуществляется в ответ на стабилизирующуюся гипергликемию постоянно, в тоническом режиме, и, несмотря на избыточную секрецию инсулина, уровень гликемии на фоне инсулинорезистентности не нормализуется. Количество выделяемого инсулина составляет ≈ 10% от количества инсулина, секретируемого за сутки, но значение раннего пика в регуляции очень велико: • вызывает немедленное подавление продукции глюкозы печенью, контролируя рост гликемии, • подавляет липолиз и секрецию глюкагона, • ↑ чувствительность периферических тканей к действию инсулина, способствуя утилизации глюкозы, • ограничивает прандиальную гликемию в норме. Ранний пик секреции инсулина выявляется в ходе внутривенного глюкозотолерантного теста.
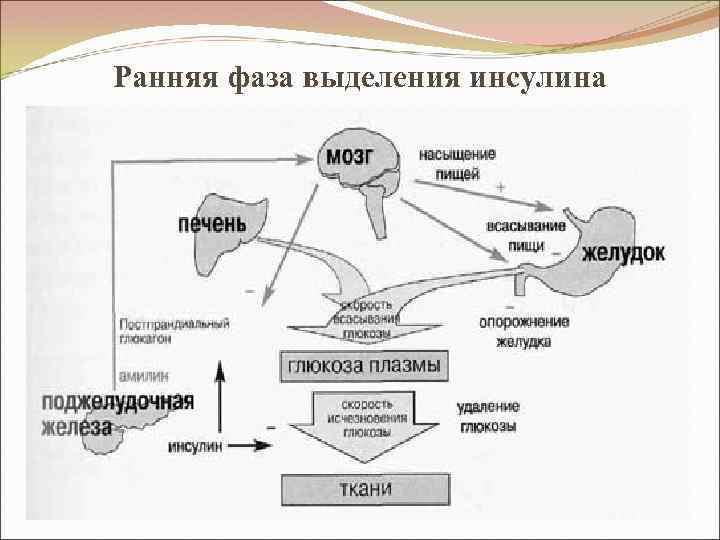
Ранняя фаза выделения инсулина

Патогенез СД 2 (продолжение) Механизмы нарушения ранней секреции 1. Генетический дефект механизма восприятия βклетками ↑ уровня глюкозы в крови. Влияние глюкозы на секрецию инсулина

Патогенез СД 2 (продолжение) Механизмы нарушения ранней секреции 2. Наследственное ↓ продукции ГПП-1 (глюкагоноподобный пептид). ГПП-1 продуцируется энтеро-эндокринными L-клетками тонкого кишечника в ответ на прием пищи. Его действие - усиление экзоцитоза секреторных гранул βклеток, содержащих инсулин. При СД II типа секреция ГПП-1 снижена на 20 -30%.

Характеристика СД 2 типа 1. Начало заболевания - в зрелом или пожилом возрасте (бывает и у детей) - старше 40 лет. 2. Постепенное начало. 3. Течение благоприятное (без кетоза), медленное (десятки лет), с поздним развитием осложнений. 4. Масса тела, в основном, повышена. 5. Нет связи с HLA системой и не выявляются АТ к островкам. 6. Уровень инсулина нормальный или ↑ (компенсаторно – для преодоления ИР).

Лечение СД 2 -го типа 1. Немедикаментозная терапия Основа – постулат: «Диабет - не болезнь, а образ жизни» : • диетотерапия - обеспечение ↓ массы тела до оптимальной для данного человека: - снижение потребления легкодоступных углеводов, - контроль количества потребляемой углеводистой пищи, - предпочтение продуктам, содержащим пищевые волокна; - растительные сахароснижающие средства, - контроль энергопотребления и энергозатрат, • дозированные физические нагрузки, • обеспечение адекватного режима труда и отдыха.

Лечение СД 2 -го типа (продолжение) 2. Медикаментозная терапия • Препараты, снижающие всасываемость глюкозы в кишечнике (угнетают кишечные ферменты, расщепляющие сложные углеводы до глюкозы) (например, акарбоза - ингибитор α-гликозидазы). • Препараты, ↑ чувствительность клеток-мишеней к действию инсулина (↓ периферическую инсулинорезистентность) ( бигуаниды – метформин; производные тиазолидиндионов – глитазоны). • Препараты, ↑ секрецию инсулина β-клетками (например, производные сульфонилмочевины (трех поколений) (толбутамид, карбутамид) и фенилаланина; прандиальные регуляторы (глиниды); агонисты рецепторов ГГП-1). Механизм сахаропонижающего действия производных сульфанилмочевины - стимуляция секреции эндогенного инсулина: они связываются с АТФ-зависимыми калиевыми каналами в мембранах βклеток, блокируют эти каналы и стимулируют секрецию инсулина. Кроме того, подавляют продукцию глюкозы и расщепление инсулина в печени и несколько повышают чувствительность тканей к инсулину.

Хирургическое лечение СД 2 типа 1. Метаболическая хирургия: - желудочное (гастрошунтирование) и - билиопанкреатическое шунтирование (пища попадает из желудка в подвздошную кишку, миную 12 -перстную). Излечение - 80 -98%. 2. Искусственная поджелудочная железа.
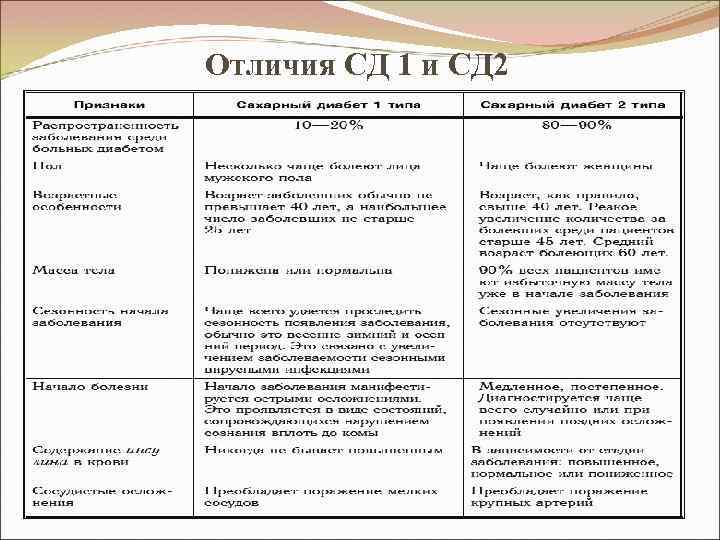
Отличия СД 1 и СД 2

Гестационный СД Возникает при беременности. Может полностью исчезнуть после родов. ГСД - нарушение толерантности к глюкозе, возникающее во время беременности и, как правило, проходящее после родов. Частота среди беременных женщин составляет 2 -5%. Механизмы возникновения схожи с СД 2 -го типа. Заболевание наносит существенный вред здоровью: • матери: - чаще встречаются осложнения беременности и родов, - у 40% женщин существует риск заболеть впоследствии (в течение 8 -10 лет) СД 2 го типа.

Гестационный СД Влияет на: • плод: - внутриутробная гибель плода (из-за кетоза или поражения сосудов плаценты и нарушений кровообращения) ≈ 1/3 беременностей спонтанно прерывается, - возникновение различных уродств и пороков развития (вследствие кетоза и токсического повреждения кетоновыми телами нервной и др. тканей), - диабетическая фетопатия - у новорожденного: * синдром ДН, из-за нарушения синтеза сурфактанта (вследствие патологии углеводного обмена у плода) - ↑ наклонность легких к ателектазам; * макросомия и висцеромегалия - ребенок рождается крупным (гипергликемия приводит к усилению у плода анаболических процессов и отложению в его тканях и органах избытка жира и гликогена) - > 5 кг → большая опасность в родах и для ребенка, и для матери).

Другие специфические формы СД 1) СД при: - органических поражениях поджелудочной железы (хронический панкреатит, панкреатэктомия (в анамнезе), панкреанекроз и др. ) или в органах, расположенных рядом с ней (холецистопанкреатит), - травмах и операции на поджелудочной железе, - атеросклерозе сосудов поджелудочной железы. Производство инсулина нарушается также при: • алиментарном дефиците: - белков и - аминокислот, - цинка (отвечает за накапливание инсулина и перенос его в кровь); • переизбытке железа (попадает в клетки поджелудочной железы, которые не справляются со своей нагрузкой и производят меньше инсулина, чем это необходимо).

Другие специфические формы СД (продолжение) 2) СД, вызванный гиперпродукцией сахароповышающих гормонов (глюкагон, КА, СТГ, АКТГ, глюкокортикоиды) – при эндокринных заболеваниях (синдром Кушинга, тиреотоксикоз, акромегалия, феохромоцитома). Примеры: • гиперпродукция СТГ (в норме СТГ ингибирует гексокиназу и глюкокиназу) → гиперфункция инсулинпродуцирующих клеток; длительная гиперфункция → истощение этих клеток и развитие инсулиновой недостаточности; • гипертиреоз → возрастает потребность тканей в глюкозе → вызывает ↑ потребности организма в инсулине → сначала гиперфункция, а затем - истощение инкреторной части pancreas. • ↑ глюкокортикоидов (например, при болезни Иценко-Кушинга) → сопровождается ↓ чувствительности тканей к инсулину → вначале ведет к усилению, а затем к резкому ↓ выработки инсулина. Соматостатинома и альдостерома, сопровождающиеся гипокалиемией, могут спровоцировать развитие СД вследствие торможения секреции инсулина. Гипергликемия обычно уменьшается после успешного лечения опухоли.

Другие специфические формы СД (продолжение) 3) СД, вызванный: • химическими веществами (многие из них нарушают секрецию или препятствуют действию инсулина; вакор (крысиный яд - N-3 -пиридил-метил-N'нитрофенилмочевина), пентамидин, многие соединения нитрозомочевины и другие нитро- или аминосодержащие вещества избирательно повреждают β-клетки) или • длительным приемом лекарственных препаратов (побочным эффектов которых является альтерация ткани pancreas): - диуретики, - стероидные и нестероидные противовоспалительные препараты, - гипотензивные препараты (например, диазоксид (его применяют также для подавления секреции инсулина при инсулиноме или незидиобластозе) в больших дозах может вызвать разрушение β-клеток), - противосудорожные препараты, - противоопухолевые препараты (например, стрептозоцин разрушает β-клетки, вызывая быстрое накопление свободных радикалов кислорода. Стрептозоцин применяют для моделирования инсулинозависимого сахарного диабета у животных).

Другие специфические формы СД (продолжение) 4) Моногенные формы инсулинонезависимого СД - мутациями генов, контролирующих секрецию инсулина. обусловлены Чаще всего – синтезируются молекулы с аминокислотными заменами (+ дефекты генов, контролирующих энергетический обмен в β-клетках и обмен глюкозы в тканях-мишенях инсулина) → количество инсулина – N, но биологическая активность ↓ до 10 -15%. При моногенных формах обычно исходно нарушена секреция инсулина, а ИР может возникнуть позже или не возникает никогда. (Например, юношеский инсулинонезависимый СД - MODY - наследуется аутосомно-доминантно, проявляется в возрасте 5 -30 лет, ≈ 15%. Характерно: нарушение стимулированной секреции инсулина, умеренная гипергликемия натощак, отсутствие кетонемии и диабетического кетоацидоза, отсутствие ИР и О. Большинство больных не нуждается в медикаментозном лечении). 5) СД, возникающие у больных с хромосомными заболеваниями (с. Дауна, Шерешевского-Тернера и др. ).
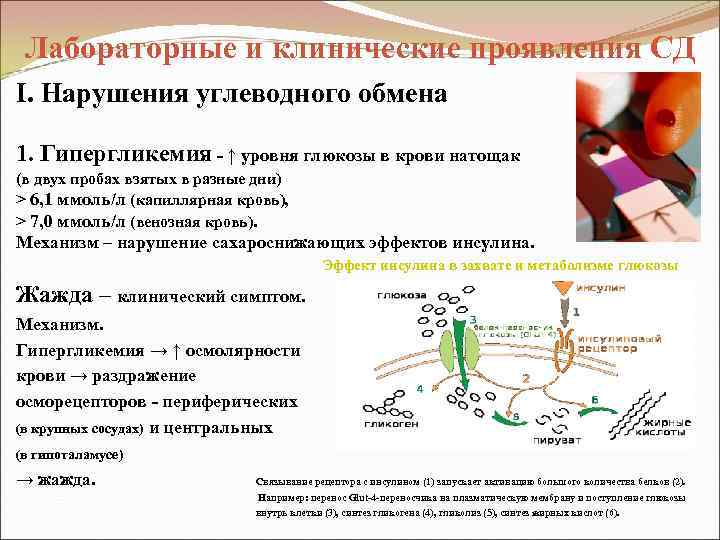
Лабораторные и клинические проявления СД I. Нарушения углеводного обмена 1. Гипергликемия - ↑ уровня глюкозы в крови натощак (в двух пробах взятых в разные дни) > 6, 1 ммоль/л (капиллярная кровь), > 7, 0 ммоль/л (венозная кровь). Механизм – нарушение сахароснижающих эффектов инсулина. Эффект инсулина в захвате и метаболизме глюкозы Жажда – клинический симптом. Механизм. Гипергликемия → ↑ осмолярности крови → раздражение осморецепторов - периферических (в крупных сосудах) и центральных (в гипоталамусе) → жажда. Связывание рецептора с инсулином (1) запускает активацию большого количества белков (2). Например: перенос Glut-4 -переносчика на плазматическую мембрану и поступление глюкозы внутрь клетки (3), синтез гликогена (4), гликолиз (5), синтез жирных кислот (6).

Лабораторные и клинические проявления СД (продолжение) 2. Глюкозурия – появление глюкозы в моче. Механизм. У здорового человека глюкоза полностью реабсорбируется в почках из первичной мочи, в которую она фильтруется из плазмы крови. Реабсорбция глюкозы – процесс активный – требует энергии и происходит с участием ферментов, активируемых инсулином. Поэтому при СД ↓ интенсивность реабсорбции глюкозы в почках → глюкозурия. Полиурия (до 8 -10 л мочи в сутки) - клинический симптом. Механизм. Нереабсорбированная из первичной мочи глюкоза создает в канальцах почек высокое осмотическое Р, которое удерживает воду в канальцах и препятствует ее переходу в интерстиций почек.

Лабораторные и клинические проявления СД (продолжение) 3. Нарушение толерантности к глюкозе – ↓ устойчивости больных к углеводной нагрузке. НТ - лабораторный синдром, свидетельствующий о наличии латентного (скрытого) диабета или о повышенном риске развития СД 2 типа. Уровень глюкозы в крови натощак слегка превышает N, глюкоза в моче отсутствует. Механизм - ↓ секреции инсулина + нарушение чувствительности клеток к инсулину. Определяется с помощью глюкозотолерантного теста (тест с сахарной нагрузкой) - позволяет определить, насколько эффективно глюкоза используется организмом. Используется, когда есть симптомы диабета, а уровень глюкозы в крови натощак N (3, 3 -5, 5 ммоль/л), или слегка превышает нормальные значения. Определение ( «золотой стандарт» ВОЗ): - измеряется уровень глюкозы натощак, - больному перорально дается 75 г (у детей 1, 75 г на кг массы тела) глюкозы (или 50 г сахарозы в 100 мл теплой воды – выпить в течение 5 минут). Диагноз СД ставится, если через 2 часа ее уровень в крови > 11, 1 ммоль/л.
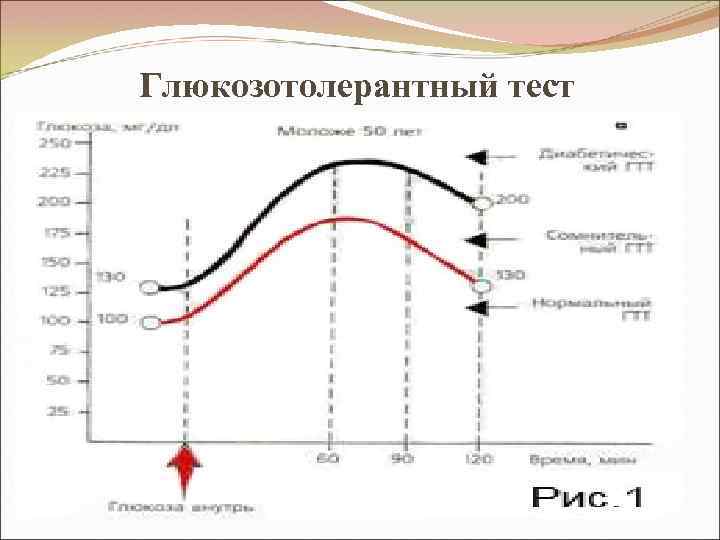
Глюкозотолерантный тест

Другие критерии диагностики СД 4. ↑ содержания в крови (гликированного) Hb (Hb. А 1: a, b, c). гликозилированного В норме составляет 4 -6% от общего количества Hb. A. У больных диабетом > 6% (может достигать - 12 -15%). ↓ Hb. A 1 c на 2% и 3% - ↓ риск смерти при СД 2 типа на 42% и 63%, соответственно. Hb. А 1 - Hb, к молекуле которого неферментативным путем необратимо присоединяется глюкоза. Чем выше уровень глюкозы, тем активнее процесс (после нормализации уровня глюкозы в крови уровень гли. Hb восстанавливается до нормы в среднем через 4 -6 недель). Поэтому уровень гли. Hb используется для оценки компенсации СД. ↑ уровня гли. Hb – свидетельство гипергликемии за 2 -3 месячный период времени. Соответственно, СД плохо компенсирован; необходимо выяснить с чем это было связано: - с нарушением диеты, либо - назначена несоответствующая доза инсулина (т. е. проводится с целью оценки эффективности терапии СД. Рекомендации ВОЗ – необходимо измерять уровень Hb. А 1 не реже, чем раз в 3 месяца).

Диагностика гестационного СД Заподозрить развитие у женщины СД беременных можно по анализу крови, в котором уровень глюкозы достигает: - 4, 8 -6, 0 ммоль/л, а также, если уровень сахара в крови, взятой натощак из пальца, - превышает 6, 0 ммоль/л. Для точной диагностики сахарного диабета беременных применяется тест с глюкозой. Вода с 50 г сахара выпивается за полчаса и часа до анализа крови из вены. Данный уровень сахара в крови показывает скорость его переработки организмом беременной. Если он превышает 7, 7 ммоль/л, то женщине ставят диагноз гестационного диабета. Обычно такой анализ проводится с 24 по 28 неделю.

Нарушения липидного обмена Лучше изучены для СД 1 типа. Абсолютный дефицит инсулина нарушает обмен липидов на уровне: • адипоцитов (жировые клетки) и • гепатоцитов (клетки печени). I. Адипоциты - происходит значительное «истощение» жировых депо: • ↓ синтез ТГ (дефицит липопротеинлипазы для их синтеза), • резко ↑ распад ТГ (→ гипертриглицеридемия, ее степень коррелирует с уровнем гликемии) – выраженный липолиз. ↓ Клиническое проявление - ↓ массы тела.

Нарушения липидного обмена (продолжение) Расщепление ТГ формирует большой объем СЖК → выбрасываются в кровоток → СЖК по портальной вене (коротким путем) поступают в печень. II. Гепатоциты. В печени СЖК утилизируются двумя путями: 1. Используются для ресинтеза ТГ → ↑ содержание жиров в печени – жировая инфильтрация печени;

Нарушения липидного обмена (продолжение) 2. Большая часть окисляется до ацетил-Ко. А: из-за нарушения утилизации Ац. Ко. А в цикле Кребса, ↑ количество субстрата, В избытке из которого синтезируются кетоновые начинает образовываться ХС (в тела (кетокислоты – ацетоуксусная составе ЛПНП) и β-оксимасляная кислоты, и ацетон). → АТС (у больных СД ≈ через 10 лет). + одновременное ↓ внепеченочного разрушения тканями кетоновых тел → ↑ концентрации кетоновых тел в крови (кетонемия).

Нарушения белкового обмена Инсулин – мощный анаболический гормон (стимулирует синтез нуклеиновых кислот, ↑ синтез белка - для роста тканей и формирования мышечной массы). Дефицит инсулина → ↑ катаболизма (преобладают процессы распада белка, особенно в лимфоидной ткани и в мышцах, что сопровождается ↑ содержания аминокислот (гипераминоацидемия) и мочевины (из-за стимуляции процессов дезаминирования) в крови, потерей организмом азота). Клинические проявления: • развивается иммунодефицит (у больных – рецидивирующие гнойные заболевания; хронические инфекции мочевыводящих и половых путей; пневмония и др. Нередко тяжелые инфекции являются одной из причин смерти); • ↓ репаративные процессы: - плохо заживают раны (в том числе и операционные), - плохо срастаются переломы; • отмечается потеря веса, слабость в мышцах; • при детском диабете – нарушаются рост и физическое развитие.
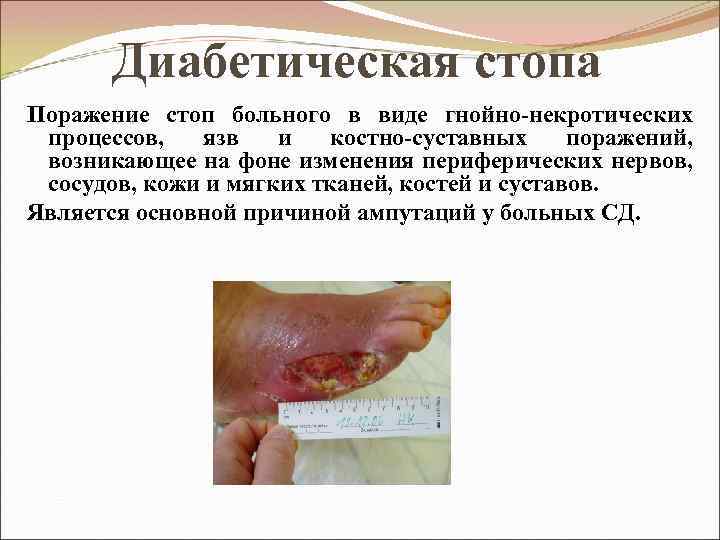
Диабетическая стопа Поражение стоп больного в виде гнойно-некротических процессов, язв и костно-суставных поражений, возникающее на фоне изменения периферических нервов, сосудов, кожи и мягких тканей, костей и суставов. Является основной причиной ампутаций у больных СД.

Водно-электролитный обмен Экскреция кетоновых тел почками уменьшает содержание в организме связанных оснований, что ведет к дополнительной потере натрия. Это означает ослабление ионного «скелета» внеклеточной жидкости и соответственно прогрессирующее уменьшение способности организма удерживать воду. Дегидратации способствует полиурия, обусловленная гипергликемией и увеличением содержания мочевины в крови. Прогрессирующая потеря воды приводит к: - клеточной дегидратации, - выходу электролитов (калия) из клетки во внеклеточную жидкость (↓ калия клетками способствует усиленный распад белков при отсутствии инсулина) с последующей его потерей.

Классификация осложнений I. Острые – кома: • собственно диабетическая: - кетоацидотическая, - гиперосмолярная, - лактацидотическая, • гипогликемическая II. Поздние (развитие сосудистой патологии) – диабетические ангиопатии: • микроангиопатии, • макроангиопатии

Кетоацидотическая кома Обусловлена токсическим влиянием кетоновых тел на клетки ЦНС (блокируют выработку энергии в нейронах мозга, необходимую для их функционирования. «Свет гаснет – возникает кома» ). Симптомы: Запах ацетона изо рта (похож на запах прокисших фруктов); Быстрое утомление, слабость; Головная боль; Снижение аппетита, а затем – отсутствие аппетита, отвращение к пищи; Боли в животе; Возможны тошнота, рвота, понос; Шумное, глубокое, учащенное дыхание.

Гиперосмолярная кома Встречается главным образом у пожилых больных с СД 2 типа. Механизм Обезвоживание клеток ЦНС (головного мозга) – ↑ В интерстициальном пространстве - ↑ уровня глюкозы → ↑ осмотическое Р → перемещение воды из клеток ЦНС в интерстициальное пространство. Лечение На догоспитальном этапе – в/в (капельное) введение гипотонического (0, 45%) р-ра Na. Cl (для нормализации осмотического Р). В стационаре - при резком снижении АД – мезатон или допамин. Целесообразно (как и при других комах) - проведение оксигенотерапии.

Лактацидотическая кома Чаще возникает у больных старше 50 лет на фоне сердечно-сосудистой, печеночной и почечной недостаточности, пониженного снабжения тканей кислородом (гипоксия) и, как следствие этого, накопления в тканях молочной кислоты. Механизм Накопление в крови молочной кислоты Гипоксия → активация анаэробного гликолиза → накопление избытка молочной кислоты → метаболический ацидоз. В норме молочная кислота быстро из крови поступает в печень → образование гликогена. При лактат-коме образуется избыточное количество молочной кислоты → превышение возможности ее использования печенью для синтеза гликогена.

Гипогликемическая кома Этиология • передозировка инсулина или пероральных сахароснижающих препаратов, • нарушение диеты (несвоевременность или прием пищи с недостаточным содержанием углеводов), • интенсивная физическая нагрузка, • прием салицилатов, β-адреноблокаторов на фоне инсулинотерапии или лечения пероральными сахароснижающими средствами, • ↑ чувствительности к инсулину у больного с СД (при диабетической нефропатии; употребление алкоголя; снижение функции надпочечников). Патогенез - ↓ утилизации глюкозы клетками ЦНС и - выраженный энергетический дефицит.

Микроангиопатии М. – это комплекс специфических (характерны только для СД) патологических изменений в сосудах микроциркуляции (артериолы, капилляры, венулы, межмикрососудистые анастомозы) и периваскулярных зонах, включающих: • утолщение (за счет избыточного синтеза коллагена IV типа – гликозилированный коллаген < растворим и > устойчив к действию коллагеназы, что приводит к его избыточному накоплению в базальной мембране капилляров; протеогликанов; фибронектина; ламинина) и разволокнение базальной мембраны (+ отложение в ней ИК), • нарушение избирательной проницаемости сосудистой стенки ( ↑ проницаемости для белков плазмы и других макромолекул) и • локальное разрастание эндотелиоцитов (пролиферация эндотелия вследствие нарушения обмена полисахаридов) и ГМК. В результате - резко ↓ суммарный просвет микрососудов и развивается ишемия органов. Больше всего страдают: - клубочки почек – нефропатия, что нередко ведет к ХПН, - сетчатка глаза (ретинопатия) - нередко ведет к слепоте.

Микроангиопатии (продолжение) Механизмы микроангиопатий Главный патогенетический фактор - хроническая гипергликемия - индуцирует ряд патологических механизмов (каскад биохимических нарушений), реализующих глюкозотоксичность на сосуды: • происходит гликирование белков мембран эндотелиоцитов, базальной мембраны (↑ количества гликозилированных белков, обладающих антигенной активностью по отношению к стенке сосуда) и других белков, с нарушением их свойств; (В частности, нарушается трансмембранная передача сигнала. Имеют значение и внутрисосудистые факторы - гликозилированный гемоглобин, обладая повышенным сродством к кислороду, способствует ↓ р. О 2 в крови, а тем самым и ишемии органов и тканей. Повышенное гликозилирование белков приводит к необратимым структурным внутрисосудистым изменениям, которые инициируют накопление иммунных комплексов. Несколько гликозилированных белков могут соединяться друг с другом через остатки 3 -дезоксиглюкозы. При этом образуются перекрестно сшитые гликозилированные белки. Связывание таких белков с рецепторами на макрофагах и эндотелиальных клетках стимулирует синтез и секрецию цитокинов, эндотелина-1 и тканевого фактора).

Механизмы микроангиопатий (продолжение) • повышенное аутоокисление глюкозы → активация процессов ПОЛ → накопление свободных радикалов (→ множество патологических процессов: нарушение функции митохондрий и внутриклеточный энергетический дефицит, изменение свойств мембран, эндотелиальная дисфункция, изменения в синтезе ненасыщенных жирных кислот и простагландинов, гиперкоагуляция и др. ) → повреждение мембран, • глюкоза локально в тканях ↑ содержание ангиотензина II → стимулирующее действие на иммунокомпетентные клетки → активация продукции некоторых цитокинов (IL-1, IL -6 и IL-8, интерферон, ФНО) (например, в почках - ↑ в 1000 раз).

Диабетические макроангиопатии МА - поражения артерий крупного и среднего калибра, с образованием на их эндотелии атеросклеротических бляшек (которые могут кальцифицироваться и изъязвляться, способствуя локальному тромбообразованию, окклюзии просвета сосуда). Риск развития АТС при СД в 4 -5 раз выше, чем в среднем в популяции (особенно среди женщин). С одной стороны - не являются специфическими осложнениями СД, но с другой – это проявления диабетической МА в силу специфики атеросклеротического процесса: - мультисегментарность поражения артерий, - более бурное течение, - возникновение в молодом возрасте (как у мужчин, так и у женщин), - слабый ответ на лечение антитромботическими препаратами, и др.

Макроангиопатии при СД (продолжение) Диабетические МА (в соответствии с локализацией и клиническими проявлениями) подразделяются на: поражения сосудов сердца (ИБC, инфаркт миокарда), поражения сосудов мозга (острое и хроническое нарушения мозгового кровообращения), поражения периферических артерий, в том числе нижних конечностей (гангрена). Механизм МА Основное - гипергликемия: • неферментативное гликозилирование белков → образование свободных радикалов (обладают мощной окислительной активностью) → ↑ проницаемости и ↓ эластичности сосудов (+ изменение функции энзимов и обмена липопротеидов), • гликозилированные ЛПНП: - не распознаются рецепторами ЛПНП в печени, поэтому концентрация ЛПНП в плазме возрастает (напротив, гликозилированные ЛПВП метаболизируются в печени гораздо быстрее, чем нормальные ЛПВП); - легко окисляются и имеют большое сродство к макрофагам → образование «пенистых клеток» (основной элемент атерогенеза).

Макроангиопатии при СД (продолжение) Дополнительно: • ↓ ЛПВП + ↑ ЛПНП (нарушения липидного обмена + АГ (наблюдается у 40 -60% больных СД) (ведущий фактор в развитии диабетической нефропатии) → нарушение элиминации атерогенных фракций липопротеидов → ускорение АТС, • усиление пролиферации ГМК артерий (под действием избыточного количества гормона роста), • повышенный синтез тромбоксана → способствует адгезии тромбоцитов и выделению митогена.

Профилактика осложнений Контроль АД. Преимущество отдаётся: - метаболически нейтральным (ИАПФ, сартаны) и - метаболически позитивным (моксонидин) препаратам. Назначение гиполипидемической терапии: - различных препаратов из группы статинов (контроль ТГ, ЛПНП и повышение ЛПВП и снижение прогрессирования ретинопатии, нейропатии, ИБС), - комбинация фенофибрата и статинов у пациентов высокого риска с макросудистыми осложнениями в анамнезе.

Прогноз В настоящее время прогноз при всех типах СД условно благоприятный. При адекватно проводимом лечении и соблюдении режима питания: - сохраняется трудоспособность, - прогрессирование осложнений значительно замедляется или полностью прекращается. Однако следует отметить, что в большинстве случаев в результате лечения причина заболевания не устраняется, и терапия носит лишь симптоматический характер.
с.диабет.ppt