[Медкниги]Физико-химические механизмы патологии клетки. Введение.ppt
- Количество слайдов: 46
 Российский Государственный Медицинский Университет Московский Государственный Университет Ю. А. Владимиров Физико-химические основы патологии клетки Митохондрии и апоптоз Москва © 1999
Российский Государственный Медицинский Университет Московский Государственный Университет Ю. А. Владимиров Физико-химические основы патологии клетки Митохондрии и апоптоз Москва © 1999
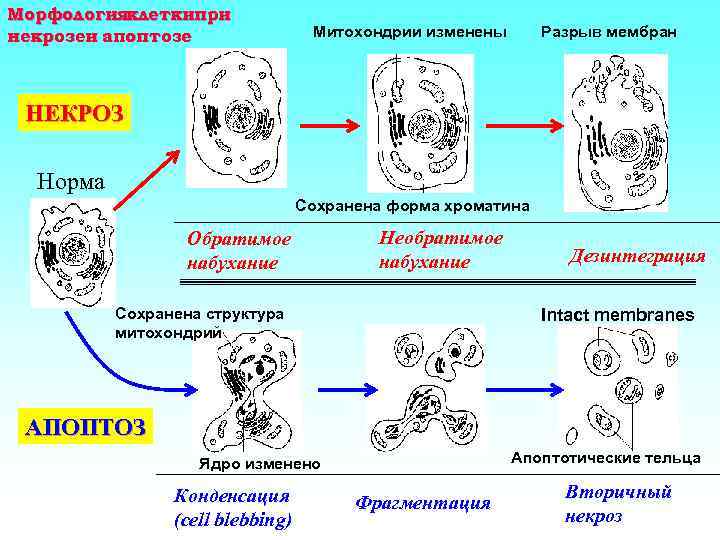 Морфологияклеткипри некрозеи апоптозе Митохондрии изменены Разрыв мембран НЕКРОЗ Норма Сохранена форма хроматина Обратимое набухание Необратимое набухание Сохранена структура митохондрий Дезинтеграция Intact membranes АПОПТОЗ Апоптотические тельца Ядро изменено Конденсация (cell blebbing) Фрагментация Вторичный некроз
Морфологияклеткипри некрозеи апоптозе Митохондрии изменены Разрыв мембран НЕКРОЗ Норма Сохранена форма хроматина Обратимое набухание Необратимое набухание Сохранена структура митохондрий Дезинтеграция Intact membranes АПОПТОЗ Апоптотические тельца Ядро изменено Конденсация (cell blebbing) Фрагментация Вторичный некроз
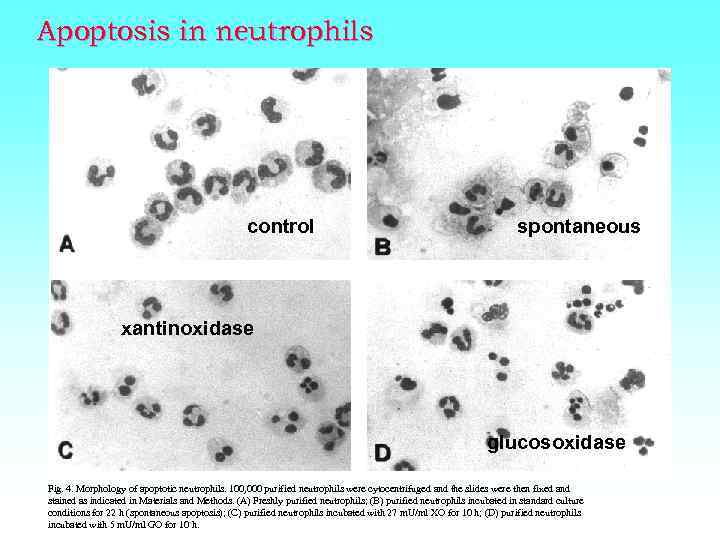 Apoptosis in neutrophils control spontaneous xantinoxidase glucosoxidase Fig. 4. Morphology of apoptotic neutrophils. 100, 000 purified neutrophils were cytocentrifuged and the slides were then fixed and stained as indicated in Materials and Methods. (A) Freshly purified neutrophils; (B) purified neutrophils incubated in standard culture conditions for 22 h (spontaneous apoptosis); (C) purified neutrophils incubated with 27 m. U/ml XO for 10 h; (D) purified neutrophils incubated with 5 m. U/ml GO for 10 h.
Apoptosis in neutrophils control spontaneous xantinoxidase glucosoxidase Fig. 4. Morphology of apoptotic neutrophils. 100, 000 purified neutrophils were cytocentrifuged and the slides were then fixed and stained as indicated in Materials and Methods. (A) Freshly purified neutrophils; (B) purified neutrophils incubated in standard culture conditions for 22 h (spontaneous apoptosis); (C) purified neutrophils incubated with 27 m. U/ml XO for 10 h; (D) purified neutrophils incubated with 5 m. U/ml GO for 10 h.
![Немитохондриальный путь активации апоптоза Fas receptor TNF receptor [46] DED is shared by FADD/MORT Немитохондриальный путь активации апоптоза Fas receptor TNF receptor [46] DED is shared by FADD/MORT](https://present5.com/presentation/3/50762570_437202129.pdf-img/50762570_437202129.pdf-4.jpg) Немитохондриальный путь активации апоптоза Fas receptor TNF receptor [46] DED is shared by FADD/MORT 1, caspase-8 and TRADD (TNF receptor associated protein) [52]. DD FADD/ MORT 1 TRADD [50, 51] Procaspase-8 DED [53, 54] [49] [52] Like CARD, DED can be used by FADD to recruit and activate caspase-8 [53, 54], in a process that occurs within minutes after receptor Caspase-8 (Active) Procaspase-1 Caspase-1 Apoptotic cascade FADD/MORT 1 - receptor associated protein DED- death ejector domain of FADD/MORT 1 TRADD - TNF receptor associated protein Fas-induced apoptotic cascade (on the basis of Cai, J. BBA 1366 (1998) 139 -149)
Немитохондриальный путь активации апоптоза Fas receptor TNF receptor [46] DED is shared by FADD/MORT 1, caspase-8 and TRADD (TNF receptor associated protein) [52]. DD FADD/ MORT 1 TRADD [50, 51] Procaspase-8 DED [53, 54] [49] [52] Like CARD, DED can be used by FADD to recruit and activate caspase-8 [53, 54], in a process that occurs within minutes after receptor Caspase-8 (Active) Procaspase-1 Caspase-1 Apoptotic cascade FADD/MORT 1 - receptor associated protein DED- death ejector domain of FADD/MORT 1 TRADD - TNF receptor associated protein Fas-induced apoptotic cascade (on the basis of Cai, J. BBA 1366 (1998) 139 -149)
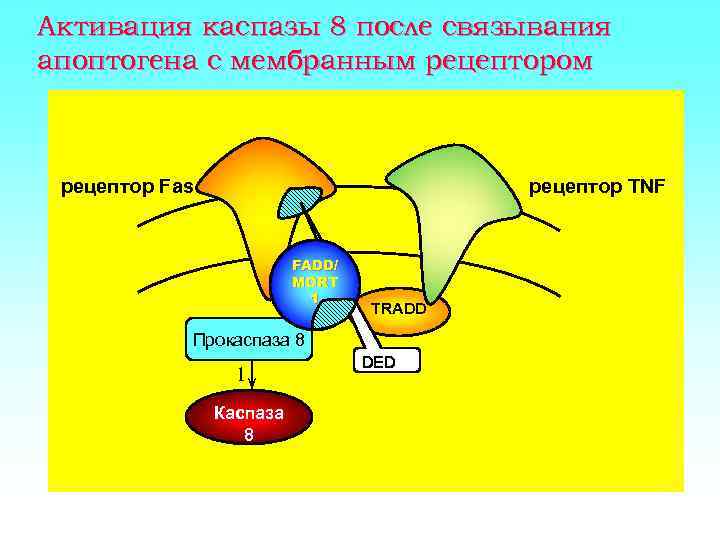 Активация каспазы 8 после связывания апоптогена с мембранным рецептором рецептор Fas рецептор TNF FADD/ MORT 1 TRADD Прокаспаза 8 1 Каспаза 8 DED
Активация каспазы 8 после связывания апоптогена с мембранным рецептором рецептор Fas рецептор TNF FADD/ MORT 1 TRADD Прокаспаза 8 1 Каспаза 8 DED
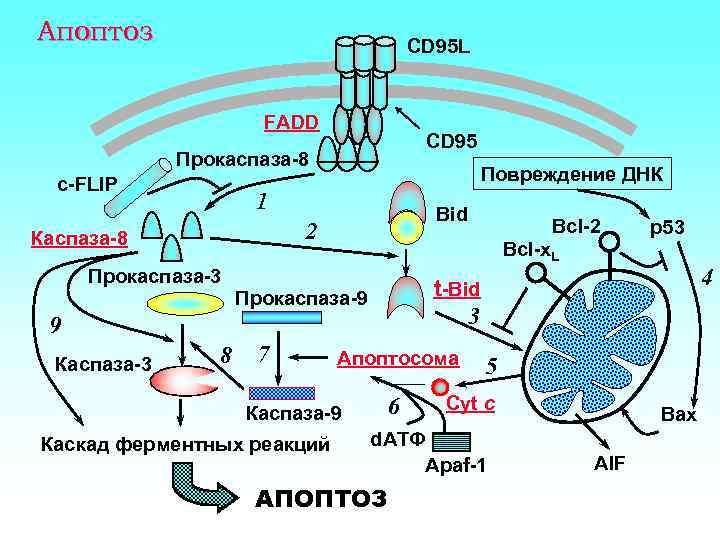 Апоптоз CD 95 L FADD CD 95 Прокаспаза-8 c-FLIP Повреждение ДНК 1 Bid 2 Каспаза-8 Прокаспаза-3 Bcl-x. L 8 Прокаспаза-9 7 Апоптосома 6 Каспаза-9 Каскад ферментных реакций p 53 4 t-Bid 3 9 Каспаза-3 Bcl-2 5 Cyt c d. АТФ Apaf-1 АПОПТОЗ Bax AIF
Апоптоз CD 95 L FADD CD 95 Прокаспаза-8 c-FLIP Повреждение ДНК 1 Bid 2 Каспаза-8 Прокаспаза-3 Bcl-x. L 8 Прокаспаза-9 7 Апоптосома 6 Каспаза-9 Каскад ферментных реакций p 53 4 t-Bid 3 9 Каспаза-3 Bcl-2 5 Cyt c d. АТФ Apaf-1 АПОПТОЗ Bax AIF
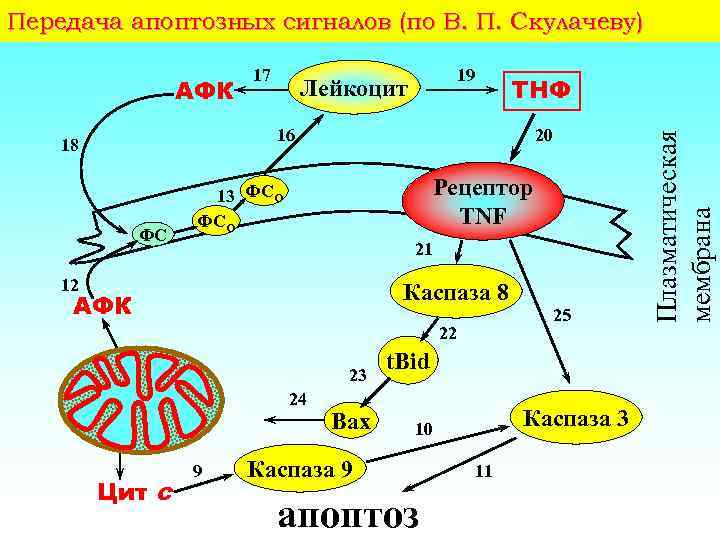 Передача апоптозных сигналов (по В. П. Скулачеву) 19 Лейкоцит ТНФ 16 18 ФС 20 Рецептор TNF 13 ФСО 21 12 Каспаза 8 АФК 22 23 24 Цит c 9 Bax 25 t. Bid Каспаза 3 10 Каспаза 9 апоптоз 11 Плазматическая мембрана АФК 17
Передача апоптозных сигналов (по В. П. Скулачеву) 19 Лейкоцит ТНФ 16 18 ФС 20 Рецептор TNF 13 ФСО 21 12 Каспаза 8 АФК 22 23 24 Цит c 9 Bax 25 t. Bid Каспаза 3 10 Каспаза 9 апоптоз 11 Плазматическая мембрана АФК 17
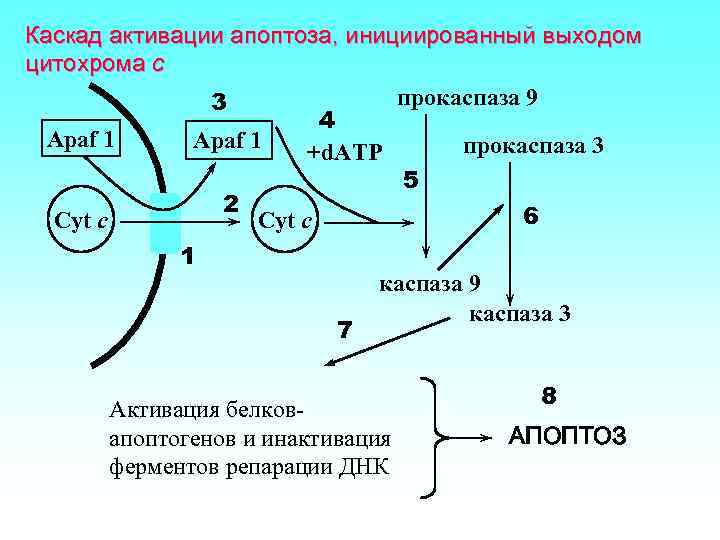 Каскад активации апоптоза, инициированный выходом цитохрома c прокаспаза 9 3 4 Apaf 1 прокаспаза 3 +d. ATP 5 2 6 Cyt c 1 7 каспаза 9 каспаза 3 Активация белковапоптогенов и инактивация ферментов репарации ДНК 8 АПОПТОЗ
Каскад активации апоптоза, инициированный выходом цитохрома c прокаспаза 9 3 4 Apaf 1 прокаспаза 3 +d. ATP 5 2 6 Cyt c 1 7 каспаза 9 каспаза 3 Активация белковапоптогенов и инактивация ферментов репарации ДНК 8 АПОПТОЗ
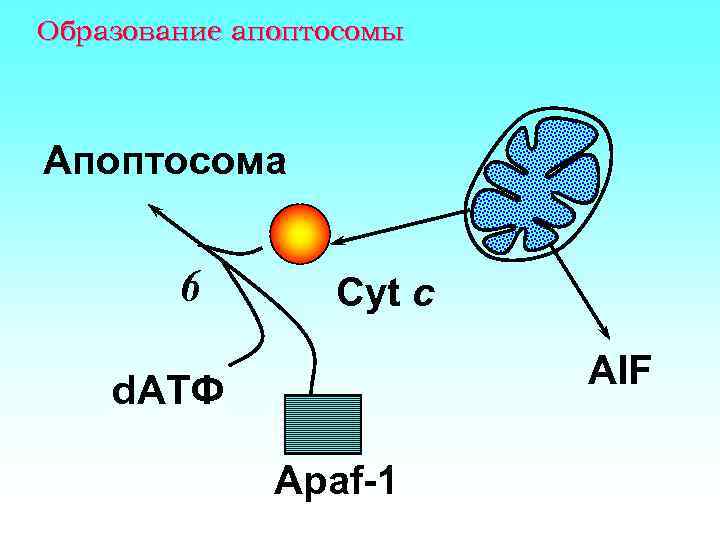 Образование апоптосомы Апоптосома 6 Cyt c AIF d. АТФ Apaf-1
Образование апоптосомы Апоптосома 6 Cyt c AIF d. АТФ Apaf-1
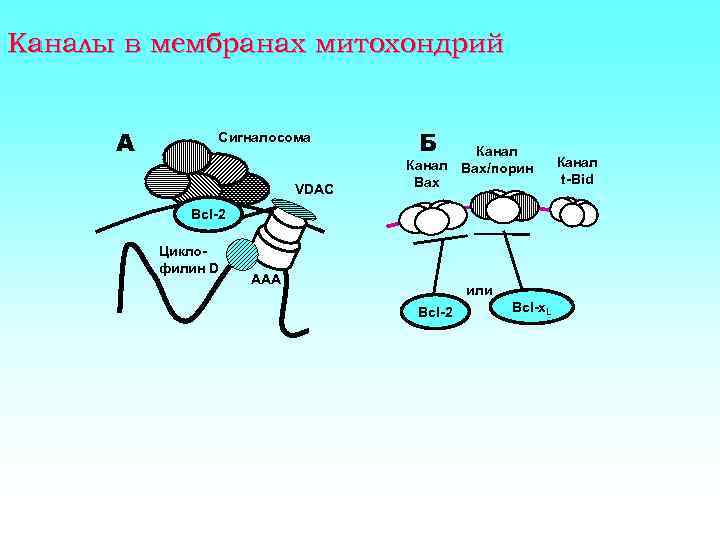 Каналы в мембранах митохондрий А Сигналосома VDAC Б Канал Bax/порин Bax Bcl-2 Циклофилин D ААА или Bcl-2 Bcl-x. L Канал t-Bid
Каналы в мембранах митохондрий А Сигналосома VDAC Б Канал Bax/порин Bax Bcl-2 Циклофилин D ААА или Bcl-2 Bcl-x. L Канал t-Bid
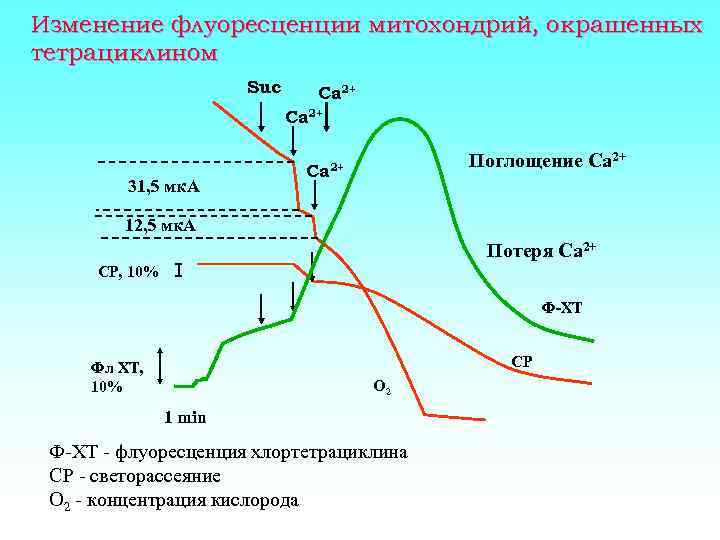 Изменение флуоресценции митохондрий, окрашенных тетрациклином Suc Ca 2+ 31, 5 мк. А Поглощение Ca 2+ 12, 5 мк. А Потеря Ca 2+ СР, 10% Ф-ХТ СР Фл ХТ, 10% O 2 1 min Ф-ХТ - флуоресценция хлортетрациклина СР - светорассеяние O 2 - концентрация кислорода
Изменение флуоресценции митохондрий, окрашенных тетрациклином Suc Ca 2+ 31, 5 мк. А Поглощение Ca 2+ 12, 5 мк. А Потеря Ca 2+ СР, 10% Ф-ХТ СР Фл ХТ, 10% O 2 1 min Ф-ХТ - флуоресценция хлортетрациклина СР - светорассеяние O 2 - концентрация кислорода
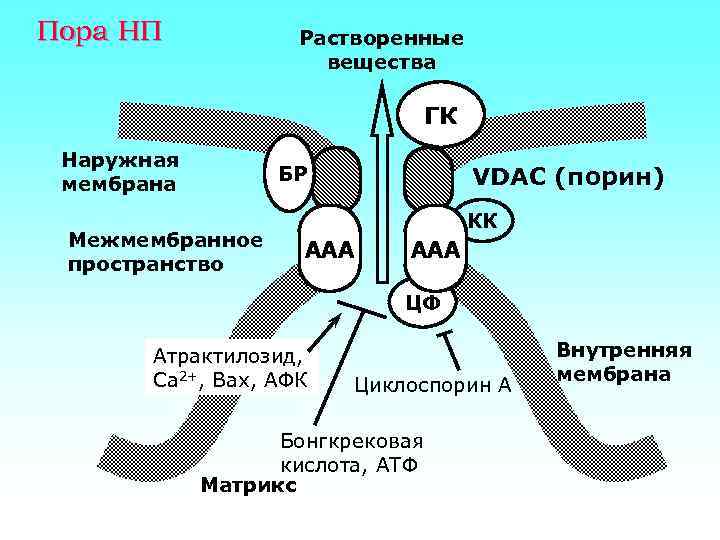 Пора НП Растворенные вещества ГК Наружная мембрана БР Межмембранное пространство VDAC (порин) КК ААА ЦФ Атрактилозид, Са 2+, Вах, АФК Циклоспорин А Бонгкрековая кислота, АТФ Матрикс Внутренняя мембрана
Пора НП Растворенные вещества ГК Наружная мембрана БР Межмембранное пространство VDAC (порин) КК ААА ЦФ Атрактилозид, Са 2+, Вах, АФК Циклоспорин А Бонгкрековая кислота, АТФ Матрикс Внутренняя мембрана
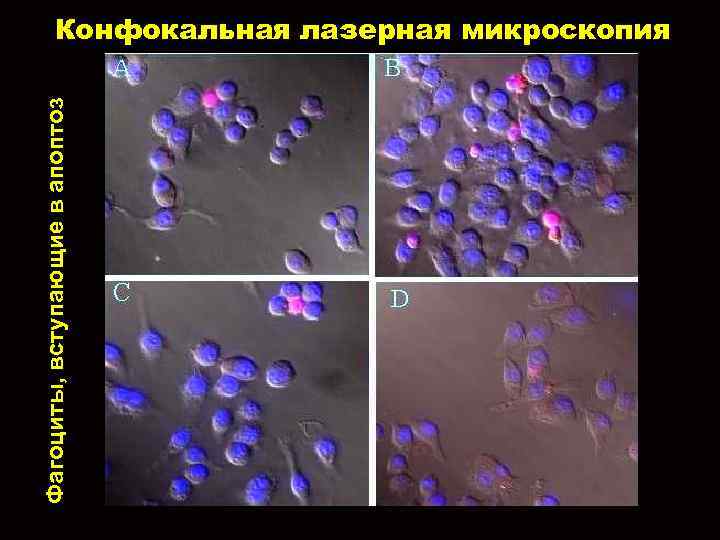 Фагоциты, вступающие в апоптоз Конфокальная лазерная микроскопия
Фагоциты, вступающие в апоптоз Конфокальная лазерная микроскопия
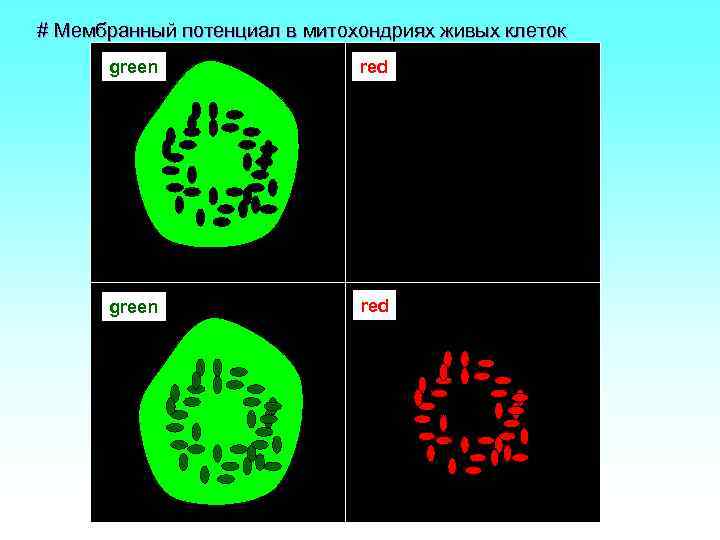 # Мембранный потенциал в митохондриях живых клеток green red
# Мембранный потенциал в митохондриях живых клеток green red
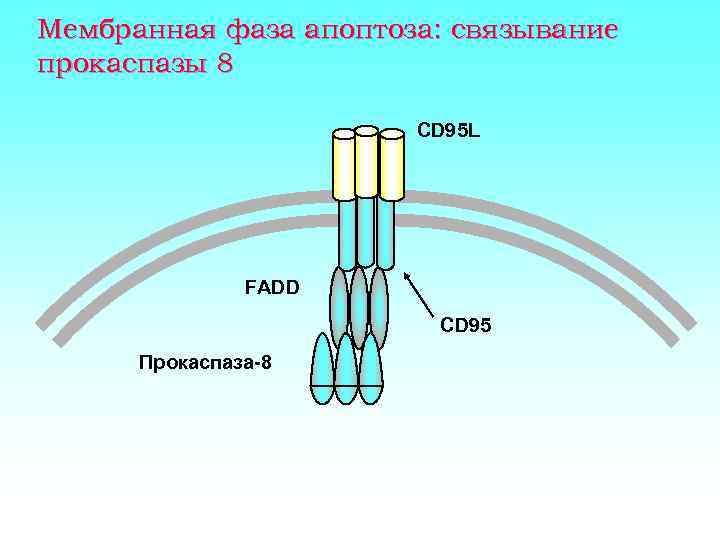 Мембранная фаза апоптоза: связывание прокаспазы 8 CD 95 L FADD CD 95 Прокаспаза-8
Мембранная фаза апоптоза: связывание прокаспазы 8 CD 95 L FADD CD 95 Прокаспаза-8
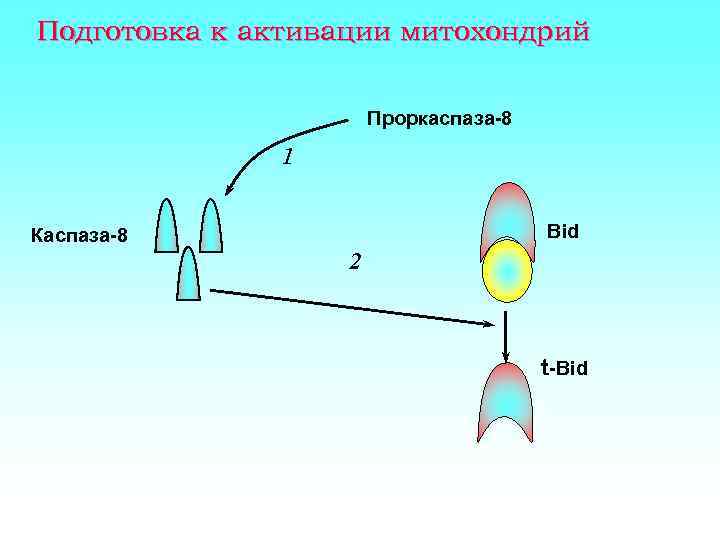 Подготовка к активации митохондрий Проркаспаза-8 1 Bid Каспаза-8 2 t-Bid
Подготовка к активации митохондрий Проркаспаза-8 1 Bid Каспаза-8 2 t-Bid
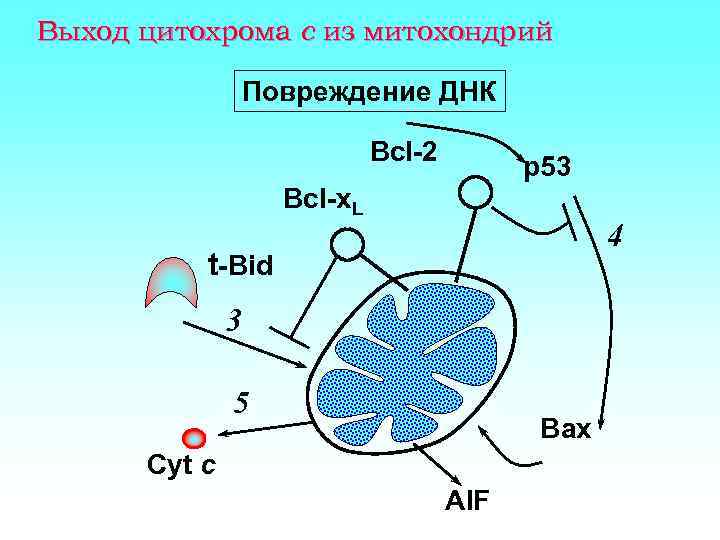 Выход цитохрома с из митохондрий Повреждение ДНК Bcl-2 p 53 Bcl-x. L 4 t-Bid 3 5 Bax Cyt c AIF
Выход цитохрома с из митохондрий Повреждение ДНК Bcl-2 p 53 Bcl-x. L 4 t-Bid 3 5 Bax Cyt c AIF
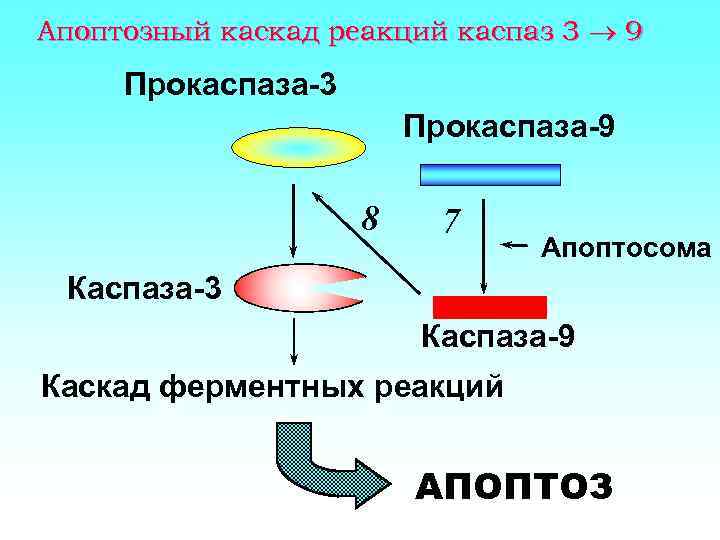 Апоптозный каскад реакций каспаз 3 9 Прокаспаза-3 Прокаспаза-9 8 7 Апоптосома Каспаза-3 Каспаза-9 Каскад ферментных реакций АПОПТОЗ
Апоптозный каскад реакций каспаз 3 9 Прокаспаза-3 Прокаспаза-9 8 7 Апоптосома Каспаза-3 Каспаза-9 Каскад ферментных реакций АПОПТОЗ
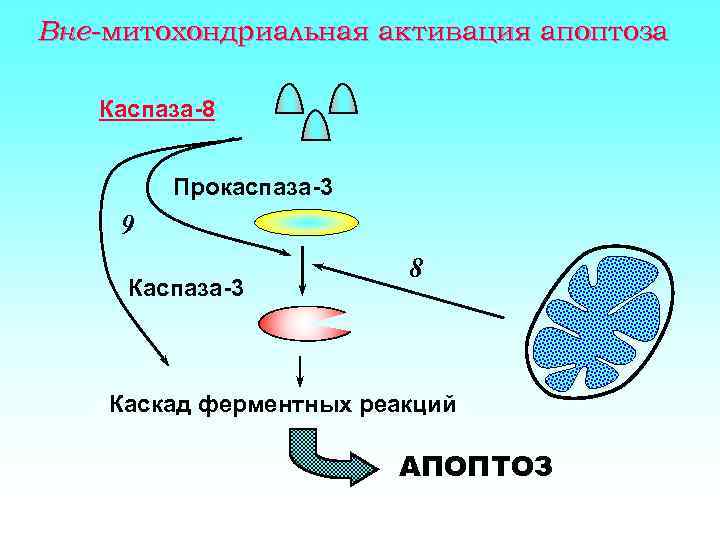 Вне-митохондриальная активация апоптоза Каспаза-8 Прокаспаза-3 9 Каспаза-3 8 Каскад ферментных реакций АПОПТОЗ
Вне-митохондриальная активация апоптоза Каспаза-8 Прокаспаза-3 9 Каспаза-3 8 Каскад ферментных реакций АПОПТОЗ
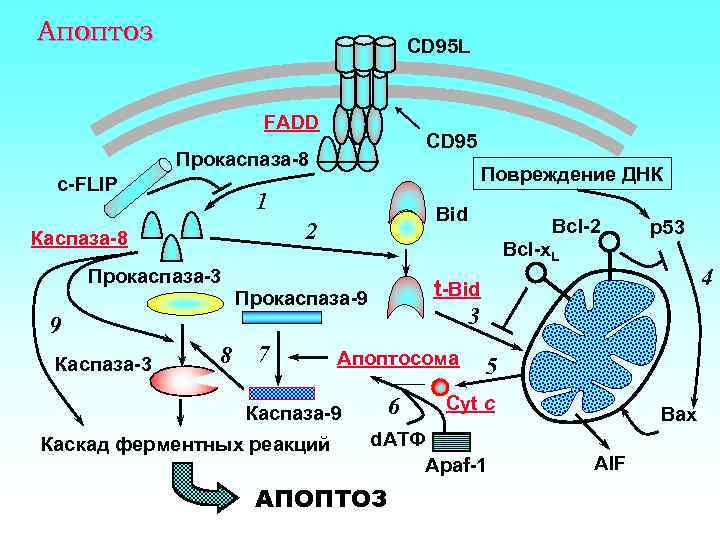 Апоптоз CD 95 L FADD CD 95 Прокаспаза-8 c-FLIP Повреждение ДНК 1 Bid 2 Каспаза-8 Прокаспаза-3 Bcl-x. L 8 Прокаспаза-9 7 Апоптосома 6 Каспаза-9 Каскад ферментных реакций p 53 4 t-Bid 3 9 Каспаза-3 Bcl-2 5 Cyt c d. АТФ Apaf-1 АПОПТОЗ Bax AIF
Апоптоз CD 95 L FADD CD 95 Прокаспаза-8 c-FLIP Повреждение ДНК 1 Bid 2 Каспаза-8 Прокаспаза-3 Bcl-x. L 8 Прокаспаза-9 7 Апоптосома 6 Каспаза-9 Каскад ферментных реакций p 53 4 t-Bid 3 9 Каспаза-3 Bcl-2 5 Cyt c d. АТФ Apaf-1 АПОПТОЗ Bax AIF
 Российский Государственный Медицинский Университет Московский Государственный Университет Ю. А. Владимиров Физико-химические основы патологии клетки АФК и апоптоз Москва © 2003
Российский Государственный Медицинский Университет Московский Государственный Университет Ю. А. Владимиров Физико-химические основы патологии клетки АФК и апоптоз Москва © 2003
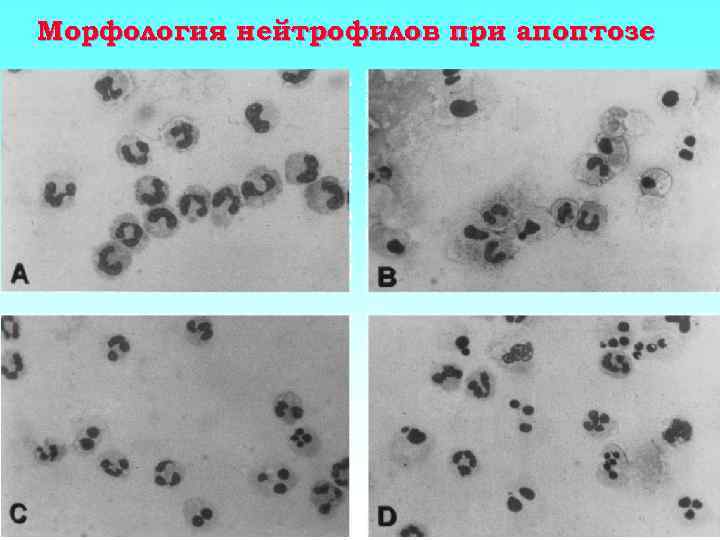 Морфология нейтрофилов при апоптозе
Морфология нейтрофилов при апоптозе
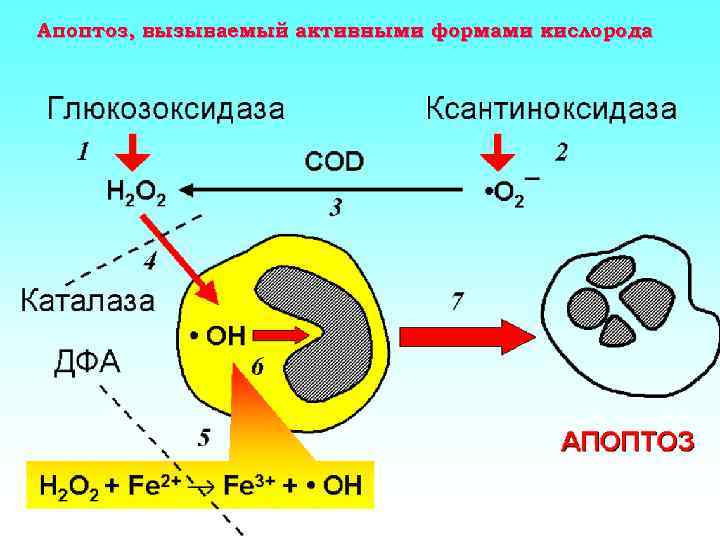 Апоптоз, вызываемый активными формами кислорода
Апоптоз, вызываемый активными формами кислорода
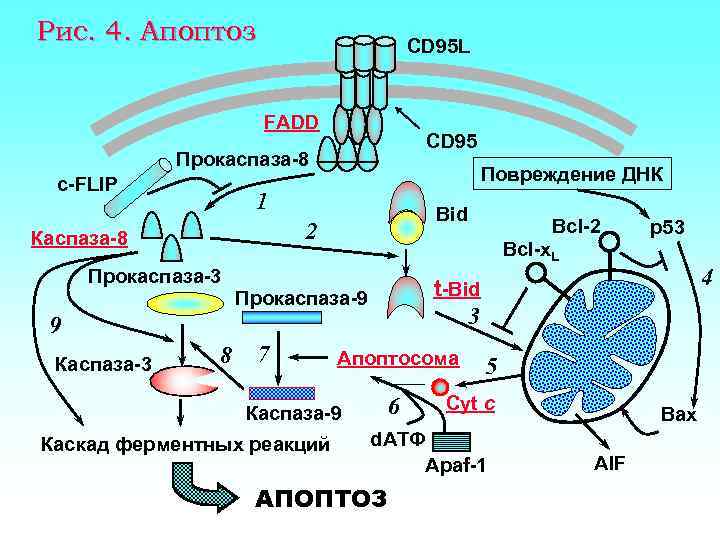 Рис. 4. Апоптоз CD 95 L FADD CD 95 Прокаспаза-8 c-FLIP Повреждение ДНК 1 Bid 2 Каспаза-8 Прокаспаза-3 Bcl-x. L 8 Прокаспаза-9 7 Апоптосома 6 Каспаза-9 Каскад ферментных реакций p 53 4 t-Bid 3 9 Каспаза-3 Bcl-2 5 Cyt c d. АТФ Apaf-1 АПОПТОЗ Bax AIF
Рис. 4. Апоптоз CD 95 L FADD CD 95 Прокаспаза-8 c-FLIP Повреждение ДНК 1 Bid 2 Каспаза-8 Прокаспаза-3 Bcl-x. L 8 Прокаспаза-9 7 Апоптосома 6 Каспаза-9 Каскад ферментных реакций p 53 4 t-Bid 3 9 Каспаза-3 Bcl-2 5 Cyt c d. АТФ Apaf-1 АПОПТОЗ Bax AIF
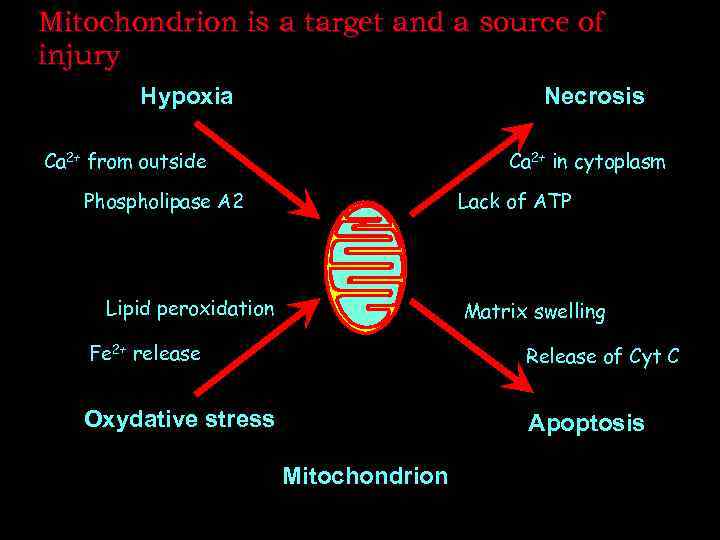 Mitochondrion is a target and a source of injury Hypoxia Necrosis Ca 2+ from outside Ca 2+ in cytoplasm Phospholipase A 2 Lack of ATP Lipid peroxidation Matrix swelling Fe 2+ release Release of Cyt C Oxydative stress Apoptosis Mitochondrion
Mitochondrion is a target and a source of injury Hypoxia Necrosis Ca 2+ from outside Ca 2+ in cytoplasm Phospholipase A 2 Lack of ATP Lipid peroxidation Matrix swelling Fe 2+ release Release of Cyt C Oxydative stress Apoptosis Mitochondrion
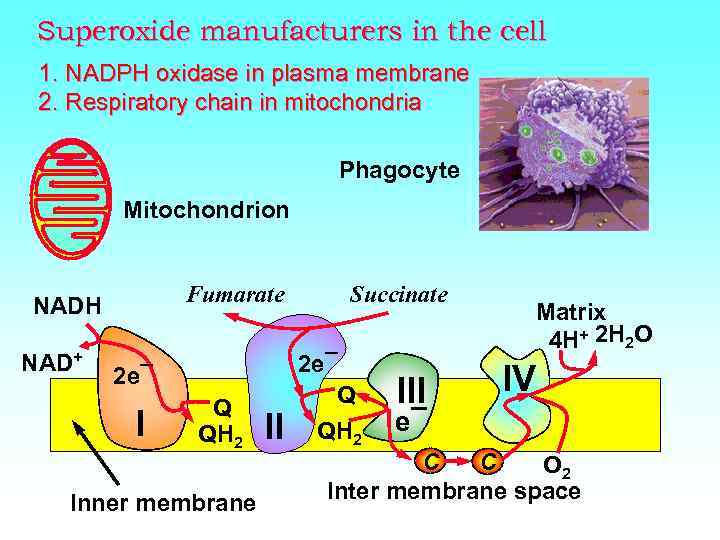 Superoxide manufacturers in the cell 1. NADPH oxidase in plasma membrane 2. Respiratory chain in mitochondria Phagocyte Mitochondrion Fumarate NADH NAD+ 2 e¯ I Q QH 2 Inner membrane II Succinate 2 e¯ Q QH 2 III Matrix 4 H+ 2 H 2 O IV e¯ C C O 2 Inter membrane space
Superoxide manufacturers in the cell 1. NADPH oxidase in plasma membrane 2. Respiratory chain in mitochondria Phagocyte Mitochondrion Fumarate NADH NAD+ 2 e¯ I Q QH 2 Inner membrane II Succinate 2 e¯ Q QH 2 III Matrix 4 H+ 2 H 2 O IV e¯ C C O 2 Inter membrane space
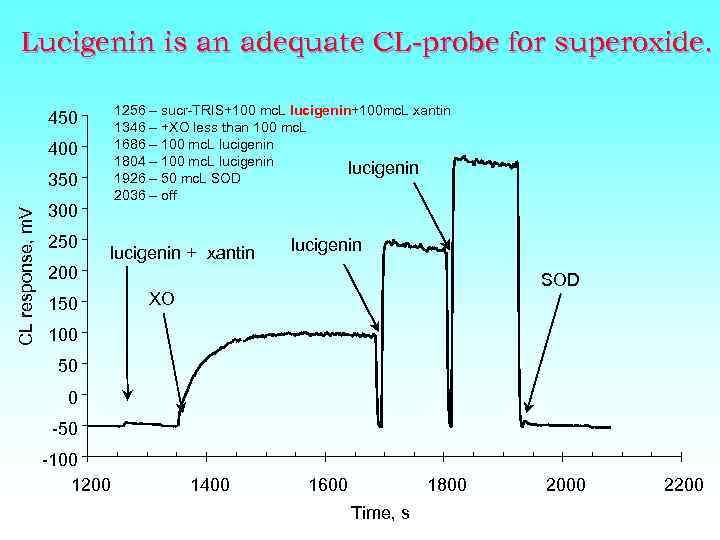 Lucigenin is an adequate CL-probe for superoxide. 1256 – sucr-TRIS+100 mc. L lucigenin+100 mc. L xantin 1346 – +XO less than 100 mc. L 1686 – 100 mc. L lucigenin 1804 – 100 mc. L lucigenin 1926 – 50 mc. L SOD 2036 – off 450 400 CL response, m. V 350 300 250 200 lucigenin + xantin 150 lucigenin SOD XO 100 50 0 -50 -100 1200 1400 1600 1800 Time, s 2000 2200
Lucigenin is an adequate CL-probe for superoxide. 1256 – sucr-TRIS+100 mc. L lucigenin+100 mc. L xantin 1346 – +XO less than 100 mc. L 1686 – 100 mc. L lucigenin 1804 – 100 mc. L lucigenin 1926 – 50 mc. L SOD 2036 – off 450 400 CL response, m. V 350 300 250 200 lucigenin + xantin 150 lucigenin SOD XO 100 50 0 -50 -100 1200 1400 1600 1800 Time, s 2000 2200
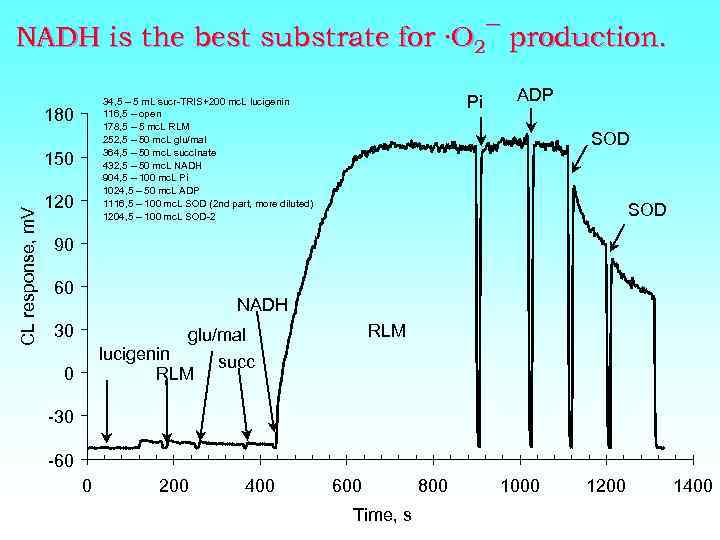 NADH is the best substrate for ·O 2¯ production. 180 150 CL response, m. V Pi 34, 5 – 5 m. L sucr-TRIS+200 mc. L lucigenin 116, 5 – open 178, 5 – 5 mc. L RLM 252, 5 – 50 mc. L glu/mal 364, 5 – 50 mc. L succinate 432, 5 – 50 mc. L NADH 904, 5 – 100 mc. L Pi 1024, 5 – 50 mc. L ADP 1116, 5 – 100 mc. L SOD (2 nd part, more diluted) 1204, 5 – 100 mc. L SOD-2 120 ADP SOD 90 60 NADH 30 RLM glu/mal lucigenin RLM 0 succ -30 -60 0 200 400 600 Time, s 800 1000 1200 1400
NADH is the best substrate for ·O 2¯ production. 180 150 CL response, m. V Pi 34, 5 – 5 m. L sucr-TRIS+200 mc. L lucigenin 116, 5 – open 178, 5 – 5 mc. L RLM 252, 5 – 50 mc. L glu/mal 364, 5 – 50 mc. L succinate 432, 5 – 50 mc. L NADH 904, 5 – 100 mc. L Pi 1024, 5 – 50 mc. L ADP 1116, 5 – 100 mc. L SOD (2 nd part, more diluted) 1204, 5 – 100 mc. L SOD-2 120 ADP SOD 90 60 NADH 30 RLM glu/mal lucigenin RLM 0 succ -30 -60 0 200 400 600 Time, s 800 1000 1200 1400
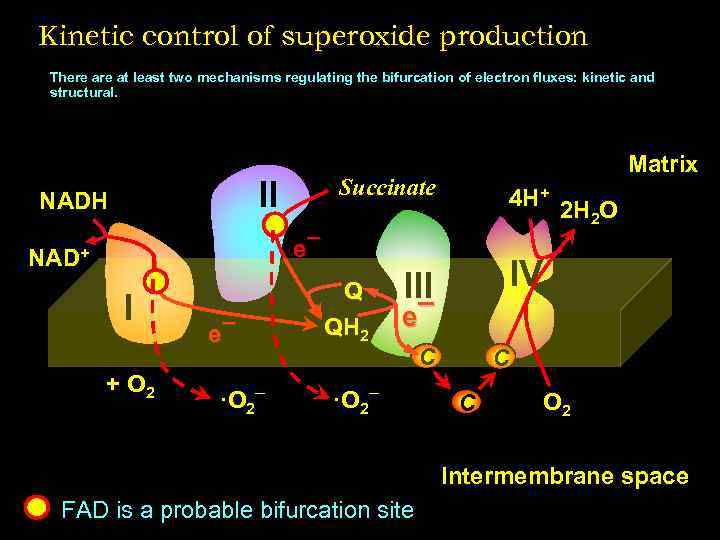 Kinetic control of superoxide production There at least two mechanisms regulating the bifurcation of electron fluxes: kinetic and structural. Succinate II NADH Matrix 4 H+ 2 H O 2 e¯ NAD+ I + O 2 e¯ ·O 2¯ Q QH 2 IV III e¯ ·O 2¯ C C C O 2 Intermembrane space FAD is a probable bifurcation site
Kinetic control of superoxide production There at least two mechanisms regulating the bifurcation of electron fluxes: kinetic and structural. Succinate II NADH Matrix 4 H+ 2 H O 2 e¯ NAD+ I + O 2 e¯ ·O 2¯ Q QH 2 IV III e¯ ·O 2¯ C C C O 2 Intermembrane space FAD is a probable bifurcation site
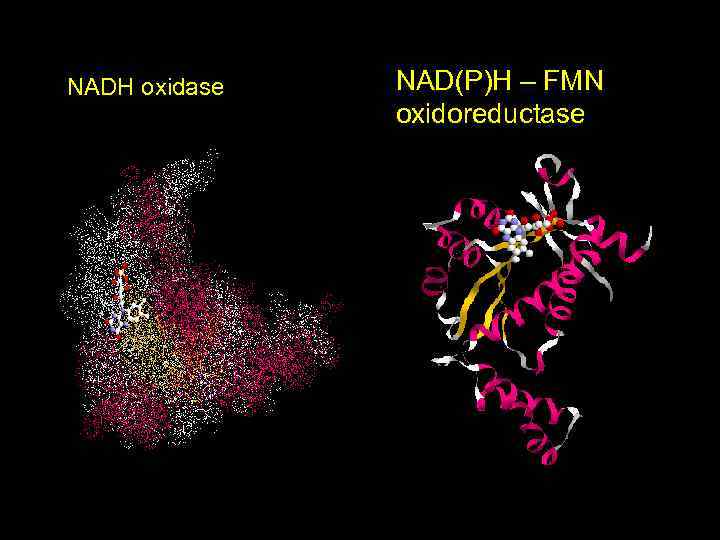 NAD(P)H – FMN oxidoreductase NADH oxidase FMN FMN
NAD(P)H – FMN oxidoreductase NADH oxidase FMN FMN
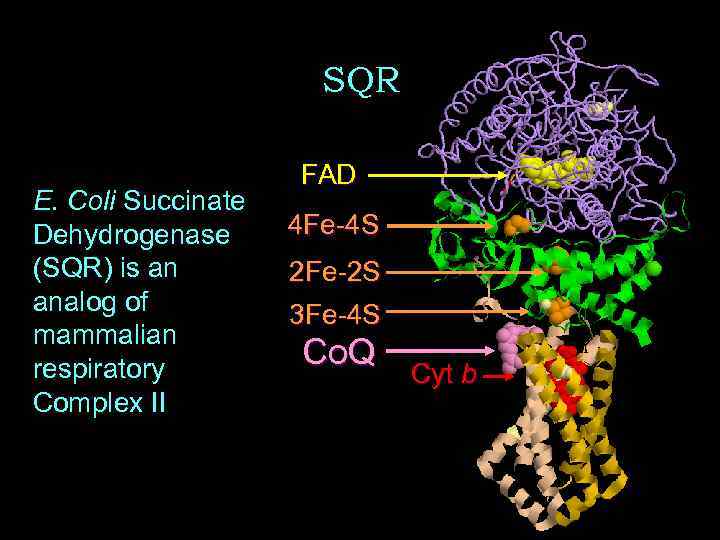 SQR E. Coli Succinate Dehydrogenase (SQR) is an analog of mammalian respiratory Complex II FAD 4 Fe-4 S 2 Fe-2 S 3 Fe-4 S Co. Q Cyt b
SQR E. Coli Succinate Dehydrogenase (SQR) is an analog of mammalian respiratory Complex II FAD 4 Fe-4 S 2 Fe-2 S 3 Fe-4 S Co. Q Cyt b
 Manifestations of mutations in SQR gene in eukaryotes Clinical phenotypes: 1. Optic atrophy 2. Tumor formation (paraganglioma, pheochromocytoma ) 3. Myopathy 4. Encephalopathy P. Rustin, A. Roetig, Biochim. Biophys. Acta 1553, 117 (2002) – a review. T. Bourgeron et al. , Nature Genet. 11, 144 (1995). B. E. Baysal et al. , Science 287, 848 (2000). S. Niemann, U. MuЁller, Nature Genet. 26, 268(2000). These disorders can be caused by oxidative stress produced by complex II
Manifestations of mutations in SQR gene in eukaryotes Clinical phenotypes: 1. Optic atrophy 2. Tumor formation (paraganglioma, pheochromocytoma ) 3. Myopathy 4. Encephalopathy P. Rustin, A. Roetig, Biochim. Biophys. Acta 1553, 117 (2002) – a review. T. Bourgeron et al. , Nature Genet. 11, 144 (1995). B. E. Baysal et al. , Science 287, 848 (2000). S. Niemann, U. MuЁller, Nature Genet. 26, 268(2000). These disorders can be caused by oxidative stress produced by complex II
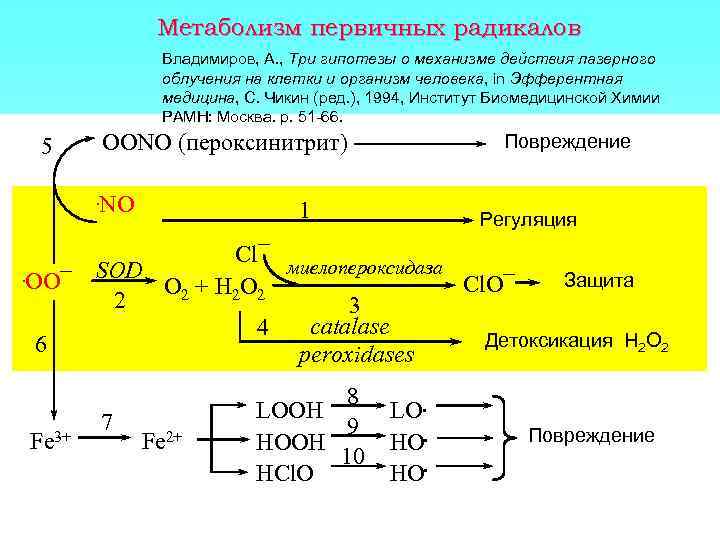 Метаболизм первичных радикалов Владимиров, А. , Три гипотезы о механизме действия лазерного облучения на клетки и организм человека, in Эфферентная медицина, С. Чикин (ред. ), 1994, Институт Биомедицинской Химии РАМН: Москва. p. 51 -66. 5 OONO (пероксинитрит). NO Повреждение 1 Регуляция Cl¯ миелопероксидаза. OO¯ SOD Защита Cl. O¯ O 2 + H 2 O 2 2 3 catalase 4 Детоксикация H 2 O 2 6 peroxidases Fe 3+ 7 Fe 2+ 8 LOOH 9 HOOH 10 HCl. O LO. HO. Повреждение
Метаболизм первичных радикалов Владимиров, А. , Три гипотезы о механизме действия лазерного облучения на клетки и организм человека, in Эфферентная медицина, С. Чикин (ред. ), 1994, Институт Биомедицинской Химии РАМН: Москва. p. 51 -66. 5 OONO (пероксинитрит). NO Повреждение 1 Регуляция Cl¯ миелопероксидаза. OO¯ SOD Защита Cl. O¯ O 2 + H 2 O 2 2 3 catalase 4 Детоксикация H 2 O 2 6 peroxidases Fe 3+ 7 Fe 2+ 8 LOOH 9 HOOH 10 HCl. O LO. HO. Повреждение
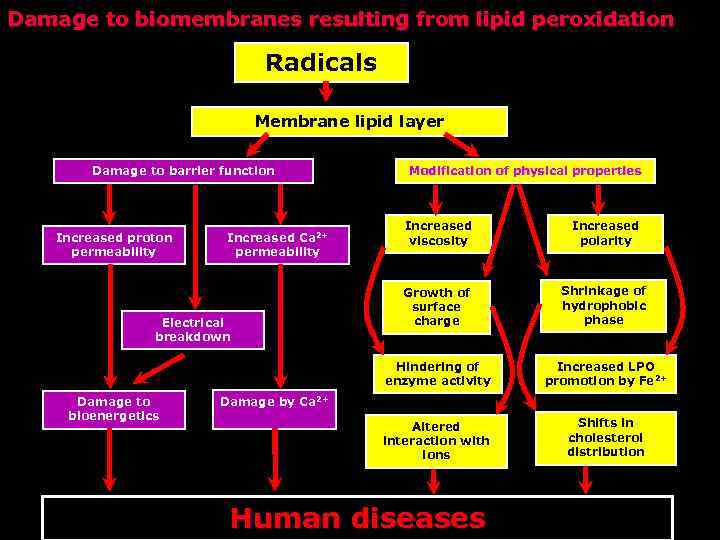 Damage to biomembranes resulting from lipid peroxidation Radicals Membrane lipid layer Damage to barrier function Modification of physical properties Electrical breakdown Damage to bioenergetics Increased polarity Growth of surface charge Shrinkage of hydrophobic phase Increased LPO promotion by Fe 2+ Altered interaction with ions Increased Ca 2+ permeability Increased viscosity Hindering of enzyme activity Increased proton permeability Shifts in cholesterol distribution Damage by Ca 2+ Human diseases
Damage to biomembranes resulting from lipid peroxidation Radicals Membrane lipid layer Damage to barrier function Modification of physical properties Electrical breakdown Damage to bioenergetics Increased polarity Growth of surface charge Shrinkage of hydrophobic phase Increased LPO promotion by Fe 2+ Altered interaction with ions Increased Ca 2+ permeability Increased viscosity Hindering of enzyme activity Increased proton permeability Shifts in cholesterol distribution Damage by Ca 2+ Human diseases
 How we created and measured the membrane potential in mitochondria? Inner mitochondrial membrane generates potential difference (Dj)and p. H Dj difference (Dp. H) between bathing p. H solutions, in the presence of respiration substrates and oxygen. Dm. H+ = RTDln[H+] + z. FDj Upon addition of permeable acid (e. g. acetic acid) Dp. H would decrease and hence Dj would increase. The fluorescence probe was used to measure the membrane potential ( ).
How we created and measured the membrane potential in mitochondria? Inner mitochondrial membrane generates potential difference (Dj)and p. H Dj difference (Dp. H) between bathing p. H solutions, in the presence of respiration substrates and oxygen. Dm. H+ = RTDln[H+] + z. FDj Upon addition of permeable acid (e. g. acetic acid) Dp. H would decrease and hence Dj would increase. The fluorescence probe was used to measure the membrane potential ( ).
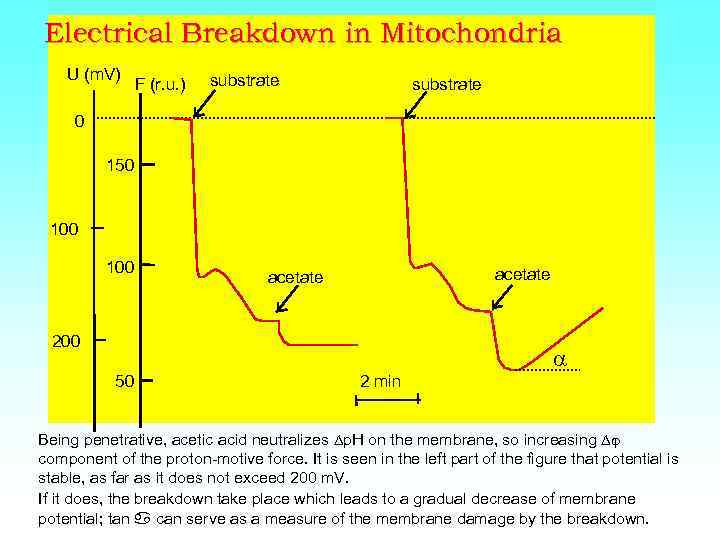 Electrical Breakdown in Mitochondria U (m. V) F (r. u. ) substrate 0 150 100 acetate 200 a 50 2 min Being penetrative, acetic acid neutralizes p. H on the membrane, so increasing component of the proton-motive force. It is seen in the left part of the figure that potential is stable, as far as it does not exceed 200 m. V. If it does, the breakdown take place which leads to a gradual decrease of membrane potential; tan can serve as a measure of the membrane damage by the breakdown.
Electrical Breakdown in Mitochondria U (m. V) F (r. u. ) substrate 0 150 100 acetate 200 a 50 2 min Being penetrative, acetic acid neutralizes p. H on the membrane, so increasing component of the proton-motive force. It is seen in the left part of the figure that potential is stable, as far as it does not exceed 200 m. V. If it does, the breakdown take place which leads to a gradual decrease of membrane potential; tan can serve as a measure of the membrane damage by the breakdown.
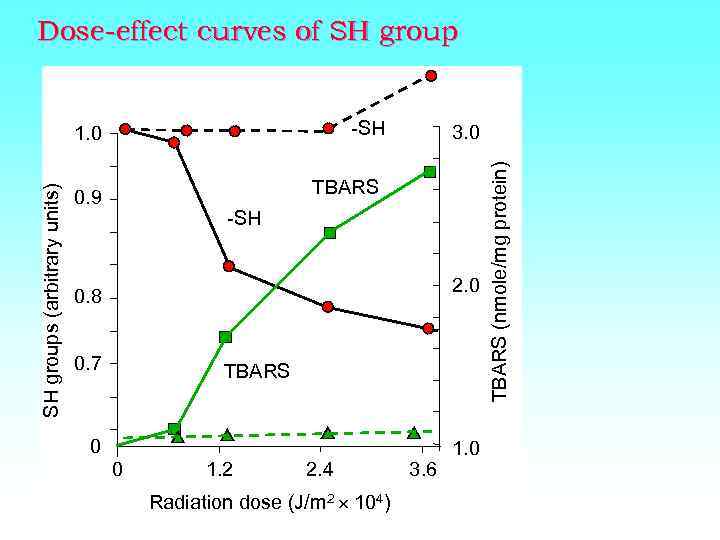 Dose-effect curves of SH group -SH 3. 0 TBARS 0. 9 -SH 2. 0 0. 8 0. 7 TBARS 0 0 1. 2 2. 4 Radiation dose (J/m 2 104) 3. 6 1. 0 TBARS (nmole/mg protein) SH groups (arbitrary units) 1. 0
Dose-effect curves of SH group -SH 3. 0 TBARS 0. 9 -SH 2. 0 0. 8 0. 7 TBARS 0 0 1. 2 2. 4 Radiation dose (J/m 2 104) 3. 6 1. 0 TBARS (nmole/mg protein) SH groups (arbitrary units) 1. 0
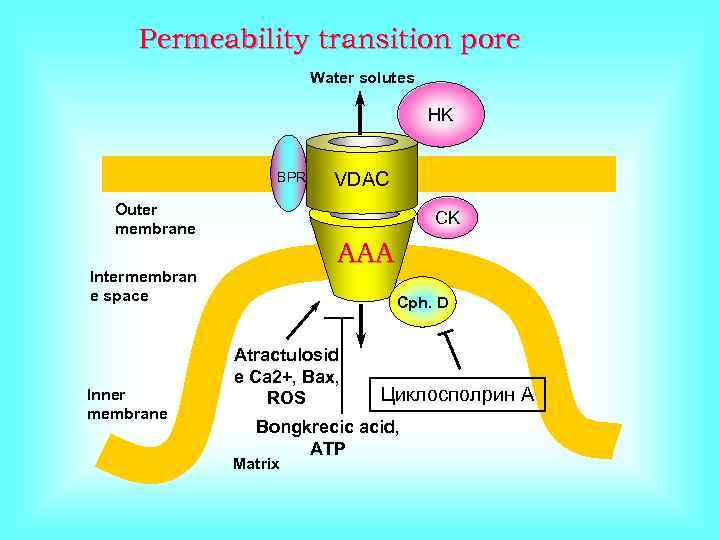 Permeability transition pore Water solutes HK BPR Outer membrane CK ААА Intermembran e space Inner membrane VDAC Cph. D Atractulosid e Ca 2+, Bax, ROS Циклосполрин А Bongkrecic acid, ATP Matrix
Permeability transition pore Water solutes HK BPR Outer membrane CK ААА Intermembran e space Inner membrane VDAC Cph. D Atractulosid e Ca 2+, Bax, ROS Циклосполрин А Bongkrecic acid, ATP Matrix
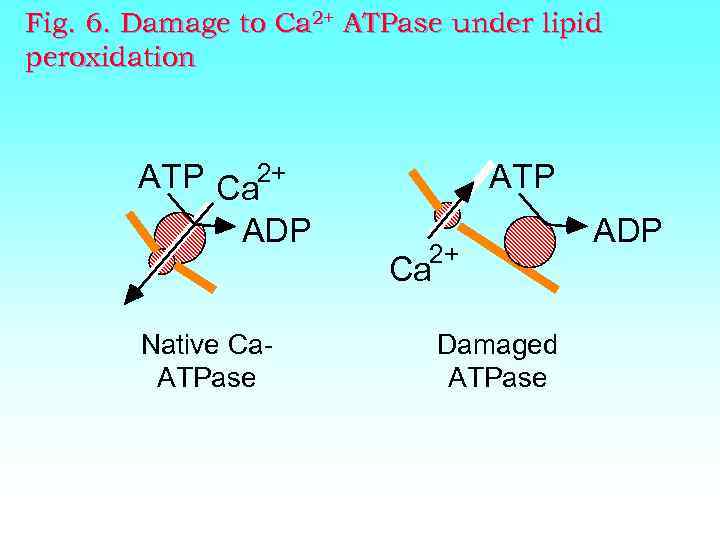 Fig. 6. Damage to Ca 2+ ATPase under lipid peroxidation ATP Ca 2+ ADP ATP 2+ Ca Native Ca. ATPase Damaged ATPase ADP
Fig. 6. Damage to Ca 2+ ATPase under lipid peroxidation ATP Ca 2+ ADP ATP 2+ Ca Native Ca. ATPase Damaged ATPase ADP
 Са-АТФаза снизу (стерео)
Са-АТФаза снизу (стерео)
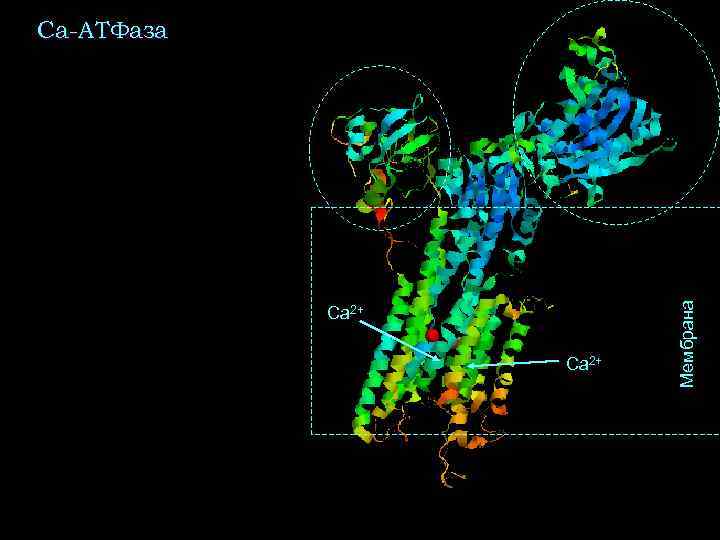 Ca 2+ Мембрана Са-АТФаза
Ca 2+ Мембрана Са-АТФаза
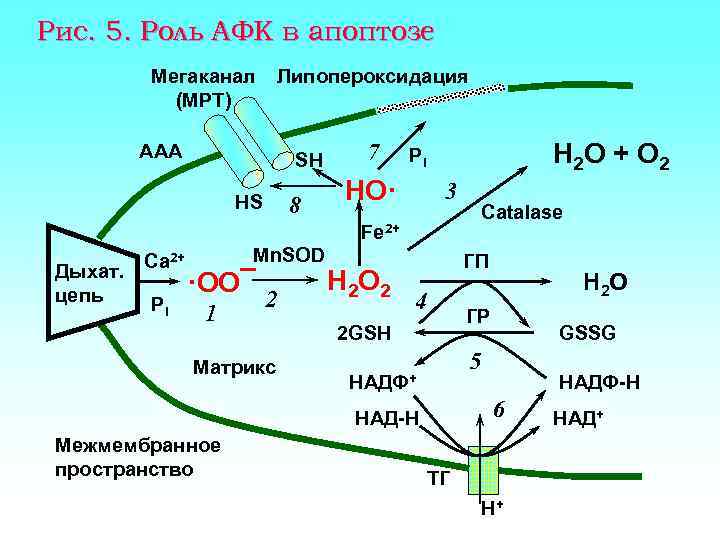 Рис. 5. Роль АФК в апоптозе Мегаканал (MPT) Липопероксидация ААА SH HS 8 7 H 2 O + O 2 Pi HO· 3 Catalase Fe 2+ Дыхат. цепь Ca 2+ Pi Mn. SOD ·OO¯ 1 2 Матрикс H 2 O 2 ГП 4 2 GSH ГР GSSG 5 НАДФ+ НАДФ-H 6 НАД-H Межмембранное пространство H 2 O ТГ H+ НАД+
Рис. 5. Роль АФК в апоптозе Мегаканал (MPT) Липопероксидация ААА SH HS 8 7 H 2 O + O 2 Pi HO· 3 Catalase Fe 2+ Дыхат. цепь Ca 2+ Pi Mn. SOD ·OO¯ 1 2 Матрикс H 2 O 2 ГП 4 2 GSH ГР GSSG 5 НАДФ+ НАДФ-H 6 НАД-H Межмембранное пространство H 2 O ТГ H+ НАД+
 Радикалы, клеточная мембрана и апоптоз
Радикалы, клеточная мембрана и апоптоз
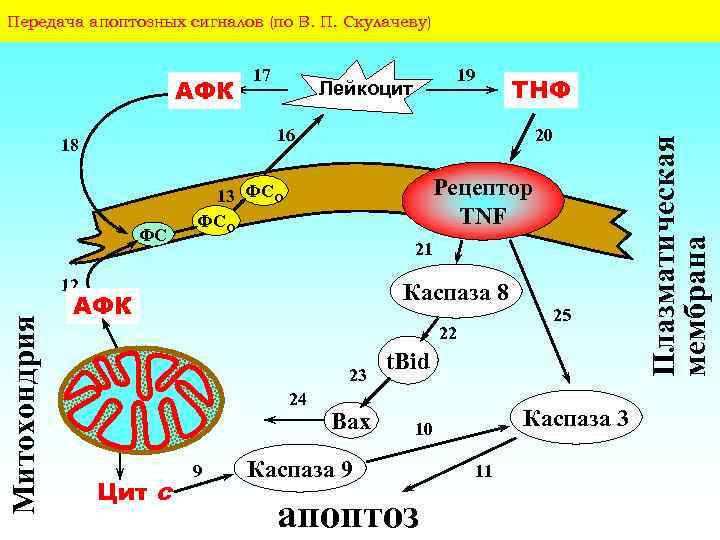 Передача апоптозных сигналов (по В. П. Скулачеву) ТНФ 16 18 ФС 20 Рецептор TNF 13 ФСО 21 12 Митохондрия 19 Лейкоцит Каспаза 8 АФК 22 23 24 Цит c 9 Bax 25 t. Bid Каспаза 3 10 Каспаза 9 апоптоз 11 Плазматическая мембрана АФК 17
Передача апоптозных сигналов (по В. П. Скулачеву) ТНФ 16 18 ФС 20 Рецептор TNF 13 ФСО 21 12 Митохондрия 19 Лейкоцит Каспаза 8 АФК 22 23 24 Цит c 9 Bax 25 t. Bid Каспаза 3 10 Каспаза 9 апоптоз 11 Плазматическая мембрана АФК 17
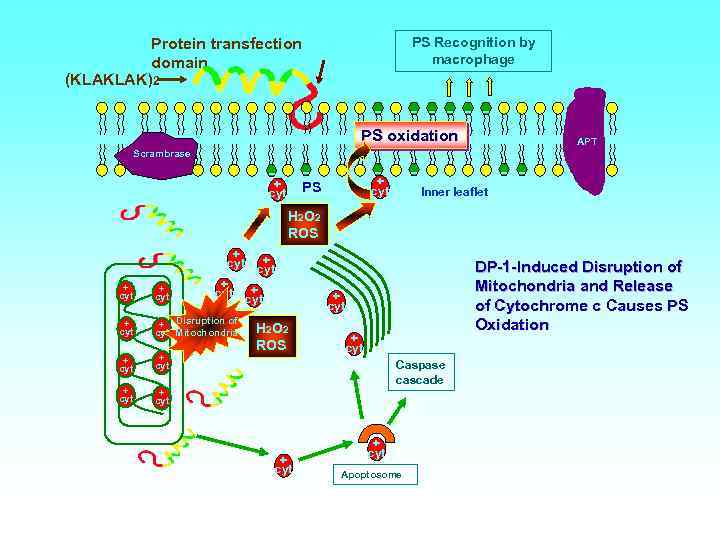 PS Recognition by macrophage Protein transfection domain (KLAKLAK)2 - - - PS oxidation Scrambrase -+ - + PS cyt APT - cyt - Inner leaflet H 2 O 2 ROS + cyt + cyt + Disruption of cyt Mitochondria + cyt DP-1 -Induced Disruption of Mitochondria and Release of Cytochrome c Causes PS Oxidation + cyt H 2 O 2 ROS + cyt Caspase cascade + cyt Apoptosome
PS Recognition by macrophage Protein transfection domain (KLAKLAK)2 - - - PS oxidation Scrambrase -+ - + PS cyt APT - cyt - Inner leaflet H 2 O 2 ROS + cyt + cyt + Disruption of cyt Mitochondria + cyt DP-1 -Induced Disruption of Mitochondria and Release of Cytochrome c Causes PS Oxidation + cyt H 2 O 2 ROS + cyt Caspase cascade + cyt Apoptosome
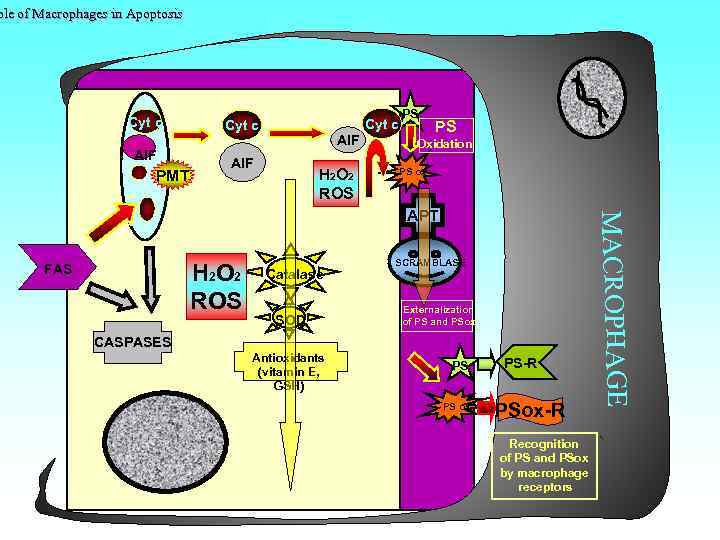 ole of Macrophages in Apoptosis Cyt c AIF PMT Cyt c AIF H 2 O 2 ROS PS PS Oxidation PS ox H 2 O 2 ROS FAS Catalase SOD SCRAMBLASE Externalization of PS and PSox CASPASES Antioxidants (vitamin E, GSH) PS PS ox PS-R PSox-R Recognition of PS and PSox by macrophage receptors MACROPHAGE APT
ole of Macrophages in Apoptosis Cyt c AIF PMT Cyt c AIF H 2 O 2 ROS PS PS Oxidation PS ox H 2 O 2 ROS FAS Catalase SOD SCRAMBLASE Externalization of PS and PSox CASPASES Antioxidants (vitamin E, GSH) PS PS ox PS-R PSox-R Recognition of PS and PSox by macrophage receptors MACROPHAGE APT


