Раздел 1. Теоретические основы химии Тема: «Основные





























lekciya_neorganicheskaya_himiya_1.ppt
- Размер: 758.0 Кб
- Автор:
- Количество слайдов: 31
Описание презентации Раздел 1. Теоретические основы химии Тема: «Основные по слайдам
 Раздел 1. Теоретические основы химии Тема: «Основные понятия и законы химии. Периодический закон и периодическая система элементов Д. И. Менделеева. Теория строения веществ. »
Раздел 1. Теоретические основы химии Тема: «Основные понятия и законы химии. Периодический закон и периодическая система элементов Д. И. Менделеева. Теория строения веществ. »
 План: 1. Введение. 2. Основные понятия и законы химии. 3. Периодический закон и периодическая система химических элементов Д. И. Менделеева. 4. Теория строения атомов. 5. Виды химической связи.
План: 1. Введение. 2. Основные понятия и законы химии. 3. Периодический закон и периодическая система химических элементов Д. И. Менделеева. 4. Теория строения атомов. 5. Виды химической связи.
 1. Введение Окружающий человека мир материален и, несмотря на все богатство его проявлений, в настоящее время выделяют всего лишь две формы существования материи: вещество и поле , которые проникают друг в друга и при определенных условиях могут превращаться друг в друга. Вот что писал в 1870 г. Д. И. Менделеев в своей книге “Основы химии” о предмете химии: “Ближайший предмет химии составляет изучение однородных веществ, из сложения которых составлены все тела мира, превращений их друг в друга и явлений, сопровождающих такие превращения.
1. Введение Окружающий человека мир материален и, несмотря на все богатство его проявлений, в настоящее время выделяют всего лишь две формы существования материи: вещество и поле , которые проникают друг в друга и при определенных условиях могут превращаться друг в друга. Вот что писал в 1870 г. Д. И. Менделеев в своей книге “Основы химии” о предмете химии: “Ближайший предмет химии составляет изучение однородных веществ, из сложения которых составлены все тела мира, превращений их друг в друга и явлений, сопровождающих такие превращения.
 Введение Химия, как и всякая наука, есть в одно время и средство, и цель. Она есть средство для достижения тех или других практических, в общем смысле этого слова, стремлений. Так, при содействии ее облегчается обладание веществом в разных его видах, она дает новую возможность пользоваться силами природы, указывает способы получения и свойства множества веществ и т. д. В этом смысле химия близка к делам заводчика и мастера, роль ее служебная, она составляет средство для достижения блага. К этому, уже почтенному, свойству присоединяется, однако, другое: в химии, как и в каждой выработанной науке, есть ряд стремлений высших, не ограничиваемых временными и частными целями (хотя и приводящих к ним и нисколько им не противоречащих). Стараясь познать бесконечное, наука сама конца не имеет и, будучи всемирной, в действительности неизбежно приобретает народный характер. . »
Введение Химия, как и всякая наука, есть в одно время и средство, и цель. Она есть средство для достижения тех или других практических, в общем смысле этого слова, стремлений. Так, при содействии ее облегчается обладание веществом в разных его видах, она дает новую возможность пользоваться силами природы, указывает способы получения и свойства множества веществ и т. д. В этом смысле химия близка к делам заводчика и мастера, роль ее служебная, она составляет средство для достижения блага. К этому, уже почтенному, свойству присоединяется, однако, другое: в химии, как и в каждой выработанной науке, есть ряд стремлений высших, не ограничиваемых временными и частными целями (хотя и приводящих к ним и нисколько им не противоречащих). Стараясь познать бесконечное, наука сама конца не имеет и, будучи всемирной, в действительности неизбежно приобретает народный характер. . »
 2. Основные понятия и законы химии. 1. Все вещества (химические соединения) Вселенной состоят из молекул, а молекулы из атомов химических элементов таблицы Д. И. Менделеева. Атомы в свою очередь состоят из более мелких частиц: протонов, нейтронов и электронов. В настоящее время известно 105 химических элементов, которые отличаются друг от друга химическими свойствами и количеством входящих в них указанных частиц. 2. При определенных условиях молекулы веществ способны превращаться друг в друга, однако атомы элементов при этом не превращаются друг в друга. Элементы способны превращаться друг в друга только в ядерных реакциях. 3. При любых химических превращениях всегда соблюдаются законы сохранения массы, энергии и заряда.
2. Основные понятия и законы химии. 1. Все вещества (химические соединения) Вселенной состоят из молекул, а молекулы из атомов химических элементов таблицы Д. И. Менделеева. Атомы в свою очередь состоят из более мелких частиц: протонов, нейтронов и электронов. В настоящее время известно 105 химических элементов, которые отличаются друг от друга химическими свойствами и количеством входящих в них указанных частиц. 2. При определенных условиях молекулы веществ способны превращаться друг в друга, однако атомы элементов при этом не превращаются друг в друга. Элементы способны превращаться друг в друга только в ядерных реакциях. 3. При любых химических превращениях всегда соблюдаются законы сохранения массы, энергии и заряда.
 Основные понятия и законы химии. 4. При протекании любой химической реакции массы реагирующих веществ и продуктов реакции всегда находятся в пропорциональных количествах, соответствующих их стехиометрическим коэффициентам. 5. В природе не существует веществ, обладающих одинаковым набором свойств. Каждое вещество уникально. 6. Свойства веществ зависят от качественного и количественного состава их молекул и от их строения.
Основные понятия и законы химии. 4. При протекании любой химической реакции массы реагирующих веществ и продуктов реакции всегда находятся в пропорциональных количествах, соответствующих их стехиометрическим коэффициентам. 5. В природе не существует веществ, обладающих одинаковым набором свойств. Каждое вещество уникально. 6. Свойства веществ зависят от качественного и количественного состава их молекул и от их строения.
 3. Периодический закон Д. И. Менделеева. «свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от величины атомных весов элементов»
3. Периодический закон Д. И. Менделеева. «свойства простых веществ, а также свойства и формы соединений элементов находятся в периодической зависимости от величины атомных весов элементов»
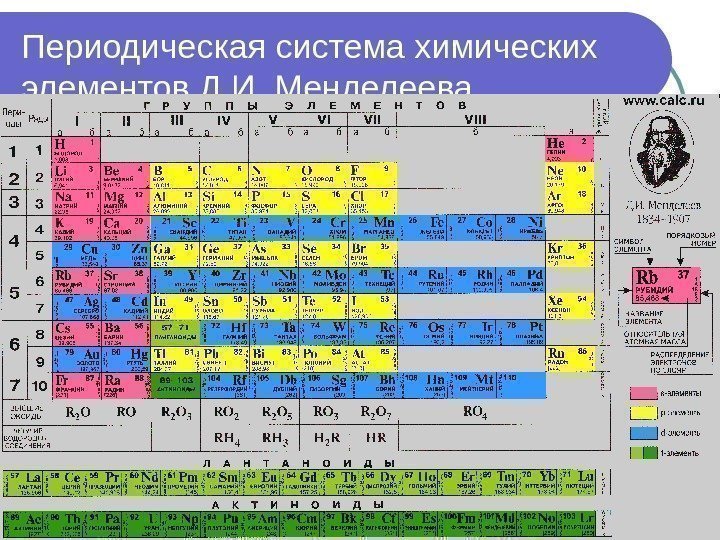
 Периодическая система химических элементов Д. И. Менделеева это наглядное графическое изображение периодического закона. Химический элемент – это вид атомов, характеризующихся определённым зарядом ядра равным порядковому номеру в периодической системе.
Периодическая система химических элементов Д. И. Менделеева это наглядное графическое изображение периодического закона. Химический элемент – это вид атомов, характеризующихся определённым зарядом ядра равным порядковому номеру в периодической системе.
 В структуре таблицы (системы) выделяют периоды, группы и подгруппы. Периодом называют горизонтальную совокупность элементов, расположенных в порядке возрастания заряда ядра. Группой называют совокупность элементов, расположенных в таблице вертикально в порядке возрастания заряда ядра. В периодической системе находится 8 групп. Каждая группа состоит из главной и побочной подгрупп.
В структуре таблицы (системы) выделяют периоды, группы и подгруппы. Периодом называют горизонтальную совокупность элементов, расположенных в порядке возрастания заряда ядра. Группой называют совокупность элементов, расположенных в таблице вертикально в порядке возрастания заряда ядра. В периодической системе находится 8 групп. Каждая группа состоит из главной и побочной подгрупп.
 Периодическая система химических элементов Д. И. Менделеева
Периодическая система химических элементов Д. И. Менделеева
 Характер изменения некоторых свойств элементов Энергия ионизации –это энергия, затраченная на отрыводного электрона от нейтрального атома, в периоде возрастает с ростом заряда ядра, в главных и третьей побочной подгруппах – убывает сверху вниз в связи с появлением нового энергетического уровня. В остальных побочных подгруппах энергия ионизации возрастает с ростом заряда ядра. Сродством к электрону (Е) – называют энергию, которая выделяется присоединении дополнительного электрона к атому, иону или молекуле. Максимальным сродством к электрону обладают атомы галогенов. Электроотрицательность (ЭО) — относительная характеристика способности атома, притягивать электронную пару. Относительная электроотрицательность в периоде возрастает и уменьшается в подгруппе с ростом заряда ядра.
Характер изменения некоторых свойств элементов Энергия ионизации –это энергия, затраченная на отрыводного электрона от нейтрального атома, в периоде возрастает с ростом заряда ядра, в главных и третьей побочной подгруппах – убывает сверху вниз в связи с появлением нового энергетического уровня. В остальных побочных подгруппах энергия ионизации возрастает с ростом заряда ядра. Сродством к электрону (Е) – называют энергию, которая выделяется присоединении дополнительного электрона к атому, иону или молекуле. Максимальным сродством к электрону обладают атомы галогенов. Электроотрицательность (ЭО) — относительная характеристика способности атома, притягивать электронную пару. Относительная электроотрицательность в периоде возрастает и уменьшается в подгруппе с ростом заряда ядра.
 3. Теория строения атомов. Атом любого элемента состоит из положительно заряженного ядра и отрицательно заряженных электронов, в целом же атом – система электронейтральная. Атомное ядро состоит из: протонов (заряд +1, массовое число 1) и нейтронов (заряд 0, массовое число 1). Заряд ядра, равный порядковому номеру элемента в таблице Д. И. Менделеева, совпадает с числом протонов: массовое число ядра равно суммарному количеству протонов и нейтронов. У одного элемента возможно существование атомов с различным массовым числом ядер – изотопов, т. е. атомов с различным числом нейтронов и одинаковым числом протонов.
3. Теория строения атомов. Атом любого элемента состоит из положительно заряженного ядра и отрицательно заряженных электронов, в целом же атом – система электронейтральная. Атомное ядро состоит из: протонов (заряд +1, массовое число 1) и нейтронов (заряд 0, массовое число 1). Заряд ядра, равный порядковому номеру элемента в таблице Д. И. Менделеева, совпадает с числом протонов: массовое число ядра равно суммарному количеству протонов и нейтронов. У одного элемента возможно существование атомов с различным массовым числом ядер – изотопов, т. е. атомов с различным числом нейтронов и одинаковым числом протонов.
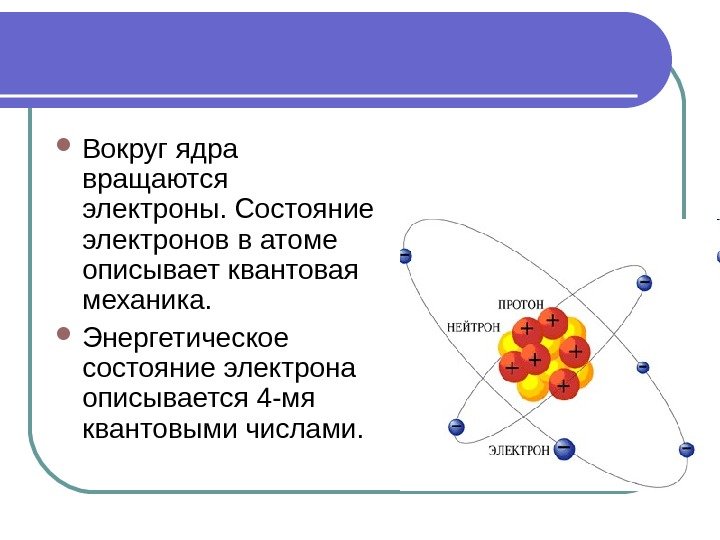
 Вокруг ядра вращаются электроны. Состояние электронов в атоме описывает квантовая механика. Энергетическое состояние электрона описывается 4 -мя квантовыми числами.
Вокруг ядра вращаются электроны. Состояние электронов в атоме описывает квантовая механика. Энергетическое состояние электрона описывается 4 -мя квантовыми числами.
 n — главное квантовое число определяет энергию АО и номер энергетического уровня, на котором находится электрон и может принимать значения от единицы до бесконечности. Указывает отдалённость энергетического уровня от ядра, оно принимает целое положительное значение. Число энергетических уровней равно № периода. Количество электронов на последнем энергетическом уровне считают по формуле: N=2 n
n — главное квантовое число определяет энергию АО и номер энергетического уровня, на котором находится электрон и может принимать значения от единицы до бесконечности. Указывает отдалённость энергетического уровня от ядра, оно принимает целое положительное значение. Число энергетических уровней равно № периода. Количество электронов на последнем энергетическом уровне считают по формуле: N=2 n
 Орбитальное квантовое число – l определяет форму АО и энергетический подуровень и может принимать значения от нуля до ( n — 1). Например: n=2, l = 0, 1 ; n= 3 , l = 0, 1 , 2. l = 0, то электрон находится на s -подуровне; l = 1 , p -подуровень; l = 2 , d -подуровень; l = 3 , f — подуровень.
Орбитальное квантовое число – l определяет форму АО и энергетический подуровень и может принимать значения от нуля до ( n — 1). Например: n=2, l = 0, 1 ; n= 3 , l = 0, 1 , 2. l = 0, то электрон находится на s -подуровне; l = 1 , p -подуровень; l = 2 , d -подуровень; l = 3 , f — подуровень.
 Магнитное квантовое число – m l ориентацию данной АО относительно направления магнитного поля и может принимать значения от – l … 0…+ l Соответственно: Для s -подуровня имеется одна АО Для p- подуровня – три АО Для d -подуровня – пять АО Для f -подуровня – семь АО
Магнитное квантовое число – m l ориентацию данной АО относительно направления магнитного поля и может принимать значения от – l … 0…+ l Соответственно: Для s -подуровня имеется одна АО Для p- подуровня – три АО Для d -подуровня – пять АО Для f -подуровня – семь АО
 Спиновое квантовое число- m s. характеризует вращение электрона вокруг своей оси. Спиновое квантовое число может принимать всего два значения: m s = 1/2, -1/2, в зависимости от того параллельно или нет магнитному полю ориентирован спин электрона.
Спиновое квантовое число- m s. характеризует вращение электрона вокруг своей оси. Спиновое квантовое число может принимать всего два значения: m s = 1/2, -1/2, в зависимости от того параллельно или нет магнитному полю ориентирован спин электрона.
 Построение электронных формул атомов хим. Элементов базируется на 3 основных положениях принцип Паули согласно которому в атоме не может быть двух электронов, у которых все четыре квантовых числа одинаковые. Основным следствием этого принципа является то, что на одной АО не может находиться более двух электронов. Состояние электронов в атоме должно отличаться значением хотя бы одного квантового числа. При переходах электронов с одной орбиты на другую атом поглощает или излучает энергию.
Построение электронных формул атомов хим. Элементов базируется на 3 основных положениях принцип Паули согласно которому в атоме не может быть двух электронов, у которых все четыре квантовых числа одинаковые. Основным следствием этого принципа является то, что на одной АО не может находиться более двух электронов. Состояние электронов в атоме должно отличаться значением хотя бы одного квантового числа. При переходах электронов с одной орбиты на другую атом поглощает или излучает энергию.
 правило Хунда устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально. S=1/2+1/2 =3/2 S=1/2+1/2 -1/2 =1/2 – не верно
правило Хунда устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально. S=1/2+1/2 =3/2 S=1/2+1/2 -1/2 =1/2 – не верно
 Принцип наименьшей энергии Первыми заполняются орбитали с наименьшей энергией Шкала энергии 1 s ® 2 p ® 3 s ® 3 p ® 4 s ® 3 d ® 4 p ® 5 s ® 4 d ® 5 p ® 6 s ® …
Принцип наименьшей энергии Первыми заполняются орбитали с наименьшей энергией Шкала энергии 1 s ® 2 p ® 3 s ® 3 p ® 4 s ® 3 d ® 4 p ® 5 s ® 4 d ® 5 p ® 6 s ® …
 Электронная конфигурация элементов Принадлежность элемента к электронному семейству определяется характером заполнения энергетических подуровней: s- элементы – заполнение внешнего s — подуровня при наличии на предвнешнем уровне двух или восьми электронов, например: Li 1 s 2 2 s 1 р- элементы – заполнение внешнего p- подуровня, например: F 1 s 2 2 p 5 d- элементы – заполнение предвнешнего d- подуровня, например: V 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d
Электронная конфигурация элементов Принадлежность элемента к электронному семейству определяется характером заполнения энергетических подуровней: s- элементы – заполнение внешнего s — подуровня при наличии на предвнешнем уровне двух или восьми электронов, например: Li 1 s 2 2 s 1 р- элементы – заполнение внешнего p- подуровня, например: F 1 s 2 2 p 5 d- элементы – заполнение предвнешнего d- подуровня, например: V 1 s 2 2 p 6 3 s 2 3 p 6 4 s 2 3 d
 4. Виды химической связи Атомы металлов способны отдавать электроны, атомы неметаллов- принимать. Образование химической связи объясняется стремлением атомов отдать, получить или разделить с другими атомами электроны, чтобы приобрести устойчивую конфигурацию благородных газов( n. S 2 n. P 6 )
4. Виды химической связи Атомы металлов способны отдавать электроны, атомы неметаллов- принимать. Образование химической связи объясняется стремлением атомов отдать, получить или разделить с другими атомами электроны, чтобы приобрести устойчивую конфигурацию благородных газов( n. S 2 n. P 6 )
 Выделяют следующие типы хим. связи: Ионная Ковалентная(полярная и не полярная) Водородная Металлическая
Выделяют следующие типы хим. связи: Ионная Ковалентная(полярная и не полярная) Водородная Металлическая
 Ионная связь Образуется между атомами элементов металла с неметаллом. Na. + . Cl: = Na + Cl — . .
Ионная связь Образуется между атомами элементов металла с неметаллом. Na. + . Cl: = Na + Cl — . .
 Ковалентная связь Образуется между атомами элементов неметаллов. CI 2 – каждый из атомов хлора делится одним из своих внешних электронов. Происходит перекрывание атомных орбиталей, общая пара электронов образует ковалентную связь. Если электроотрицательность атомов(способность атомов притягивать к себе электроны) одинаковая, образуется ковалентная неполярная связь. ( H 2 , O 2 , N 2 и т. д. )
Ковалентная связь Образуется между атомами элементов неметаллов. CI 2 – каждый из атомов хлора делится одним из своих внешних электронов. Происходит перекрывание атомных орбиталей, общая пара электронов образует ковалентную связь. Если электроотрицательность атомов(способность атомов притягивать к себе электроны) одинаковая, образуется ковалентная неполярная связь. ( H 2 , O 2 , N 2 и т. д. )
 Ковалентная полярная связь Возникает между атомами элементов неметаллов с разной электроотрицательностью. Самый электроотрицательный элемент – F. Примеры: H 2 O, NO 2 , HCl и т. д. F 2 O – фторид кислорода
Ковалентная полярная связь Возникает между атомами элементов неметаллов с разной электроотрицательностью. Самый электроотрицательный элемент – F. Примеры: H 2 O, NO 2 , HCl и т. д. F 2 O – фторид кислорода
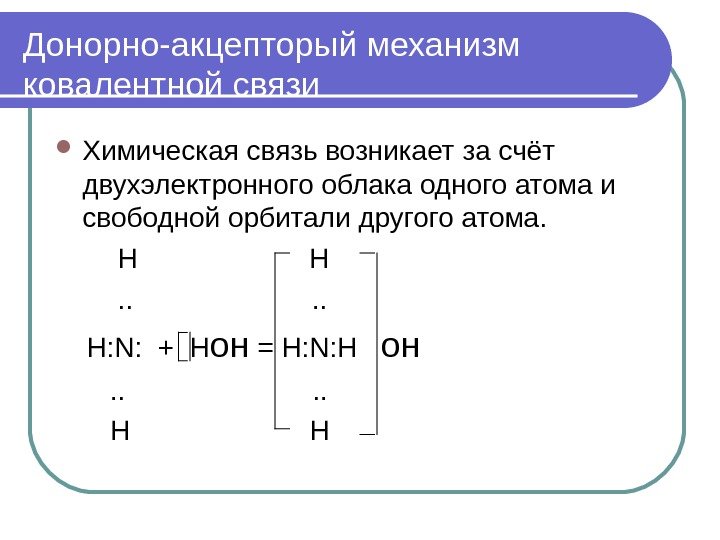
 Донорно-акцепторый механизм ковалентной связи Химическая связь возникает за счёт двухэлектронного облака одного атома и свободной орбитали другого атома. Н H . . H: N: + H он = H: N: H он . . H
Донорно-акцепторый механизм ковалентной связи Химическая связь возникает за счёт двухэлектронного облака одного атома и свободной орбитали другого атома. Н H . . H: N: + H он = H: N: H он . . H
 Водородная связь(межмолекулярная) Возникает между молекулами в состав которых входит водород и сильно электроотрицательный элемент ( F, O, N, реже Cl, S ).
Водородная связь(межмолекулярная) Возникает между молекулами в состав которых входит водород и сильно электроотрицательный элемент ( F, O, N, реже Cl, S ).
 Металлическая связь В твердом состоянии металлы отличаются от всех остальных веществ своими характерными свойствами — очень высокими теплопроводностью и электропроводностью, почти полной непрозрачностью и высокой отражательной способностью по отношению к видимому свету благодаря так называемому металлическому блеску.
Металлическая связь В твердом состоянии металлы отличаются от всех остальных веществ своими характерными свойствами — очень высокими теплопроводностью и электропроводностью, почти полной непрозрачностью и высокой отражательной способностью по отношению к видимому свету благодаря так называемому металлическому блеску.
 Металлическая связь Эти свойства обусловлены металлической связью. У металлов имеется избыток орбиталей и недостаток электронов. Валентные электроны слабо удерживаются ядром и электроны могут свободно перемещаться по свободным орбиталям(по всему кристаллу).
Металлическая связь Эти свойства обусловлены металлической связью. У металлов имеется избыток орбиталей и недостаток электронов. Валентные электроны слабо удерживаются ядром и электроны могут свободно перемещаться по свободным орбиталям(по всему кристаллу).
 Задание: Написать электронную конфигурацию: Са, М n, CI. Определить типы химических связей: С a. CI 2 ; Br 2 ; Al ; H 2 O.
Задание: Написать электронную конфигурацию: Са, М n, CI. Определить типы химических связей: С a. CI 2 ; Br 2 ; Al ; H 2 O.

