растворы.pptx
- Количество слайдов: 22

Раствор – это гомогенная система переменного состава, образованная двумя или более компонентами. физиологические жидкости: кровь, лимфа, желудочный сок, кишечный сок, внутриклеточные соки, слюна, желчь, моча. Растворенными веществами в них будут: белки, пептиды, аминокислоты, углеводы, липиды; ионы Na+, K+, Ca 2+, Mg 2+, Cl –, HCO 3 –, H 2 PO 4 –; газы О 2, N 2, CO 2. Растворитель – вода.

Антагонизм ионов – способность ионов растворов организма ослаблять действие друга, действовать в противоположном направлении. Синергизм ионов – способность одного иона усиливать действие другого. Вода – как растворитель. В. И. Слесарев «Основы химии живого» стр. 125 -134. Термодинамика растворения. В. И. Слесарев «Основы химии живого» стр. 134 -135

Способы выражения концентрации растворов 1. Массовая доля (х) (x) = 100% 2. Молярная концентрация раствора с (х)= [моль/л], где n(х)=

3. Молярная концентрация эквивалента с( x) c ( x) = где n ( x) = [моль/л], , а М( x) = М(x) Число эквивалентности z равно для: а) кислот – основности кислоты H 2 SO 4 z = 2. б) оснований – кислотности основания Aℓ(OH)3 z = 3. в) солей – произведению степени окисления (с. о. ) металла на число его атомов в молекуле Fe 2(SO 4)3 z = 2 3 = 6. г) окислителей – числу присоединенных электронов Mn+7 + 5ē → Mn+2 z = 5 д) восстановителей – числу отданных электронов Fe+2 – 1ē → Fe+3 z = 1
![4. Моляльная концентрация b(x) = = [моль/кг] 5. Молярная доля (xi) = 4. Моляльная концентрация b(x) = = [моль/кг] 5. Молярная доля (xi) =](https://present5.com/presentation/95372064_19250023/image-5.jpg)
4. Моляльная концентрация b(x) = = [моль/кг] 5. Молярная доля (xi) =

Коллигативные свойства растворов Коллигативные свойства – это свойства растворов, которые не зависят от природы растворенного вещества и определяются только числом частиц растворенного вещества, его концентрацией. qдавление насыщенного пара над раствором qповышение температуры кипения qпонижение температуры замерзания qосмос, осмотическое давление

Давление насыщенного пара над раствором Пар, находящийся в равновесии с жидкостью, называют насыщенным. Давление такого пара называют давлением насыщенного пара чистого растворителя. Ро Закон Рауля Р = Р 0 0 0 + (X) = 1

Повышение температуры кипения и понижение температуры замерзания Следствие из закона Рауля ΔТк= Кэ · b(x) ΔТз= Кк · b(x) Кэ и Кк , К кг/моль – эбулиоскопическая и криоскопическая константы растворителя, приводятся в справочной литературе. ΔТк и ΔТз - изменение температуры кипения и замерзания b(Х) – моляльная концентрация раствора
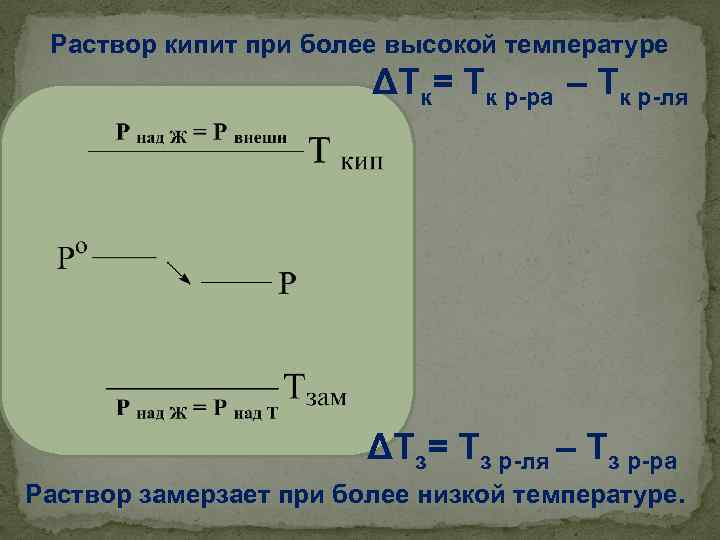
Раствор кипит при более высокой температуре ΔТк= Тк р-ра – Тк р-ля ΔТз= Тз р-ля – Тз р-ра Раствор замерзает при более низкой температуре.

Осмос. Осмотическое давление. Осмос – самопроизвольная диффузия молекул растворителя через полупроницаемую мембрану из растворителя в раствор или из раствора с меньшей концентрацией в раствор с большей концентрацией.

Осмотическое давление – давление, которое нужно приложить к раствору, чтобы осмос прекратился. Уравнение Вант-Гоффа: Росм = c. RT 103 Осмотическое давление крови: 7, 7 -8, 1 атм или 780202, 5 -820732, 5 Па Онкотическое давление – это часть осмотического давления, обусловленного белками.
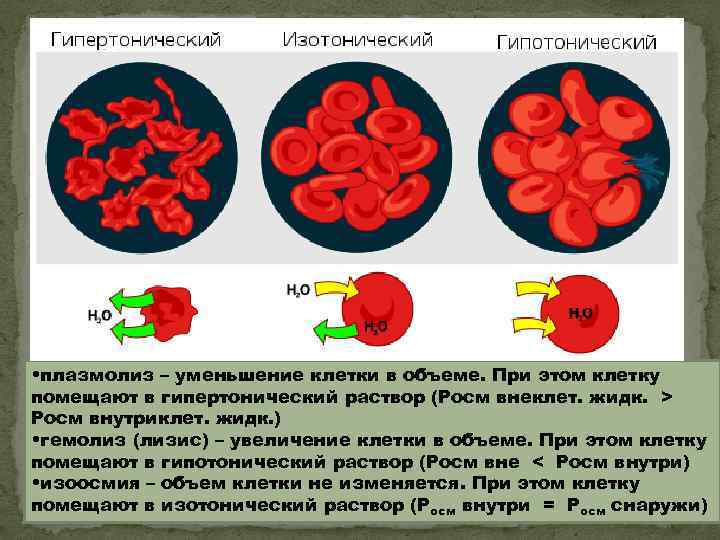
• плазмолиз – уменьшение клетки в объеме. При этом клетку помещают в гипертонический раствор (Росм внеклет. жидк. > Росм внутриклет. жидк. ) • гемолиз (лизис) – увеличение клетки в объеме. При этом клетку помещают в гипотонический раствор (Росм вне < Росм внутри) • изоосмия – объем клетки не изменяется. При этом клетку помещают в изотонический раствор (Росм внутри = Росм снаружи)

Протолитическая теория кислот и оснований 1923 год Бренстед и Лоури Основные положения протолитической теории q. Кислотно-основные реакции осуществляются за счет переноса протона Н+ от кислоты к основанию. q. Реакции, сопровождающиеся переносом Н+, называются протолитическими, а вещества, участвующие в них – протолитами.

q. Кислота – это протолит, который является донором Н+, т. е. способна отдавать протон. Кислота, отдавая протон, превращается в основание, которое называется сопряженным. Кислота ⇄ H+ + сопряженное основание + + Cl – HCl ⇄ H к со q. Основание – это протолит, который является акцептором H+, т. е. способно принимать H+. Основание, присоединив H+, превращается в кислоту, которая называется сопряженной. Основание + H+ ⇄ сопряженная кислота NН 3 + H+ ⇄ NH 4+ о ск

q. Кислота и соответствующее ей сопряженное основание или основание и сопряженная с ним кислота образуют протолитические пары или сопряженные кислотно-основные пары: – ; NН HCl - Cl 3 - NH 4 к со о ск +
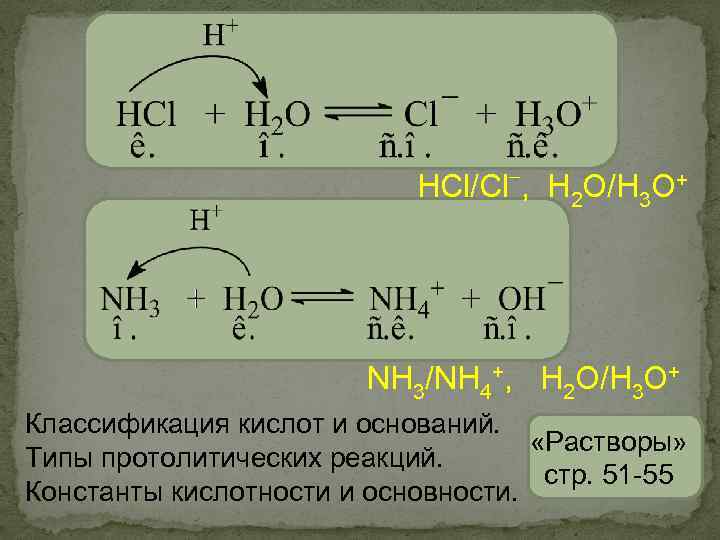
- HCl/Cl , H 2 O/H 3 O+ NH 3/NH 4+, H 2 O/H 3 O+ Классификация кислот и оснований. «Растворы» Типы протолитических реакций. стр. 51 -55 Константы кислотности и основности.

H 2 О ⇄ H+ + ОН – Н 2 О + H+ ⇄ H 3 О+ к со ск Протолиты, способные как отдавать протон, так и принимать протон, т. е. обладающие как протонодонорными, так и протоноакцепторными свойствами, называются амфолиты. Это: H 2 O, спирты, жидкий NH 3, гидрид анионы многоосновных кислот, карбоновые кислоты и т. д. реакция автопротолиза (самоионизации) или кислотно-основного диспропорционирования
![Автопротолиз воды. Ионное произведение воды. Кравн = КН 2 О = [H 3 +] Автопротолиз воды. Ионное произведение воды. Кравн = КН 2 О = [H 3 +]](https://present5.com/presentation/95372064_19250023/image-18.jpg)
Автопротолиз воды. Ионное произведение воды. Кравн = КН 2 О = [H 3 +] [OH–] = К O упрощенно КН 2 О равн. [H 2 2 = 1 10 – 14 O] +] [OH–] = 10 – 14 = [H КН 2 О – ионное произведение воды
![+] = [OH– ] В химически чистой воде [H нейтральная среда. +] < [OH– +] = [OH– ] В химически чистой воде [H нейтральная среда. +] < [OH–](https://present5.com/presentation/95372064_19250023/image-19.jpg)
+] = [OH– ] В химически чистой воде [H нейтральная среда. +] < [OH– ] В растворе может быть [H кислая среда. +] > [OH– ] [H щелочная среда. +] [OH–] = 10 – 14 [H [H+] = ; [OH –] =
![Водородный показатель р. Н = – lg [H+] ⇒ [H+] = 10 –р. Н Водородный показатель р. Н = – lg [H+] ⇒ [H+] = 10 –р. Н](https://present5.com/presentation/95372064_19250023/image-20.jpg)
Водородный показатель р. Н = – lg [H+] ⇒ [H+] = 10 –р. Н В нейтральной среде р. Н = 7 В кислой р. Н < 7 В щелочной р. Н > 7 гидроксильный показатель р. ОН = – lg [ОH– ] ⇒ [ОH– ] = 10 –р. ОН р. Н + р. ОН = 14 р. Н = 14 – р. ОН Ацидоз – смещение р. Н в Алкалоз – смещение р. Н в кислую сторону, р. Н щелочную область, р. Н уменьшается, концентрация растет, концентрация ионов водорода растет. водорода уменьшается.
![Формулы расчёта р. Н = – lg [H+] qдля сильных кислот: [H+] = С(1/z Формулы расчёта р. Н = – lg [H+] qдля сильных кислот: [H+] = С(1/z](https://present5.com/presentation/95372064_19250023/image-21.jpg)
Формулы расчёта р. Н = – lg [H+] qдля сильных кислот: [H+] = С(1/z кислоты) qдля сильных оснований: [ОH– ] = С(1/z основания) [H+] = qдля слабых кислот: [H+] = qдля слабых оснований: [OH–] = [H+] =

Совмещённые и изолированные протолитические равновесия. ИЗОЛИРОВАННЫЕ - несколько одновременно существующих равновесий независимы друг от друга Если же изменение равновесия в одном из них приводит к изменению равновесия в другом, то говорят о СОВМЕЩЁННЫХ (сопряжённых, конкурирующих) равновесиях.
растворы.pptx