2_перв_втор структура.ppt
- Количество слайдов: 52

ПРОСТРАНСТВЕННАЯ ОРГАНИЗАЦИЯ БЕЛКА

ФУНКЦИИ БЕЛКОВ В КЛЕТКЕ И ОРГАНИЗМЕ

ПЕРВИЧНАЯ СТРУКТУРА БЕЛКА
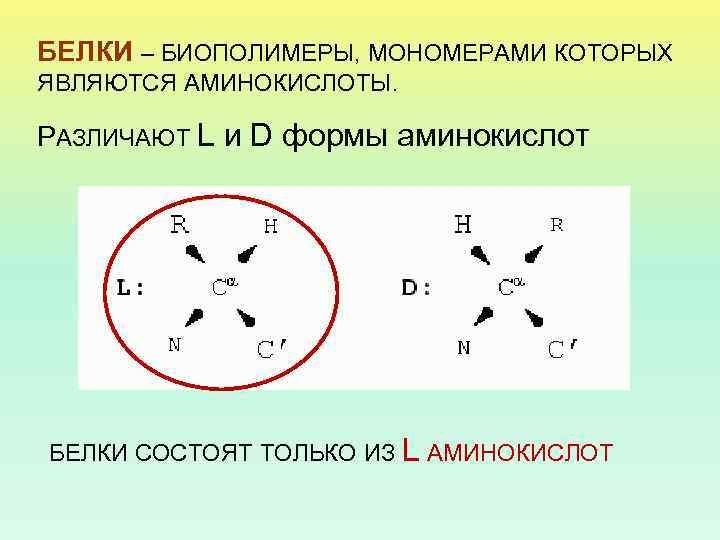
БЕЛКИ – БИОПОЛИМЕРЫ, МОНОМЕРАМИ КОТОРЫХ ЯВЛЯЮТСЯ АМИНОКИСЛОТЫ. РАЗЛИЧАЮТ L и D формы аминокислот БЕЛКИ СОСТОЯТ ТОЛЬКО ИЗ L АМИНОКИСЛОТ
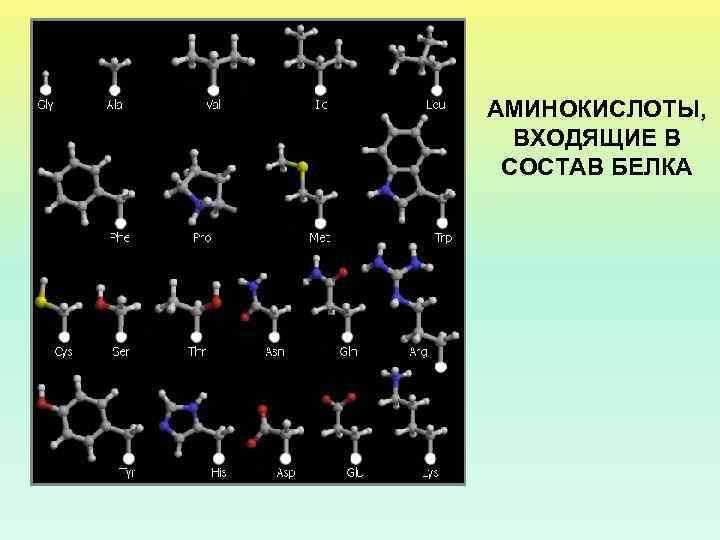
АМИНОКИСЛОТЫ, ВХОДЯЩИЕ В СОСТАВ БЕЛКА
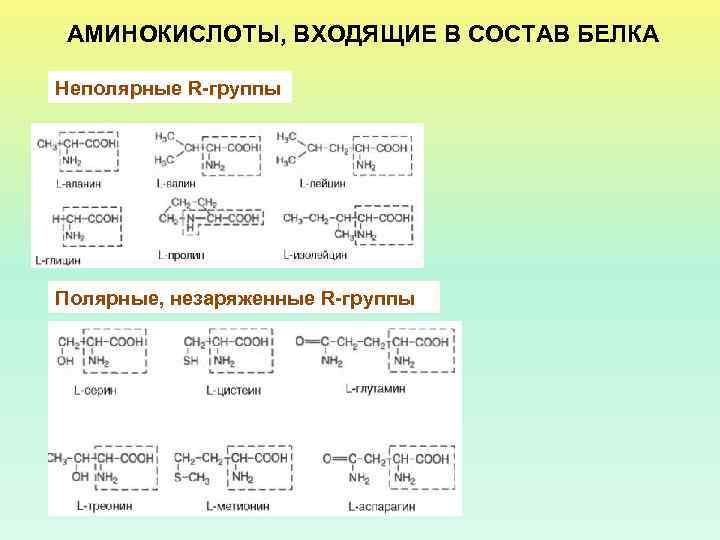
АМИНОКИСЛОТЫ, ВХОДЯЩИЕ В СОСТАВ БЕЛКА Неполярные R-группы Полярные, незаряженные R-группы
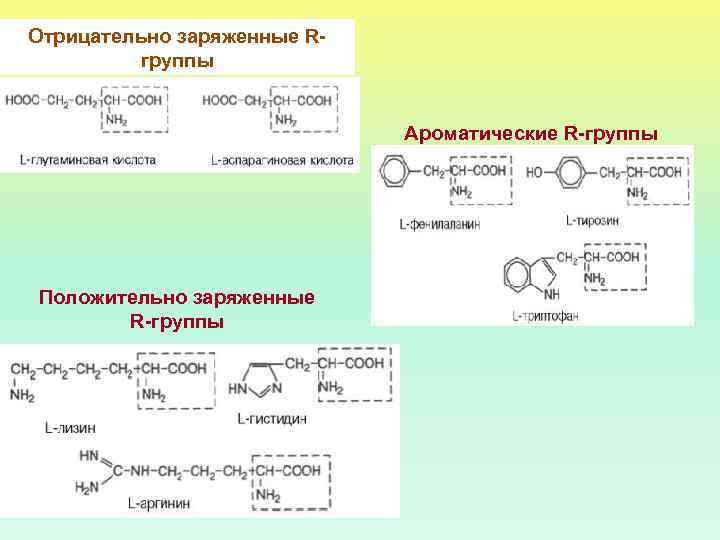
Отрицательно заряженные Rгруппы Ароматические R-группы Положительно заряженные R-группы
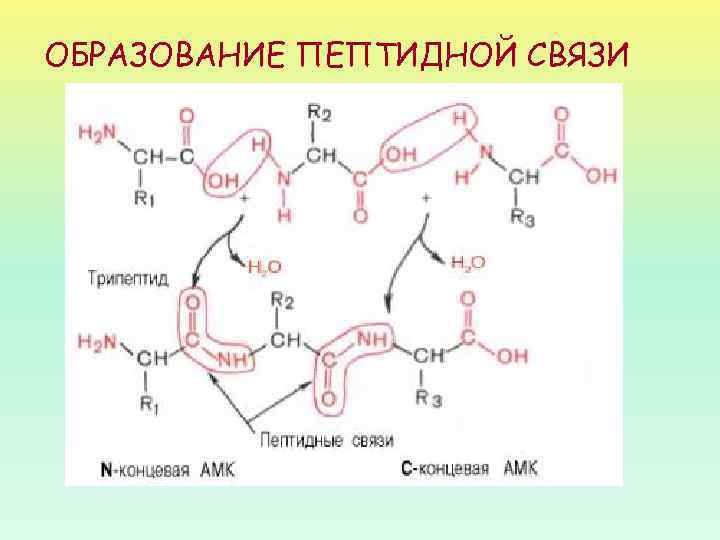
ОБРАЗОВАНИЕ ПЕПТИДНОЙ СВЯЗИ
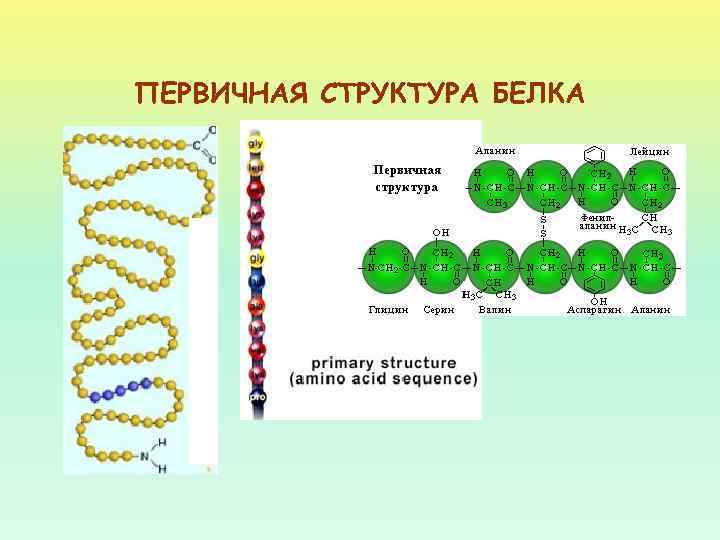
ПЕРВИЧНАЯ СТРУКТУРА БЕЛКА
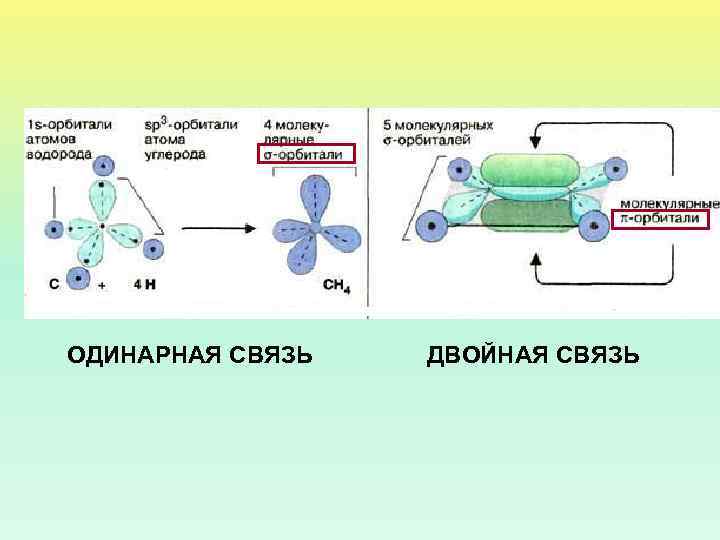
ОДИНАРНАЯ СВЯЗЬ ДВОЙНАЯ СВЯЗЬ
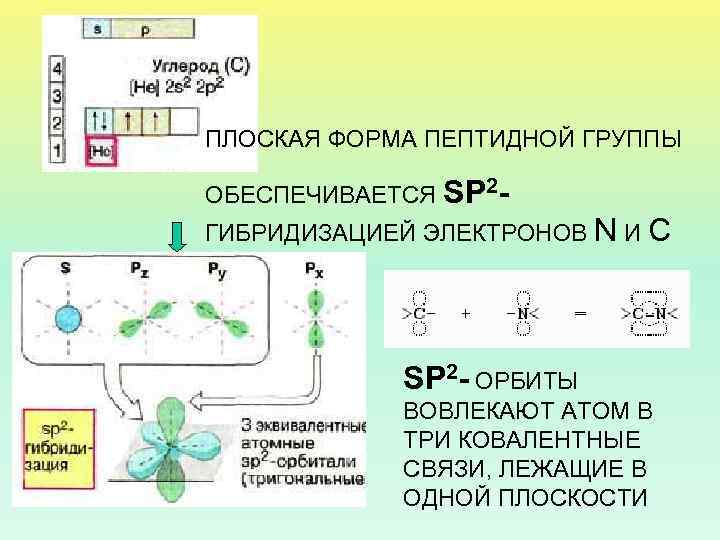
ПЛОСКАЯ ФОРМА ПЕПТИДНОЙ ГРУППЫ ОБЕСПЕЧИВАЕТСЯ SP 2 ГИБРИДИЗАЦИЕЙ ЭЛЕКТРОНОВ N И C SP 2 - ОРБИТЫ ВОВЛЕКАЮТ АТОМ В ТРИ КОВАЛЕНТНЫЕ СВЯЗИ, ЛЕЖАЩИЕ В ОДНОЙ ПЛОСКОСТИ
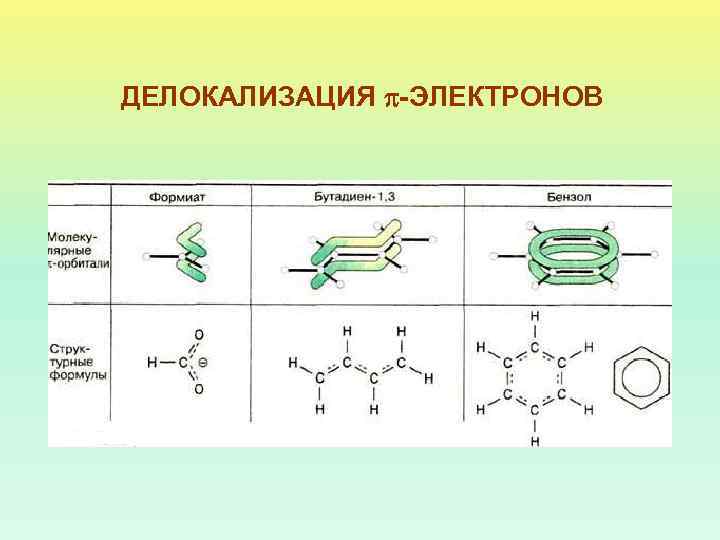
ДЕЛОКАЛИЗАЦИЯ -ЭЛЕКТРОНОВ
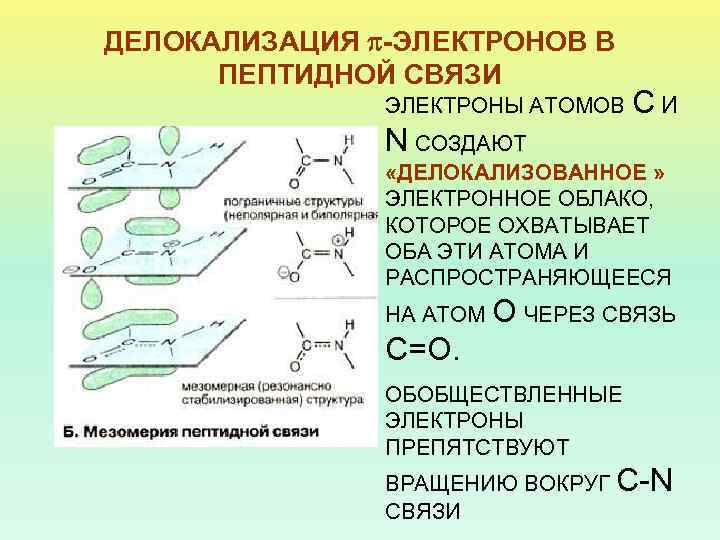
ДЕЛОКАЛИЗАЦИЯ -ЭЛЕКТРОНОВ В ПЕПТИДНОЙ СВЯЗИ ЭЛЕКТРОНЫ АТОМОВ С И N СОЗДАЮТ «ДЕЛОКАЛИЗОВАННОЕ » ЭЛЕКТРОННОЕ ОБЛАКО, КОТОРОЕ ОХВАТЫВАЕТ ОБА ЭТИ АТОМА И РАСПРОСТРАНЯЮЩЕЕСЯ НА АТОМ О ЧЕРЕЗ СВЯЗЬ С=О. ОБОБЩЕСТВЛЕННЫЕ ЭЛЕКТРОНЫ ПРЕПЯТСТВУЮТ ВРАЩЕНИЮ ВОКРУГ C-N СВЯЗИ
ПРИ ДЕЛОКАЛИЗАЦИИ ЭНЕРГИЯ ЭЛЕКТРОНОВ ПАДАЕТ И ОНИ ПЕРЕХОДЯТ В БОЛЕЕ СТАБИЛЬНОЕ СОСТОЯНИЕ

ДЛИНЫ СВЯЗЕЙ N – C (ПЕПТИДНАЯ СВЯЗЬ) 0, 132 НМ N – C (ОДИНОЧНАЯ) 0, 147 НМ N = C (ДВОЙНАЯ) 0, 125 НМ 0, 147 < 0, 132 < 0, 125 ПЕПТИДНАЯ СВЯЗЬ ЗАНИМАЕТ ПРОМЕЖУТОЧНОЕ ПОЛОЖЕНИЕ
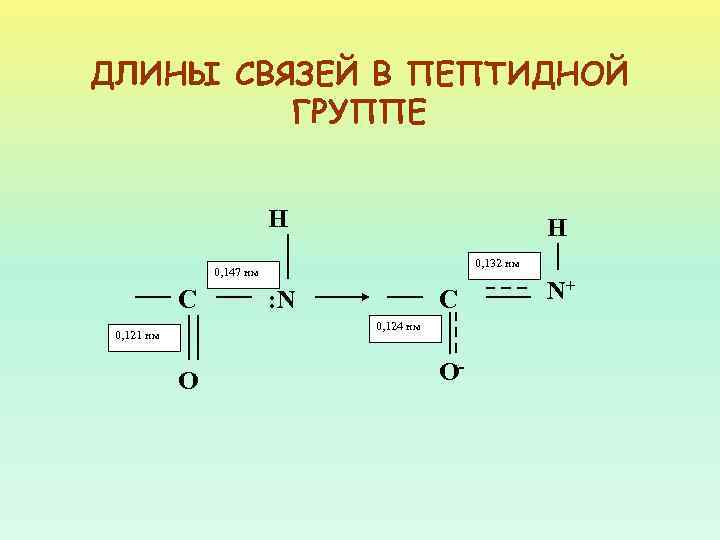
ДЛИНЫ СВЯЗЕЙ В ПЕПТИДНОЙ ГРУППЕ H H 0, 132 нм 0, 147 нм С : N С 0, 124 нм 0, 121 нм O O- N+
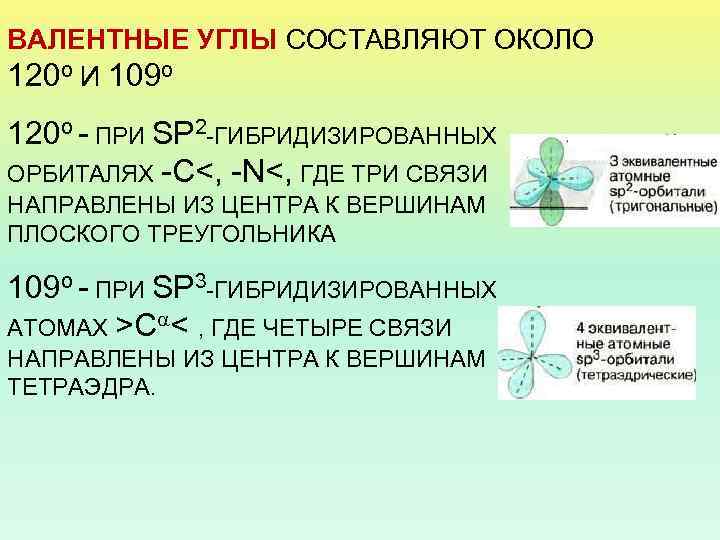
ВАЛЕНТНЫЕ УГЛЫ СОСТАВЛЯЮТ ОКОЛО 120 о И 109 о 120 о - ПРИ SP 2 -ГИБРИДИЗИРОВАННЫХ ОРБИТАЛЯХ -С<, -N<, ГДЕ ТРИ СВЯЗИ НАПРАВЛЕНЫ ИЗ ЦЕНТРА К ВЕРШИНАМ ПЛОСКОГО ТРЕУГОЛЬНИКА 109 о - ПРИ SP 3 -ГИБРИДИЗИРОВАННЫХ АТОМАХ >С < , ГДЕ ЧЕТЫРЕ СВЯЗИ НАПРАВЛЕНЫ ИЗ ЦЕНТРА К ВЕРШИНАМ ТЕТРАЭДРА.

ПРИ КОМНАТНОЙ ТЕМПЕРАТУРЕ ВАЛЕНТНЫЕ СВЯЗИ НЕ ФЛУКТУИРУЮТ: ЧАСТОТА КОЛЕБАНИЙ ЭТИХ СВЯЗЕЙ 2 х1013 сек – 1 ЧАСТОТА ТЕПЛОВЫХ КОЛЕБАНИЙ 7 х1012 сек – 1 АМПЛИТУДА ТЕПЛОВЫХ КОЛЕБАНИЙ ВАЛЕНТНЫХ УГЛОВ НЕВЕЛИКА И СОСТАВЛЯЕТ ОКОЛО 5 о. ТАКИМ ОБРАЗОМ, ГИБКОСТЬ ПОЛИПЕПТИДНОЙ ЦЕПИ ОБЕСПЕЧИВАЕТСЯ ДРУГИМИ ФАКТОРАМИ.

ГИБКОСТЬ ПОЛИПЕПТИДНОЙ ЦЕПИ, А, ЗНАЧИТ, И ЕЕ СПОСОБНОСТЬ ОБРАЗОВЫВАТЬ СПИРАЛИ И ГЛОБУЛЫ ОБЕСПЕЧИВАЕТ ВРАЩЕНИЕ ВОКРУГ ВАЛЕНТНЫХ СВЯЗЕЙ.
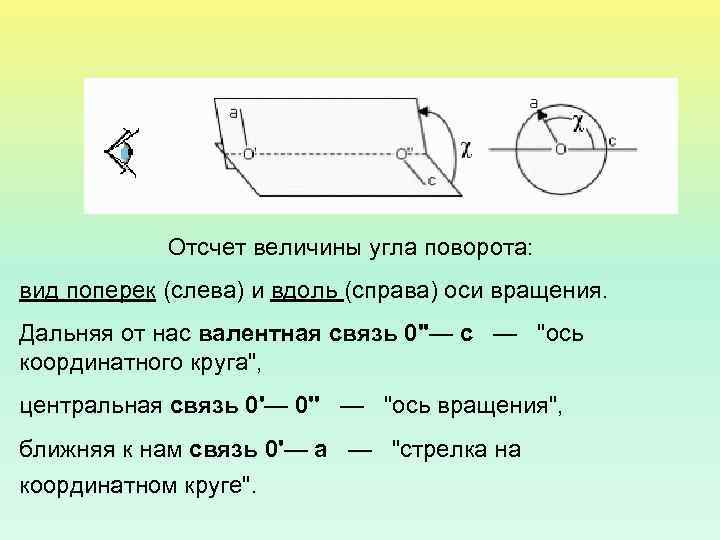
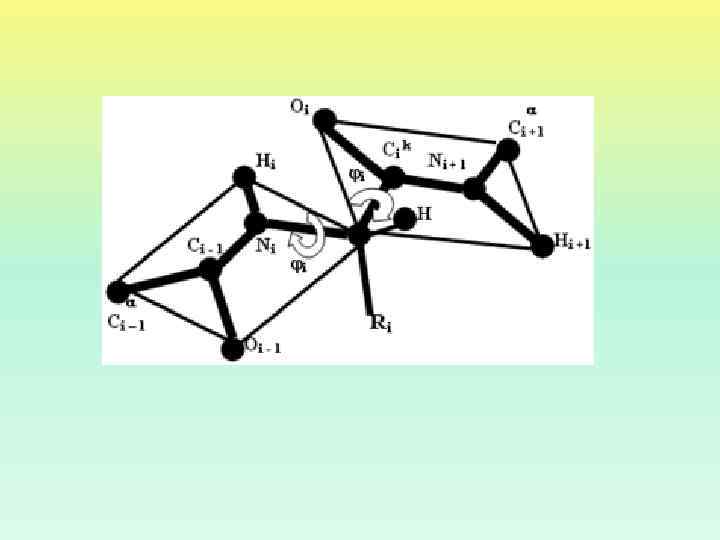
Отсчет величины угла поворота: вид поперек (слева) и вдоль (справа) оси вращения. Дальняя от нас валентная связь 0''— c — "ось координатного круга", центральная связь 0'— 0'' — "ось вращения", ближняя к нам связь 0'— a — "стрелка на координатном круге".
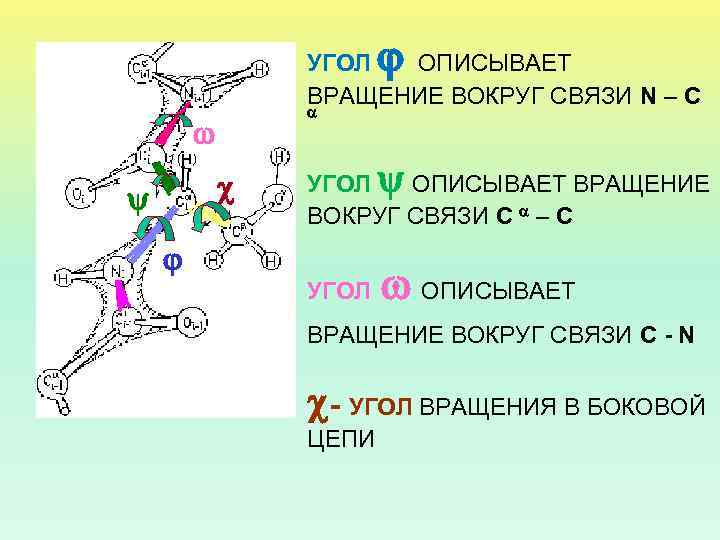
УГОЛ ОПИСЫВАЕТ ВРАЩЕНИЕ ВОКРУГ СВЯЗИ N – C УГОЛ ОПИСЫВАЕТ ВРАЩЕНИЕ ВОКРУГ СВЯЗИ C – C УГОЛ ОПИСЫВАЕТ ВРАЩЕНИЕ ВОКРУГ СВЯЗИ C - N - УГОЛ ВРАЩЕНИЯ В БОКОВОЙ ЦЕПИ
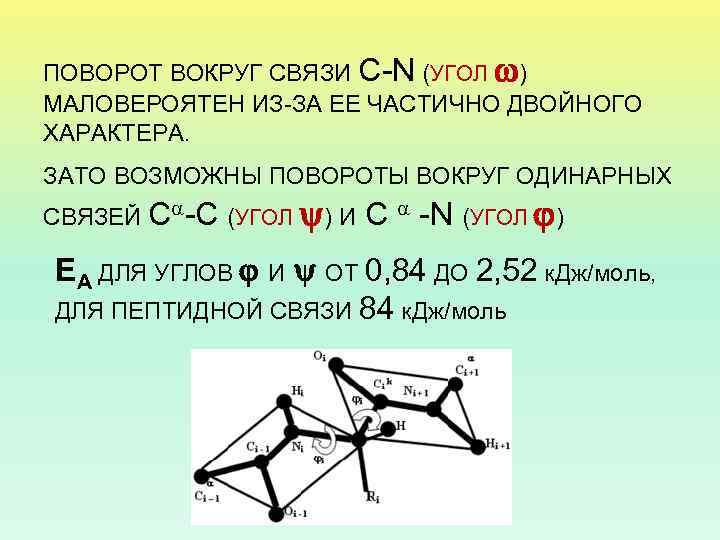
ПОВОРОТ ВОКРУГ СВЯЗИ С-N (УГОЛ ) МАЛОВЕРОЯТЕН ИЗ-ЗА ЕЕ ЧАСТИЧНО ДВОЙНОГО ХАРАКТЕРА. ЗАТО ВОЗМОЖНЫ ПОВОРОТЫ ВОКРУГ ОДИНАРНЫХ СВЯЗЕЙ C -C (УГОЛ ) И C -N (УГОЛ ) ЕА ДЛЯ УГЛОВ И ОТ 0, 84 ДО 2, 52 к. Дж/моль, ДЛЯ ПЕПТИДНОЙ СВЯЗИ 84 к. Дж/моль

ВТОРИЧНАЯ СТРУКТУРА БЕЛКА
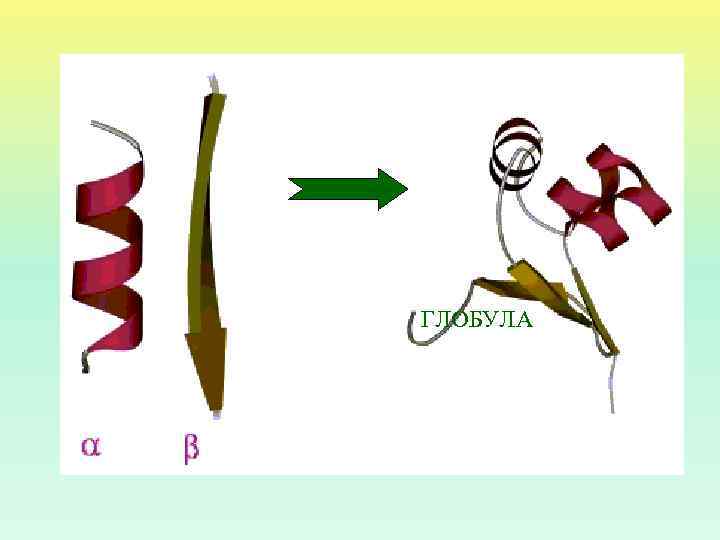
ГЛОБУЛА
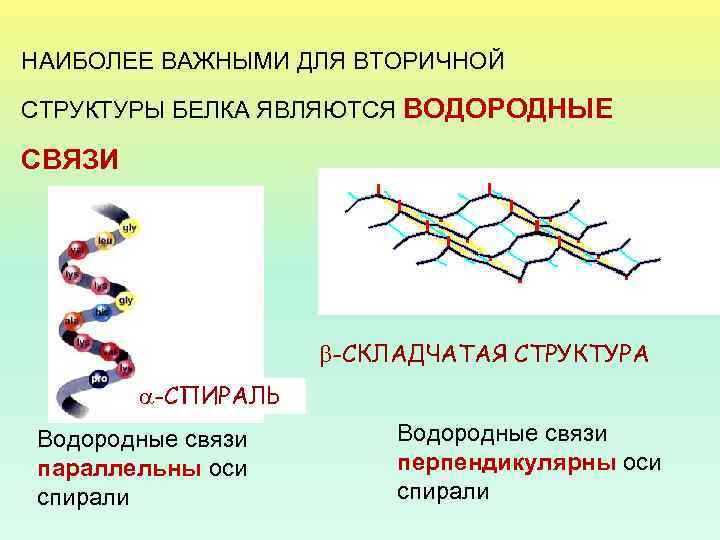
НАИБОЛЕЕ ВАЖНЫМИ ДЛЯ ВТОРИЧНОЙ СТРУКТУРЫ БЕЛКА ЯВЛЯЮТСЯ ВОДОРОДНЫЕ СВЯЗИ -СКЛАДЧАТАЯ СТРУКТУРА -СПИРАЛЬ Водородные связи параллельны оси спирали Водородные связи перпендикулярны оси спирали
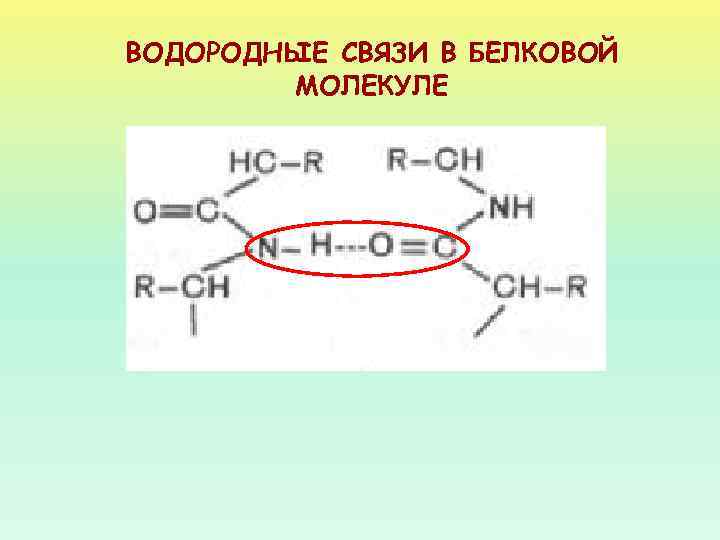
ВОДОРОДНЫЕ СВЯЗИ В БЕЛКОВОЙ МОЛЕКУЛЕ
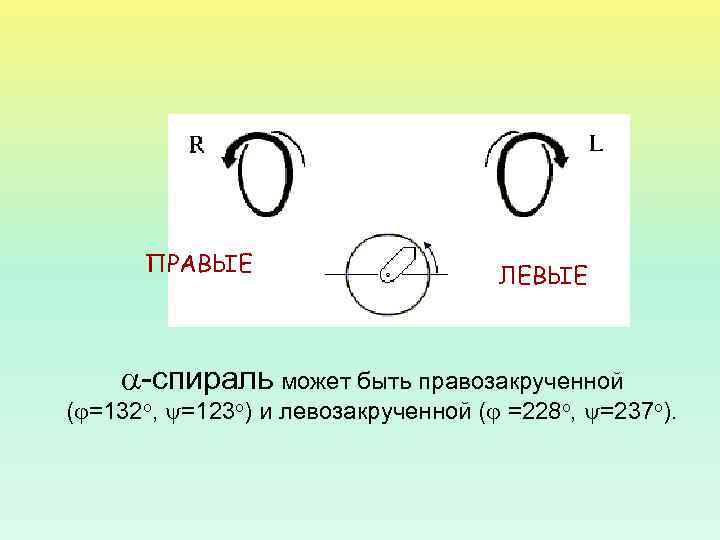
ПРАВЫЕ ЛЕВЫЕ -спираль может быть правозакрученной ( =132 о, =123 о) и левозакрученной ( =228 о, =237 о).
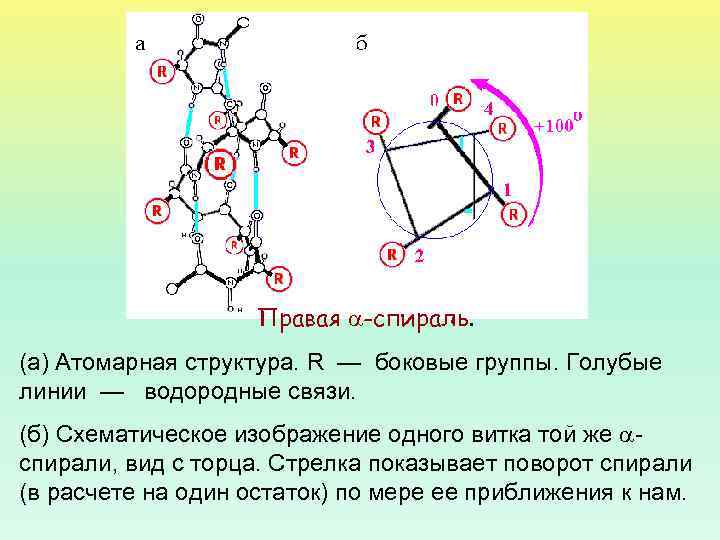
Правая -спираль. (а) Атомарная структура. R — боковые группы. Голубые линии — водородные связи. (б) Схематическое изображение одного витка той же спирали, вид с торца. Стрелка показывает поворот спирали (в расчете на один остаток) по мере ее приближения к нам.
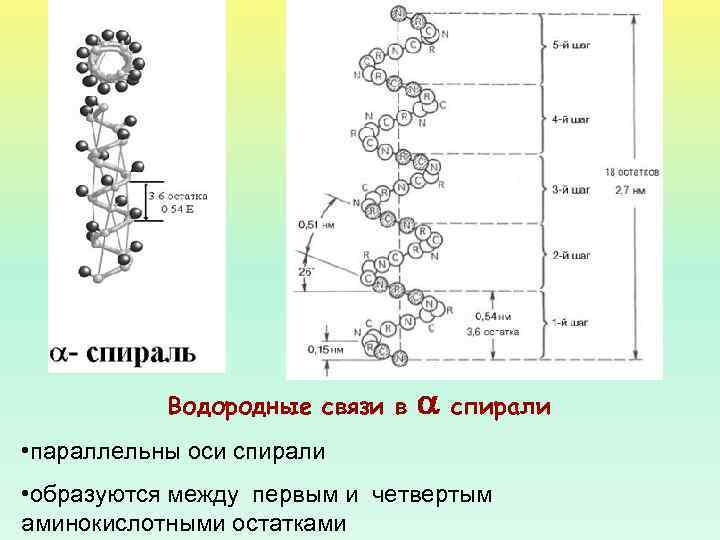
Водородные связи в спирали • параллельны оси спирали • образуются между первым и четвертым аминокислотными остатками

ПАРАМЕТРЫ -СПИРАЛИ НА КАЖДЫЙ ВИТОК (ШАГ) СПИРАЛИ ПРИХОДИТСЯ 3, 6 АМИНОКИСЛОТНЫХ ОСТАТКОВ. ШАГ СПИРАЛИ (РАССТОЯНИЕ ВДОЛЬ ОСИ) – 0, 54 НМ. НА ОДИН АМИНОКИСЛОТНЫЙ ОСТАТОК ПРИХОДИТСЯ 0, 15 НМ. ЧЕРЕЗ 5 ВИТКОВ СПИРАЛИ (18 АМИНОКИСЛОТНЫХ ОСТАТКОВ) СТРУКТУРНАЯ КОНФИГУРАЦИЯ ПОЛИПЕПТИДНОЙ ЦЕПИ ПОВТОРЯЕТСЯ
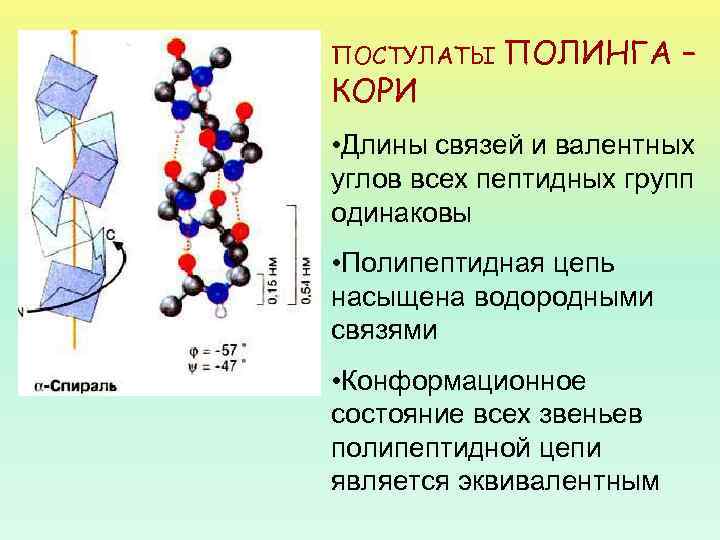
ПОСТУЛАТЫ КОРИ ПОЛИНГА – • Длины связей и валентных углов всех пептидных групп одинаковы • Полипептидная цепь насыщена водородными связями • Конформационное состояние всех звеньев полипептидной цепи является эквивалентным

Некоторые остатки аминокислот могут нарушать формирование -спирали. ØПРОЛИН Его атом азота входит в состав жёсткого кольца, что исключает возможность вращения вокруг -N-CH - связи. Пролин не способен образовать водородную связь в данном месте пептидного остова, и -спиральная структура нарушается. Обычно в этом месте пептидной цепи возникает петля или изгиб.
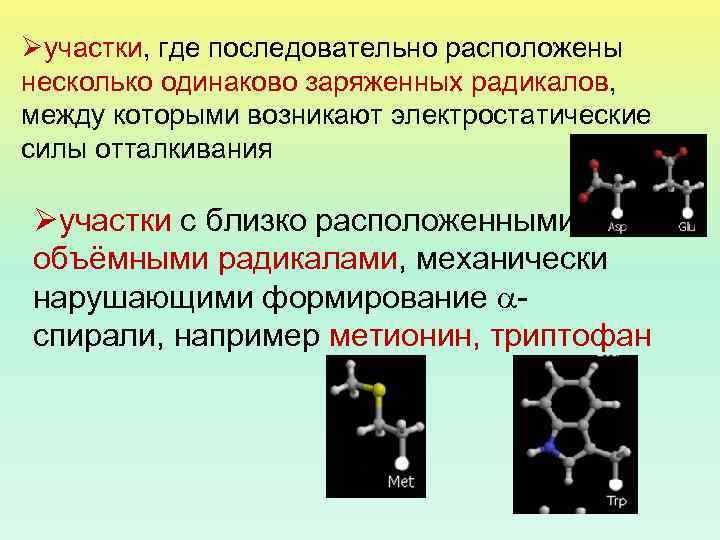
Øучастки, где последовательно расположены несколько одинаково заряженных радикалов, между которыми возникают электростатические силы отталкивания Øучастки с близко расположенными объёмными радикалами, механически нарушающими формирование спирали, например метионин, триптофан

-складчатые структуры
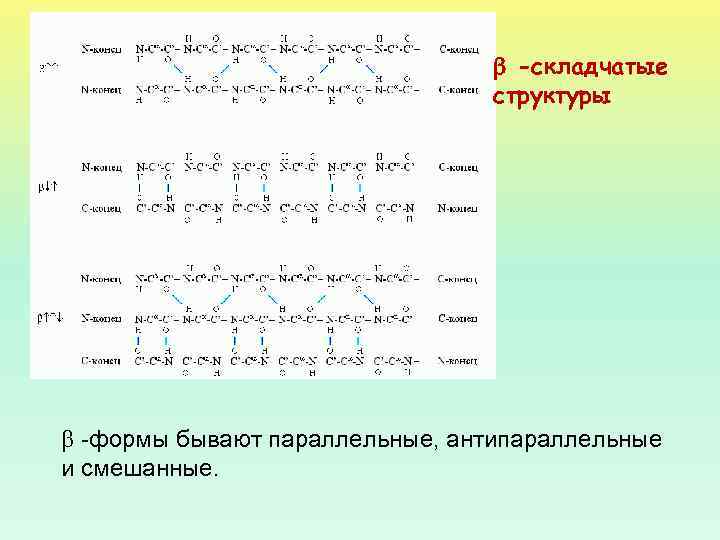
-складчатые структуры -формы бывают параллельные, антипараллельные и смешанные.
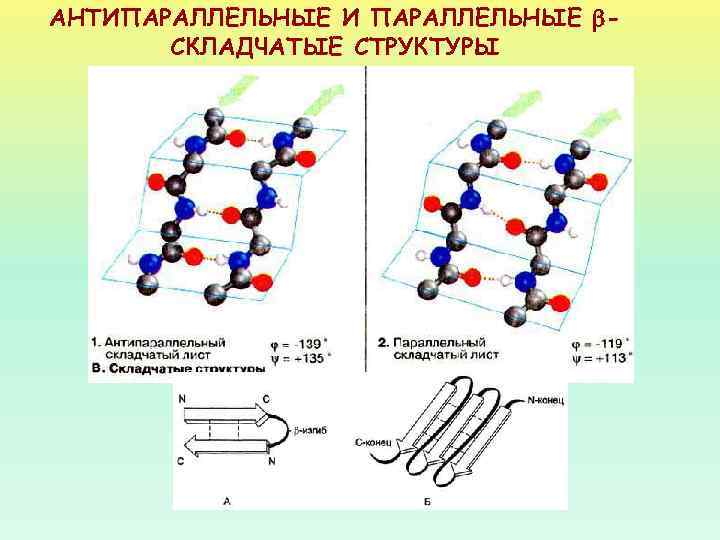
АНТИПАРАЛЛЕЛЬНЫЕ И ПАРАЛЛЕЛЬНЫЕ СКЛАДЧАТЫЕ СТРУКТУРЫ
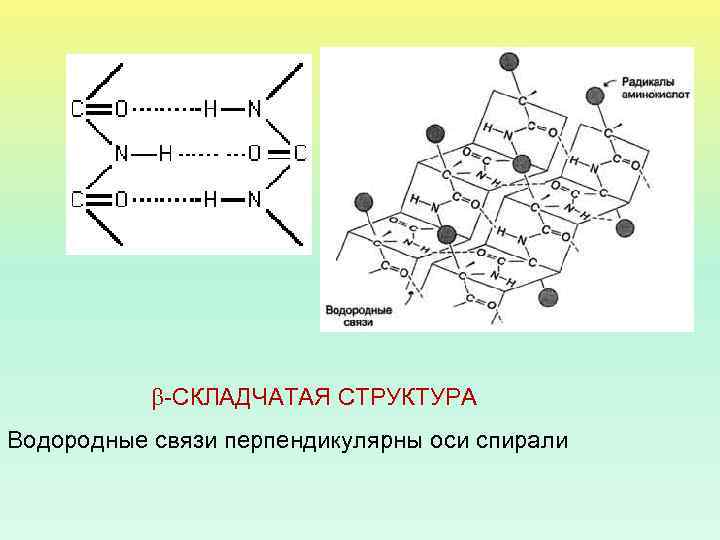
-СКЛАДЧАТАЯ СТРУКТУРА Водородные связи перпендикулярны оси спирали

ИМЕЮТСЯ СПИРАЛИ И БЕЗ ВОДОРОДНЫХ СВЯЗЕЙ, КОТОРЫЕ СУЩЕСТВУЮТ ЗА СЧЕТ ВАНДЕРВААЛЬСОВЫХ СИЛ. ЭТО ПОЛИПРОЛИНОВАЯ СПИРАЛЬ, КОТОРАЯ РЕАЛИЗУЕТСЯ В КОЛЛАГЕНЕ.
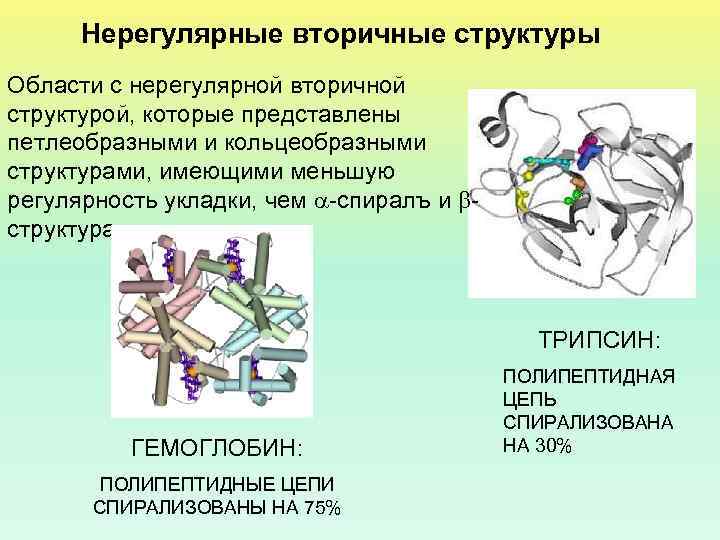
Нерегулярные вторичные структуры Области с нерегулярной вторичной структурой, которые представлены петлеобразными и кольцеобразными структурами, имеющими меньшую регулярность укладки, чем -спиралъ и структура. ТРИПСИН: ГЕМОГЛОБИН: ПОЛИПЕПТИДНЫЕ ЦЕПИ СПИРАЛИЗОВАНЫ НА 75% ПОЛИПЕПТИДНАЯ ЦЕПЬ СПИРАЛИЗОВАНА НА 30%

ДРУГИЕ СПИРАЛЬНЫЕ КОНФОРМАЦИИ СПИРАЛЬ 310 • 3 ОСТАТКА АМИНОКИСЛОТ НА ШАГ (ВИТОК) СПИРАЛИ • РАДИУС 0, 19 НМ p. СПИРАЛЬ 4, 4 ОСТАТКА НА ШАГ СПИРАЛИ РАДИУС 0, 28 НМ

СВЕРХВТОРИЧНЫЕ СТРУКТУРЫ

СВЕРХВТОРИЧНЫЕ СТРУКТУРЫ – ЭТО ТЕРМОДИНАМИЧЕСКИ ИЛИ КИНЕТИЧЕСКИ СТАБИЛЬНЫЕ КОМПЛЕКСЫ -СПИРАЛЕЙ И СТРУКТУР, КОТОРЫЕ ФОРМИРУЮТСЯ ЗА СЧЕТ МЕЖРАДИКАЛЬНЫХ ВЗАИМОДЕЙСТВИЙ.
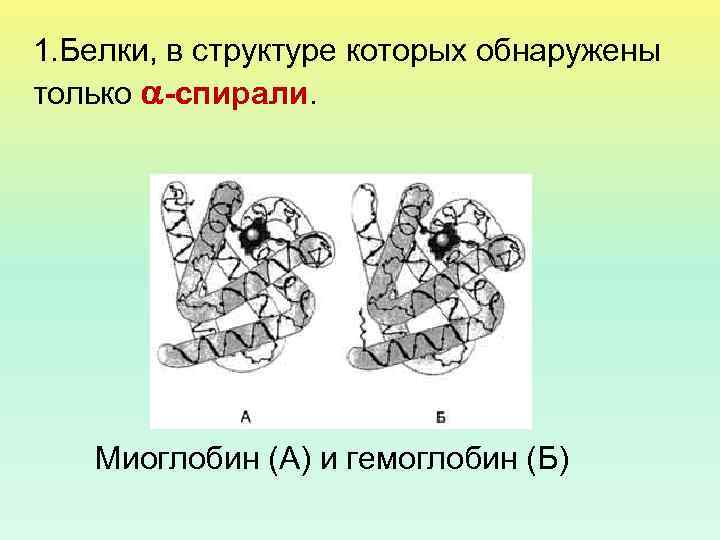
1. Белки, в структуре которых обнаружены только -спирали. Миоглобин (А) и гемоглобин (Б)
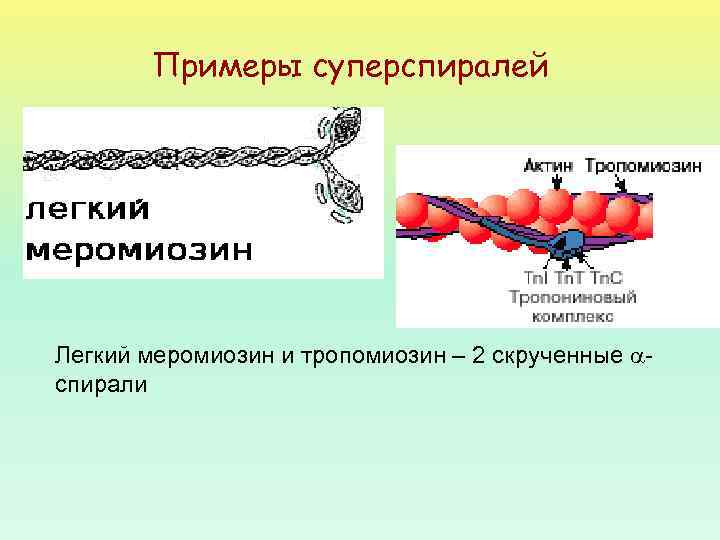
Примеры суперспиралей Легкий меромиозин и тропомиозин – 2 скрученные спирали
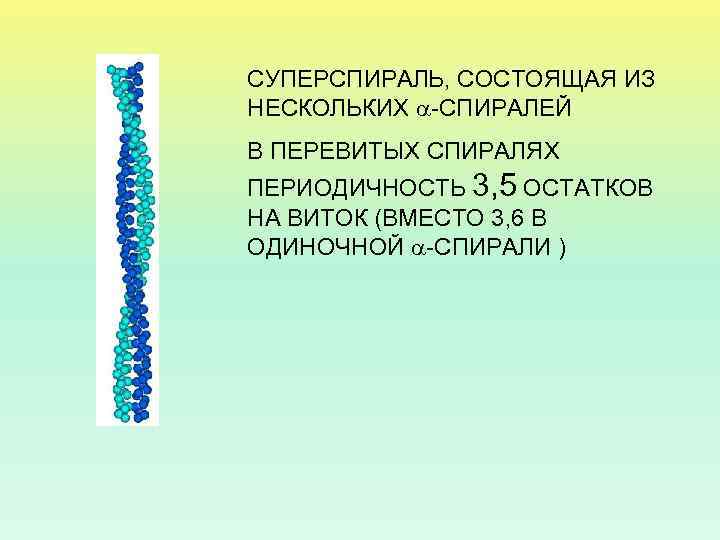
СУПЕРСПИРАЛЬ, СОСТОЯЩАЯ ИЗ НЕСКОЛЬКИХ -СПИРАЛЕЙ В ПЕРЕВИТЫХ СПИРАЛЯХ ПЕРИОДИЧНОСТЬ 3, 5 ОСТАТКОВ НА ВИТОК (ВМЕСТО 3, 6 В ОДИНОЧНОЙ -СПИРАЛИ )
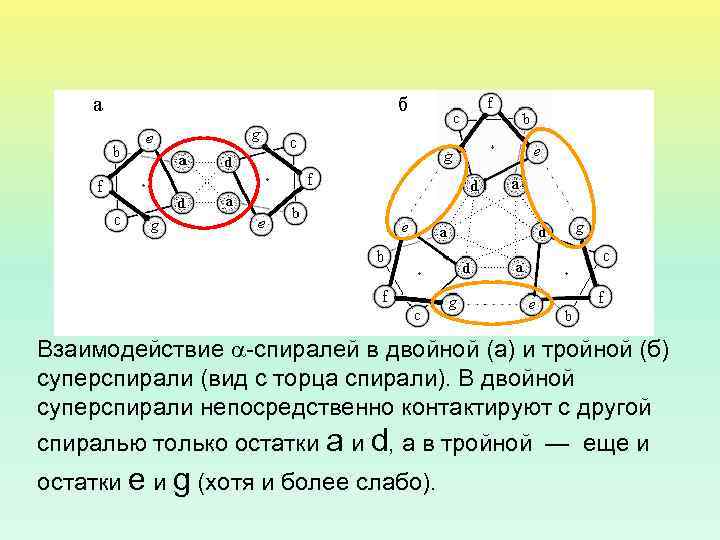
Взаимодействие -спиралей в двойной (а) и тройной (б) суперспирали (вид с торца спирали). В двойной суперспирали непосредственно контактируют с другой спиралью только остатки а и d, а в тройной — еще и остатки e и g (хотя и более слабо).
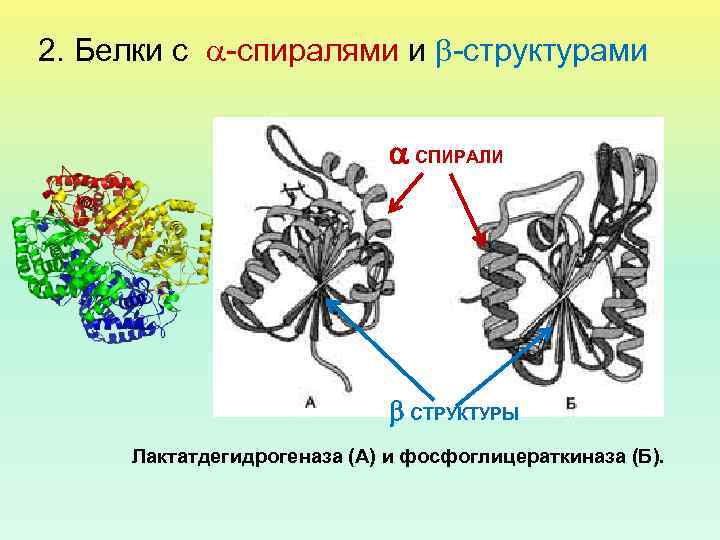
2. Белки с -спиралями и -структурами СПИРАЛИ СТРУКТУРЫ Лактатдегидрогеназа (А) и фосфоглицераткиназа (Б).
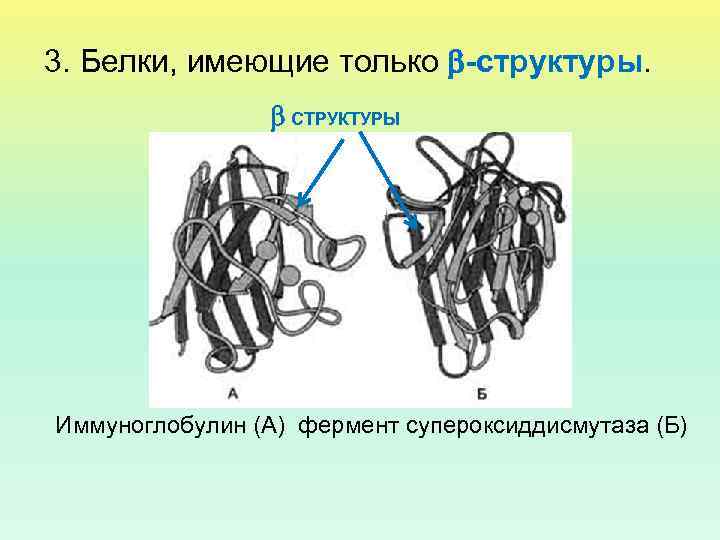
3. Белки, имеющие только -структуры. СТРУКТУРЫ Иммуноглобулин (А) фермент супероксиддисмутаза (Б)
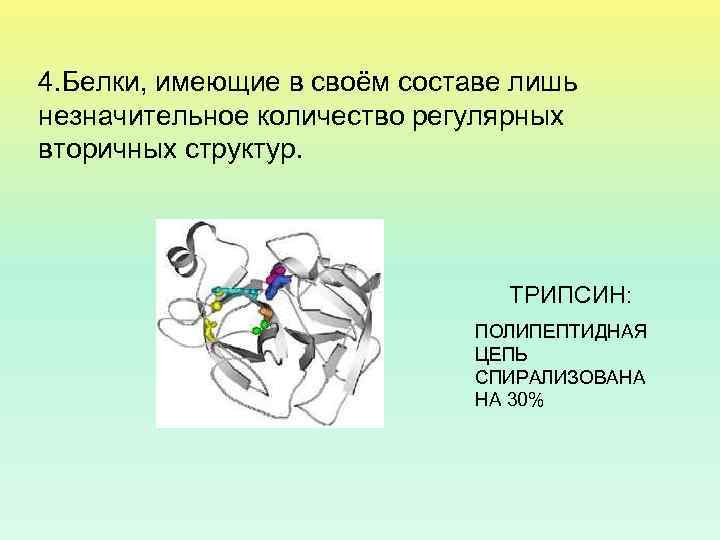
4. Белки, имеющие в своём составе лишь незначительное количество регулярных вторичных структур. ТРИПСИН: ПОЛИПЕПТИДНАЯ ЦЕПЬ СПИРАЛИЗОВАНА НА 30%

5. Модель тройной суперспирали коллагена для последовательности (глицин — пролин)n. Каждая цепь выделена своим цветом. Отмечены завязывающие водородные связи Н-атомы NH-групп глицина (синим) и О-атомы СО-групп первого пролина тройки Gly-Pro (красным). При этом Gly цепи "1" завязывает связь с цепью "2", а Pro — с цепью "3", и т. д. Завиваясь вокруг двух других, каждая цепь коллагена образует правую суперспираль.
2_перв_втор структура.ppt