Процессы изменения состояния термодинамических систем Классификация термодинамических процессов





























lekciya_5-6.ppt
- Размер: 545.0 Кб
- Автор: Anastasia Verteletskaya
- Количество слайдов: 32
Описание презентации Процессы изменения состояния термодинамических систем Классификация термодинамических процессов по слайдам
 Процессы изменения состояния термодинамических систем Классификация термодинамических процессов Термодинамический процесс может быть задан либо графическим способом в виде изображения процесса в координатах p — v , p — T , Т- s , либо в аналити-ческой форме в виде зависимости Уравнение процесса может быть также задано исходным условием о неизменном значении в этом процессе какой — либо функции состояния или условием о равенстве нулю какого – либо эффекта термодинамического процесса 0)v, p( s, h, u, t, v, pz; idemz 0 q
Процессы изменения состояния термодинамических систем Классификация термодинамических процессов Термодинамический процесс может быть задан либо графическим способом в виде изображения процесса в координатах p — v , p — T , Т- s , либо в аналити-ческой форме в виде зависимости Уравнение процесса может быть также задано исходным условием о неизменном значении в этом процессе какой — либо функции состояния или условием о равенстве нулю какого – либо эффекта термодинамического процесса 0)v, p( s, h, u, t, v, pz; idemz 0 q
 При изучении термодинамических процессов определяются: 1) закономерность изменения параметров состояния рабочего тела, то есть выводится уравнение процесса или дается его графическое изображение в координатах p — v , p — T , Т- s и т. д. ; 2) параметры состояния системы в начальной и конечной точках процесса; 3) численные значения работы и теплообмена в процессе; 4) изменение значений внутренней энергии, энтальпии и энтропии рабочего тела. Простейшие термодинамические процессы Простейшими термодинамическими процессами обычно считают изобарный, изохорный и изопотенциальные процессы.
При изучении термодинамических процессов определяются: 1) закономерность изменения параметров состояния рабочего тела, то есть выводится уравнение процесса или дается его графическое изображение в координатах p — v , p — T , Т- s и т. д. ; 2) параметры состояния системы в начальной и конечной точках процесса; 3) численные значения работы и теплообмена в процессе; 4) изменение значений внутренней энергии, энтальпии и энтропии рабочего тела. Простейшие термодинамические процессы Простейшими термодинамическими процессами обычно считают изобарный, изохорный и изопотенциальные процессы.
 Изобарный процесс – процесс в котором давление в системе остается постоянным. 0 dp; idemp v 12 P P= ide m 1, 2 v 1 v 2 P
Изобарный процесс – процесс в котором давление в системе остается постоянным. 0 dp; idemp v 12 P P= ide m 1, 2 v 1 v 2 P
 Изобарные процессы подвода или отвода теплоты происходят в поршневых двигателях внутреннего сгорания, газотурбинных, паросиловых, холодильных установках и др. Для идеального газа в изобарном процессе ( 1 -2 ) соотношение объемов прямо пропорционально соотношению температур Удельная термодинамическая и потенциальная работы в изобарном процессе определяются из соотношений 1 2 v v T T 12 2 1 2, 1 vvpdvpl ; 0 dpvw 2 1 2,
Изобарные процессы подвода или отвода теплоты происходят в поршневых двигателях внутреннего сгорания, газотурбинных, паросиловых, холодильных установках и др. Для идеального газа в изобарном процессе ( 1 -2 ) соотношение объемов прямо пропорционально соотношению температур Удельная термодинамическая и потенциальная работы в изобарном процессе определяются из соотношений 1 2 v v T T 12 2 1 2, 1 vvpdvpl ; 0 dpvw 2 1 2,
 Для идеального газа Количество теплоты, подведенной к рабочему телу или отведенной от него в изобарном процессе, опреде-ляется из выражения первого начала термодинамики Для идеального газа 12122, 1 TTRvvpl hluq 2, 1 121212 2, 1)(TTc. TTRTTc hluq pmvm
Для идеального газа Количество теплоты, подведенной к рабочему телу или отведенной от него в изобарном процессе, опреде-ляется из выражения первого начала термодинамики Для идеального газа 12122, 1 TTRvvpl hluq 2, 1 121212 2, 1)(TTc. TTRTTc hluq pmvm
 Изохорный процесс – процесс, при котором объем системы или удельный объем рабо- чего тела остается постоянным. 0 dv; idemv v 1 2 P = idem w 1, 2 v 1 v 2 P 1 P 2 = v
Изохорный процесс – процесс, при котором объем системы или удельный объем рабо- чего тела остается постоянным. 0 dv; idemv v 1 2 P = idem w 1, 2 v 1 v 2 P 1 P 2 = v
 В изохорных процессах происходит увеличение или уменьшение давления, что связано с соответствен – ным изменением температуры – подводом или отводом теплоты. Изохорные процессы подвода или отвода теплоты происходят в поршневых двигателях внутреннего сго- рания, газотурбинных, паросиловых установках и др. Для идеального газа в изохорном процессе соотношение давлений прямо пропорционально соотношению температур1 2 p p T T
В изохорных процессах происходит увеличение или уменьшение давления, что связано с соответствен – ным изменением температуры – подводом или отводом теплоты. Изохорные процессы подвода или отвода теплоты происходят в поршневых двигателях внутреннего сго- рания, газотурбинных, паросиловых установках и др. Для идеального газа в изохорном процессе соотношение давлений прямо пропорционально соотношению температур1 2 p p T T
 Удельная термодинамическая и потенциальная работы в изохорном процессе определяются из соотно- шений Для идеального газа Количество теплоты, подведенной к рабочему телу или отведенной от него в изохорном процессе, определя- ется из выражения первого начала термодинамики; 0 dvpl 2 1 2, 1 2 1212, 1 ppvvdpw 21212, 1 TTRppvw
Удельная термодинамическая и потенциальная работы в изохорном процессе определяются из соотно- шений Для идеального газа Количество теплоты, подведенной к рабочему телу или отведенной от него в изохорном процессе, определя- ется из выражения первого начала термодинамики; 0 dvpl 2 1 2, 1 2 1212, 1 ppvvdpw 21212, 1 TTRppvw
 Для идеального газа Изопотенциальный процесс – термодинамический процесс изменения состояния системы, при котором значение потенциальной функции сохраняет неизменное значение 0)pv(d; idempv uwhq 2, 1 122112 2, 1 TTc. TTRTTc uwhq vmpm
Для идеального газа Изопотенциальный процесс – термодинамический процесс изменения состояния системы, при котором значение потенциальной функции сохраняет неизменное значение 0)pv(d; idempv uwhq 2, 1 122112 2, 1 TTc. TTRTTc uwhq vmpm
 Для идеального газа, согласно уравнению Клапейрона изопотенциальный процесс является и изотермическим . Удельная термодинамическая и потенциальная работы в изопотенциальном процессе определяются из следую- щих соотношений: RTpvidempv idem. T 2 1 2, 1 dvpl 2 1 v dv vp 1 2 v v lnpv 2 1 2, 1 dpvw 2 1 p dp vp 1 2 p dp pv 2 1 p p lnpv 1 2 11 22 T T vp vp
Для идеального газа, согласно уравнению Клапейрона изопотенциальный процесс является и изотермическим . Удельная термодинамическая и потенциальная работы в изопотенциальном процессе определяются из следую- щих соотношений: RTpvidempv idem. T 2 1 2, 1 dvpl 2 1 v dv vp 1 2 v v lnpv 2 1 2, 1 dpvw 2 1 p dp vp 1 2 p dp pv 2 1 p p lnpv 1 2 11 22 T T vp vp
 Нетрудно заметить, что постоянство приводит к условию Поэтому, в изопотенциальном процессе численные значения термодинамической и потенциальной работ равны между собой. 1 2 2 1 v v p p idempv 2, 1 l 1 2 v v lnpv 2, 1 w 2 1 p p lnpv
Нетрудно заметить, что постоянство приводит к условию Поэтому, в изопотенциальном процессе численные значения термодинамической и потенциальной работ равны между собой. 1 2 2 1 v v p p idempv 2, 1 l 1 2 v v lnpv 2, 1 w 2 1 p p lnpv
 Для идеального газа pv=RT=idem ( изотермический) Количество теплоты, подведенной к рабочему телу или отведенной от него в изопотенциальном процессе определяется из выражения первого начала термодинамики по балансу рабочего тела Для идеалного газа du=0; dh=02, 1 l 2, 1 w 1 2 v v ln. RT 2 1 p p ln. RT 2, 12, 1 whluq 2, 1 q 1 2 v v ln. RT 2 1 p p ln. RT
Для идеального газа pv=RT=idem ( изотермический) Количество теплоты, подведенной к рабочему телу или отведенной от него в изопотенциальном процессе определяется из выражения первого начала термодинамики по балансу рабочего тела Для идеалного газа du=0; dh=02, 1 l 2, 1 w 1 2 v v ln. RT 2 1 p p ln. RT 2, 12, 1 whluq 2, 1 q 1 2 v v ln. RT 2 1 p p ln. RT
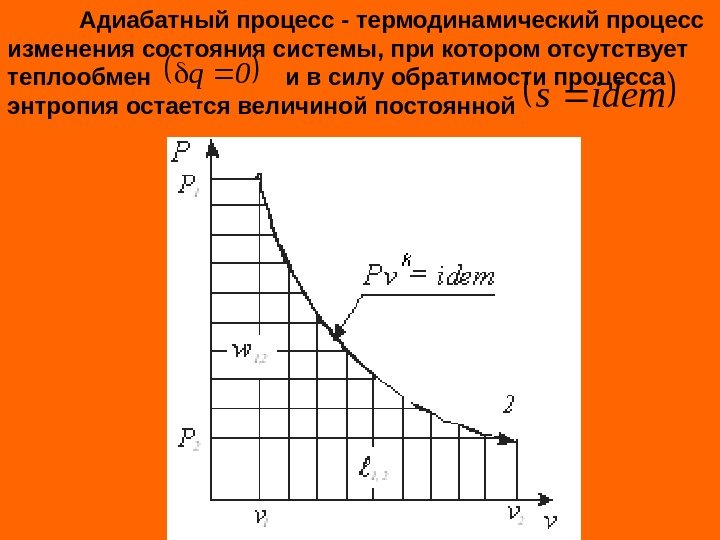
 Адиабатный процесс — термодинамический процесс изменения состояния системы, при котором отсутствует теплообмен и в силу обратимости процесса энтропия остается величиной постоянной 0 q idems
Адиабатный процесс — термодинамический процесс изменения состояния системы, при котором отсутствует теплообмен и в силу обратимости процесса энтропия остается величиной постоянной 0 q idems
 Из выражения первого начала термодинамики для простого тела при условии имеем Отсюда следует выражение для показателя адиабатного процесса где ns =k – показатель адиабаты. Расчетное выражение для расчета показателя адиабатного процесса idems 0 q 0 vdpdhpdvduqqq *** kn pdv vdp du dh s
Из выражения первого начала термодинамики для простого тела при условии имеем Отсюда следует выражение для показателя адиабатного процесса где ns =k – показатель адиабаты. Расчетное выражение для расчета показателя адиабатного процесса idems 0 q 0 vdpdhpdvduqqq *** kn pdv vdp du dh s
 После интегрирования при условия постоянства показателя процесса имеем Для идеального газа показатель адиабаты равен k = cp /cv. vlogd plogd vlnd plnd v dv p dp kns 1 2 2 1 2, 1 s v v log p p log l w u h kn
После интегрирования при условия постоянства показателя процесса имеем Для идеального газа показатель адиабаты равен k = cp /cv. vlogd plogd vlnd plnd v dv p dp kns 1 2 2 1 2, 1 s v v log p p log l w u h kn
 Из уравнения адиабатного процесса получим выражение для связи параметров состояния потенцируя имеем; idempv k ; idemvp k 1 1 p p v v p pk 1 1 2 k 1 2 , p p log v v logk
Из уравнения адиабатного процесса получим выражение для связи параметров состояния потенцируя имеем; idempv k ; idemvp k 1 1 p p v v p pk 1 1 2 k 1 2 , p p log v v logk
 Выражения конечных (интегральных) величин термодинамической и потенциальных работа в адиабат- ном процесс можно получить при сопоставлении их элементарных значений С учетом определения показателя адиабаты имеем : vdpw, . . . pdvl pvdvdppdvwl pvdlk 1 wl pvd k 1 1 l
Выражения конечных (интегральных) величин термодинамической и потенциальных работа в адиабат- ном процесс можно получить при сопоставлении их элементарных значений С учетом определения показателя адиабаты имеем : vdpw, . . . pdvl pvdvdppdvwl pvdlk 1 wl pvd k 1 1 l
 Интегрируя последнее выражение с учетом того, что k= idem , получим интегрального уравнения термодинамической работы Введем понятие характеристики процесса расширения или сжатия 212211 2 1 2, 1 uu)vpvp( k 1 1 )pv(d k 1 1 l 11 22 2, 1 vp vp
Интегрируя последнее выражение с учетом того, что k= idem , получим интегрального уравнения термодинамической работы Введем понятие характеристики процесса расширения или сжатия 212211 2 1 2, 1 uu)vpvp( k 1 1 )pv(d k 1 1 l 11 22 2, 1 vp vp
 Окончательно имеем уравнения для определения термодинамической и потенциальной работы Различные уравнения для определения характе- ристики расширения или сжатия определяются с учетом уравнения адиабаты 212, 1 11 2, 1 uu 1 1 k vp l 212, 1112, 1 hh 1 vp 1 k k klw 2, 1 1 k 2 1 k 1 k 1 2 11 22 v v p p vp vp
Окончательно имеем уравнения для определения термодинамической и потенциальной работы Различные уравнения для определения характе- ристики расширения или сжатия определяются с учетом уравнения адиабаты 212, 1 11 2, 1 uu 1 1 k vp l 212, 1112, 1 hh 1 vp 1 k k klw 2, 1 1 k 2 1 k 1 k 1 2 11 22 v v p p vp vp
 Применительно для идеального газа имеем: 212, 1 1 1 ttc k RT l vm 212, 1112, 11 1 ttc. TR k k klwpm 2, 1 1 k 2 1 k 1 k 1 2 11 22 1 2 v v p p vp vp T T
Применительно для идеального газа имеем: 212, 1 1 1 ttc k RT l vm 212, 1112, 11 1 ttc. TR k k klwpm 2, 1 1 k 2 1 k 1 k 1 2 11 22 1 2 v v p p vp vp T T
 Уравнения перечисленных простейших и любых других термодинамических процессов могут быть представлены одним уравнением. Это уравнение назы- вается уравнением политропы , а термодинамические процессы, описываемые этим уравнением, называются политропными. Политропные процессы Политропным процессом с постоянным показателем называется обратимый термодинамический процесс изменения состояния простого тела, подчиняющийся уравнению ; Cidempv n ; Cidemvp 1 n/1 n 22 n 11 vpvp
Уравнения перечисленных простейших и любых других термодинамических процессов могут быть представлены одним уравнением. Это уравнение назы- вается уравнением политропы , а термодинамические процессы, описываемые этим уравнением, называются политропными. Политропные процессы Политропным процессом с постоянным показателем называется обратимый термодинамический процесс изменения состояния простого тела, подчиняющийся уравнению ; Cidempv n ; Cidemvp 1 n/1 n 22 n 11 vpvp
 где п – показатель политропы, являющий в рассматриваемом процессе постоянной величиной, которая может иметь любые частные значения — положительные и отрицательные (- n + ). Физический смысл показателя политропы п определяется после дифференцирования уравнения политропы0 pdvvndpv 1 nn ; Cidempv n 2, 1 l w pdv vdp n
где п – показатель политропы, являющий в рассматриваемом процессе постоянной величиной, которая может иметь любые частные значения — положительные и отрицательные (- n + ). Физический смысл показателя политропы п определяется после дифференцирования уравнения политропы0 pdvvndpv 1 nn ; Cidempv n 2, 1 l w pdv vdp n

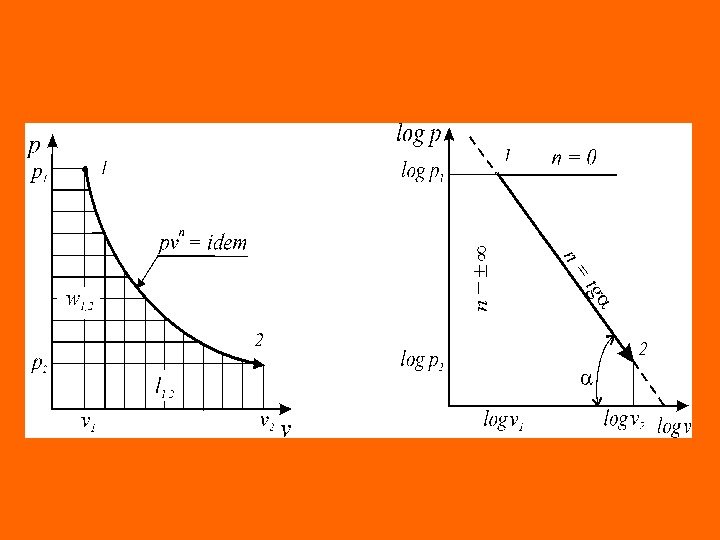
 Это значит, что постоянный показатель политропы определяется соотношением потенциальной и термодинамической работ в элементарном или конечном процессах. Значения этих работ могут быть определены графически в координатах В логарифмических координатах политропный процесс ( политропа ) с постоянным показателем представляет собой прямую линию При этом, постоянный показатель политропы определяется как тангенс угла наклона линии процесса к оси абсцисс ( )vp Clogvlognplog
Это значит, что постоянный показатель политропы определяется соотношением потенциальной и термодинамической работ в элементарном или конечном процессах. Значения этих работ могут быть определены графически в координатах В логарифмических координатах политропный процесс ( политропа ) с постоянным показателем представляет собой прямую линию При этом, постоянный показатель политропы определяется как тангенс угла наклона линии процесса к оси абсцисс ( )vp Clogvlognplog
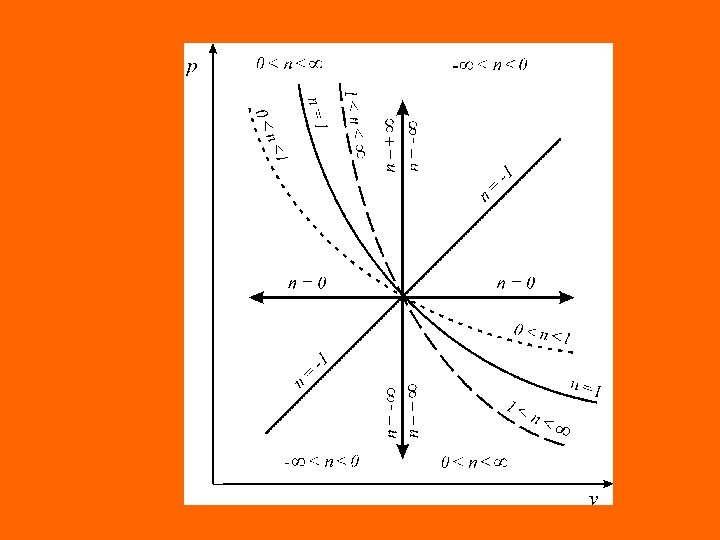
 Из соотношения показателя политропи следует, что для изобарного процесса , для изохорного процесса nv = ± ∞ , для изопотенциальног процесса npv = 1 (для идеального газа =1 , это означает, что для идеального газа изоротенциальный, изотермический, изоэнергетический и изоэнтальпийный процессы совпа дают), для адиабатного процесс n = k. hutpvnnnn tg vlogd pdv vdp l w n )v/vlog( )p/plog( 12 21 0 np
Из соотношения показателя политропи следует, что для изобарного процесса , для изохорного процесса nv = ± ∞ , для изопотенциальног процесса npv = 1 (для идеального газа =1 , это означает, что для идеального газа изоротенциальный, изотермический, изоэнергетический и изоэнтальпийный процессы совпа дают), для адиабатного процесс n = k. hutpvnnnn tg vlogd pdv vdp l w n )v/vlog( )p/plog( 12 21 0 np
 Работа в политропных процессах Выражения конечных (интегральных) величин термодинамической и потенциальных работ в политро- пных процессах для идеального газа pv = RT и 12 11 22 2, 1 T T vp vp ; 1 1 n vp l 2, 1 11 2, 1112, 11 vp 1 n n lnw 11 22 2, 1 vp vp n 1 n 1 2 p p 1 n 2 1 v v
Работа в политропных процессах Выражения конечных (интегральных) величин термодинамической и потенциальных работ в политро- пных процессах для идеального газа pv = RT и 12 11 22 2, 1 T T vp vp ; 1 1 n vp l 2, 1 11 2, 1112, 11 vp 1 n n lnw 11 22 2, 1 vp vp n 1 n 1 2 p p 1 n 2 1 v v
 Теплообмен в политропном процессе для простых тел выводится также на основе рассмотрения выражения первого начала термодинамики . lduq dp dp u dv dv u du vp Последнее выражение можно представить в виде. Удельная внутренняя энергия для простых тел может быть представлена в виде функции u =и ( p , v ). Тогда дифференциал внутренней энергии запишется в следующем виде: vdp dp u v 1 pdv dv u p 1 du vp
Теплообмен в политропном процессе для простых тел выводится также на основе рассмотрения выражения первого начала термодинамики . lduq dp dp u dv dv u du vp Последнее выражение можно представить в виде. Удельная внутренняя энергия для простых тел может быть представлена в виде функции u =и ( p , v ). Тогда дифференциал внутренней энергии запишется в следующем виде: vdp dp u v 1 pdv dv u p 1 du vp
 Введем следующие обозначения: , dv u p 1 a p v dp u v 1 a v p При этом выражение примет вид: l)ana(lnala waladu pvpv pv Подставив полученное уравнение в выражение первого начала термодинамики . lduq получим
Введем следующие обозначения: , dv u p 1 a p v dp u v 1 a v p При этом выражение примет вид: l)ana(lnala waladu pvpv pv Подставив полученное уравнение в выражение первого начала термодинамики . lduq получим
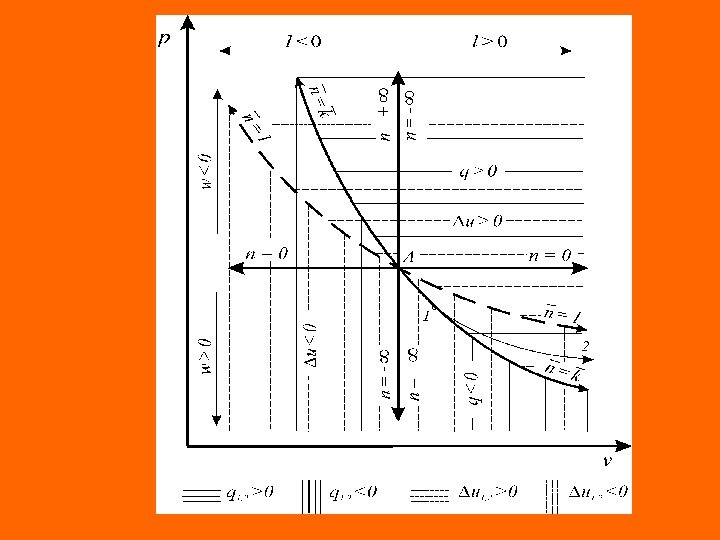
 Для определения величин ( и ) рассмотрим два термодинамических процесса: . l)1 ana(qpv vapa Изоэнергетический процесс ( u = idem , du = 0 , n = n u. ) Так как в изоэнергетическом процессе , 0 l , 0 anapuv ana Адиабатный процесс ( q = 0 ). Для этого процесса показатель политропы принимает значение n = k и элемен- тарная термодинамическая работа также не равна нулю , nk 1 a u p nk n a u u v отсюда 1 kaan, 01 akappupv
Для определения величин ( и ) рассмотрим два термодинамических процесса: . l)1 ana(qpv vapa Изоэнергетический процесс ( u = idem , du = 0 , n = n u. ) Так как в изоэнергетическом процессе , 0 l , 0 anapuv ana Адиабатный процесс ( q = 0 ). Для этого процесса показатель политропы принимает значение n = k и элемен- тарная термодинамическая работа также не равна нулю , nk 1 a u p nk n a u u v отсюда 1 kaan, 01 akappupv
 С учетом полученных соотношений для определения av и a p , находим выражения для расчета удельных значений изменения внутренней энергии и теплообмена в элементарном процессе: , l nk nn du u u l nk nk q u Соотношения для расчета удельных значений изменения внутренней энергии и теплообмена в конечном процессе имеют следующий вид: ; l nk nn u 2, 1 u u 2, 1 l nk nk q 2, 1 u 2, 1 Для идеального газа n u =
С учетом полученных соотношений для определения av и a p , находим выражения для расчета удельных значений изменения внутренней энергии и теплообмена в элементарном процессе: , l nk nn du u u l nk nk q u Соотношения для расчета удельных значений изменения внутренней энергии и теплообмена в конечном процессе имеют следующий вид: ; l nk nn u 2, 1 u u 2, 1 l nk nk q 2, 1 u 2, 1 Для идеального газа n u =



