ПРЕЗЕНТАЦИЯ НА ТЕМУ: Химические элементы IV группы
























































4 гр глав углер.ppt
- Количество слайдов: 59
 ПРЕЗЕНТАЦИЯ НА ТЕМУ: Химические элементы IV группы главной подгруппы
ПРЕЗЕНТАЦИЯ НА ТЕМУ: Химические элементы IV группы главной подгруппы
 Элементы главной подгруппы IV группы: углерод С, кремний Si, германий Ge, олово Sn, свинец Pb недавно открытый искусственный радиоактивный элемент флеровий Fl.
Элементы главной подгруппы IV группы: углерод С, кремний Si, германий Ge, олово Sn, свинец Pb недавно открытый искусственный радиоактивный элемент флеровий Fl.
 Общая характеристика элементов IV группы главной подгруппы n. Элементы С Si Ge Sn Pb n Строение внешней электронной оболочки: 2 S 22 P 2 3 S 23 P 2 4 S 24 P 2 5 S 25 P 2 6 S 26 P 2 n Энергия ионизации, э. В 11, 26 8, 15 7, 90 7, 34 7, 42 n Характерная
Общая характеристика элементов IV группы главной подгруппы n. Элементы С Si Ge Sn Pb n Строение внешней электронной оболочки: 2 S 22 P 2 3 S 23 P 2 4 S 24 P 2 5 S 25 P 2 6 S 26 P 2 n Энергия ионизации, э. В 11, 26 8, 15 7, 90 7, 34 7, 42 n Характерная

 Аллотропные модификации углерода n алмаз n графит n карбин
Аллотропные модификации углерода n алмаз n графит n карбин
 n Кристаллическая решетка - атомная. n У атома углерода - sp 3 -гибридизация. n Алмаз имеет высокую твердость, плотность 3, 5 г/см 2, плохо проводит тепло, не проводит электрический ток, преломляет свет. n tпл =3730 С. n Его применяют как украшение, для резки стекла, бурения горных пород, шлифования особо твердых материалов.
n Кристаллическая решетка - атомная. n У атома углерода - sp 3 -гибридизация. n Алмаз имеет высокую твердость, плотность 3, 5 г/см 2, плохо проводит тепло, не проводит электрический ток, преломляет свет. n tпл =3730 С. n Его применяют как украшение, для резки стекла, бурения горных пород, шлифования особо твердых материалов.
 n Видоизменения графита - кокс, сажа, древесный уголь. n Углерод в графите находится в состоянии sp 2– гибридизации. n Графит - жирное на ощупь вещество с металлическим блеском, тугоплавок, полупроводник, мягок, легко расслаивается. n Из графита изготавливают огнестойкие, химически устойчивые изделия, карандаши, краски, смазки. Графит применяется в электротехнике, в атомной технике как замедлитель нейтронов, изоляционный материал.
n Видоизменения графита - кокс, сажа, древесный уголь. n Углерод в графите находится в состоянии sp 2– гибридизации. n Графит - жирное на ощупь вещество с металлическим блеском, тугоплавок, полупроводник, мягок, легко расслаивается. n Из графита изготавливают огнестойкие, химически устойчивые изделия, карандаши, краски, смазки. Графит применяется в электротехнике, в атомной технике как замедлитель нейтронов, изоляционный материал.
 n Представляет собой черный порошок. n Углерод находится в состоянии sp– гибридизации. Ξ С – С Ξ n Карбин является полупроводником. n Впервые карбин получен в 1963 году при каталитическом окислении ацетилена (учеными В. В. Коршак, А. М. Сладковым, В. Ш. Касаточкиным). Позднее карбин обнаружили в природе.
n Представляет собой черный порошок. n Углерод находится в состоянии sp– гибридизации. Ξ С – С Ξ n Карбин является полупроводником. n Впервые карбин получен в 1963 году при каталитическом окислении ацетилена (учеными В. В. Коршак, А. М. Сладковым, В. Ш. Касаточкиным). Позднее карбин обнаружили в природе.
 Химические свойства углерода При нагревании до 800 – 900 о. С 1. С кислородом С+O 2=СO 2 (оксид) 2. С азотом 2 С+N 2=С 2 N 2 (циан) 3. С серой С+2 S=СS 2(сероуглерод) 4. С водородом С+2 H 2=СH 4 (метан) 5. С кремнием С+Si=Si. C (карборунд) 6. С металлами 3 C + 4 Al = Al 4 C 3 (карбид алюминия) 7. С оксидами Cu. O + C = CO 2 +Cu металлов
Химические свойства углерода При нагревании до 800 – 900 о. С 1. С кислородом С+O 2=СO 2 (оксид) 2. С азотом 2 С+N 2=С 2 N 2 (циан) 3. С серой С+2 S=СS 2(сероуглерод) 4. С водородом С+2 H 2=СH 4 (метан) 5. С кремнием С+Si=Si. C (карборунд) 6. С металлами 3 C + 4 Al = Al 4 C 3 (карбид алюминия) 7. С оксидами Cu. O + C = CO 2 +Cu металлов
 n Адсорбция - свойство угля и других твёрдых веществ удерживать на своей поверхности пары, газы и растворённые вещества. n Адсорбент - вещество, на поверхности которого происходит адсорбция.
n Адсорбция - свойство угля и других твёрдых веществ удерживать на своей поверхности пары, газы и растворённые вещества. n Адсорбент - вещество, на поверхности которого происходит адсорбция.
 Нахождение в природе n Свободный углерод находится в природе в виде алмаза и графита. n Основная масса углерода в виде природных и горючих ископаемых n В атмосфере и гидросфере находится в виде диоксида углерода СО 2, (в воздухе 0, 046 % СО 2 по массе). n Углерод входит в состав растений и животных (~18 %). Общее содержание углерода в организме человека достигает 21 %/.
Нахождение в природе n Свободный углерод находится в природе в виде алмаза и графита. n Основная масса углерода в виде природных и горючих ископаемых n В атмосфере и гидросфере находится в виде диоксида углерода СО 2, (в воздухе 0, 046 % СО 2 по массе). n Углерод входит в состав растений и животных (~18 %). Общее содержание углерода в организме человека достигает 21 %/.
 Природные карбонаты кальция и магния мел мрамор доломит известняк
Природные карбонаты кальция и магния мел мрамор доломит известняк
 Горючие ископаемые антрацит природный газ каменный уголь нефть битум торф
Горючие ископаемые антрацит природный газ каменный уголь нефть битум торф
 Шунгит (содержит углерод и оксид кремния) ШУНГИТ
Шунгит (содержит углерод и оксид кремния) ШУНГИТ
 Оксид углерода (II) C Ξ O C O n Газ без цвета и запаха, ядовит. Получается при сгорании угля в недостатке кислорода. n Получение в лабораторных условиях СООН H 2 SO 4→ СО + Н 2 О n Получение в промышленности С+ Н 2 О t→ СО+Н 2 водяной газ
Оксид углерода (II) C Ξ O C O n Газ без цвета и запаха, ядовит. Получается при сгорании угля в недостатке кислорода. n Получение в лабораторных условиях СООН H 2 SO 4→ СО + Н 2 О n Получение в промышленности С+ Н 2 О t→ СО+Н 2 водяной газ
 Химические свойства оксида углерода (II) n 1. Восстановитель Cu. O + CO = Cu + CO 2 n 2. Вступает в реакции присоединения: CO + Cl 2 = COCl 2 (фосген) CO + S = COS (тиооксид углерода) n 3. Выступает в роли лигандов: Ni + 4 CO = [Ni(CO)4] Карбонильные комплексы – ядовитые жидкости; широко используются для получения чистых металлов.
Химические свойства оксида углерода (II) n 1. Восстановитель Cu. O + CO = Cu + CO 2 n 2. Вступает в реакции присоединения: CO + Cl 2 = COCl 2 (фосген) CO + S = COS (тиооксид углерода) n 3. Выступает в роли лигандов: Ni + 4 CO = [Ni(CO)4] Карбонильные комплексы – ядовитые жидкости; широко используются для получения чистых металлов.
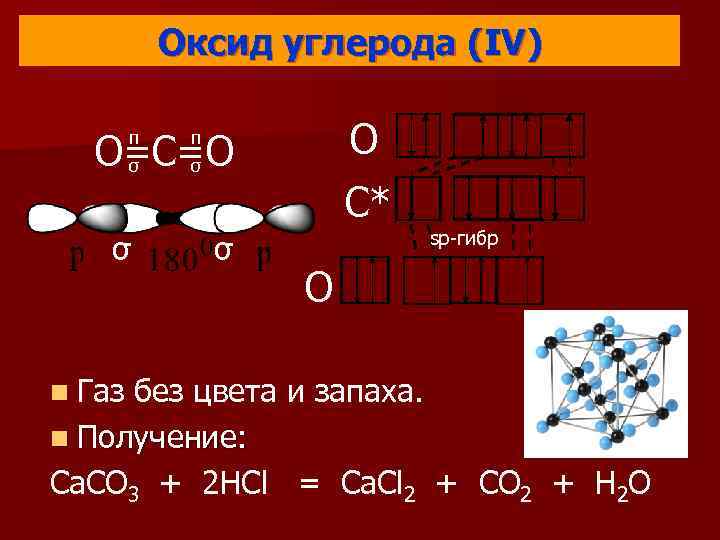
 Оксид углерода (IV) O=С=О σ π σ π O C* sp-гибр σ O n Газ без цвета и запаха. n Получение: Ca. CO 3 + 2 HCl = Ca. Cl 2 + CO 2 + H 2 O
Оксид углерода (IV) O=С=О σ π σ π O C* sp-гибр σ O n Газ без цвета и запаха. n Получение: Ca. CO 3 + 2 HCl = Ca. Cl 2 + CO 2 + H 2 O
 Химические свойства оксида углерода (IV) n Магний горит в углекислом газе Mg + CO 2 = 2 Mg. O + C n При 1000 о. С образуется карбамид (мочевина): СO 2 + 2 NH 3 = CO(NH 2)2 + H 2 O n Является кислотным оксидом: H 2 O + СО 2 H 2 CO 3 n Качественная реакция: CO 2 + Сa(OH)2 = Са. CO 3 + H 2 O Ca. CO 3 + CO 2 + H 2 O = Ca(HCO 3)2
Химические свойства оксида углерода (IV) n Магний горит в углекислом газе Mg + CO 2 = 2 Mg. O + C n При 1000 о. С образуется карбамид (мочевина): СO 2 + 2 NH 3 = CO(NH 2)2 + H 2 O n Является кислотным оксидом: H 2 O + СО 2 H 2 CO 3 n Качественная реакция: CO 2 + Сa(OH)2 = Са. CO 3 + H 2 O Ca. CO 3 + CO 2 + H 2 O = Ca(HCO 3)2
 Химические свойства угольной кислоты n 1. Слабый электролит H 2 CO 3 H+ + HCO 3 – HCO 3– H+ + CO 32– n 2. Разлагается, поэтому в уравнениях пишут не угольную кислоту, а углекислый газ. Карбонаты n 1. Гидролизуются n 2. Нерастворимые карбонаты при нагревании разлагаются Zn. CO 3 = Zn. O + CO 2
Химические свойства угольной кислоты n 1. Слабый электролит H 2 CO 3 H+ + HCO 3 – HCO 3– H+ + CO 32– n 2. Разлагается, поэтому в уравнениях пишут не угольную кислоту, а углекислый газ. Карбонаты n 1. Гидролизуются n 2. Нерастворимые карбонаты при нагревании разлагаются Zn. CO 3 = Zn. O + CO 2
 Сероуглерод CS 2 n Сероуглерод - тяжелая, маслянистая жидкость, хороший растворитель лаков, красок, каучуков. Ядовит. n Легко воспламеняется. n CS 2 является ангидридом тиоугольной кислоты H 2 CS 3 : CS 2 + Na 2 S = Na 2 CS 3 + 2 HCl = H 2 CS 3 + 2 Na. Cl
Сероуглерод CS 2 n Сероуглерод - тяжелая, маслянистая жидкость, хороший растворитель лаков, красок, каучуков. Ядовит. n Легко воспламеняется. n CS 2 является ангидридом тиоугольной кислоты H 2 CS 3 : CS 2 + Na 2 S = Na 2 CS 3 + 2 HCl = H 2 CS 3 + 2 Na. Cl
 Соединения углерода с азотом 2 C + N 2 = (CN)2 n Дициан взаимодействует с водой (CN)2 + 4 H 2 O = (NH 4)2 C 2 O 4 n Дициан взаимодействует со щелочами: (CN)2 + 2 KOH = KCN + KNCO + H 2 O n KCN – соль цианистоводородной кислоты (цианид калия). n KNCO – соль циановой кислоты (цианат калия).
Соединения углерода с азотом 2 C + N 2 = (CN)2 n Дициан взаимодействует с водой (CN)2 + 4 H 2 O = (NH 4)2 C 2 O 4 n Дициан взаимодействует со щелочами: (CN)2 + 2 KOH = KCN + KNCO + H 2 O n KCN – соль цианистоводородной кислоты (цианид калия). n KNCO – соль циановой кислоты (цианат калия).
 Цианистоводородная (синильная) кислота HCN n Бесцветная жидкость с запахом миндаля, сильнейший яд. n Получение (500 о. С, катализатор Th. O 2): NH 3 +CO = HCN + H 2 O n Эта кислота слабее угольной. n Cоли получаются по реакции: K 2 CO 3 + C + 2 NH 3 = 2 KCN + 3 H 2 O n Цианиды используются при извлечении золота из руды и производстве K 4[Fe(CN)6] и K 3[Fe(CN)6].
Цианистоводородная (синильная) кислота HCN n Бесцветная жидкость с запахом миндаля, сильнейший яд. n Получение (500 о. С, катализатор Th. O 2): NH 3 +CO = HCN + H 2 O n Эта кислота слабее угольной. n Cоли получаются по реакции: K 2 CO 3 + C + 2 NH 3 = 2 KCN + 3 H 2 O n Цианиды используются при извлечении золота из руды и производстве K 4[Fe(CN)6] и K 3[Fe(CN)6].
 Соединения углерода с азотом Формула HNCO соответствует трем изомерам: H-O-C N (циановая кислота) H-N=C=O (изоциановая кислота) H-O-N=C (гремучая кислота)
Соединения углерода с азотом Формула HNCO соответствует трем изомерам: H-O-C N (циановая кислота) H-N=C=O (изоциановая кислота) H-O-N=C (гремучая кислота)
 Галогениды углерода n Соединения углерода с галогенами получают косвенным путем, например: CH 4 + Cl 2 = CH 3 Cl + HCl; CH 3 Cl + Cl 2 = CH 2 CL 2 + HCl n Смешанные галогениды CCl 2 F 2, CCl 3 F, CBr 3 F называются фреонами и используются в качестве хладагентов в холодильной технике.
Галогениды углерода n Соединения углерода с галогенами получают косвенным путем, например: CH 4 + Cl 2 = CH 3 Cl + HCl; CH 3 Cl + Cl 2 = CH 2 CL 2 + HCl n Смешанные галогениды CCl 2 F 2, CCl 3 F, CBr 3 F называются фреонами и используются в качестве хладагентов в холодильной технике.
 Кремний
Кремний
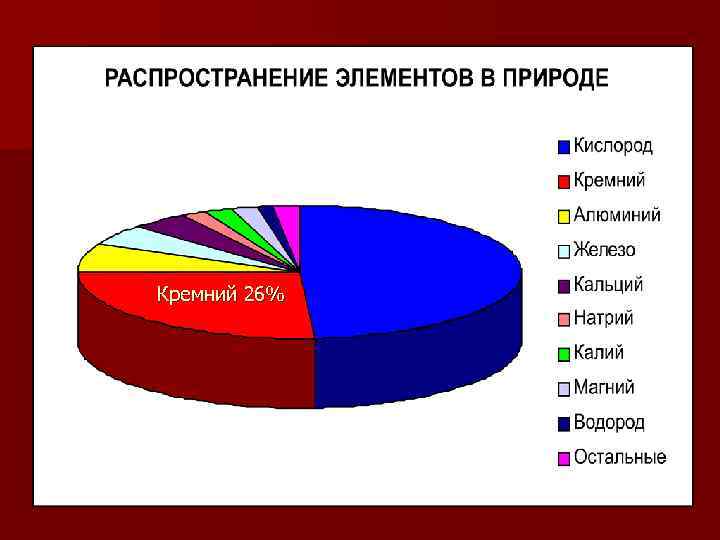
 Кремний 26%
Кремний 26%
 Нахождение в природе n Кремний в природе содержится в минералах в виде оксида Si. O 2 (кремнезем). n Общее число минералов, содержащих кремнезем, превышает 400.
Нахождение в природе n Кремний в природе содержится в минералах в виде оксида Si. O 2 (кремнезем). n Общее число минералов, содержащих кремнезем, превышает 400.
 Разновидности кремнезёма Горный хрусталь Опал
Разновидности кремнезёма Горный хрусталь Опал
 Яшма – загрязненный кремнезем Халцедон
Яшма – загрязненный кремнезем Халцедон
 Разновидности кремнезёма n Окраска цитринов обусловлена присутствием примесей трехвалентного железа цитрин агат
Разновидности кремнезёма n Окраска цитринов обусловлена присутствием примесей трехвалентного железа цитрин агат
 Разновидности кремнезёма Сардоникс Сердолик (оникс) Особенности окраски обусловлены присутствием минерала гематита
Разновидности кремнезёма Сардоникс Сердолик (оникс) Особенности окраски обусловлены присутствием минерала гематита
 Разновидности кремнезёма Цвет аметиста обусловлен примесью Хризопраз органического красящего вещества. (содержит никель)
Разновидности кремнезёма Цвет аметиста обусловлен примесью Хризопраз органического красящего вещества. (содержит никель)
 Алюмосиликаты Полевой шпат Слюда К 2 O∙Al 2 O 3∙ 6 Si. O 2
Алюмосиликаты Полевой шпат Слюда К 2 O∙Al 2 O 3∙ 6 Si. O 2
 Хризолит Ортосиликат железа-магния (Mg, Fe)2 Si. O 4
Хризолит Ортосиликат железа-магния (Mg, Fe)2 Si. O 4
 Получение кремния n Из кремнезема восстанавлением магнием или углеродом : Si. O 2+2 Mg = Si+2 Mg. O Si. O 2+С = Si+СО 2 n При разложении силана: Si. H 4=Si+2 H 2
Получение кремния n Из кремнезема восстанавлением магнием или углеродом : Si. O 2+2 Mg = Si+2 Mg. O Si. O 2+С = Si+СО 2 n При разложении силана: Si. H 4=Si+2 H 2
 Химические свойства Si ØВ реакциях с неметаллами кремний окисляется: Si + O 2 = Si. O 2 Si + 2 F 2 = Si. F 4 Si + C = Si. C ØКремний растворим в щелочах: Si + 2 Na. OH + H 2 O = Na 2 Si. O 3 + 2 H 2 ØНерастворим в кислотах (кроме плавиковой). Si + 4 HF = Si. F 4 + 2 H 2 Si. F 4 + 2 HF = H 2[Si. F 6] ØВ реакциях с металлами восстанавливается: 2 Mg + Si = Mg 2 Si
Химические свойства Si ØВ реакциях с неметаллами кремний окисляется: Si + O 2 = Si. O 2 Si + 2 F 2 = Si. F 4 Si + C = Si. C ØКремний растворим в щелочах: Si + 2 Na. OH + H 2 O = Na 2 Si. O 3 + 2 H 2 ØНерастворим в кислотах (кроме плавиковой). Si + 4 HF = Si. F 4 + 2 H 2 Si. F 4 + 2 HF = H 2[Si. F 6] ØВ реакциях с металлами восстанавливается: 2 Mg + Si = Mg 2 Si
 Химические свойства Si. O 2 – атомная решетка, tпл=1715 о. С, кремний в состоянии sp 3 -гибридизации. Взаимодействует с плавиковой кислотой n Si. O 2 + 4 HF = Si. F 4 + 2 H 2 O Кислотный оксид. Растворяется в щелочах: n Si. O 2 + 2 Na. OH = Na 2 Si. O 3 + H 2 O
Химические свойства Si. O 2 – атомная решетка, tпл=1715 о. С, кремний в состоянии sp 3 -гибридизации. Взаимодействует с плавиковой кислотой n Si. O 2 + 4 HF = Si. F 4 + 2 H 2 O Кислотный оксид. Растворяется в щелочах: n Si. O 2 + 2 Na. OH = Na 2 Si. O 3 + H 2 O
 Кремниевая кислота и силикаты n Na 2 Si. O 3 – силикат натрия (жидкое стекло, конторский клей) в водном растворе сильно гидролизуется. n Кремневую кислоту можно получить взаимодействием соли с любой кислотой: Na 2 Si. O 3 + CO 2 + H 2 O = H 2 Si. O 3 + Na 2 CO 3 n Формулу кремневой кислоты правильно записывать в виде x. Si. O 2 ∙ y. H 2 O. n При прокаливании кремневой кислоты образуется Si. O 2 (силикагель), используется в качестве поглотителя влаги.
Кремниевая кислота и силикаты n Na 2 Si. O 3 – силикат натрия (жидкое стекло, конторский клей) в водном растворе сильно гидролизуется. n Кремневую кислоту можно получить взаимодействием соли с любой кислотой: Na 2 Si. O 3 + CO 2 + H 2 O = H 2 Si. O 3 + Na 2 CO 3 n Формулу кремневой кислоты правильно записывать в виде x. Si. O 2 ∙ y. H 2 O. n При прокаливании кремневой кислоты образуется Si. O 2 (силикагель), используется в качестве поглотителя влаги.
 Водородные соединения кремния n Водородные соединения (силаны) получают из силицидов: Mg 2 Si+4 HCl=2 Mg. Cl 2+Si. H 4 (моносилан) n Силаны могут быть различного состава - Si 2 H 6, Si 3 H 8, Si 6 H 14 , . . . n Это сильные восстановители, химически очень активны, на воздухе самовоспламеняются: Si. H 4 + 2 O 2 = Si. O 2 + 2 H 2 O
Водородные соединения кремния n Водородные соединения (силаны) получают из силицидов: Mg 2 Si+4 HCl=2 Mg. Cl 2+Si. H 4 (моносилан) n Силаны могут быть различного состава - Si 2 H 6, Si 3 H 8, Si 6 H 14 , . . . n Это сильные восстановители, химически очень активны, на воздухе самовоспламеняются: Si. H 4 + 2 O 2 = Si. O 2 + 2 H 2 O
 Стекло n Стекло – аморфный сплав. Имеет только ближний порядок, не имеет четких температур плавления и кипения. n Сырьем для производства стекла являются сода, известняк и песок: Na 2 CO 3 + Ca. CO 3 + 6 Si. O 2 1400 C> Na 2 O∙Ca. O∙ 6 Si. O 2 + 2 CO 2 n Виды стекла: кварцевое стекло, хрусталь (К, Рb), химическое стекло (В)
Стекло n Стекло – аморфный сплав. Имеет только ближний порядок, не имеет четких температур плавления и кипения. n Сырьем для производства стекла являются сода, известняк и песок: Na 2 CO 3 + Ca. CO 3 + 6 Si. O 2 1400 C> Na 2 O∙Ca. O∙ 6 Si. O 2 + 2 CO 2 n Виды стекла: кварцевое стекло, хрусталь (К, Рb), химическое стекло (В)
 Применение
Применение
 Германий
Германий
 Нахождение в природе n Собственные минералы германия встречаются исключительно редко. n Германий встречается с рудами цинка, олова, свинца, присутствует почти во всех силикатах, внедряясь в кристаллические решётки минералов.
Нахождение в природе n Собственные минералы германия встречаются исключительно редко. n Германий встречается с рудами цинка, олова, свинца, присутствует почти во всех силикатах, внедряясь в кристаллические решётки минералов.
 Получение n Вначале получают четыреххлористый германий Ge. Cl 4 , который растворяют в воде : Ge. Cl 4 + H 2 O = Ge. O 2 + 4 HCl n Ge. O 2 + 2 H 2 = Ge + 2 H 2 O
Получение n Вначале получают четыреххлористый германий Ge. Cl 4 , который растворяют в воде : Ge. Cl 4 + H 2 O = Ge. O 2 + 4 HCl n Ge. O 2 + 2 H 2 = Ge + 2 H 2 O
 Химические свойства n При нормальных условиях устойчив к действию воздуха и воды, щелочей и кислот. n При нагревании взаимодействует с кислородом, серой, хлором. Ge + 2 S = Ge. S 2 n Растворим в азотной кислоте, царской водке и в щелочном растворе перекиси водорода: Ge + 4 HNO 3 = H 2 Ge. O 3 + 4 NO 2 + H 2 O Ge + 2 Na. OH + 2 H 2 O 2 = Na 2[Ge(OH)6]
Химические свойства n При нормальных условиях устойчив к действию воздуха и воды, щелочей и кислот. n При нагревании взаимодействует с кислородом, серой, хлором. Ge + 2 S = Ge. S 2 n Растворим в азотной кислоте, царской водке и в щелочном растворе перекиси водорода: Ge + 4 HNO 3 = H 2 Ge. O 3 + 4 NO 2 + H 2 O Ge + 2 Na. OH + 2 H 2 O 2 = Na 2[Ge(OH)6]
 Оксиды германия n Германий образует Ge. O и Ge. O 2 оба оксида амфотерны: Ge. O + 2 HCl = Ge. Cl 2 + H 2 O Ge. O + 2 Na. OH = Na 2 Ge. O 2 + H 2 O германит n Гидролиз солей анионного типа идет практически необратимо: Na 2 Ge. O 2 + 2 H 2 O = 6 Ge(OH)2 ↓ + 2 Na. OH n Соли катионного типа гидролизуются только по I ступени, т. к. получающиеся основные соли выпадают в осадок: Ge. Cl 2 + H 2 O = Ge. OHCl + HCl
Оксиды германия n Германий образует Ge. O и Ge. O 2 оба оксида амфотерны: Ge. O + 2 HCl = Ge. Cl 2 + H 2 O Ge. O + 2 Na. OH = Na 2 Ge. O 2 + H 2 O германит n Гидролиз солей анионного типа идет практически необратимо: Na 2 Ge. O 2 + 2 H 2 O = 6 Ge(OH)2 ↓ + 2 Na. OH n Соли катионного типа гидролизуются только по I ступени, т. к. получающиеся основные соли выпадают в осадок: Ge. Cl 2 + H 2 O = Ge. OHCl + HCl
 Гидроксиды германия n Гидроксиды германия можно получить при действии на соли щелочей: Ge. Cl 2 + 2 Na. OH = Ge(OH)2 ↓ + 2 Na. Cl Ge. Cl 4 + 4 Na. OH = Ge(OH)4 ↓ + 4 Na. Cl n Оба гидроксида амфотерны: Ge(OН)2 + 2 HCl = Ge. Cl 2 + 2 H 2 O Ge(OН)2 + 2 Na. OH = Na 2[Ge(OH)4] Sn(OH)4 + H 2 SO 4 = Sn(SO 4)2 + H 2 O Sn(OH)4 + 2 Na. OH = Na 2[Sn(OH)6]
Гидроксиды германия n Гидроксиды германия можно получить при действии на соли щелочей: Ge. Cl 2 + 2 Na. OH = Ge(OH)2 ↓ + 2 Na. Cl Ge. Cl 4 + 4 Na. OH = Ge(OH)4 ↓ + 4 Na. Cl n Оба гидроксида амфотерны: Ge(OН)2 + 2 HCl = Ge. Cl 2 + 2 H 2 O Ge(OН)2 + 2 Na. OH = Na 2[Ge(OH)4] Sn(OH)4 + H 2 SO 4 = Sn(SO 4)2 + H 2 O Sn(OH)4 + 2 Na. OH = Na 2[Sn(OH)6]
 Применение n Применение находят сплавы германия и стёкла на основе диоксида германия. Полупроводниковая техника Дозиметрические приборы Инфракрасная техника
Применение n Применение находят сплавы германия и стёкла на основе диоксида германия. Полупроводниковая техника Дозиметрические приборы Инфракрасная техника
 Олово и свинец
Олово и свинец
 Нахождение в природе. Нахождение в природе Получение. n В природе олово и свинец обычно встречаются в виде: Sn. O 2 – кассетерит, Pb. S – свинцовый блеск. n Олово получают восста- новлением углеродом из оксида. n Свинец получают обжигом сульфида с последующим восстановлением СО : 2 Pb. S + 3 О 2 = 2 Pb. О + 2 SО 2 Pb. О + СО = Pb + СО 2
Нахождение в природе. Нахождение в природе Получение. n В природе олово и свинец обычно встречаются в виде: Sn. O 2 – кассетерит, Pb. S – свинцовый блеск. n Олово получают восста- новлением углеродом из оксида. n Свинец получают обжигом сульфида с последующим восстановлением СО : 2 Pb. S + 3 О 2 = 2 Pb. О + 2 SО 2 Pb. О + СО = Pb + СО 2
 «Оловянная чума» n При температуре ниже 13, 2 °C β-олово переходит в α - модификацию. происходит увеличение удельного объёма олова на 25, 6 %. Олово трескается и превращается в порошок. Причём соприкосновение серого (α-) олова и белого (β-) приводит к «заражению» последнего. Эти явления называют «оловянной чумой» . n «Оловянная чума» — одна из причин гибели экспедиции Скотта к Южному полюсу в 1912 г. Она осталась без горючего из-за того, что топливо просочилось из запаянных оловом баков, поражённых «оловянной чумой» . n «Оловянная чума» — одно из обстоятельств поражения армии Наполеона в России — сильные морозы привели к превращению оловянных пуговиц на мундирах солдат в порошок.
«Оловянная чума» n При температуре ниже 13, 2 °C β-олово переходит в α - модификацию. происходит увеличение удельного объёма олова на 25, 6 %. Олово трескается и превращается в порошок. Причём соприкосновение серого (α-) олова и белого (β-) приводит к «заражению» последнего. Эти явления называют «оловянной чумой» . n «Оловянная чума» — одна из причин гибели экспедиции Скотта к Южному полюсу в 1912 г. Она осталась без горючего из-за того, что топливо просочилось из запаянных оловом баков, поражённых «оловянной чумой» . n «Оловянная чума» — одно из обстоятельств поражения армии Наполеона в России — сильные морозы привели к превращению оловянных пуговиц на мундирах солдат в порошок.
 Химические свойства n 1. При нагревании реагируют с кислородом, серой, хлором, не реагируют с водородом, углеродом, азотом. 2 Pb + O 2 = 2 Pb. O Sn + O 2 = Sn. О 2 (Образуется оксидная пассивирующая пленка Sn. О 2) n 2. Олово с водой не взаимодействует. Свинец медленно растворяется в воде: 2 Pb + O 2 + 2 H 2 O = 2 Pb(OH)2 n Олово вытесняет водород из кислот: Sn + H 2 SO 4 (pазб) = Sn. SO 4 + H 2 Sn + 2 HCl = Sn. Cl 2 + H 2 n Аналогичные реакции со свинцом практически не идут, т. к. Pb. Cl 2 и Pb. SO 4 плохо растворимы.
Химические свойства n 1. При нагревании реагируют с кислородом, серой, хлором, не реагируют с водородом, углеродом, азотом. 2 Pb + O 2 = 2 Pb. O Sn + O 2 = Sn. О 2 (Образуется оксидная пассивирующая пленка Sn. О 2) n 2. Олово с водой не взаимодействует. Свинец медленно растворяется в воде: 2 Pb + O 2 + 2 H 2 O = 2 Pb(OH)2 n Олово вытесняет водород из кислот: Sn + H 2 SO 4 (pазб) = Sn. SO 4 + H 2 Sn + 2 HCl = Sn. Cl 2 + H 2 n Аналогичные реакции со свинцом практически не идут, т. к. Pb. Cl 2 и Pb. SO 4 плохо растворимы.
 Химические свойства n Свинец и олово взаимодействуют с разбавленной азотной кислотой: 3 Pb + 8 HNO 3 (разб) = 3 Pb(NO 3)2 + 2 NO + 4 H 2 O 3 Sn + 8 HNO 3 (разб) = 3 Sn(NO 3)2 + 2 NO + 4 H 2 O n. В концентрированной азотной кислоте cвинец пассивируется. Олово взаимодействует с конц HNO 3: Sn + 4 HNO 3 = H 2 Sn. O 3 + 4 NO 2 + H 2 O n. В горячей концентрированной H 2 SO 4 при нагревании олово и свинец растворяются, образуя Sn(SO 4)2 или Pb(SO 4)2 и SO 2. n При нагревании в концентрированных растворах щелочей: Sn + 2 КОН + 4 Н 2 О = K 2[Sn (OH)6] + 2 H 2
Химические свойства n Свинец и олово взаимодействуют с разбавленной азотной кислотой: 3 Pb + 8 HNO 3 (разб) = 3 Pb(NO 3)2 + 2 NO + 4 H 2 O 3 Sn + 8 HNO 3 (разб) = 3 Sn(NO 3)2 + 2 NO + 4 H 2 O n. В концентрированной азотной кислоте cвинец пассивируется. Олово взаимодействует с конц HNO 3: Sn + 4 HNO 3 = H 2 Sn. O 3 + 4 NO 2 + H 2 O n. В горячей концентрированной H 2 SO 4 при нагревании олово и свинец растворяются, образуя Sn(SO 4)2 или Pb(SO 4)2 и SO 2. n При нагревании в концентрированных растворах щелочей: Sn + 2 КОН + 4 Н 2 О = K 2[Sn (OH)6] + 2 H 2
 Оксиды и гидроксиды олова и свинца n Все оксиды и гидроксиды олова и свинца амфотерны. n Pb. O 2 можно получить по реакции: Pb(CH 3 COO)2 + Ca. OCl 2 + H 2 O = Pb. O 2↓ + Ca. Cl 2 + 2 CH 3 COOH n Существует смешанный оксид свинца Pb 3 O 4 – свинцовый сурик. Pb 3 O 4 + 4 HNO 3 = Pb. O 2↓ + 2 Pb(NO 3)2 + 2 H 2 O разб
Оксиды и гидроксиды олова и свинца n Все оксиды и гидроксиды олова и свинца амфотерны. n Pb. O 2 можно получить по реакции: Pb(CH 3 COO)2 + Ca. OCl 2 + H 2 O = Pb. O 2↓ + Ca. Cl 2 + 2 CH 3 COOH n Существует смешанный оксид свинца Pb 3 O 4 – свинцовый сурик. Pb 3 O 4 + 4 HNO 3 = Pb. O 2↓ + 2 Pb(NO 3)2 + 2 H 2 O разб
 Применение олова n Безопасное, нетоксичное, коррозионностойкое покрытие. n В белой жести (лужёное железо) для изготовления тары пищевых продуктов. n В припоях для электроники, в домовых трубопроводах, в подшипниковых сплавах. n Сплав олова с медью — бронза, сплав с цинком (упаковочная фольга). n Дисульфид олова Sn. S 2 применяют в составе красок, имитирующих позолоту ( «поталь» ).
Применение олова n Безопасное, нетоксичное, коррозионностойкое покрытие. n В белой жести (лужёное железо) для изготовления тары пищевых продуктов. n В припоях для электроники, в домовых трубопроводах, в подшипниковых сплавах. n Сплав олова с медью — бронза, сплав с цинком (упаковочная фольга). n Дисульфид олова Sn. S 2 применяют в составе красок, имитирующих позолоту ( «поталь» ).
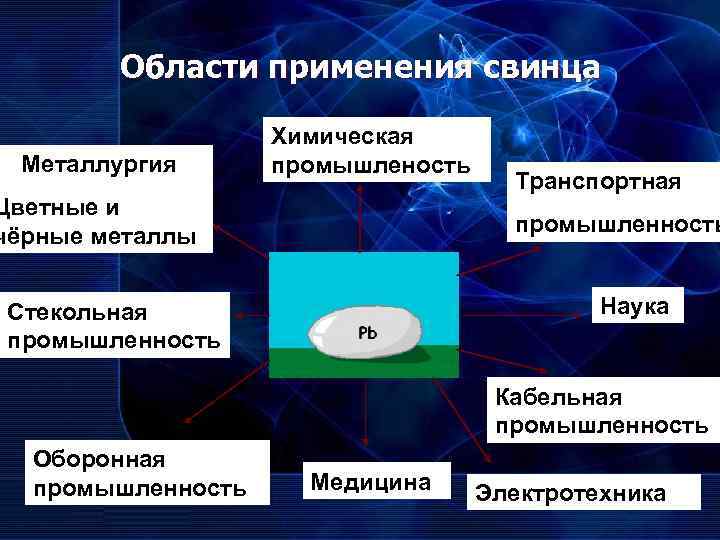
 Области применения свинца Химическая Металлургия промышленость Транспортная Цветные и чёрные металлы промышленность Стекольная Наука промышленность Кабельная промышленность Оборонная промышленность Медицина Электротехника
Области применения свинца Химическая Металлургия промышленость Транспортная Цветные и чёрные металлы промышленность Стекольная Наука промышленность Кабельная промышленность Оборонная промышленность Медицина Электротехника
 Флеровий n Флеро вий (лат. Flerovium, Fl), ранее был известен как унунква дий (лат. Ununquadium, Uuq), использовалось также неофициальное название эка-свинец — 114 -й химический элемент периодической системы.
Флеровий n Флеро вий (лат. Flerovium, Fl), ранее был известен как унунква дий (лат. Ununquadium, Uuq), использовалось также неофициальное название эка-свинец — 114 -й химический элемент периодической системы.
 Изотопы
Изотопы
 Химические свойства n В некоторых исследованиях были получены указания на то, что Флеровий по химическим свойствам похож не на свинец, а на благородные газы. Это поведение объясняется заполнением стабилизирующей 7 p 2 подоболочки валентных электронов, предсказанной расчётами с учётом релятивистских эффектов в электронной оболочке сверхтяжёлых атомов.
Химические свойства n В некоторых исследованиях были получены указания на то, что Флеровий по химическим свойствам похож не на свинец, а на благородные газы. Это поведение объясняется заполнением стабилизирующей 7 p 2 подоболочки валентных электронов, предсказанной расчётами с учётом релятивистских эффектов в электронной оболочке сверхтяжёлых атомов.
