Презентация Медкниги Снижение электрической прочности и электрический пробой мембран











































medknigi_snighenie_elektricheskoy_prochnosti_i_elektricheskiy_proboy_membran.ppt
- Размер: 2.9 Mегабайта
- Количество слайдов: 45
Описание презентации Презентация Медкниги Снижение электрической прочности и электрический пробой мембран по слайдам
 Снижение электрической прочности и электрический пробой мембран Учебник Биофизики ЧАСТЬ 4. Физико-химические основы патологии клетки
Снижение электрической прочности и электрический пробой мембран Учебник Биофизики ЧАСТЬ 4. Физико-химические основы патологии клетки
 ЭЭ лектрический пробой плоских фосфолипидных мембран (БЛМ)
ЭЭ лектрический пробой плоских фосфолипидных мембран (БЛМ)
 Приготовление БЛМ А В Г 1 54 32 Б
Приготовление БЛМ А В Г 1 54 32 Б
 Установка для получсения БЛМ и измерения ее электрических свойств
Установка для получсения БЛМ и измерения ее электрических свойств
 БЛМ как объект изучения ионной проницаемости липидного слоя мембран HCl U VV AA IR i R u Электроды Электролит БЛМИсточник тока
БЛМ как объект изучения ионной проницаемости липидного слоя мембран HCl U VV AA IR i R u Электроды Электролит БЛМИсточник тока
 Зависимость времени жизни липидных пор от напряжения (V)6 4 2 0, 4 0, 6ФХ + лизо. ФХ ФЭ ФХ L g м с. Точки – эксперимент Линии — теория
Зависимость времени жизни липидных пор от напряжения (V)6 4 2 0, 4 0, 6ФХ + лизо. ФХ ФЭ ФХ L g м с. Точки – эксперимент Линии — теория
 ПП робой БЛМ при действии постоянного электрического поля
ПП робой БЛМ при действии постоянного электрического поля
 BLM as a tool to measure membrane ionic permeability HCl U Iemp R i R u emp — electro motive force. The potential difference applied to our system from an external source. U — membrane potential. I — membrane current. Electrode Electrolyte Bilayer lipid membrane (BLM)Voltmeter Ampermeter
BLM as a tool to measure membrane ionic permeability HCl U Iemp R i R u emp — electro motive force. The potential difference applied to our system from an external source. U — membrane potential. I — membrane current. Electrode Electrolyte Bilayer lipid membrane (BLM)Voltmeter Ampermeter
 Измерение потенциала на мембране (слева) и тока через мембрану (справа) R o – нагрузочное сопротивление , R i – внутреннее сопротивление милливольтметра , R m – сопротивление БЛМ. При снижении R m ток через мембрану и потенциал на мембране уменьшаются. R i R m. R om i m
Измерение потенциала на мембране (слева) и тока через мембрану (справа) R o – нагрузочное сопротивление , R i – внутреннее сопротивление милливольтметра , R m – сопротивление БЛМ. При снижении R m ток через мембрану и потенциал на мембране уменьшаются. R i R m. R om i m
 Вольт-амперные характеристики БЛМ 40 80 1200Т о к , п А Разость потенциалов, м. В + 20% холестерина+ УФ контроль
Вольт-амперные характеристики БЛМ 40 80 1200Т о к , п А Разость потенциалов, м. В + 20% холестерина+ УФ контроль
 ““ Динамический” метод измерения потенциала пробоя БЛМБЛМ Время, с0 30 60 90 120200 150 100 50 0U (m. V) Выкл Вкл. U * Потенциал пробоя Стресс
““ Динамический” метод измерения потенциала пробоя БЛМБЛМ Время, с0 30 60 90 120200 150 100 50 0U (m. V) Выкл Вкл. U * Потенциал пробоя Стресс
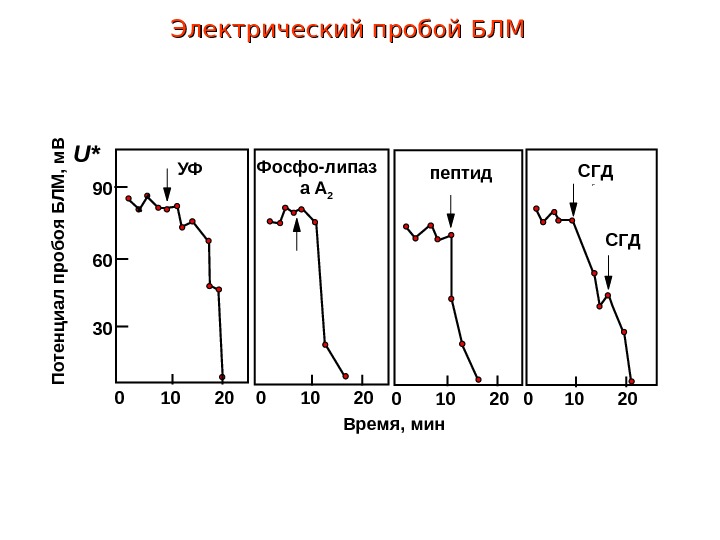
 Электрический пробой БЛМ PУФ Фосфо-липаз а A 2 пептид СГД 0 20100 2010 Время, мин. U* 306090П о те н ц и ал п р о б о я Б Л М , м В СГД
Электрический пробой БЛМ PУФ Фосфо-липаз а A 2 пептид СГД 0 20100 2010 Время, мин. U* 306090П о те н ц и ал п р о б о я Б Л М , м В СГД
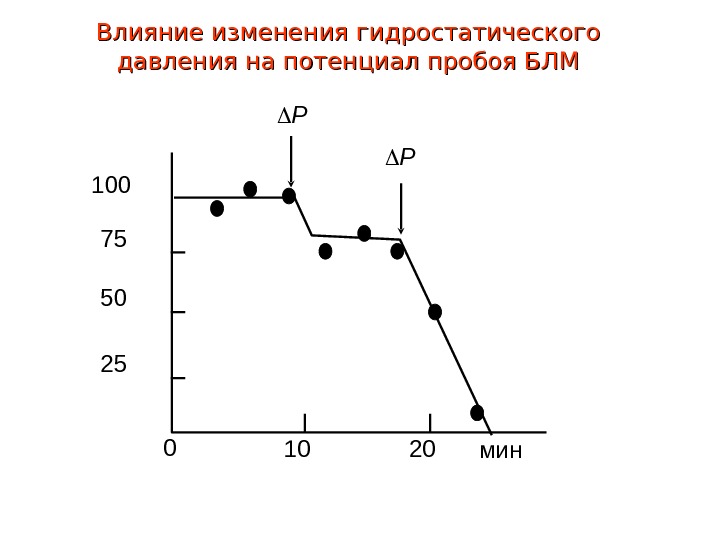
 Влияние изменения гидростатического давления на потенциал пробоя БЛМ P P 100 75 50 25 0 10 20 мин
Влияние изменения гидростатического давления на потенциал пробоя БЛМ P P 100 75 50 25 0 10 20 мин
 Влияние пробоя на электрическую прочность БЛМБЛМ Смирнов, А. А. ; Путвинский, А. В. ; Рощупкин, Д. И. ; Владимиров, Ю. А. Необратимое повреждение липидных бислойных мембран в состоянии электрического пробоя. Биофизика 25 : 140-142 (1980). 1 – Контроль 2 – 1 + пробой 3 – 2 + Са 2+ 4 – 1 + УФ 68 4 82 10050 150 Напряжение (m. V)4 2 3 1С и л а т о к а , п А
Влияние пробоя на электрическую прочность БЛМБЛМ Смирнов, А. А. ; Путвинский, А. В. ; Рощупкин, Д. И. ; Владимиров, Ю. А. Необратимое повреждение липидных бислойных мембран в состоянии электрического пробоя. Биофизика 25 : 140-142 (1980). 1 – Контроль 2 – 1 + пробой 3 – 2 + Са 2+ 4 – 1 + УФ 68 4 82 10050 150 Напряжение (m. V)4 2 3 1С и л а т о к а , п А
 ПП робой мембран собственным (ионным диффузионным) потенциалом
ПП робой мембран собственным (ионным диффузионным) потенциалом
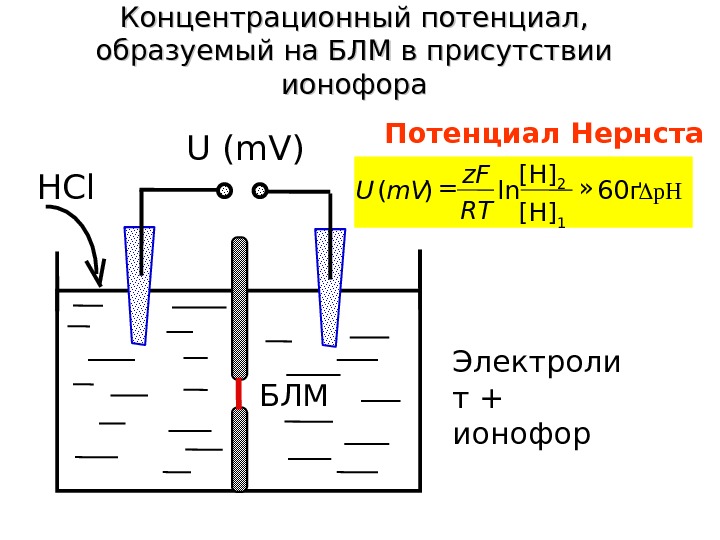
 Концентрационный потенциал, образуемый на БЛМ в присутствии ионофора Потенциал Нернста 60 ґ p. Hln)( » = [H] 2 RT z. F m. VU [H] 1HCl U (m. V) Электроли т + ионофор. БЛМ
Концентрационный потенциал, образуемый на БЛМ в присутствии ионофора Потенциал Нернста 60 ґ p. Hln)( » = [H] 2 RT z. F m. VU [H] 1HCl U (m. V) Электроли т + ионофор. БЛМ
 Самопробой БЛМ при высоком ионном диффузионном потенциале 1 2 3 4 5 6 7 8 9120 100 80 60 40 20 0П о т е н ц и а л н а м е м б р а н е , м В Время, мин p. H = 1. 2 p. H = 3. 2 Потенциал Нернста Потенциал пробоя
Самопробой БЛМ при высоком ионном диффузионном потенциале 1 2 3 4 5 6 7 8 9120 100 80 60 40 20 0П о т е н ц и а л н а м е м б р а н е , м В Время, мин p. H = 1. 2 p. H = 3. 2 Потенциал Нернста Потенциал пробоя
 Самопробойц БЛМРис. 4. Самопробой БЛМ протонным диффузионным потенциалом HCl (m. V) 1 2 3 4 5 6 7 8 9120 100 80 60 40 20 0 Time (min) p. H = 1. 2 p. H = 3. 2 Измерение потенциала, генерируемого мембраной в результате диффузии ионов в присутствии переносчика протонов Cl. CCP (слева). Запись изменения потенциала (справа). После добавления Cl. CCP с одной стороны мембраны добавляли кислоту для создания разности р. Н ( p. H ). (m V )Потенциал пробоя
Самопробойц БЛМРис. 4. Самопробой БЛМ протонным диффузионным потенциалом HCl (m. V) 1 2 3 4 5 6 7 8 9120 100 80 60 40 20 0 Time (min) p. H = 1. 2 p. H = 3. 2 Измерение потенциала, генерируемого мембраной в результате диффузии ионов в присутствии переносчика протонов Cl. CCP (слева). Запись изменения потенциала (справа). После добавления Cl. CCP с одной стороны мембраны добавляли кислоту для создания разности р. Н ( p. H ). (m V )Потенциал пробоя
 Электрический пробой мембран собственным мембранным потенциалом 2 мин 1 мин 2 5 м В замыкание М ем бр а нн ы й потен ц иа л Cl. CCP замыкание 3 0 м В Val * * П р о б о й Время
Электрический пробой мембран собственным мембранным потенциалом 2 мин 1 мин 2 5 м В замыкание М ем бр а нн ы й потен ц иа л Cl. CCP замыкание 3 0 м В Val * * П р о б о й Время
 Кинетическая кривая изменения протонного диффузионного потенциала при УФ-облучении БЛМ Путвинский, А. В. ; Пучкова, Т. В. Протонная проницаемость и электрический пробой фосфолипидных мембран после УФ-облучения. Биофизика 26 (3): 481-486 (1981)
Кинетическая кривая изменения протонного диффузионного потенциала при УФ-облучении БЛМ Путвинский, А. В. ; Пучкова, Т. В. Протонная проницаемость и электрический пробой фосфолипидных мембран после УФ-облучения. Биофизика 26 (3): 481-486 (1981)
 HCl УФ 40 21020 30 0 64 7. 5 8. 0Потенциал пробоя Время, мин. Самопробой БЛМ при УФ облучении. Р а з н о с т ь п о т е н ц и а л о в , м В
HCl УФ 40 21020 30 0 64 7. 5 8. 0Потенциал пробоя Время, мин. Самопробой БЛМ при УФ облучении. Р а з н о с т ь п о т е н ц и а л о в , м В
 Пробой БЛМ при УФ облучении Путвинский, А. В. ; Пучкова, Т. В. Протонная проницаемость и электрический пробой фосфолипидных мембран после УФ-облучения. Биофизика 26 (3): 481-486 (1981) Рис. 1. Изменение сопротивления БЛМ (R), приготовленных из митохондриальных липидов (а) и яичного лецитина ( б ). Потенциал на мембранах до облучения 28 м. В. Стрелка показывает начало Уф-облучения
Пробой БЛМ при УФ облучении Путвинский, А. В. ; Пучкова, Т. В. Протонная проницаемость и электрический пробой фосфолипидных мембран после УФ-облучения. Биофизика 26 (3): 481-486 (1981) Рис. 1. Изменение сопротивления БЛМ (R), приготовленных из митохондриальных липидов (а) и яичного лецитина ( б ). Потенциал на мембранах до облучения 28 м. В. Стрелка показывает начало Уф-облучения
 Electrical breakdown of BLM under UV
Electrical breakdown of BLM under UV
 Потенциал пробоя БЛМ (Uпр), приготовленных из ми-тохондриальных липидов (а) и яичного лецитина (б)(б) Путвинский, А. В. ; Пучкова, Т. В. Протонная проницаемость и электрический пробой фосфолипидных мембран после УФ-облучения. Биофизика 26 (3): 481-486 (1981)
Потенциал пробоя БЛМ (Uпр), приготовленных из ми-тохондриальных липидов (а) и яичного лецитина (б)(б) Путвинский, А. В. ; Пучкова, Т. В. Протонная проницаемость и электрический пробой фосфолипидных мембран после УФ-облучения. Биофизика 26 (3): 481-486 (1981)
 Пробой БЛМ при разном диффузионном потенциале
Пробой БЛМ при разном диффузионном потенциале
 ЭЭ лектрический пробой фосфолипидных везикул (липосом)
ЭЭ лектрический пробой фосфолипидных везикул (липосом)
 Electrical breakdown of the membrane of liposomes Changes in light transmittancc of liposomal suspension on the addition of СССР (100 nmol/1). Liposomes (0. 2 mg/ml) were formed from egg lecithin in sucrose solution (10 mmol/I) with KAc added: a — 5 mmol/I, b — 15 mmol/I, с — 40 mmol/I.
Electrical breakdown of the membrane of liposomes Changes in light transmittancc of liposomal suspension on the addition of СССР (100 nmol/1). Liposomes (0. 2 mg/ml) were formed from egg lecithin in sucrose solution (10 mmol/I) with KAc added: a — 5 mmol/I, b — 15 mmol/I, с — 40 mmol/I.
 Электрический пробой мембран липосом. С в е т о п р о п у с к а н и е Время а б в TCl. CCPKAc 2 мин 1 %
Электрический пробой мембран липосом. С в е т о п р о п у с к а н и е Время а б в TCl. CCPKAc 2 мин 1 %
![Электрический пробой мембран липосом T / T (о т н. е д. ) Lg [KAc] o Электрический пробой мембран липосом T / T (о т н. е д. ) Lg [KAc] o](/docs//medknigi_snighenie_elektricheskoy_prochnosti_i_elektricheskiy_proboy_membran_images/medknigi_snighenie_elektricheskoy_prochnosti_i_elektricheskiy_proboy_membran_28.jpg) Электрический пробой мембран липосом T / T (о т н. е д. ) Lg [KAc] o / [KAc] i. Мембранный потенциал KAc. Набухание Сжатие 90 60 1209060 -4 -2 0 -1, 5 -2, 0-1, 0 -2-1 0 -1, 5-2, 0 -1,
Электрический пробой мембран липосом T / T (о т н. е д. ) Lg [KAc] o / [KAc] i. Мембранный потенциал KAc. Набухание Сжатие 90 60 1209060 -4 -2 0 -1, 5 -2, 0-1, 0 -2-1 0 -1, 5-2, 0 -1,
 20% холестерина Ac. OK ( м. М)Потенциал на мембране ( м. В)Влияние холестерина на пробой в липосомах
20% холестерина Ac. OK ( м. М)Потенциал на мембране ( м. В)Влияние холестерина на пробой в липосомах
 Breakdown of membrane during continuous introduction of KAc Time-course of light transmittance ( T ) in the liposomal suspension (a) and the calculated membrane potential (b) during continuous introduction of concentrated potassium acetate solution. Liposomes (0. 2 mg lipids/ml) prepared from egg lecithin were formed in 10 mmol/1 sucrose solution. Final concentration of CCCP was 0. 1 mmol/l.
Breakdown of membrane during continuous introduction of KAc Time-course of light transmittance ( T ) in the liposomal suspension (a) and the calculated membrane potential (b) during continuous introduction of concentrated potassium acetate solution. Liposomes (0. 2 mg lipids/ml) prepared from egg lecithin were formed in 10 mmol/1 sucrose solution. Final concentration of CCCP was 0. 1 mmol/l.
 Холестерин увеличивает электрическую прочность мембран липосом. П о т е н ц и а л п р о б о я (м В ) Холестерин / фосфолипиды (моль / моль)
Холестерин увеличивает электрическую прочность мембран липосом. П о т е н ц и а л п р о б о я (м В ) Холестерин / фосфолипиды (моль / моль)
 Снижение мембранного потенциала в липосомах при пероксидации липидов Доза (Дж / см 2 )П о т е н ц и а л п р о б о я (м В ) Продукты ПОЛ (мл) Слева – При УФ-облучении разными дозами. Справа – Про добавлении водорастворимых продуктов пероксидации липидов.
Снижение мембранного потенциала в липосомах при пероксидации липидов Доза (Дж / см 2 )П о т е н ц и а л п р о б о я (м В ) Продукты ПОЛ (мл) Слева – При УФ-облучении разными дозами. Справа – Про добавлении водорастворимых продуктов пероксидации липидов.
 Детергенты снижают электрическую прочность мембран липосом SDS CTAB Triton X-100 Логарифм молярной концентрации детергента. П о т е н ц и а л п р о б о я (м В )
Детергенты снижают электрическую прочность мембран липосом SDS CTAB Triton X-100 Логарифм молярной концентрации детергента. П о т е н ц и а л п р о б о я (м В )
 ЭЭ лектрический пробой мембран эритроцитов
ЭЭ лектрический пробой мембран эритроцитов
 Электрический пробой мембран эритроцитов 5, 8 6, 2 6, 6 7, 0 7, 4 0 20 40 60 минp. H 7 6 5 4 3 2 1 6, 0 6, 4 6, 8 7, 2 7, 6 100 80 60 40 20 0, 3 1, 5 2, 4 3, 2p. H , м. В * Lg ( C i / C o )
Электрический пробой мембран эритроцитов 5, 8 6, 2 6, 6 7, 0 7, 4 0 20 40 60 минp. H 7 6 5 4 3 2 1 6, 0 6, 4 6, 8 7, 2 7, 6 100 80 60 40 20 0, 3 1, 5 2, 4 3, 2p. H , м. В * Lg ( C i / C o )
![[Cl] i and [C 1] o , Cl - - concentrations in the cells [Cl] i and [C 1] o , Cl - - concentrations in the cells](/docs//medknigi_snighenie_elektricheskoy_prochnosti_i_elektricheskiy_proboy_membran_images/medknigi_snighenie_elektricheskoy_prochnosti_i_elektricheskiy_proboy_membran_36.jpg) [Cl] i and [C 1] o , Cl — — concentrations in the cells and in the surrounding isotonic medium, respectively; фm [Сl — ] , membrane (chlorine) potential as calculated by the Nernst equation on the basis of (Сl — ) i /(Cl — )o ratio; ф m (H + ), membrane potential as calculated from the р. Н value arising in the medium after the addition of erythrocytes. The breaks on the curves attest to increased cationic permeability of the membranes. 1, Original erythrocytes; 2, Erythrocytes after UV-induced lipoperoxidation. Note that the peroxidation decreased the critical potential from ф 2 * = 110 to ф 2 * = 93 m. V. Electrical breakdown of erythrocyle membranes by chlorine diffusion potential.
[Cl] i and [C 1] o , Cl — — concentrations in the cells and in the surrounding isotonic medium, respectively; фm [Сl — ] , membrane (chlorine) potential as calculated by the Nernst equation on the basis of (Сl — ) i /(Cl — )o ratio; ф m (H + ), membrane potential as calculated from the р. Н value arising in the medium after the addition of erythrocytes. The breaks on the curves attest to increased cationic permeability of the membranes. 1, Original erythrocytes; 2, Erythrocytes after UV-induced lipoperoxidation. Note that the peroxidation decreased the critical potential from ф 2 * = 110 to ф 2 * = 93 m. V. Electrical breakdown of erythrocyle membranes by chlorine diffusion potential.
 Растяжение мембран эритроцитов снижает потенциал пробоя
Растяжение мембран эритроцитов снижает потенциал пробоя
 Release of hemoglobin from erythrocytes
Release of hemoglobin from erythrocytes
 ЭЭ лектрический пробой мембран митохондрий
ЭЭ лектрический пробой мембран митохондрий
 2 мин 0 100 200 150 100 50U ( м. В ) F (r. u. ) Субстрат Ацетат Электрический пробой внутренней мембраны митохондрий
2 мин 0 100 200 150 100 50U ( м. В ) F (r. u. ) Субстрат Ацетат Электрический пробой внутренней мембраны митохондрий
 Membrane potential changes in mitochondria upon their energization, the addition of permeant acid, and electrical breakdown, as assessed from variations in the fluorescence intensity of the probe di. S-C 3-(5). Precalibration of de-energized mitochondria in a KCl + valinomycin system enabled the variation in fluorescence to be expressed in membrane potential units (ф m , m. V). фs is the change in potential inside the mitochondria after the addition of succinate to the mitochondrial suspension containing rotenone; ф A is the change in potential after the addition of potassium acetate (Ac. OK). When the membrane is broken down electrically, i. e. when ф A ф*, the membrane potential falls ( ).
Membrane potential changes in mitochondria upon their energization, the addition of permeant acid, and electrical breakdown, as assessed from variations in the fluorescence intensity of the probe di. S-C 3-(5). Precalibration of de-energized mitochondria in a KCl + valinomycin system enabled the variation in fluorescence to be expressed in membrane potential units (ф m , m. V). фs is the change in potential inside the mitochondria after the addition of succinate to the mitochondrial suspension containing rotenone; ф A is the change in potential after the addition of potassium acetate (Ac. OK). When the membrane is broken down electrically, i. e. when ф A ф*, the membrane potential falls ( ).
 o 1 2tg 180 190 200 210Потенциал на мембране ( м. В ) 1. 00. 1 10 Концентрация соли ( м. М )Скорость падения мембранного потенциала (tg ) ) при различных потенциалах на внутренней мембране Tg ( см. предыдущий слайд ) – жто скорость падения мембранного потенциала в результате электрического пробоя. Добавление KCl не создает дополнительного потенциала на мембране и не приводит к пробою. При добавлении ацетата пробоцй наступает при мембранном потенциале выше 200 м. В.
o 1 2tg 180 190 200 210Потенциал на мембране ( м. В ) 1. 00. 1 10 Концентрация соли ( м. М )Скорость падения мембранного потенциала (tg ) ) при различных потенциалах на внутренней мембране Tg ( см. предыдущий слайд ) – жто скорость падения мембранного потенциала в результате электрического пробоя. Добавление KCl не создает дополнительного потенциала на мембране и не приводит к пробою. При добавлении ацетата пробоцй наступает при мембранном потенциале выше 200 м. В.
 При добавлении сукцината (S) , а потом — ацетата (Ac. OK) создается мембранный потенциал, величина которого растет с увеличением концентрации Ac. OK. При больших концентрациях Ac. OK (8 и 20 м. М) и, следовательно, — высоких потенциалах (>200 м. В) происходит пробой мембраны и наблюдается набухание митохондрий (tga > 0). Набухание митохондрий в результате электрического пробоя. С в е то п р о п уска н и е Внизу дана зависимость скорости набухания митохондрий (tga) от концентрации ацетата. После УФ облучения потенциал пробоя снижается. Цифры у кривых – доза УФ в милли Эйнштейнах на м 2. Мембранный потенциал Пробой
При добавлении сукцината (S) , а потом — ацетата (Ac. OK) создается мембранный потенциал, величина которого растет с увеличением концентрации Ac. OK. При больших концентрациях Ac. OK (8 и 20 м. М) и, следовательно, — высоких потенциалах (>200 м. В) происходит пробой мембраны и наблюдается набухание митохондрий (tga > 0). Набухание митохондрий в результате электрического пробоя. С в е то п р о п уска н и е Внизу дана зависимость скорости набухания митохондрий (tga) от концентрации ацетата. После УФ облучения потенциал пробоя снижается. Цифры у кривых – доза УФ в милли Эйнштейнах на м 2. Мембранный потенциал Пробой
 УФ-доза, вызывающая набухание митохондрий тем меньше, чем выше мембранный потенциал
УФ-доза, вызывающая набухание митохондрий тем меньше, чем выше мембранный потенциал

