Повторим материал прошлых уроков Тест Выберите все вещества,


Повторим материал прошлых уроков
Тест Выберите все вещества, нерастворимые в воде А) NaBr Б) H2SiO3 В) BaSO4 Г) AlCl3 Д) Fe3PO4 Е) Zn(OH)2 Ж) Ba(OH)2

Подумайте Какой раствор из трех предложенных - насыщенный? А Б В
Тест Отметьте, какие из следующих четырех утверждений относительно растворов правильные, а какие — неправильные. А. Раствор, в котором данное вещество больше не растворяется при данной температуре, называется разбавленный. Б. Максимальное количество вещества, которое растворяется в 100 г воды при данной температуре, называется растворимостью этого вещества. В. Растворы — это простые вещества. Г. В природе чаще встречаются растворы, в которых в качестве растворителя выступает спирт.
Тест Выберите правильное утверждение относительно записи формулы, которая имеет состав CaSO4 · 2H2O. А. Запись CaSO4 · 2H2O означает, что сульфат кальция хорошо растворяется в воде. Б. Запись CaSO4 · 2H2O означает, что в насыщенном растворе сульфата кальция на одну молекулу соли приходится две молекулы воды. В. Запись CaSO4 · 2H2O означает, что в природе сульфат кальция существует в виде кристаллогидрата, в котором на одну молекулу соли приходится две молекулы воды. Г. Запись CaSO4 · 2H2O означает, что гипс при обычных условиях находится в жидком агрегатном состоянии.

Тест Выберите правильные утверждения относительно растворимости веществ. А. При измельчении твердых веществ скорость растворения уменьшается. Б. При повышении температуры растворимость твердых веществ увеличивается. В. Растворимость вещества не зависит ни от каких факторов. Г. При повышении давления растворимость газов уменьшается.

ВЫРАЖЕНИЕ КОЛИЧЕСТВЕННОГО СОСТАВА РАСТВОРА Тема:

Чем отличаются по составу следующие вещества: Дистиллированная вода и морская вода; Кислород и воздух; Сталь и железо; бронза и медь; Глюкоза и мёд Чистое вещество индивидуальное имеющее определённую формулу Смесь веществ, состоит не менее, чем из двух веществ

Качественная характеристика растворов: концентрированный разбавленный

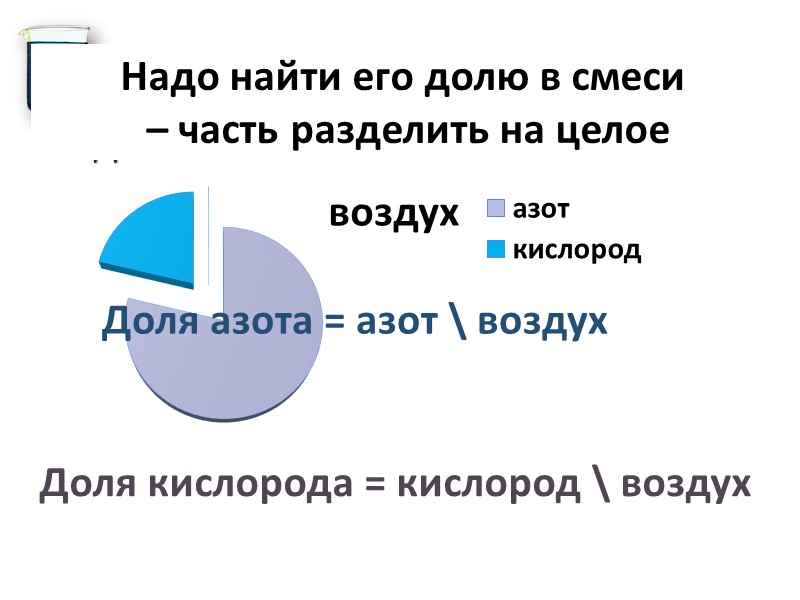
Как определить содержание одного из компонентов смеси? Надо найти его долю в смеси – часть разделить на целое Доля азота = азот \ воздух Доля кислорода = кислород \ воздух

Зачем нам нужны эти расчёты? Можно ли в жизни обойтись без них?

Самостоятельное изготовление физиологического раствора

Количественная характеристика растворов: массовая доля растворенного вещества в растворе Доля - часть от целого

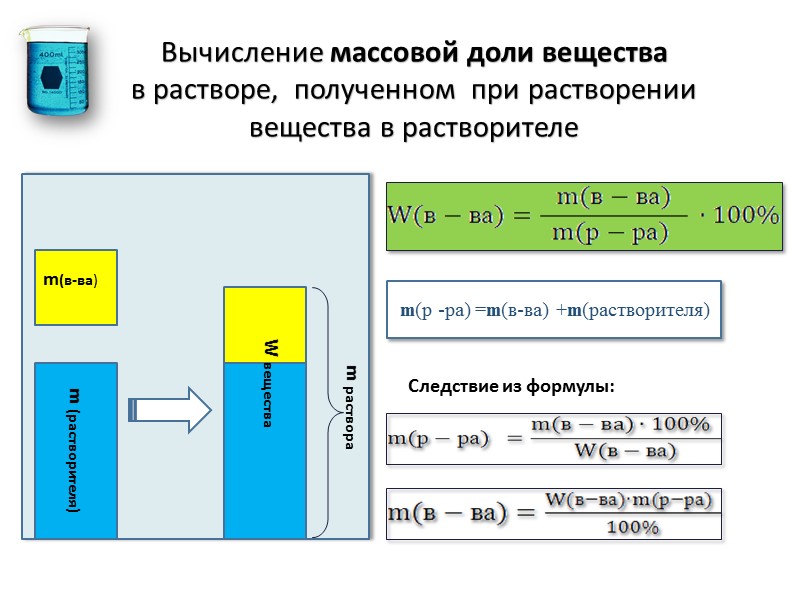
m (растворителя) m(в-ва) m раствора W вещества m(р -ра) =m(в-ва) +m(растворителя) Вычисление массовой доли вещества в растворе, полученном при растворении вещества в растворителе Следствие из формулы:

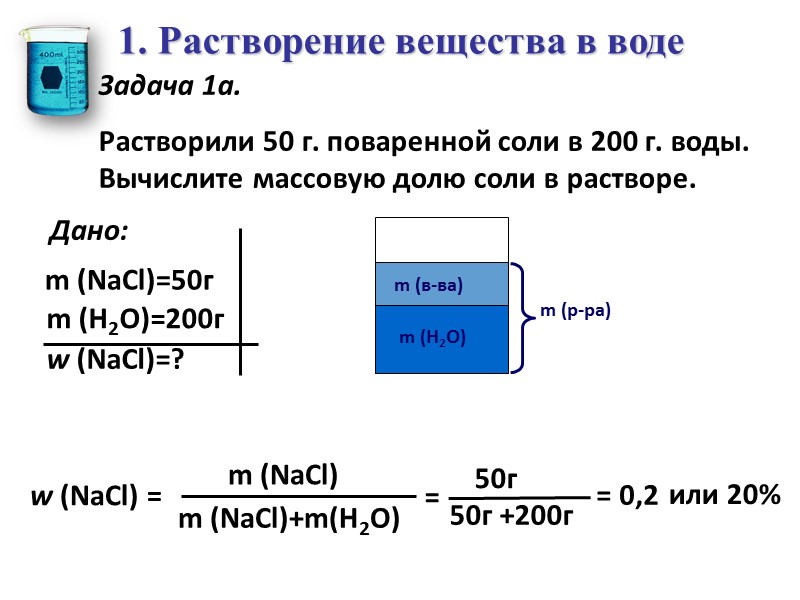
1. Растворение вещества в воде Задача 1а. Растворили 50 г. поваренной соли в 200 г. воды. Вычислите массовую долю соли в растворе. или 20%

1. Растворение вещества в воде Задача 1б. В растворе массой 240 г. содержится 60 г. сахара. Вычислите массовую долю сахара в растворе.

В 300 г морской воды содержится 9 г соли. Вычислите массовую долю соли. Соль тв-ва траствора = = W = ? 9 г ? 300 г ? 9 г 300 г W= тв-ва / траствора 9 г 300 г 0,03 или 3 %
81-8_urok,_9_kl_massovaya_dolya_zadachi.pptx
- Количество слайдов: 21

