Почвоведение. Лекция 4 ППК-кисл..ppt
- Количество слайдов: 12

Поглотительная способность почв Кислотность, щелочность, буферность почвы Экологическое значение поглотительной способности Кафедра ботаники и микробиологии Доцент И. Н. Волкова

Реакция почвенной среды обусловлена наличием и соотношением в почвенном растворе водородных (Н+) и гидроксильных (ОН-) ионов Из одного моля воды при 250 С диссоциирует на ионы 0, 0000001 или 1 x 10 -7 молей воды: [ H+] = [OH-] = 1 x 10 -7 моль/литр Число ионов в чистой воде выражается ионным произведением: К = [H+] x [OH -] = [1 x 10 -7] x [1 x 10 -7 ] = 10 -14

Ионное произведение обозначают показателем р. Н – отрицательный логарифм активности ионов водорода р. Н = - lg [ H+]

Кислотность почвы – способность почв нейтрализовать компоненты щелочной природы, подкислять воду и растворы нейтральных солей Факторы, влияющие на реакцию почвы • • • Химический и минералогический состав почвы Наличие свободных солей Состав почвенного воздуха Влажность Жизнедеятельность организмов

Интервалы значений р. Н почвы 2 -12 • • • Реакция почвенной среды : очень сильнокислая (<4) сильнокислая (4, 1… 4, 5) среднекислая (4, 6. . 5, 0) слабокислая (5, 1… 5, 5) нейтральная (5, 6… 7, 4) слабощелочная (7, 5… 8, 0) среднещелочная (8, 1… 8, 5) сильнощелочная (8, 6… 10) защелоченная (10, 1… 12, 0)
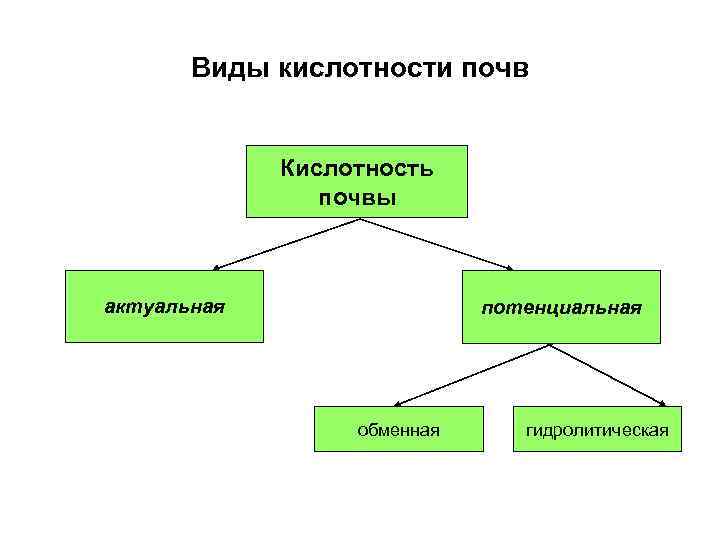
Виды кислотности почв Кислотность почвы актуальная потенциальная обменная гидролитическая

Актуальная кислотность – это концентрация ионов Н+ в почвенном растворе в грамм-эквивалентах (моль) на 1 литр, выражаемая единицами р. Н

Потенциальная кислотность – это количество обменных ионов Н+ и Al 3+, связанных с твердой фазой почвы, выражаемое в милиграммэквивалентах на 100 граммов почвы(м. -экв. /100 г) Обменная кислотность проявляется при взаимодействии с почвой нейтральных солей [ППК]H+ + KCl = [ППK]K+ + HCl Гидролитическая кислотность обнаруживается при воздействии на почву гидролитически щелочных солей [ППК]H+ + CH 3 COONa = [ППK]Na+ + CH 3 COOH

Щелочность почв – способность почв нейтрализовать компоненты кислой природы и подщелачивать воду Актуальная щелочность связана с наличием в почвенном растворе гидролитически щелочных солей (Са. СО 3, Na 2 CO 3, Na. HCO 3, Mg. СО 3, Mg(HСО 3)2 ) Потенциальная щелочность обусловлена наличием в ППК обменно-поглощенного иона натрия [ППК]Na. Na + H 2 CO 3 =[ ППK]HH + Na 2 CO 3

Буферность почвы – способность почвы противостоять изменению реакции почвенного раствора - Буферность почвы зависит от: количества коллоидов и емкости поглощения почвы; химического состава почв; количества и состава обменных катионов; присутствия в почве буферных систем (слабая кислота + слабое основание: H 2 CO 3 + Ca(HСО 3)2 )
![Регулирование почвенной реакции • Известкование [ ППK]HH + Ca(HСО 3)2 [ ППK]HCa + 2 Регулирование почвенной реакции • Известкование [ ППK]HH + Ca(HСО 3)2 [ ППK]HCa + 2](https://present5.com/presentation/3/-29342332_132180847.pdf-img/-29342332_132180847.pdf-11.jpg)
Регулирование почвенной реакции • Известкование [ ППK]HH + Ca(HСО 3)2 [ ППK]HCa + 2 H 2 О +2 CO 2 • Гипсование [ППK]2 Na + Ca. SO 4 [ ППK] Ca. Ca + Na 2 SO 4

Экологическое значение поглотительной способности почв • Образование и стабилизация гумусового профиля почвы за счет сорбционного закрепления гумуса • ППК определяет питательный режим почв, т. к. является доступным хранилищем всех элементов питания растений (биофильных, макро- и микроэлементов), защищающим их от вымывания • От состояния коллоидов зависят физические свойства почв (структура, плотность, водно-воздушные свойства) • Состав ППК определяет реакцию почвенной среды, химический состав почвенного раствора, буферность • ППК является геохимическим барьером для катионовзагрязнителей (тяжелых металлов и радионуклидов)
Почвоведение. Лекция 4 ППК-кисл..ppt