Подготовительная подсистема ХТС 1) Классификация сырья, запасы сырья






















32206-2011_okht_min_lk_2_syryo.ppt
- Количество слайдов: 25
 Подготовительная подсистема ХТС 1) Классификация сырья, запасы сырья и энергии, вторичные материальные и энергетические ресурсы. 2) Рациональное и комплексное использование сырьевых ресурсов. 3) Способы обогащения сырья. 4) Использование воды и воздуха в промышленности. Промышленная водоподготовка.
Подготовительная подсистема ХТС 1) Классификация сырья, запасы сырья и энергии, вторичные материальные и энергетические ресурсы. 2) Рациональное и комплексное использование сырьевых ресурсов. 3) Способы обогащения сырья. 4) Использование воды и воздуха в промышленности. Промышленная водоподготовка.
 Подготовительная подсистема ХТС Сырьё – природные вещества, используемые для переработки в полезные для человека продукты Все вещественные потоки, поступающие в производство называют исходными материалами. Они делятся на сырье, реагенты, вспомогательные материалы. Реагент – химически активный материал, с помощью которого сырье перерабатывают в конечный продукт (кислота, щелочь, окислитель и т.д.), но не содержащий основы (ядра), которая переходила бы в конечный продукт. Вспомогательный материал – вещество, которое необходимо в производстве заданного продукта, т.е. выполняет полезную функцию, но в состав продукта не входит. Не расходуется в процессе. При производстве фосфорной кислоты из апатита и серной кислоты протекает химический процесс: [Ca5(PO4)3F]+5{H2SO4}=3{H3PO4}+5[CaSO4]+HF↑ сырье реагент целевой побочный продукт продукт
Подготовительная подсистема ХТС Сырьё – природные вещества, используемые для переработки в полезные для человека продукты Все вещественные потоки, поступающие в производство называют исходными материалами. Они делятся на сырье, реагенты, вспомогательные материалы. Реагент – химически активный материал, с помощью которого сырье перерабатывают в конечный продукт (кислота, щелочь, окислитель и т.д.), но не содержащий основы (ядра), которая переходила бы в конечный продукт. Вспомогательный материал – вещество, которое необходимо в производстве заданного продукта, т.е. выполняет полезную функцию, но в состав продукта не входит. Не расходуется в процессе. При производстве фосфорной кислоты из апатита и серной кислоты протекает химический процесс: [Ca5(PO4)3F]+5{H2SO4}=3{H3PO4}+5[CaSO4]+HF↑ сырье реагент целевой побочный продукт продукт
 Природные материалы классифицируют: по происхождению – минеральные, растительные и животные; по запасам – невозобновляемые (руды, минералы, горючие ископаемые) и возобновляемые (вода, воздух, растительное и животное сырье); по химическому составу – неорганические (руды, минералы) и органические (нефть, уголь, природный газ); по агрегатному состоянию – твердые (руды, минералы, уголь, сланцы, торф), жидкие (вода, рассолы, нефть) и газообразные (воздух, природный газ). Сырье можно подразделить: Первичное (минеральное, растительное и животное, горючие ископаемые, вода и воздух) Вторичное (промышленные и потребительские отходы)
Природные материалы классифицируют: по происхождению – минеральные, растительные и животные; по запасам – невозобновляемые (руды, минералы, горючие ископаемые) и возобновляемые (вода, воздух, растительное и животное сырье); по химическому составу – неорганические (руды, минералы) и органические (нефть, уголь, природный газ); по агрегатному состоянию – твердые (руды, минералы, уголь, сланцы, торф), жидкие (вода, рассолы, нефть) и газообразные (воздух, природный газ). Сырье можно подразделить: Первичное (минеральное, растительное и животное, горючие ископаемые, вода и воздух) Вторичное (промышленные и потребительские отходы)
 Сырье, применяемое в химико-технологических процессах, должно удовлетворять ряду требований, в частности обеспечивать: минимальное число стадий переработки в конечный продукт; минимальные энергетические и материальные затраты на подготовку сырья к химическому превращению и в целом на осуществление процесса; минимальное рассеяние исходной энергии, т. е. характеризоваться максимумом эксергии; возможно более низкий уровень температуры, давления, расхода энергии на изменение агрегатного состояния реагирующих веществ; максимальную концентрацию полезного компонента (реагента) и, соответственно, максимальную концентрацию целевого продукта в реакционной смеси. Подготовительная подсистема ХТС
Сырье, применяемое в химико-технологических процессах, должно удовлетворять ряду требований, в частности обеспечивать: минимальное число стадий переработки в конечный продукт; минимальные энергетические и материальные затраты на подготовку сырья к химическому превращению и в целом на осуществление процесса; минимальное рассеяние исходной энергии, т. е. характеризоваться максимумом эксергии; возможно более низкий уровень температуры, давления, расхода энергии на изменение агрегатного состояния реагирующих веществ; максимальную концентрацию полезного компонента (реагента) и, соответственно, максимальную концентрацию целевого продукта в реакционной смеси. Подготовительная подсистема ХТС
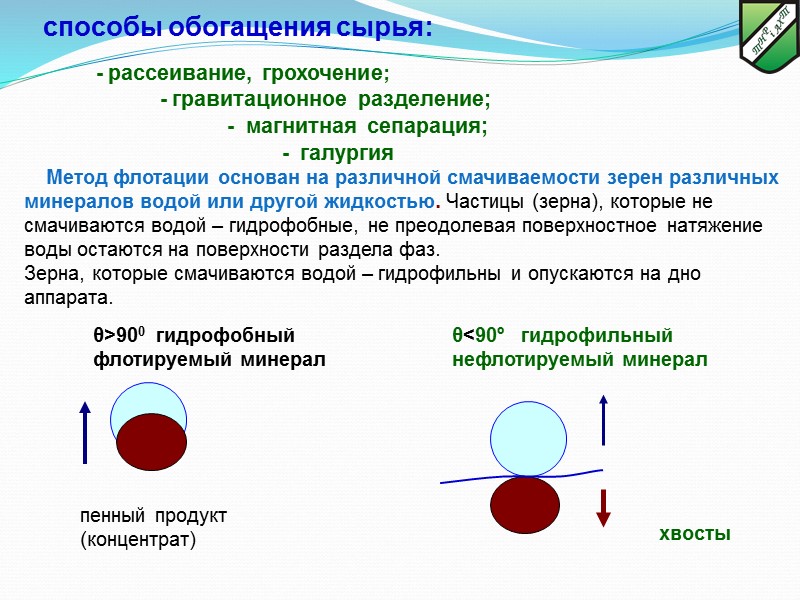
 - рассеивание, грохочение; - гравитационное разделение; - магнитная сепарация; - галургия Метод флотации основан на различной смачиваемости зерен различных минералов водой или другой жидкостью. Частицы (зерна), которые не смачиваются водой – гидрофобные, не преодолевая поверхностное натяжение воды остаются на поверхности раздела фаз. Зерна, которые смачиваются водой – гидрофильны и опускаются на дно аппарата. θ>900 гидрофобный флотируемый минерал способы обогащения сырья: хвосты пенный продукт (концентрат) θ<90º гидрофильный нефлотируемый минерал
- рассеивание, грохочение; - гравитационное разделение; - магнитная сепарация; - галургия Метод флотации основан на различной смачиваемости зерен различных минералов водой или другой жидкостью. Частицы (зерна), которые не смачиваются водой – гидрофобные, не преодолевая поверхностное натяжение воды остаются на поверхности раздела фаз. Зерна, которые смачиваются водой – гидрофильны и опускаются на дно аппарата. θ>900 гидрофобный флотируемый минерал способы обогащения сырья: хвосты пенный продукт (концентрат) θ<90º гидрофильный нефлотируемый минерал
 Чистый кислород, выделяемый ректификацией жидкого воздуха, обычно применяется для кислородной плавки металлов, в доменном процессе и т. п. Азот применяют как сырье в производстве синтетического аммиака и других азотсодержащих веществ и как инертный газ. Жидкий азот в синтезе аммиака используют для промывки конвертированного газа от оксида углерода, метана и аргона. Из воздуха в промышленном масштабе получают почти все инертные газы Использование воды и воздуха в промышленности. Промышленная водоподготовка. Воздух в химической промышленности используют, в основном, как сырье или реагент в технологических процессах, а также для энергетических целей. Состав воздуха об. %: азот – 78,16; кислород – 20,90; аргон – 0,93; гелий, неон, криптон, ксенон и другие инертные газы – 0,01. В технических расчетах принимают, что воздух содержит 79 об. % азота и 21 об. % кислорода.
Чистый кислород, выделяемый ректификацией жидкого воздуха, обычно применяется для кислородной плавки металлов, в доменном процессе и т. п. Азот применяют как сырье в производстве синтетического аммиака и других азотсодержащих веществ и как инертный газ. Жидкий азот в синтезе аммиака используют для промывки конвертированного газа от оксида углерода, метана и аргона. Из воздуха в промышленном масштабе получают почти все инертные газы Использование воды и воздуха в промышленности. Промышленная водоподготовка. Воздух в химической промышленности используют, в основном, как сырье или реагент в технологических процессах, а также для энергетических целей. Состав воздуха об. %: азот – 78,16; кислород – 20,90; аргон – 0,93; гелий, неон, криптон, ксенон и другие инертные газы – 0,01. В технических расчетах принимают, что воздух содержит 79 об. % азота и 21 об. % кислорода.
 Основными источниками водоснабжения промышленных предприятий служат поверхностные и грунтовые воды. Речные воды делятся на маломинерализованные (до 200 мгл), среднеминерализованные (200–500 мгл) и повышенной минерализации (свыше 1000 мгл). Согласно наиболее известной и признанной классификации примесей по фазово-дисперсному составу они делятся на следующие группы: вещества, которые образуют с водой взвеси, суспензии, эмульсии, – удаляются с использованием сил тяжести и адгезии; вещества в коллоидом состоянии и вирусы – удаляются окислением О2, О, Сl2, адсорбцией на золях Al(OH)3, Fe(OH)3; молекулярные растворы, образованные газами и органическими веществами, – удаляются окислением, десорбцией газов и легколетучих веществ, адсорбцией на золях, гелях, твердых сорбентах (уголь), экстракцией (углеводородами), биологической очисткой; ионные растворы (растворы солей, кислот и щелочей) – удаляются переводом в труднорастворимые соединения, ионным обменом, перегонкой, экстракцией, вымораживанием, электродиализом или электроосмосом. Использование воды и воздуха в промышленности. Промышленная водоподготовка.
Основными источниками водоснабжения промышленных предприятий служат поверхностные и грунтовые воды. Речные воды делятся на маломинерализованные (до 200 мгл), среднеминерализованные (200–500 мгл) и повышенной минерализации (свыше 1000 мгл). Согласно наиболее известной и признанной классификации примесей по фазово-дисперсному составу они делятся на следующие группы: вещества, которые образуют с водой взвеси, суспензии, эмульсии, – удаляются с использованием сил тяжести и адгезии; вещества в коллоидом состоянии и вирусы – удаляются окислением О2, О, Сl2, адсорбцией на золях Al(OH)3, Fe(OH)3; молекулярные растворы, образованные газами и органическими веществами, – удаляются окислением, десорбцией газов и легколетучих веществ, адсорбцией на золях, гелях, твердых сорбентах (уголь), экстракцией (углеводородами), биологической очисткой; ионные растворы (растворы солей, кислот и щелочей) – удаляются переводом в труднорастворимые соединения, ионным обменом, перегонкой, экстракцией, вымораживанием, электродиализом или электроосмосом. Использование воды и воздуха в промышленности. Промышленная водоподготовка.
 Распределение воды в мире Общий объем воды на Земле составляет около 1500 млн. куб. км. Если эту воду равномерно распределить по поверхности Земли, то толщина ее слоя составила бы почти 4 км. Из чего же складывается этот запас воды? - Большая часть воды – 97,5% находится в океанах и морях. Эти безбрежные просторы воды малопригодны для человека. Пресная вода составляет всего 2,5 % от всего объёма воды Земли. -Большая часть пресных вод (68,7%) сосредоточена в ледниках Арктики, Антарктики и мало используется человеком. -Значительное количество воды 30,1% содержится в земной коре – подземные воды. -На долю поверхностной и атмосферной воды приходится 0,4 %.
Распределение воды в мире Общий объем воды на Земле составляет около 1500 млн. куб. км. Если эту воду равномерно распределить по поверхности Земли, то толщина ее слоя составила бы почти 4 км. Из чего же складывается этот запас воды? - Большая часть воды – 97,5% находится в океанах и морях. Эти безбрежные просторы воды малопригодны для человека. Пресная вода составляет всего 2,5 % от всего объёма воды Земли. -Большая часть пресных вод (68,7%) сосредоточена в ледниках Арктики, Антарктики и мало используется человеком. -Значительное количество воды 30,1% содержится в земной коре – подземные воды. -На долю поверхностной и атмосферной воды приходится 0,4 %.
 Вода в Беларуси На сегодняшний день в Республике Белерусь при величине эксплуатационных ресурсов подземных вод 18 104 млн. м3 в год и численности населения в 2020 году по прогнозам НИЭИ Минэкономики 9,03 млн. человек потенциальные возможности водообеспечения достигает почти 2005 м3 в год на одного жителя, что в 2 раза превышает критический уровень потребления воды в 1000 м3 в год. И это только за счет наиболее качественных подземных вод, без учета поверхностного стока. Между тем, именно магия приведенных выше чисел, привела к устойчивому заблуждению о высоком качестве наших водных ресурсов. В целом для республики свойственны маломинерализованные подземные воды, которые на участках, не испытывающих природного или хозяйственного загрязнения, отвечают основным требованиям европейского и белорусского стандартов. Вместе с тем выявлены обширные территории, где их качество не соответствует указанным параметрам из-за высокого содержания железа, реже — марганца, бора, бария, кремния, а также почти повсеместно дефицита фтора, йода, селена, что определяется природными геолого-гидрогеологическими условиями страны. В последние десятилетия на состав подземных вод большое влияние оказывают антропогенные загрязнения: промышленное, коммунально-бытовое, сельскохозяйственное, транспортное и др.
Вода в Беларуси На сегодняшний день в Республике Белерусь при величине эксплуатационных ресурсов подземных вод 18 104 млн. м3 в год и численности населения в 2020 году по прогнозам НИЭИ Минэкономики 9,03 млн. человек потенциальные возможности водообеспечения достигает почти 2005 м3 в год на одного жителя, что в 2 раза превышает критический уровень потребления воды в 1000 м3 в год. И это только за счет наиболее качественных подземных вод, без учета поверхностного стока. Между тем, именно магия приведенных выше чисел, привела к устойчивому заблуждению о высоком качестве наших водных ресурсов. В целом для республики свойственны маломинерализованные подземные воды, которые на участках, не испытывающих природного или хозяйственного загрязнения, отвечают основным требованиям европейского и белорусского стандартов. Вместе с тем выявлены обширные территории, где их качество не соответствует указанным параметрам из-за высокого содержания железа, реже — марганца, бора, бария, кремния, а также почти повсеместно дефицита фтора, йода, селена, что определяется природными геолого-гидрогеологическими условиями страны. В последние десятилетия на состав подземных вод большое влияние оказывают антропогенные загрязнения: промышленное, коммунально-бытовое, сельскохозяйственное, транспортное и др.
 Химическая промышленность – крупнейший потребитель воды. Показатели качества воды - Жесткость общая, карбонатная (ммоль эквл) - Щелочность, ммоль эквл - Общее содержание солей, мгл - Окисляемость перманганатная, мг О2л - Химическое потребление кислорода, мг О2л - Содержание, мгл: взвешенных веществ масел и маслообразующих веществ поверхностно-активных веществ (ПАВ) анионов Сl- (хлоридов) анионов SO42- (сульфатов) анионов РО43- (фосфатов) соединений азота в пересчете на ионы тяжелых металлов растворенного кислорода остаточного активного хлора - рН Использование воды и воздуха в промышленности. Промышленная водоподготовка.
Химическая промышленность – крупнейший потребитель воды. Показатели качества воды - Жесткость общая, карбонатная (ммоль эквл) - Щелочность, ммоль эквл - Общее содержание солей, мгл - Окисляемость перманганатная, мг О2л - Химическое потребление кислорода, мг О2л - Содержание, мгл: взвешенных веществ масел и маслообразующих веществ поверхностно-активных веществ (ПАВ) анионов Сl- (хлоридов) анионов SO42- (сульфатов) анионов РО43- (фосфатов) соединений азота в пересчете на ионы тяжелых металлов растворенного кислорода остаточного активного хлора - рН Использование воды и воздуха в промышленности. Промышленная водоподготовка.
 Основой промышленной водоподготовки является совокупность физических и физико-химических процессов, направленных на очистку воды от механических примесей, взвешенных и коллоидных частиц, растворенных солей и газов: Методы осаждения Осветление воды Мембранные методы Адсорбция Обезжелезивание воды Умягчение воды Обессоливание воды Кондиционирование воды Обеззараживание воды Удаление органических загрязнений Дехлорирование воды Удаление нитратов Использование воды и воздуха в промышленности. Промышленная водоподготовка.
Основой промышленной водоподготовки является совокупность физических и физико-химических процессов, направленных на очистку воды от механических примесей, взвешенных и коллоидных частиц, растворенных солей и газов: Методы осаждения Осветление воды Мембранные методы Адсорбция Обезжелезивание воды Умягчение воды Обессоливание воды Кондиционирование воды Обеззараживание воды Удаление органических загрязнений Дехлорирование воды Удаление нитратов Использование воды и воздуха в промышленности. Промышленная водоподготовка.
 Мембранный метод основан на пропускании загрязненного раствора через полупроницаемую перегородку с отверстиями меньшими, чем размер частиц загрязнений. Мембранные процессы включают в себя: макрофильтрацию; микрофильтрацию; ультрафильтрацию; нанофильтрацию; обратный осмос. Осмос (от греч. ὄσμος «толчок, давление») — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону большей концентрации Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос через полупроницаемую мембрану Использование воды и воздуха в промышленности. Промышленная водоподготовка.
Мембранный метод основан на пропускании загрязненного раствора через полупроницаемую перегородку с отверстиями меньшими, чем размер частиц загрязнений. Мембранные процессы включают в себя: макрофильтрацию; микрофильтрацию; ультрафильтрацию; нанофильтрацию; обратный осмос. Осмос (от греч. ὄσμος «толчок, давление») — процесс односторонней диффузии через полупроницаемую мембрану молекул растворителя в сторону большей концентрации Явление осмоса наблюдается в тех средах, где подвижность растворителя больше подвижности растворённых веществ. Важным частным случаем осмоса является осмос через полупроницаемую мембрану Использование воды и воздуха в промышленности. Промышленная водоподготовка.
 Обессоливание воды означает уменьшение содержания в ней растворенных солей. Этот процесс называют также деионизацией, или деминерализацией. Для морских и засоленных (солоноватых) вод такой процесс называют опреснением. Существует несколько способов обессоливания: термический; ионообменный; мембранные; обратный осмос; электродиализ; комбинированные. Осветление воды - это удаление из воды взвешенных и коллоидных веществ, которые окрашивают воду и делают ее мутной. Для осветления воды на станциях водоочистки применяется две технологии: мембранное фильтрование и осаждение. Использование воды и воздуха в промышленности. Промышленная водоподготовка.
Обессоливание воды означает уменьшение содержания в ней растворенных солей. Этот процесс называют также деионизацией, или деминерализацией. Для морских и засоленных (солоноватых) вод такой процесс называют опреснением. Существует несколько способов обессоливания: термический; ионообменный; мембранные; обратный осмос; электродиализ; комбинированные. Осветление воды - это удаление из воды взвешенных и коллоидных веществ, которые окрашивают воду и делают ее мутной. Для осветления воды на станциях водоочистки применяется две технологии: мембранное фильтрование и осаждение. Использование воды и воздуха в промышленности. Промышленная водоподготовка.
 Механическая очистка обеспечивает эффективное удаление из исходной воды: мутности, которая появляется при наличии в воде взвешенных частиц коллоидного железа и кремния, ила, глины, песка, трубопроводной ржавчины и других механических примесей; прозрачности (или светопропускания) природных вод, которая обусловлена их цветом и мутностью, т.е. содержанием в них различных окрашенных и взвешенных органических и минеральных веществ; цветности - показателя качества воды, характеризующего интенсивность окраски воды и обусловленного содержанием окрашенных соединений; выражается в градусах платиново-кобальтовой шкалы. Цветность определяется путем сравнения окраски испытуемой воды с эталонами; привкуса и запаха, которые определяются как естественными, так и искусственными причинами: наличие растворенных нефтепродуктов, хлорокисленной органики и других антропогенных загрязнений. Использование воды и воздуха в промышленности. Промышленная водоподготовка
Механическая очистка обеспечивает эффективное удаление из исходной воды: мутности, которая появляется при наличии в воде взвешенных частиц коллоидного железа и кремния, ила, глины, песка, трубопроводной ржавчины и других механических примесей; прозрачности (или светопропускания) природных вод, которая обусловлена их цветом и мутностью, т.е. содержанием в них различных окрашенных и взвешенных органических и минеральных веществ; цветности - показателя качества воды, характеризующего интенсивность окраски воды и обусловленного содержанием окрашенных соединений; выражается в градусах платиново-кобальтовой шкалы. Цветность определяется путем сравнения окраски испытуемой воды с эталонами; привкуса и запаха, которые определяются как естественными, так и искусственными причинами: наличие растворенных нефтепродуктов, хлорокисленной органики и других антропогенных загрязнений. Использование воды и воздуха в промышленности. Промышленная водоподготовка

 Материальный баланс – это вещественное выражение закона сохранения массы вещества: во всякой замкнутой системе масса веществ, вступивших во взаимодействие равна массе веществ, оставшихся в результате взаимодействия. Для ХТС это значит, что масса веществ, поступивших на технологическую операцию (приход), равна массе веществ, покидающих технологическую операцию (расход) Материальный баланс может быть представлен уравнением, левую часть которого составляет масса всех видов сырья и материалов, поступающих на переработку (Σmприх), а правую – масса получаемых продуктов плюс производственные потери (Σmрасх): Σmприх = Σmрасх. Уравнение материального баланса может быть представлено в следующем виде: m1 + m2 + m3 + m4 = m5 + m6+ m7 + m8 где m1 m2 m3 m4 массы поступившего газообразного, жидкого и твердого сырья и вспомогательного материала; m5, m6 соответственно полученные целевой и побочный продукты; m7 непрореагировавшее сырье; m8 – производственные потери. Материальный баланс химико-технологического процесса
Материальный баланс – это вещественное выражение закона сохранения массы вещества: во всякой замкнутой системе масса веществ, вступивших во взаимодействие равна массе веществ, оставшихся в результате взаимодействия. Для ХТС это значит, что масса веществ, поступивших на технологическую операцию (приход), равна массе веществ, покидающих технологическую операцию (расход) Материальный баланс может быть представлен уравнением, левую часть которого составляет масса всех видов сырья и материалов, поступающих на переработку (Σmприх), а правую – масса получаемых продуктов плюс производственные потери (Σmрасх): Σmприх = Σmрасх. Уравнение материального баланса может быть представлено в следующем виде: m1 + m2 + m3 + m4 = m5 + m6+ m7 + m8 где m1 m2 m3 m4 массы поступившего газообразного, жидкого и твердого сырья и вспомогательного материала; m5, m6 соответственно полученные целевой и побочный продукты; m7 непрореагировавшее сырье; m8 – производственные потери. Материальный баланс химико-технологического процесса
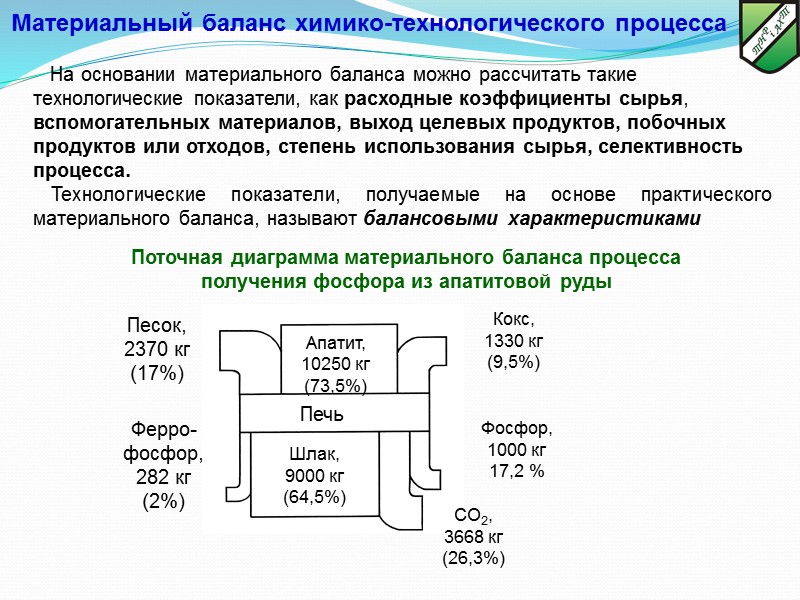
 На основании материального баланса можно рассчитать такие технологические показатели, как расходные коэффициенты сырья, вспомогательных материалов, выход целевых продуктов, побочных продуктов или отходов, степень использования сырья, селективность процесса. Технологические показатели, получаемые на основе практического материального баланса, называют балансовыми характеристиками Печь Шлак, 9000 кг (64,5%) Фосфор, 1000 кг 17,2 % СО2, 3668 кг (26,3%) Апатит, 10250 кг (73,5%) Песок, 2370 кг (17%) Ферро-фосфор, 282 кг (2%) Кокс, 1330 кг (9,5%) Поточная диаграмма материального баланса процесса получения фосфора из апатитовой руды Материальный баланс химико-технологического процесса
На основании материального баланса можно рассчитать такие технологические показатели, как расходные коэффициенты сырья, вспомогательных материалов, выход целевых продуктов, побочных продуктов или отходов, степень использования сырья, селективность процесса. Технологические показатели, получаемые на основе практического материального баланса, называют балансовыми характеристиками Печь Шлак, 9000 кг (64,5%) Фосфор, 1000 кг 17,2 % СО2, 3668 кг (26,3%) Апатит, 10250 кг (73,5%) Песок, 2370 кг (17%) Ферро-фосфор, 282 кг (2%) Кокс, 1330 кг (9,5%) Поточная диаграмма материального баланса процесса получения фосфора из апатитовой руды Материальный баланс химико-технологического процесса
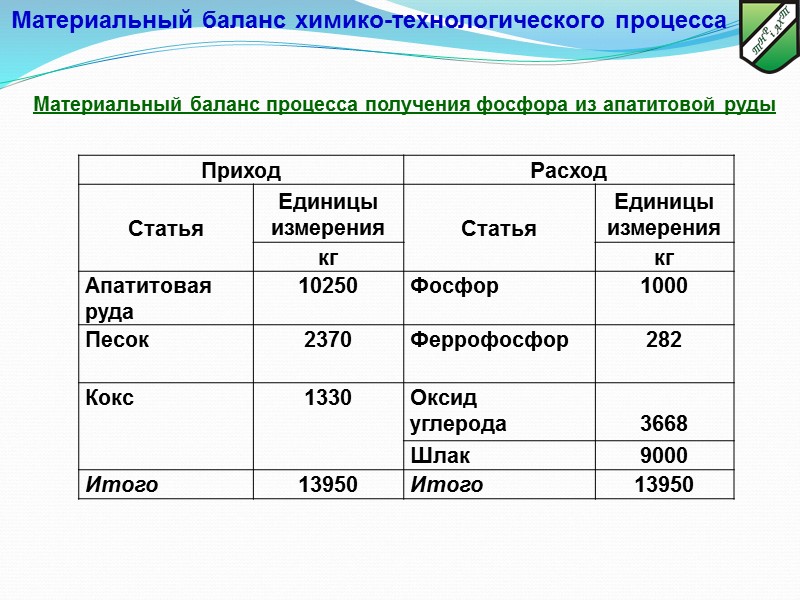
 Материальный баланс процесса получения фосфора из апатитовой руды Материальный баланс химико-технологического процесса
Материальный баланс процесса получения фосфора из апатитовой руды Материальный баланс химико-технологического процесса
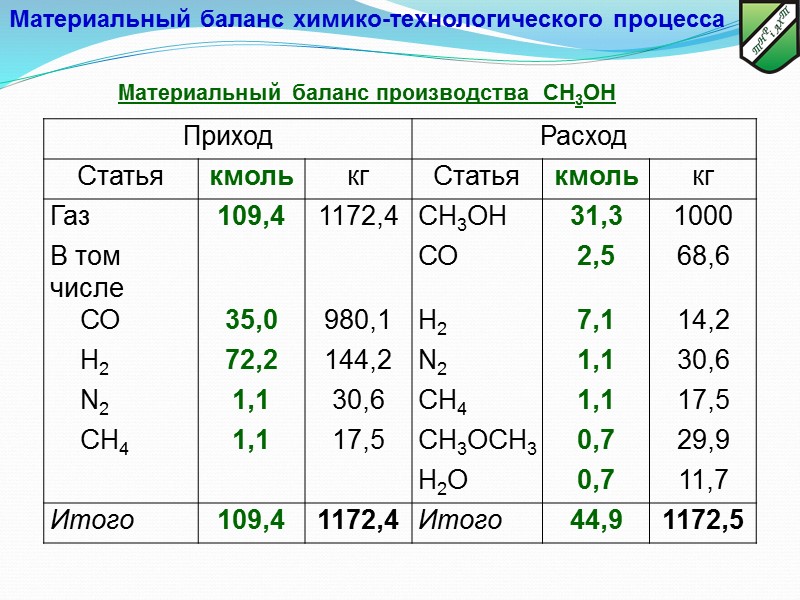
 Материальный баланс производства СН3ОН Материальный баланс химико-технологического процесса
Материальный баланс производства СН3ОН Материальный баланс химико-технологического процесса
 Энергетический баланс основан на законе превращения и сохранения энергии, в соответствии с которым сумма всех энергий в замкнутой системе постоянна. В химической промышленности часто пользуются названием тепловой баланс. Этот термин не эквивалентен энергетическому балансу, т.к. тепловой энергией не учитывается работа, что учитывает энергетический баланс. Энергетический баланс химико-технологического процесса Многообразие форм существования и передачи характерно для энергии. Энергия делится на три вида: внутренняя энергия, работа, внешняя энергия. С учетом этого выразим закон сохранения и превращения энергии: Где U – внутренняя энергия, А – работа, Е – внешний поток энергии
Энергетический баланс основан на законе превращения и сохранения энергии, в соответствии с которым сумма всех энергий в замкнутой системе постоянна. В химической промышленности часто пользуются названием тепловой баланс. Этот термин не эквивалентен энергетическому балансу, т.к. тепловой энергией не учитывается работа, что учитывает энергетический баланс. Энергетический баланс химико-технологического процесса Многообразие форм существования и передачи характерно для энергии. Энергия делится на три вида: внутренняя энергия, работа, внешняя энергия. С учетом этого выразим закон сохранения и превращения энергии: Где U – внутренняя энергия, А – работа, Е – внешний поток энергии
 Энергетический баланс выражают как тепловой баланс: - химическое тепло экзотермических процессов - химическое тепло эндотермического процесса - физическое вещественное тепло, входных потоков (знак -) или выходных потоков (знак +), Q3 – внешнее тепло (внешняя энергия – подведенная (знак -) или отведена (знак +), в том числе потери тепла. y – мольный пробег реакции Энергетический баланс химико-технологического процесса
Энергетический баланс выражают как тепловой баланс: - химическое тепло экзотермических процессов - химическое тепло эндотермического процесса - физическое вещественное тепло, входных потоков (знак -) или выходных потоков (знак +), Q3 – внешнее тепло (внешняя энергия – подведенная (знак -) или отведена (знак +), в том числе потери тепла. y – мольный пробег реакции Энергетический баланс химико-технологического процесса
 Количество теплоты, которое выделяется или поглощается в результате реакции, вычисляется из термохимического уравнения аА + bB + … = rR + sS + … + Q(Н), где Q – тепловой эффект реакции; Н энтальпия реакции. Тепловой эффект Q и энтальпия Н реакции противоположны по знаку (Q = Н) Энергетический баланс химико-технологического процесса
Количество теплоты, которое выделяется или поглощается в результате реакции, вычисляется из термохимического уравнения аА + bB + … = rR + sS + … + Q(Н), где Q – тепловой эффект реакции; Н энтальпия реакции. Тепловой эффект Q и энтальпия Н реакции противоположны по знаку (Q = Н) Энергетический баланс химико-технологического процесса
 Количество выделившейся (или поглощенной) теплоты при протекании химической реакции зависит от степени превращения исходного реагента (хА) и значения теплового эффекта (изменения энтальпии): Qх. р = Q хАnА, где nА – химическое количество исходного реагента, моль (кмоль); Q – тепловой эффект реакции. Следовательно, уравнение теплового баланса будет иметь следующие составляющие: Qисх = nА Ср(м) А(ТА – Т0), Qх. р = QТ xАnА Qпрод = nRСр(м)R(ТR – Т0), где nА, nR – химическое количество входящих реагентов и выходящих продуктов, моль или кмоль; ТА, ТR – температуры реагентов и продуктов соответственно, К; Т0 – температура начала отcчета энтальпии, 298 К; Q , QТ – тепловой эффект реакции при стандартной температуре и температуре в зоне реакции соответственно, кДж. Энергетический баланс химико-технологического процесса
Количество выделившейся (или поглощенной) теплоты при протекании химической реакции зависит от степени превращения исходного реагента (хА) и значения теплового эффекта (изменения энтальпии): Qх. р = Q хАnА, где nА – химическое количество исходного реагента, моль (кмоль); Q – тепловой эффект реакции. Следовательно, уравнение теплового баланса будет иметь следующие составляющие: Qисх = nА Ср(м) А(ТА – Т0), Qх. р = QТ xАnА Qпрод = nRСр(м)R(ТR – Т0), где nА, nR – химическое количество входящих реагентов и выходящих продуктов, моль или кмоль; ТА, ТR – температуры реагентов и продуктов соответственно, К; Т0 – температура начала отcчета энтальпии, 298 К; Q , QТ – тепловой эффект реакции при стандартной температуре и температуре в зоне реакции соответственно, кДж. Энергетический баланс химико-технологического процесса
 Уравнение теплового баланса в упрощенном виде: Энергетический баланс химико-технологического процесса mисх Ср исхТ1 + Qх. р = mпрод Ср продТ2
Уравнение теплового баланса в упрощенном виде: Энергетический баланс химико-технологического процесса mисх Ср исхТ1 + Qх. р = mпрод Ср продТ2


