Охорона навколишнього середовища від забруднення викидами сульфуровмісних речовин.
































virobnictvo_sulyfatnoї_kisloti.ppt
- Размер: 943.0 Кб
- Автор:
- Количество слайдов: 36
Описание презентации Охорона навколишнього середовища від забруднення викидами сульфуровмісних речовин. по слайдам
 Охорона навколишнього середовища від забруднення викидами сульфуровмісних речовин. Сульфатна кислота і сульфати. Найважливіші природні сульфати, якісна реакція на сульфат-іон. Застосування сульфатної кислоти і сульфатів
Охорона навколишнього середовища від забруднення викидами сульфуровмісних речовин. Сульфатна кислота і сульфати. Найважливіші природні сульфати, якісна реакція на сульфат-іон. Застосування сульфатної кислоти і сульфатів
 Мета: Відновити знання про склад, фізичні властивості і відношення до води сульфатної кислоти. Ознайомити з сульфатами та їхніми властивостями, практичним застосуванням. Розкрити значення для хімічної промисловості і народного господарства. Розвинути вміння встановлювати причинно-наслідковий зв’язок між властивостями сульфатної кислоти та її застосуванням. Загострити увагу на правилах (Т/Б) при роботі з сульфатною кислотою та приготуванні її водних розчинів. Пояснити окиснювальну здатність концентрованої сульфатної кислоти. Удосконалити вміння складати рівняння реакцій з металами, оксидами, основами і солями в молекулярній, повній і скороченій йонних формах. Дати поняття про якісну реакцію на сульфат-іон. Ознайомити із сировиною та хімічними реакціями, що покладені в основу виробництва сульфатної кислоти, з умовами їх здійснення. Розкрити значення цих знань для управління процесом виробництва. Формувати вміння складати рівняння реакцій, що лежать в основі виробництва сульфатної кислоти (випалювання піриту та сульфідів, окиснення сульфур( IV ) оксиду, гідратація сульфур( VI ) оксиду). Розвивати поняття про каталіз, формувати поняття “вихід продукту реакцій”. Висвітлити проблему охорони праці і довкілля від забруднення.
Мета: Відновити знання про склад, фізичні властивості і відношення до води сульфатної кислоти. Ознайомити з сульфатами та їхніми властивостями, практичним застосуванням. Розкрити значення для хімічної промисловості і народного господарства. Розвинути вміння встановлювати причинно-наслідковий зв’язок між властивостями сульфатної кислоти та її застосуванням. Загострити увагу на правилах (Т/Б) при роботі з сульфатною кислотою та приготуванні її водних розчинів. Пояснити окиснювальну здатність концентрованої сульфатної кислоти. Удосконалити вміння складати рівняння реакцій з металами, оксидами, основами і солями в молекулярній, повній і скороченій йонних формах. Дати поняття про якісну реакцію на сульфат-іон. Ознайомити із сировиною та хімічними реакціями, що покладені в основу виробництва сульфатної кислоти, з умовами їх здійснення. Розкрити значення цих знань для управління процесом виробництва. Формувати вміння складати рівняння реакцій, що лежать в основі виробництва сульфатної кислоти (випалювання піриту та сульфідів, окиснення сульфур( IV ) оксиду, гідратація сульфур( VI ) оксиду). Розвивати поняття про каталіз, формувати поняття “вихід продукту реакцій”. Висвітлити проблему охорони праці і довкілля від забруднення.
 Демонстрації: 5. Спалювання сірки і доведення кислотного характеру утвореного оксиду. 6. Виділення теплоти під час розчинення у воді концентрованої сульфатної кислоти. 7. Водовідбірні властивості концентрованої сульфатної кислоти (дія на цукор і папір). 8. Якісна реакція на сульфат-іон. Лабораторні досліди: 4. Ознайомлення зі зразками природних сполук Сульфуру. 5. Виявлення сульфат-іонів у розчині.
Демонстрації: 5. Спалювання сірки і доведення кислотного характеру утвореного оксиду. 6. Виділення теплоти під час розчинення у воді концентрованої сульфатної кислоти. 7. Водовідбірні властивості концентрованої сульфатної кислоти (дія на цукор і папір). 8. Якісна реакція на сульфат-іон. Лабораторні досліди: 4. Ознайомлення зі зразками природних сполук Сульфуру. 5. Виявлення сульфат-іонів у розчині.
 Сульфатна кислота. Сульфатна, або сірчана, кислота їїформула — H 2 SO 4. Будова молекули. Графічна формула молекули: Сульфатна кислота, як і всі інші кислоти, — молекулярна сполука Кулестержневамодель молекули сульфатної кислоти
Сульфатна кислота. Сульфатна, або сірчана, кислота їїформула — H 2 SO 4. Будова молекули. Графічна формула молекули: Сульфатна кислота, як і всі інші кислоти, — молекулярна сполука Кулестержневамодель молекули сульфатної кислоти
 Укажіть значення валентності та ступеня окиснення Сульфуру в сульфатній кислоті.
Укажіть значення валентності та ступеня окиснення Сульфуру в сульфатній кислоті.
 Фізичні властивості. За звичайних умов чиста сульфатна кислота — безбарвна оліїста рідина без запаху, майже удвічі важча за воду (ρ = 1, 83 г/см 3). Температура плавлення споолуки становить +10, 3 °С, а кипіння +280 °С. Під час кипіння кислота починає розкладатиися на сульфур(VI) оксид і воду.
Фізичні властивості. За звичайних умов чиста сульфатна кислота — безбарвна оліїста рідина без запаху, майже удвічі важча за воду (ρ = 1, 83 г/см 3). Температура плавлення споолуки становить +10, 3 °С, а кипіння +280 °С. Під час кипіння кислота починає розкладатиися на сульфур(VI) оксид і воду.
 Переконатися в тому, що розчинення сульфатної кислоти — процес екзотермічний, допоможе такий демонстраційний дослід. Зберемо прилад помістимо в стакан закріплену в лапці штатива пробірку, у яку налито легкокиплячу (t кип. 40 °С)органічну речовину — діетиловий етер. У хімічний стакан наллємо 50 мл води кімнатної температури. Після цього повільно, по скляній паличці, час від часу помішуючи, увіллємо в стакан 50 мл концентрованої сульфатної кислоти. Спостерігатимемо, як рідина в пробірці закипає і випаровується. Причина цього явища —підвищення температури розчину. Якщо відкрити пробку й піднести до отвору пробірки запалену скіпку, пари етеру спалахнуть
Переконатися в тому, що розчинення сульфатної кислоти — процес екзотермічний, допоможе такий демонстраційний дослід. Зберемо прилад помістимо в стакан закріплену в лапці штатива пробірку, у яку налито легкокиплячу (t кип. 40 °С)органічну речовину — діетиловий етер. У хімічний стакан наллємо 50 мл води кімнатної температури. Після цього повільно, по скляній паличці, час від часу помішуючи, увіллємо в стакан 50 мл концентрованої сульфатної кислоти. Спостерігатимемо, як рідина в пробірці закипає і випаровується. Причина цього явища —підвищення температури розчину. Якщо відкрити пробку й піднести до отвору пробірки запалену скіпку, пари етеру спалахнуть
 Потр і бно знати Розчинення кислоти у воді супроводжується виділенням великої кількості теплоти. Для того щоб із концентрованої сульфатної кислоти виготовити її розбавлений розчин, кислоту доливають у воду, а не навпаки. Тоді температура рідини зростає повільніше, і вдається запобігти її закипанню й розбризкуванню.
Потр і бно знати Розчинення кислоти у воді супроводжується виділенням великої кількості теплоти. Для того щоб із концентрованої сульфатної кислоти виготовити її розбавлений розчин, кислоту доливають у воду, а не навпаки. Тоді температура рідини зростає повільніше, і вдається запобігти її закипанню й розбризкуванню.
 Вона взаємодіє з: 1)металами, розміщеними в ряді активності до водню; 2) основними й амфотерними оксидами; 3) основами; 4) амфотерними гідроксидами; 5) солями
Вона взаємодіє з: 1)металами, розміщеними в ряді активності до водню; 2) основними й амфотерними оксидами; 3) основами; 4) амфотерними гідроксидами; 5) солями
 Хімічні властивості. Сульфатна кислота завдяки наявності в молекулі двох ковалентт них полярних зв’язків О–Н є двохосновною. Її дисоціація за першою стадією в розбавленому розчині відбувається майже повністю (це сильна кислота), а за другою — частково: H 2 SO 4 →H + HSO 4 ; HSO 4 →H + SO 4 ²ˉ. Проте у йонноомолекулярних рівняннях сульфатну кислоту записують такою сукупністю йонів: 2 H+ SO 4 ²ˉ.
Хімічні властивості. Сульфатна кислота завдяки наявності в молекулі двох ковалентт них полярних зв’язків О–Н є двохосновною. Її дисоціація за першою стадією в розбавленому розчині відбувається майже повністю (це сильна кислота), а за другою — частково: H 2 SO 4 →H + HSO 4 ; HSO 4 →H + SO 4 ²ˉ. Проте у йонноомолекулярних рівняннях сульфатну кислоту записують такою сукупністю йонів: 2 H+ SO 4 ²ˉ.
 Реакції з металами. взаємодіє майже з усіма металами. Можливість цих реакцій, а також склад їх продуктів залежать від концентрації кислоти і хімічної активності металу. Метал завжди є відновником. Тому сульфатна кислота, реагуючи з ним, буде окисником і відновлюватиметься. +1 +6 – 2 У молекулі H 2 SO 4 можуть відновлюватися (зменшувати ступінь окиснення) два елементи — Гідроген і Сульфур. Якщо з металом взаємодіє розбавлена сульфатна кислота, то відновлюється Гідроген. Продукти реакції — сульфат металічного елемента і водень: 2 Al + 3 H 2 SO 4 (розб. ) = Al 2 (SO 4 ) 3 + 3 H 2 ↑.
Реакції з металами. взаємодіє майже з усіма металами. Можливість цих реакцій, а також склад їх продуктів залежать від концентрації кислоти і хімічної активності металу. Метал завжди є відновником. Тому сульфатна кислота, реагуючи з ним, буде окисником і відновлюватиметься. +1 +6 – 2 У молекулі H 2 SO 4 можуть відновлюватися (зменшувати ступінь окиснення) два елементи — Гідроген і Сульфур. Якщо з металом взаємодіє розбавлена сульфатна кислота, то відновлюється Гідроген. Продукти реакції — сульфат металічного елемента і водень: 2 Al + 3 H 2 SO 4 (розб. ) = Al 2 (SO 4 ) 3 + 3 H 2 ↑.
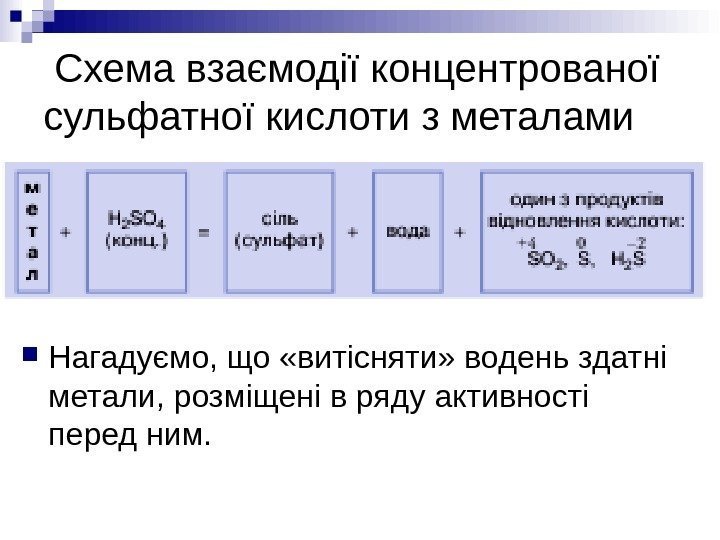
 Схема взаємодії концентрованої сульфатної кислоти з металами Нагадуємо, що «витісняти» водень здатні метали, розміщені в ряду активності перед ним.
Схема взаємодії концентрованої сульфатної кислоти з металами Нагадуємо, що «витісняти» водень здатні метали, розміщені в ряду активності перед ним.
 Із розбавленою сульфатною кислотою не реагують мідь а), ртуть, золото, платина, інші хімічно пасивні метали. Якщо реагентом є концентрована сульфатна кислота, то відновлюється Сульфур. Із концентрованою кислотою реагують також метали, розміщені в ряду активності після водню (крім золота, платини).
Із розбавленою сульфатною кислотою не реагують мідь а), ртуть, золото, платина, інші хімічно пасивні метали. Якщо реагентом є концентрована сульфатна кислота, то відновлюється Сульфур. Із концентрованою кислотою реагують також метали, розміщені в ряду активності після водню (крім золота, платини).
 Малоактивні метали відновлюють +4 – 2 кислоту до SO 2 , а дуже активні —до H 2 S: Cu + H 2 SO 4 (конц. ) →Cu. SO 4+ SO 2↑+ H 2 O; Mg + H 2 SO 4 (конц. ) →Mg. SO 4+ H 2 S↑+ H 2 O. Складіть схеми окиснення, відновлення й доберіть коефіцієнти методом електронного балансу.
Малоактивні метали відновлюють +4 – 2 кислоту до SO 2 , а дуже активні —до H 2 S: Cu + H 2 SO 4 (конц. ) →Cu. SO 4+ SO 2↑+ H 2 O; Mg + H 2 SO 4 (конц. ) →Mg. SO 4+ H 2 S↑+ H 2 O. Складіть схеми окиснення, відновлення й доберіть коефіцієнти методом електронного балансу.
 Якщо в холодну концентровану сульфатну кислоту занурити кусочок заліза, то ми не помітимо взаємодії речовин. Насправді кислота починає реагувати з металом: 2 Fe + 3 H 2 SO 4 (конц. ) = Fe 2 O 3+ 3 SO 2↑+ 3 H 2 O. Однак реакція відразу припиняється, бо на поверхні металу утворюється тонка плівка ферум(ІІІ) оксиду, інертна щодо кислоти (оксид реагує з кислотою тільки при нагріванні). Таке явище називають пасивацією. Аналогічно поводиться щодо цієї кислоти алюміній.
Якщо в холодну концентровану сульфатну кислоту занурити кусочок заліза, то ми не помітимо взаємодії речовин. Насправді кислота починає реагувати з металом: 2 Fe + 3 H 2 SO 4 (конц. ) = Fe 2 O 3+ 3 SO 2↑+ 3 H 2 O. Однак реакція відразу припиняється, бо на поверхні металу утворюється тонка плівка ферум(ІІІ) оксиду, інертна щодо кислоти (оксид реагує з кислотою тільки при нагріванні). Таке явище називають пасивацією. Аналогічно поводиться щодо цієї кислоти алюміній.
 Реакції зі складними речовинами. Сульфатна кислота взаємодіє з основними оксидами амфотерними оксидами, основами, амфотерними гідроксидами з утворенням у кожному випадку солі (сульфату) і води. • H 2 SO 4 + Ві(OH) 3 → • H 2 SO 4 + Mn. O →
Реакції зі складними речовинами. Сульфатна кислота взаємодіє з основними оксидами амфотерними оксидами, основами, амфотерними гідроксидами з утворенням у кожному випадку солі (сульфату) і води. • H 2 SO 4 + Ві(OH) 3 → • H 2 SO 4 + Mn. O →
 Будучи нелеткою і сильною кислотою, вона вступає в реакції обміну з більшістю солей. Напишіть рівняння реакцій сульфатної кислоти зі сполуками, що мають такі формули: Li 2 O, Fe(OH) 3 , Na 3 PO 4. H 2 SO 4 + Pb(NO 3 ) 2 → H 2 SO 4 + Na. F →
Будучи нелеткою і сильною кислотою, вона вступає в реакції обміну з більшістю солей. Напишіть рівняння реакцій сульфатної кислоти зі сполуками, що мають такі формули: Li 2 O, Fe(OH) 3 , Na 3 PO 4. H 2 SO 4 + Pb(NO 3 ) 2 → H 2 SO 4 + Na. F →
 Розклад цукру і целюлози під дією сульфатної кислоти
Розклад цукру і целюлози під дією сульфатної кислоти

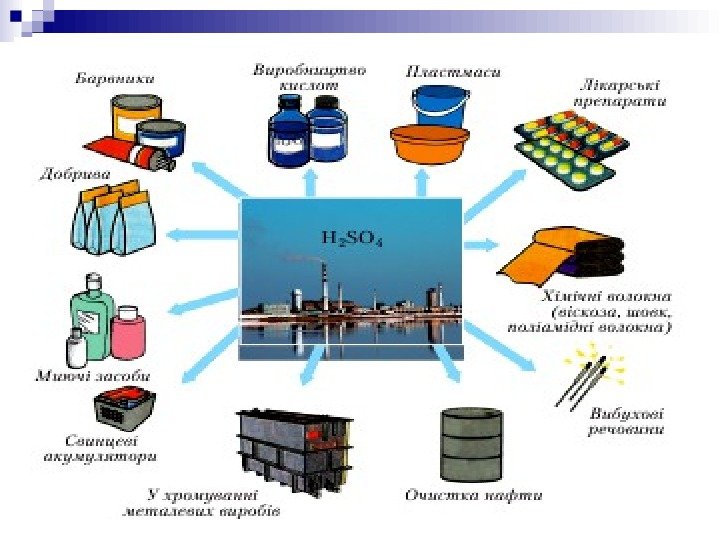
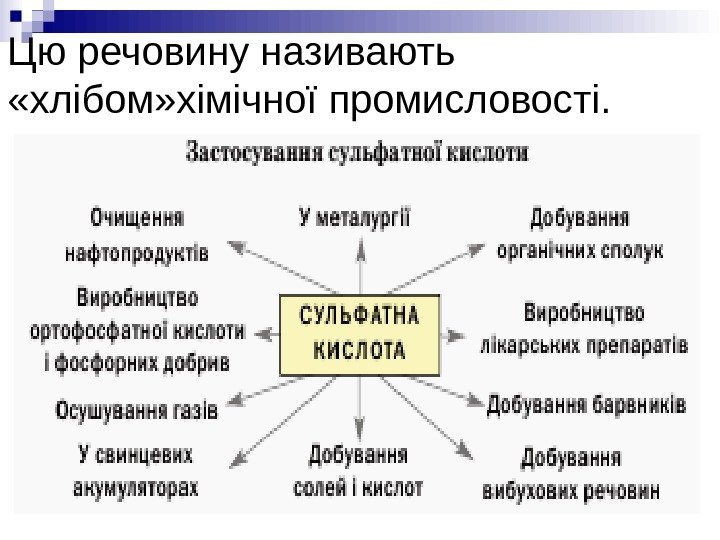
 Цю речовину називають «хлібом» хімічної промисловості.
Цю речовину називають «хлібом» хімічної промисловості.
 Сульфати. Сульфатна кислота утворює солі, загальна назва яких — сульфати Більшість сульфатів розчиняється у воді. При випарюванні їх розчинів часто виділяються кристалогідрати, наприклад Cu. SO 4 • 5 H 2 O, Fe. SO 4 • 7 H 2 O, Al 2(SO 4)3 • 18 H 2 O. Малорозчинними є солі Ca. SO 4 і Ag 2 SO 4, а практично нерозчинними — Ba. SO 4 і Pb. SO 4.
Сульфати. Сульфатна кислота утворює солі, загальна назва яких — сульфати Більшість сульфатів розчиняється у воді. При випарюванні їх розчинів часто виділяються кристалогідрати, наприклад Cu. SO 4 • 5 H 2 O, Fe. SO 4 • 7 H 2 O, Al 2(SO 4)3 • 18 H 2 O. Малорозчинними є солі Ca. SO 4 і Ag 2 SO 4, а практично нерозчинними — Ba. SO 4 і Pb. SO 4.

 Найважливіші природні сульфати гіпс. Са. SO 4· 2 Н 2 О; глауберова сіль. Na 2 SO 4· 10 H 2 О; гірка сіль. Mg. SO 4· 7 H 2 О. Із наведених формул стає зрозуміло, що це кристалогідрати, тобто вони містять кристалізаційну воду, яка при нагріванні випаровується. На цій властивості кристалогідратів ґрунтується виробництво алебастру 2 Са. SO 4·Н 2 О з природного гіпсу, який нагрівають до 120– 190 °С, у наслідок чого він втрачає частину води. При змочуванні водою кімнатної температури алебастр легко приєднує воду й знову перетворюється на гіпс. Це відбувається щоразу при накладанні гіпсових пов’язок на травмовані частини тіла, під час виготовлення гіпсових виробів художнього та будівельного призначення.
Найважливіші природні сульфати гіпс. Са. SO 4· 2 Н 2 О; глауберова сіль. Na 2 SO 4· 10 H 2 О; гірка сіль. Mg. SO 4· 7 H 2 О. Із наведених формул стає зрозуміло, що це кристалогідрати, тобто вони містять кристалізаційну воду, яка при нагріванні випаровується. На цій властивості кристалогідратів ґрунтується виробництво алебастру 2 Са. SO 4·Н 2 О з природного гіпсу, який нагрівають до 120– 190 °С, у наслідок чого він втрачає частину води. При змочуванні водою кімнатної температури алебастр легко приєднує воду й знову перетворюється на гіпс. Це відбувається щоразу при накладанні гіпсових пов’язок на травмовані частини тіла, під час виготовлення гіпсових виробів художнього та будівельного призначення.

 Глауберову сіль Na 2 SO 4· 10 H 2 О застосовують у виробництві скла, соди, фарб, у медицині. Гірку сіль Mg. SO 4· 7 H 2 О використовують в обробці тканин, дубінні шкіри, виготовленні медичних препаратів. Купрум(ІІ) сульфат, пентагідрат, або мідний купорос Cu. SO 4 • 5 H 2 O, застосовують у сільському господарстві як засіб проти хвороб і шкідників рослин.
Глауберову сіль Na 2 SO 4· 10 H 2 О застосовують у виробництві скла, соди, фарб, у медицині. Гірку сіль Mg. SO 4· 7 H 2 О використовують в обробці тканин, дубінні шкіри, виготовленні медичних препаратів. Купрум(ІІ) сульфат, пентагідрат, або мідний купорос Cu. SO 4 • 5 H 2 O, застосовують у сільському господарстві як засіб проти хвороб і шкідників рослин.


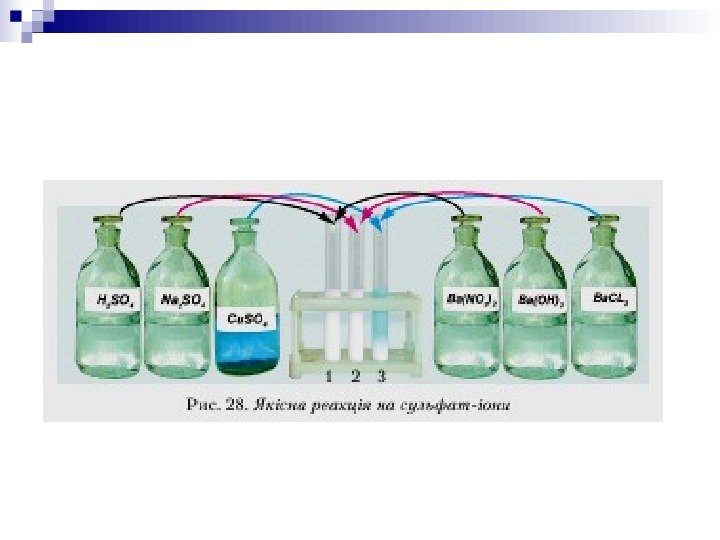
 Якісною реакцією на сульфат аніони є взаємодія їх з катіонами Барію (розчинними у воді сполуками Барію), у результаті чого утворюється нерозчинний у воді і кислотах білий дрібнокристалічний осад барій сульфату. Скорочене йонне рівняння якісної реакції таке: Ba ² + SO 4 = Ba. SO 4 ²ˉ↓
Якісною реакцією на сульфат аніони є взаємодія їх з катіонами Барію (розчинними у воді сполуками Барію), у результаті чого утворюється нерозчинний у воді і кислотах білий дрібнокристалічний осад барій сульфату. Скорочене йонне рівняння якісної реакції таке: Ba ² + SO 4 = Ba. SO 4 ²ˉ↓
 Охорона навколишнього середовища від забруднення викидами сульфуровмісних речовин. Серед сульфуровмісних забрудників навколишнього середовища найбільш шкідливими є сульфур(ІV) оксид і гідроген сульфід, або сірководень. Щодо гідроген сульфіду, то потрібно наголосити на високій токсичності цієї газуватої речовини з неприємним запахом тухлих яєць (утворюється при гнитті білка курячого яйця й спричинює його неприємний запах).
Охорона навколишнього середовища від забруднення викидами сульфуровмісних речовин. Серед сульфуровмісних забрудників навколишнього середовища найбільш шкідливими є сульфур(ІV) оксид і гідроген сульфід, або сірководень. Щодо гідроген сульфіду, то потрібно наголосити на високій токсичності цієї газуватої речовини з неприємним запахом тухлих яєць (утворюється при гнитті білка курячого яйця й спричинює його неприємний запах).

 Поняття про кислотні дощі та причини їх виникнення. Чи доводилося вам спостерігати, як після довгоочікуваного літнього дощу рослини замість того, щоб рости й давати врожай, жовкнуть, в’януть і навіть гинуть (досить часто це трапляється з огірками)? З великою ймовірністю можна стверджувати, що дощ був не звичайний, а кислотний, і завдав шкоди рослинам. Кислотні дощі пошкоджують листки, руйнують їх захисні воскові покриви, через що ті стають легкопроникними для комах, шкідливих грибів і мікроорганізмів. Окрім рослин, кислотні дощі завдають шкоди тваринам, водоймам, ґрунтам. Хімічний аналіз кислотних дощів показує наявність у них сульфатної та нітратної кислот. Поява цих речовин — наслідок розглянутих хімічних перетворень оксидів Сульфуру і Нітрогену в атмосфері. Кислотний дощ— це дощ, що містить певну кількість кислот, утворених унаслідок взаємодії з водою наявних у повітрі таких забруднювачів, як оксиди Сульфуру і Нітрогену. Щороку внаслідок спалювання твердого палива, роботи двигунів внутрішнього згорання, промислових викидів заводів по виробництву сульфатної і нітратної кислот концентрація цих оксидів у повітрі збільшується. Тому кислотні дощі створюють реальну загрозу людині, рослинному й тваринному світу.
Поняття про кислотні дощі та причини їх виникнення. Чи доводилося вам спостерігати, як після довгоочікуваного літнього дощу рослини замість того, щоб рости й давати врожай, жовкнуть, в’януть і навіть гинуть (досить часто це трапляється з огірками)? З великою ймовірністю можна стверджувати, що дощ був не звичайний, а кислотний, і завдав шкоди рослинам. Кислотні дощі пошкоджують листки, руйнують їх захисні воскові покриви, через що ті стають легкопроникними для комах, шкідливих грибів і мікроорганізмів. Окрім рослин, кислотні дощі завдають шкоди тваринам, водоймам, ґрунтам. Хімічний аналіз кислотних дощів показує наявність у них сульфатної та нітратної кислот. Поява цих речовин — наслідок розглянутих хімічних перетворень оксидів Сульфуру і Нітрогену в атмосфері. Кислотний дощ— це дощ, що містить певну кількість кислот, утворених унаслідок взаємодії з водою наявних у повітрі таких забруднювачів, як оксиди Сульфуру і Нітрогену. Щороку внаслідок спалювання твердого палива, роботи двигунів внутрішнього згорання, промислових викидів заводів по виробництву сульфатної і нітратної кислот концентрація цих оксидів у повітрі збільшується. Тому кислотні дощі створюють реальну загрозу людині, рослинному й тваринному світу.
 Фізіологічна дія гідроген сульфіду проявляється в тому, що він блокує дихальний центр. Смертельною дозою для людини є вдихання протягом 5– 10 хв повітря з об’ємною часткою гідроген сульфіду 0, 08%. Забруднюють повітря сульфуровмісними речовинами викиди нафтопереробних заводів, теплові електростанції.
Фізіологічна дія гідроген сульфіду проявляється в тому, що він блокує дихальний центр. Смертельною дозою для людини є вдихання протягом 5– 10 хв повітря з об’ємною часткою гідроген сульфіду 0, 08%. Забруднюють повітря сульфуровмісними речовинами викиди нафтопереробних заводів, теплові електростанції.
 Охорона навколишнього середовища полягає насамперед у зменшенні викидів, а отже, у модернізації виробництва, запровадженні технології замкненого циклу, коли гази, що є відходами названих виробництв, використовують як сировину для інших виробництв. Користь від цього подвійна — не забруднюється навколишнє середовище, а вироблена з гідроген сульфідних відходів нафтопереробної промисловості сульфатна кислота має найменшу вартість. Удосконаленням технології виробництва сульфатної кислоти займався український хімік Іван Євграфович Ададуров (1879– 1938).
Охорона навколишнього середовища полягає насамперед у зменшенні викидів, а отже, у модернізації виробництва, запровадженні технології замкненого циклу, коли гази, що є відходами названих виробництв, використовують як сировину для інших виробництв. Користь від цього подвійна — не забруднюється навколишнє середовище, а вироблена з гідроген сульфідних відходів нафтопереробної промисловості сульфатна кислота має найменшу вартість. Удосконаленням технології виробництва сульфатної кислоти займався український хімік Іван Євграфович Ададуров (1879– 1938).
 З якими з перелічених речовин взаємодіє розбавлена сульфатна кислота: залізо, купрум(ІІ) оксид, мідь, натрій гідроксид, нітратна кислота, калій карбонат, нітроген(ІІ) оксид? Напишіть молекулярні рівняння реакцій, зазначте їх типи. Запропонуйте спосіб розпізнавання концентрованої та розбавленої сульфатної кислоти, що перебувають у банках без етикеток. Мотивуйте його. Обчисліть масову частку кристалізаційної води в гіркій солі.
З якими з перелічених речовин взаємодіє розбавлена сульфатна кислота: залізо, купрум(ІІ) оксид, мідь, натрій гідроксид, нітратна кислота, калій карбонат, нітроген(ІІ) оксид? Напишіть молекулярні рівняння реакцій, зазначте їх типи. Запропонуйте спосіб розпізнавання концентрованої та розбавленої сульфатної кислоти, що перебувають у банках без етикеток. Мотивуйте його. Обчисліть масову частку кристалізаційної води в гіркій солі.
 Ознайомтеся з виданими вам зразками сульфатів і сульфідів. Дослідіть агрегатний стан й такі їх фізичні властивості: колір, розчинність у воді. Використовуючи міжпредметні зв’язки з географією, назвіть поклади природних сульфатів і сульфідів в Україні. Одержані результати оформіть у робочому зошиті у вигляді таблиці.
Ознайомтеся з виданими вам зразками сульфатів і сульфідів. Дослідіть агрегатний стан й такі їх фізичні властивості: колір, розчинність у воді. Використовуючи міжпредметні зв’язки з географією, назвіть поклади природних сульфатів і сульфідів в Україні. Одержані результати оформіть у робочому зошиті у вигляді таблиці.
 ВИСНОВКИ Сульфатна кислота H 2 SO 4 — безбарвна оліїста рідина без запаху, яка необмежено розчиняється у воді. Це сильна й нелетка двохосновна кислота. Вона реагує з металами, основними й амфотерними оксидами, основами, амфотерними гідроксидами, а також солями з утворенням сульфатів. Сульфатну кислоту та її солі широко використовують у різних галузях.
ВИСНОВКИ Сульфатна кислота H 2 SO 4 — безбарвна оліїста рідина без запаху, яка необмежено розчиняється у воді. Це сильна й нелетка двохосновна кислота. Вона реагує з металами, основними й амфотерними оксидами, основами, амфотерними гідроксидами, а також солями з утворенням сульфатів. Сульфатну кислоту та її солі широко використовують у різних галузях.

