генетика развития растений 2-1.ppt
- Количество слайдов: 126

ОСОБЕННОСТИ ОРГАНИЗАЦИИ И ЭКСПРЕССИИ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА РАСТЕНИЙ Растения содержат в своих клетках не только характерные для эукариот ядро и митохондрии, но и пластиды — специфичесий тип органелл, непосредственно участвующих в процессе фотосинтеза. В соответствии с этим растительная клетка совмещает в себе три относительно автономные генетические системы (хромосомную, митохондриальную и пластидную ДНК), тесно взаимодействующие друг с другом в контроле обмена веществ. Подобная ситуация отражает симбиотическое происхождение растительных клеток по меньшей мере из трех исходно самостоятельных форм: 1) гипотетического «хозяйского» организма, генетический аппарат которого постепенно преобразовался в ядро; 2) гетеротрофной бактерии (по видимому, родоспириллы), послужившей предшественником митохондрий; 3) цианобактерии, ставшей родоначальником пластид.

ЯДЕРНЫЙ ГЕНЕТИЧЕСКИЙ МАТЕРИАЛ РАСТЕНИЙ

ГЕНОМНЫЕ ПОСЛЕДОВАТЕЛЬНОСТИ, ОБЕСПЕЧИВАЮЩИЕ СТАБИЛЬНОСТЬ ХРОМОСОМНОГО НАБОРА - теломерная ДНК, предотвращающая деградацию и слипание концов хромосом и тем самым обеспечивающая их стабильность; так называемые последовательности ARS (от autonomous replication sequence), служащие точками начала репликации хромосомной ДНК; - центромерная ДНК, обеспечивающая закономерное расхож дение хромосом при делении клетки.

ЯДЕРНЫЕ ГЕНЫ Всю совокупность ядерных генов растений можно подразделить на 4 следующие группы: 1) гены, кодирующие структуру различных белков; 2) гены рибосомных РНК (р. РНК); 3) гены различных транспортных РНК (т. РНК); 4) гены разнообразных малых ядерных РНК (мя. РНК).

Ядерные гены, кодирующие структуру белков. Для подавляющего большинства ядерных генов, кодирующих структуру тех или иных белков, показано типичное для эукариот строение, а именно: • отсутствие оперенной регуляции; • соответствующая структура промоторов; • наличие интронов (до 42 в составе одной из открытых рамок считывания у арабидопсиса); • присутствие сигналов полиаденилирования и. РНК
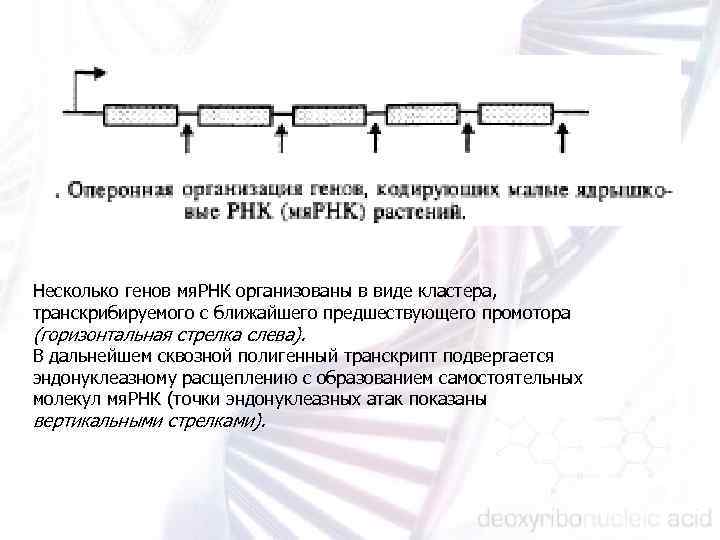
Несколько генов мя. РНК организованы в виде кластера, транскрибируемого с ближайшего предшествующего промотора (горизонтальная стрелка слева). В дальнейшем сквозной полигенный транскрипт подвергается эндонуклеазному расщеплению с образованием самостоятельных молекул мя. РНК (точки эндонуклеазных атак показаны вертикальными стрелками).

У высших растений, как и у прочих эукариотических организмов, транскрипция ядерных генов обслуживается тремя вариантами РНК полимераз, а именно: РНК полимераза I обеспечивает транскрипцию оперонов 18 S— 5. 8 S— 25 S; РНК полимераза II транскрибирует структурные гены белков и некоторых мя. РНК; РНК полимераза III осуществляет транскрипцию генов, продуктами которых являются транспортные, большинство малых ядерных и 55 рибосомная РНК. Каждый из этих ферментов представлен сложным мультисубъ единичным комплексом, включающим в себя около 10 различных белков. Некоторые субъединицы входят в состав всех трех РНК полимераз.



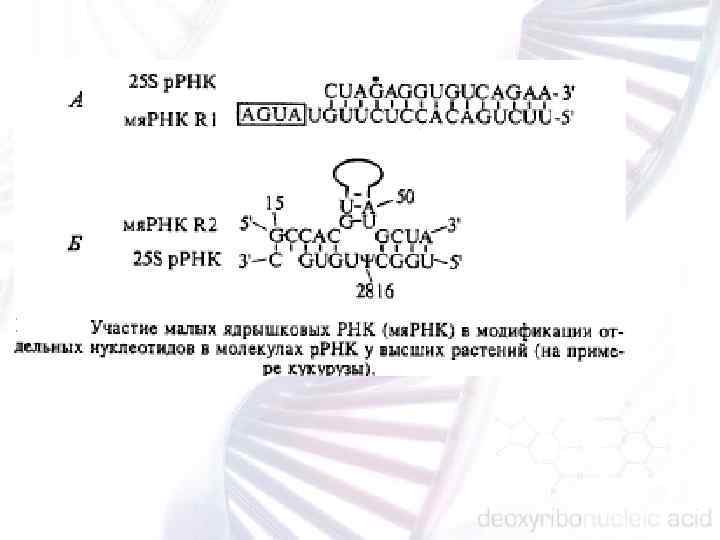
Созревание ядерных РНК. • кэпирование и полиаденилирование подавляющего большинства и. РНК; • сплайсинг транскриптов, обладающих интрон экзонной структурой; • расщепление полигенных транскриптов; • модификация отдельных положений в составе некоторых транскриптов; • наращивание 3' конца у ядерных т. РНК.

МОБИЛЬНЫЕ ГЕНЕТИЧЕСКИЕ ЭЛЕМЕНТЫ РАСТЕНИЙ В соответствии с механизмами этого перемещения мобильные элементы эукариот принято подразделять на две большие группы. 1. Мобильные элементы I класса, миграция которых происходит путем возникновения новых геномных копий при сохранении старой. Подобный процесс, получивший название репликативной транспозиции, осуществляется за счет активности обратной транскриптазы с использованием молекул РНК в качестве матриц. По аналогии с ретровирусами, имеющими сходный механизм воспроизведения, мобильные элементы этого класса обычно называют ретротранспозонами. 2. Мобильные элементы II класса, в основе перемещения которых лежит так называемая нерепликативная транспозиция, состоящая в вырезании и реинтеграции самой исходной копии. Поскольку этот механизм не требует наличия промежуточной РНК матрицы, соответствующие мобильные элементы получили название ДНК- транспозоны.

n. Ретротранспозоны растений n длинные концевые повторы (LTR от long terminal repeats) n LTR-несодержащие ретротранспозоны

LTR coдержащие ретротранспозоны Ген POL кодирует длинную полипептидную молекулу (polyprotein) • ДНК связывающий полипептид, гомологичный Gag белкам дрожжей и дрозофилы; • протеиназа Prot, расщепляющая единый продукт гена POL на самостоятельные функционально активные домены; • эндонуклеаза Endo, способная встраивать в геном новые копии ретротранспозона и в связи с этим обычно называемая интегразой; • высококонсервативный полипептид, совмещающий функции обратной транскриптазы (RT от reverse transcriptase) и РНКазы. Н.

• группа Ty 1/copia подобных элементов (последовательность доменов: Gag—Prot—Endo—RT/RNAse. H). Транспозоны этой группы широко распространены у эукариот и к настоящему времени обнаружены у более чем 100 видов растений, начиная от одноклеточных водорослей и кончая обоими классами цветковых; • группа Ту3/gypsy подобных элементов (последовательность доменов: Gag—Prot—RT/RNAse. H—Endo) исследована у растений в значительно меньшей степени. Отдельные представители этой группы обнаружены у цветковых и голосемен ных.

LTR несодержащие ретротранспозоны или LINE (от long interspersed elements) элементов LINE элементы, скорее всего, представляют собой геномные копии различных и. РНК, считанных с внутренних областей ретротранспозонов. ретрогены или SINE (от short interspersed elements) элементов.

Ретротранспозоны растений представляют собой весьма гетерогенную группу мобильных генетических элементов, общей чертой которых служит репликативный характер транспозиции. Первыми элементами, освоившими такой механизм перемещения, по видимому, являлись интегрированные копии генетического материала ретровирусов, впоследствии давшие начало LTR содержащим ретротранспозонам. Кодируемая ретротранспозонами обрат ная транскриптаза оказалась способной использовать в качестве матриц разнообразные полиаденилированные транскрипты гена POL, что постепенно привело к возникновению широкого спектра LINE элементов. Наконец, аналогичные процессы, по видимому, могли происходить и на других типах транскриптов, в результате чего сформировались относительно короткие SINE элементы. Несмотря на свою, как правило, очень низкую степень мобильности, ретротранспозоны растений могут составлять весьма существенную часть генома.
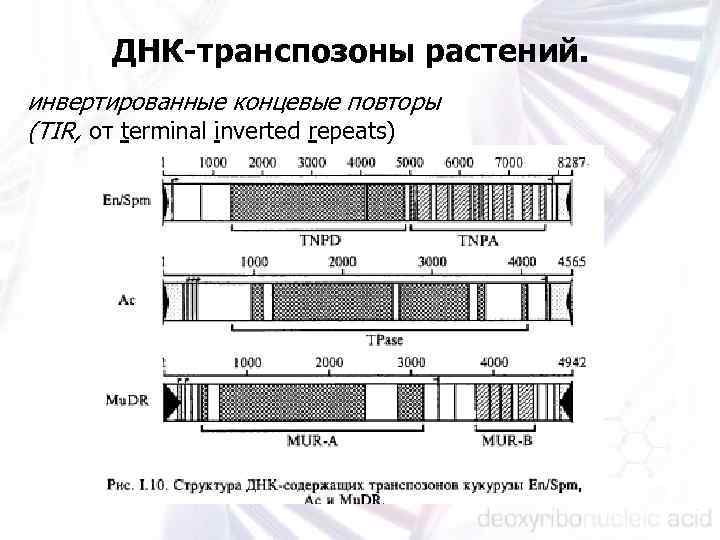
ДНК-транспозоны растений. инвертированные концевые повторы (TIR, от terminal inverted repeats)

Генетические последствия транспозиции состоят не только в физическом перемещении мобильного элемента, но и в изменении экспрессии генов, локализованных в области старого и нового сайтов мишени. Так, встраивание ДНК транспозона в промоторную или кодирующую область функционально активного гена обычно приводит к образо ванию дефектной (мутантной) аллели, характеризующейся типичным рецессивным проявлением. В свою очередь интегрированная копия мобильного элемента способна к последующей эксцизии, что обеспечивает высокую нестабиль ность такой мутантной аллели. Учитывая тот факт, что оставляемые ДНК транспозонами «следы» имеют весьма небольшие размеры и в некоторых случаях даже не нарушают открытую рамку считывания, эксцизия мобильного элемента может проявляться как реверсия мутантной аллели к псевдо нормальному состоянию. Именно высокая нестабильность определенных мутантных аллелей обычно служит формаль ной генетической основой для выявления мобильных

группа Ac подобных элементов, для которых характерны ко роткие инвертированные концевые повторы (5— 15 п. н. ), содержащие консервативный мотив 5' CAGGGATGAAA 3'; n группа En/Spm подобных элементов, концевые области ко торых представлены короткими (преимущественно 13 п. н. ) инвертированными повторами, начинающимися с мотива 5' САСТА 3'. По этой причине En/Spm подобные транспозоны часто называют САСТА элементами; n Mu подобные элементы, резко выделяющиеся среди всех ДНК транспозонов своими длинными концевыми повторами (около 220 п. н. ). n

каждый тип ДНК транспозонов может быть представлен в геноме по меньшей мере тремя вариантами: n полноценные мобильные элементы, способные к автономно му перемещению даже вгетерологичной системе; n неавтономные элементы, мобильность которых может быть обеспечена только за счет функционально активной транспозазы, кодируемой другими копиями данного транспозона; n полностью неподвижные элементы, способные тем не менее активировать транспозицию родственных неавтономных копий.

Ac элемент кукурузы. Концевые области Ac элемента представлены 11 нуклеотидными инвертированными повторами, неидентичными по своему первому положению (5' CAGGGATGAAA 3' — 3' AAAGTAGGGAT 5'). Большую роль в обеспечении мобильности Ac элемента играют и его субтерминальные области. Каждая из них имеет в длину приблизительно 240 п. н. и содержит многократно повторенные мотивы AAACGG, организованные в небольшие кластеры. Искусственное укорочение этих областей приводит к пропорциональному ослаблению мобильности элемента вплоть до ее полной утраты. Минимальный размер каждой из этих областей, необходимый для обеспечения транспозиции, составляет около 100 п. н.

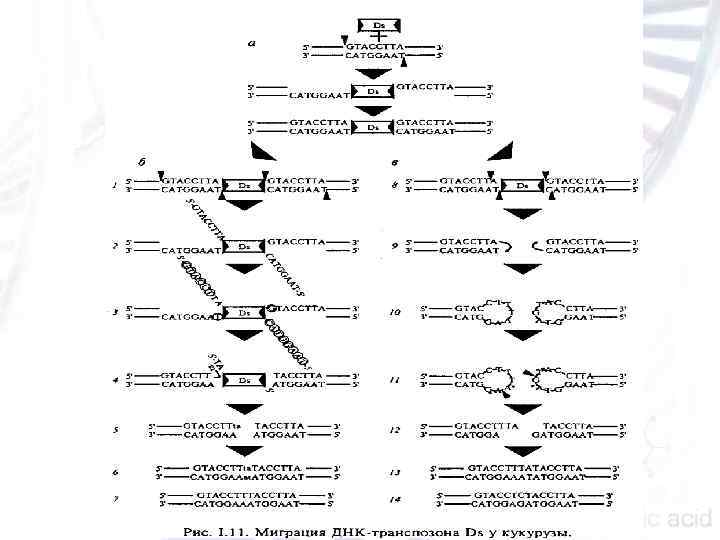
n. Ds элементы (от dissociation) I типа, часто вызывающие разрывы хромосом, но проявляющие низкую мобильность; n. Ds элементы II типа, редко вызывающие хромосомные разрывы, но зато способные к эффективной транспозиции.
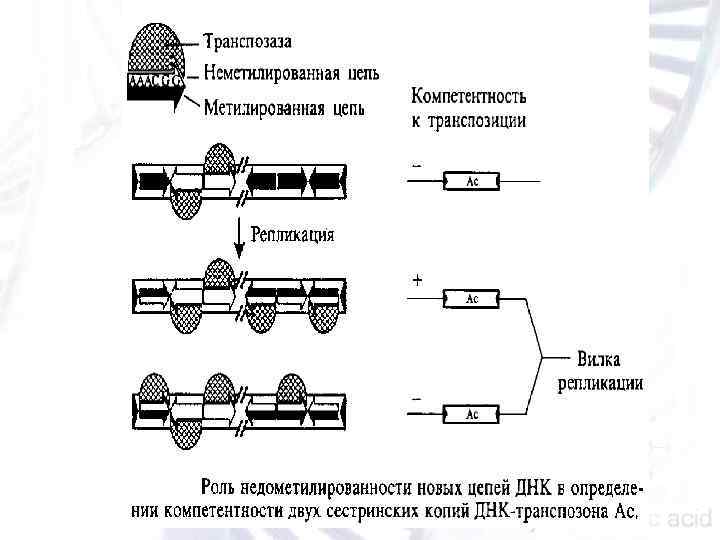

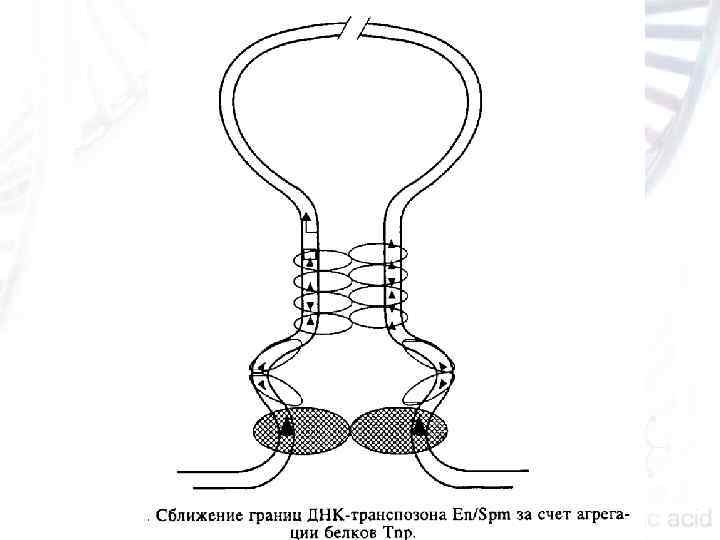
En/Spm элемент кукурузы. Инвертированные концевые повторы данного элемента образованы идентичными 13 нуклеотидными последовательностями 5' САС TACAAGAAAA 3', абсолютно необходимыми для обеспечения его мобильности. Отсутствие в этой последовательности всего лишь двух первых нуклеотидов резко снижает частоту транспозиции. 5' и 3' субтерминальные области En/Spm элемента имеют различную длину (приблизительно 180 и 300 п. н. соответственно) и в сумме содержат 24 копии слабо гетерогенного 12 нуклеотидного мотива 5' TAAGAGTGTCGG 3'. С внутренней области полноценного En/Spm элемента считывается один крупный транскрипт, преобразующийся в результате альтернативного сплайсинга в две матричные РНК размером 2. 4 и 6 т. п. н. Продуктами этих м. РНК являются белки Т nр. А и Tnp. D соответственно. Молекулы белка Тnр. А эффективно связываются с неметилированными копиями субтерминального мотива, а также содержат в своем С концевом домене типичные сигналы, отвечающие за образование агрегатов. Функционально активной транспозазой в случае En/Spm элемента, скорее всего, является белок Tnp. D

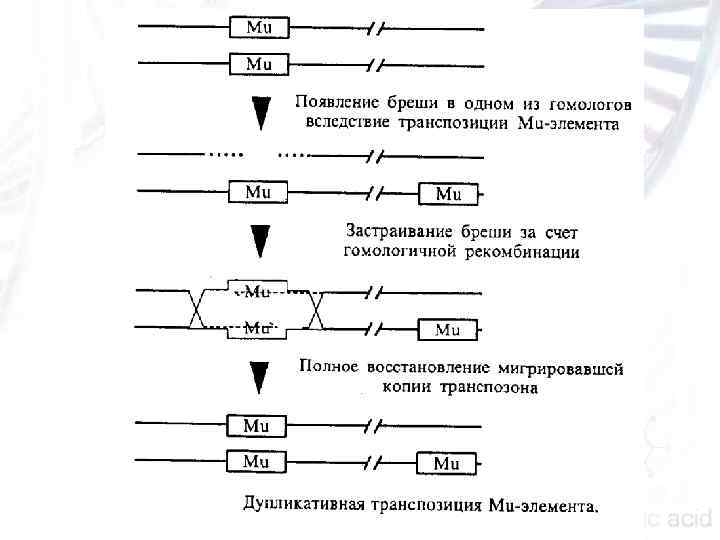
Mu элементы кукурузы n n n Дупликативная транспозиция стандартная нерепликативная транспозиция Ми элемента, приводящая к возникновению двунитевой бреши в месте его исходной локализации; репарация возникшей двунитевой бреши за счет однонитево го участка ДНК из состава сестринской хроматиды (или го мологичной хромосомы, если она также несет Mu элемент в соответствующем положении).

основными отличительными чертами ДНК транспозонов растений являются: n наличие, как правило, коротких инвертированных повторов, фланкирующих мобильный элемент; n способность к нерепликативной транспозиции путем вырезания исходной копии элемента с последующей реинтеграцией в геном. Все основные этапы этого процесса, по видимому, осуществляются высоко специфичной транспозазой, кодируемой внутренней областью самого мобильного элемента. В некоторых случаях мобильный элемент несет информацию не только о самой транспозазе, но и о неких вспомогательных белках; n наличие неавтономных ДНК транспозонов, представляющих собой разнообразные делеционные варианты полноценных копий.

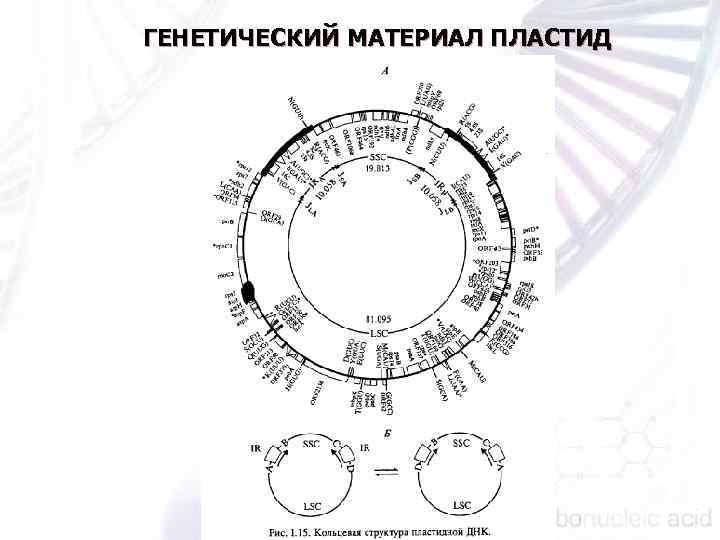
ГЕНЕТИЧЕСКИЙ МАТЕРИАЛ ПЛАСТИД

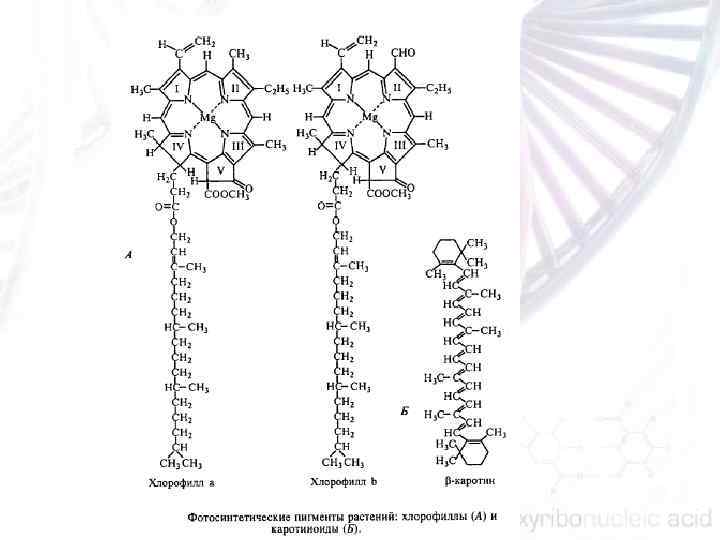
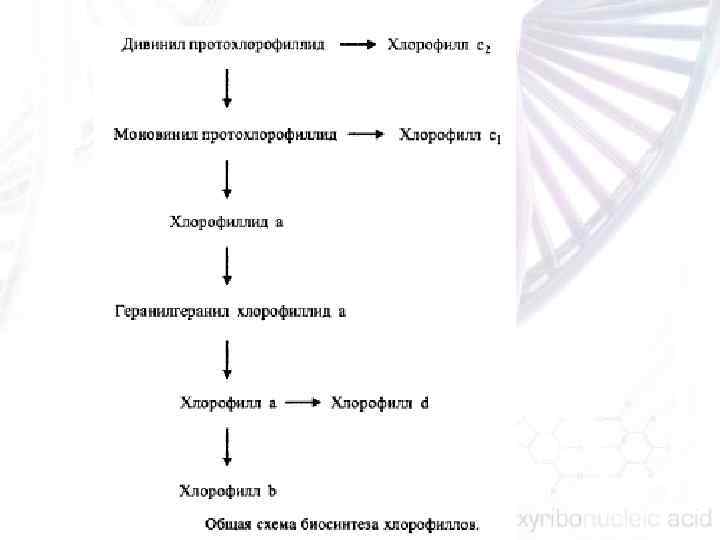
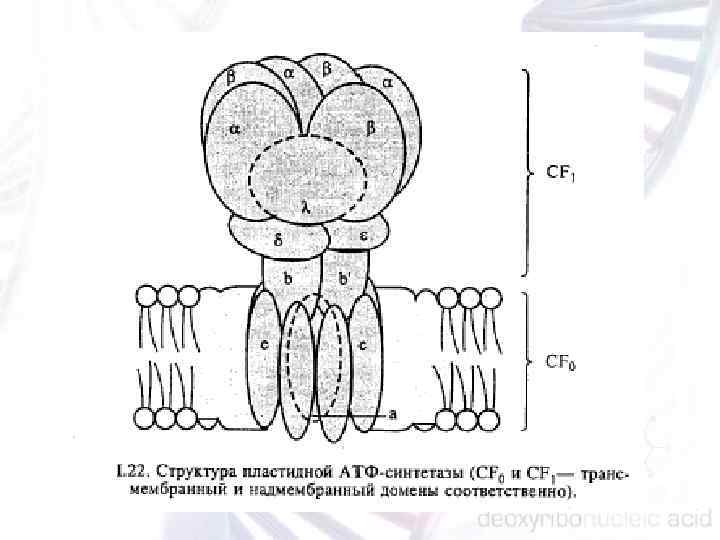
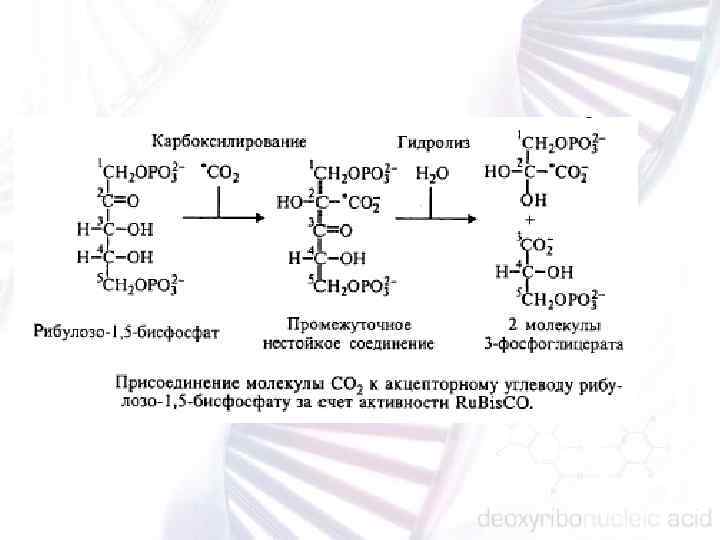
Световая фаза фотосинтеза обслуживается несколькими молекулярными комплексами, весьма консервативными у большинства фототрофных эукариот. К числу этих комплексов относятся: n n n ферментативные системы, осуществляющие биосинтез основных фотосинтетических пигментов; белковые компоненты светособирающих антенн; фотосистемы I и II, способные преобразовы вать поглощенную солнечную энергию в химическую; система транспорта возбужденных электронов, обеспечиваю щая поляризацию внутренних мембран хлоропласта; комплекс пластидной АТФ синтетазы; комплекс пластидной НАД • Н дегидрогеназы.


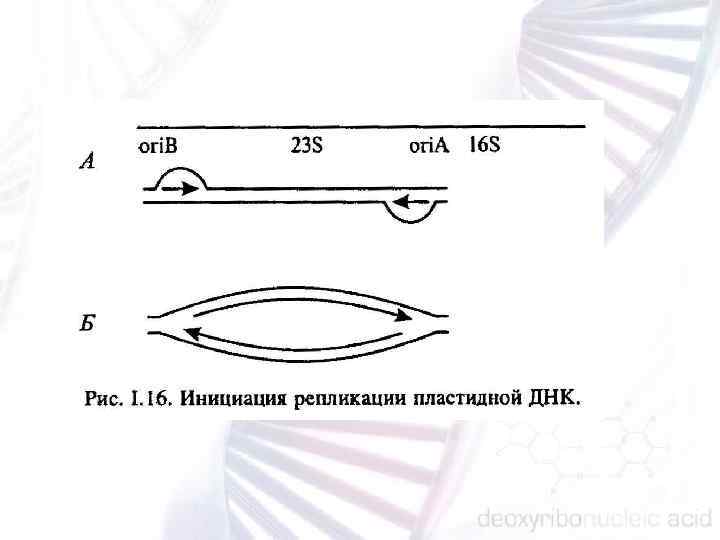
В соответствии со своей структурой промоторы всех пластидных генов подразделяются на три следующие группы: канонические эубактериальные промоторы, распознаваемые собственной РНК полимеразой пластид. Промоторы этой группы обеспечивают транскрипцию подавляющего большинства пластидных генов, непосредственно контролирующих процесс фотосинтеза; неканонические промоторы, обслуживаемые ядерно кодируемой РНК полимеразой. Такие промоторы свойственны нескольким пластидным локусам, в том числе rif оперону, включающему в себя гены rро. В, rpo. Cl и rро. С 2; универсальные промоторы, которые содержат оба типа регу ляторных последовательностей, а потому успешно распознаются обеими РНК полимеразами. Подобные промоторы характерны для большинства генов «домашнего хозяйства» пластид.

Созревание пластидных РНК. Экспрессия пластидных генов не требует кэпирования и полиаденилирования транскриптов. Тем не менее многие пластидные РНК претерпевают процесс созревания, состоящий из одного или нескольких этапов. К числу таких этапов относятся: n сплайсинг транскриптов, обладающих интрон экзонной структурой; n формирование зрелых концов у транскриптов; n редактирование некоторых и. РНК; n посттранскрипционное наращивание З' конца у большинства т. РНК.

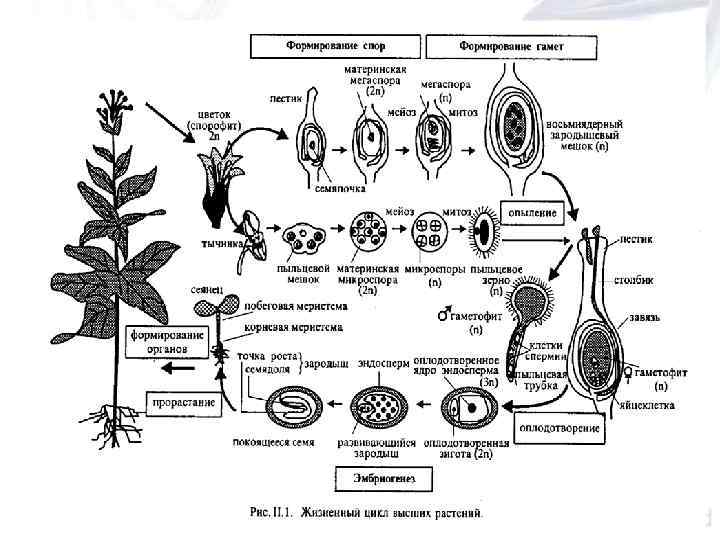
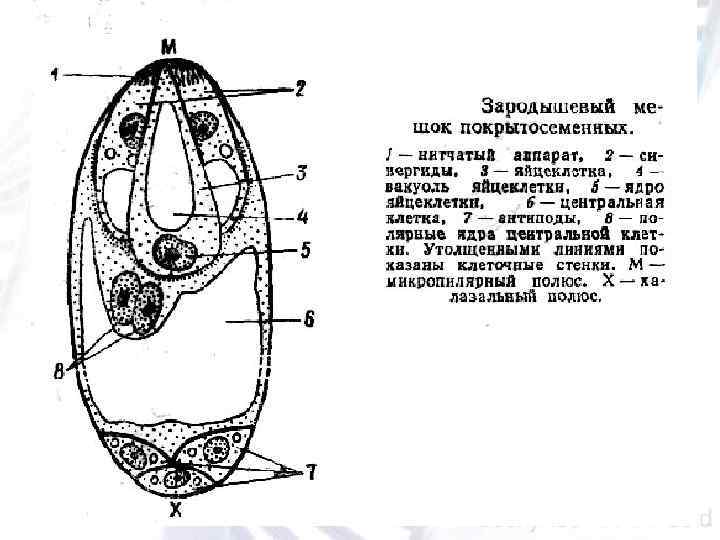
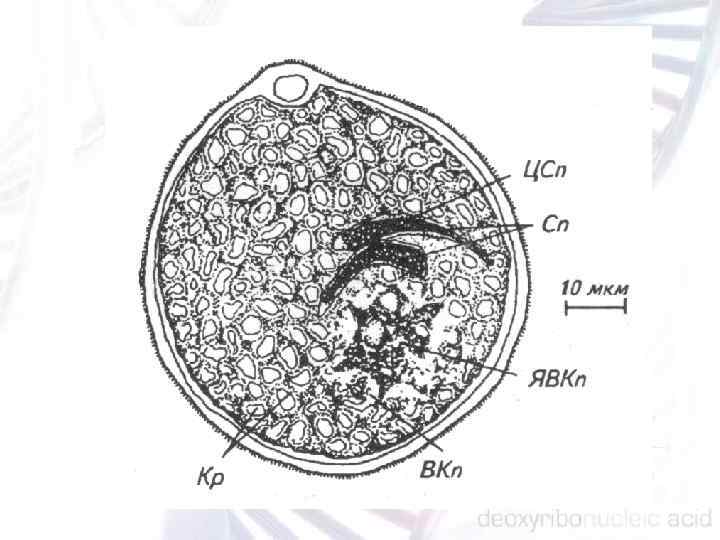
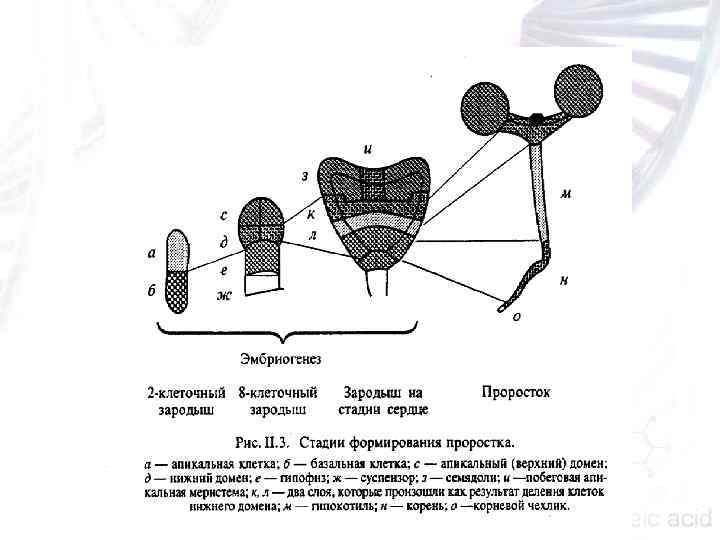
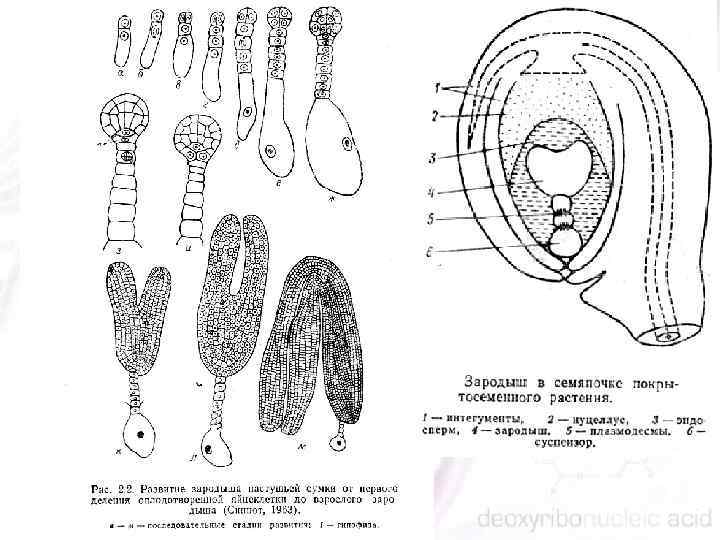
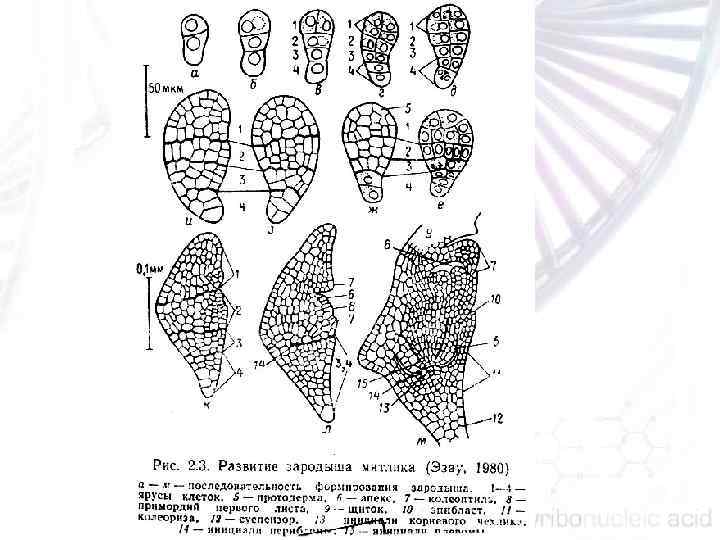

Апикальная клетка делится с формированием 4 , 8 , 16 клеточного зародыша. 4 клеточный зародыш состоит из двух основных слоев: верхнего и нижнего, которые сохраняются в течение всего эмбриогенеза Из верхнего слоя в дальнейшем формируются побеговая апикальная меристема (ПАМ) и верхняя часть семядолей. Из нижнего слоя в свою очередь формируются три слоя, которые в литературе получили название: апикальный, центральный и базальный домены. Из апикального домена формируется нижняя часть семядолей, из центрального — гипокотиль, а из базального — корневая апикальная меристема (КАМ), из которой образуется корень

При формировании зародыша происходит изменение скорости и направления деления, появление асимметрии и дифференциация тканей и органов. n Перемещения клеток, как у животных, не происходит. В процессе развития зародыша накапливаются питательные вещества. Созревание зародыша заканчивается тем, что его органы сформированы, ткани теряют воду, уменьшается метаболическая активность и наступает период покоя. n Зародыш в определенных условиях может развиваться без окружающих тканей. n

n К моменту отделения семени от материнского растения зародыш уже дифференцирован на три основные части: n апекс корня, апекс побега и семядоли (одна или две). n n

Полиплоидизация широко распространена в тканях растений. Только 20 % его клеток строго диплоидны. Полиплоидия — это не обязательное свойство дифференцированных клеток, а скорее, последствие дифференцировки. Умножение генетического материала зародыша важно для его функциональной активности.

ГЕНЫ, ЭКСПРЕССИРУЮЩИЕСЯ В РАННЕМ ЭМБРИОГЕНЕЗЕ 1) гены «домашнего хозяйства» — экспрессируются конститутивно в процессе всей жизни растения, в том числе и в зародыше; 2) эмбриоспецифические гены, которые можно подразделить на гены раннего эмбриогенеза, гены, экспрессирующиеся в процессе созревания зародыша, гены, экспрессирующиеся в позднем эмбриогенезе и захватывающие процесс прорастания семени
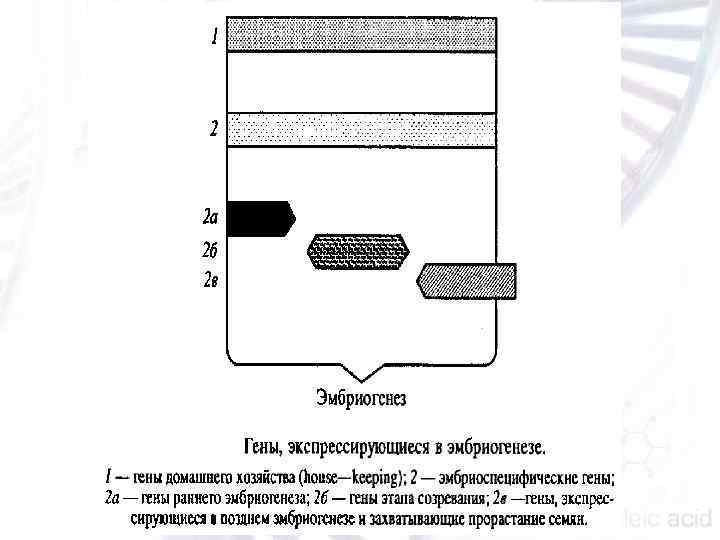

АТМ 1 (от Arabidopsis thaliana rneristem L 1). n KUNITZ (KTI) n

ГЕНЫ, ЭКСПРЕССИРУЮЩИЕСЯ В ПРОЦЕССЕ СОЗРЕВАНИЯ ЗАРОДЫША В семядолях двудольных экспрессируются гены, контролирующие синтез таких белков, как легумины, вицилины, фазеолины и др. n В эндосперме однодольных экспрессируются гены, которые контролируют синтез таких белков, как зеины, глиадины, глютенины. n n гены, которые экспрессируются в алейроновом слое.

МУТАНТЫ ПО ЭМБРИОГЕНЕЗУ 1. Нарушения на ранних этапах деления зиготы и формирования эмбрио. Мутации проявляются в F 2 на уровне проростков. n 2. Эмбриональные летали, которые проявляются в стручках на растениях Fl. Это самый большой класс мутантов, характеризующийся нарушениями в аккумуляции пигмента и запасных веществ. n 3. Нарушение покоя семян, которое проявляется как прорастание семян в стручке на растениях Fl. n

Мутанты раннего эмбриогенеза По оси зародыш можно разделить на 3 части: n апикальная, содержащая семядоли и побеговую апикальную меристему; n центральная, содержащая гипокотиль; n базальная, которая содержит корневую апикальную меристему.
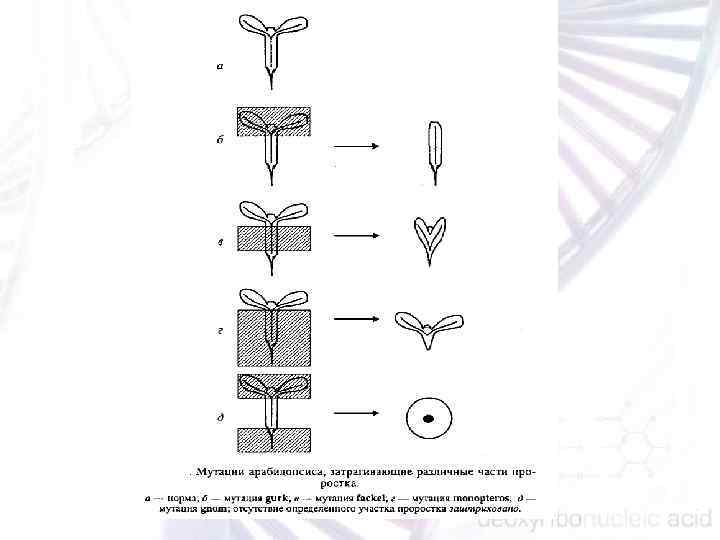

n n мутанты, характеризующиеся специфическими изменениями в разных частях зародыша Ген GURKE (GK) действует на уровне семядолей и апикальной меристемы. У мутантов, в зависимости от аллельного состояния, в разной степени редуцирован апикальный район — отсутству ют семядоли и побеговая апикальная меристема. Как правило, у мутантных проростков в апикальной зоне формируется неорганизованная клеточная масса. Ген FACKEL (FK) действует на уровне центрального района. У мутантов отсутствует гипокотиль, в результате чего семядоли «сидят» прямо на корневой части. У мутантов нарушена структура семядолей и их количество, которое может быть больше двух. У проростков нормально развита корневая система. Ген MONOPTEROS (МР) действует в центральной и базальной частях зародыша. У мутанта отсутствует гипокотиль и корни. Эта мутация по своему проявлению комплементарна мутации gurk, которая характеризуется отсутствием верхней части проростка. Количество семядолей у мутанта тр варьирует от одной до двух. У мутанта mр первые деления зиготы проходят без нарушений вплоть до 8 клеточного зародыша. Изменения отмечены лишь начиная со стадии перехода сердце к стадии торпедо в нижнем слое зародыша и в начале гипофиза и не затрагивают верхнего слоя зародыша. Ген GNOM (GM) действует на уровне апикального и базального районов проростка. У мутанта редуцированы апикальная побеговая и корневая меристемы, а также сильно изменены семядоли. У мутан таgnom первое деление характеризуется формированием двух оди наковых клеток вместо терминальной и базальной, как это имеет место у форм дикого типа. Для gnom характерны нарушения и последующих делений.

n Анализ мутантов показал, что мутация, затрагивающая одну часть зародыша, как правило, не проявляется в другой его части. Таким образом, экспрессия «эмбриональных» генов пространственно-специфична, а клетки, формирующие определенные домены зародыша, автономны. Все описанные мутации являются ядерными и рецессивными.

Мутант raspberry был получен с помощью Т ДНК мутагенеза у арабидопсиса. У него потеряна способность к переходу от стадии глобула к стадии сердце, при этом первая стадия долго сохра няется. Как сказано выше, дифференциация тканей начинается на стадии глобула. Нарушения на этой стадии приводят к серьезным аномалиям в развитии зародыша. У мутанта отсутствуют семядоли и часть гипокотиля, расширен район суспензора. Таким образом, нарушения в момент дифференциации тканей приводят к критическим изменениям в формировании зародыша.

У мутантов keule (keu) и knolle (kn) также нарушена дифференцировка тканей. В частности, у мутанта knolle нарушена дифференциа ция эпидермальных и проводящих тканей. В резуль тате у мутантных зародышей эпидермальная ткань отсутствует, а проводящая ткань состоит из аномаль но крупных клеток, при этом сам зародыш выглядит округлым. В результате таких нарушений зародыш сильно изменен и характеризуется отсутствием апикальной и базальной части. У другого мутанта keule отмечены нарушения в эпидермальной ткани — эпидермальные клетки раздуты. Однако даже столь незначительное нарушение в дифференцировке тканей приводит к тому, что измененный зародыш приобретает ненормально округлые очертания. n Нарушения в дифференцировке тканей приводят к нарушениям в морфогенезе.

Мутанты позднего эмбриогенеза. Мутация leafy cotyledons (lec 1) у арабидоп сиса получена на основе химического мутаге неза. У этих мутантов семядоли проростков имеют листоподобное строение, так как на их поверхности из протодермального слоя фор мируются трихомы. Трихомы — это маркер постэмбрионального развития, и формируют ся они только на поверхности листа, стебля и цветков. Кроме того, у мутанта в тканях семядолей обна ружены характерные для листа мезофильные клетки — устьица, а в клетках семядолей отсутствуют запасные белки. Для мутантов также характерно раннее прорастание и потеря стадии покоя семян.

Другой мутант — lес2 — имеет такой же фенотип, но у него не нарушена стадия покоя и аккумуляция запасных белков в тканях семядолей. Гены LEC функционируют в норме независимо на стадии созревания. Анализ мутантов показал, что в норме гены LEC контролируют формирование семядолей, аккумуляцию запасных белков, поддержание покоя семян. Кроме того, гены LEC супрессируют проявление признаков листа (наличие трихом, мезофила, устьиц) в эмбриогенезе.

Ген FUS 3 (FUSCA 3) также действует на поздней стадии эмбриогенеза. Рецессивная мутация по этому гену приводит к аккумуляции антоциана в семенах, а сами семена имеют измененную морфологию. Кроме того, у мутантов не накапливаются запасные белки в семядолях, нарушен ответ на свет. В целом фенотип этих мутантов сходен с фенотипом lес. В отличие от мутантов lес у мутанта fus 3 трихомы появляются на семядолях проростков при условии, если проростки выращивать in vitro. Кроме того, у мутанта fus 3 не изменен гипокотиль, а семядоли тоньше и более вытянуты, чем у мутантов lес. В ходе генетического анализа было показано, что в процессе развития ген LEC 1 действует раньше генов LEC 2 и FUS, и мутация по гену LEC 1 вызывает большее число нарушений в эмбриогенезе. n
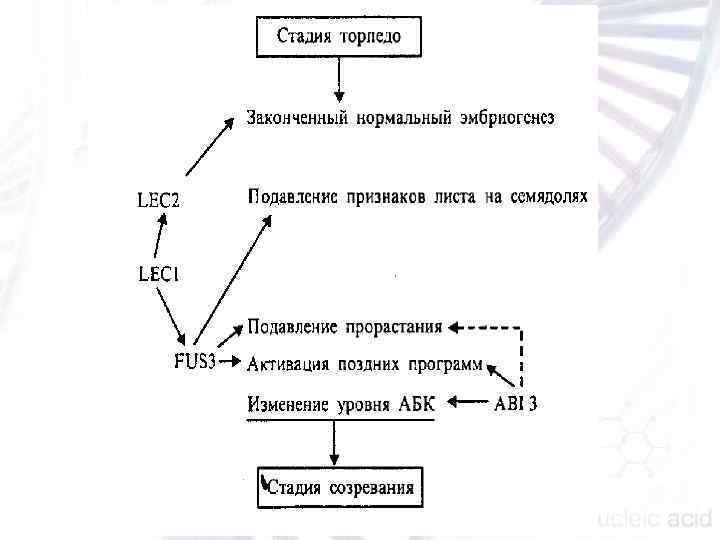

n n Продуктом гена LEC 1 является транскрипционный фактор, который регулирует экспрессию генов LEC 2 и FUS 3. Показано, что гены группы LEC и ABI 3 регулируют развитие семени через разные пути, предотвращая потерю таких функций, как способность к «высыханию» и «покою семян» . Мутанты по гену ABI 3 также характеризуются чувствительностью к АБК и нарушением покоя семян. Двойной контроль важнейших процессов у растений является широко распространенным явлением. То, что разные гены с одинаковыми функциями могут «подстраховывать» друга, эволюционно оправдано и является одним из принципов адаптации растений.

Основными факторами, лимитирующими дифференцировку зародыша, являются: n скорость деления клеток; n асимметричность в делении; n полярность клеток. Как показал анализ мутантов, затрагивающих структуру зародыша, каждый его район формируется автономно, а мутация, затрагивающая одну часть зародыша, не влияет на другую. Дифференциация тканей происходит раньше и независимо от морфогенеза. Пока клетка не дифференцирована, ее судьба не определена.

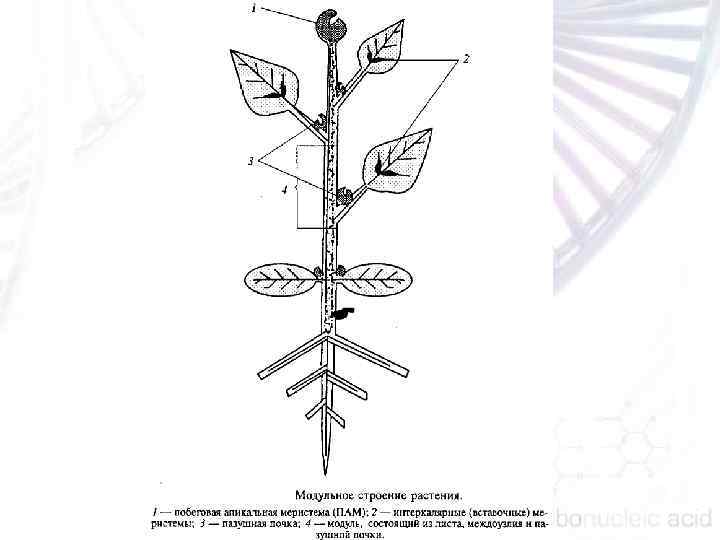
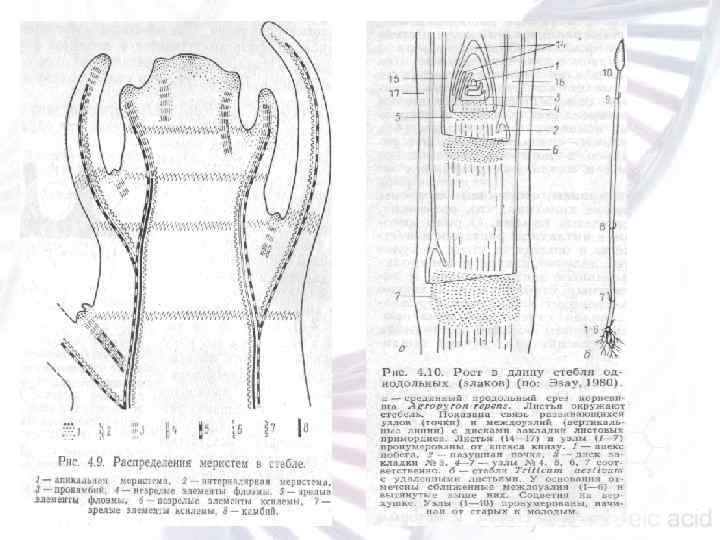
Меристемы — это очаг недифференцированных клеток, способных к активному делению. У растений выделяют несколько типов меристем — апикальные (недетерминированные), детерминированные и интеркалярные. Апикальные меристемы выполняют следующие функции: поддержание меристемы, формирование органов.

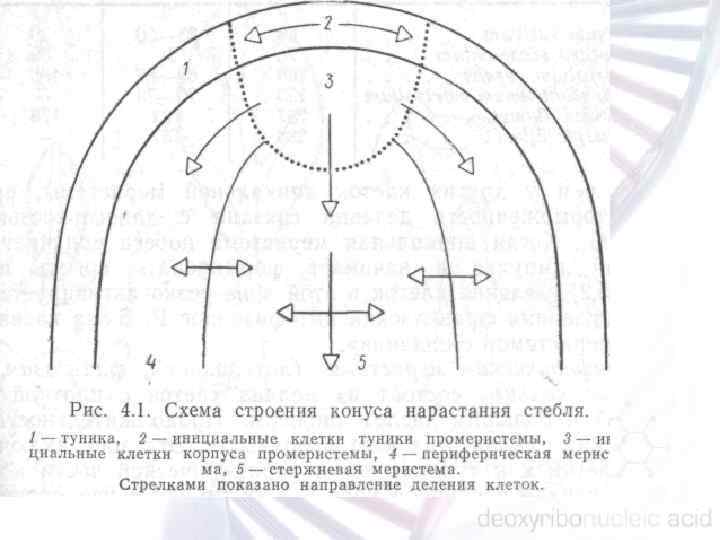
ПАМ, или SAM (от Shoot Apical Meristem), — небольшая группа клеток, которая формируются из верхнего слоя апикальной клетки в эмбриогенезе на стадии глобула сердце и сохраняются в постэмбриональном развитии. Это мелкие клетки с плотной цитоплазмой. Побеговая апикальная меристема у цветковых растений имеет размер в среднем 100 мкм в диаметре и включает 800— 1200 клеток. У арабидопсиса ПАМ много меньше и включает 50— 70 клеток n Центральная зона (ЦЗ) находится на дистальном конце и содержит инициальные медленно делящиеся клетки с выпуклыми ядрами. Клетки в этой зоне функционируют по типу стволовых у животных и служат источником клеток для других зон меристемы. n Клетки периферической зоны (ПЗ) окружают центральную зону в виде наружной трубы. Скорость митоза в этой зоне много выше, чем в ЦЗ. Из клеток этой зоны формируются латеральные органы, например листовые зачатки (примордии). Формирование листовых примордиев, из которых развиваются листья, происходит на фланкирующих участках этой зоны. n В основании ЦЗ расположена зона РИБ (подстилающая зона), которая является границей между недифференцированными и дифференцированными клетками. Клетки зоны РИБ делятся с высокой скоростью и формируют центральную часть побега — стебель.
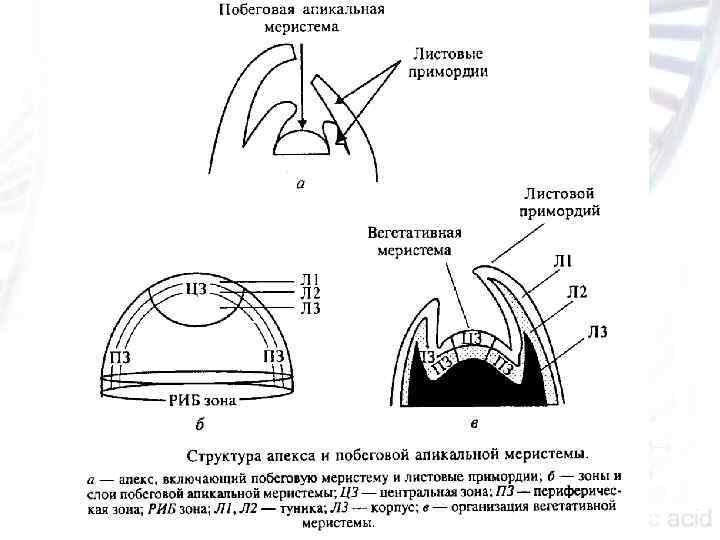

В свою очередь каждую зону подразделяют на три слоя: Л 1, Л 2, ЛЗ. В слое Л 1 клетки делятся антиклинально (параллельно поверхности), что обеспечивает рост тканей в длину. В слое Л 2 клетки делятся также антиклинально, оба слоя вместе формируют тунику и служат основой для образования тканей эпидермиса и мезофилла. В слое ЛЗ деления происходят в двух направлениях — параллельно и перпендикулярно поверхности (антиклинально и периклинально).
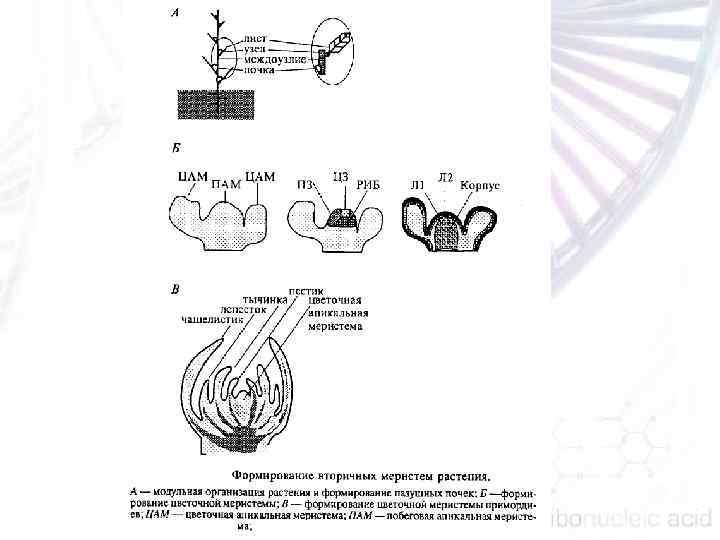

При переходе к репродуктивной фазе развития ПАМ изменяет свою активность и назначение и формирует уже не листовые, а цветочные (флоральные) меристемы (ЦАМ). Цветочные меристемы имеют измененную форму, количество клеток в ней увеличено. Кроме того, ПАМ и ЦАМ имеют разную судьбу: ПАМ — это недетерминированные меристемы, которые дают начало большому числу органов, а ЦАМ — это детерминированные меристемы, из которых образуются в центре цветка пестики и тычинки, характеризующиеся детерминированным ростом. Из определенных участков флоральной меристемы на строго определенном расстоянии друг от друга формируются зачатки органов цветка.

Тип клеточного деления (параллельно или перпендикулярно поверхности) определяет форму органа, а число клеточных делений — его размер. Различные сочетания направления, скорости и числа делений обеспечивают формирование органов растения, которые различаются по морфологии и размеру. Анализ мутаций, затрагивающих меристему, показал, что различные способы деления клетки генетически контролируются независимо

МУТАНТЫ С НАРУШЕНИЯМИ ПОБЕГОВЫХ АПИКАЛЬНЫХ МЕРИСТЕМ Процесс формирования ПАМ нарушен у мутантов stm (shoot meristem less), wus (wuschell), zll (zwill), pnh (pinhead), clv (clavata) и др. , также у всех перечисленных мутантов она в той или иной степени редуцирована, у мутантов clv — увеличена.

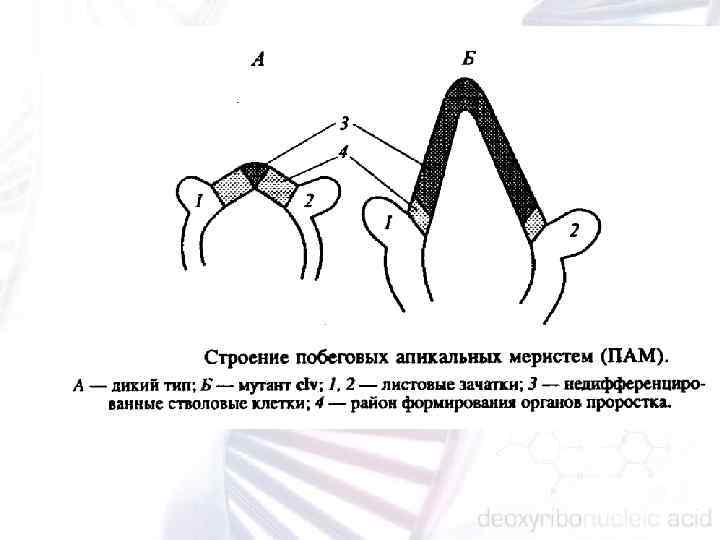
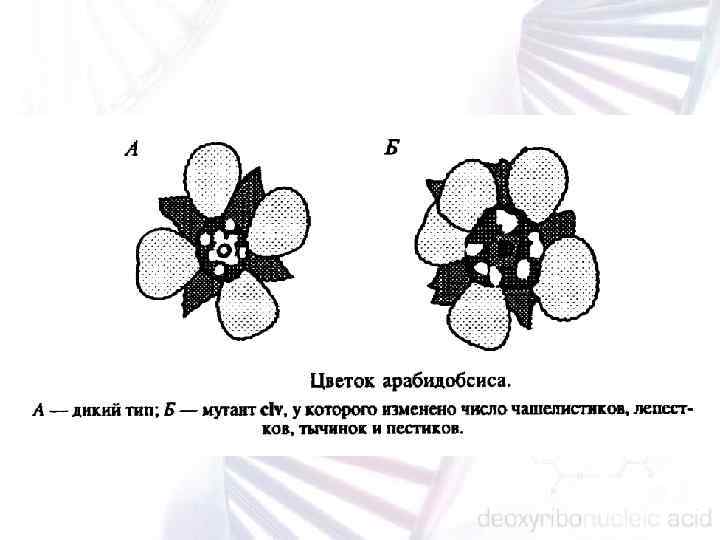

Ген STM (от Shoot Meristem Less) регулирует поддержание ство ловых клеток в недифференцированном состоянии и ингибирует их переход к инициации листовых примордиев. Ген WUS (от Wushel) необходим для поддержания клеточного деления в меристематическом центре, а мутация wus приводит к терминации меристематической активности. В противоположность генам STM и WUS, ген CLV 1 регулирует формирование органов и репрессирует клеточные деления. Гены STM и CLV 1 являются антагонистами и комплементарно ре гулируют баланс между недифференцированными и дифференци рованными клетками в ответ на эндо и экзогенные факторы. В ходе генетического анализа показано, что ген WUS регулируется генами STM и CLV 1. Ген ZLL (от ZWILLE) требуется для поддержания центрально периферической организации ПАМ. Его экспрессия является кри тической точкой всамореорганизации ПАМ, которая приводит к формированию органов. Ген ZLL необходим для поддержания стволовых клеток в развивающихся побеговых меристемах в недифференцированном состоянии в течение перехода от эмбрионального развития к постэмбриональному формированию органов. Ген STM экспрессируется в течение эмбриогенеза до начала экспрессии гена ZLL и является эпистатичным по отношению к нему.

Постэмбриональное развитие высших растений связано с повторяющимся формированием органов через реорганизацию стволовых клеток в ПАМ, которая формируется после закладки основных тканей, семядолей и гипокотиля в эмбриогенезе. Органы инициируются на периферии побеговых апикальных меристем, тогда как в центральной зоне стволовые клетки поддерживаются в недифференцированном состоянии. В ПАМ экспрессируется группа генов, часть из которых регулирует поддержание популяции стволовых клеток в недифференцированном состоянии, тогда как другие приводят к дифференцировке клеток с последующим формированием органов


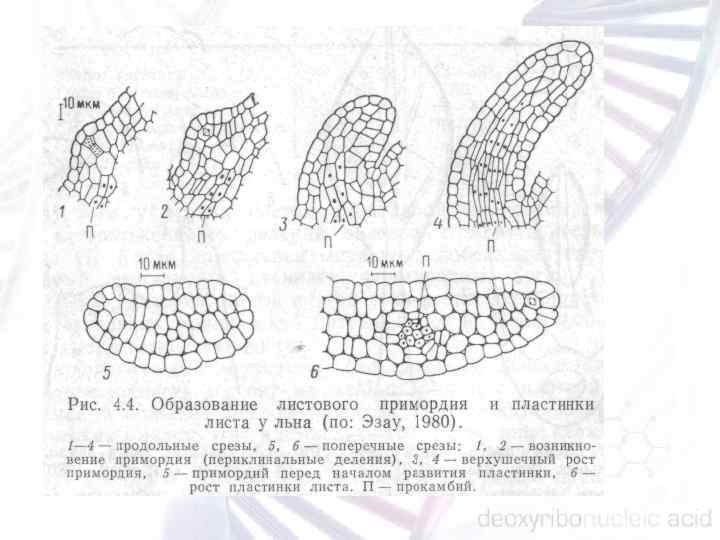
РАЗВИТИЕ ЛИСТА
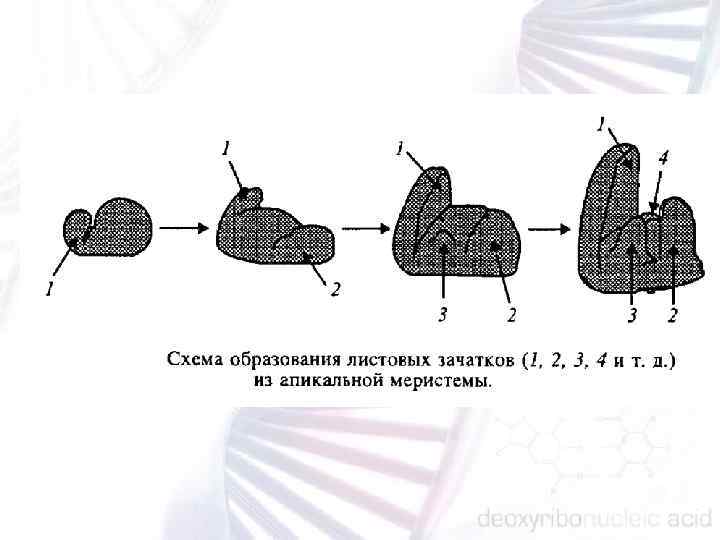

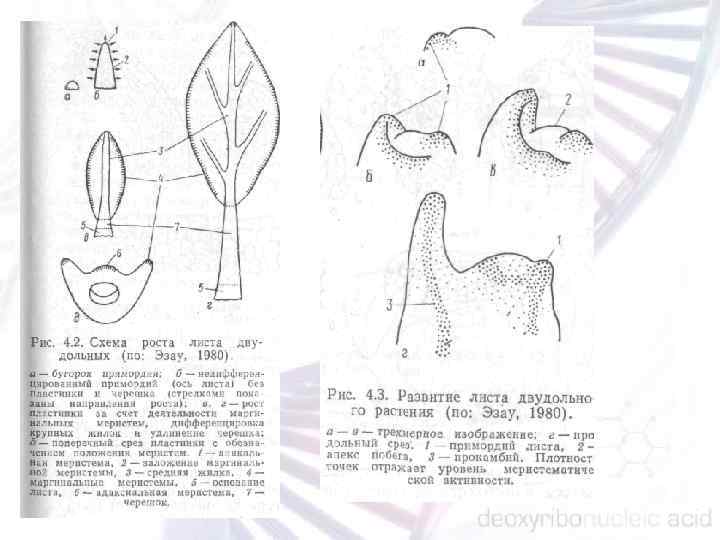
Развитие листа можно разделить на три стадии: образование листового зачатка; образование оси листа; образование листовой пластинки.

forever young (fey) narrow sheath revoluta (rev) Knotted 1 (KN 1) у кукурузы и у арабидопсиса гена KNAT 1
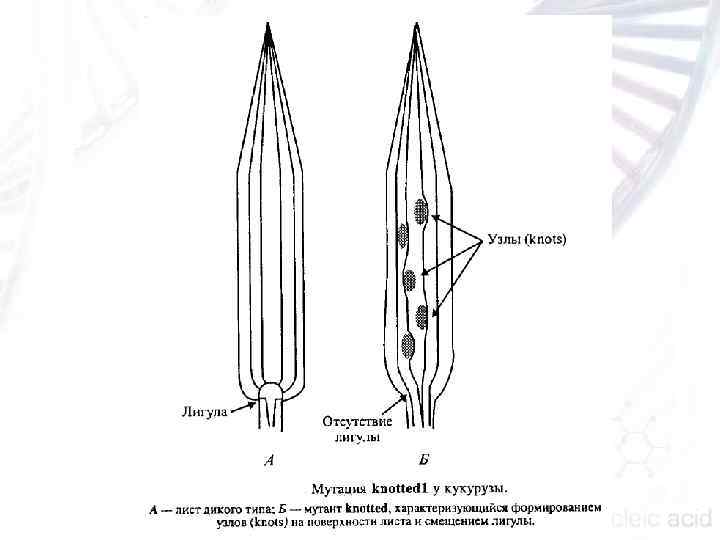
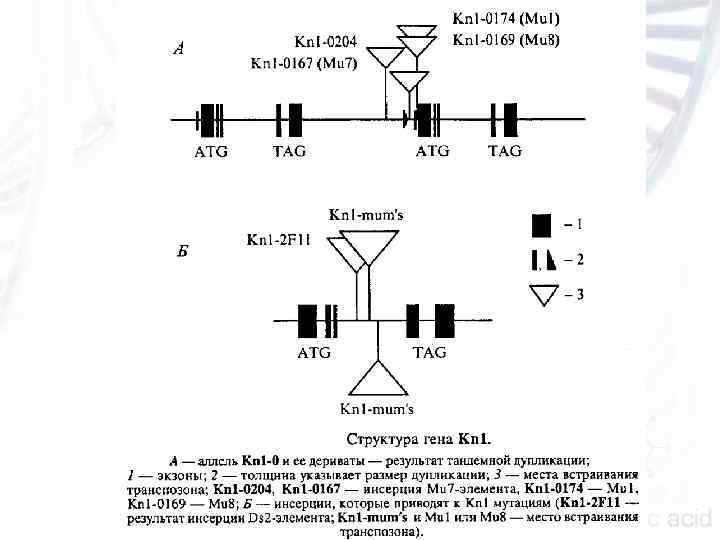

Полученные мутанты в зависимости от фенотипа разделили на три группы: для мутантов 1 го типа характерна потеря большого числа меристем соцветий. В результате у растений не хватает ветвей и колосков в мужских соцветиях; у мутантов 2 го типа значительно изменен процесс форми рования пестика. У таких растений появляется множество пести ков, которые создают эффект «пестик в пестике» , при этом они сливаются и формируется крупный пестик с большим количест вом шелковых нитей, торчащих из початка. у мутантов 3 го типа образуется увеличенное количество листьев.

n гены KNAT 1 и KNAT 2, в норме, также как и KN 1, активируют клеточное деление, репрессируя клеточную дифференцировку. Гены KN 1, KNAT 1 и KNAT 2 действуют на уровне меристем и оказывают свое влияние на развитие листа. Это неудивительно, так как листовые зачатки развиваются из апикальных меристем.
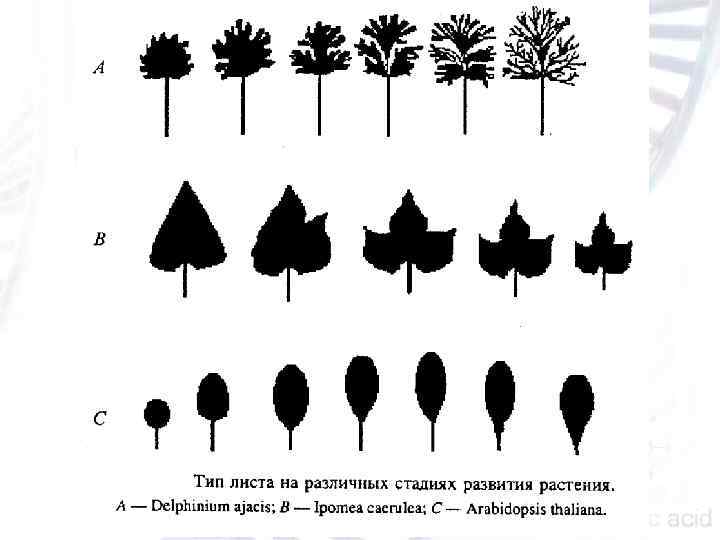


У кукурузы и арабидопсиса выделено наибольшее количество мутаций по развитию и типу листа, которые можно разделить на две группы, затрагивающие: инициацию органа (organ initiation) и его идентичность (organ identity). Для первой группы мутаций характерно изменение морфологии листа на всех стадиях развития растения. Гены, контролирующие такие изменения, вовлечены в регуляцию перехода от ювенильной к вегетативной и репродуктивной фазам развития. К генам первой группы можно отнести ген Viviparous (VP 8) и гены, контролирующие биосинтез гиббереллина (ГК) — Dwarf 1 (Dl), Dwarf 3 (D 3), Dwarf 5 (D 5) и Anther ear (AN 1). Для мутантов по этим генам характерно длительное формирование листьев ювенильного типа. Экзогенное применение ГК фенотипически супрессирует эффект мутаций. Ген VP 8 контролирует фактор, который необходим для перехода к цветению. мутация amp 1 (altered meristem pjrogram 1) характеризуется ускоренной программой инициации развития листа и приводит к формированию большего числа ювенильных листьев и трансформации части листьев в семядоли Мутант psd (paused) характеризуется задержкой развития листьев, которая приводит к полному отсутствию ювенильных листьев. У мутанта hasty на месте формирования ювенильных листьев развиваются взрослые листья.

У второй группы мутаций (organ identity) затронуты только стадие специфические признаки. Гены, контролирующие эти изменения, необходимы для формирования листа, морфологически характерного для определенной фазы. Их экспрессия зависит от эн догенных сигналов. n К ним группе относятся мутации по генам Teogod I (TP 1), Teopod 2 (ТР 2), Teopod 3 (ТРЗ), Corngrass (CG), Glossy 15 (GL 15), которые выделены у кукурузы. n У мутантов затронуты такие признаки, как морфология листовой пластинки, восковой налет, наличие трихом и опушение.

Таким образом, анализ мутантов показал, что процессы инициации листа (organ initiation) и собственно формирование листа (organ identity) генетически контролируются независимо. Координированная экспрессия двух групп генов и определяет время появления определенного типа листа. ПАМ играют немаловажную роль в инициации листовых зачатков, так как мутации, затрагивающие формирование ПАМ, приводят к формированию измененных листьев. Ярким примером является мутация по гену KN 1, функция которого заключается в поддержании клеток ПАМ в недифференцированном состоянии, с одной стороны, и репрессией процессов дифференцировки — с другой. Именно гены класса KNOX 1 участвуют в передаче сигнала на пути инициации и формирования листа от семядолей до листьев, в основе которых лежит единая структура. Образование листа начинается с изменения ориентации и скорости клеточных делений в LI, L 2 и L 3 слоях. Скорость деления, которая в конечном итоге определяет размер листа и направление клеточных делений, генетически детерминированы независимо.

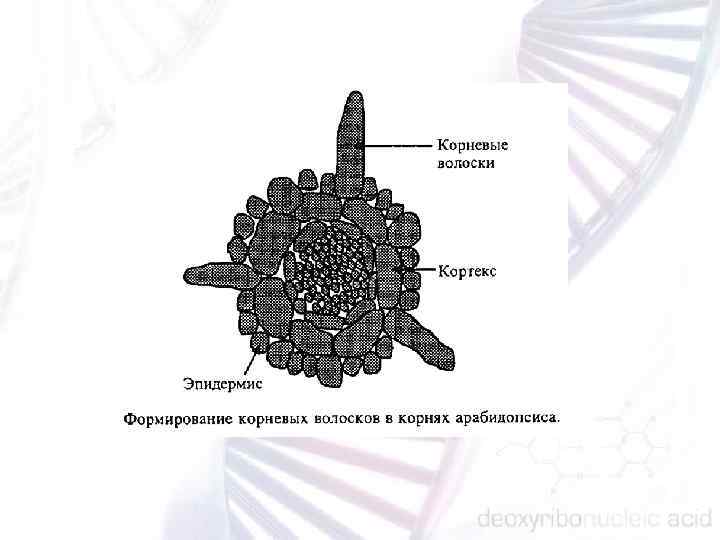
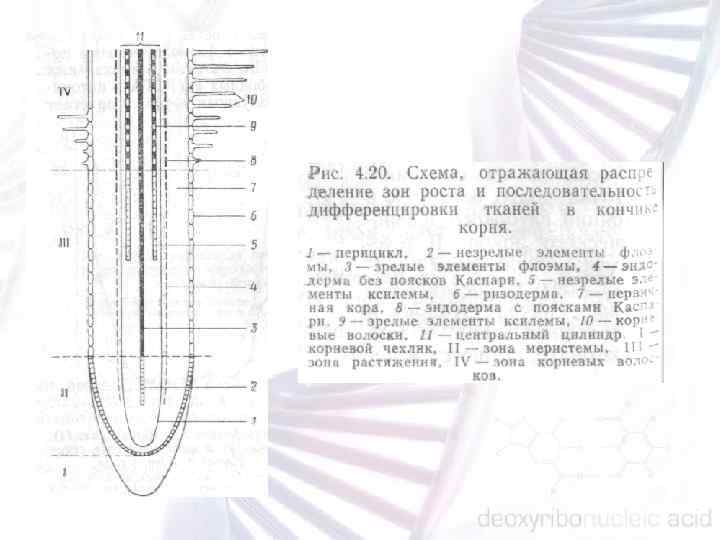
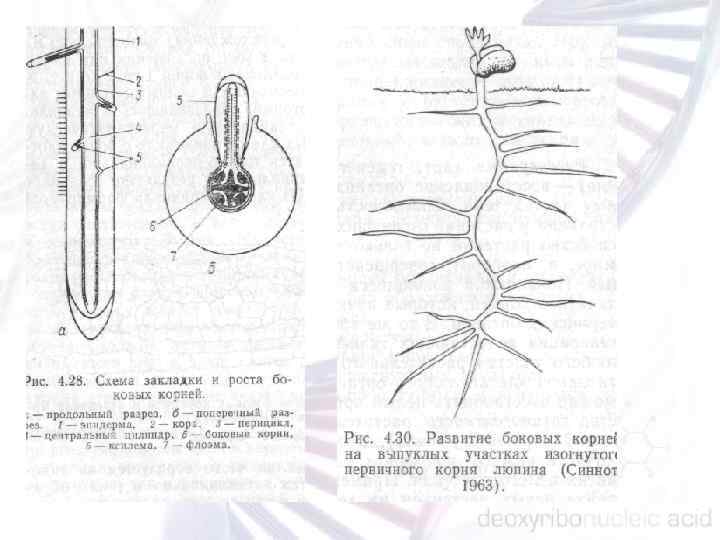
РАЗВИТИЕ КОРНЯ Корень — осевой орган, обладающий радиальной симметрией, он способен к длительному росту благодаря деятельности корневой апикальной меристемы (КАМ), которая находится на его дистальном конце и покрыта корневым чехликом. Боковыми органами корня являются корни 1 го и 2 го порядка, которые образуются из внутренних тканей. В корне выделяют следующие зоны: деление, растяжение, поглощение (зона корневых волосков), вся остальная часть корня относится к зоне проведения. Корень включает три главные тканевые системы: эпидермис, проводящую (васкулярную) ткань, которая состоит из флоэмы и ксилемы, и основная ткань, состоящая из эндодермы, кортекса и перицикла. Корневой чехлик часто выделяют как самостоятельную ткань.

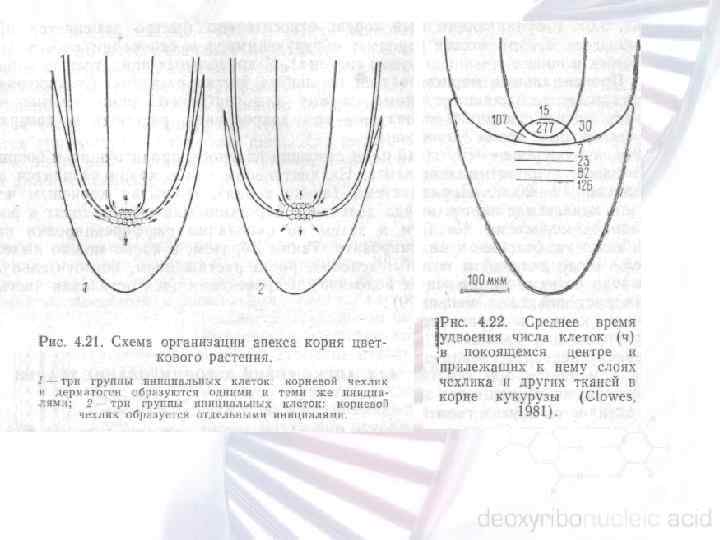
Ткани корня развиваются из четырех инициальных (стволовых) клеток: колумелла (columella) развитие корневого чехлика; перицикл/васкулярных инициации; клетки, из которых развивается эпидермис; кортекс/эндодермальный инициалий.
fass и tonneaw (ton) short root (shr) scarecrow (scr) hobbit (hbt) bombadil
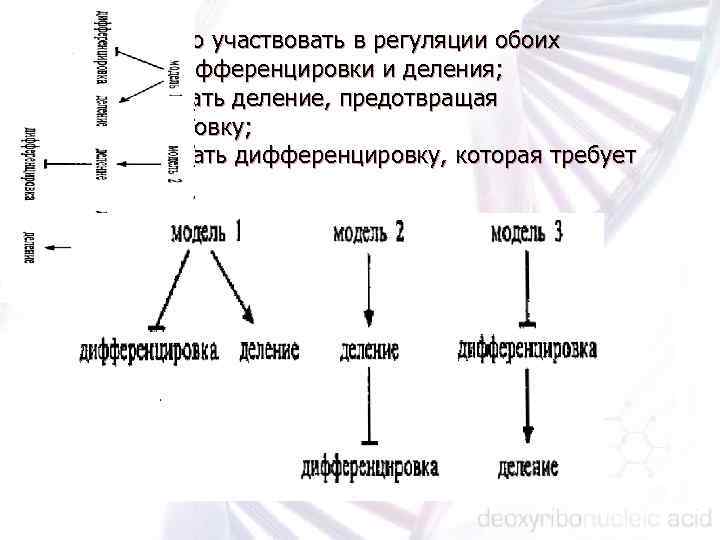
1) независимо участвовать в регуляции обоих процессов: дифференцировки и деления; 2) регулировать деление, предотвращая дифференцировку; 3) ингибировать дифференцировку, которая требует деления;

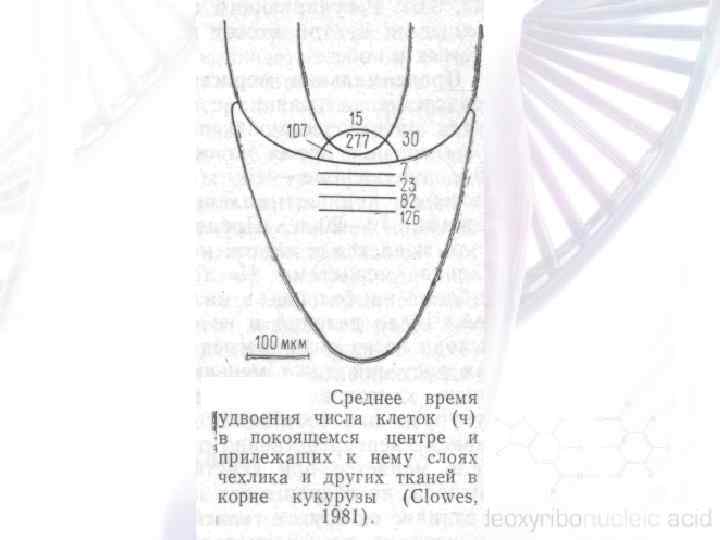
В меристеме корня арабидопсиса позиционные сигналы поступают из уже дифференцированных клеток и определяют направление дифференцировки клеток. Клетки, которые контактируют с неподвижным (покоящемся) центром, поддерживаются в инициальном состоянии, т. е. клетки неподвижного центра ингибируют дифференцировку окружающих клеток. Баланс между двумя антагонистическими сигналами является механизмом, который приводит к формированию определенной структуры в корневой меристеме, и определяют «судьбу» клетки.

transparent testa glabra (ttg) glabra 2 (gl 2) Constitutive Triple Response 1 (CTR 1) dwarf (dwr)


rml 1 rml 2 (root meristem less) cobra root epidermal blebbing sabre lion's tail

Основную роль в морфогенезе корня играет позиционный контроль, который определяет направление дифференцировки. Это заключение может быть неожиданным, так как имеется строгая корреляция между происхождением клеток от определенных инициалий и последующей структурой корня у многих видов, в том числе и у арабидопсиса. Однако примеры генетического анализа (анализ мутантов) и физических методов (лазерное облучение единичных клеток) показали, что «история» клеток или тканей в меньшей степени важна, чем их позиция в определении пути дифференцировки.


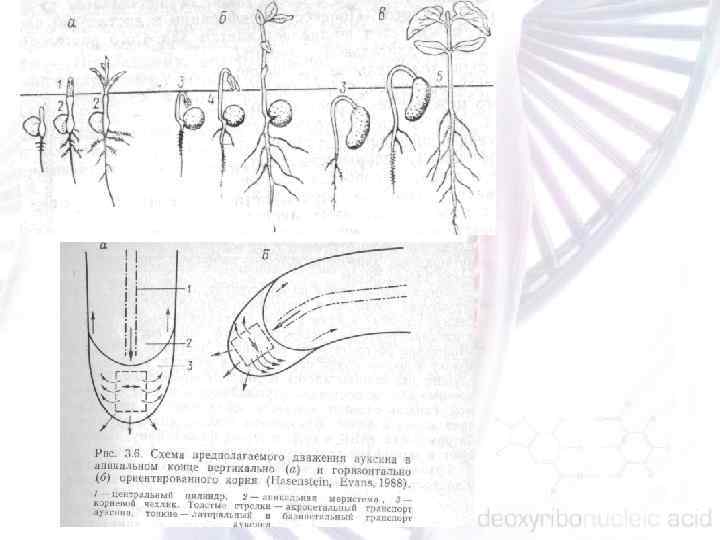


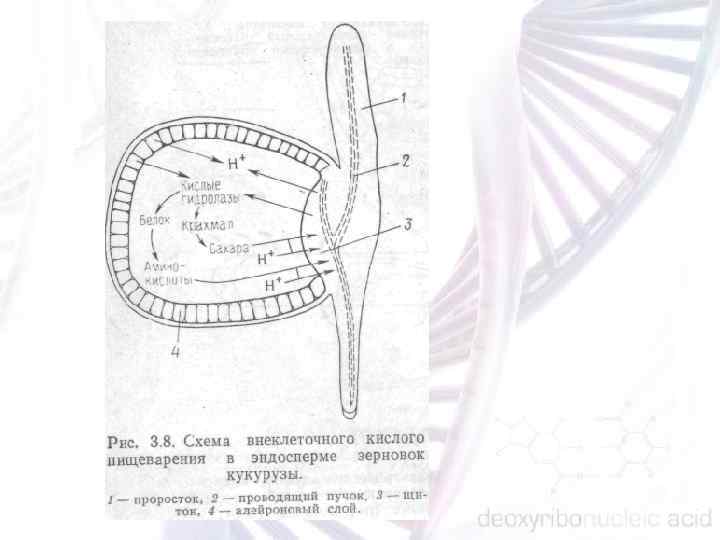
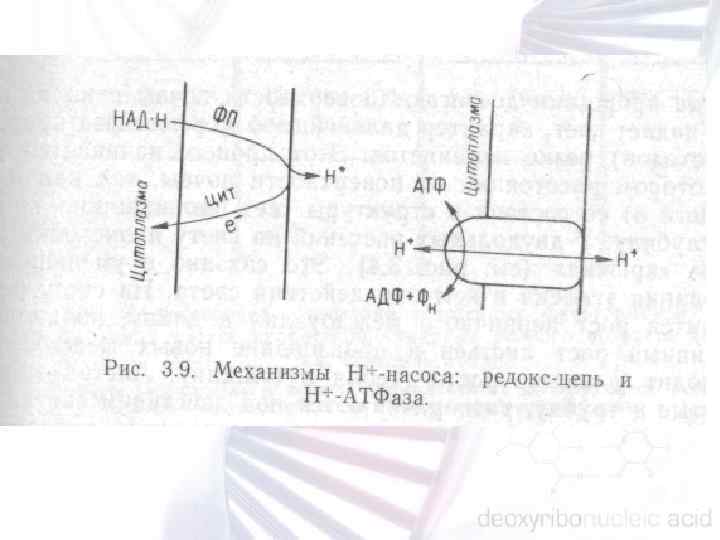
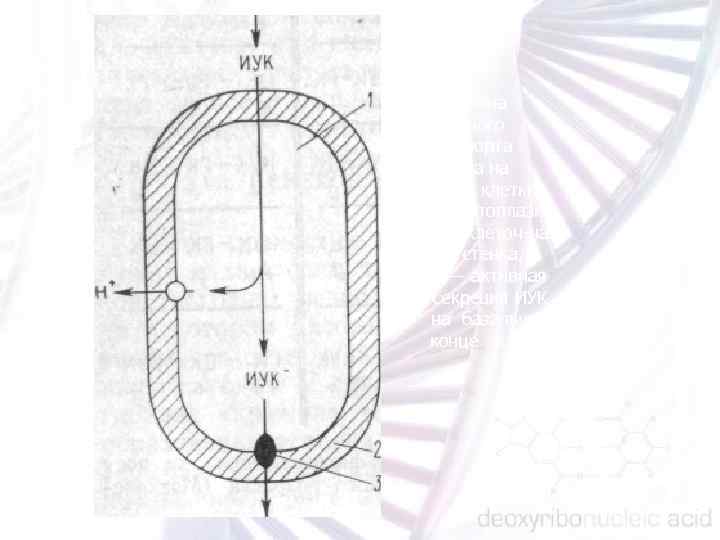
Схема механизма полярного транспорта ауксина на уровне клетки. 1 — цитоплазма, 2 — клеточ ная стенка, 3 — активная секреция ИУК на базальном конце клетки.
генетика развития растений 2-1.ppt