Биология. Лекция 5. Трансляция.ppt
- Количество слайдов: 43
Основы молекулярной биологии. Биосинтез белка. Трансляция. 1

План: 1. Рибосомный цикл биосинтеза белка а) строение рибосомы. Полисома б) эпицикл трансляции: инициация, элонгация, терминация в) особенности трансляции у про- и эукариот. 2. Посттрансляционные изменения белков: фолдинг, транспорт и деградация белков 2

1. Рибосомный цикл биосинтеза белка

а). Строение рибосомы. Полисома

Биосинтез белков 1. Наиболее сложный из генетических процессов; 2. Наиболее энергоемкий процесс; 3. Протекает с высокой скоростью (при 37˚ белок из 100 аминокислотных остатков синтезируется E. coli за 5 секунд) В 2009 году В. Рамакришнан (Великобритания), Т. Стейтс (США) и А. Йонат (Израиль) получили Нобелевскую премию "за исследования структуры и функции рибосомы". Собственно трансляция осуществляется рибосомой – белоксинтезирующей машиной 5
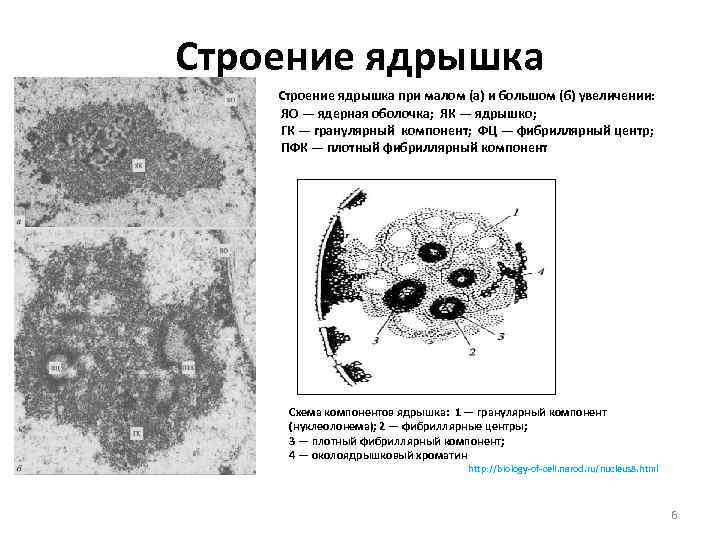
Строение ядрышка » » » Строение ядрышка при малом (а) и большом (б) увеличении: ЯО — ядерная оболочка; ЯК — ядрышко; ГК — гранулярный компонент; ФЦ — фибриллярный центр; ПФК — плотный фибриллярный компонент Схема компонентов ядрышка: 1 — гранулярный компонент (нуклеолонема); 2 — фибриллярные центры; 3 — плотный фибриллярный компонент; 4 — околоядрышковый хроматин http: //biology-of-cell. narod. ru/nucleus 8. html 6
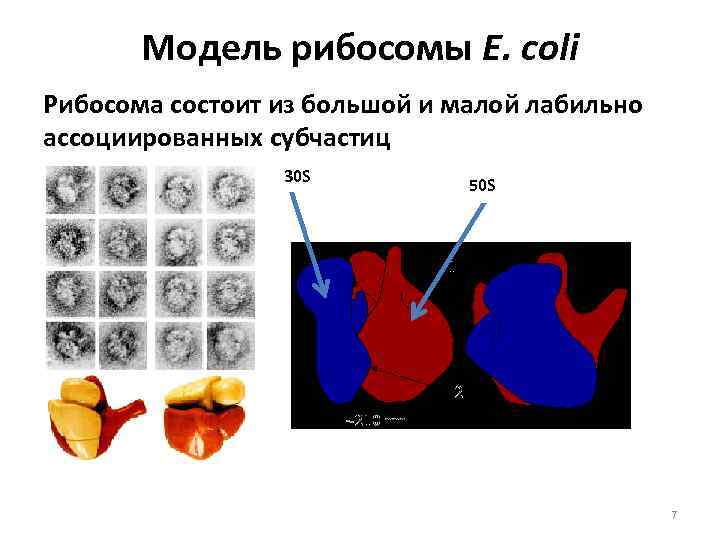
Модель рибосомы E. coli Рибосома состоит из большой и малой лабильно ассоциированных субчастиц 30 S 50 S 7
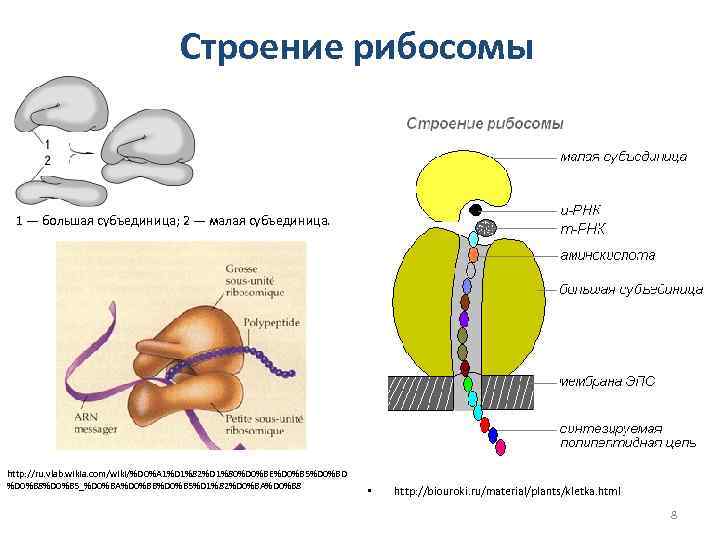
Строение рибосомы 1 — большая субъединица; 2 — малая субъединица. http: //ru. vlab. wikia. com/wiki/%D 0%A 1%D 1%82%D 1%80%D 0%BE%D 0%B 5%D 0%BD %D 0%B 8%D 0%B 5_%D 0%BA%D 0%BB%D 0%B 5%D 1%82%D 0%BA%D 0%B 8 • http: //biouroki. ru/material/plants/kletka. html 8
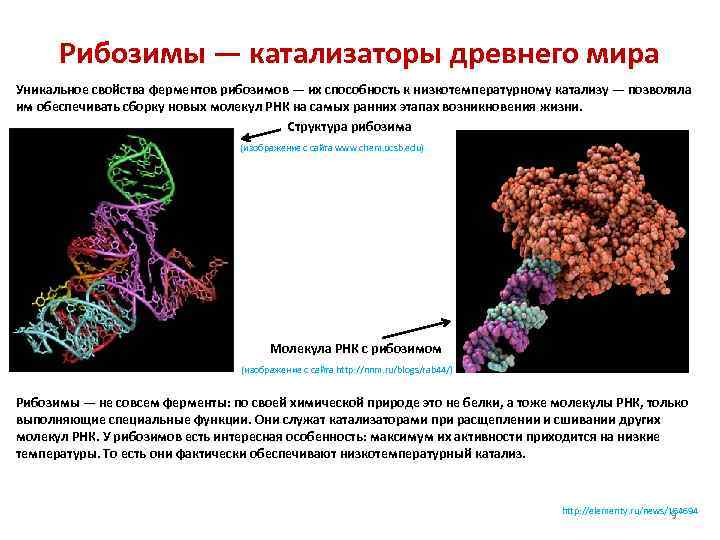
Рибозимы — катализаторы древнего мира Уникальное свойства ферментов рибозимов — их способность к низкотемпературному катализу — позволяла им обеспечивать сборку новых молекул РНК на самых ранних этапах возникновения жизни. Структура рибозима (изображение с сайта www. chem. ucsb. edu) Молекула РНК с рибозимом (изображение с сайта http: //nnm. ru/blogs/rab 44/) Рибозимы — не совсем ферменты: по своей химической природе это не белки, а тоже молекулы РНК, только выполняющие специальные функции. Они служат катализаторами при расщеплении и сшивании других молекул РНК. У рибозимов есть интересная особенность: максимум их активности приходится на низкие температуры. То есть они фактически обеспечивают низкотемпературный катализ. http: //elementy. ru/news/164694 9

Рибосома: 1. химически – рибонуклеопротеид, 2. физически – компактная частица, диаметром около 30 нм, 3. функционально – молекулярная машина, протягивающая вдоль себя м. РНК, считывающая закодированную в м. РНК генетическую информацию и синтезирующая полинуклеотидную цепь. Схематическое изображение рибосомы. Рибосома „считывает“ код и присоединяет нужную аминокислоту к строящейся пептидной цепочке. На рисунке аминокислоты обозначены буквами: М — метионин, R — аргинин, S — серин. 10
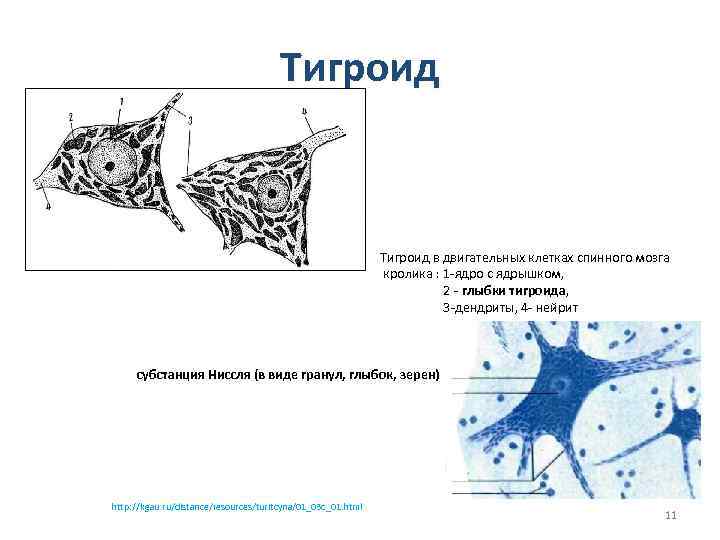
Тигроид • Тигроид в двигательных клетках спинного мозга кролика : 1 -ядро с ядрышком, 2 - глыбки тигроида, тигроида 3 -дендриты, 4 - нейрит субстанция Ниссля (в виде гранул, глыбок, зерен) http: //kgau. ru/distance/resources/turitcyna/01_03 c_01. html 11
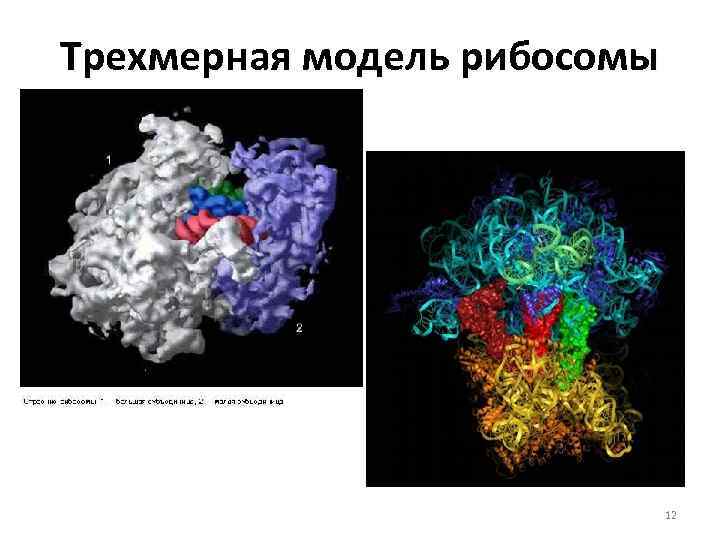
Трехмерная модель рибосомы 12

Генетическая программа должна не только копироваться, но и выполняться. В ходе ее работы создаются белки — главные молекулярные машины и строительные блоки живой клетки. Процесс происходит в два этапа. Вначале информация с ДНК транскрибируется — переписывается на другой, очень похожий носитель — молекулу РНК. От ДНК она отличается строением одного зубчика из четырех, а также основой, на которой эти зубчики сидят — она у РНК менее прочная. Причина понятна — если ДНК нужна для продолжительного хранения информации, то РНК — временный носитель, расходный материал, одноразовые дискеты или флэшки. Такая молекула РНК, на которую записана копия гена, называется информационной, или матричной (м. РНК). Эта длинная цепочка — одна половинка «застежки-молнии» — может содержать до сотни тысяч зубчиков. Когда переписывание информации завершено, м. РНК выходит из клеточного ядра и встречается с рибосомой — образуется молекулярный конвейер по производству белка. Каждые три зубчика РНК кодируют один строительный блок белка — аминокислоту. Всего же в белках встречаются 20 видов таких строительных блоков, и они выстраиваются в цепочку строго в порядке, запрограммированном в РНК. Этот процесс называется трансляцией — в компьютерном мире этим термином обозначают перевод текста программы в исполняемый машинный код. Сходя с рибосомы, цепочка аминокислот сразу сворачивается и образует устойчивую трехмерную структуру. Именно в таком виде белки выполняют свои функции в клетке. Рибосомы могут неоднократно транслировать матричную РНК, раз за разом производя новые молекулы белка. Но м. РНК неустойчива и через несколько часов разрушается. Поэтому считалось, что синтез каждого белка зависит главным образом от синтеза соответствующей м. РНК в ядре клетки. Покинув ядро клетки, РНК несет генетическую депешу к огромному молекулярному комплексу — рибосоме. Здесь происходит трансляция — перевод генетического кода в структуру белковых молекул. Рибосома, двигаясь вдоль цепочки РНК (синяя), считывает код и добавляет к растущей молекуле белка (желтая) соответствующие аминокислоты. Фото: SPL/EAST NEWS 13 http: //www. vokrugsveta. ru/vs/article/6503/

Строение рибосомы Рибосома Прокариотическая рибосома Эукариотическая рибосома 70 S 80 S Коэффициент седиментации рибосомы Большая Малая субчастица Коэффициент седиментации рибосомы Количество белков 50 S 34 молекулы 30 S 21 молекула белков Большая субчастица Малая субчастица 60 S разных 40 S не менее 50 разных белков не менее 33 разных белков Покинув ядро клетки, РНК несет генетическую депешу к огромному молекулярному комплексу - рибосоме. Здесь происходит трансляция - перевод генетического кода в структуру белковых молекул. Рибосома, двигаясь вдоль цепочки РНК (синяя), считывает код и добавляет к растущей молекуле белка (желтая) соответствующие аминокислоты. Фото: SPL/EAST NEWS http: //www. vokrugsveta. ru/vs/article/6503/ 14
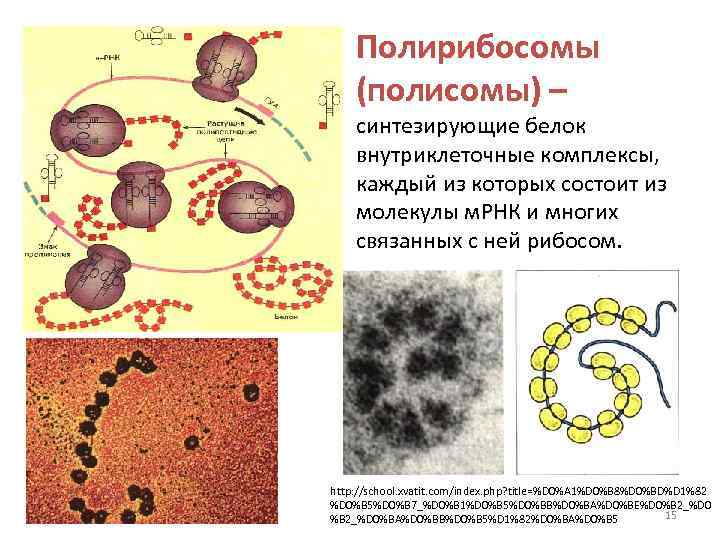
Полирибосомы (полисомы) – синтезирующие белок внутриклеточные комплексы, каждый из которых состоит из молекулы м. РНК и многих связанных с ней рибосом. http: //school. xvatit. com/index. php? title=%D 0%A 1%D 0%B 8%D 0%BD%D 1%82 %D 0%B 5%D 0%B 7_%D 0%B 1%D 0%B 5%D 0%BB%D 0%BA%D 0%BE%D 0%B 2_%D 0 15 %B 2_%D 0%BA%D 0%BB%D 0%B 5%D 1%82%D 0%BA%D 0%B 5

б). эпицикл трансляции: инициация, элонгация, терминация

Синтез белков молекулой РНК http: //nnm. ru/blogs/rab 44/ 17
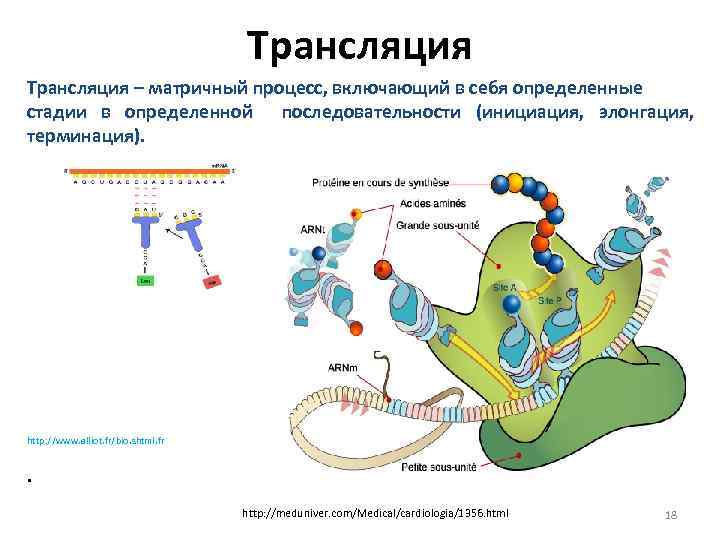
Трансляция – матричный процесс, включающий в себя определенные стадии в определенной последовательности (инициация, элонгация, терминация). http: //www. alliot. fr/bio. shtml. fr • http: //meduniver. com/Medical/cardiologia/1356. html 18

Инициация трансляции • Это серия молекулярных событий, происходящих с рибосомой, которая приводит к взаимодействию рибосомы с началом кодирующей нуклеотидной последовательности м. РНК и последующему считыванию (трансляции) этой последовательности. • Начинается с распадения рибосомы на субчастицы (диссоциации рибосомы). • Малая субчастица: • 1. связывает специальные белки-факторы инициации; • 2. распознает специальный инициаторный кодон и. РНК; • 3. обеспечивает взаимодействие инициаторного кодона и. РНК с антикодоном специальной инициаторной метионил-т. РНК; • 4. задает рамку считывания. • После этого большая субчастица связывается с малой, что завершает инициацию.

У эукариот инициирующий (стартовый) кодон – кодон аминокислоты метионина – АУГ. У прокариот (а также в митохондриях) к метионину присоединяется формильная группа с образованием формилметионина. 20
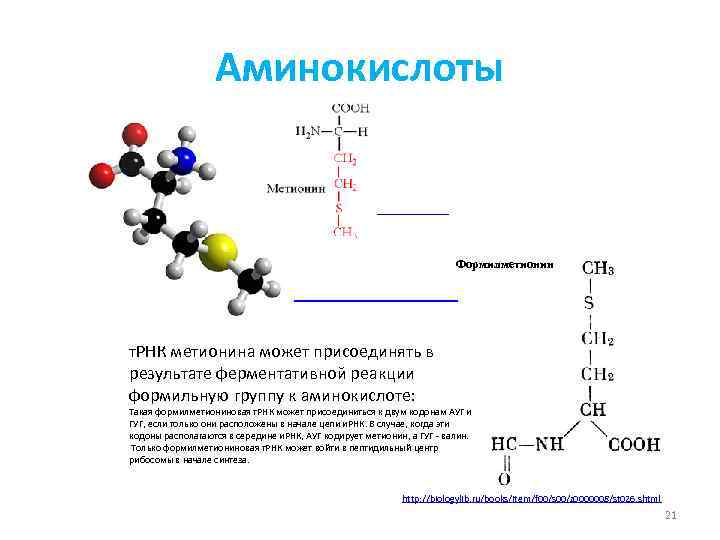
Аминокислоты » Формилметионин » т. РНК метионина может присоединять в результате ферментативной реакции формильную группу к аминокислоте: Такая формилметиониновая т. РНК может присоединиться к двум кодонам АУГ и ГУГ, если только они расположены в начале цепи и. РНК. В случае, когда эти кодоны располагаются в середине и. РНК, АУГ кодирует метионин, а ГУГ - валин. Только формилметиониновая т. РНК может войти в пептидильный центр рибосомы в начале синтеза. http: //biologylib. ru/books/item/f 00/s 00/z 0000008/st 026. shtml 21
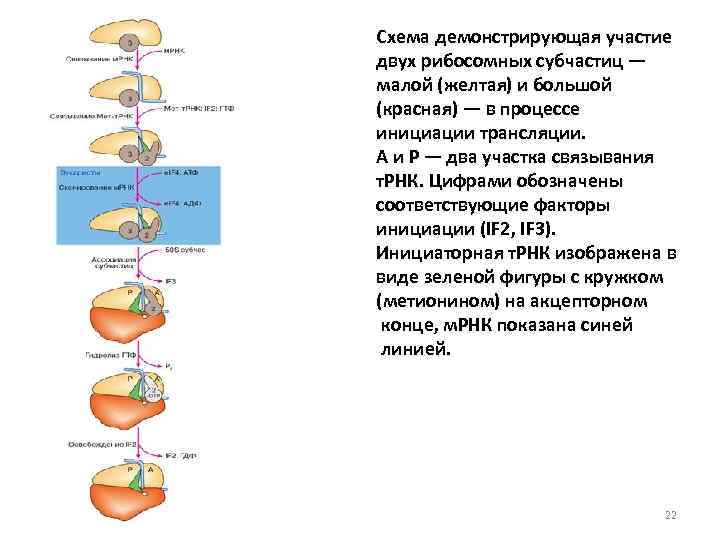
Схема демонстрирующая участие двух рибосомных субчастиц — малой (желтая) и большой (красная) — в процессе инициации трансляции. A и P — два участка связывания т. РНК. Цифрами обозначены соответствующие факторы инициации (IF 2, IF 3). Инициаторная т. РНК изображена в виде зеленой фигуры с кружком (метионином) на акцепторном конце, м. РНК показана синей линией. 22
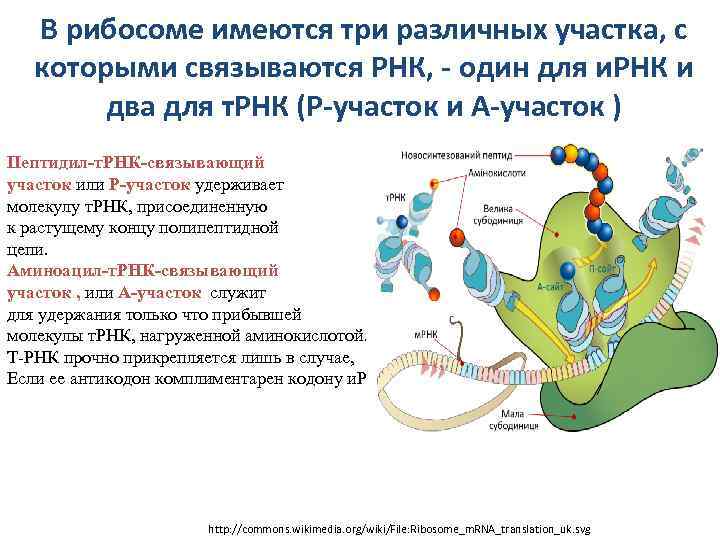
В рибосоме имеются три различных участка, с которыми связываются РНК, - один для и. РНК и два для т. РНК (Р-участок и А-участок ) Пептидил-т. РНК-связывающий участок или Р-участок удерживает молекулу т. РНК, присоединенную к растущему концу полипептидной цепи. Аминоацил-т. РНК-связывающий участок , или А-участок служит для удержания только что прибывшей молекулы т. РНК, нагруженной аминокислотой. Т-РНК прочно прикрепляется лишь в случае, Если ее антикодон комплиментарен кодону и. РНК. http: //commons. wikimedia. org/wiki/File: Ribosome_m. RNA_translation_uk. svg

Элонгация полипептидной цепи на рибосомах слагается из трех отдельных этапов • На первом этапе молекула аминоацил-т. РНК связывается со свободным участком рибосомы, примыкающим к занятому Р-участку. Связывание осуществляется путем спаривания трех нуклеотидов антикодона с тремя нуклеотидами и. РНК, находящимися в Аучастке. • На втором этапе карбоксильный конец полипептидной цепи отделяется в Р-участке от молекулы т. РНК и образует пептидную связь с аминокислотой, присоединенной к молекуле т. РНК в А-участке. Соединение аминокислот в цепи возможно потому, что у каждой из них имеются две разные химические группы: обладающая основными свойствами аминогруппа, NH 2, и кислотная карбоксильная группа, СООН. Карбоксильная группа одной аминокислоты может образовать амидную (пептидную) связь с аминогруппой другой аминокислоты. • На третьем этапе новая пептидил-т. РНК переносится в Р-участок рибосомы, в то время как рибосома продвигается вдоль молекулы и. РНК ровно на три нуклеотида. • Таким образом, в результате элементарного элонгационного цикла полипептид удлиняется на одну аминокислоту.
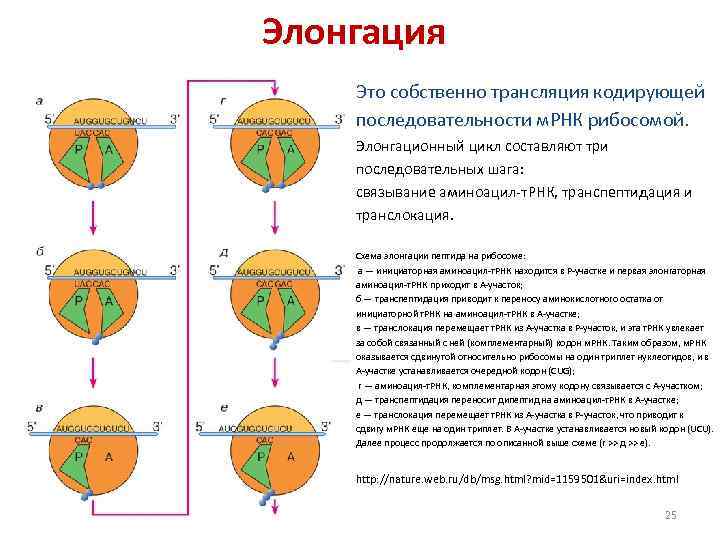
Элонгация Это собственно трансляция кодирующей последовательности м. РНК рибосомой. Элонгационный цикл составляют три последовательных шага: связывание аминоацил-т. РНК, транспептидация и транслокация. Схема элонгации пептида на рибосоме: а — инициаторная аминоацил-т. РНК находится в P-участке и первая элонгаторная аминоацил-т. РНК приходит в A-участок; б — транспептидация приводит к переносу аминокислотного остатка от инициаторной т. РНК на аминоацил-т. РНК в A-участке; в — транслокация перемещает т. РНК из А-участка в Р-участок, и эта т. РНК увлекает за собой связанный с ней (комплементарный) кодон м. РНК. Таким образом, м. РНК оказывается сдвинутой относительно рибосомы на один триплет нуклеотидов, и в А-участке устанавливается очередной кодон (CUG); г — аминоацил-т. РНК, комплементарная этому кодону связывается с А-участком; д — транспептидация переносит дипептид на аминоацил-т. РНК в А-участке; е — транслокация перемещает т. РНК из А-участка в Р-участок, что приводит к сдвигу м. РНК еще на один триплет. В А-участке устанавливается новый кодон (UCU). Далее процесс продолжается по описанной выше схеме (г >> д >> е). http: //nature. web. ru/db/msg. html? mid=1159501&uri=index. html 25

Стадии трансляции Из 64 возможных кодонов м. РНК три: УАА, УАГ, УГА, являются терминирующими или стоп-кодонами: они останавливают трансляцию. Терминация — узнавание терминирующего кодона (стоп-кодона) и отделение продукта. 26
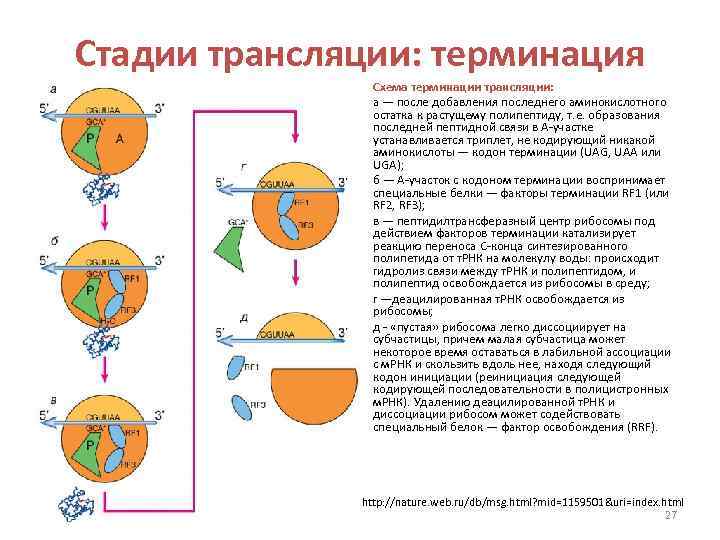
Стадии трансляции: терминация Схема терминации трансляции: а — после добавления последнего аминокислотного остатка к растущему полипептиду, т. е. образования последней пептидной связи в А-участке устанавливается триплет, не кодирующий никакой аминокислоты — кодон терминации (UAG, UAA или UGA); б — А-участок с кодоном терминации воспринимает специальные белки — факторы терминации RF 1 (или RF 2, RF 3); в — пептидилтрансферазный центр рибосомы под действием факторов терминации катализирует реакцию переноса С-конца синтезированного полипетида от т. РНК на молекулу воды: происходит гидролиз связи между т. РНК и полипептидом, и полипептид освобождается из рибосомы в среду; г —деацилированная т. РНК освобождается из рибосомы; д - «пустая» рибосома легко диссоциирует на субчастицы, причем малая субчастица может некоторое время оставаться в лабильной ассоциации с м. РНК и скользить вдоль нее, находя следующий кодон инициации (реинициация следующей кодирующей последовательности в полицистронных м. РНК). Удалению деацилированной т. РНК и диссоциации рибосом может содействовать специальный белок — фактор освобождения (RRF). http: //nature. web. ru/db/msg. html? mid=1159501&uri=index. html 27

в). особенности трансляции у про- и эукариот.
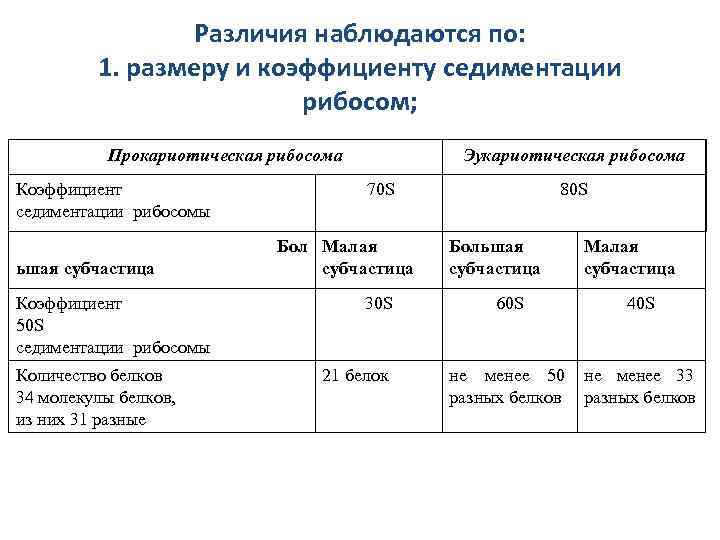
Различия наблюдаются по: 1. размеру и коэффициенту седиментации рибосом; Прокариотическая рибосома Коэффициент седиментации рибосомы ьшая субчастица Коэффициент 50 S седиментации рибосомы Количество белков 34 молекулы белков, из них 31 разные Эукариотическая рибосома 70 S Бол Малая субчастица 30 S 21 белок 80 S Большая субчастица Малая субчастица 60 S 40 S не менее 50 разных белков не менее 33 разных белков
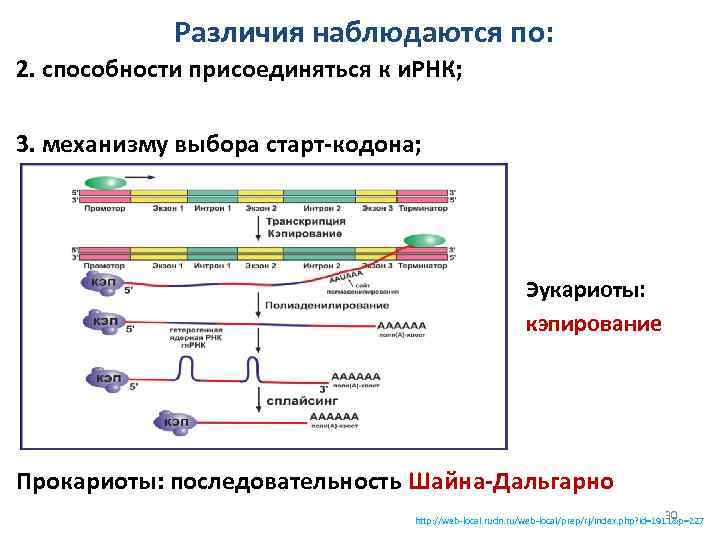
Различия наблюдаются по: 2. способности присоединяться к и. РНК; 3. механизму выбора старт-кодона; Эукариоты: кэпирование Прокариоты: последовательность Шайна-Дальгарно 30 http: //web-local. rudn. ru/web-local/prep/rj/index. php? id=1911&p=227
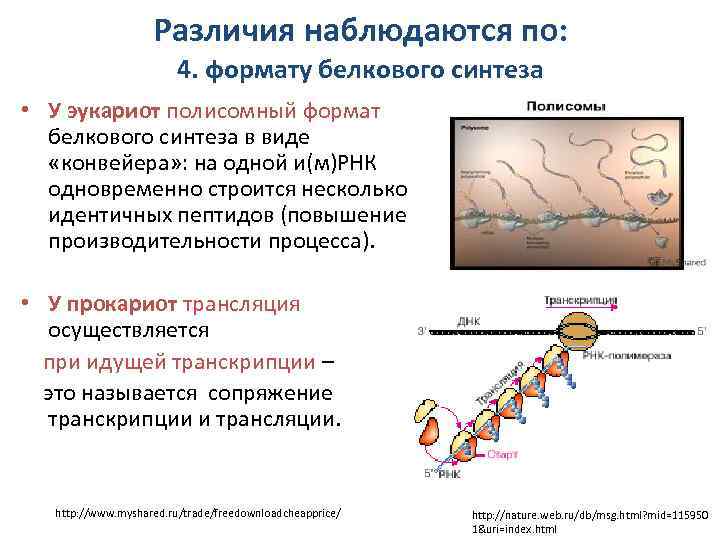
Различия наблюдаются по: 4. формату белкового синтеза • У эукариот полисомный формат белкового синтеза в виде «конвейера» : на одной и(м)РНК одновременно строится несколько идентичных пептидов (повышение производительности процесса). • У прокариот трансляция осуществляется при идущей транскрипции – это называется сопряжение транскрипции и трансляции. http: //www. myshared. ru/trade/freedownloadcheapprice/ http: //nature. web. ru/db/msg. html? mid=115950 1&uri=index. html

Основные стратегии регуляции биосинтеза белка 1. Прокариоты. Немедленное использование производимой генами и. РНК и ее быстрая деградация (метаболически нестабильная и. РНК). 2. Эукариоты. Характерна стратегия активациинеактивации. Наработка метаболически стабильных и. РНК впрок. 32

2. Посттрансляционные изменения белков: фолдинг, транспорт и деградация белков

Посттрансляционные изменения белков Посттрансляционной модификацией белков называют изменение первичной структуры полипептидной цепи после завершения ее синтеза рибосомами; то есть, это химические превращения, изменяющие ковалентную структуру полипептидной цепи. Особенности реакций пострансляционных модификаций: • Катализируются специфическими ферментами; • Могут происходить как во время синтеза полипептидной цепи, так и после окончания синтеза; • Нематричные процессы, отсюда – образование множественных форм белков; • Некоторые реакции характерны для очень многих белков, а некоторые – для ограниченной группы (или отдельных) белков; • Более 5% генов в геноме человека кодируют ферменты, участвующие в пострансляционной модификации белков. 34
Фолдинг белков Что такое фолдинг? В клетках за производство белков отвечают рибосомы, где белки собираются из отдельных аминокислот в соответствии с последовательностью, считываемой из ДНК. Результатом работы такого биологического конвейера являются длинные молекулы — «заготовки» для белков. И хотя геном сегодня расшифрован, то есть, известна первичная структура некоторого количества белков, в том числе — человека, даже в этом случае невозможно судить о его функциях. Последние проявляются только после того, как длинная цепочка аминокислот свернется и примет характерную для его функционирования пространственную структуру (нативное состояние). Этот процесс и называется фолдингом. Сворачивание белковой молекулы в нативную третичную структуру (фолдинг) является необходимым условием функционирования белка. Таким образом, в организме образуются готовые к работе гемоглобин, инсулин и др. Процесс сворачивания может проходить в несколько стадий длительностью от нескольких секунд до нескольких минут. В последней фазе протеин из «предварительного состояния» мгновенно принимает окончательную форму. Именно эта фаза продолжительностью несколько десятков микросекунд представляет собой сложнейшую проблему для моделирования. 35
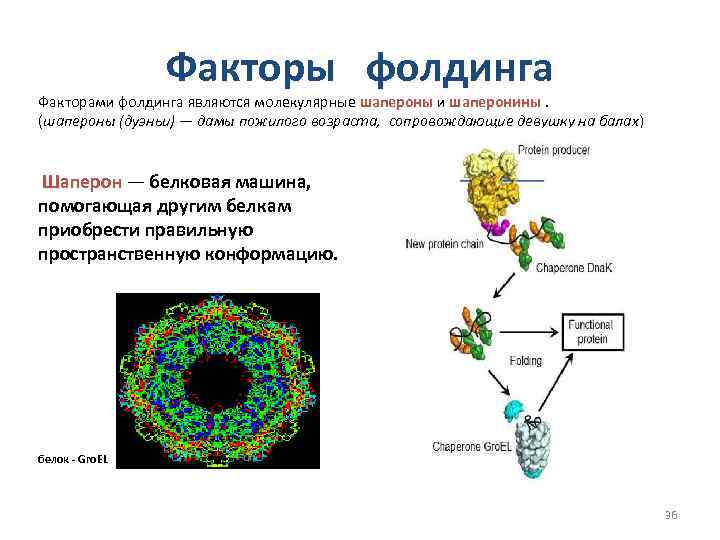
Факторы фолдинга Факторами фолдинга являются молекулярные шапероны и шаперонины. (шапероны (дуэньи) — дамы пожилого возраста, сопровождающие девушку на балах) Шаперон — белковая машина, помогающая другим белкам приобрести правильную пространственную конформацию. белок - Gro. EL 36
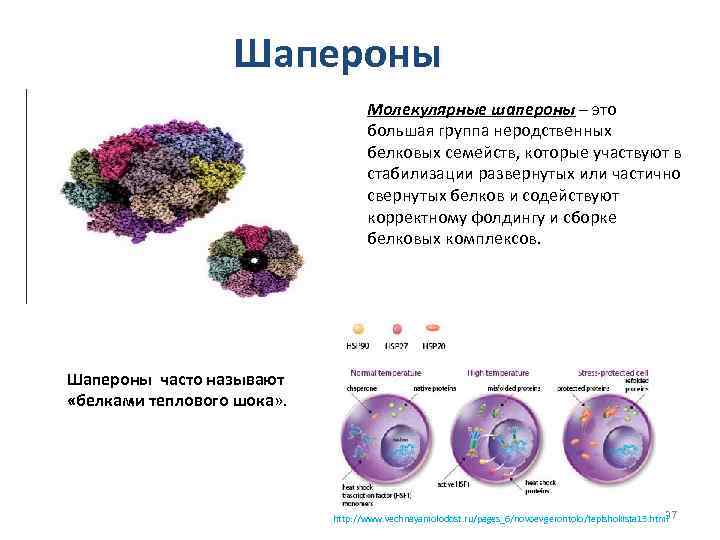
Шапероны Молекулярные шапероны – это большая группа неродственных белковых семейств, которые участвуют в стабилизации развернутых или частично свернутых белков и содействуют корректному фолдингу и сборке белковых комплексов. Шапероны часто называют «белками теплового шока» . 37 http: //www. vechnayamolodost. ru/pages_6/novoevgerontolo/teplshokista 13. html
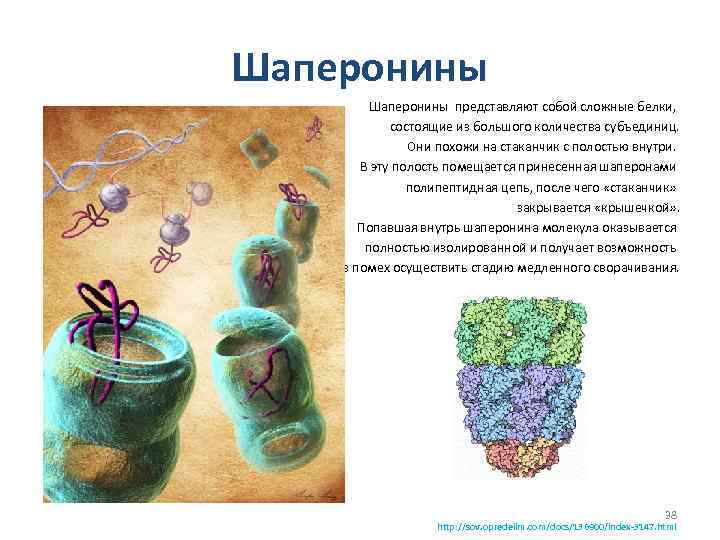
Шаперонины представляют собой сложные белки, состоящие из большого количества субъединиц. Они похожи на стаканчик с полостью внутри. В эту полость помещается принесенная шаперонами полипептидная цепь, после чего «стаканчик» закрывается «крышечкой» . Попавшая внутрь шаперонина молекула оказывается полностью изолированной и получает возможность без помех осуществить стадию медленного сворачивания. 38 http: //sov. opredelim. com/docs/136900/index-3147. html

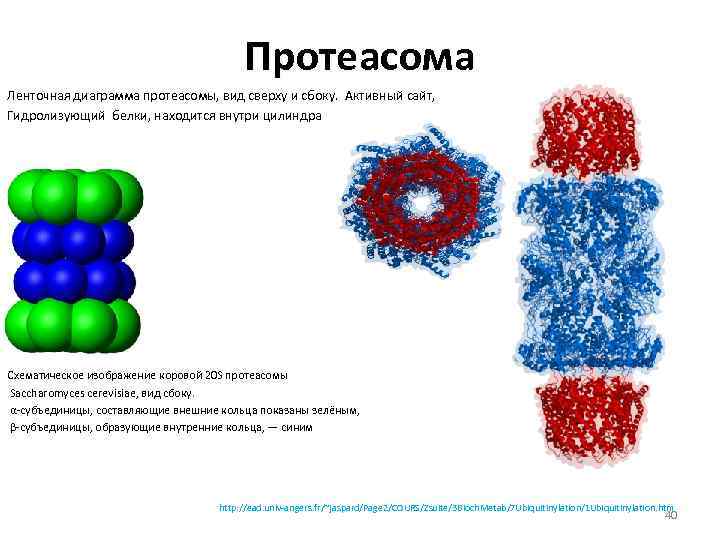
Протеасома Ленточная диаграмма протеасомы, вид сверху и сбоку. Активный сайт, Гидролизующий белки, находится внутри цилиндра Схематическое изображение коровой 20 S протеасомы Saccharomyces cerevisiae, вид сбоку. α-субъединицы, составляющие внешние кольца показаны зелёным, β-субъединицы, образующие внутренние кольца, — синим http: //ead. univ-angers. fr/~jaspard/Page 2/COURS/Zsuite/3 Bioch. Metab/7 Ubiquitinylation/1 Ubiquitinylation. htm 40
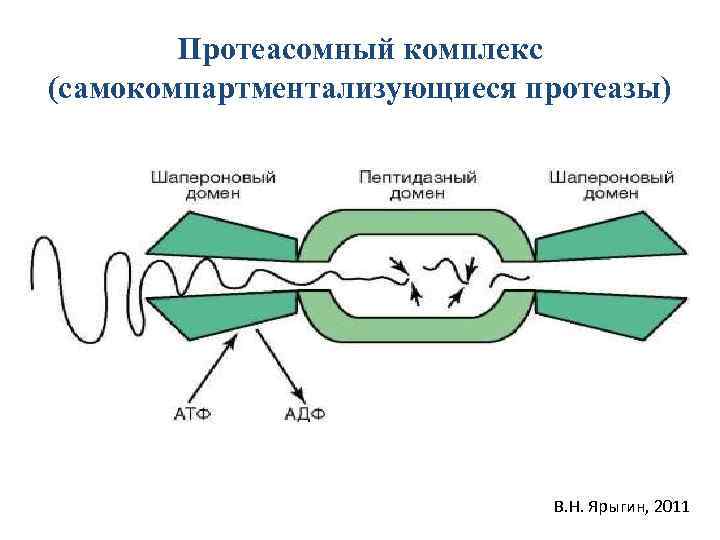
Протеасомный комплекс (самокомпартментализующиеся протеазы) В. Н. Ярыгин, 2011
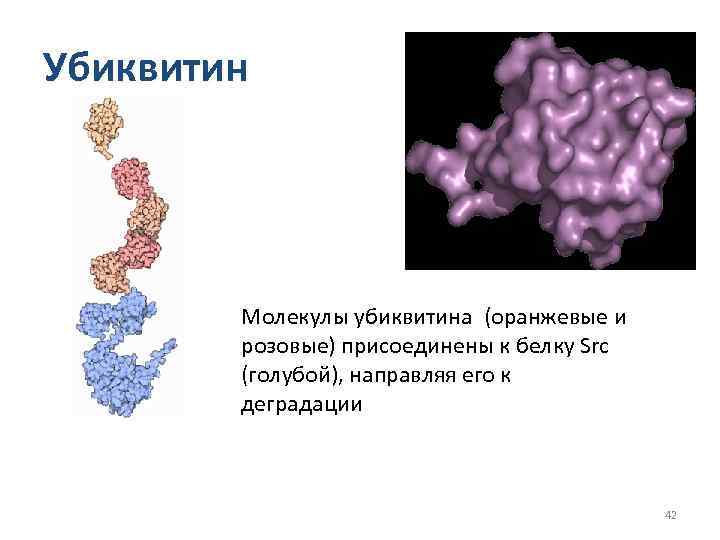
Убиквитин Молекулы убиквитина (оранжевые и розовые) присоединены к белку Src (голубой), направляя его к деградации 42
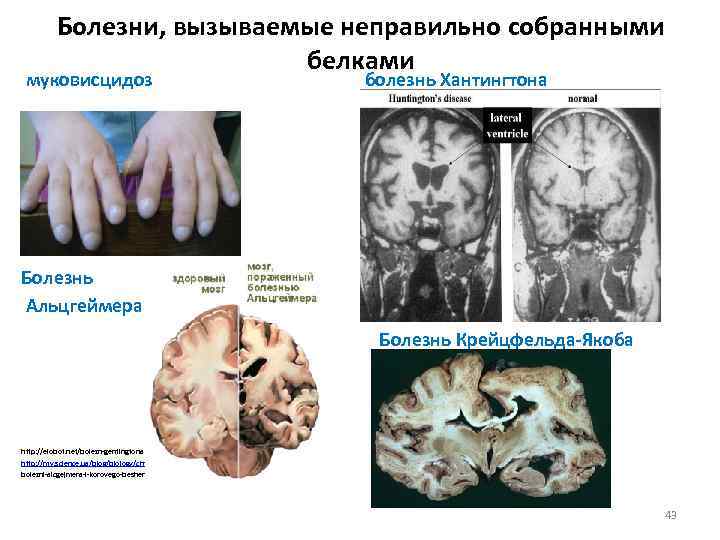
Болезни, вызываемые неправильно собранными белками муковисцидоз болезнь Хантингтона Болезнь Альцгеймера Болезнь Крейцфельда-Якоба http: //elobot. net/bolezn-gentingtona http: //my. science. ua/blog/biology/chto-obshego-u-pamjatibolezni-alcgejmera-i-korovego-beshenstva. html 43
Биология. Лекция 5. Трансляция.ppt