Презентация_геохимия 5.ppt
- Количество слайдов: 32

Общие закономерности физико-химической миграции

Химические элементы мигрируют в земной коре в виде: • Ионов • Недиссоциированных молекул • Коллоидных мицелл • Свободных радикалов

Миграция в ионной форме характеризуется: • • • Потенциалом ионизации Потенциалом возбуждения Ионным радиусом Электроотрицательностью Энергетическим коэффициентом

Изоморфизм возможен при: • Радиусы ионов и атомов различаются не более 15% • Химическая индифферентность • Одинаковые поляризационные свойства атомов • Ионы одного знака • Сходная природа межатомной связи

Химическая индифферентность Аu (0, 144 нм) и Аl (0, 143 нм) образуют Аu Аl 2 и другие соединения. Ga(0, 062 нм) и As(0, 058 нм) образуют Ga As

Одинаковые поляризационные свойства атомов Изоморфизма нет между: - Na+1 (0, 97 А) Cu+1 (0, 96 А) - Si и P

Валентная компенсация Сa 5(PO 4)3(F, Cl, OH) – апатит Сa+2 изоморфно замещается ТR+3 Одновременно F-1 изоморфно замещается O-2 Сa 5(PO 4)3 F ТR 5(PO 4)3 O

Сходная природа межатомной связи Na. Cl – галит и Pb. S – галенит У обоих кубические кристаллические решетки Ионные радиусы близки у Na (0, 98 нм)и Pb(1, 3 нм) Cl (1, 81 нм) S (1, 74 нм ), но Связь Na. Cl ионная, а Pb. S ковалентная
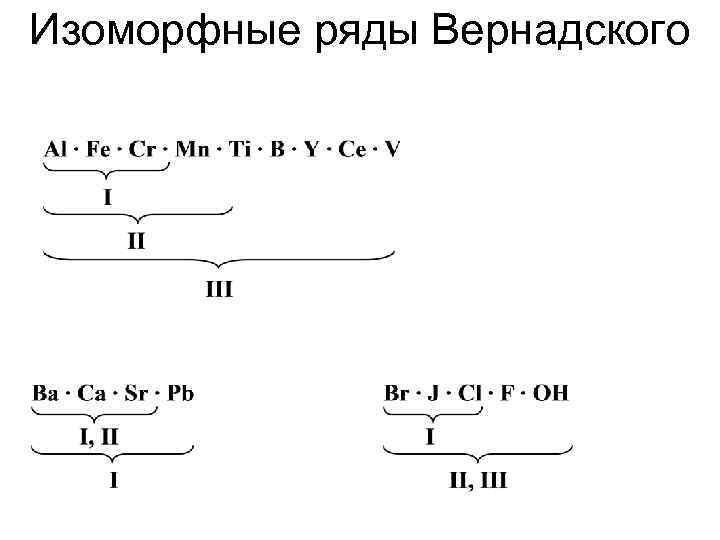
Изоморфные ряды Вернадского

Важнейшие окислители: О 2, SO 42 -, CO 2, NO 3 - , NO 2 - , Fe 3+, Mn+4 Mn+3 , Ti 4+ , Cu 2+ , Cr. O 42 - , Cr 3+

Важнейшие восстановители • Гидратированный электрон – образующийся при радиолизе воды • Атомарный и молекулярный водород • Сероводород • СН 4, СО, органические соединения, Fe 2+, Mn+2

Ультраокислительная обстановка Cr 6+, V 5+, Mn+4 , Мо+6, Fe+3 N+5, U+6 (степи, пустыни, содовые озера ) Окислительная обстановка Fe+3 , Mn+4 , Cu+2 , U+6 (океаны, реки, озера)

Слабоокислительная обстановка Fe+3 , Mn+2 , Cu+2 , U+6 (трещинные воды скальных пород) Слабовосстановительная обстановка Fe+2 , Fe+3 , Mn+2 (магма) Восстановительная обстановка Fe+2 (сероводородные гидротермы и илы морей, соляных озер, болта тайги, тундры, влажных тропиков ).

Восстановительная обстановка Fe+2 (сероводородные гидротермы и илы морей, соляных озер, болта тайги, тундры, влажных тропиков ) Ультровосстановительная обстановка Fe 0 (земное ядро, нижняя мантия, железные и каменные метиориты)

Механизмы массопереноса: • Диффузия • Конвекция

Термодинамика физико-химической миграции

Энергия Гиббса Ca 2+ + 2 F- ----- Ca. F 2 раствор твердый G°(Ca 2+ ) = - 132, 18 к. Дж/моль G°(F- ) = - 66, 08, к. Дж/моль G°(Ca. F 2) = - 277, 7, к. Дж/моль

G = n G°(Ca. F 2) – [n G°(Ca 2+ ) + +n G°(F- ) ] G = - 277, 7 – (- 132, 18 ) + 2(- 66, 08) = = - 13, 36 к. Дж/моль, т. е. При активностях действующих ионов равных 1 и Т=25°С реакция термодинамически возможна
![Примем (влажный климат, слабоминерализованные воды) [Ca 2+ ] = 10 -3 моль/л (0, 04 Примем (влажный климат, слабоминерализованные воды) [Ca 2+ ] = 10 -3 моль/л (0, 04](https://present5.com/presentation/3/-42636264_222539048.pdf-img/-42636264_222539048.pdf-19.jpg)
Примем (влажный климат, слабоминерализованные воды) [Ca 2+ ] = 10 -3 моль/л (0, 04 г/л) [ F-] = 10 -5 моль/л ( 10 -5 г/л ) G = 1. 364 lg [Ca. F 2 ] / [Ca 2+ ] [ F-] 2 + G° = 1. 364 lg 102 * 1010 - 13. 36 = +4. 37 к. Дж/моль, т. е. в данных условиях Ca. F 2 не образуется, а наоборот растворяется.

Произведение растворимости Ca 2+ + 2 F- ----- Ca. F 2 ПР = [Ca 2+ ] [ F-] 2 = 10 -9, 8 [Ca 2+ ] = 10 -2 моль/л, тогда [ F-] = 10 -3, 9 моль/л

Правило фаз F = К – Р + 2 где F — число степеней свободы, т. е. число возможных изменений в системе; К — число компонентов; Р — число фаз.

F=0 система называется инвариантной; такая система не допускает изменений ни температуры, ни давления без нарушения равновесия.

F=1 система моновариантная может измениться только либо температура либо давление (без нарушения равновесия), другая при этом должна оставаться неизменной.

F=2 система бивариантная: равновесие сохраняется при одновременном изменении и температуры и давления.

Вода - парообразная Р=1 (только пар), К=1(вода) и F= 1 -1+2 = 2, т. е. система - бивариантна в которой можно (до известного предела) менять и t и р: пар будет оставаться паром, только будет меняться его объем.

вода жидкая – вода пар Р = 2 (жидкость и пар) К=1(вода) F = 1 -2 + 2=1 моновариантная система Равновесие сохраняется при изменении двух переменных (t, p) т. е. каждой определенной температуре будет отвечать определенное давление.

Модификации отдельных минералов устойчивы только в определенных условиях температуры и давления. -кварц, устойчивый до 573° С, при этой температуре переходит в кварц

Система -кварц - - кварц - пар К=1 (Si. O 2) P = 3 (две модификации + пар) F=K-Р+2=1 -3+2=0 Система инвариантная, т. е. при изменении одной из переменных (t или р) или обеих вместе одна из модификаций будет переходить в другую

F = K - Р + 2, Р =K + 2 - F число фаз возрастает с увеличением числа компонентов

Минералогическое правило фаз максимальное число n твердых минералов, которые одновременно совместно устойчиво существуют при произвольных давлении и температуре, равно числу n компонентов, составляющих эти минералы.

Система с n=1 (Si. O 2 ) При любых t и р в равновесии со своим насыщенным раствором будет находиться только одна модификация (при атмосферном давлении: до 573° - -кварц , 573 - 870° - -кварц 870 -1470° - тридимит, 1470 - 1710°С - кристобалит, выше - расплав).

Презентация_геохимия 5.ppt