Общая и неорганическая химия. Лекция 18 Галогены (окончание).


Общая и неорганическая химия. Лекция 18 Галогены (окончание). Хлор, бром, иод

Галогены в природе 11. Хлор (0, 19%) рассеянные элементы 43. Бром Редкие 70. Иод 94. Астат Карналлит Сильвинит Галит (каменная соль) Na. Cl Сильвинит Na. Cl·KCl) Карналлит KCl·Mg. Cl 2· 6 H 2 O Галит

Редкие минералы Бромаргирит Ag. Br Иодаргирит Ag. I Лаутарит Ca(IO 3)2 Лаутарит Диэтзеит 7 Ca(IO 3)2· 8 Ca. Cr. O 4 Бромаргирит Иодаргирит
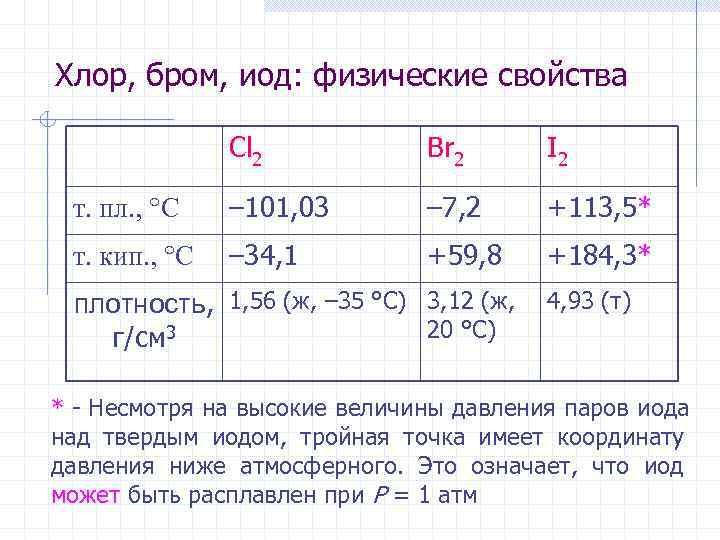
Хлор, бром, иод: физические свойства Cl 2 Br 2 I 2 т. пл. , °C – 101, 03 – 7, 2 +113, 5* т. кип. , °C – 34, 1 +59, 8 +184, 3* плотность, 1, 56 (ж, – 35 °C) 3, 12 (ж, 4, 93 (т) г/см 3 20 °C) * - Несмотря на высокие величины давления паров иода над твердым иодом, тройная точка имеет координату давления ниже атмосферного. Это означает, что иод может быть расплавлен при P = 1 атм

Окисл. св-ва убывают Г 2: Cl Br I (At) Неметаллич. св-ва убывают Примеры: 1. Cl 2(Br 2) + Cu Cu. Cl 2 (Cu. Br 2); Sтв + Cl 2 г SCl 4 г; SCl 2 г, S 2 Cl 2 г ½ I 2 + Cu Cu. I; Sтв + Br 2 г SBr 2 г; S 2 Br 2 г; S + I 2 T-x диаграмма S-Cl (см. рис. ): три соединения: SCl 4; SCl 2, S 2 Cl 2 T-x диаграмма системы S-Br: Фаза S 2 Br 2 – конгр. пл. (-40 С) и инконгр. пл. SBr 2; T-x диаграмма S-I – нет соединений, диаграмма эвтектического типа

Окисл. св-ва убывают Г 2: Cl Br I (At) Неметаллич. св-ва убывают Примеры (продолжение): 3. H 2(г) + Cl 2(г) 2 HCl(г); G = – 95 к. Дж/моль H 2(г) + Br 2(г) 2 HBr(г); G = – 54 к. Дж/моль H 2(г) + I 2(т) 2 HI(г); G = – 1 к. Дж/моль 4. 2 KBr + Cl 2 2 KCl + Br 2 2 KI + Br 2 2 KBr + I 2 3 I 2 + 10 HNO 3 конц. 6 HIO 3 + 10 NO + 2 H 2 O (HI+5 O 3)

3. Взаимодействие с водой Г 2 + n H 2 O Г 2 · n H 2 O (гидратация) Г 2 · n H 2 O HГ + HГO + (n – 1)H 2 O (дисмутация) Cl 2 Br 2 I 2 Растворимость в 9· 10– 2 0, 5 1· 10– 3 воде, моль/л Степень превр. в 0, 5 0, 05 0, 0017 Hal- и OHal- (нас. ) Cl 2 + 2 H 2 O HCl + HCl. O (ОВР) Cl 2 + 2 e = 2 Cl 2 + 2 H 2 O – 2 e = 2 H+ + 2 HCl. O

Растворимость галогенов повышается: В р-ре KI: KI + I 2 (т) = K[I(I)2] I– + I 2 (т) = [I(I)2]– дииодоиодат(I)-ион [ I–I ····· I+I ····· I–I ]

В растворах щелочей Br 2 + 2 KOH = KBr + KBr. O + H 2 O (на холоду) Br 2 + 2 e = 2 Br 2 + 4 OH– – 2 e = 2 Br. O– + 2 H 2 O 3 Br 2 + 6 KOH = 5 KBr + KBr. O 3 + 3 H 2 O (при нагревании) Br 2 + 2 e = 2 Br 2 + 12 OH– – 10 e = 2 Br. O 3– + 6 H 2 O

В органических растворителях Органические растворители, не смешивающиеся с водой, используют для извлечения (экстракции) брома и иода. Экстракция иода Экстракция брома
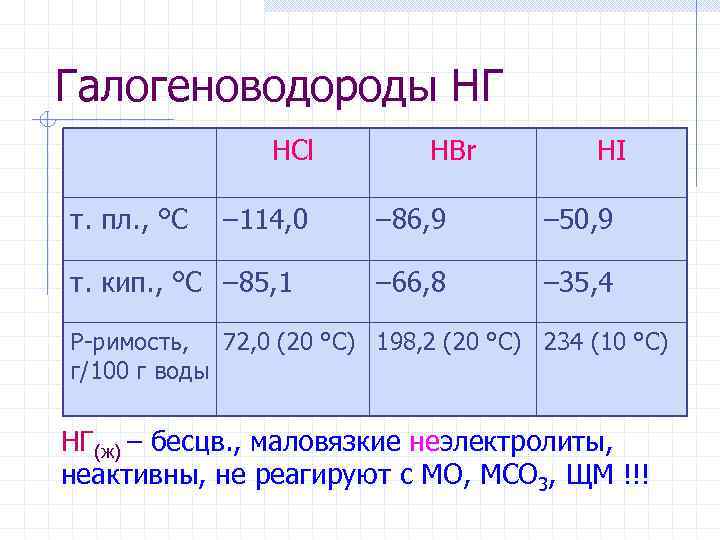
Галогеноводороды НГ HCl HBr HI т. пл. , °C – 114, 0 – 86, 9 – 50, 9 т. кип. , °C – 85, 1 – 66, 8 – 35, 4 Р-римость, 72, 0 (20 °C) 198, 2 (20 °C) 234 (10 °C) г/100 г воды НГ(ж) – бесцв. , маловязкие неэлектролиты, неактивны, не реагируют c МО, МCO 3, ЩМ !!!
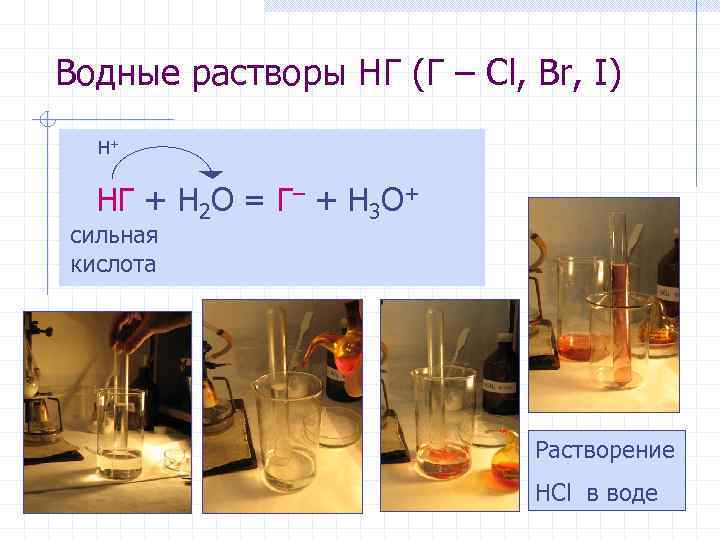
Водные растворы HГ (Г – Cl, Br, I) H+ НГ + H 2 O = Г– + H 3 O+ сильная кислота Растворение HCl в воде

восстановит. св-ва растут HCl HBr HI KCl + H 2 SO 4 конц = HCl + KHSO 4 HCl + H 2 SO 4 конц KBr + H 2 SO 4 конц = HBr + KHSO 4 2 HBr + H 2 SO 4 конц Br 2 + SO 2 + 2 H 2 O 8 KI + 9 H 2 SO 4 конц = 4 I 2 + H 2 S + 4 H 2 O + 8 KHSO 4 2 KI + 3 H 2 SO 4 конц = I 2 + SO 2 + 2 H 2 O + 2 KHSO 4 8 HI + H 2 SO 4 конц = 4 I 2 + H 2 S + 4 H 2 O и параллельно 2 HI + H 2 SO 4 конц = I 2 + SO 2 + 2 H 2 O

Получение НCl В промышл. – прямым синтезом: • H 2 + Cl 2 = 2 HCl В лаборатории: • Na. Cl + H 2 SO 4 = HCl + Na. HSO 4 (без нагревания) или • 2 Na. Cl + H 2 SO 4 = 2 HCl + Na 2 SO 4 (при нагревании)

Получение НBr и HI В лаборатории и в промышл. усл. – синтез галогенидов фосфора с последующим их необр. гидролизом: • 2 P + 3 Г 2 = 2 PГ 3 • PГ 3 + 3 H 2 O = 3 HГ + H 2(PHO 3) Восст. в водн. среде сероводородом: • Г 2 + H 2 S = S + 2 HГ
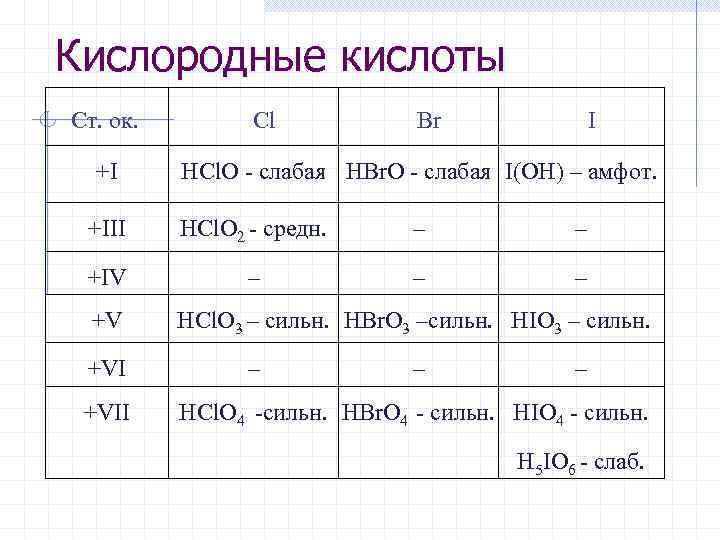
Кислородные кислоты Ст. ок. Cl Br I +I HCl. O - слабая HBr. O - слабая I(OH) – амфот. +III HCl. O 2 - средн. – +IV – – +V HCl. O 3 – сильн. HBr. O 3 –сильн. HIO 3 – сильн. +VI – – +VII HCl. O 4 -сильн. HBr. O 4 - сильн. HIO 4 - сильн. H 5 IO 6 - слаб.

Взаимодействие с водой В водном растворе HCl. O, HCl. O 2, HBr. O и H 5 IO 6 – слабые кислоты: • HCl. O + H 2 O Cl. O + H 3 O+; KК = 2, 82. 10 8 • HCl. O 2 + H 2 O Cl. O 2 + H 3 O+; KК = 1, 07. 10 2 • HBr. O + H 2 O Br. O + H 3 O+; KК = 2, 06. 10 9 • H 5 IO 6+ H 2 O H 4 IO 6 + H 3 O+; KК = 2, 82. 10 2; Остальные кислородсодержащие кислоты – сильные: • HCl. O 3 + H 2 O = Cl. O 3 + H 3 O+ • HCl. O 4 + H 2 O = Cl. O 4 + H 3 O+

Оксиды галогенов: все, кроме I 2 O 5 метастабильны Ст. ок. Cl Br I +I Cl 2 O Br 2 O – +III – Br 2 O 3 – +IV Cl. O 2 Br 2 O 4 I 2 O 4 +V – Br 2 O 5 I 2 O 5 +VI Cl 2 O 6 – I 2 O 6 +VII Cl 2 O 7 – I 2 O 7

Получение и реакции оксидов: Cl 2 + Ag 2 O Cl 2 O + 2 Ag. Cl (в неводном растворителе); 3 KCl. O 3 + 2 H 2 SO 4 Cl. O 2 + KCl. O 4 + KHSO 4; 2 KCl. O 3 + 3 H 2 C 2 O 4 Cl. O 2 + KHC 2 O 4 + CO 2 + H 2 O 4 HCl. O 4 + P 4 O 10 (HPO 3)4 + 2 Cl 2 O 7; H 2 SO 4 3 I 2 + 10 HNO 3 конц. 3 I 2 O 5 + 10 NO + 5 H 2 O

В щелочной среде – дисмутация: 3 Г 2 + 6 Na. OH = 5 Na. Г + Na. ГO 3 + 3 H 2 O Г 2 + 2 e – = 2 Г– (Г 2 – окислитель) Г 2 + 12 OH– – 10 e– = 2 ГO 3– + 6 H 2 O (Г 2 – восстановитель) = Br 2/ Br – – Br. O 3–/ Br 2 = 1, 09 – 0, 52 = 0, 57 В = I 2/ I– – IO 3–/ I 2 = 0, 54 – 0, 20 = 0, 34 В

В кислотной среде – конмутация: 5 Na. Г + Na. ГO 3 + 3 H 2 SO 4 = 3 Г 2 + 3 Na 2 SO 4+ + 3 H 2 O • 2 Г– – 2 e– = Г 2 (Г– – восстановитель) • 2 ГO 3– + 12 H+ + 10 e– = Г 2 + 6 H 2 O (ГO 3– – окислитель) = Br. O 3–/ Br 2 – Br 2/ Br– = 1, 51 – 1, 09 = 0, 42 В = IO 3–/ I 2 – I 2/ I– = 1, 19 – 0, 54 = 0, 65 В
VII_гр_лек_2.ppt
- Количество слайдов: 21

