Obmen_aminokislot.ppt
- Количество слайдов: 44

ОБМЕН И ФУНКЦИИ АМИНОКИСЛОТ

Значение аминокислот для организма в первую очередь определяется тем, что они используются для синтеза белков, метаболизм которых занимает особое место в процессах обмена веществ между организмом и внешней средой. Белки входят во все основные структурные компоненты клеток, тканей и органов, выполняют ферментативные функции, участвуют в переносе веществ через мембраны.

Аминокислоты выполняют в организме разнообразные функции. Структурную – большая часть аминокислот используется для построения белков (до 400 г/сут), количество которых в организме человека составляет примерно 12 -15 кг. Анаболическую – аминокислоты являются предшественниками многих биологически активных соединений, таких как гормоны, пуриновые и пиримидиновые нуклеотиды, гем, креатин, холин, нейромедиаторы. Энергетическую – аминокислоты могут служить источниками энергии, при длительном голодании или избыточном употреблении белков. Именно обмен аминокислот взаимосвязь многообразных превращений в живом организме. осуществляет химических

ИСТОЧНИКИ И ПУТИ ИСПОЛЬЗОВАНИЯ АМИНОКИСЛОТ В КЛЕТКАХ Фонд свободных аминокислот организма составляет примерно 30 -100 г, содержание их в крови в среднем – 35 -65 мг. Источники свободных аминокислот в клетках – белки пищи, собственные белки тканей и синтез аминокислот из углеводов. Многие клетки, за исключением эритроцитов, используют аминокислоты для синтеза белков, фосфолипидов мембран, пуриновых и пиримидиновых нуклеотидов, биогенных аминов (катехоламинов, гистамина).
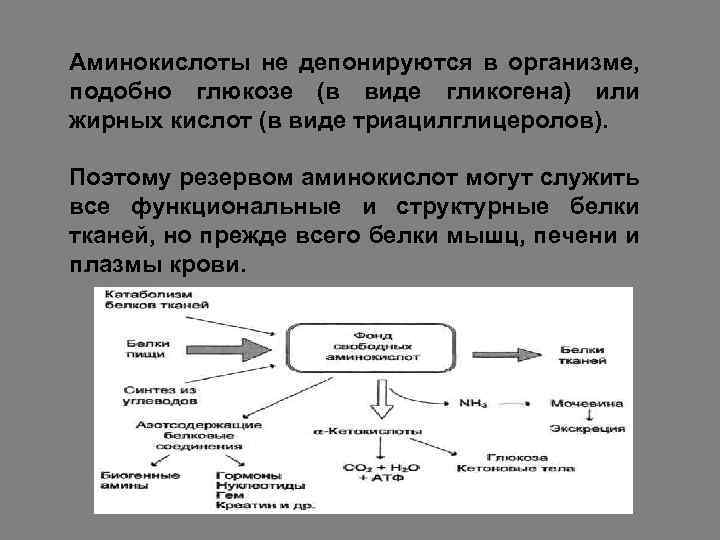
Аминокислоты не депонируются в организме, подобно глюкозе (в виде гликогена) или жирных кислот (в виде триацилглицеролов). Поэтому резервом аминокислот могут служить все функциональные и структурные белки тканей, но прежде всего белки мышц, печени и плазмы крови.

В организме человека постоянно происходит обновление белков - в сутки распадается на аминокислоты около 400 г белков и примерно такое же количество синтезируется. Синтез и обновление белков в разных тканях происходят с разной скоростью. Так коллаген полностью обновляется за 300 дней, а белки системы свертывания крови – от нескольких минут до нескольких дней. Основным источником, восполняющим фонд аминокислот организма являются белки пищи. Небольшая их часть пополняется за счет катаболизма тканевых белков или синтезируются, причем из углеводов образуется только углеродная часть молекулы большинства аминокислот, а аминогруппа поступает от других аминокислот.

БИОЛОГИЧЕСКАЯ ЦЕННОСТЬ БЕЛКОВ Азотистый баланс Аминокислоты (свободные и в составе белков) содержат почти 95% всего азота, поэтому баланс азота в организме является показателем состояния белкового и аминокислотного обмена. Азотистый баланс определяют как разницу между количеством азота, поступающего с пищей, и количеством выделяемого азота (преимущественно в виде мочевины и аммонийных солей).

Азотистый баланс может быть: Равным нулю (азотистое равновесие). У здорового человека при сбалансированном питании количество поступающего азота в сутки равно количеству выделяемого. Положительным - у детей у пациентов, выздоравливающих после тяжёлых болезней, а также при обильном белковом питании азота поступает больше, чем выводится. Отрицательным - при старении, голодании и во время тяжёлых заболеваний выделение азота преобладает над его поступлением.

Полноценность белкового питания В продуктах животного происхождения (сыр, мясо, рыба) и бобовых (горох, соя), белков содержится 20 -30% и более, в продуктах растительного происхождения (яблоки, картофель, капуста) только 0, 3 -2%. 20 аминокислот, которые имеются в белках, можно разделить на 4 группы по способности синтезироваться в организме человека.

Заменимые аминокислоты синтезируются в клетках в необходимых количествах (аланин, аспарагиновая кислота, аспарагин, глутаминовая кислота, глицин, пролин, серин) Незаменимые аминокислоты не могут синтезироваться в организме (фенилаланин, метионин, треонин, триптофан, валин, лизин, лейцин, изолейцин) Частично заменимые аминокислоты синтезируются очень медленно в количествах, не перекрывающих потребности организма, особенно у детей (аргинин и гистидин) Условно заменимые аминокислоты синтезируются из незаменимых аминокислот (тирозин и цистеин). Тирозин синтезируется из фенилаланина, а для образования цистеина необходим атом серы метионина.
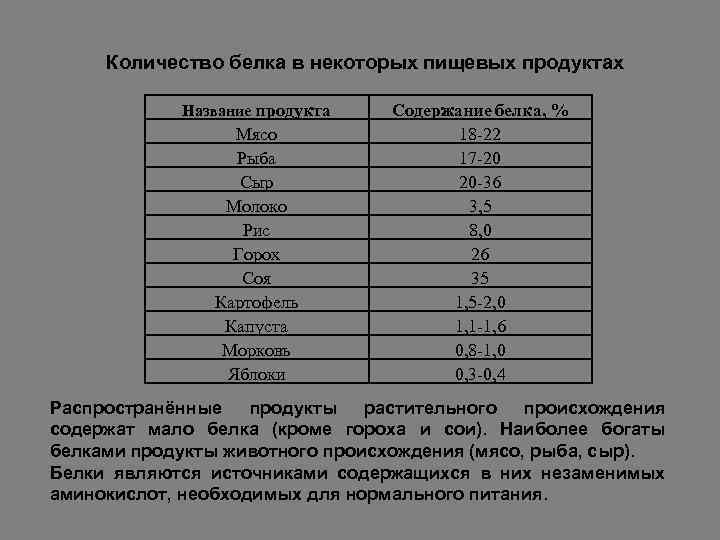
Количество белка в некоторых пищевых продуктах Название продукта Мясо Рыба Сыр Молоко Рис Горох Соя Картофель Капуста Морковь Яблоки Содержание белка, % 18 -22 17 -20 20 -36 3, 5 8, 0 26 35 1, 5 -2, 0 1, 1 -1, 6 0, 8 -1, 0 0, 3 -0, 4 Распространённые продукты растительного происхождения содержат мало белка (кроме гороха и сои). Наиболее богаты белками продукты животного происхождения (мясо, рыба, сыр). Белки являются источниками содержащихся в них незаменимых аминокислот, необходимых для нормального питания.

Питательная ценность белка зависит от его аминокислотного состава и способности усваиваться организмом. Белки значительно различаются по аминокислотному составу. Некоторые их них содержат полный набор незаменимых аминокислот в оптимальных соотношениях, другие не содержат одной или нескольких незаменимых аминокислот.

Растительные белки, особенно пшеницы и других злаковых, полностью не перевариваются, так как защищены оболочкой, состоящей из целлюлозы и других полисахаридов, которые не гидролизуются пищеварительными ферментами. Некоторые белки по аминокислотному близки к белкам тела человека, используются в качестве пищевых, имеют фибриллярное строение расщепляются протеазами ЖКТ. составу но не так как и не К ним относят белки волос, шерсти, перьев.

Если белок содержит все незаменимые аминокислоты в необходимых пропорциях и легко подвергается действию протеаз, то биологическая ценность такого белка условно принимается за 100, и он считается полноценным (белки яиц и молока). Белки мяса говядины имеют биологическую ценность 98. Растительные белки по биологической ценности уступают животным, так как труднее перевариваются и бедны лизином, метионином и триптофаном.

Так, белки кукурузы (биологическая ценность - 36) содержат мало лизина, но достаточное количество триптофана. А белки бобов богаты лизином, но содержат мало триптофана. Каждый из этих белков в отдельности является неполноценным. Однако смесь бобов и кукурузы содержит необходимое человеку количество незаменимых аминокислот.

Нормы белка в питании Минимальное количество белков в пище, необходимое для поддержания азотистого равновесия, составляет 30 -50 г/cyт, оптимальное при повышенной физической нагрузке – примерно 120 -150 г/сут. При тяжёлой физической работе эта норма увеличивается до 130 -150 г/сут. Таким образом, норма потребления белков составляет 100 г/сут. При этом подразумевается, что в пишу входят разнообразные белки животного и растительного происхождения.

Белковая недостаточность Длительное исключение из рациона человека жиров или углеводов не вызывает тяжёлых расстройств здоровья. Однако безбелковое питание (особенно продолжительное) вызывает серьёзные нарушения обмена и неизбежно заканчивается гибелью организма. Исключение даже одной незаменимой аминокислоты из пищевого рациона ведёт к неполному усвоению других аминокислот и сопровождается развитием отрицательного азотистого баланса, циррозу печени, анемии, поражению почек, истощением, остановкой роста и нарушениями функций нервной системы.

ПЕРЕВАРИВАНИЕ БЕЛКОВ В ЖКТ В пищевых продуктах свободных аминокислот очень мало, они поступают в ЖКТ в составе белков и становятся доступными только после их переваривания. В процессе переваривания происходит гидролиз белков до свободных аминокислот в ЖКТ под действием ферментов протеаз. Субстратная специфичность этих ферментов заключается в том, что каждый из них с наибольшей скоростью расщепляет пептидные связи, образованные определёнными аминокислотами.

Протеазы, гидролизующие пептидные связи внутри белковой молекулы, относят к группе эндопептидаз (пепсин, трипсин, химотрипсин). Ферменты, относящиеся к группе экзопептидаз, гидролизуют пептидную связь, образованную Nконцевыми аминокислотами (аминопептидаза) и С-концевыми аминокислотами (карбоксипептидаза). Под действием всех протеаз ЖКТ белки пищи распадаются на отдельные аминокислоты, которые затем поступают в клетки тканей.

Переваривание белков в желудке Желудочный сок - продукт нескольких типов клеток. Обкладочные (париетальные) клетки стенок желудка образуют соляную кислоту, главные клетки секретируют пепсиноген. Добавочные и другие клетки эпителия желудка выделяют муцинсодержащую слизь. Париетальные клетки секретируют в полость желудка также гликопротеины, которые предотвращает разрушение витамина В 12, и способствует его всасыванию.

Образование и роль соляной кислоты Основная пищеварительная функция желудка заключается в том, что в нём начинается переваривание белка. Существенную роль в этом процессе играет соляная кислота. Белки, поступающие в желудок, стимулируют выделение гистамина и группы белковых гормонов - гастринов, которые, в свою очередь, вызывают секрецию НСI и профермента - пепсиногена. НСI образуется в обкладочных клетках желудочных желёз.
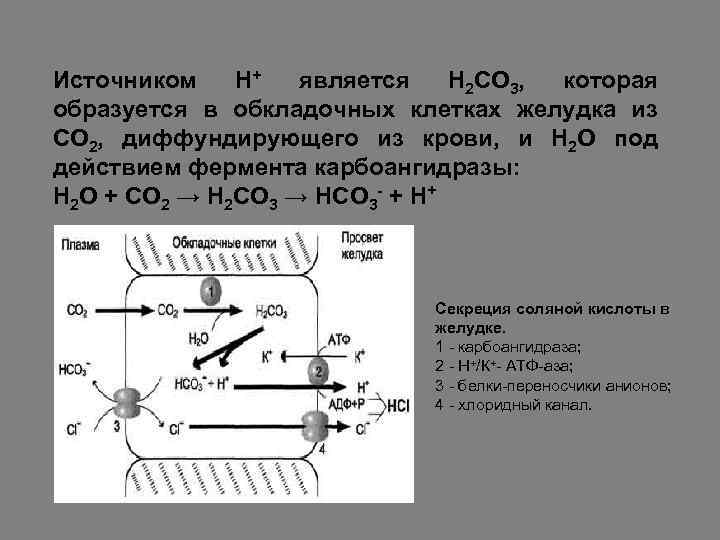
Источником Н+ является Н 2 СО 3, которая образуется в обкладочных клетках желудка из СО 2, диффундирующего из крови, и Н 2 О под действием фермента карбоангидразы: Н 2 О + СО 2 → Н 2 СО 3 → НСО 3 - + H+ Секреция соляной кислоты в желудке. 1 - карбоангидраза; 2 - Н+/К+- АТФ-аза; 3 - белки-переносчики анионов; 4 - хлоридный канал.

Диссоциация Н 2 СО 3 приводит к образованию бикарбоната, который с участием специальных белков выделяется в плазму в обмен на Сl-, и ионов Н+, которые поступают в просвет желудка путём активного транспорта, катализируемого мембранной Н+/К+-АТФазой. При этом концентрация протонов в просвете желудка увеличивается в 106 раз. Ионы Сl- поступают в просвет желудка через хлоридный канал. Концентрация НСl в желудочном соке может достигать 0, 16 М, за счёт чего значение р. Н снижается до 1, 0 -2, 0. Приём белковой пищи часто сопровождается выделением щелочной мочи за счёт секреции большого количества бикарбоната в процессе образования НСl.

Под действием НСl происходит денатурация белков пищи, не подвергшихся термической обработке, что увеличивает доступность пептидных связей для протеаз. НСl обладает бактерицидным действием и препятствует попаданию патогенных бактерий в кишечник. Кроме того, соляная кислота активирует пепсиноген и создаёт оптимум р. Н для действия пепсина.

Механизм активации пепсина Под действием гастринов в главных клетках желудочных желёз стимулируются синтез и секреция пепсиногена - неактивной формы пепсина. Пепсиноген - белок, состоящий из одной полипептидной цепи с молекулярной массой 40 к. Д. Под действием НСl он превращается в активный пепсин (молекулярная масса 32, 7 к. Д) с оптимумом р. Н 1, 0 -2, 5. В процессе активации в результате частичного протеолиза от N-конца молекулы пепсиногена отщепляются 42 аминокислотных остатка, которые содержат почти все положительно заряженные аминокислоты, имеющиеся в пепсиногене.

Таким образом, в активном пепсине преобладающими оказываются отрицательно заряженные аминокислоты, которые участвуют в конформационных перестройках молекулы и формировании активного центра. Образовавшиеся под действием НСl активные молекулы пепсина быстро активируют остальные молекулы пепсиногена (аутокатализ). Пепсин в первую очередь гидролизует пептидные связи в белках, образованные ароматическими аминокислотами (фенилаланин, триптофан, тирозин) и несколько медленнее - образованные лейцином и дикарбоновыми аминокислотами.

Нарушения переваривания белков в желудке

Нарушения переваривания белков в желудке При различных заболеваниях ЖКТ в желудке нарушается выделение НСl и пепсиногена, при этом переваривание белков заметно снижается. Наиболее часто встречаются патологические изменения кислотности желудочного сока. Нарушение образования пепсина отмечают реже и выявляют при более значительных поражениях желудка. Определение кислотности желудочного сока используют для диагностики различных заболеваний желудка.

Повышенная кислотность желудочного сока может быть симптомом язвы желудка и двенадцатиперстной кишки, а также гиперацидного гастрита. Пониженная кислотность бывает при некоторых видах гастритов. Анацидность (р. Н желудочного сока > 6, 0) свидетельствует о значительной потере слизистой оболочкой желудка обкладочных клеток, секретирующих соляную кислоту, что часто вызывает рак желудка. Кислотность желудочного сока выражается в титрационных единицах (ТЕ) – количество 0, 1 М Na. OH в 1 мл, затраченное на титрование 100 мл желудочного сока по определённому индикатору. При определении кислотности желудочного сока различают: общую кислотность, связанную НСl и свободную НСl.

Общая кислотность желудочного сока совокупность всех кислотореагирующих веществ желудочного сока, представляет собой секрет желудка, собираемый в течение 1 ч. Значения общей кислотности в норме составляют 40 -60 ТЕ. Связанная соляная кислота - НСl, связанная с белками и продуктами их переваривания. Значения связанной НСl у здоровых людей - 20 -30 ТЕ. Свободная соляная кислота - НСl, не связанная с компонентами желудочного сока. Значения свободной НСl в норме - 20 -40 ТЕ. р. Н желудочного сока в норме - 1, 5 -2, 0.

Молочная кислота в норме в желудочном соке отсутствует. Она образуется при уменьшении содержания или отсутствии свободной соляной кислоты в результате размножения молочнокислых бактерий или при злокачественных опухолях желудка, в клетках которых глюкоза окисляется анаэробным путём. При диагностике заболеваний желудка, кроме биохимических анализов, обязательно проводят рентгенологические и эндоскопические исследования, а также биопсию.

Переваривание белков в кишечнике Происходит под действием ферментов поджелудочной железы и клеток кишечника. Активация панкреатических ферментов В поджелудочной железе синтезируются проферменты ряда протеаз: трипсиноген, химотрипсиноген, проэластаза, прокарбоксипептидазы А и В. В кишечнике они путём частичного протеолиза превращаются в активные ферменты трипсин, химотрипсин, эластазу и карбоксипептидазы А и В.

Активация трипсиногена происходит под действием фермента эпителия кишечника энтеропептидазы. Этот фермент отщепляет с N-конца молекулы трипсиногена гексапептид Вал-(Асп)4 -Лиз. Изменение конформации оставшейся части полипептидной цепи приводит к формированию активного центра, и образуется активный трипсин. Образовавшийся трипсин активирует химотрипсиноген, из которого получается несколько активных ферментов.

Химотрипсиноген состоит из одной полипептидной цепи, содержащей 245 аминокислотных остатков и пяти дисульфидных мостиков. Под действием трипсина расщепляется пептидная связь между 15 -й и 16 -й аминокислотами, в результате чего образуется активный π-химотрипсин. Затем под действием πхимотрипсина отщепляется дипептид сер(14)-арг(15), что приводит к образованию δ-химотрипсина. Отщепление дипептида тре(147)-арг(148) завершает образование стабильной формы активного фермента αхимотрипсина, который состоит из трёх полипептидных цепей, соединённых дисульфидными мостиками. Остальные проферменты панкреатических протеаз (проэластаза и прокарбоксипептидазы А и В) также активируются трипсином путём частичного протеолиза. В результате образуются активные ферменты - эластаза и карбоксипептидазы А и В.

Специфичность действия протеаз Трипсин преимущественно гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина. Химотрипсины наиболее активны в отношении пептидных связей, образованных карбоксильными группами ароматических аминокислот (Фен, Тир, Три). Карбоксипептидазы А и В - цинксодержащие ферменты, отщепляют С-концевые остатки аминокислот. Причём карбоксипептидаза А отщепляет преимущественно аминокислоты, содержащие ароматические или гидрофобные радикалы, а карбоксипептидаза В - остатки аргинина и лизина.

Последний этап переваривания - гидролиз небольших пептидов, происходит под действием ферментов аминопептидаз и дипептидаз, которые синтезируются клетками тонкого кишечника в активной форме. Аминопептидазы последовательно отщепляют Nконцевые аминокислоты пептидной цепи. Наиболее известна лейцинаминопептидаза – Zn 2+ - или Мn 2+ содержащий фермент, несмотря на название, обладающий широкой специфичностью по отношению к N-концевым аминокислотам. Дипептидазы расщепляют дипептиды на аминокислоты, но не действуют на трипептиды. В результате последовательного действия всех пищеварительных протеаз большинство пищевых белков расщепляется до свободных аминокислот.

Транспорт аминокислот в клетки Аминокислоты, образовавшиеся при переваривании белков, быстро всасываются в кишечнике. Транспорт их осуществляется двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной лимфатический проток. Максимальная концентрация аминокислот в крови достигается через 30 -50 мин после приёма белковой пищи (углеводы и жиры замедляют всасывание аминокислот). Всасывание Lаминокислот (но не D-изомеров) - активный процесс, требующий затраты энергии. Аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь.
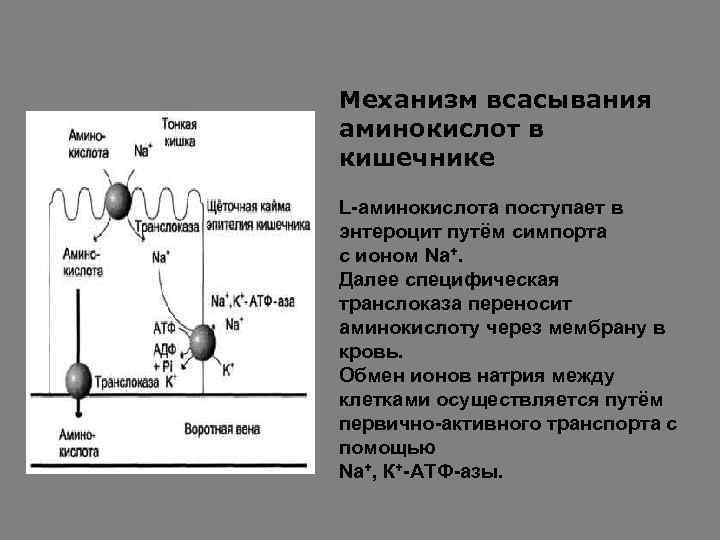
Механизм всасывания аминокислот в кишечнике L-аминокислота поступает в энтероцит путём симпорта с ионом Na+. Далее специфическая транслоказа переносит аминокислоту через мембрану в кровь. Обмен ионов натрия между клетками осуществляется путём первично-активного транспорта с помощью Nа+, К+-АТФ-азы.

Перенос через щёточную кайму осуществляется целым рядом переносчиков, многие из которых действуют при участии Nа+-зависимых механизмов симпорта, подобно переносу глюкозы. Различная скорость проникновения аминокислот через мембраны клеток указывает на наличие транспортных систем, обеспечивающих перенос аминокислот как через внешнюю плазматическую мембрану, так и через внутриклеточные мембраны.

В настоящее время известно по крайней мере пять специфических транспортных систем, каждая из которых функционирует для переноса определённой группы близких по строению аминокислот: • нейтральных, с короткой боковой цепью (аланин, серии, треонин); • нейтральных, с длинной или разветвлённой боковой цепью (валин, лейцин, изолейцин); • с катионными радикалами (лизин, аргинин); • с анионными радикалами (глутаминовая и аспарагиновая кислоты); • иминокислот (пролин, оксипролин).

Аминокислоты конкурируют друг с другом за специфические участки связывания. Например, всасывание лейцина (если концентрация его достаточно высока) уменьшает всасывание изолейцина и валина. Одна из специфических транспортных систем для некоторых нейтральных аминокислот функционирует в кишечнике, почках и, повидимому, мозге. Она получила название γ-глутамильного цикла.
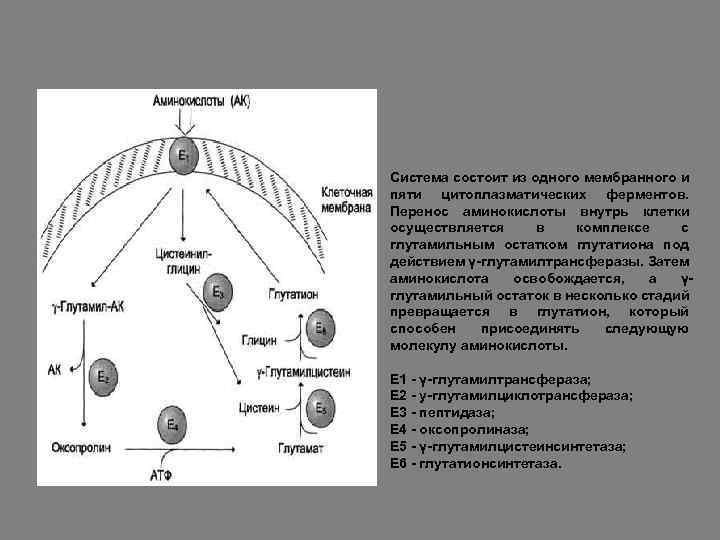
Система состоит из одного мембранного и пяти цитоплазматических ферментов. Перенос аминокислоты внутрь клетки осуществляется в комплексе с глутамильным остатком глутатиона под действием γ-глутамилтрансферазы. Затем аминокислота освобождается, а γглутамильный остаток в несколько стадий превращается в глутатион, который способен присоединять следующую молекулу аминокислоты. Е 1 - γ-глутамилтрансфераза; Е 2 - у-глутамилциклотрансфераза; Е 3 - пептидаза; Е 4 - оксопролиназа; Е 5 - γ-глутамилцистеинсинтетаза; Е 6 - глутатионсинтетаза.

В этой системе участвуют 6 ферментов, один из которых находится в клеточной мембране, а остальные - в цитозоле. Ключевую роль в транспорте аминокислоты играет мембранносвязанный фермент γглутамилтрансфераза. Этот фермент является гликопротеином и катализирует перенос γ-глутамильной группы от глутатиона (иногда другого γ-глутамильного пептида) на транспортируемую аминокислоту и последующий перенос комплекса в клетку. Глутатион представляет собой трипептид - γглутамилцистеинилглицин, который находится во всех тканях животных.

Аминокислота, связанная с γ-глутамильным остатком, оказывается внутри клетки. В следующей реакции происходит отщепление γглутамильного остатка под действием фермента γ -глутамилциклотрансферазы. Дипептид цистеинилглицин расщепляется под действием пептидазы на 2 аминокислоты цистеин и глицин. В результате этих 3 реакций происходит перенос одной молекулы аминокислоты в клетку (или внутриклеточную структуру). Следующие 3 реакции обеспечивают регенерацию глутатиона, благодаря чему цикл повторяется многократно. Для транспорта в клетку одной молекулы аминокислоты с участием γ-глутамильного цикла затрачиваются 3 молекулы АТФ.
Obmen_aminokislot.ppt