Нано-Лекция 2-3.pptx
- Количество слайдов: 79

Нанохимия и нанотехнологии

Лекция 2 Общие представления о нанохимии и нанотехнологии 1 Размерный эффект Наночастицы - объекты, состоящие из атомов, ионов или молекул и имеющие размер менее 100 нм. Примеры - частицы металлов: наночастицы золота, равномерно распределенные в воде, образуют коллоидный раствор – золь. В зависимости от размера частиц золь золота может иметь оранжевую, пурпурную, красную или даже зеленую окраску (рисунок). Рисунок 1 - Зависимость цвета золей золота от размера частиц Рисунок 2 - Наночастицы серебра Они могут обладать бактерицидным и фунгицидным действием. Самый простой способ получения золя металлического серебра - простое кипячение аммиачного комплекса «оксида серебра» в воде (рис. 2).

Рисунок 2 – коллоидный раствор наночастиц серебра Из-за малого размера наночастицы серебра отличаются по свойствам и от отдельных атомов, и от объемного материала, состоящего из многих миллиардов атомов, например слитка серебра. Многие физические свойства вещества (его окраска, тепло- и электропроводность, температура плавления) зависят от размера частиц. Например, температура плавления наночастиц золота размером 5 нм на 250° ниже, чем у обычного золота (1337 °С) (рисунок 3). По мере увеличения размера наночастиц золота температура плавления возрастает и достигает обычного значения, характерного для материала, который называют объемной фазой, или макрофазой.
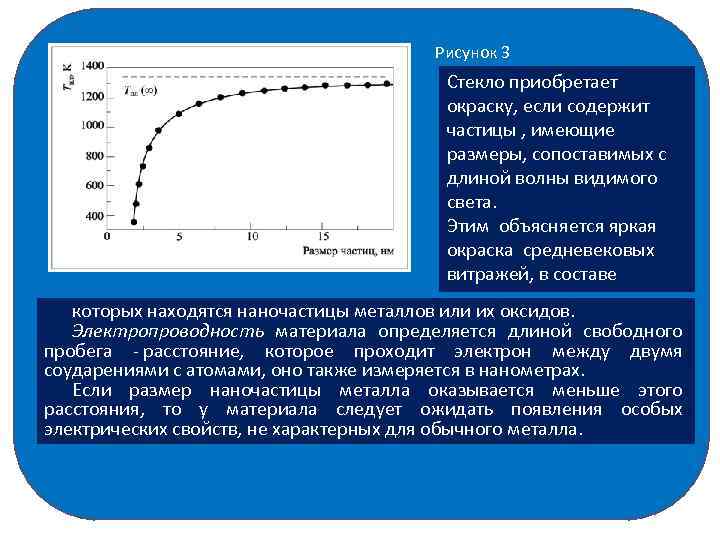
Рисунок 3 Стекло приобретает окраску, если содержит частицы , имеющие размеры, сопоставимых с длиной волны видимого света. Этим объясняется яркая окраска средневековых витражей, в составе которых находятся наночастицы металлов или их оксидов. Электропроводность материала определяется длиной свободного пробега - расстояние, которое проходит электрон между двумя соударениями с атомами, оно также измеряется в нанометрах. Если размер наночастицы металла оказывается меньше этого расстояния, то у материала следует ожидать появления особых электрических свойств, не характерных для обычного металла.

Итак, нанообъекты характеризуются не только малым размером, но и особыми свойствами, которые они проявляют как составная часть материала. Так, окраска стекла «золотой рубин» или коллоидного раствора золота вызвана не одной наночастицей золота, а их ансамблем, т. е. большим количеством частиц, расположенных на определенном расстоянии друг от друга. Отдельные наночастицы, содержащие не более 1000 атомов, называют нанокластерами. Свойства таких частиц значительно отличаются от свойств кристалла, в котором содержится огромное число атомов. Это объясняется особой ролью поверхности. Известно, что реакции с участием твердых тел происходят не в объеме, а на поверхности. .

Атомы на поверхности обладают большей энергией, т. к. у них меньше соседей в кристаллической решетке. Уменьшение размера частиц приводит к увеличению общей площади поверхности, росту доли атомов на поверхности и возрастанию роли поверхностной энергии. Особенно велика она у нанокластеров, где большинство атомов находится на поверхности. Поэтому нанозолото по химической активности во много раз превосходит обычное: наночастицы золота, содержащие 55 атомов (диаметр 1, 4 нм), нанесенные на поверхность Ti. O 2, - хороший катализатор селективного окисления стирола кислородом воздуха до бензальдегида. Частицы диаметром более 2 нм, а тем более обычное золото совсем не проявляют каталитической активности.

Зависимость физических и химических свойств наночастиц от их размера называют размерным эффектом. Это – один из важнейших эффектов в нанохимии. Теоретическое объяснение размерному эффекту даёт химическая термодинамика. Так, зависимость температуры плавления от размера объясняется тем, что атомы внутри наночастиц испытывают дополнительное поверхностное давление, которое изменяет их энергию Гиббса. 2 Классификация нанообъектов Общепринятым подходом к определению нанообъектов является положение о том, что к ним относятся такие объекты, размеры которых хотя бы в одном из пространственных направлений составляют примерно 0, 1. . 100 нм - это так называемые малоразмерные объекты.
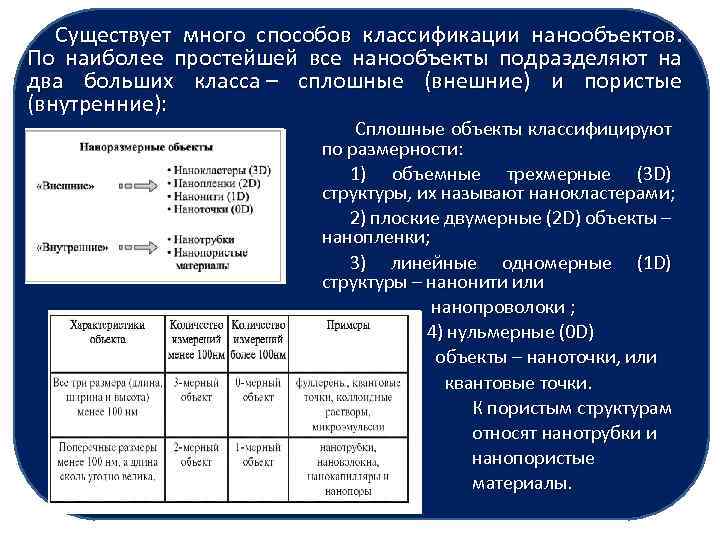
Существует много способов классификации нанообъектов. По наиболее простейшей все нанообъекты подразделяют на два больших класса – сплошные (внешние) и пористые (внутренние): Сплошные объекты классифицируют по размерности: 1) объемные трехмерные (3 D) структуры, их называют нанокластерами; 2) плоские двумерные (2 D) объекты – нанопленки; 3) линейные одномерные (1 D) структуры – нанонити или нанопроволоки ; 4) нульмерные (0 D) объекты – наноточки, или квантовые точки. К пористым структурам относят нанотрубки и нанопористые материалы.
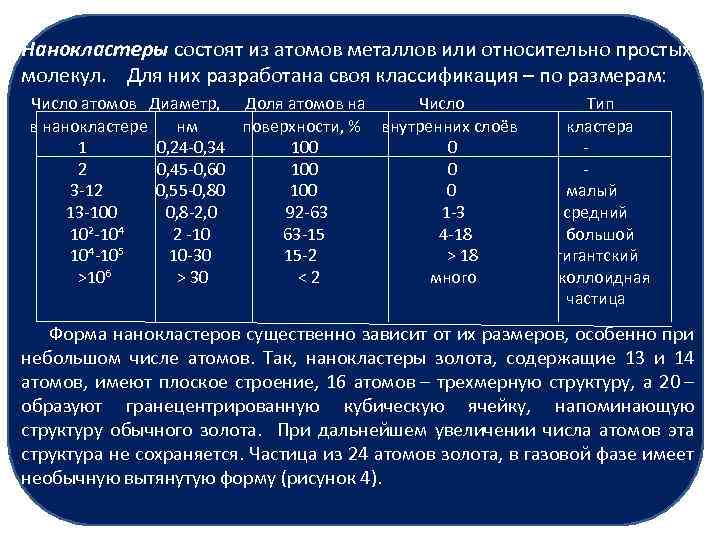
Нанокластеры состоят из атомов металлов или относительно простых молекул. Для них разработана своя классификация – по размерам: Число атомов Диаметр, Доля атомов на Число Тип в нанокластере нм поверхности, % внутренних слоёв кластера 1 0, 24 -0, 34 100 2 0, 45 -0, 60 100 3 -12 0, 55 -0, 80 100 малый 13 -100 0, 8 -2, 0 92 -63 1 -3 средний 10²-10⁴ 2 -10 63 -15 4 -18 большой 10⁴-10⁵ 10 -30 15 -2 > 18 гигантский >10⁶ > 30 < 2 много коллоидная частица Форма нанокластеров существенно зависит от их размеров, особенно при небольшом числе атомов. Так, нанокластеры золота, содержащие 13 и 14 атомов, имеют плоское строение, 16 атомов – трехмерную структуру, а 20 – образуют гранецентрированную кубическую ячейку, напоминающую структуру обычного золота. При дальнейшем увеличении числа атомов эта структура не сохраняется. Частица из 24 атомов золота, в газовой фазе имеет необычную вытянутую форму (рисунок 4).

Рисунок 4 –Возможные структуры нанокластера Au 24. Наиболее устойчивая – а. Нанокластеры присутствуют даже в обычной воде - агломераты из отдельных молекул воды, соединенных друг с другом водородными связями. Особенно много их - в воде при низкой температуре, вблизи точки плавления. Такая вода характеризуется особыми свойствами: имеет большую плотность, по сравнению со льдом, и лучше усваивается растениями. Это пример того, что свойства вещества определяются не только его химической формулой, но и его строением, в том числе и на наноуровне.

Наиболее полно изучены нанотрубки. Это цилиндрические структуры нанометровых размеров. Углеродные нанотрубки открыты в 1951 г. советскими физиками Л. В. Радушкевичем и В. М. Лукьяновичем. Но они опубликовали своё открытие в отечественном научном журнале год спустя. Их работа прошла незамеченной.

Вновь интерес к нанотрубкам возник после работ зарубежных исследователей в 1990 -е гг. Углеродные нанотрубки в 100 раз прочнее стали, многие из них хорошо проводят тепло и электрический ток. Ученым удалось синтезировать нанотрубки нитрида бора и некоторых металлов, например золота. По прочности они уступают углеродным, но благодаря гораздо большему диаметру, способны включать в себя сравнительно крупные молекулы.

Рисунок 5 – Микрофотографии золотых нанотрубок Одномерные нанообъекты - нанонити, или нанопроволоки. Это протяженные наноструктуры с сечением менее 10 нм. При этом объект начинает проявлять особые, квантовые свойства. Известны нанопроволоки металлов (никеля, золота, меди) и полупроводников (кремния), диэлектриков (оксида кремния).

При медленном взаимодействии паров кремния с кислородом в особых условиях получают нанопроволоки оксида кремния, на которых, как на веточках , висят шаровидные образования из кремнезема, напоминающие ягоды вишни. Размер такой «ягоды» составляет всего 20 микрон (мкм). Известны молекулярные нанопроволоки, например, молекула ДНК – хранитель наследственной информации.

Небольшое количество неорганических молекулярных нанопроволок представляют собой сульфиды или селениды молибдена. Фрагмент структуры одного из этих соединений приведен на рисунке 5. Рисунок 5 – Структура нанопроволоки селенида молибдена, состоящей из 7 слабо взаимодействующих молекулярных цепочек Двумерные нанообъекты - нанопленки. Благодаря очень малой толщине (всего в одну или две молекулы) они пропускают свет и незаметны для глаза. Полимерные нанопокрытия из полистирола и других полимеров надежно защищают многие предметы, используемые в быту, – экраны компьютеров, окошки сотовых телефонов, линзы очков.

Одиночные нанокристаллы полупроводников (например, Zn. S или Cd. Se) размером до 10– 50 нм называют квантовыми точками. Их считают нуль-мерными нанообъектами. Они содержат от 100 до 100 000 атомов. При облучении квантового полупроводника возникает пара «электрон–дырка» (экситон), движение которой в квантовой точке ограничено по всем направлениям. Переходя из возбужденного состояния в основное, квантовая точка испускает свет. Длина волны зависит от размера точки. Эту способность используют для разработки лазеров и дисплеев нового поколения. Квантовые точки можно использовать и в качестве биологических меток (маркеров), соединяя их с определенными белками.

Методы синтеза и исследования наночастиц Все методы синтеза делятся на 2 группы. 1 -я группа объединяет способы, позволяющие получить и изучить наночастицы. Это: - конденсация при сверхнизких температурах; - некоторые варианты химического, фотохимического и радиационного восстановления; - лазерное испарение. 2 -я группа включает методы, позволяющие на основе наночастиц получать наноматериалы и нанокомпозиты: - различные варианты механохимического дробления; - конденсация из газовой фазы; - плазмохимические методы и др.

Разделение методов - условное, но отражает еще одну их особенность: - получение частиц путем укрупнения отдельных атомов, или подход «снизу вверх» ; - различные варианты диспергирования и агрегации, или подход «сверху вниз» . Первый подход характерен : для химических методов получения наночастиц, второй - для физических методов.

При получении наночастиц «снизу вверх» единичные атомы рассматриваются как нижняя граница нанохимии. Верхняя граница определяется количеством атомов в кластере, при котором дальнейшее увеличение размера частиц не ведет к качественным изменениям химических свойств. Количество атомов, определяющих верхнюю границу, индивидуально для каждого элемента периодической системы.

Все методы «снизу вверх» делят на 2 больших класса: 1)осаждение наночастиц из газовой фазы; 2) образование наночастиц в коллоидном растворе. Если осаждение из газовой фазы происходит с изменением состава вещества, его называют химическим, если химической реакции при осаждении нет, это физический процесс (см. рис. ).
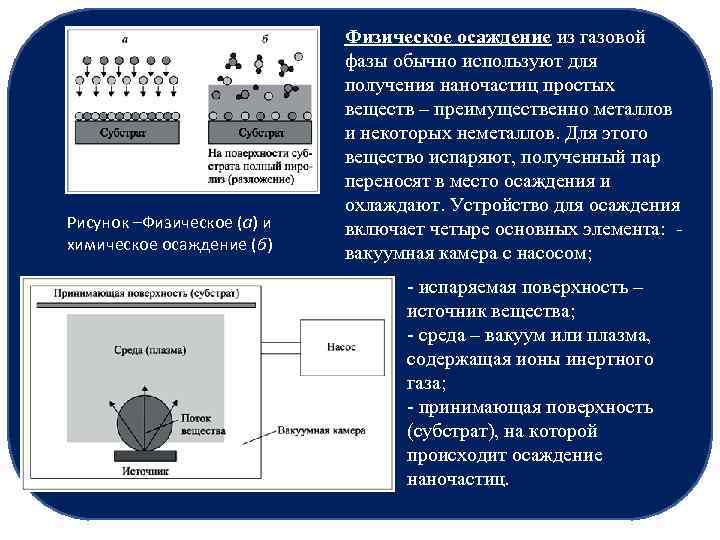
Рисунок –Физическое (а) и химическое осаждение (б) Физическое осаждение из газовой фазы обычно используют для получения наночастиц простых веществ – преимущественно металлов и некоторых неметаллов. Для этого вещество испаряют, полученный пар переносят в место осаждения и охлаждают. Устройство для осаждения включает четыре основных элемента: - вакуумная камера с насосом; - испаряемая поверхность – источник вещества; - среда – вакуум или плазма, содержащая ионы инертного газа; - принимающая поверхность (субстрат), на которой происходит осаждение наночастиц.

Порядок процесса осаждения - в камере создаётся высокий вакуум (10– 4– 10– 6 Па); - камеру заполняют инертным газом, чаще всего аргоном; - при химическом осаждении в камеру добавляют газы, которые реагируют с веществом – кислород, азот, ацетилен; - идёт процесс испарения. Для этого используют разные способы: нагревание излучением импульсного лазера высокой интенсивности (лазерная абляция), бомбардировку пучком электронов в высоком вакууме, воздействие газоразрядной плазмой, нагревание в электрической дуге;

- идёт охлаждение. Атомы или молекулы из газовой фазы осаждаются в виде наночастиц на специальной поверхности – подложке (субстрате). Это могут быть грани кристаллов, тонкие пленки и др. Размер и форма образующихся наночастиц существенно зависят от условий осаждения (Т, Р, скорость потока газа) и свойств подложки. Так получают нанокластеры металлов – серебра, золота, платиновых металлов, железа, кобальта, а также оксидов металлов, например Zn. O, Ti. O 2 и др.

Меняя условия осаждения, можно получать одномерные металлические нити или более сложные наноансамбли. При химическом осаждении из газовой фазы на поверхности подложки адсорбируются атомы и молекулы веществ, образующихся в результате химических реакций, которые протекают, как правило, при высокой температуре – от 600 до 1000 °С. Реагенты, используемые для химического осаждения, называют прекурсорами (предшественниками синтезируемых наночастиц). Прекурсор испаряют при нагревании и под давлением инертного газа направляют в реакционную зону, где и происходит его превращение в нанопродукт. Многие реакции требуют катализатора, он играет роль затравки для кристаллизации.
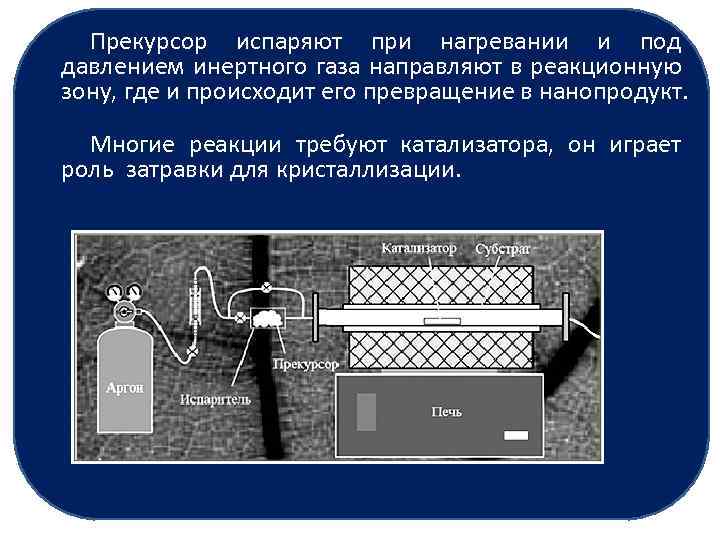
Прекурсор испаряют при нагревании и под давлением инертного газа направляют в реакционную зону, где и происходит его превращение в нанопродукт. Многие реакции требуют катализатора, он играет роль затравки для кристаллизации.

ВАРИАНТ 1 1) Наночастицы – это _______ Приведите примеры. 2) Приведите 3 -4 свойства частиц, которые зависят от их размера. 3) Приведите примеры, подтверждающие наличие особых свойств у нанокластеров в отличие от Кристаллов с огромным числом атомов. 4) Внешние нанообъекты делятся на: ________________ 5) Приведите примеры пористых нанообъектов: __________ ВАРИАНТ 2 1) Нанокластеры – это _______ 2) Дайте понятие: «Размерный наноэффект» - _______ 3) Особые свойства нанокластеров объясняются _________ 4) Все нанообъекты делят на два больших класса. Назовите их: 5) Приведите примеры нульмерных, одномерных и двумерных нанообъектов

ЛЕКЦИЯ 3 Вопросы: 1) Методы синтеза и исследования наночастиц - получение наночастиц «снизу - вверх» (химические методы) и «сверху - вниз» (физические методы); - 2 класса химических методов получения и исследования (сущность методов, примеры, порядок процессов, понятие «прекурсора» , аппаратура, применяемая для получения и исследования наночастиц. 2) Химические методы исследования (снизу-вверх)

Химические методы синтеза «снизу вверх» Для углеродных нанотрубок прекурсорами служат метан или бензол. Термическая диссоциация метана в присутствии катализатора (наночастиц переходных металлов): CH 4 = C + 2 H 2, Образуются атомы углерода, которые последовательно, один за одним, формируют углеродную трубку. Частицы катализатора выступают в роли зародышей. Атомы углерода осаждаются на поверхности субстрата, диффундируют через наночастицу металла и соединяются в нанотрубку, которая растет снизу вверх.
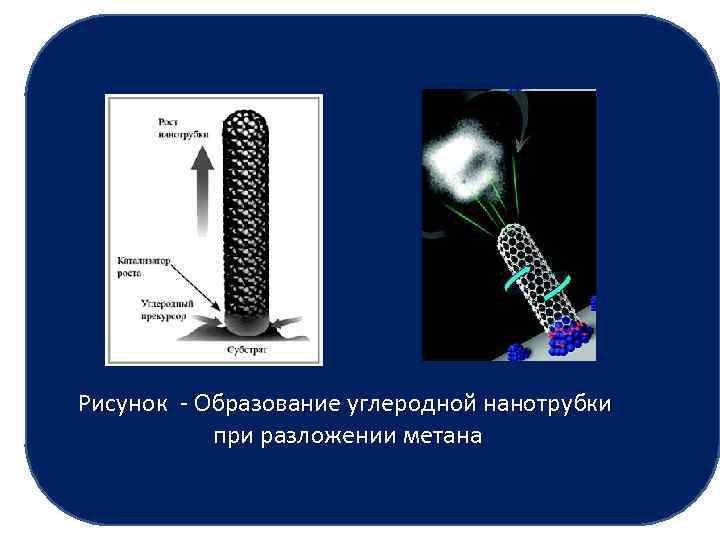
Рисунок - Образование углеродной нанотрубки Рисунок при разложении метана
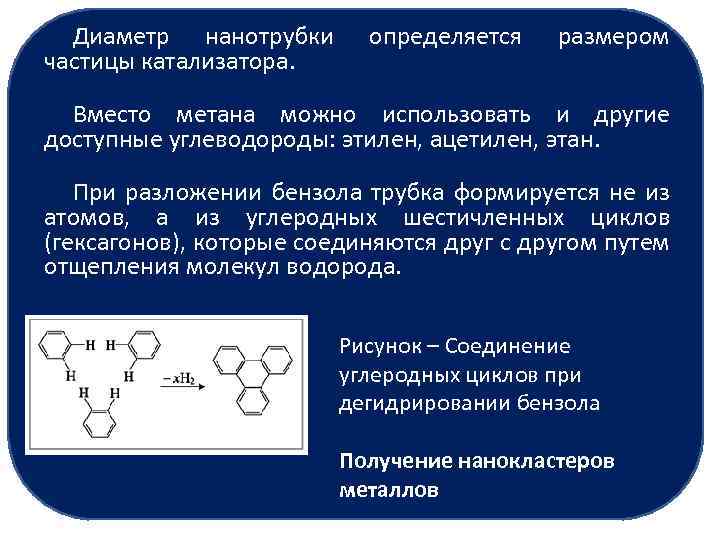
Диаметр нанотрубки частицы катализатора. определяется размером Вместо метана можно использовать и другие доступные углеводороды: этилен, ацетилен, этан. При разложении бензола трубка формируется не из атомов, а из углеродных шестичленных циклов (гексагонов), которые соединяются друг с другом путем отщепления молекул водорода. Рисунок – Соединение углеродных циклов при дегидрировании бензола Получение нанокластеров металлов

Получение нанокластеров металлов Используют летучие соединения, способные разлагаться н атомы металла и молекулы газа. Примеры: 1) Карбонил никеля Ni(CO)4 – бесцветная жидкость, пр нагревании легко превращается в металлический никель: Ni(CO)4 = Ni + 4 CO 2) Разложением азида лития Li. N 3 получают литий: 2 Li. N 3 = 2 Li + 3 N 2, Этими методами получают кластеры металла диаметро менее 5 нм.

Нанокластеры металлов легко вступают в реакции и поэтому неустойчивы. Чтобы их стабилизировать, к атомам, находящимся на поверхности, присоединяют органические молекулы – лиганды. Более устойчивы к внешним воздействиям - наночастицы оксидов. Их получают сжиганием веществ в пламени: Распыляя мелкие порошки кремния, алюминия и других металлов, получают наночастицы оксидов этих элементов: Si + O 2 = Si. O 2 4 Al + 3 O 2 = 2 Al 2 O 3 Наночастицы оксида титана получают при окислении паров хлорида титана(IV) кислородом : Ti. Cl 4 + O 2 = Ti. O 2 + 2 Cl 2

Сначала образуются отдельные зародыши оксидов, а затем - более крупные наночастицы. Частицы оксидов должны находиться в зоне реакции незначительное время (тысячные доли секунды), иначе они укрупнятся и превзойдут «наноуровень» . Наночастицы можно получать и в более мягких условиях, например, в жидкой фазе. Обычно наночастицы металлов получают восстановлением различных соединений золота(III), например , солей. Один из стандартных методов получения коллоидных растворов золота: восстановление Na. Au. Cl 4 цитратом натрия (натриевая соль лимонной кислоты) в присутствии 12 -аминододецилтиола H 2 N(CH 2)12 SH.

Соль лимонной кислоты теряет одну карбоксильную группу (происходит декарбоксилирование), а вторичная спиртовая группа CH–OH окисляется в кетонную C=O. Уравнение реакции: Молекулы аминоалкантиола (аминотиольные лиганды) покрывают поверхность образующихся наночастиц за счет реакции с атомами золота: и защищают их от взаимодействия друг с другом и укрупнения до макроразмеров

Рисунок - Наночастица золота, покрытая слоем молекул аминоалкантиола Наночастицы оксидов в растворах часто получают гидролизом солей при повышенной температуре. При нагревании раствора хлорида железа(III) при 95 °С получают нанопорошок оксида железа(III): 2 Fe. Cl 3 + 3 H 2 O = Fe 2 O 3 + 6 HCl

Гидролиз протекает необратимо, т. к. образующийся HCl плохо растворим в очень горячей воде и выделяется в виде газа. В результате равновесие гидролиза смещается вправо. Образующийся первоначально при гидролизе гидроксид железа(III) разлагается с образованием оксида. Часто при гидролизе отдельные наночастицы объединяются в более крупные агрегаты или образуют коллоидный раствор – золь, далее переходящий в нерастворимый гель. Например, гидролиз сложных эфиров ортокремниевой кислоты (тетраалкоксисиланов) приводит к образованию геля кремниевой кислоты: Si(OR)4 + 3 H 2 O = Si. O 2 • H 2 O + 4 ROH Если требуется получить отдельные наночастицы оксида кремния, то в раствор необходимо ввести вещество, которое будет препятствовать объединению отдельных частиц.

Наночастицы полупроводниковых материалов осаждают из растворов, используя обменные реакции. Например, наночастицы селенида цинка получают, пропуская ток селеноводорода через слабый раствор ацетата цинка: Zn(CH 3 COO)2 + H 2 Se = Zn. Se + 2 CH 3 COOH Чтобы предотвратить слипание частиц и образование крупнокристаллического осадка, в раствор соли добавляют ПАВ, например олеиновую кислоту. Так получают квантовые точки – нанокристаллы полупроводников.
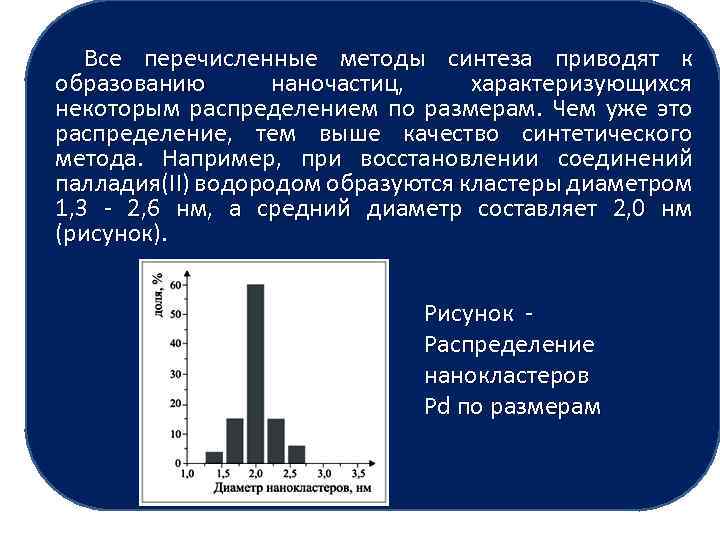
Все перечисленные методы синтеза приводят к образованию наночастиц, характеризующихся некоторым распределением по размерам. Чем уже это распределение, тем выше качество синтетического метода. Например, при восстановлении соединений палладия(II) водородом образуются кластеры диаметром 1, 3 - 2, 6 нм, а средний диаметр составляет 2, 0 нм (рисунок). Рисунок - Распределение нанокластеров Pd по размерам

Во многих нанотехнологиях требуются частицы совершенно одинакового размера – монодисперсные. Для получения таких систем смесь наночастиц разделяют по размерам, используя разнообразные физические методы : – седиментацию, -электрофорез или селективную адсорбцию молекулярными ситами. В качестве адсорбента используют пористые материалы на основе оксида кремния со строго фиксированными размерами пор.

Рисунок - Селективная по размерам адсорбция наночастиц молекулярными ситами

Методы исследования и диагностики нанообъектов Важное значение в химических превращениях наночастиц имеют размера и их физико-химические свойства. Исследования свойств частиц на поверхности и в объеме различаются. Методы определения размера и свойств наночастиц в газовой фазе: - ионизация фотонами и электронами и последующий анализ получаемых масс-спектров; - атомное распыление и последующая селекция по массам нейтральных кластеров; - электронная просвечивающая микроскопия на сетках (позволяет определить размер и форму частиц)

Для исследования наночастиц на поверхности используют: - просвечивающую и сканирующую электронную микроскопию (ПЭМ и СЭМ); - дифракцию электронов; - сканирующую туннельную микроскопию (СТМ); - адсорбцию газов; - фотоэлектронную спектроскопию; - электропроводность. Важнейшая роль принадлежит электронной микроскопии и сканирующей зондовой микроскопии.

Обычный оптический микроскоп не позволяет разглядеть не только атомы, но и наночастицы. Причина в том, что в нём для получения изображения используют видимый свет с длиной волны 400 -700 нм. Волновая оптика учит, что 2 объекта нельзя различить, если расстояние между ними значительно меньше длины волны излучаемого света. Поэтому в оптический микроскоп можно увидеть, например, живые клетки, размер которых составляет микроны (т. е. тысячи нанометров), более мелкие объекты не видны. Для этого нужно излучение со значительно меньшей длиной волны.
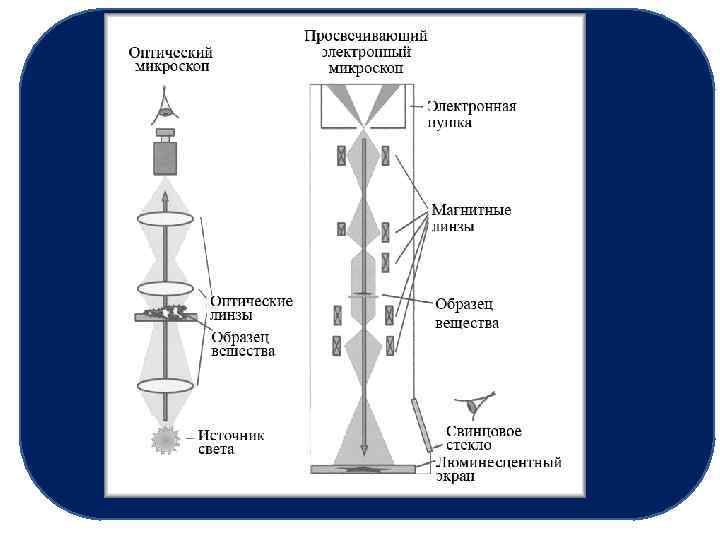

Устройства оптического и электронного микроскопа похожи. Они состоят из: -источника излучения; - системы фокусировки излучения на изучаемом объекте; - регистрирующего устройства – детектора. В электронном микроскопе: - источником электронов служит электронная пушка; - фокусировка пучка электронов осуществляется электромагнитными линзами; - детектором является люминесцентный экран.

Различают просвечивающие и сканирующие (растровые) электронные микроскопы. Они дают различную информацию об объекте и часто используются совместно. В просвечивающем электронном микроскопе (ПЭМ) пучок электронов проходит через очень тонкий (< 100 нм) слой вещества, давая информацию о его внутренней микроструктуре.
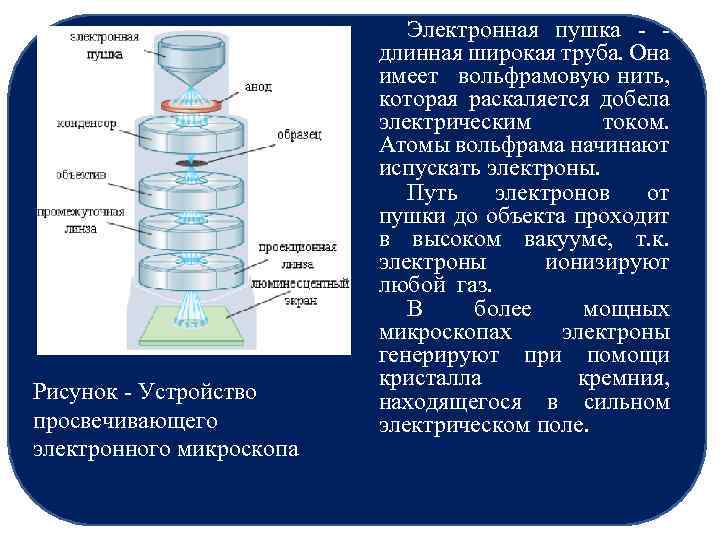
Рисунок - Устройство просвечивающего электронного микроскопа Электронная пушка - - длинная широкая труба. Она имеет вольфрамовую нить, которая раскаляется добела электрическим током. Атомы вольфрама начинают испускать электроны. Путь электронов от пушки до объекта проходит в высоком вакууме, т. к. электроны ионизируют любой газ. В более мощных микроскопах электроны генерируют при помощи кристалла кремния, находящегося в сильном электрическом поле.
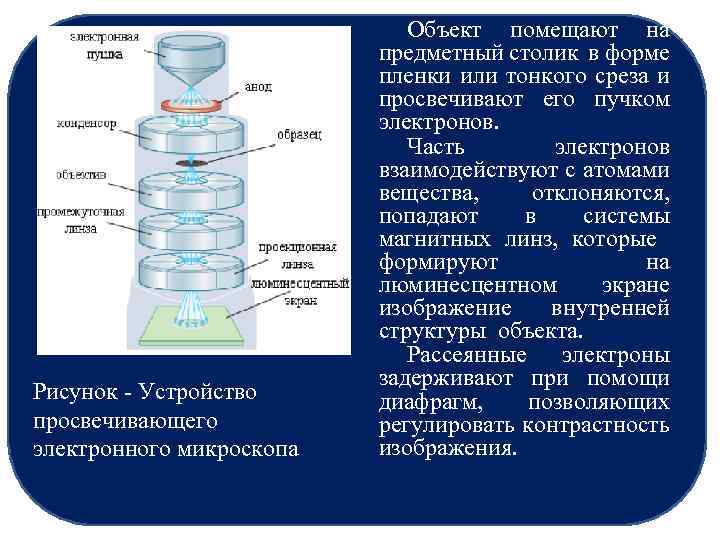
Рисунок - Устройство просвечивающего электронного микроскопа Объект помещают на предметный столик в форме пленки или тонкого среза и просвечивают его пучком электронов. Часть электронов взаимодействуют с атомами вещества, отклоняются, попадают в системы магнитных линз, которые формируют на люминесцентном экране изображение внутренней структуры объекта. Рассеянные электроны задерживают при помощи диафрагм, позволяющих регулировать контрастность изображения.

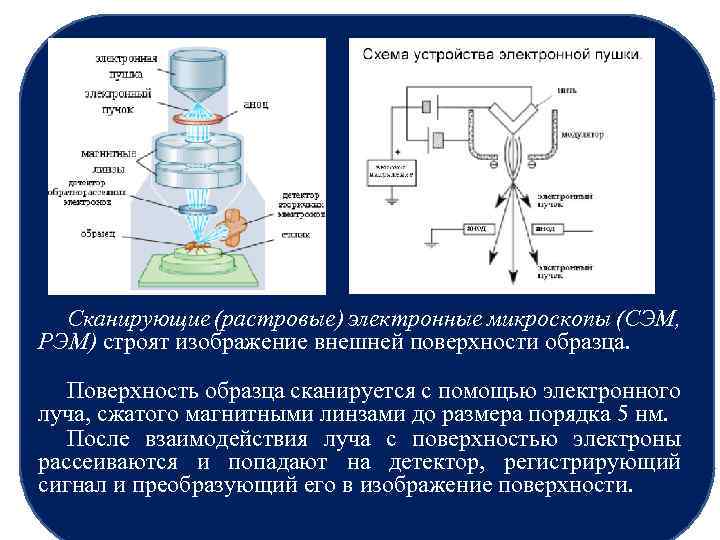
Сканирующие (растровые) электронные микроскопы (СЭМ, РЭМ) строят изображение внешней поверхности образца. Поверхность образца сканируется с помощью электронного луча, сжатого магнитными линзами до размера порядка 5 нм. После взаимодействия луча с поверхностью электроны рассеиваются и попадают на детектор, регистрирующий сигнал и преобразующий его в изображение поверхности.
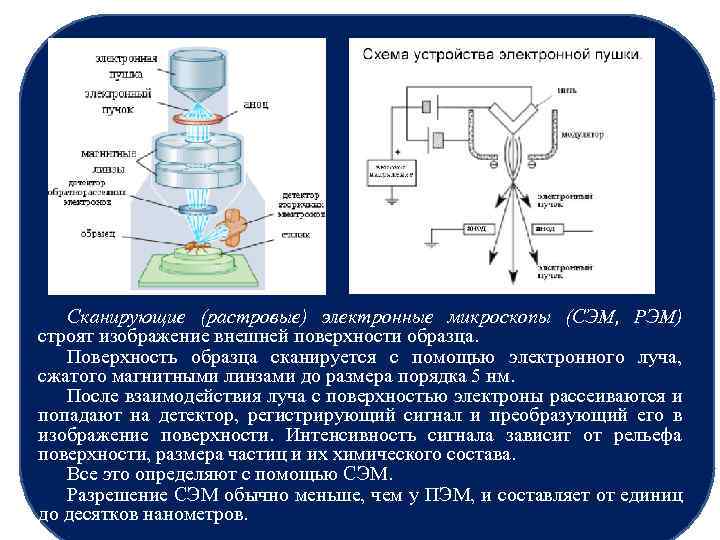
Сканирующие (растровые) электронные микроскопы (СЭМ, РЭМ) строят изображение внешней поверхности образца. Поверхность образца сканируется с помощью электронного луча, сжатого магнитными линзами до размера порядка 5 нм. После взаимодействия луча с поверхностью электроны рассеиваются и попадают на детектор, регистрирующий сигнал и преобразующий его в изображение поверхности. Интенсивность сигнала зависит от рельефа поверхности, размера частиц и их химического состава. Все это определяют с помощью СЭМ. Разрешение СЭМ обычно меньше, чем у ПЭМ, и составляет от единиц до десятков нанометров.

а) в) б) Рисунок – микрофотографии с помощью СЭМ: а) поверхность оксида цинка, осажденного на золотой подложке; б) разрыв кровеносного сосуда, видны гладкая эндотелиальная выстилка сосуда и несколько эритроцитов; в) поверхность дигидрофосфата калия.

Все микрофотографии черно-белые, они не способны передавать цвет. Исследователи часто сами придают им ту или иную окраску. В пространстве, через которое проходит электронный пучок в микроскопе, создают вакуум, т. к. электроны поглощаются молекулами, входящими в состав воздуха. Образец также помещают в отсек, из которого откачивают воздух специальным насосом.

Электронный микроскоп – очень дорогое оборудование и доступен лишь крупным исследовательским лабораториям. Существуют и другие виды сканирующих устройств – сканирующие зондовые микроскопы (СЗМ). Построение изображения СЗМ основано на сканировании поверхности зондом. СЗМ позволяет получить трёхмерное изображение поверхности (топографию) с высоким разрешением.
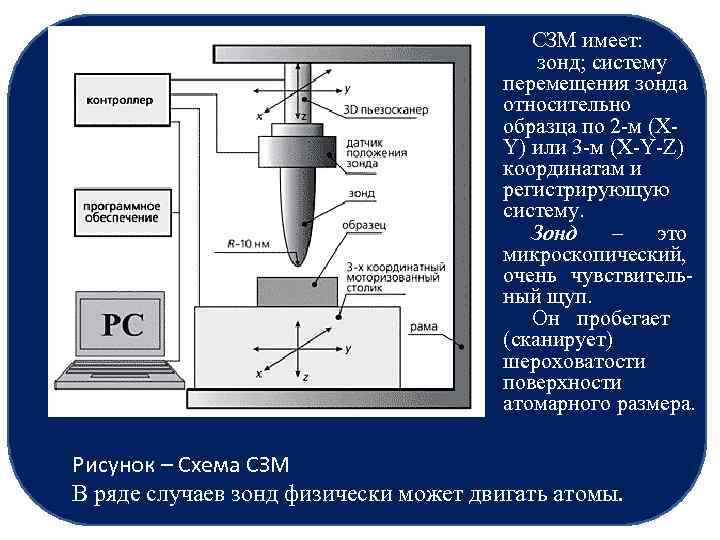
СЗМ имеет: зонд; систему перемещения зонда относительно образца по 2 -м (XY) или 3 -м (X-Y-Z) координатам и регистрирующую систему. Зонд – это микроскопический, очень чувствительный щуп. Он пробегает (сканирует) шероховатости поверхности атомарного размера. Рисунок – Схема СЗМ В ряде случаев зонд физически может двигать атомы.

Регистрирующая система фиксирует значение функции, зависящей от расстояния зонд-образец. Регистрируемое значение обрабатывается системой, которая управляет положением образца или зонда по одной из координат (Z). Основой всех типов сканирующей зондовой микроскопии является взаимодействие зонда с исследуемой поверхностью за счет механических, электрических или магнитных сил. Природа взаимодействия и определяет принадлежность прибора к тому или иному семейству зондовых микроскопов. Основные типы СЗМ: Сканирующий туннельный микроскоп (СТМ); Сканирующий атомно-силовой микроскоп (АСМ); Ближнепольный оптический микроскоп (БОМ).
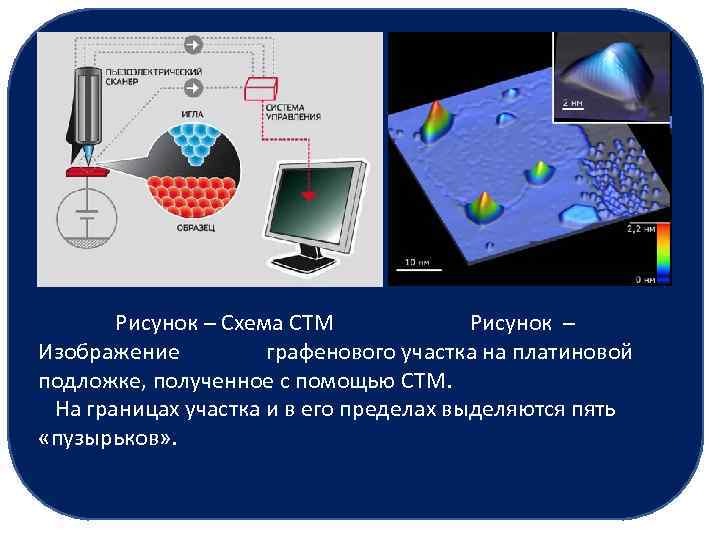
Рисунок – Схема СТМ Рисунок – Изображение графенового участка на платиновой подложке, полученное с помощью СТМ. На границах участка и в его пределах выделяются пять «пузырьков» .

СТМ имеет миниатюрный зонд – тончайшую иглу из золота , которая скользит по поверхности образца. Конец иглы состоит всего из одного атома! Он приближается к образцу на расстояние около 1 нм. На поверхности иглы возникает небольшой положительный заряд, и электроны с поверхности образца переходят на зонд. Явление беспрепятственного прохождения частиц через потенциальный барьер называют туннельным эффектом.

Зонд сканирует поверхность, перемещаясь вдоль поверхности образца на постоянной высоте. При этом фиксируют изменение потока электронов через зонд (величины туннельного тока), который преобразуют в изображение поверхности. В другом методе кончик зонда перемещают вдоль поверхности образца так, чтобы туннельный ток был постоянным, а фиксируют изменение расстояния от зонда до поверхности. Траектория движения острия зонда отображает поверхность образца. .
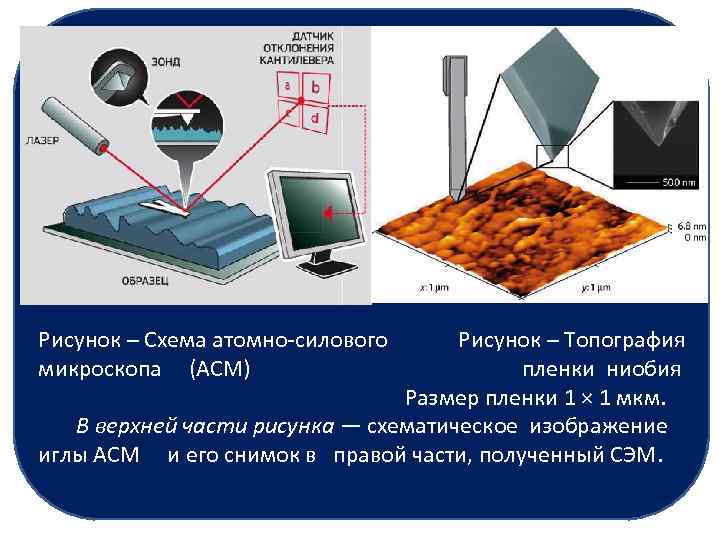
Рисунок – Схема атомно-силового Рисунок – Топография микроскопа (АСМ) пленки ниобия Размер пленки 1 × 1 мкм. В верхней части рисунка — схематическое изображение иглы АСМ и его снимок в правой части, полученный СЭМ.

Принцип действия АСМ аналогичен СТМ. Вместо туннельного тока измеряют силу отталкивания зонда от поверхности образца. В качестве зонда используется наноразмерное остриё, располагающееся на конце упругой консоли - кантилевера. Сила, действующая на зонд со стороны поверхности, приводит к изгибу кантилевера с помощью оптической системы, выполненной по схеме оптического рычага (схема на след. слайде). Регистрируя величину изгиба, можно сделать вывод о рельефе поверхности.
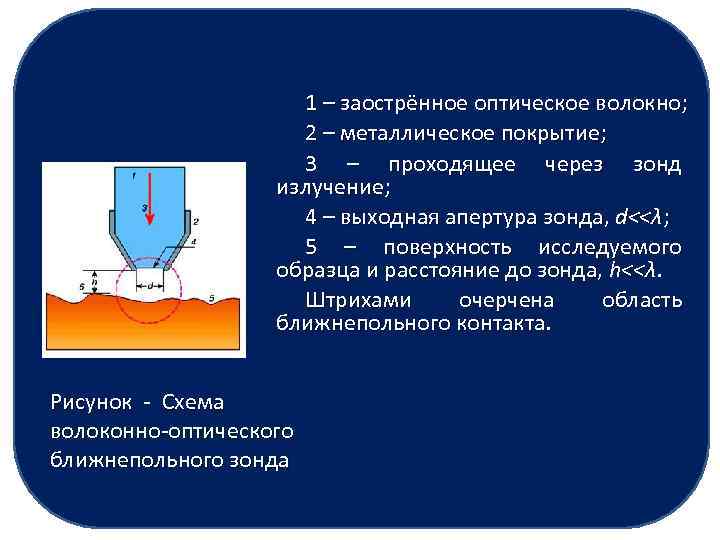
1 – заострённое оптическое волокно; 2 – металлическое покрытие; 3 – проходящее через зонд излучение; 4 – выходная апертура зонда, d<<λ; 5 – поверхность исследуемого образца и расстояние до зонда, h<<λ. Штрихами очерчена область ближнепольного контакта. Рисунок - Схема волоконно-оптического ближнепольного зонда

Кантилевер - массивное прямоугольное основание с размерами 1, 5 х. З, 5 х. О, 5 мм и выступающей из него балкой (собственно кантилевер) шириной до 0, 03 мм и длиной порядка 0, 1— 0, 5 мм. Одна из сторон балки зеркальная. Это позволяет использовать оптическую систему, контролирующую изгиб кантилевера. На противоположном свободном конце балки находится игла, взаимодействующая с измеряемым образцом. Вся конструкция, кроме иглы, — кремниевый монокристалл. Схематическое изображение и электронная микрофотография типичного кантилевера с зондом
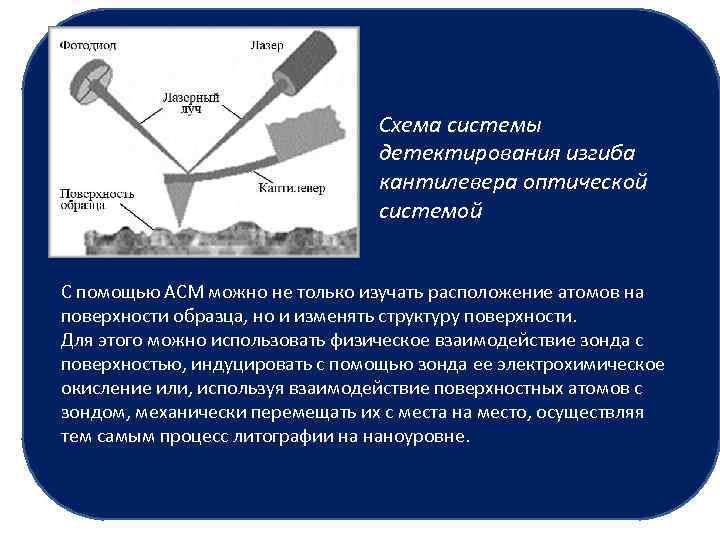
Схема системы детектирования изгиба кантилевера оптической системой C помощью АСМ можно не только изучать расположение атомов на поверхности образца, но и изменять структуру поверхности. Для этого можно использовать физическое взаимодействие зонда с поверхностью, индуцировать с помощью зонда ее электрохимическое окисление или, используя взаимодействие поверхностных атомов с зондом, механически перемещать их с места на место, осуществляя тем самым процесс литографии на наноуровне.

Cамый простой режим работы АСМ - измерение нанорельефа поверхности при перемещении образца под зондом по заданной траектории. В отличие от СЭМ, АСМ не требует сверхвысокого вакуума, он может работать в обычной воздушной или даже жидкой среде, что позволяет изучать биологические объекты. Но по скорости сканирования АСМ значительно уступают СЭМ. C помощью АСМ можно не только изучать расположение атомов на поверхности образца, но и изменять саму структуру поверхности, используя физическое взаимодействие зонда с поверхностью, проводя с помощью зонда ее электрохимическое окисление или, используя взаимодействие поверхностных атомов с зондом, механически перемещать их с места на место, осуществляя процесс литографии на АСМ-изображение наноуровне. поверхности графита Размер изображения (2× 2) нм 2

Пример АСМ-нанолитографии. Размер изображения (7, 7× 4, 8) нм 2 В 2005 г. ученые из Японии, используя сверхвысоковакуумный АСМ, построили изображение химического символа олова, состоящее из 120 атомов этого элемента, нанесенных на поверхность германия (рисунок). Изображение получено при комнатной температуре.

Другая модификация зондового микроскопа - ближнепольный оптический микроскоп (БОМ). Он имеет оптический зонд - заостренное оптическое волокно, наружная поверхность которого, за исключением вершины конуса, покрыта непрозрачным слоем металла. Кроме микроскопии для исследования нанообъектов используют и другие физические методы: -рассеяние рентгеновских лучей, - спектроскопия, - масс-спектрометрия. -Различные методы хорошо дополняют друга. Таким образом, в настоящее время существует возможность детально описывать реальную структуру наночастиц с высоким пространственным разрешением.

В нашей стране создано учебное оборудование для преподавания основ нанотехнологии. Разработан научноучебный комплекс , который включает базовый СЗМ, учебное пособие и апробированный лабораторный практикум с набором учебных образцов для микроскопических исследований. Это – учебный класс для обучения основам нанотехнологий. Микроскоп позволяет проводить как АСМ-, так и СТМ- измерения таких объектов, как ДНК, накопители нформации (CD, DVD и матрицы для их изготовления), микро- и наноструктуры, оптоэлектронные элементы и др.

Вопросы 1 Какие основные способы получения наночастиц вы знаете? 2 Чем отличаются физическое и химическое осаждение из газовой фазы? 3 Нанокластеры молибдена получают химическим осаждением из газовой фазы, используя в качестве прекурсора карбонил молибдена Mo(CO)6. Напишите уравнение реакции, происходящей в газовой фазе. 4 Предложите эксперимент по внедрению наночастиц серебра в нанотрубки из оксида титана. 5 Предположите, какие соединения можно использовать в качестве прекурсоров для химического осаждения из газовой фазы наночастиц золота и серебра. 6 На чем основан принцип действия электронного микроскопа? 7 Опишите, как работает сканирующий туннельный микроскоп. 8 Почему образец, исследуемый при помощи электронного микроскопа, не может находиться на воздухе? 9 Каковы преимущества и недостатки атомно-силовой микроскопии по сравнению со сканирующей электронной микроскопией? 10 Изучите рис. 16. Считая, что маленькая светлая точка изображает один атом олова, оцените, сколько атомов входит в состав больших точек, формирующих буквы символа Sn?

Контрольная работа № 1 Вариант 1 Вариант 2 1)Объясните значение терминов: кластер, наночастица, нанотрубка, квантовая точка, нанопроволока. 2)Почему окраска коллоидных растворов золота, содержащих наночастицы, отличается от цвета обычного металла? 3) К какому типу кластеров относится частица Au 55? 4) В чём сходство и отличие воды, полученной плавлением льда, и воды, образующейся при конденсации пара? 5) Сферическая наночастица золота имеет радиус1, 5 нм. Радиус атома золота -0, 15 нм. Сколько атомов золота содержится в наночастице? 1)Чем отличаются физические методы получения наночастиц от химических? 2) Объясните смысл понятия «размерный эффект» . В каких свойствах он проявляется? 3) Нанопорошок меди , в отличие от медной проволоки, быстро растворяется в кислоте HI. Как это можно объяснить? 4) Приведите примеры нанообъектов размерностью 3, 2, 1, 0. 5) Определите число атомов золота, содержащихся в 1 м 3 и в 1 нм 3. 1 м 3 золота весит 19, 3 т. Атомная масса Au -197.

ЛЕКЦИЯ 4 Нанотехнология

Понятие о нанотехнологии претерпело несколько изменений. Впервые термин «нанотехнология» употребил в 1974 г. японский инженер Норио Танигучи как «технологию производства, позволяющую достигать сверхвысокую точность и ультрамалые размеры. . . порядка 1 нм» . В 1980 -1990 гг. после работ Дрекслера нанотехнологией стали называть создание различных устройств из отдельных молекул. Под нанотехнологией понимали область науки.

Более близким к истине стало определение нанотехнологии, данное А. Франксом в 1987 г. : «Нанотехнология – это производство с размерами и точностями в области 0, 1– 100 нм» . Это проявилось в развитии микроэлектроники: с субнанометровой точностью (менее 100 нм) производятся микросхемы и микроэлектромеханические устройства. Таким образом, термин «нанотехнология» означает практическое применение объектов наномира.

Существует четкое определение нанотехнологии: – это совокупность методов и приемов, применяемых при изучении, проектировании, производстве и использовании структур, устройств и систем, включающих целенаправленный контроль и модификацию формы, размера, интеграции и взаимодействия составляющих их наномасштабных элементов (1– 100 нм) для получения объектов с новыми химическими, физическими, биологическими свойствами. Ключевой в этом определении является последняя часть, подчеркивающая, что основная задача нанотехнологий – получение объектов с новыми свойствами.

В определении несколько ключевых выражений: 1) Определен масштаб наноэлементов – от 1 до 100 нм (хотя бы в одном измерении). 2) Наноэлементы должны обусловливать новые свойства по сравнению с объектами, состоящими из макрофазы вещества такого же состава. 3) Определение отражает междисциплинарный характер нанотехнологии – в ее развитии участвуют все ключевые естественные науки, а также математика и информационные технологии.

Все существующие технологии, и «нано» – не исключение, основаны на достижениях фундаментальной науки. Цели нанотехнологии – проектирование, производство и использование наноструктур. Основная цель нанотехнологии, как и любой другой технологии, – производство товара и получение прибавочной стоимости, поэтому состояние и развитие нанотехнологии определяются рыночными механизмами. В контексте нанотехнологий часто употребляют слово «инновация» , означающее научное открытие, доведенное до уровня практического использования.

Слово «инновация» означает научное открытие, доведенное до уровня практического использования. Инновационный путь включает ряд этапов: - фундаментальные исследования; - прикладные исследования; - опытное производство; - промышленное производство; - товар. Рынок. Нанотехнология охватывает все этапы этой цепочки, объединяя в себе научную, производственную и экономическую стороны деятельности.

Какие же достижения нанонауки уже нашли свое применение или обещают это сделать в ближайшем будущем? Вот несколько примеров достижений нанонауки, нашедших своё применение. Механические наноустройства Одну из научных основ нанотехнологии составляет наномеханика, исследующая механические свойства наносистем. Для управления свойствами наномира надо овладеть, в первую очередь, механическим движением и научиться контролировать перемещения отдельных наночастиц – поступательные или вращательные. К числу самых интересных проблем наномеханики относится создание наномоторов – устройств, способных превращать тепловую, электрическую или световую энергию в движение.

Другое название этих устройств – актюаторы (от англ. act – действовать). Такие моторы существуют и в природе – с их помощью перемещаются некоторые бактерии. К клетке бактерии прикреплен миниатюрный жгутик, колебания которого и приводят микроорганизм в движение. «Вал»
Нано-Лекция 2-3.pptx