Органическая химия (1).pptx
- Количество слайдов: 64
 Начала органической химии
Начала органической химии
 Предмет органической химии Органическая химия изучает соединения углерода, называемые органическими веществами. В связи с этим органическую химию называют также химией соединений углерода. Органическая химия может быть определена также как химия углеводородов и их производных.
Предмет органической химии Органическая химия изучает соединения углерода, называемые органическими веществами. В связи с этим органическую химию называют также химией соединений углерода. Органическая химия может быть определена также как химия углеводородов и их производных.
 Теория А. М. Бутлерова (предпосылки возникновения) Насущные задачи органической химии требовали разрешения основного вопроса: являются ли молекулы беспорядочным нагромождением атомов, удерживаемых силами притяжения, или они представляют собой частицы с определенным строением, которое можно установить, исследуя свойства вещества. Решающую роль сыграло открытие валентности элементов. Исследуя состав металлоорганических соединений, Франкланд (1853) нашел, что каждый металл дает соединения со строго определенным числом радикалов; это число и представляет собой валентность данного металла. Так, были получены следующие соединения: CH 3 Na (CH 3)2 Hg (СН 3)3 Аl (CH 3)4 Sn метилнатрий диметилртуть триметилалюминий тетраметилолово
Теория А. М. Бутлерова (предпосылки возникновения) Насущные задачи органической химии требовали разрешения основного вопроса: являются ли молекулы беспорядочным нагромождением атомов, удерживаемых силами притяжения, или они представляют собой частицы с определенным строением, которое можно установить, исследуя свойства вещества. Решающую роль сыграло открытие валентности элементов. Исследуя состав металлоорганических соединений, Франкланд (1853) нашел, что каждый металл дает соединения со строго определенным числом радикалов; это число и представляет собой валентность данного металла. Так, были получены следующие соединения: CH 3 Na (CH 3)2 Hg (СН 3)3 Аl (CH 3)4 Sn метилнатрий диметилртуть триметилалюминий тетраметилолово
 Теория А. М. Бутлерова (предпосылки возникновения) Стало ясно, что атомы могут соединяться в молекулы только в отношениях, определяемых валентностью атомов. В частности, было установлено, что углерод четырехвалентен (Кекуле, 1858). Открытие валентности непосредственно подводило к мысли, что молекулы имеют определенное строение. Оставался открытым вопрос, как определять строение молекулы. Этот вопрос не мог быть решен без подлинно научной теории органической химии, которая и была создана А. М. Бутлеровым.
Теория А. М. Бутлерова (предпосылки возникновения) Стало ясно, что атомы могут соединяться в молекулы только в отношениях, определяемых валентностью атомов. В частности, было установлено, что углерод четырехвалентен (Кекуле, 1858). Открытие валентности непосредственно подводило к мысли, что молекулы имеют определенное строение. Оставался открытым вопрос, как определять строение молекулы. Этот вопрос не мог быть решен без подлинно научной теории органической химии, которая и была создана А. М. Бутлеровым.
 Теория химического строения Александра Михайловича Бутлерова (1861) Основные положения и следствия теории строения Бутлерова могут быть кратко сформулированы следующим образом. 1. В молекулах соединений существует определенный порядок связи атомов, который и носит название строения. 2. Химические свойства соединения определяются составом и строением его молекул. 3. Различное строение при одном и том же составе и молекулярной массе вещества обусловливает явление изомерии. 4. Так как при отдельных реакциях изменяются не все, а только некоторые части молекул, то, изучая продукты химических превращений соединения, можно установить его строение. 5. Химический характер (т. е. реакционная способность) атомов, входящих в молекулу, меняется в зависимости от того, с какими атомами они связаны в данной молекуле. Это изменение химического характера обусловливается главным образом взаимным влиянием непосредственно связанных друг с другом атомов. Взаимное влияние атомов, не связанных непосредственно, обычно проявляется значительно слабее.
Теория химического строения Александра Михайловича Бутлерова (1861) Основные положения и следствия теории строения Бутлерова могут быть кратко сформулированы следующим образом. 1. В молекулах соединений существует определенный порядок связи атомов, который и носит название строения. 2. Химические свойства соединения определяются составом и строением его молекул. 3. Различное строение при одном и том же составе и молекулярной массе вещества обусловливает явление изомерии. 4. Так как при отдельных реакциях изменяются не все, а только некоторые части молекул, то, изучая продукты химических превращений соединения, можно установить его строение. 5. Химический характер (т. е. реакционная способность) атомов, входящих в молекулу, меняется в зависимости от того, с какими атомами они связаны в данной молекуле. Это изменение химического характера обусловливается главным образом взаимным влиянием непосредственно связанных друг с другом атомов. Взаимное влияние атомов, не связанных непосредственно, обычно проявляется значительно слабее.
 Алканы Предельными углеводородами (алканами, алифатическими углеводородами) называются соединения, состоящие из атомов углерода и водорода, соединенных между собой только одинарными связями, и не содержащие циклов. Общая формула Сn. H 2 n+2
Алканы Предельными углеводородами (алканами, алифатическими углеводородами) называются соединения, состоящие из атомов углерода и водорода, соединенных между собой только одинарными связями, и не содержащие циклов. Общая формула Сn. H 2 n+2
 Алканы Простейшим соединением этого класса является метан (СН 4) — углеводород, содержащий один атом углерода и четыре атома водорода Этан (С 2 H 6) — предельный углеводород с двумя атомами углерода с формальных позиций как бы образован из метана: разорвана одна из эквивалентных связей С—Н и вместо разрыва вставлена группа —СН 2— Точно так же из этана может быть образован предельный углеводород с тремя атомами углерода — пропан (C 3 H 8)и т. д.
Алканы Простейшим соединением этого класса является метан (СН 4) — углеводород, содержащий один атом углерода и четыре атома водорода Этан (С 2 H 6) — предельный углеводород с двумя атомами углерода с формальных позиций как бы образован из метана: разорвана одна из эквивалентных связей С—Н и вместо разрыва вставлена группа —СН 2— Точно так же из этана может быть образован предельный углеводород с тремя атомами углерода — пропан (C 3 H 8)и т. д.
 Алканы. Понятие о гомологическом ряде Ряд сходных по строению соединений, обладающих близкими химическими свойствами, в котором отдельные члены ряда отличаются друг от друга лишь числом групп —СН 2—, называется гомологическим рядом. Соединения, образующие гомологический ряд называются гомологами Формула, отражающая соотношение между атомами углерода и водорода у членов ряда называется общей формулой гомологического ряда. Любое из соединений гомологического ряда алканов с неразветвленной углеродной цепью, состоит из n групп —СН 2— и еще двух атомов водорода у концевых групп. Таким образом, на n атомов углерода в ней приходится (2 n + 2) атомов водорода. Общая формула Сn. H 2 n+2
Алканы. Понятие о гомологическом ряде Ряд сходных по строению соединений, обладающих близкими химическими свойствами, в котором отдельные члены ряда отличаются друг от друга лишь числом групп —СН 2—, называется гомологическим рядом. Соединения, образующие гомологический ряд называются гомологами Формула, отражающая соотношение между атомами углерода и водорода у членов ряда называется общей формулой гомологического ряда. Любое из соединений гомологического ряда алканов с неразветвленной углеродной цепью, состоит из n групп —СН 2— и еще двух атомов водорода у концевых групп. Таким образом, на n атомов углерода в ней приходится (2 n + 2) атомов водорода. Общая формула Сn. H 2 n+2
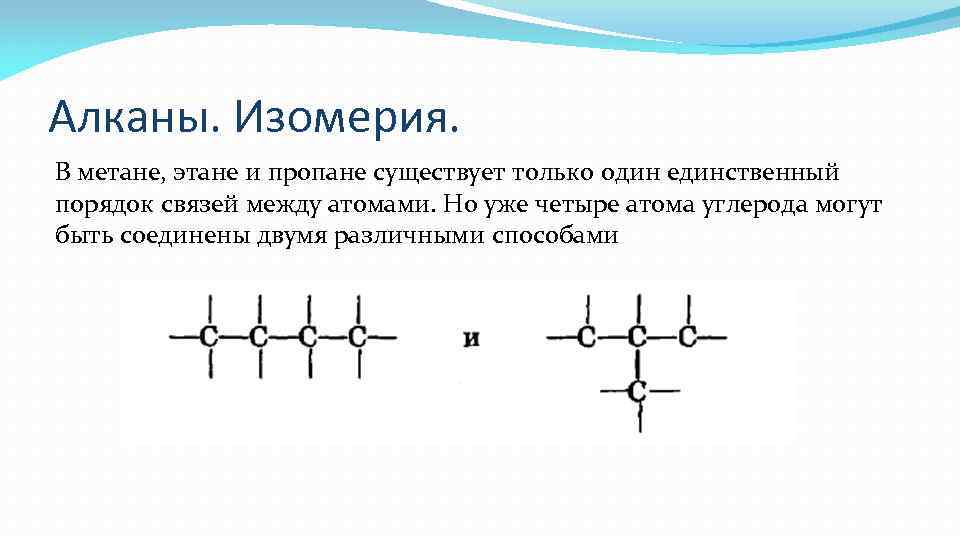 Алканы. Изомерия. В метане, этане и пропане существует только один единственный порядок связей между атомами. Но уже четыре атома углерода могут быть соединены двумя различными способами
Алканы. Изомерия. В метане, этане и пропане существует только один единственный порядок связей между атомами. Но уже четыре атома углерода могут быть соединены двумя различными способами
 Алканы. Изомерия. В обоих случаях углеводороды имеют одну и ту же молекулярную формулу С 4 Н 10. Однако в первом случае все четыре атома углерода образуют неразветвленную, или нормальную, цепь, а во втором — разветвленную на конце, или цепь изо-строения. Это разные вещества: бутан и изобутан, которые имеют раз личные физическиеконстанты. n-бутан изобутан Для углеводорода С 5 Н 12 существуют уже три изомера.
Алканы. Изомерия. В обоих случаях углеводороды имеют одну и ту же молекулярную формулу С 4 Н 10. Однако в первом случае все четыре атома углерода образуют неразветвленную, или нормальную, цепь, а во втором — разветвленную на конце, или цепь изо-строения. Это разные вещества: бутан и изобутан, которые имеют раз личные физическиеконстанты. n-бутан изобутан Для углеводорода С 5 Н 12 существуют уже три изомера.
 Алканы. Номенклатура ИЮПАК (IUPAC). По номенклатуре ИЮПАК названия предельных углеводородов характеризуются суффиксом -ан.
Алканы. Номенклатура ИЮПАК (IUPAC). По номенклатуре ИЮПАК названия предельных углеводородов характеризуются суффиксом -ан.
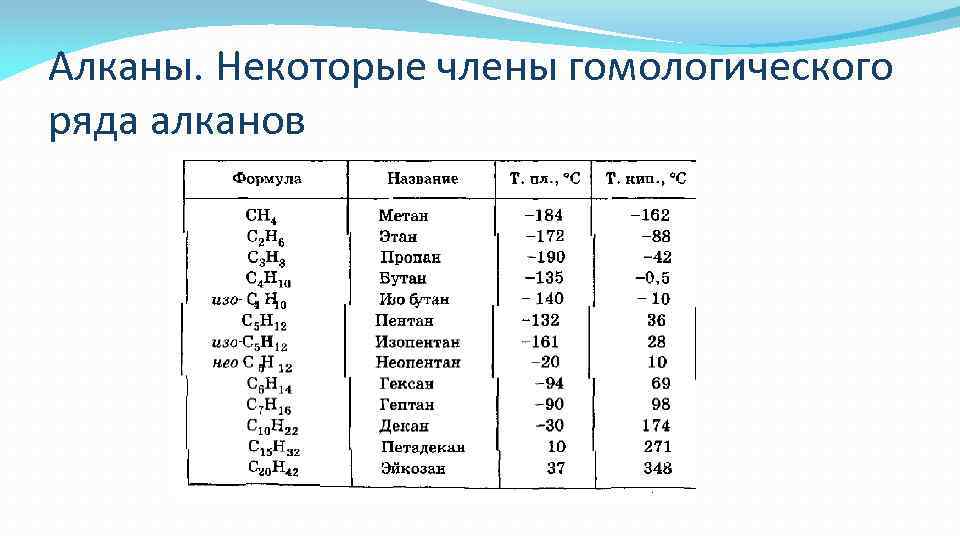 Алканы. Некоторые члены гомологического ряда алканов
Алканы. Некоторые члены гомологического ряда алканов
 Номенклатура ИЮПАК Названия предельных углеводородов с разветвленными цепями строятся следующим образом. 1. За основу названия данного соединения берут название углеводорода, соответствующее числу углеродных атомов главной цепи. Главной цепью углеродных атомов считают: 1) самую длинную; 2) самую сложную (с максимальным числом разветвлений). Если в углеводороде можно выделить две или несколько одинаково длинных цепей, то за главную выбирают ту из них, которая имеет наибольшее число разветвлений:
Номенклатура ИЮПАК Названия предельных углеводородов с разветвленными цепями строятся следующим образом. 1. За основу названия данного соединения берут название углеводорода, соответствующее числу углеродных атомов главной цепи. Главной цепью углеродных атомов считают: 1) самую длинную; 2) самую сложную (с максимальным числом разветвлений). Если в углеводороде можно выделить две или несколько одинаково длинных цепей, то за главную выбирают ту из них, которая имеет наибольшее число разветвлений:
 Номенклатура ИЮПАК 2. После установления главной цепи необходимо перенумеровать углеродные атомы. Нумерацию начинают с того конца цепи, к которому ближе примыкает любой из алкилов. Если разные алкилы находятся на равном расстоянии от обоих концов цепи, то нумерацию определяет алкил по алфавитному признаку. Например:
Номенклатура ИЮПАК 2. После установления главной цепи необходимо перенумеровать углеродные атомы. Нумерацию начинают с того конца цепи, к которому ближе примыкает любой из алкилов. Если разные алкилы находятся на равном расстоянии от обоих концов цепи, то нумерацию определяет алкил по алфавитному признаку. Например:
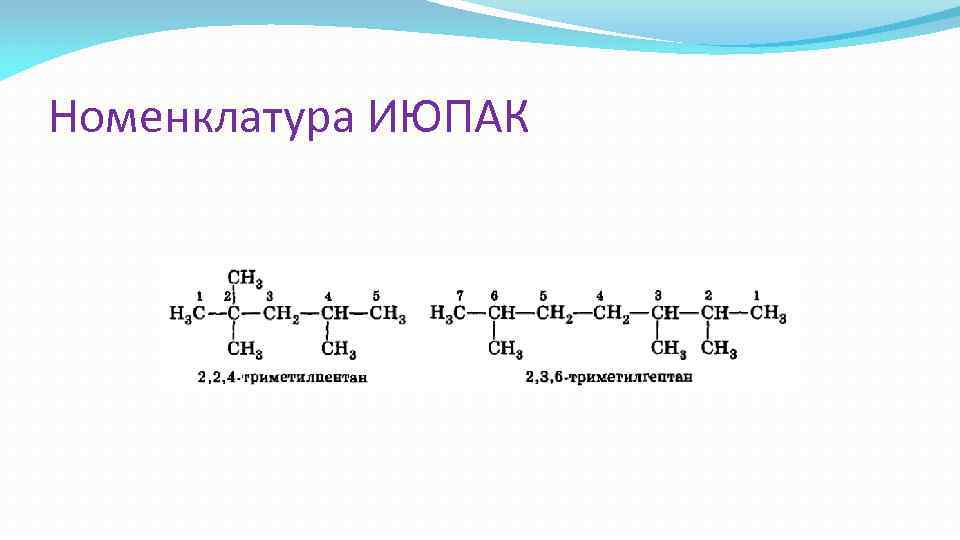 Номенклатура ИЮПАК
Номенклатура ИЮПАК
 Номенклатура ИЮПАК Называя соединение, сначала перечисляют заместители в алфавитном порядке , причем перед названием радикала ставят цифру, соответствующую номеру углеродного атома главной цепи, при котором находится данный радикал. После этого называют углеводород, соответствующий главной цепи углеродных атомов, отделяя слово от цифр дефисом. Если углеводород содержит несколько одинаковых радикалов, то число их обозначают греческим числительным (ди, три, тетра и т. д. ) и ставят перед названием этих радикалов, а их положение указывают, как обычно, цифрами, причем цифры разделяют запятыми, располагают в порядке их возрастания и ставят перед названием данных радикалов, отделяя их от него дефисом.
Номенклатура ИЮПАК Называя соединение, сначала перечисляют заместители в алфавитном порядке , причем перед названием радикала ставят цифру, соответствующую номеру углеродного атома главной цепи, при котором находится данный радикал. После этого называют углеводород, соответствующий главной цепи углеродных атомов, отделяя слово от цифр дефисом. Если углеводород содержит несколько одинаковых радикалов, то число их обозначают греческим числительным (ди, три, тетра и т. д. ) и ставят перед названием этих радикалов, а их положение указывают, как обычно, цифрами, причем цифры разделяют запятыми, располагают в порядке их возрастания и ставят перед названием данных радикалов, отделяя их от него дефисом.
 Источники предельных углеводородов Главным природным источником предельных углеводородов является нефть. Состав нефти различается в зависимости от месторождения, однако все нефти простой перегонке обычно разделяют на следующие фракции: газовая фракция бензин лигроин керосин газойль смазочные масла парафин (воск) мазут гудрон
Источники предельных углеводородов Главным природным источником предельных углеводородов является нефть. Состав нефти различается в зависимости от месторождения, однако все нефти простой перегонке обычно разделяют на следующие фракции: газовая фракция бензин лигроин керосин газойль смазочные масла парафин (воск) мазут гудрон
 Непредельные углеводороды Углеводороды, в молекуле которых помимо простых одинарных связей «углерод — углерод» и «углерод — водород» имеются углеродные двойные связи, называются непредельными. Так как образование двойной связи формально эквивалентно потере моле кулой двух атомов водорода, то непредельные углеводороды содержат на 2 п атомов водорода меньше, чем предельные: Ряд, члены которого отличаются друг от друга на (2 Н)n, называется изологическим рядом. Так, в приведенной выше схеме изологами являются гексаны, гексены, гексадиены, гек сины, гексатриены и т. д.
Непредельные углеводороды Углеводороды, в молекуле которых помимо простых одинарных связей «углерод — углерод» и «углерод — водород» имеются углеродные двойные связи, называются непредельными. Так как образование двойной связи формально эквивалентно потере моле кулой двух атомов водорода, то непредельные углеводороды содержат на 2 п атомов водорода меньше, чем предельные: Ряд, члены которого отличаются друг от друга на (2 Н)n, называется изологическим рядом. Так, в приведенной выше схеме изологами являются гексаны, гексены, гексадиены, гек сины, гексатриены и т. д.
 Алкены Углеводороды, содержащие одну двойную связь, называются алкенами (олефинами) или, по первому члену ряда — этилену, этиленовыми углеводородами. Общая формула их гомологического ряда Сп. Н 2 п.
Алкены Углеводороды, содержащие одну двойную связь, называются алкенами (олефинами) или, по первому члену ряда — этилену, этиленовыми углеводородами. Общая формула их гомологического ряда Сп. Н 2 п.
 Алкены. Номенклатура ИЮПАК. По номенклатуре ИЮПАК названия предельных углеводородов характеризуются суффиксом -ен. С 2 H 4 (CH 2=CH 2) – этен (этилен); С 3 H 6 (CH 2=CH CH 3) – пропен (пропилен); С 4 H 8 (CH 2=CH CH 2 СH 3) – бутен (бутилен); С 4 H 8 (CH 2=CH CH 2) – изобутен (изобутилен); СH 3
Алкены. Номенклатура ИЮПАК. По номенклатуре ИЮПАК названия предельных углеводородов характеризуются суффиксом -ен. С 2 H 4 (CH 2=CH 2) – этен (этилен); С 3 H 6 (CH 2=CH CH 3) – пропен (пропилен); С 4 H 8 (CH 2=CH CH 2 СH 3) – бутен (бутилен); С 4 H 8 (CH 2=CH CH 2) – изобутен (изобутилен); СH 3
 Алкены. Номенклатура. В соответствии с правилами ИЮПАК при построении назва ний алкенов наиболее длинная углеродная цепь, содержащая двойную связь, получает название соответствующего алкана, в котором окончание -ан заменено на -ен. Эта цепь нумеруется таким образом, чтобы углеродные атомы, участвующие в образовании двойной связи, получили номера, наименьшие из возможных:
Алкены. Номенклатура. В соответствии с правилами ИЮПАК при построении назва ний алкенов наиболее длинная углеродная цепь, содержащая двойную связь, получает название соответствующего алкана, в котором окончание -ан заменено на -ен. Эта цепь нумеруется таким образом, чтобы углеродные атомы, участвующие в образовании двойной связи, получили номера, наименьшие из возможных:
 Алкены. Изомерия. Помимо изомерии углеродного скелета, в ряду алкенов по является еще и изомерия положения двойной связи. В общем виде изомерия такого типа — изомерия положения заместителя (функции) – наблюдается во всех случаях, когда в молекуле имеются какие-либо функциональные группы. Для алканы С 4 Н 10 возможны два структурных изомера. Для алкена С 4 Н 8 (бутена) возможны три изомера:
Алкены. Изомерия. Помимо изомерии углеродного скелета, в ряду алкенов по является еще и изомерия положения двойной связи. В общем виде изомерия такого типа — изомерия положения заместителя (функции) – наблюдается во всех случаях, когда в молекуле имеются какие-либо функциональные группы. Для алканы С 4 Н 10 возможны два структурных изомера. Для алкена С 4 Н 8 (бутена) возможны три изомера:
 Алкины. Алкинами называются углеводороды, содержащие кроме одинарных связей тройную связь у одной пары углеродных ато мов. Общая формула гомологического ряда ацетиленовых уг леводородов. Сn. Н 2 n _ 2 Гомологический ряд алкинов начинает ацетилен С 2 H 2: СН СН
Алкины. Алкинами называются углеводороды, содержащие кроме одинарных связей тройную связь у одной пары углеродных ато мов. Общая формула гомологического ряда ацетиленовых уг леводородов. Сn. Н 2 n _ 2 Гомологический ряд алкинов начинает ацетилен С 2 H 2: СН СН
 Алкины. Номенклатура. Согласно номенклатуре ИЮПАК, при построении названий алкинов в названиях соответствующих полностью насыщенных углеводородов окончание –ан заменяют окончанием –ин. Для указания положения тройной связи цепь нумеруют так же, как в соответствующих алкенах:
Алкины. Номенклатура. Согласно номенклатуре ИЮПАК, при построении названий алкинов в названиях соответствующих полностью насыщенных углеводородов окончание –ан заменяют окончанием –ин. Для указания положения тройной связи цепь нумеруют так же, как в соответствующих алкенах:
 Диены Из названия класса видно, что молекула диена должна содержать две двойные связи. Следовательно, общая формула гомологического ряда диеновых углеводородов будет такая же, как и для ряда ацетилена: Сп. Н 2 n _ 2. По взаимному расположению двойных связей и химическим свойствам диены делятся на три группы. 1. Диены с соседним положением двойных связей называют диенами с алленовыми или кумулированными связями. Эти соединения мало устойчивы и легко перегруппировываются в алкины. Их простейший представитель — аллен СН 2=С=СН 2. 2. Диены, у которых двойные связи разделены более чем одной простой связью, называются диенами с изолированными связями. Их реакции ничем не отличаются от реакций алкенов, но в реакции могут вступать одна или две связи. Простейшим представителем данного соединения является диаллил Н 2 С=СН—СН 2—СН=СН 2. 3. Диены с 1, 3 положением двойных связей (двойные связи разделены одной простой связью) несколько отличаются по свойствам от алкенов и настолько важны с практической точки зрения, что это послужило причиной выделения их в отдельную группу. Диены с таким расположением двойных связей называют диенами с сопряженными связями. Обычно, когда речь идет просто о диенах, подразумеваются всегда именно 1, 3 диены. Наличие двух или более двойных связей обозначают суф фиксами-диен, -триен и т. д. , все двойные связи должны входить в главную цепь. Общие родовые названия углеводородов (разветвленых и неразветвленных) с двумя, тремя двойными связями и т. д. – алкадиены, алкатриены и т. д. Цепи нумеруются так, чтобы положение двойных связей обозначалось наименьшими номерами:
Диены Из названия класса видно, что молекула диена должна содержать две двойные связи. Следовательно, общая формула гомологического ряда диеновых углеводородов будет такая же, как и для ряда ацетилена: Сп. Н 2 n _ 2. По взаимному расположению двойных связей и химическим свойствам диены делятся на три группы. 1. Диены с соседним положением двойных связей называют диенами с алленовыми или кумулированными связями. Эти соединения мало устойчивы и легко перегруппировываются в алкины. Их простейший представитель — аллен СН 2=С=СН 2. 2. Диены, у которых двойные связи разделены более чем одной простой связью, называются диенами с изолированными связями. Их реакции ничем не отличаются от реакций алкенов, но в реакции могут вступать одна или две связи. Простейшим представителем данного соединения является диаллил Н 2 С=СН—СН 2—СН=СН 2. 3. Диены с 1, 3 положением двойных связей (двойные связи разделены одной простой связью) несколько отличаются по свойствам от алкенов и настолько важны с практической точки зрения, что это послужило причиной выделения их в отдельную группу. Диены с таким расположением двойных связей называют диенами с сопряженными связями. Обычно, когда речь идет просто о диенах, подразумеваются всегда именно 1, 3 диены. Наличие двух или более двойных связей обозначают суф фиксами-диен, -триен и т. д. , все двойные связи должны входить в главную цепь. Общие родовые названия углеводородов (разветвленых и неразветвленных) с двумя, тремя двойными связями и т. д. – алкадиены, алкатриены и т. д. Цепи нумеруются так, чтобы положение двойных связей обозначалось наименьшими номерами:
 Сырье для синтетического каучука Наиболее важными с практической точки зрения являются бутадиен 1, 3. Н 2 С=СН—СН=СН 2 – бутадиен 1, 3; и изопрен (2 метилбутадиен 1, 3) : СН 2=С(СН 3) СН=СН 2 Изопрен является мономером натурального каучука и синтетических каучуков.
Сырье для синтетического каучука Наиболее важными с практической точки зрения являются бутадиен 1, 3. Н 2 С=СН—СН=СН 2 – бутадиен 1, 3; и изопрен (2 метилбутадиен 1, 3) : СН 2=С(СН 3) СН=СН 2 Изопрен является мономером натурального каучука и синтетических каучуков.
 Арены (ароматические углеводороды Циклические углеводороды с сопряженными (чередующимися с одинарными)двойными связями называются ароматическими углеводородами (аренами). Первые представители класса ароматических углеводородов (аренов), выделенные из природных объектов, обладали свое образным запахом и получили название «ароматических» . Однако сегодня в понятие «ароматический углеводород» вкла дывают совсем другой смысл.
Арены (ароматические углеводороды Циклические углеводороды с сопряженными (чередующимися с одинарными)двойными связями называются ароматическими углеводородами (аренами). Первые представители класса ароматических углеводородов (аренов), выделенные из природных объектов, обладали свое образным запахом и получили название «ароматических» . Однако сегодня в понятие «ароматический углеводород» вкла дывают совсем другой смысл.
 Арены Под ароматичностью понимают способность некоторых не предельных соединений легко вступать в реакции замещения, а не присоединения и устойчивость к действию окислителей, температуры и т. п. Это понятие сформировалось в результате изучения свойств соединений ряда бензола, в частности угле водородов состава. Сn. Н 2 n-6, которые, несмотря на формальную ненасыщенность, легко вступают в реакции замещения и устойчивы по отношению к окислителям. Важнейшим представителем ароматических углеводоро дов является бензол С 6 Н 6. Молекула бензола состоит из шести атомов углерода и шести атомов водорода, образующих шести членный цикл. Молекулу бензола принято изображать сле дующей формулой (Кекуле, 1865 ).
Арены Под ароматичностью понимают способность некоторых не предельных соединений легко вступать в реакции замещения, а не присоединения и устойчивость к действию окислителей, температуры и т. п. Это понятие сформировалось в результате изучения свойств соединений ряда бензола, в частности угле водородов состава. Сn. Н 2 n-6, которые, несмотря на формальную ненасыщенность, легко вступают в реакции замещения и устойчивы по отношению к окислителям. Важнейшим представителем ароматических углеводоро дов является бензол С 6 Н 6. Молекула бензола состоит из шести атомов углерода и шести атомов водорода, образующих шести членный цикл. Молекулу бензола принято изображать сле дующей формулой (Кекуле, 1865 ).
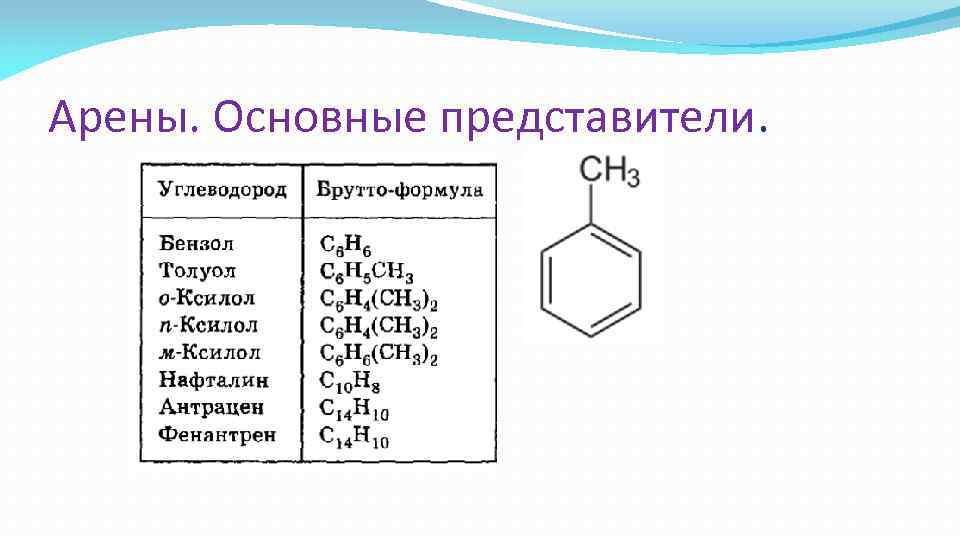 Арены. Основные представители.
Арены. Основные представители.
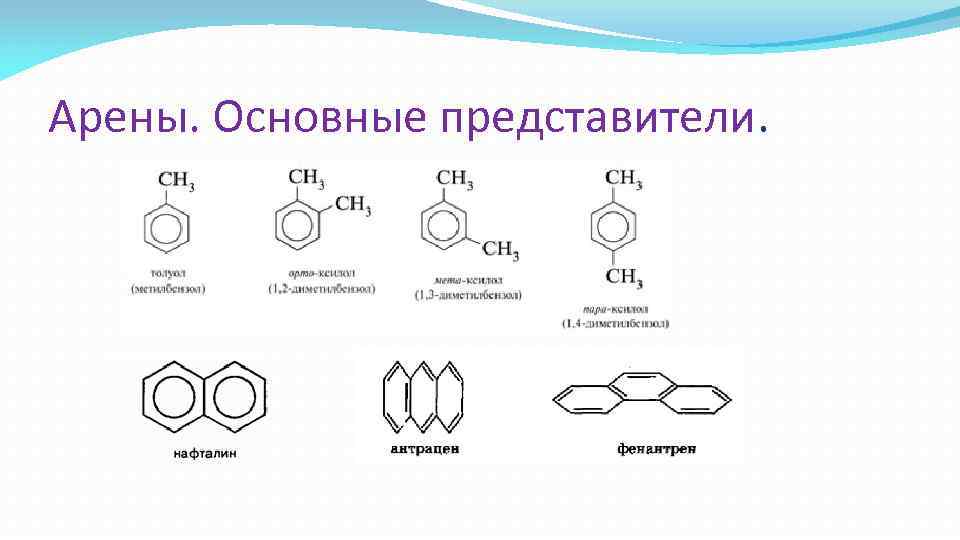 Арены. Основные представители.
Арены. Основные представители.
 Алициклические углеводороды Углеводороды, в которых углеродные цепи образуют циклы, не обладающие ароматическим характером, относятся к классу алициклических (т. е. алифатических циклических) углеводородов.
Алициклические углеводороды Углеводороды, в которых углеродные цепи образуют циклы, не обладающие ароматическим характером, относятся к классу алициклических (т. е. алифатических циклических) углеводородов.
 Алициклические углеводороды Их состав выражается формулой Сn. Н 2 n, той же, что и углеводородов ряда этилена, однако это предельные углеводороды, их углеродные атомы связаны лишь простыми одинарными связями. По номенклатуре ИЮПАК их называют циклоалканами.
Алициклические углеводороды Их состав выражается формулой Сn. Н 2 n, той же, что и углеводородов ряда этилена, однако это предельные углеводороды, их углеродные атомы связаны лишь простыми одинарными связями. По номенклатуре ИЮПАК их называют циклоалканами.
 Алициклические углеводороды Названия циклоалканов образуют добавлением префикса цикло- к названию соответствующего ациклического неразветвленного углеводорода с тем же числом углеродных атомов. Если в цикле имеются кратные связи, углеводород относят соответствующему классу. Например:
Алициклические углеводороды Названия циклоалканов образуют добавлением префикса цикло- к названию соответствующего ациклического неразветвленного углеводорода с тем же числом углеродных атомов. Если в цикле имеются кратные связи, углеводород относят соответствующему классу. Например:
 Алициклические углеводороды Заместители нумеруются в соответствии с их положением в цикле таким образом, чтобы сумма номеров была минимальной
Алициклические углеводороды Заместители нумеруются в соответствии с их положением в цикле таким образом, чтобы сумма номеров была минимальной
 Галогенпроизводные углеводородов Галогенопроизводными углеводородов называются органические соединения, образующиеся при замене атомов водорода в углеводородах на атомы галогенов. В зависимости от числа атомов водорода, замещенных галогеном, различают моно , ди , тригалогенопроизводные и т. д. например:
Галогенпроизводные углеводородов Галогенопроизводными углеводородов называются органические соединения, образующиеся при замене атомов водорода в углеводородах на атомы галогенов. В зависимости от числа атомов водорода, замещенных галогеном, различают моно , ди , тригалогенопроизводные и т. д. например:
 Галогенпроизводные углеводородов. Изомерия и номенклатура. Моногалогенопроизводные предельных углеводородов называются алкилгалогенидами: их состав можно выразить общей формулой Сn. Н 2 n + X, где X может быть F, Cl, Вr, I. В молекулах метана и этана все атомы водорода по положению равноценны. Поэтому замещение атома водорода в метане и этане каким либо галогеном, например иодом, дает только галогенопроизводное:
Галогенпроизводные углеводородов. Изомерия и номенклатура. Моногалогенопроизводные предельных углеводородов называются алкилгалогенидами: их состав можно выразить общей формулой Сn. Н 2 n + X, где X может быть F, Cl, Вr, I. В молекулах метана и этана все атомы водорода по положению равноценны. Поэтому замещение атома водорода в метане и этане каким либо галогеном, например иодом, дает только галогенопроизводное:
 Галогенпроизводные углеводородов. Изомерия и номенклатура. Но уже из пропана СН 3—СН 2—СН 3, замещая водород галогеном, можно получить два изомерных галогенопроизводных: Названия простейших моногалогенопроизводных часто производят от названий соответствующих одновалентных радикалов (алкилов) Сn. Н 2 n + 1, прибавляя к названию радикала слова: хлористый, бромистый и т. д. Так, СН 3 Сl называется хлористым метилом или метилхлоридом, С 2 Н 5 I— этилиодидом или йодистым этилом. Галогенопроизводные, у которых все имевшиеся в молекулах атомы водорода замещены на галоген, называются пергалогенопроизводными
Галогенпроизводные углеводородов. Изомерия и номенклатура. Но уже из пропана СН 3—СН 2—СН 3, замещая водород галогеном, можно получить два изомерных галогенопроизводных: Названия простейших моногалогенопроизводных часто производят от названий соответствующих одновалентных радикалов (алкилов) Сn. Н 2 n + 1, прибавляя к названию радикала слова: хлористый, бромистый и т. д. Так, СН 3 Сl называется хлористым метилом или метилхлоридом, С 2 Н 5 I— этилиодидом или йодистым этилом. Галогенопроизводные, у которых все имевшиеся в молекулах атомы водорода замещены на галоген, называются пергалогенопроизводными
 Спирты. Спиртами называются производные углеводородов, содержащие группу (или несколько групп) —ОН, называемую гидроксильной группой или гидроксилом. По числу гидроксильных групп, содержащихся в молекуле, спирты делятся на одноатомные (с одним гидроксилом), двухатомные (с двумя гидроксилами), трехатомные (с тремя гидроксилами) и многоатомные. Подобно предельным углеводородам, одноатомные спирты образуют закономерно построенный ряд гомологов:
Спирты. Спиртами называются производные углеводородов, содержащие группу (или несколько групп) —ОН, называемую гидроксильной группой или гидроксилом. По числу гидроксильных групп, содержащихся в молекуле, спирты делятся на одноатомные (с одним гидроксилом), двухатомные (с двумя гидроксилами), трехатомные (с тремя гидроксилами) и многоатомные. Подобно предельным углеводородам, одноатомные спирты образуют закономерно построенный ряд гомологов:
 Спирты. Как и в других гомологических рядах, каждый член ряда спиртов отличается по составу от предыдущего и последующего членов на гомологическую разность (—СН 2—). В зависимости от того, при каком атоме углерода находится гидроксил, различают первичные, вторичные и третичные спирты. В молекулах первичных спиртов содержится группа —СН 2 ОН, связанная с одним радикалом или с атомом водорода у метанола (гидроксил при первичном атоме углерода). Для вторичных спиртов характерна группа >СНОН, связанная с двумя радикалами (гидроксил при вторичном атоме углерода). В молекулах третичных спиртов имеется группа >COH, связанная с тремя радикалами (гидроксил при третичном атоме углерода). Обозначим радикал R и получим:
Спирты. Как и в других гомологических рядах, каждый член ряда спиртов отличается по составу от предыдущего и последующего членов на гомологическую разность (—СН 2—). В зависимости от того, при каком атоме углерода находится гидроксил, различают первичные, вторичные и третичные спирты. В молекулах первичных спиртов содержится группа —СН 2 ОН, связанная с одним радикалом или с атомом водорода у метанола (гидроксил при первичном атоме углерода). Для вторичных спиртов характерна группа >СНОН, связанная с двумя радикалами (гидроксил при вторичном атоме углерода). В молекулах третичных спиртов имеется группа >COH, связанная с тремя радикалами (гидроксил при третичном атоме углерода). Обозначим радикал R и получим:
 Спирты. Номенклатура. В соответствии с номенклатурой ИЮПАК при построении названия одноатомного спирта к названию родоначального углеводорода добавляется суффикс -ол. При наличии в соединении более старших функций гидроксильная группа обозначается префиксом гидрокси- (в русском языке часто используется префикс окси-), В качестве основной цепи выбирается наиболее длинная неразветвленная цепь углеродных атомов, в состав которой входит атом углерода, связанный с гидроксильной группой; если соединение является ненасыщенным, то в эту цепь включается также и кратная связь. Следует заметить, что при определении начала нумерации гидроксильная функция обычно имеет преимущество перед галогеном, двойной связью алкилом, следовательно, нумерацию начинают с того конца цепи, ближе к которому расположена гидроксильная группа:
Спирты. Номенклатура. В соответствии с номенклатурой ИЮПАК при построении названия одноатомного спирта к названию родоначального углеводорода добавляется суффикс -ол. При наличии в соединении более старших функций гидроксильная группа обозначается префиксом гидрокси- (в русском языке часто используется префикс окси-), В качестве основной цепи выбирается наиболее длинная неразветвленная цепь углеродных атомов, в состав которой входит атом углерода, связанный с гидроксильной группой; если соединение является ненасыщенным, то в эту цепь включается также и кратная связь. Следует заметить, что при определении начала нумерации гидроксильная функция обычно имеет преимущество перед галогеном, двойной связью алкилом, следовательно, нумерацию начинают с того конца цепи, ближе к которому расположена гидроксильная группа:
 Спирты. Гомологический ряд. Знать метанол , этанол, фенол
Спирты. Гомологический ряд. Знать метанол , этанол, фенол
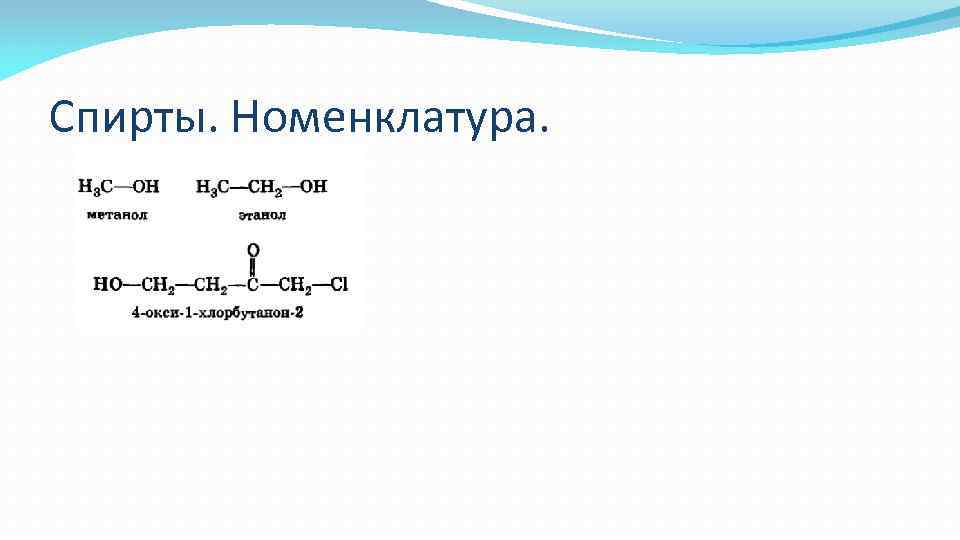 Спирты. Номенклатура.
Спирты. Номенклатура.
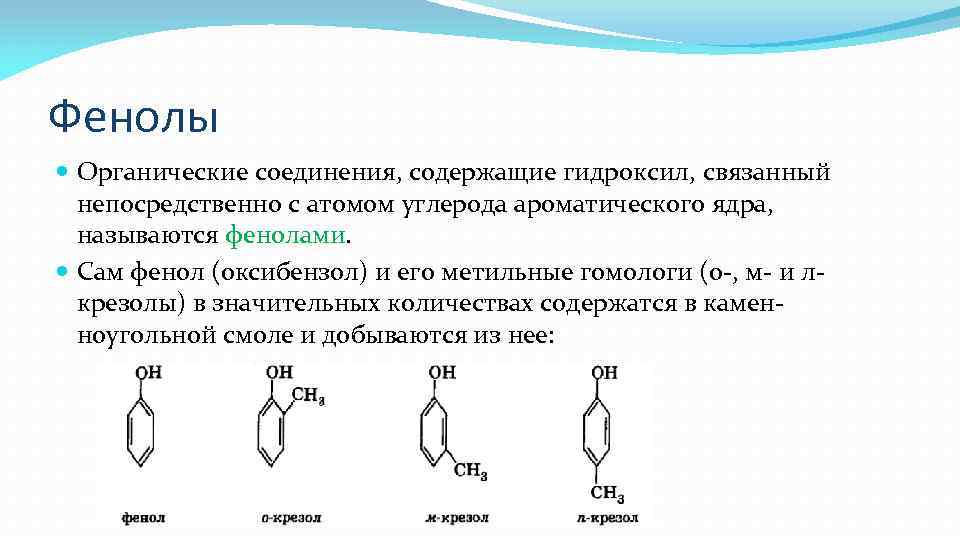 Фенолы Органические соединения, содержащие гидроксил, связанный непосредственно с атомом углерода ароматического ядра, называются фенолами. Сам фенол (оксибензол) и его метильные гомологи (о , м и л крезолы) в значительных количествах содержатся в камен ноугольной смоле и добываются из нее:
Фенолы Органические соединения, содержащие гидроксил, связанный непосредственно с атомом углерода ароматического ядра, называются фенолами. Сам фенол (оксибензол) и его метильные гомологи (о , м и л крезолы) в значительных количествах содержатся в камен ноугольной смоле и добываются из нее:
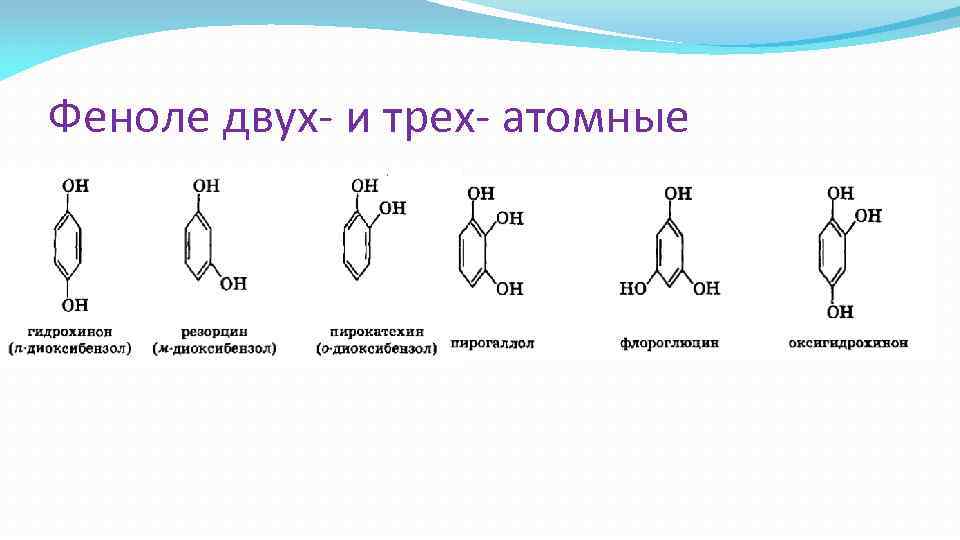 Феноле двух- и трех- атомные
Феноле двух- и трех- атомные
 Меркаптаны Сернистые аналоги спиртов называются меркаптанами (тиоспиртами, тиолами).
Меркаптаны Сернистые аналоги спиртов называются меркаптанами (тиоспиртами, тиолами).
 Эфиры представляют собой продукты замещения атома водорода гидроксильной группы спиртов или фенолов на какой либо радикал:
Эфиры представляют собой продукты замещения атома водорода гидроксильной группы спиртов или фенолов на какой либо радикал:
 Эфиры В зависимости от характера радикала R' различают три типа эфиров: 1) простые эфиры, R' — углеводородный радикал; 2) сложные эфиры неорганических кислот, R' — остаток неорганической кислородсодержащей кислоты: азотной (—NO 2), азотистой (—NO), серной (—SO 3 H) и т. п. ; 3) сложные эфиры карбоновых кислот, R' — остаток карбоновой кислоты — ацил, например СН 3 СО—, С 2 Н 5 СО— и т. д. ;
Эфиры В зависимости от характера радикала R' различают три типа эфиров: 1) простые эфиры, R' — углеводородный радикал; 2) сложные эфиры неорганических кислот, R' — остаток неорганической кислородсодержащей кислоты: азотной (—NO 2), азотистой (—NO), серной (—SO 3 H) и т. п. ; 3) сложные эфиры карбоновых кислот, R' — остаток карбоновой кислоты — ацил, например СН 3 СО—, С 2 Н 5 СО— и т. д. ;
 Простые эфиры. Номенклатура. Согласно номенклатуре ИЮПАК, простые эфиры называют двумя способами, прибавляя к названию старшего (наиболее длинного) углеводородного радикала в качестве префикса звание алкоксигруппы (R—О—) или для эфиров фенолов — арилоксигруппы (Аr—О—), например:
Простые эфиры. Номенклатура. Согласно номенклатуре ИЮПАК, простые эфиры называют двумя способами, прибавляя к названию старшего (наиболее длинного) углеводородного радикала в качестве префикса звание алкоксигруппы (R—О—) или для эфиров фенолов — арилоксигруппы (Аr—О—), например:
 Простые эфиры. Номенклатура. Простые эфиры называют также, использую название радикалов и слово эфир:
Простые эфиры. Номенклатура. Простые эфиры называют также, использую название радикалов и слово эфир:
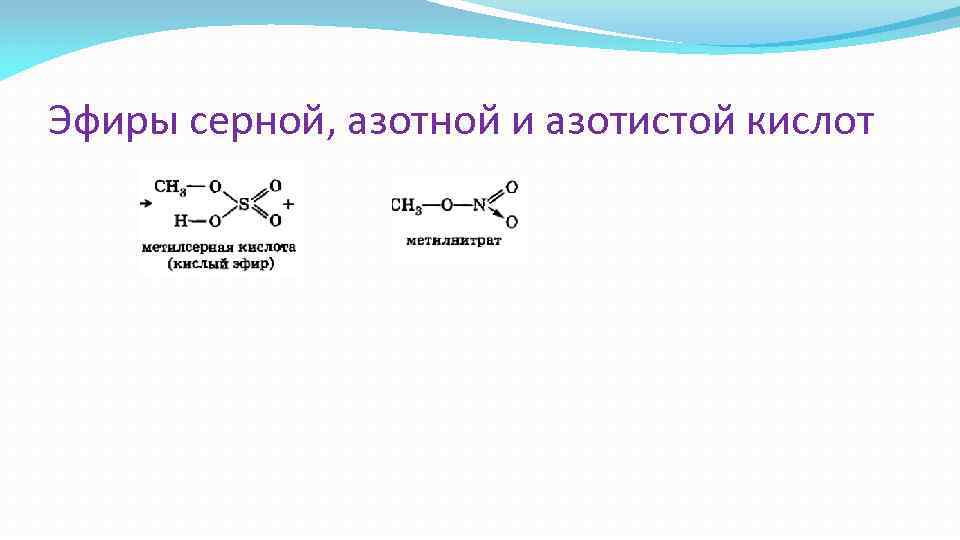 Эфиры серной, азотной и азотистой кислот
Эфиры серной, азотной и азотистой кислот
 Амины Аминами называются производные углеводородов, образованные замещением в последних атомов водорода на группы —NH 2, —NHR' или — NR'R": В зависимости от числа атомов водорода у атома азота, замещенных радикалами, амины называются первичными, вторичными или третичными. При этом не имеет значения, какие радикалы (первичные, вторичные или третичные) являются заместителями. Группа —NH 2, входящая в состав первичных аминов, называется аминогруппой. Группа >NH во вторичных аминах называется иминогруппой.
Амины Аминами называются производные углеводородов, образованные замещением в последних атомов водорода на группы —NH 2, —NHR' или — NR'R": В зависимости от числа атомов водорода у атома азота, замещенных радикалами, амины называются первичными, вторичными или третичными. При этом не имеет значения, какие радикалы (первичные, вторичные или третичные) являются заместителями. Группа —NH 2, входящая в состав первичных аминов, называется аминогруппой. Группа >NH во вторичных аминах называется иминогруппой.
 Амины Названия аминов обычно производят от названий входящих в них радикалов с присоединением окончания амин: метиламин СН 3— NH 2, диметиламин (CH 3)2 NH, триметиламин (CH 3)3 N, пропиламин CH 3 CH 2 NH 2, трет бутиламин и т. д. В более сложных случаях аминогруппу рассматривают как функциональную группу и ее название амино ставят перед названием основной цепи (ИЮПАК):
Амины Названия аминов обычно производят от названий входящих в них радикалов с присоединением окончания амин: метиламин СН 3— NH 2, диметиламин (CH 3)2 NH, триметиламин (CH 3)3 N, пропиламин CH 3 CH 2 NH 2, трет бутиламин и т. д. В более сложных случаях аминогруппу рассматривают как функциональную группу и ее название амино ставят перед названием основной цепи (ИЮПАК):
 Ароматические амины Ароматическими аминами называют амины, в которых аминогруппа связана непосредственно с ароматическим ядром. Простейшим ароматическим амином является фениламин, называемый анилином:
Ароматические амины Ароматическими аминами называют амины, в которых аминогруппа связана непосредственно с ароматическим ядром. Простейшим ароматическим амином является фениламин, называемый анилином:
 Оксосоединения: альдегиды и кетоны. К классу оксосоединений относятся органические вещества, содержащие группу >С=О, называемую карбонильной группой или карбонилом, причем две валентности атома углерода карбонила могут быть заняты алкильными радикалами — кетоны кетон или алкильным радикалом и атомом водорода — альдегиды. Кетоны и альдегиды называют также карбонильными соединениями. Реакции альдегидов и кетонов весьма похожи, что и позволяет рассматривать их в общем классе оксосоединений. Общая формула гомологического ряда предельных алифатических альдегидов и кетонов одинакова: Сn. Н 2 n. О.
Оксосоединения: альдегиды и кетоны. К классу оксосоединений относятся органические вещества, содержащие группу >С=О, называемую карбонильной группой или карбонилом, причем две валентности атома углерода карбонила могут быть заняты алкильными радикалами — кетоны кетон или алкильным радикалом и атомом водорода — альдегиды. Кетоны и альдегиды называют также карбонильными соединениями. Реакции альдегидов и кетонов весьма похожи, что и позволяет рассматривать их в общем классе оксосоединений. Общая формула гомологического ряда предельных алифатических альдегидов и кетонов одинакова: Сn. Н 2 n. О.
 Оксосоединения. Номенклатура. Тривиальные названия альдегидов очень распространены, они связаны с тривиальными наименованиями кислот с тем же углеродным скелетом, в которые альдегиды легко переходят при окислении: муравьиный альдегид (формальдегид), уксусный альдегид (ацетальдегид) см. слайд 57, пропионовый, масляный, валериановый и т. д. По номенклатуре ИЮПАК наличие альдегидной группы обозначается суффиксом -ал (-аль):
Оксосоединения. Номенклатура. Тривиальные названия альдегидов очень распространены, они связаны с тривиальными наименованиями кислот с тем же углеродным скелетом, в которые альдегиды легко переходят при окислении: муравьиный альдегид (формальдегид), уксусный альдегид (ацетальдегид) см. слайд 57, пропионовый, масляный, валериановый и т. д. По номенклатуре ИЮПАК наличие альдегидной группы обозначается суффиксом -ал (-аль):
 Оксосоединения. Номенклатура. Названия простых кетонов обычно составляются из названий радикалов, связанных с карбонильной группой, и слова кетон: Для названия более сложных кетонов используют суффикс –он (ИЮПАК): При наличии более старшей группы кетоновая группа обозначается префиксом оксо-:
Оксосоединения. Номенклатура. Названия простых кетонов обычно составляются из названий радикалов, связанных с карбонильной группой, и слова кетон: Для названия более сложных кетонов используют суффикс –он (ИЮПАК): При наличии более старшей группы кетоновая группа обозначается префиксом оксо-:
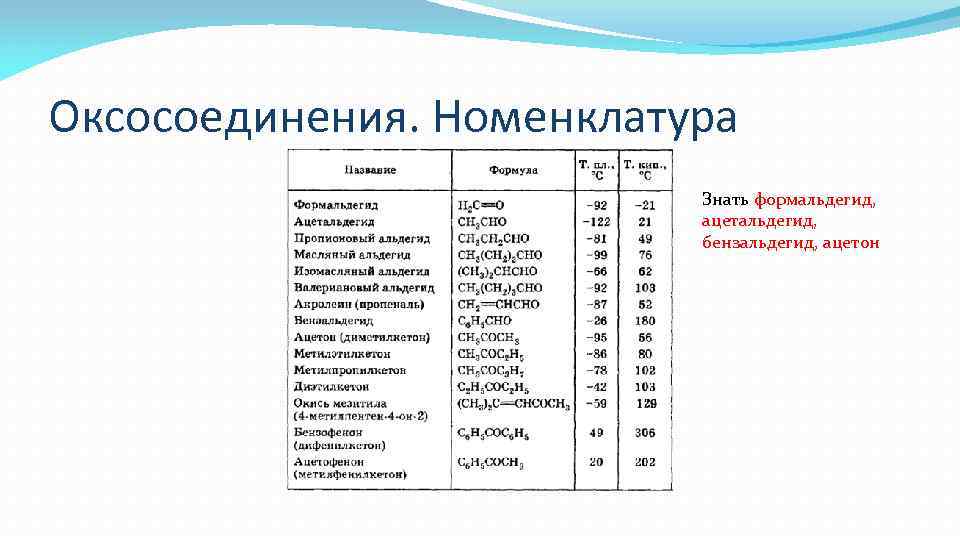 Оксосоединения. Номенклатура Знать формальдегид, ацетальдегид, бензальдегид, ацетон
Оксосоединения. Номенклатура Знать формальдегид, ацетальдегид, бензальдегид, ацетон
 Карбоновые кислоты и их производные К классу карбоновых кислот относятся соединения, содержащие карбоксильную группу Соединения, содержащие одну карбоксильную группу, называются одноосновными карбоновыми кислотами, две — двухосновными и т. д. Гомологический ряд одноосновных предельных карбоновых кислот (иногда их называют жирными кислотами) начинается с муравьиной кислоты НCООН Формула гомологического ряда кислот Сn. Н 2 n. O 2 или Cn. H 2 n+1 COOH. Номенклатура ИЮПАК разрешает сохранять для многих слот их тривиальные названия. Для более сложных случаев названия кислот производят от названия углеводородов с тем же числом атомов углерода, что и в молекуле кислоты, с добавлением окончания -овая и слова кислота. Муравьиная кислота Н—СООН называется метановой кислотой, уксусная кислота СН 3 СООН — этановой кислотой и т. д. Таким образом, кислоты рассматриваются как производные углеводородов, одно звено которых превращено в карбоксил:
Карбоновые кислоты и их производные К классу карбоновых кислот относятся соединения, содержащие карбоксильную группу Соединения, содержащие одну карбоксильную группу, называются одноосновными карбоновыми кислотами, две — двухосновными и т. д. Гомологический ряд одноосновных предельных карбоновых кислот (иногда их называют жирными кислотами) начинается с муравьиной кислоты НCООН Формула гомологического ряда кислот Сn. Н 2 n. O 2 или Cn. H 2 n+1 COOH. Номенклатура ИЮПАК разрешает сохранять для многих слот их тривиальные названия. Для более сложных случаев названия кислот производят от названия углеводородов с тем же числом атомов углерода, что и в молекуле кислоты, с добавлением окончания -овая и слова кислота. Муравьиная кислота Н—СООН называется метановой кислотой, уксусная кислота СН 3 СООН — этановой кислотой и т. д. Таким образом, кислоты рассматриваются как производные углеводородов, одно звено которых превращено в карбоксил:
 Карбоновые кислоты. Номенклатура.
Карбоновые кислоты. Номенклатура.
 Сложные эфиры карбоновых кислот. Сложным эфиром карбоновой кислоты называют продукт замещения гидроксильной группы кислоты на остаток спирта RO— Эфиры получают при обработке карбоновых кислот спиртами, как правило, в присутствии ионов водорода:
Сложные эфиры карбоновых кислот. Сложным эфиром карбоновой кислоты называют продукт замещения гидроксильной группы кислоты на остаток спирта RO— Эфиры получают при обработке карбоновых кислот спиртами, как правило, в присутствии ионов водорода:
 Галогенангидриды карбоновых кислот. Галогенангидридами карбоновых кислот называют продукт замещения гидроксильной группы на атом галогена. Галогенангидриды кислот являются активными ацилирующими агентами, т. е. соединениями, с помощью которых ацил (остаток кислоты) R—вводится в другие молекулы:
Галогенангидриды карбоновых кислот. Галогенангидридами карбоновых кислот называют продукт замещения гидроксильной группы на атом галогена. Галогенангидриды кислот являются активными ацилирующими агентами, т. е. соединениями, с помощью которых ацил (остаток кислоты) R—вводится в другие молекулы:
 Ангидриды карбоновых кислот. Хотя с формальных позиций ангидриды следует рассматривать как продукт дегидратации двух молекул кислоты, получить их таким образом можно только для некоторых двухосновных кислот. Обычно их получают действием хлорангидридов кислот на соли кислот:
Ангидриды карбоновых кислот. Хотя с формальных позиций ангидриды следует рассматривать как продукт дегидратации двух молекул кислоты, получить их таким образом можно только для некоторых двухосновных кислот. Обычно их получают действием хлорангидридов кислот на соли кислот:
 Амиды карбоновых кислот. Амидами кислот называют продукт замещения гидроксильной группы кислоты на аминогруппу или на замещенную аминогруппу. Связь азот – углерод фрагмента называют амидной связью
Амиды карбоновых кислот. Амидами кислот называют продукт замещения гидроксильной группы кислоты на аминогруппу или на замещенную аминогруппу. Связь азот – углерод фрагмента называют амидной связью
 Рефераты: Аминокислоты. Белки. Молекулы – носители генетической информации.
Рефераты: Аминокислоты. Белки. Молекулы – носители генетической информации.


