модификация НК_С5-С6_С4_лекция_7.ppt
- Количество слайдов: 33
 Модификация гетероциклических оснований нуклеиновых кислот Реакции по С(6)-С(5) связи ВЗАИМОДЕЙСТВИЕ С НУКЛЕОФИЛЬНЫМИ РЕАГЕНТАМИ И НУКЛЕОФИЛЬНЫМИ ГРУППАМИ БЕЛКОВ 1
Модификация гетероциклических оснований нуклеиновых кислот Реакции по С(6)-С(5) связи ВЗАИМОДЕЙСТВИЕ С НУКЛЕОФИЛЬНЫМИ РЕАГЕНТАМИ И НУКЛЕОФИЛЬНЫМИ ГРУППАМИ БЕЛКОВ 1
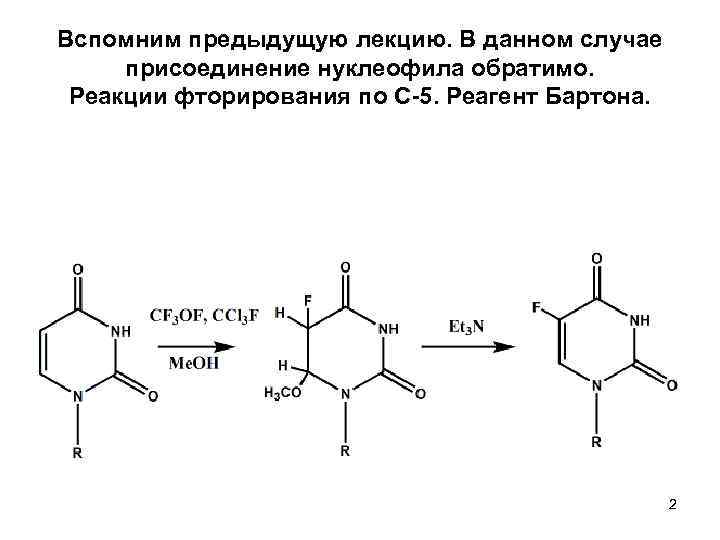 Вспомним предыдущую лекцию. В данном случае присоединение нуклеофила обратимо. Реакции фторирования по С-5. Реагент Бартона. 2
Вспомним предыдущую лекцию. В данном случае присоединение нуклеофила обратимо. Реакции фторирования по С-5. Реагент Бартона. 2
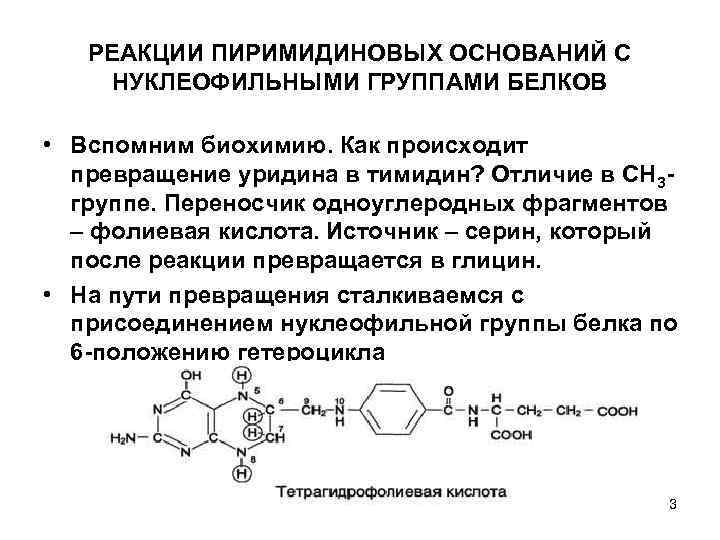 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С НУКЛЕОФИЛЬНЫМИ ГРУППАМИ БЕЛКОВ • Вспомним биохимию. Как происходит превращение уридина в тимидин? Отличие в СН 3 группе. Переносчик одноуглеродных фрагментов – фолиевая кислота. Источник – серин, который после реакции превращается в глицин. • На пути превращения сталкиваемся с присоединением нуклеофильной группы белка по 6 -положению гетероцикла 3
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С НУКЛЕОФИЛЬНЫМИ ГРУППАМИ БЕЛКОВ • Вспомним биохимию. Как происходит превращение уридина в тимидин? Отличие в СН 3 группе. Переносчик одноуглеродных фрагментов – фолиевая кислота. Источник – серин, который после реакции превращается в глицин. • На пути превращения сталкиваемся с присоединением нуклеофильной группы белка по 6 -положению гетероцикла 3
 4
4
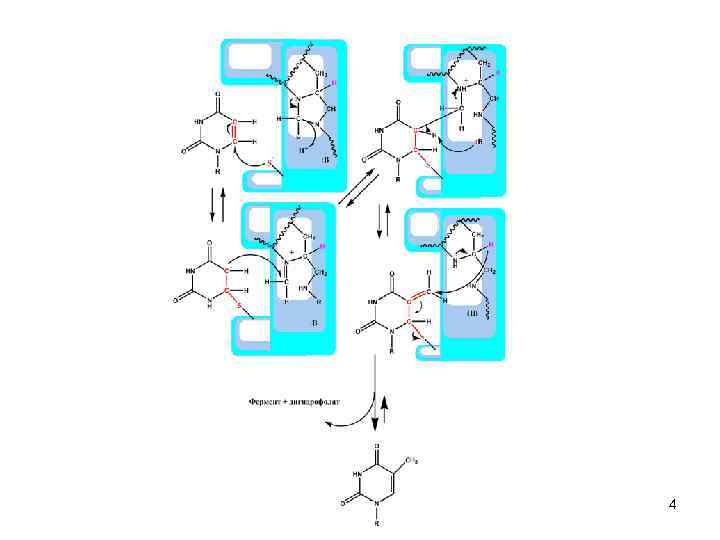
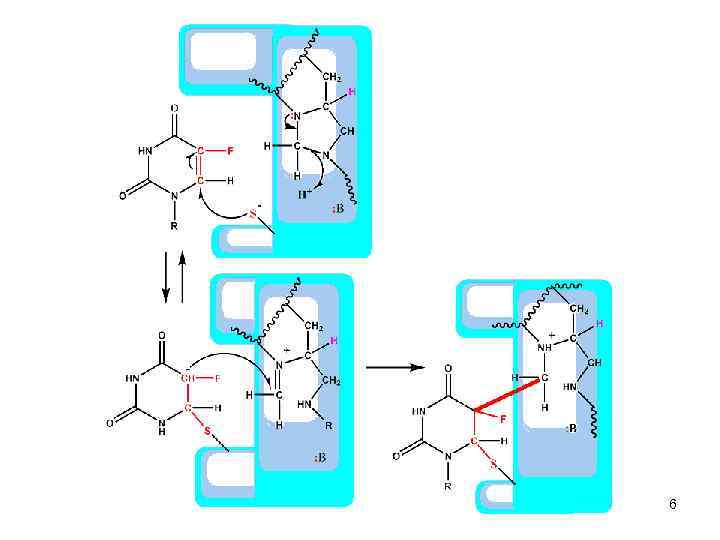
 Отличительные особенности фторпроизводных уридина • Присоединение нуклеофильной сульфгидрильной группы тимидилатсинтазы также обратимо. А что будет, если вместо дезоксиуридин-5’-монофосфата в реакционной смеси будет 5 фтордезоксиуридин-5’-монофосфат? 5
Отличительные особенности фторпроизводных уридина • Присоединение нуклеофильной сульфгидрильной группы тимидилатсинтазы также обратимо. А что будет, если вместо дезоксиуридин-5’-монофосфата в реакционной смеси будет 5 фтордезоксиуридин-5’-монофосфат? 5
 6
6
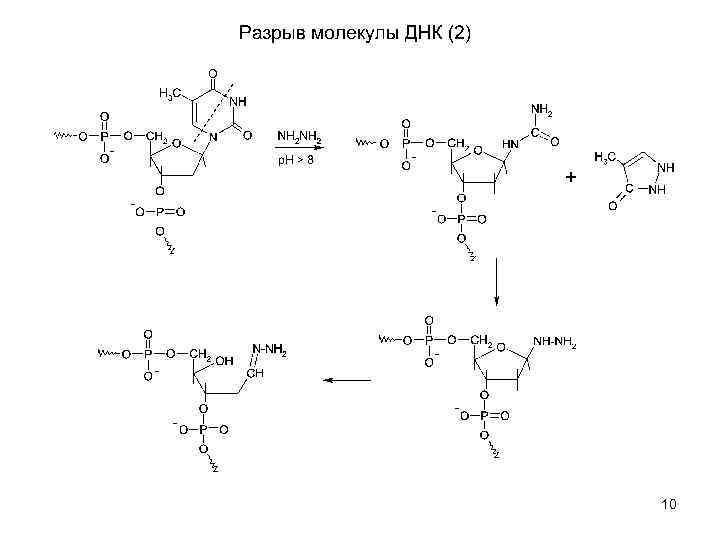
 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С ГИДРАЗИНОМ (вспоминаем метод Максама-Гилберта) • Для определения положения тимидина используется деградация по остаткам пиримидинов, для чего ДНК последовательно обрабатывается гидразином, а затем пиперидином. • Расщепление по цитозину осуществляется при высокой концентрации Na. Cl с последующей обработкой продуктов модификации пипердином. ПОЧЕМУ? • В щелочных условиях реакции с гидразином приводят к расщеплению гетероциклических колец пиримидинов, практически не затрагивая пуриновых оснований. 7
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С ГИДРАЗИНОМ (вспоминаем метод Максама-Гилберта) • Для определения положения тимидина используется деградация по остаткам пиримидинов, для чего ДНК последовательно обрабатывается гидразином, а затем пиперидином. • Расщепление по цитозину осуществляется при высокой концентрации Na. Cl с последующей обработкой продуктов модификации пипердином. ПОЧЕМУ? • В щелочных условиях реакции с гидразином приводят к расщеплению гетероциклических колец пиримидинов, практически не затрагивая пуриновых оснований. 7
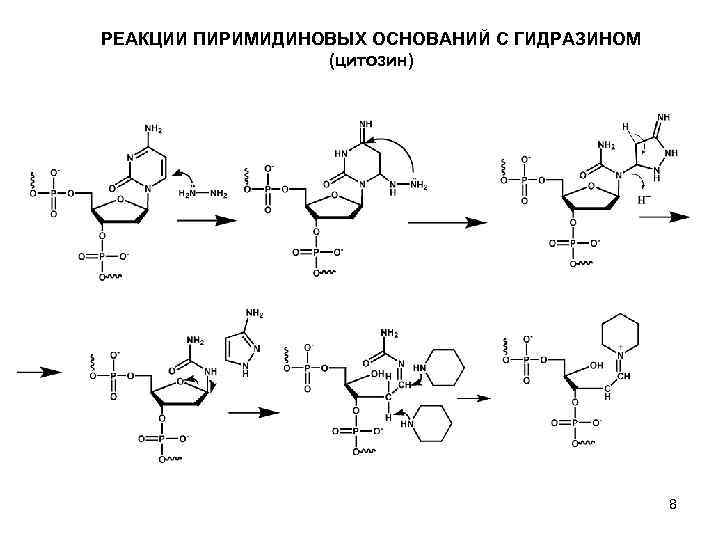 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ C ГИДРАЗИНОМ (цитозин) 8
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ C ГИДРАЗИНОМ (цитозин) 8
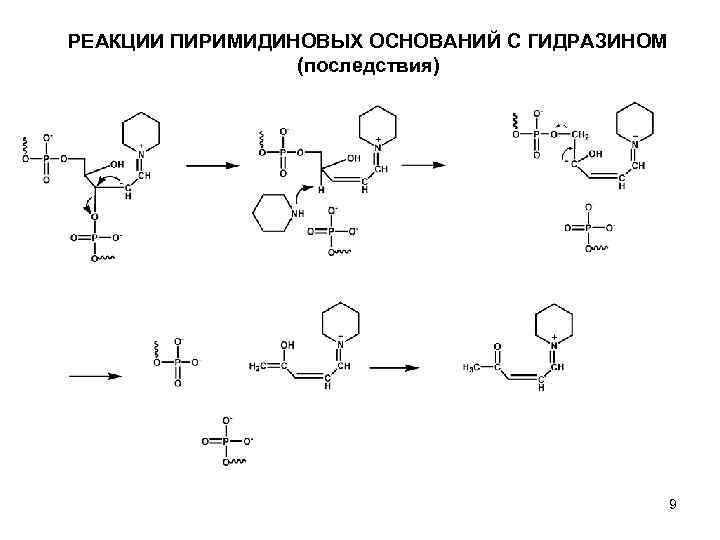 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ C ГИДРАЗИНОМ (последствия) 9
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ C ГИДРАЗИНОМ (последствия) 9
 10
10
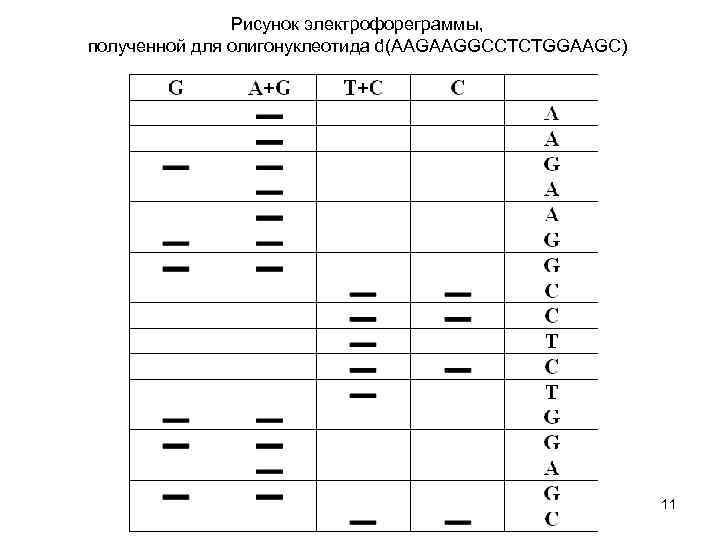 Рисунок электрофореграммы, полученной для олигонуклеотида d(AAGAAGGCCTCTGGAAGC) 11
Рисунок электрофореграммы, полученной для олигонуклеотида d(AAGAAGGCCTCTGGAAGC) 11
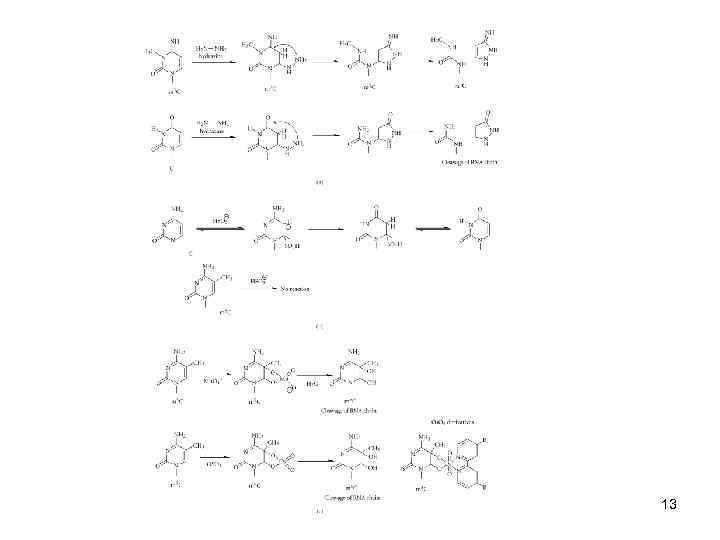
 ИДЕНТИФИКАЦИЯ МОДИФИЦИРОВАННЫХ (АЛКИЛИРОВАНЫХ) ОСТАТКОВ ЦИТОЗИНА • Реакция с Os. O 4, широко применяемая в органической химии для гидроксилирования двойных связей, гладко протекает и в случае пиримидиновых оснований. Скорость реакции возрастает в ряду Т U C, так, тимидин реагирует почти на два порядка быстрее цитидина и в 10 раз быстрее уридина. Поэтому ее можно рассматривать как специфический метод модификации тимидина. При взаимодействии с Os. O 4 образуется циклический эфир осмиевой кислоты, который легко гидролизуется до диола. Диольные соединения также образуются и при взаимодействии с Mn. O 4 и H 2 O 2. Однако в этом случае быстро происходит разрушение цикла. 12
ИДЕНТИФИКАЦИЯ МОДИФИЦИРОВАННЫХ (АЛКИЛИРОВАНЫХ) ОСТАТКОВ ЦИТОЗИНА • Реакция с Os. O 4, широко применяемая в органической химии для гидроксилирования двойных связей, гладко протекает и в случае пиримидиновых оснований. Скорость реакции возрастает в ряду Т U C, так, тимидин реагирует почти на два порядка быстрее цитидина и в 10 раз быстрее уридина. Поэтому ее можно рассматривать как специфический метод модификации тимидина. При взаимодействии с Os. O 4 образуется циклический эфир осмиевой кислоты, который легко гидролизуется до диола. Диольные соединения также образуются и при взаимодействии с Mn. O 4 и H 2 O 2. Однако в этом случае быстро происходит разрушение цикла. 12
 13
13
 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ • Бисульфит-ион способен обратимо присоединяться к С 5 -С 6 -двойным связям цитозина, урацила и тимина в мягких условиях, образуя соответствующий аддукт, неустойчивый в случае тимина; практическое значение имеют только реакции с урацилом и цитозином. Продукты присоединения к урацилу и цитозину довольно стабильны в нейтральной кислой средах, но отщепляют бисульфит-ион в щелочной среде. 14
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ • Бисульфит-ион способен обратимо присоединяться к С 5 -С 6 -двойным связям цитозина, урацила и тимина в мягких условиях, образуя соответствующий аддукт, неустойчивый в случае тимина; практическое значение имеют только реакции с урацилом и цитозином. Продукты присоединения к урацилу и цитозину довольно стабильны в нейтральной кислой средах, но отщепляют бисульфит-ион в щелочной среде. 14
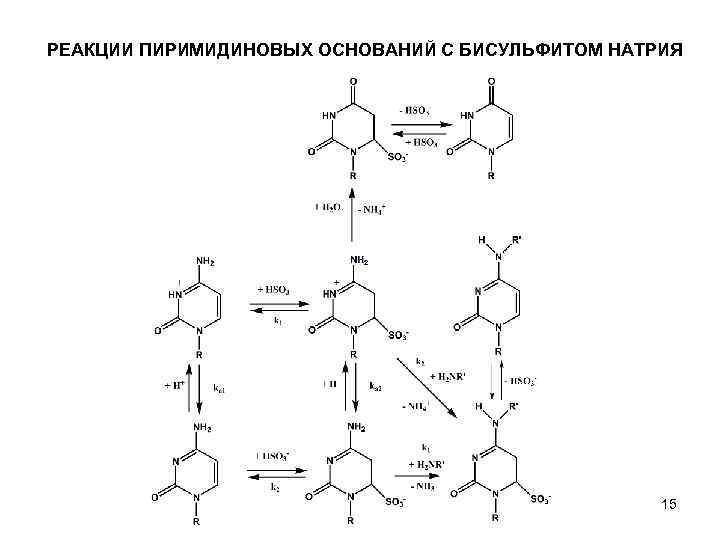 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ 15
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ 15
 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ • Важным свойством 5, 6 -дигидропроизводных цитозина является повышенная реакционноспособность аминогруппы, которая легко замещается под действием различных нуклеофильных агентов. Замещение аминогруппы на гидроксигруппу приводит к производному урацила, которое легко превращается в урацил при слабоосновных значениях р. Н. Таким образом, эта реакция дает возможность специфического преобразования цитозиновых колец в урацильные. 16
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ • Важным свойством 5, 6 -дигидропроизводных цитозина является повышенная реакционноспособность аминогруппы, которая легко замещается под действием различных нуклеофильных агентов. Замещение аминогруппы на гидроксигруппу приводит к производному урацила, которое легко превращается в урацил при слабоосновных значениях р. Н. Таким образом, эта реакция дает возможность специфического преобразования цитозиновых колец в урацильные. 16
 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ • Модификация нуклеиновых кислот бисульфитом часто используется как способ введения мутационных замен. С этой целью участок ДНК, выбранный для введения мутаций, превращают в одноцепочечный и затем обрабатывают бисульфитом в условия дезаминирования. Таким образом, например, пары G-C могут быть заменены на пары А-Т (такие замены называются транзициями). 17
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ • Модификация нуклеиновых кислот бисульфитом часто используется как способ введения мутационных замен. С этой целью участок ДНК, выбранный для введения мутаций, превращают в одноцепочечный и затем обрабатывают бисульфитом в условия дезаминирования. Таким образом, например, пары G-C могут быть заменены на пары А-Т (такие замены называются транзициями). 17
 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ • Реакция бисульфита с одноцепочечными нуклеиновыми кислотами протекает значительно медленнее, чем с мономерами. И практически не идет с двухцепочечными молекулами. • Специфичность к вторичной структуре используется для анализа пространственного строения полинуклеотида. Так, обработка т. РНК бисульфитом приводит к модификации только цитозиновых оснований, которые находятся в петлях. • Предварительная модификация цитозиновых гетероциклов бисульфитом обеспечивает возможность введения по С-4 различных группировок, напрмер остатка биотина или флуоресцеина. 18
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ • Реакция бисульфита с одноцепочечными нуклеиновыми кислотами протекает значительно медленнее, чем с мономерами. И практически не идет с двухцепочечными молекулами. • Специфичность к вторичной структуре используется для анализа пространственного строения полинуклеотида. Так, обработка т. РНК бисульфитом приводит к модификации только цитозиновых оснований, которые находятся в петлях. • Предварительная модификация цитозиновых гетероциклов бисульфитом обеспечивает возможность введения по С-4 различных группировок, напрмер остатка биотина или флуоресцеина. 18
 РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ (способ введения различных группировок по С 4 -положению цитозина) • Однако надо помнить, что выход производных цитозина уменьшается с увеличением р. Ка аминомостика. ПОЧЕМУ? • J. Molander et al. Bioconjugate Chem. 1994 19
РЕАКЦИИ ПИРИМИДИНОВЫХ ОСНОВАНИЙ С БИСУЛЬФИТОМ НАТРИЯ (способ введения различных группировок по С 4 -положению цитозина) • Однако надо помнить, что выход производных цитозина уменьшается с увеличением р. Ка аминомостика. ПОЧЕМУ? • J. Molander et al. Bioconjugate Chem. 1994 19
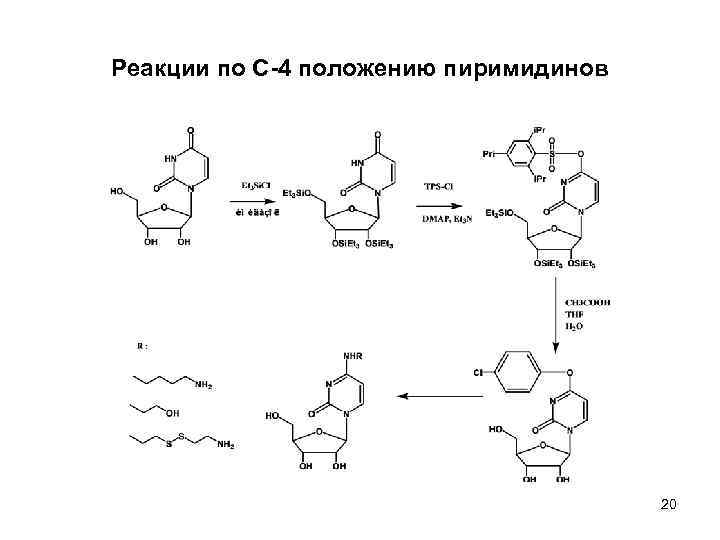 Реакции по С-4 положению пиримидинов 20
Реакции по С-4 положению пиримидинов 20
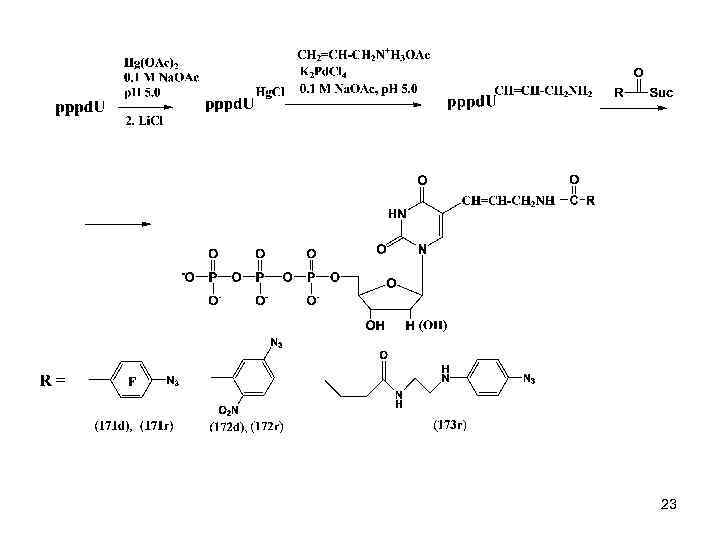
 МЕРКУРИРОВАНИЕ • Широко распространенная в органической химии реакция непредельных соединений с ацетатом ртути в случае нуклеиновых кислот проходит в мягких условиях (вода, р. Н 6. 0 -7. 0, 40 -50 0 С). Результатом реакции является образование производных 5 -ацетоксимеркуриоурацила и 5 ацетоксимеркуриоцитозина. 5 Меркуриопроизводные вследствие легкого обмена атома ртути на атомы галогена или трития используются для получения специфически меченных пиримидиновых оснований нуклеиновых кислот. 21
МЕРКУРИРОВАНИЕ • Широко распространенная в органической химии реакция непредельных соединений с ацетатом ртути в случае нуклеиновых кислот проходит в мягких условиях (вода, р. Н 6. 0 -7. 0, 40 -50 0 С). Результатом реакции является образование производных 5 -ацетоксимеркуриоурацила и 5 ацетоксимеркуриоцитозина. 5 Меркуриопроизводные вследствие легкого обмена атома ртути на атомы галогена или трития используются для получения специфически меченных пиримидиновых оснований нуклеиновых кислот. 21
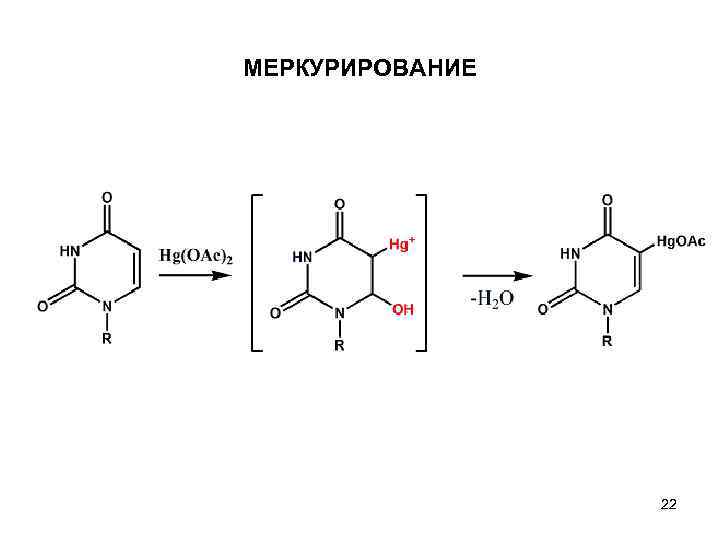 МЕРКУРИРОВАНИЕ 22
МЕРКУРИРОВАНИЕ 22
 23
23
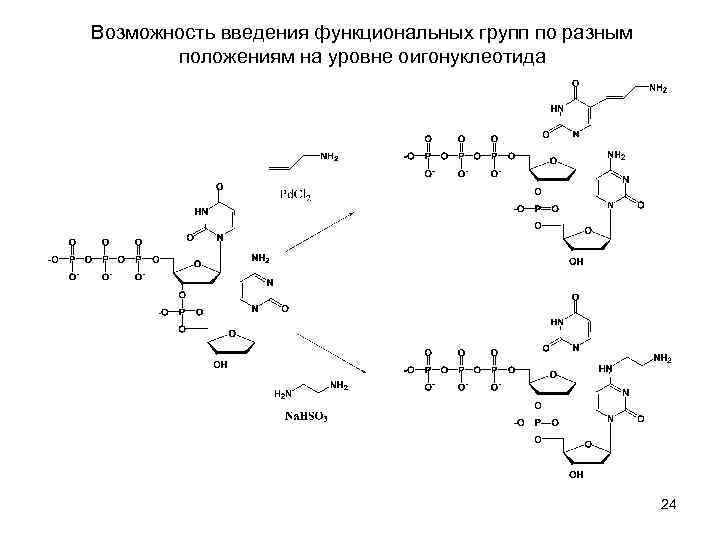 Возможность введения функциональных групп по разным положениям на уровне оигонуклеотида 24
Возможность введения функциональных групп по разным положениям на уровне оигонуклеотида 24
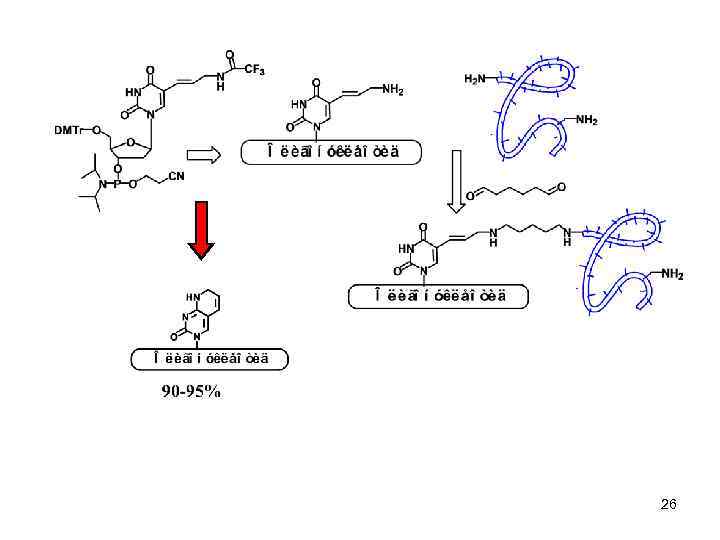
 «ПОДВОДНЫЕ КАМНИ» • При работе с аллиламином и его производными могут протекать «незапланированные» реакции по С-4 положению гетероцикла. 25
«ПОДВОДНЫЕ КАМНИ» • При работе с аллиламином и его производными могут протекать «незапланированные» реакции по С-4 положению гетероцикла. 25
 26
26
 ПРИМЕРЫ ИСПОЛЬЗОВАНИЯ Введение фотоактивируемых и репортерных групп в нуклеиновые кислоты 27
ПРИМЕРЫ ИСПОЛЬЗОВАНИЯ Введение фотоактивируемых и репортерных групп в нуклеиновые кислоты 27
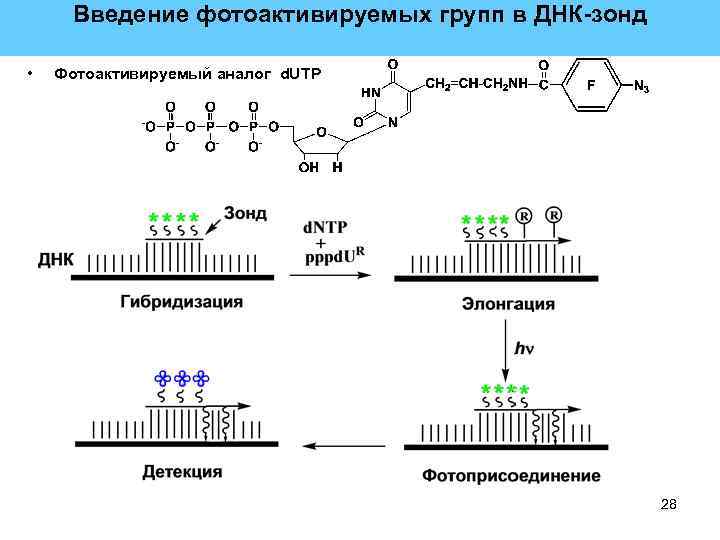 Введение фотоактивируемых групп в ДНК-зонд • Фотоактивируемый аналог d. UTP 28
Введение фотоактивируемых групп в ДНК-зонд • Фотоактивируемый аналог d. UTP 28
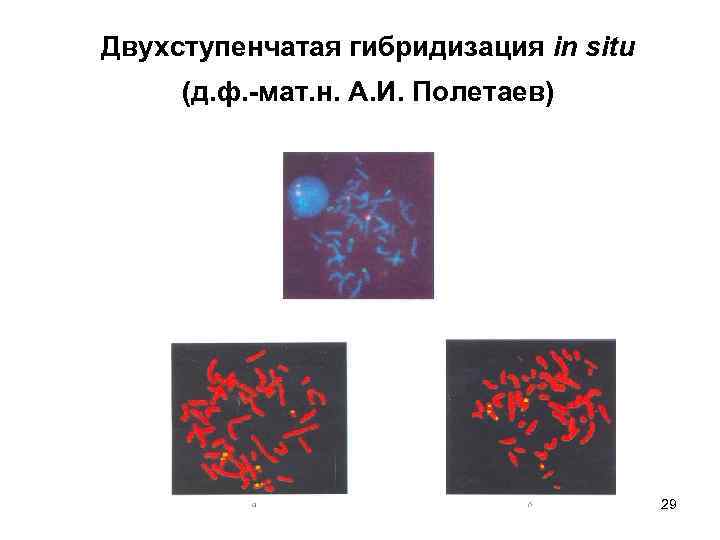 Двухступенчатая гибридизация in situ (д. ф. -мат. н. А. И. Полетаев) 29
Двухступенчатая гибридизация in situ (д. ф. -мат. н. А. И. Полетаев) 29
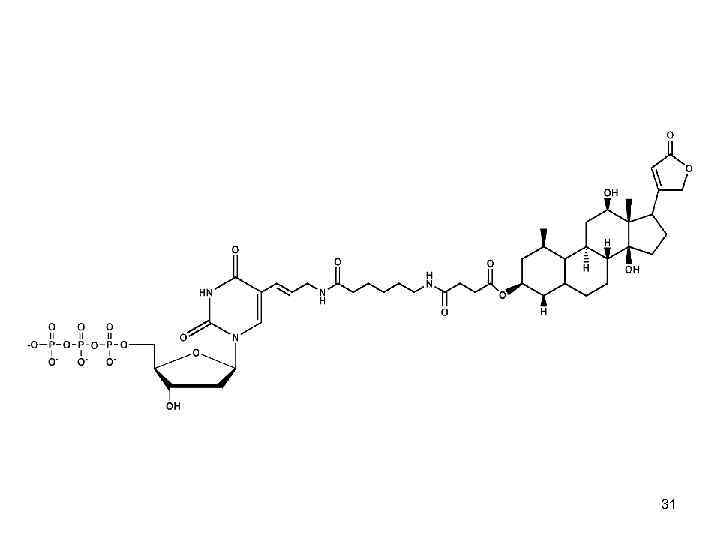
 Мечение нуклеиновых кислот • Поиски эффективных нерадиоактивных маркеров, пригодных для мечения зондов, привели к созданию как минимум двух альтернативных меток: биотинd. NTP (bio-d. NTP, фирмы Sigma и Gibco-BRL) и дигоксигенин-d. UTP (digd. UTP, фирма Boehringer Mannheim). 30
Мечение нуклеиновых кислот • Поиски эффективных нерадиоактивных маркеров, пригодных для мечения зондов, привели к созданию как минимум двух альтернативных меток: биотинd. NTP (bio-d. NTP, фирмы Sigma и Gibco-BRL) и дигоксигенин-d. UTP (digd. UTP, фирма Boehringer Mannheim). 30
 31
31
 Производные нуклеиновых кислот, снабженные дигогсигениновой меткой • Использование в качестве метки дигоксигенина, обеспечивает большую специфичность и воспроизводимость, а чувствительность метода близка к таковой для случая радиоактивно меченных зондов. Дигоксигенин присутствует только в растении дигиталис (наперстянка), что уменьшает неспецифичное окрашивание, обусловленное взаимодействием с эндогенными соединениями. 32
Производные нуклеиновых кислот, снабженные дигогсигениновой меткой • Использование в качестве метки дигоксигенина, обеспечивает большую специфичность и воспроизводимость, а чувствительность метода близка к таковой для случая радиоактивно меченных зондов. Дигоксигенин присутствует только в растении дигиталис (наперстянка), что уменьшает неспецифичное окрашивание, обусловленное взаимодействием с эндогенными соединениями. 32
 Что нужно знать после лекции • • Реакции присоединения и замещения по атомам углерода. Реакция присоединения-отщепления по двойной связи С 5 -С 6 пиримидинов: меркурирование в водной среде; взаимодействие с бисульфитом натрия. Окисление четырехокисью осмия. Действие гидразина и его производных. Реакции переаминирования как способ введения реакционноспособных групп и меток по С 4 -положению цитидина. Реакции расщепления и перегруппировки гетероциклических оснований нуклеиновых кислот и их производных. Раскрытие пиримидинового цикла. Расщепление ДНК по остаткам цитозина гидразином при высокой концентрации Na. Cl. Деградация ДНК по остаткам пиримидинов после обработке гидразином в отсутствие Na. Cl. Способы введения фотоактивируемых и репортерных групп по С 5 положению пиримидинов. Взаимопревращения природных нуклеозидов. Получение уридина методом дезаминирования цитидина. Аминирование как способ превращения уридина в цитидин, тимидина в 5 -метил-2`дезоксицитидин. 33
Что нужно знать после лекции • • Реакции присоединения и замещения по атомам углерода. Реакция присоединения-отщепления по двойной связи С 5 -С 6 пиримидинов: меркурирование в водной среде; взаимодействие с бисульфитом натрия. Окисление четырехокисью осмия. Действие гидразина и его производных. Реакции переаминирования как способ введения реакционноспособных групп и меток по С 4 -положению цитидина. Реакции расщепления и перегруппировки гетероциклических оснований нуклеиновых кислот и их производных. Раскрытие пиримидинового цикла. Расщепление ДНК по остаткам цитозина гидразином при высокой концентрации Na. Cl. Деградация ДНК по остаткам пиримидинов после обработке гидразином в отсутствие Na. Cl. Способы введения фотоактивируемых и репортерных групп по С 5 положению пиримидинов. Взаимопревращения природных нуклеозидов. Получение уридина методом дезаминирования цитидина. Аминирование как способ превращения уридина в цитидин, тимидина в 5 -метил-2`дезоксицитидин. 33


