Метод молекулярных орбиталей (Линейная комбинация атомных орбиталей) ММО


Метод молекулярных орбиталей (Линейная комбинация атомных орбиталей) ММО (ЛКАО) Электроны принадлежат молекуле в целом. Вместо атомных орбиталей рассматриваются молекулярные орбитали.

В образовании химической связи могут участвовать как пара, так и один электрон. Состояние электронов в молеку-лах соответствует принципам минимальной энергии, Паули и Гунда.

Молекулярные орбитали строятся из атомных орбиталей путем линейных комбинаций, т. е. путем сложения и вычитания волновых функций. Из N атомных получают N молекулярных орбиталей.

При ЛКАО форму молекулярных орбиталей можно предвидеть, зная форму атомных орбиталей. Во втором периоде валентными электронами являются только s-, px, py , pz.
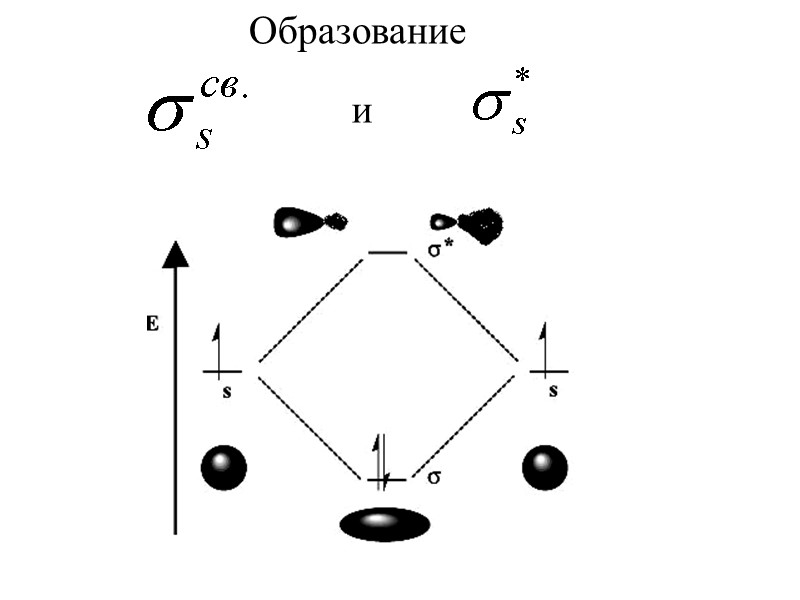
Образование и
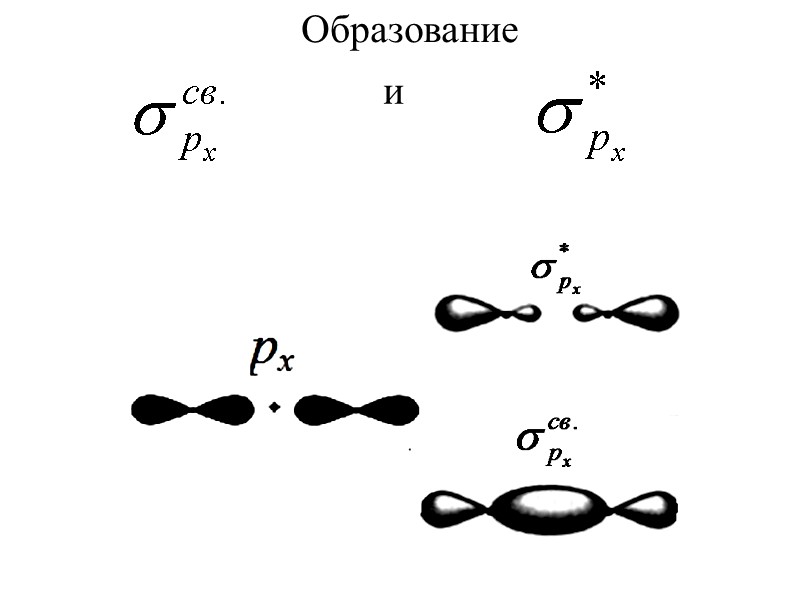
Образование и
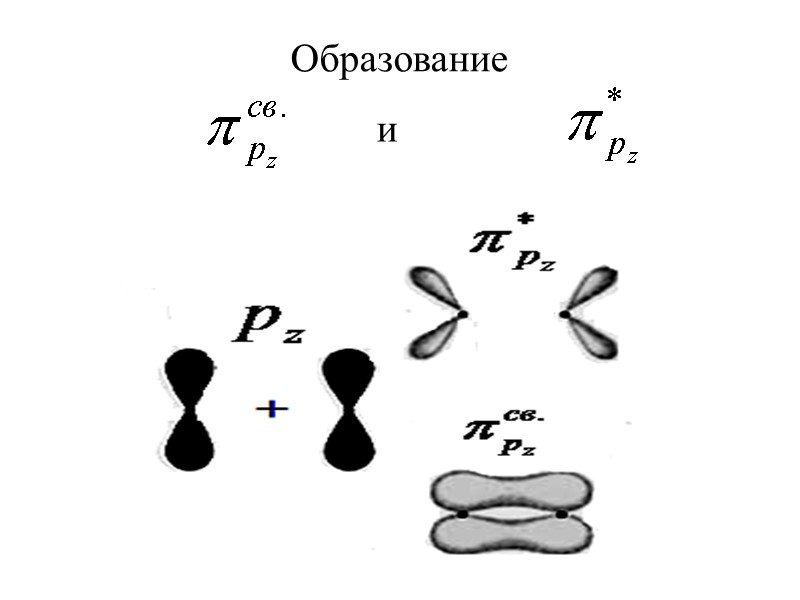
и Образование
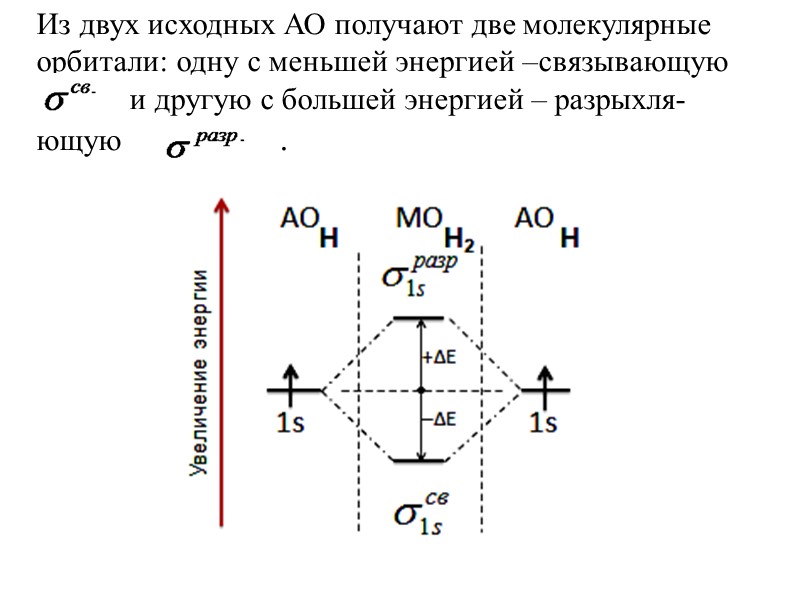
Из двух исходных АО получают две молекулярные орбитали: одну с меньшей энергией –связывающую и другую с большей энергией – разрыхля- ющую . .
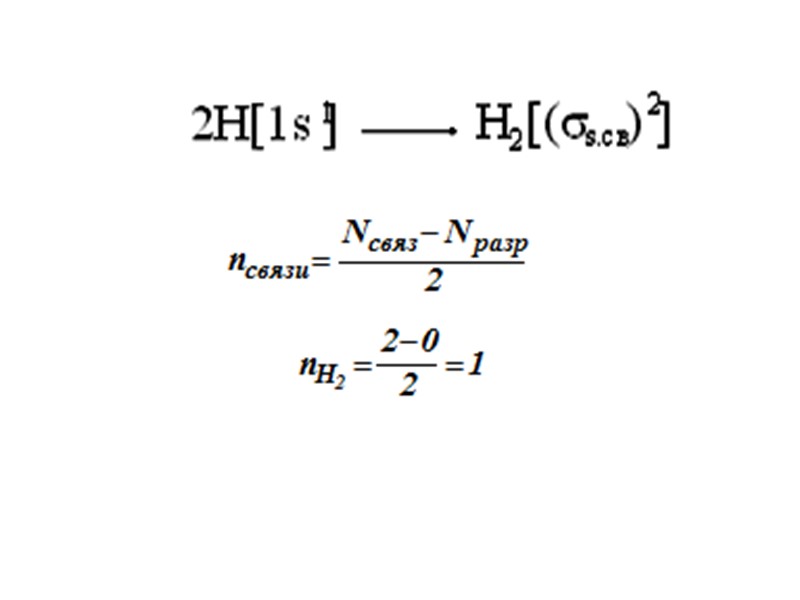
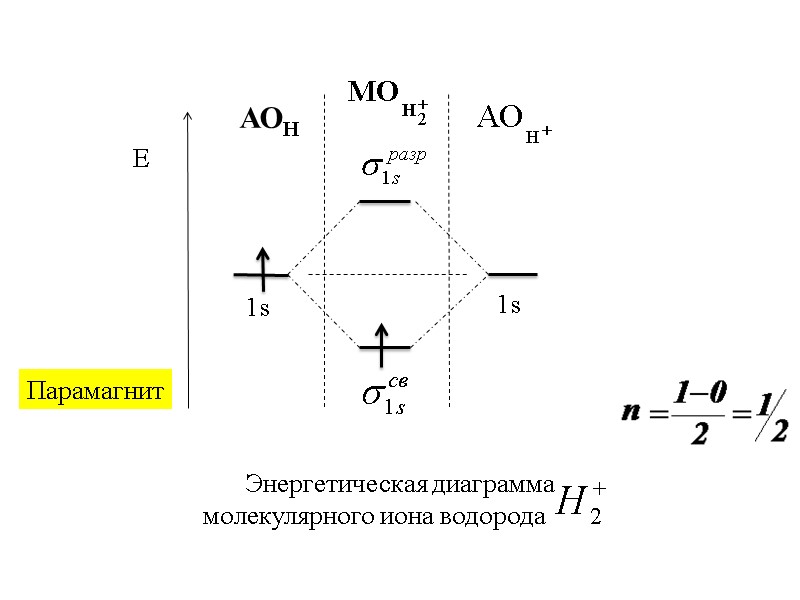
АОН Парамагнит

Последовательность располо-жения молекулярных орбиталей в зависимости от возрастания их энергии: σ1s < σ1s* < σ2s < σ2s* < πy = πz < σx < πy* = πz* < σx*
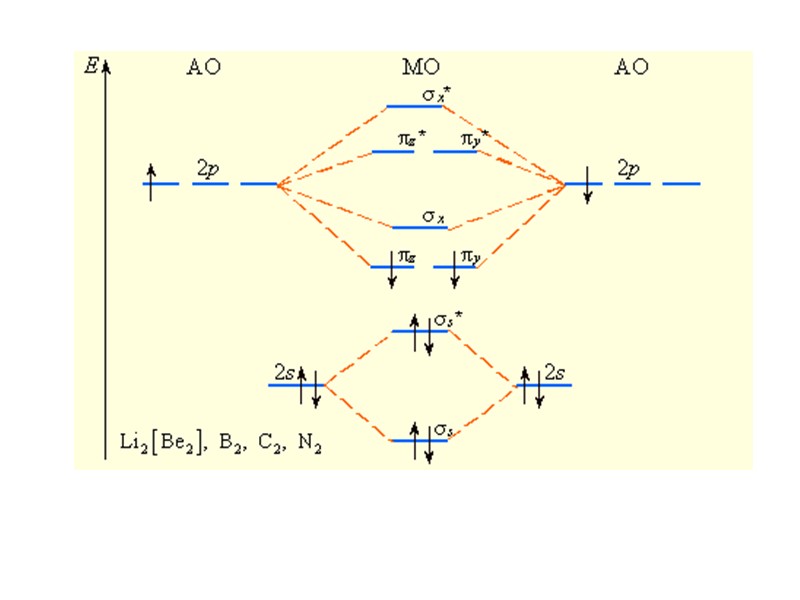

Изоэлектронные частицы N2, CO, NO+ имеют одинаковый набор МО, одинаковую энергетическую последовательность, заселенность электронами и одинаковый порядок связи
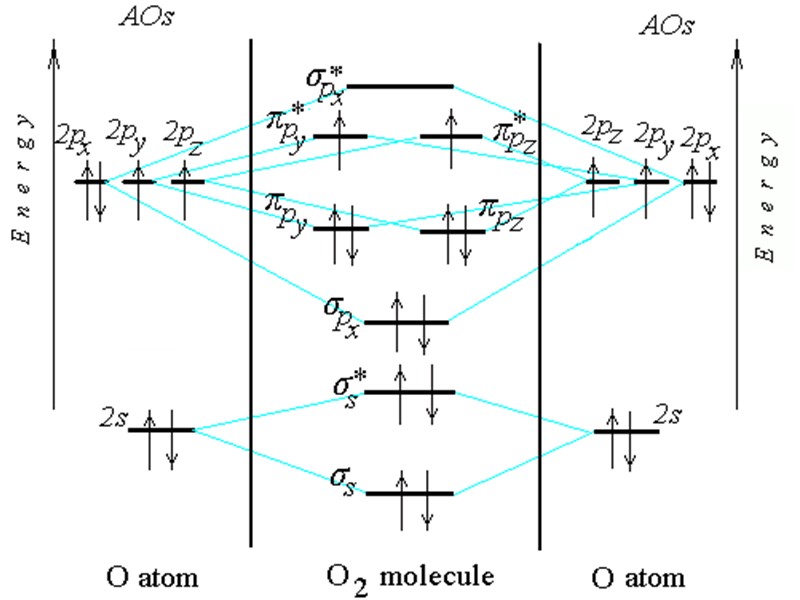
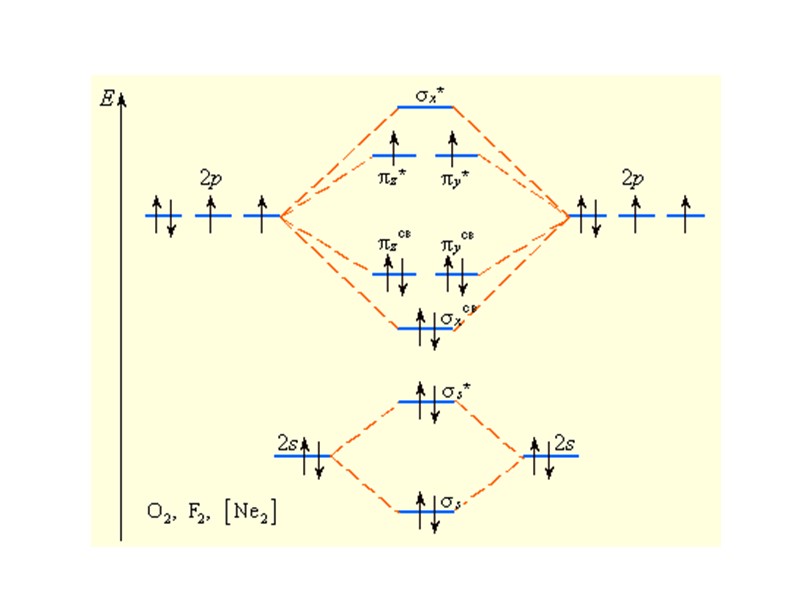
O2

O2 (KK)s2s*2px2 y2z2y*1z*1 Обозначение (KK) относится к внутренним электронам в O2 N2 (KK)s2s*2px2y2z2
40658-mmo_for_students.ppt
- Количество слайдов: 16

