Мембранное материаловедение проф. д. х. н. Ямпольский




















08.ppt
- Размер: 3.1 Мб
- Автор:
- Количество слайдов: 36
Описание презентации Мембранное материаловедение проф. д. х. н. Ямпольский по слайдам
 Мембранное материаловедение проф. д. х. н. Ямпольский Ю. П. д. х. н. Алентьев А. Ю. ИНХС РАН
Мембранное материаловедение проф. д. х. н. Ямпольский Ю. П. д. х. н. Алентьев А. Ю. ИНХС РАН
 8 ТОПЛИВНЫЕ ЭЛЕМЕНТЫ
8 ТОПЛИВНЫЕ ЭЛЕМЕНТЫ
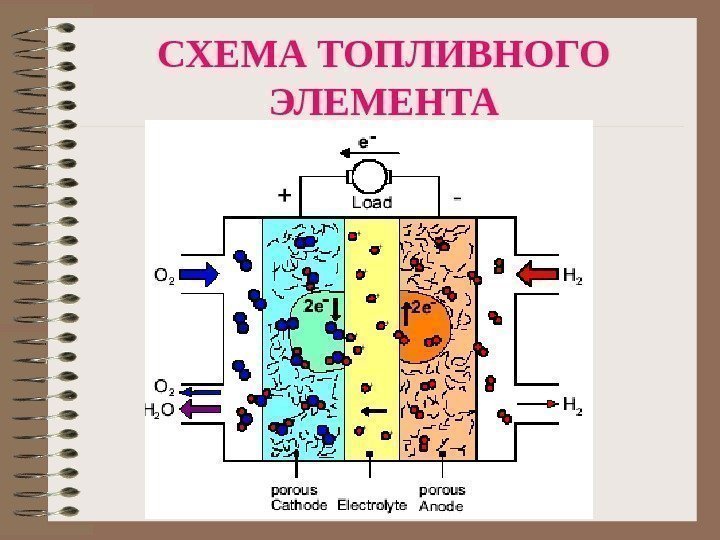
 СХЕМА ТОПЛИВНОГО ЭЛЕМЕНТА
СХЕМА ТОПЛИВНОГО ЭЛЕМЕНТА
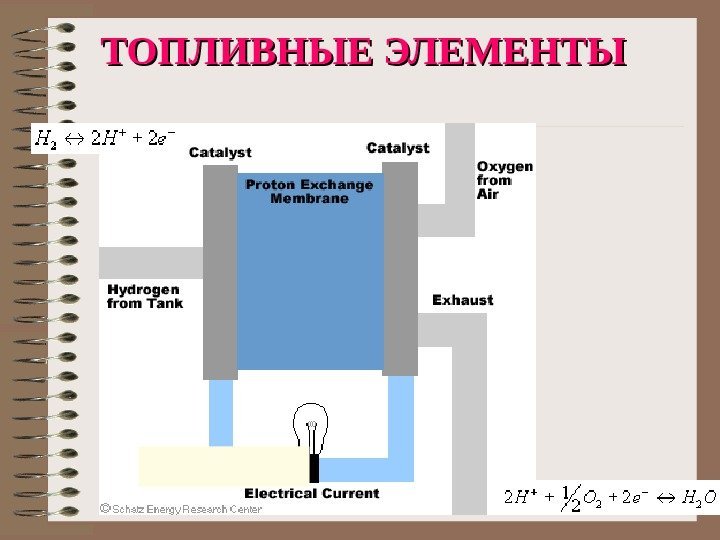
 ТОПЛИВНЫЕ ЭЛЕМЕНТЫ
ТОПЛИВНЫЕ ЭЛЕМЕНТЫ
 Топливные элементы – междисциплинарная проблема • Электрохимия • Мембранный транспорт • Катализ • Материаловедение • Инжениринг и проблемы энергетики
Топливные элементы – междисциплинарная проблема • Электрохимия • Мембранный транспорт • Катализ • Материаловедение • Инжениринг и проблемы энергетики
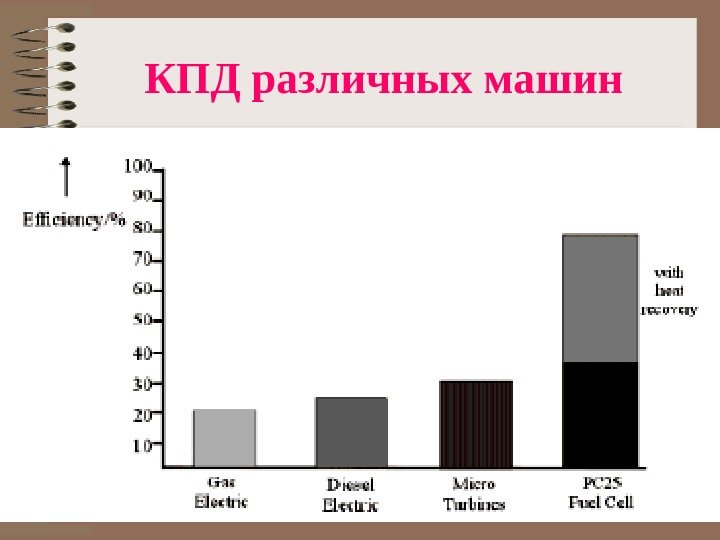
 КПД различных машин
КПД различных машин
 Причины высоких КПД в ТЭ
Причины высоких КПД в ТЭ
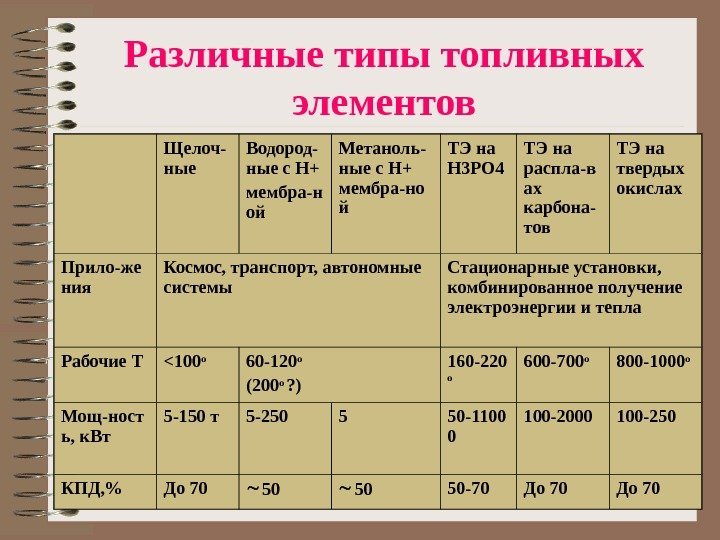
 Различные типы топливных элементов Щелоч- ные Водород- ные с Н+ мембра-н ой Метаноль- ные с Н+ мембра-но й ТЭ на H 3 PO 4 ТЭ на распла-в ах карбона- тов ТЭ на твердых окислах Прило-же ния Космос, транспорт, автономные системы Стационарные установки, комбинированное получение электроэнергии и тепла Рабочие Т <100 o 60 -120 o ( 2 0 0 o ? ) 160 -220 o 600 -700 o 800 -1000 o Мощ-ност ь, к. Вт 5 -150 т 5 -250 5 50 -1100 0 100 -2000 100 -250 КПД, % До 70 50 50 50 -70 До
Различные типы топливных элементов Щелоч- ные Водород- ные с Н+ мембра-н ой Метаноль- ные с Н+ мембра-но й ТЭ на H 3 PO 4 ТЭ на распла-в ах карбона- тов ТЭ на твердых окислах Прило-же ния Космос, транспорт, автономные системы Стационарные установки, комбинированное получение электроэнергии и тепла Рабочие Т <100 o 60 -120 o ( 2 0 0 o ? ) 160 -220 o 600 -700 o 800 -1000 o Мощ-ност ь, к. Вт 5 -150 т 5 -250 5 50 -1100 0 100 -2000 100 -250 КПД, % До 70 50 50 50 -70 До
 Щелочные топливные элементы Электролит КОН (стаб. на матрице или циркулирующий) Реагенты Н 2 , О 2 Ион-переносчик ОН — Электроды Катод: Ni ( добавки Pt? ) Анод: Pt/C, Pt-Co/C, Pt-Pd/C Анодная реакция H 2 + 2 OH- 2 H 2 O + 2 e- Катодная реакция 1/2 O 2 + H 2 O + 2 e — 2 OH — Проблемы Образование карбонатов: С + О 2 CO 2 + 2 OH — CO 3 2 — + H 2 O
Щелочные топливные элементы Электролит КОН (стаб. на матрице или циркулирующий) Реагенты Н 2 , О 2 Ион-переносчик ОН — Электроды Катод: Ni ( добавки Pt? ) Анод: Pt/C, Pt-Co/C, Pt-Pd/C Анодная реакция H 2 + 2 OH- 2 H 2 O + 2 e- Катодная реакция 1/2 O 2 + H 2 O + 2 e — 2 OH — Проблемы Образование карбонатов: С + О 2 CO 2 + 2 OH — CO 3 2 — + H 2 O
 Водородные ТЭ с Н + проводящей мембраной Электролит Ионообменная мембрана (поликислота) Реагенты Н 2 , воздух (О 2 ) Ион-переносчик Н + Электроды Катод: Pt/C Анод: Pt/C, Pt-Ru/C Анодная реакция H 2 2 H + + 2 e — Катодная реакция 1/2 O 2 + 2 H + + 2 e — H 2 O Проблемы Отравление анодной Pt CO Гидратация-дегидратация Кроссовер (Н 2 + О 2 )
Водородные ТЭ с Н + проводящей мембраной Электролит Ионообменная мембрана (поликислота) Реагенты Н 2 , воздух (О 2 ) Ион-переносчик Н + Электроды Катод: Pt/C Анод: Pt/C, Pt-Ru/C Анодная реакция H 2 2 H + + 2 e — Катодная реакция 1/2 O 2 + 2 H + + 2 e — H 2 O Проблемы Отравление анодной Pt CO Гидратация-дегидратация Кроссовер (Н 2 + О 2 )
 Метанольные ТЭ с Н+ проводящей мембраной Электролит Ионообменная мембрана (поликислота) Реагенты CH 3 OH , воздух (О 2 ) Ион-переносчик Н + Электроды Катод: Pt/C Анод: Pt-Ru/C ( Os, Rh…) Анодная реакция CH 3 OH + H 2 O CO 2 + 6 H + + 6 e — Катодная реакция 3/2 O 2 + 6 H + + 6 e — 3 H 2 O Проблемы Гидратация-дегидратация Кроссовер ( Me. OH)
Метанольные ТЭ с Н+ проводящей мембраной Электролит Ионообменная мембрана (поликислота) Реагенты CH 3 OH , воздух (О 2 ) Ион-переносчик Н + Электроды Катод: Pt/C Анод: Pt-Ru/C ( Os, Rh…) Анодная реакция CH 3 OH + H 2 O CO 2 + 6 H + + 6 e — Катодная реакция 3/2 O 2 + 6 H + + 6 e — 3 H 2 O Проблемы Гидратация-дегидратация Кроссовер ( Me. OH)
 ТЭ на фосфорной кислоте Электролит H 3 PO 4 ( на тв. носителе – Si. C и др. ) Реагенты Н 2 , воздух (О 2 ) Ион-переносчик Н + Электроды Катод: Pt/C, Pt-WO 3 /C Анод: Pt/C, Pt-Ru/C Анодная реакция H 2 2 H + + 2 e — Катодная реакция 1/2 O 2 + 2 H + + 2 e — H 2 O Проблемы Кроссовер (Н 2 + О 2 ) Отравление СО не так страшно (при 200 о С)
ТЭ на фосфорной кислоте Электролит H 3 PO 4 ( на тв. носителе – Si. C и др. ) Реагенты Н 2 , воздух (О 2 ) Ион-переносчик Н + Электроды Катод: Pt/C, Pt-WO 3 /C Анод: Pt/C, Pt-Ru/C Анодная реакция H 2 2 H + + 2 e — Катодная реакция 1/2 O 2 + 2 H + + 2 e — H 2 O Проблемы Кроссовер (Н 2 + О 2 ) Отравление СО не так страшно (при 200 о С)
 ТЭ на расплавах карбонатов Электролит Li. KCO 3 , Li. Na. CO 3 на матрице Li. Al. O 2 + Al 2 O 3 Реагенты CH 4 , синтез-газ ( H 2 , CO 2 ), O 2 Ион-переносчик CO 3 2 — Электроды Катод: Ni. O, Li. Fe. O 2 и др. Анод: Ni-Al, Ni-Cr Анодная реакция H 2 + CO 3 2 — H 2 O + CO 2 + 2 e — Катодная реакция 1/2 O 2 + CO 2 + 2 e- CO 3 2 — Проблемы Попадание частиц Ni. O в электролит; материаловедение, работа с горючими газами при высоких Т
ТЭ на расплавах карбонатов Электролит Li. KCO 3 , Li. Na. CO 3 на матрице Li. Al. O 2 + Al 2 O 3 Реагенты CH 4 , синтез-газ ( H 2 , CO 2 ), O 2 Ион-переносчик CO 3 2 — Электроды Катод: Ni. O, Li. Fe. O 2 и др. Анод: Ni-Al, Ni-Cr Анодная реакция H 2 + CO 3 2 — H 2 O + CO 2 + 2 e — Катодная реакция 1/2 O 2 + CO 2 + 2 e- CO 3 2 — Проблемы Попадание частиц Ni. O в электролит; материаловедение, работа с горючими газами при высоких Т
 ТЭ на твердых оксидах Электролит Zr. O 2 , Ce. O 2 , Y 2 O 3 Реагенты CH 4 , синтез-газ ( H 2 , CO 2 ), O 2 или воздух Ион-переносчик О 2 2 — Электроды Катод: La. Sr. Mn. O 3, лантанидные перовскиты и др. Анод: Ni (+Ni. O) и др. Анодная реакция 2 Н 2 + O 2 2 — 2 H 2 O + 2 e — Катодная реакция O 2 + 2 e — O 2 2 — Проблемы Материаловедение (уплотнения, газо-распределение и т. д. ) Долгосрочная стабильность материалов
ТЭ на твердых оксидах Электролит Zr. O 2 , Ce. O 2 , Y 2 O 3 Реагенты CH 4 , синтез-газ ( H 2 , CO 2 ), O 2 или воздух Ион-переносчик О 2 2 — Электроды Катод: La. Sr. Mn. O 3, лантанидные перовскиты и др. Анод: Ni (+Ni. O) и др. Анодная реакция 2 Н 2 + O 2 2 — 2 H 2 O + 2 e — Катодная реакция O 2 + 2 e — O 2 2 — Проблемы Материаловедение (уплотнения, газо-распределение и т. д. ) Долгосрочная стабильность материалов
 Требования к мембранам • Низкая стоимость ( 120 -150 o C, > 10 000 час • Механическая стабильность • Электроизолирующие свойства
Требования к мембранам • Низкая стоимость ( 120 -150 o C, > 10 000 час • Механическая стабильность • Электроизолирующие свойства
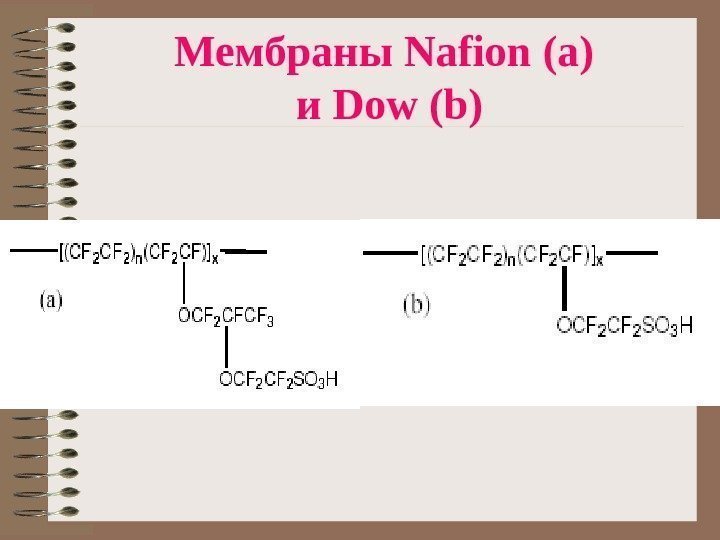
 Мембраны Nafion (a) и Dow (b)
Мембраны Nafion (a) и Dow (b)
 Мембрана сулфонилимида (более проводящая чем Nafion)
Мембрана сулфонилимида (более проводящая чем Nafion)
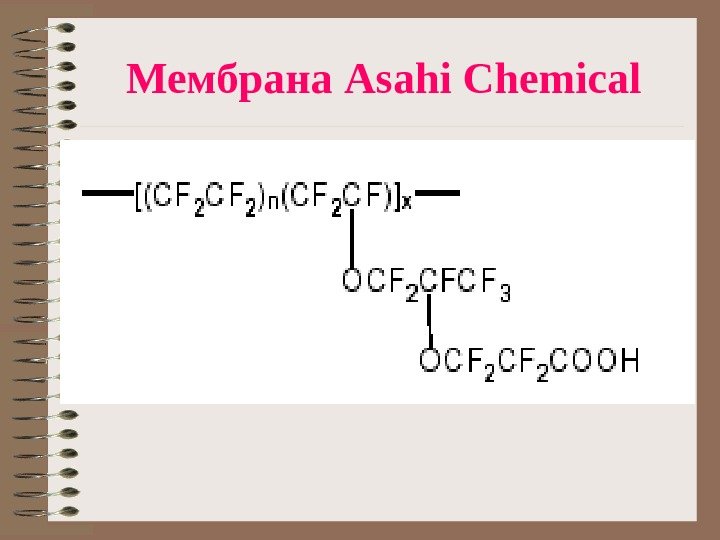
 Мембрана Asahi Chemical
Мембрана Asahi Chemical
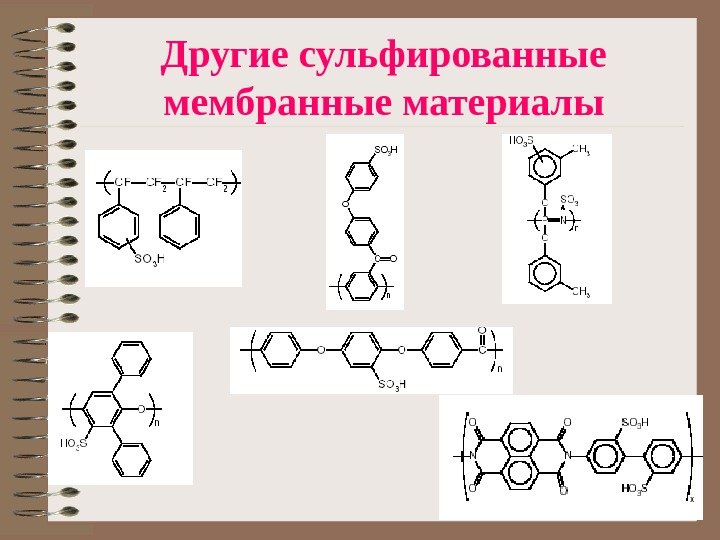
 Другие сульфированные мембранные материалы
Другие сульфированные мембранные материалы
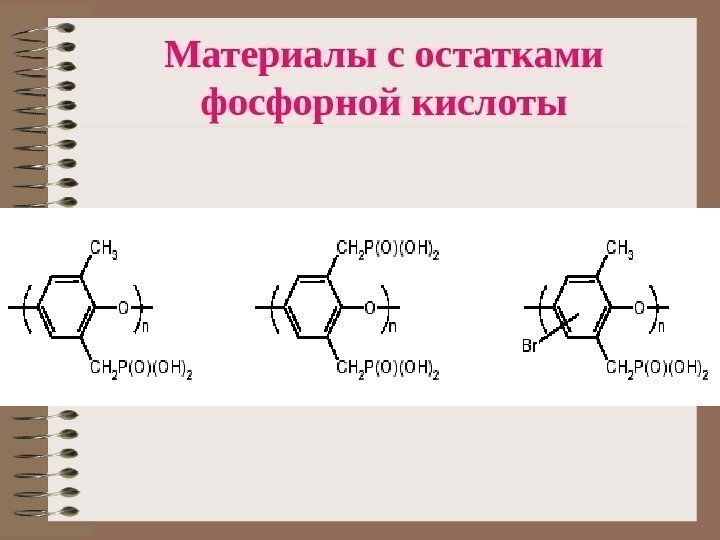
 Материалы с остатками фосфорной кислоты
Материалы с остатками фосфорной кислоты
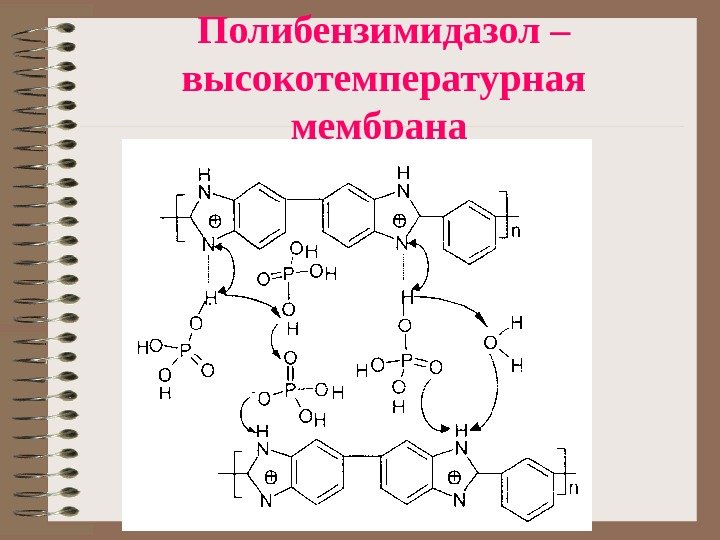
 Полибензимидазол – высокотемпературная мембрана
Полибензимидазол – высокотемпературная мембрана
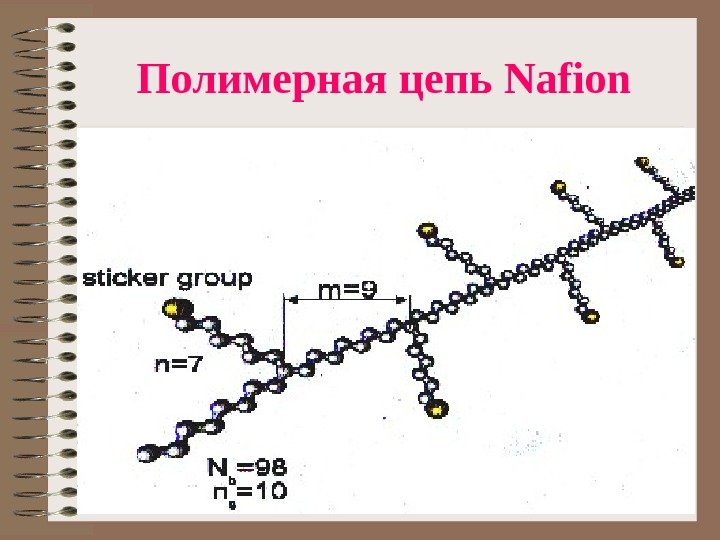
 Полимерная цепь Nafion
Полимерная цепь Nafion
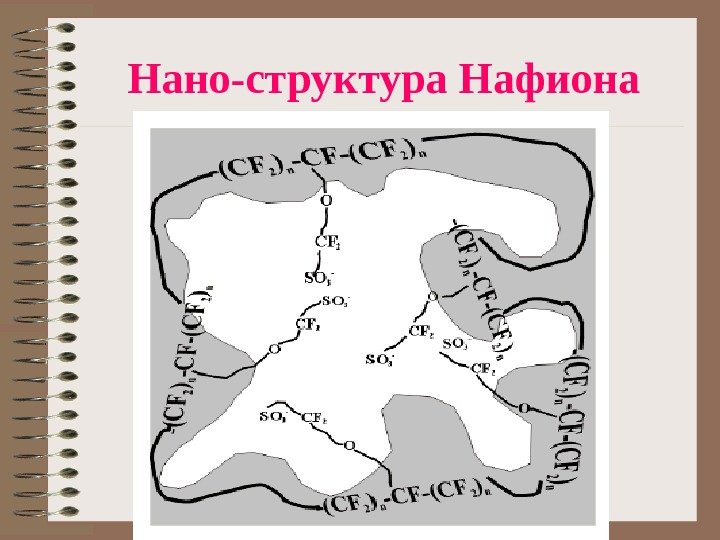
 Нано-структура Нафиона
Нано-структура Нафиона
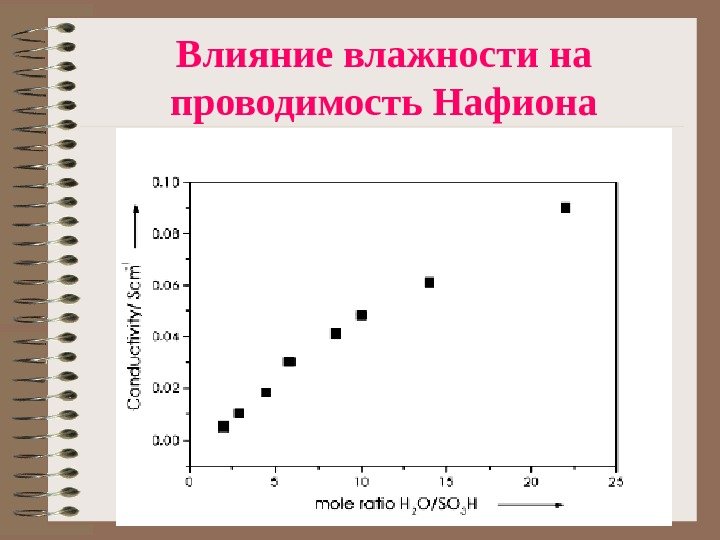
 Влияние влажности на проводимость Нафиона
Влияние влажности на проводимость Нафиона
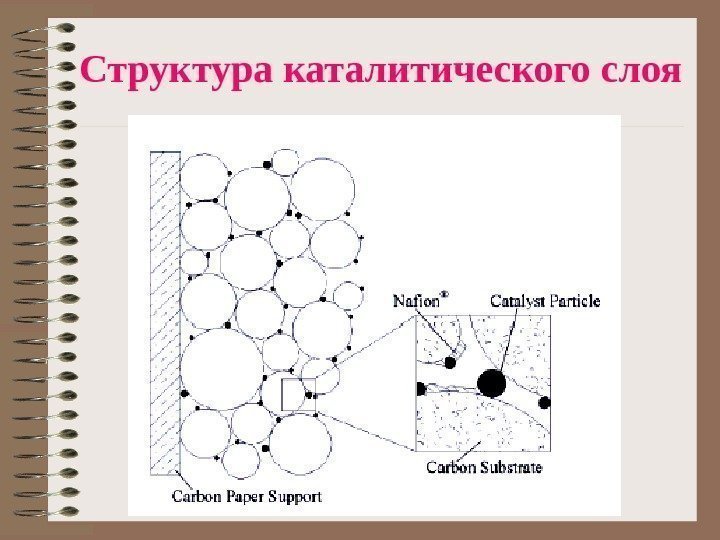
 Структура каталитического слоя
Структура каталитического слоя
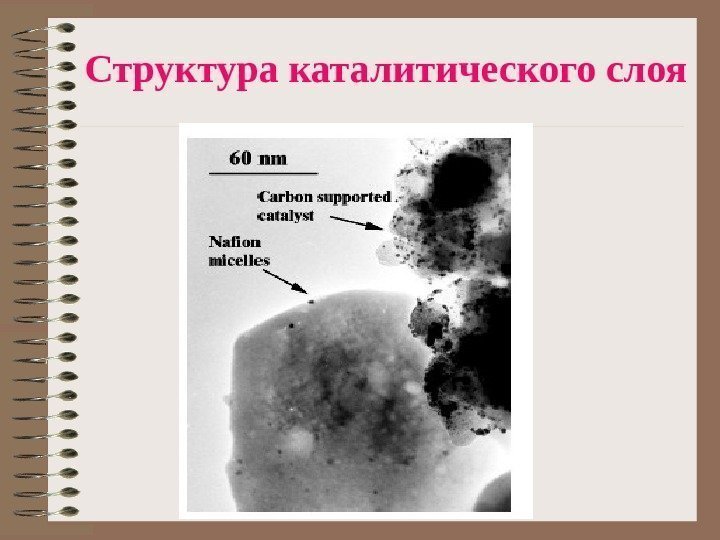
 Структура каталитического слоя
Структура каталитического слоя
 Водные проблемы (water management) • Состояние воды в мембране: сольватация –SO 3 H групп сольватация Н + «объемная» воды • Дегидратация: “ асимметрия ” образования воды; температурный режим ( <100 o C); возможное влияние на мех. стабильность • Увлажнение: роль кроссовера; “ заливание ” пор в электроде.
Водные проблемы (water management) • Состояние воды в мембране: сольватация –SO 3 H групп сольватация Н + «объемная» воды • Дегидратация: “ асимметрия ” образования воды; температурный режим ( <100 o C); возможное влияние на мех. стабильность • Увлажнение: роль кроссовера; “ заливание ” пор в электроде.
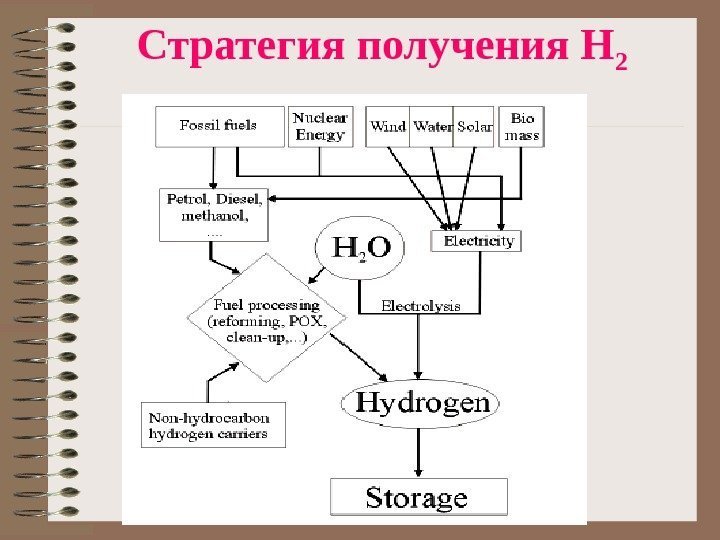
 Стратегия получения Н
Стратегия получения Н
 Методы получения водорода (ископаемые топлива) • Паровая конверсия природного газа: CH 4 + H 2 O CO + 3 H 2 CO + H 2 O = CO 2 + H 2 • Каталитический риформинг C 6 H 14 C 6 H 6 + 4 H 2 • Пиролиз C n Hm C 2 H 4 + H
Методы получения водорода (ископаемые топлива) • Паровая конверсия природного газа: CH 4 + H 2 O CO + 3 H 2 CO + H 2 O = CO 2 + H 2 • Каталитический риформинг C 6 H 14 C 6 H 6 + 4 H 2 • Пиролиз C n Hm C 2 H 4 + H
 Альтернативные методы получения водорода • Электролиз • Фотолиз воды • Высокотемпературные ядерные (Не) реактора
Альтернативные методы получения водорода • Электролиз • Фотолиз воды • Высокотемпературные ядерные (Не) реактора
 Термохимический цикл в Не ядерном реакторе Источник энергии – Не ( 1000 о С) 2 H 2 О + SO 2 + J 2 H 2 SO 4 + 2 HJ ( при 900 о ) 2 HJ J 2 + H 2 ( при 450 о С) H 2 SO 4 + SO 2 + H 2 O + 1/2 O 2 ( при 850 o C)
Термохимический цикл в Не ядерном реакторе Источник энергии – Не ( 1000 о С) 2 H 2 О + SO 2 + J 2 H 2 SO 4 + 2 HJ ( при 900 о ) 2 HJ J 2 + H 2 ( при 450 о С) H 2 SO 4 + SO 2 + H 2 O + 1/2 O 2 ( при 850 o C)
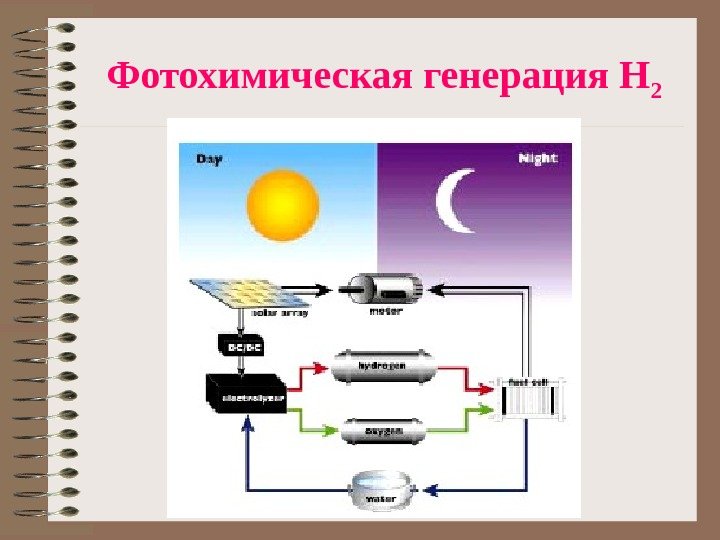
 Фотохимическая генерация Н
Фотохимическая генерация Н
 Методы очистки водорода • Мембраны: Pd полимерные мембраны • Химические: дожигание: СО + 1/2 O 2 CO 2 реакция водяного пара: CO + H 2 O = CO 2 + H 2 метанирование: С O + 3 H 2 CH 4 + H 2 O • Адсорбционные
Методы очистки водорода • Мембраны: Pd полимерные мембраны • Химические: дожигание: СО + 1/2 O 2 CO 2 реакция водяного пара: CO + H 2 O = CO 2 + H 2 метанирование: С O + 3 H 2 CH 4 + H 2 O • Адсорбционные
 Хранение водорода • Газовые баллоны (0, 5 кг Н 2 ) • Жидкий водород (-253 о С, теплопотери) • Гидрирды металлов, нано-трубки и т. п. • Химические источники Н 2 : СН 3 ОН, СН 4 , НС, биомасса.
Хранение водорода • Газовые баллоны (0, 5 кг Н 2 ) • Жидкий водород (-253 о С, теплопотери) • Гидрирды металлов, нано-трубки и т. п. • Химические источники Н 2 : СН 3 ОН, СН 4 , НС, биомасса.
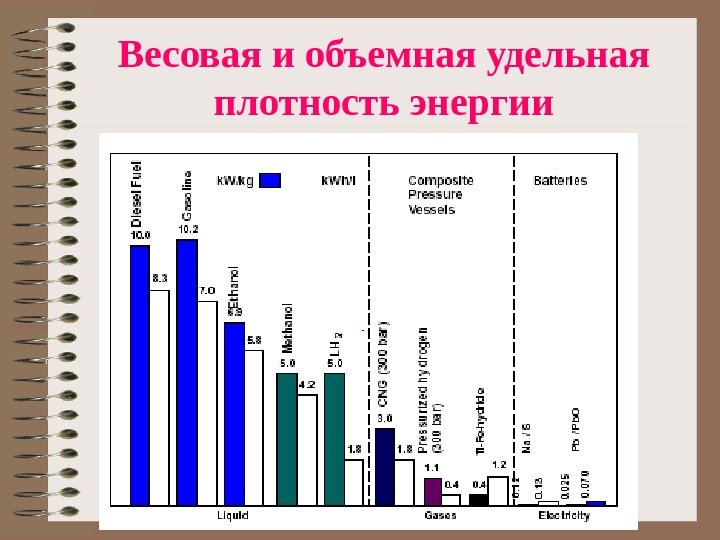
 Весовая и объемная удельная плотность энергии
Весовая и объемная удельная плотность энергии
 ТЭ – будущие основные источники энергии
ТЭ – будущие основные источники энергии

