09 КОНСУЛЬТИРОВАНИЕ ПРИНЦИПЫ ЛЕЧЕНИЯ.ppt
- Количество слайдов: 29

Медико-генетическое консультирование Цели: • определение прогноза рождения больных детей в семье, • консультирование по вопросам дальнейшего планирования семьи. На территории Российской Федерации существует около 80 медико-генетических учреждений, услугами которых ежегодно пользовались около 80 тыс. семей.

Необходимость консультирования вытекает из: • на 1000 новорожденных приходится 35 -40 с различными типами наследственных болезней. В смертности детей в возрасте до 5 лет: • хромосомные болезни составляют 2 -3%, • генные — 8 -10%, • мультифакториальные — 35 -40%. Ежегодно в нашей стране рождается 180 тыс. детей с наследственными заболеваниями: • более половины из них имеют врожденные пороки, • около 35 тыс. — хромосомные болезни и • свыше 35 тыс. — генные болезни. Выявляются новые формы наследственной патологии: • в 1956 г. было известно 700 форм наследственных заболеваний, • а к 1986 году число их увеличилось до 2000, • в 1992 количество известных наследственных болезней и признаков возросло около 4000.

Классификация наследственных болезней I. Генные болезни вызваны генными мутациями. Частота в популяции составляет 1 -2%. • аутосомно-доминантные, • аутосомно-рецессивные, • сцепленные с Х- или Y-хромосомами, Мутантный аллель -» измененный первичный продукт —» цепь последующих биохимических процессов клетки -» органы —> организм. В результате мутации гена на молекулярном уровне возможны следующие варианты: 1) синтез аномального белка; 2) выработка избыточного количества генного продукта; 3) отсутствие выработки первичного продукта; 4) выработка уменьшенного количества нормального первичного продукта.
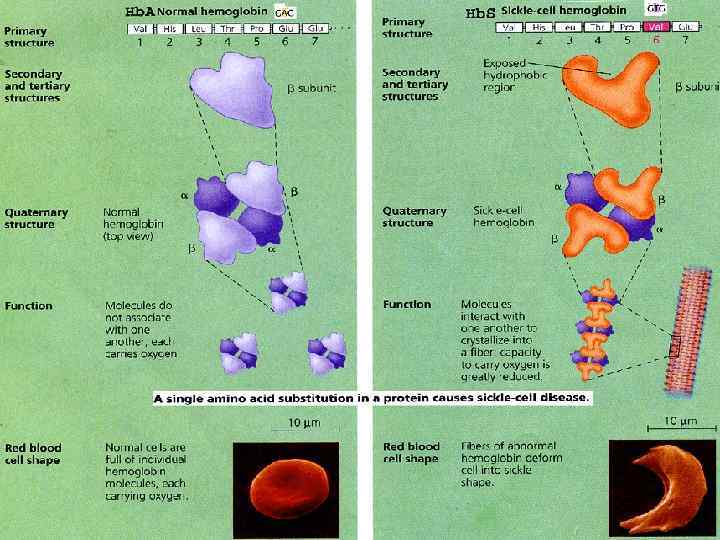

Клинические проявления генных болезней, тяжесть и скорость их развития зависят: • от особенностей генотипа (гены-модификаторы, доза генов, время действия мутантного гена, гомо- и гетерозиготность и др. ), • возраста больного, условий внешней среды (питание, охлаждение, стрессы, переутомление и др. ). Особенностью генных болезней является их гетерогенность.

II. Хромосомные болезни. (из 1000 новорожденных 7 имели различные хромосомные аномалии). Они возникают в результате мутаций в половых клетках одного из родителей. Из поколения в поколение передаются не более 3 -5 % из них. Хромосомными нарушениями обусловлены примерно 50 % спонтанных абортов и 7 % всех мертворождений. Хромосомные болезни связаны: 1. С аномалиями числа хромосом: • Болезни, обусловленные нарушением числа аутосом. • Болезни, связанные с нарушением числа половых Х- и Yхромосом. 2. Со структурными изменениями хромосом. Транслокации, делеции и др. 3. Болезни, причиной которых является полиплодия. Около 22, 6% всех спонтанных абортов обусловлены полиплоидией.
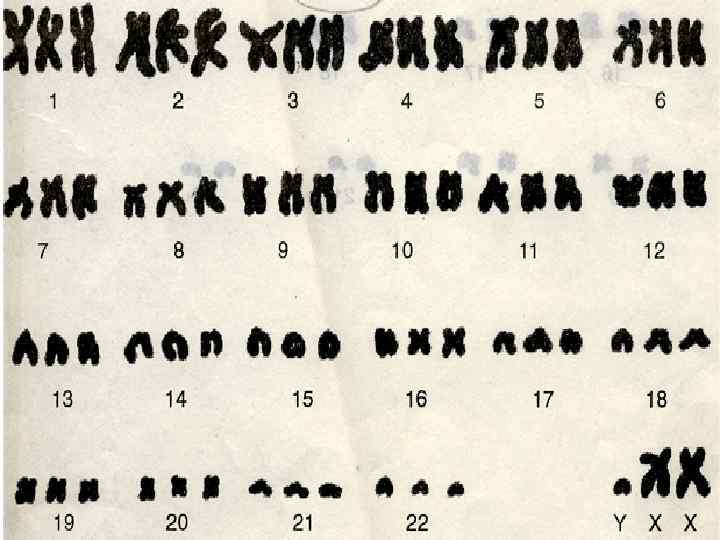

Причины возникновения хромосомных болезней: • действие ионизирующих излучении, • химических веществ, • вирусов, • сезонность, • возраст отца и матери, • порядок рождения детей, • прием лекарств во время беременности, • гормональные нарушения, • алкоголизм и др.
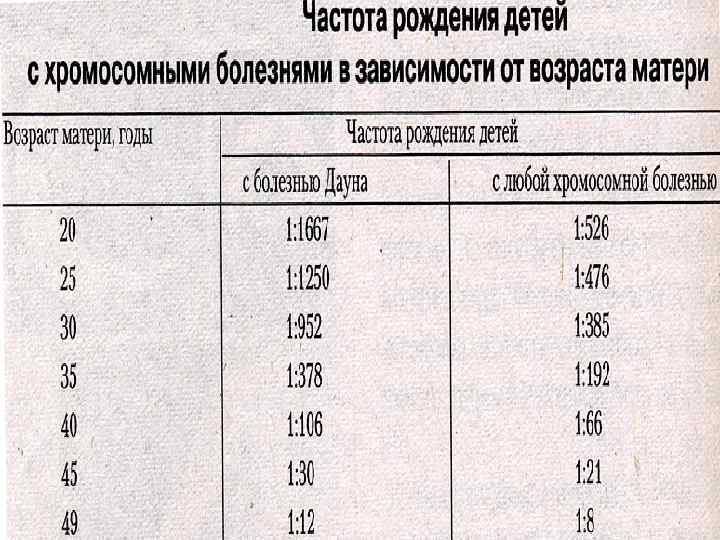

III. Болезни с наследственной предрасположенностью (мультифакториальные) обусловлены как наследственными, так и, факторами внешней среды. В настоящее время составляют 92% от наследственных патологий человека. С возрастом частота заболеваний возрастает. В детском возрасте - 10 %, а в пожилом - 25 -30 %. Наследственная предрасположенность может иметь моноили полигенную природу.


Выделяют следующие общие особенности: 1. Высокая частота заболеваний в популяции. 2. Клинический полиморфизм 3. Особенности наследования заболеваний не соответствуют менделевским закономерностям. 4. Степень проявления болезни зависит от многих факторов. 5. Полигенная пороговая модель
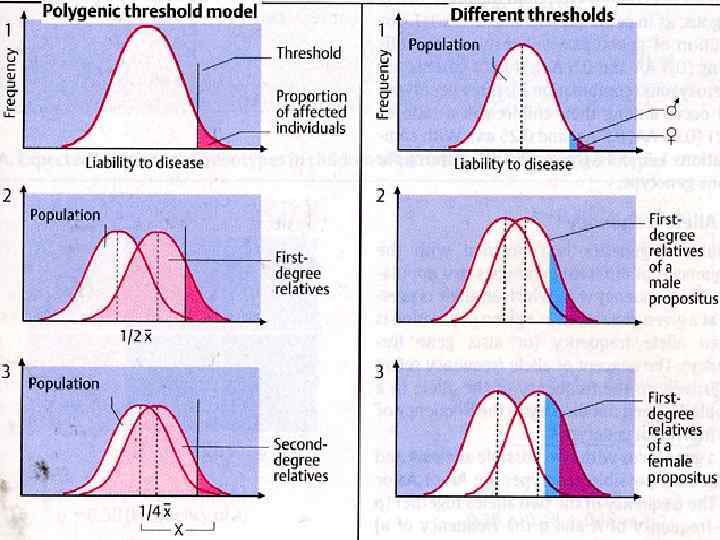

Генетический прогноз при мультифакториальных заболеваниях зависит от следующих факторов: 1) чем ниже частота болезни в популяции, тем выше риск для родственников пробанда; 2) чем сильнее степень выраженности болезни у пробанда, тем больше риск развития болезни у его родственников; 3) риск для родственников пробанда зависит от степени родства с пораженным членом семьи; 4) риск для родственников будет выше, если пробанд относится к менее поражаемому полу;

IY Генетические болезни соматических клеток. • злокачественные новообразования (ретинобластома, опухоль Вильмса), • спорадические случаи врождённых пороков развития. Y Болезни при несовместимости матери и плода по антигенам. гемолитическая болезнь новорождённых.

Медико-генетическое консультирование. Главными задачами МГК являются: 1. Установление точного диагноза наследственной патологии. 2. Пренатальная диагностика. 3. Определение типа наследования заболевания. 4. Оценка величины риска рождения больного ребенка и оказание помощи в принятии решения родителей. 5. Пропаганда медико-генетических знаний среди врачей и населения. Поводом для МГК могут быть: 1. Рождение ребенка с врожденными пороками развития, умственной и физической отсталостью и др. 2. Спонтанные аборты, выкидыши, мертворождения. 3. Близкородственные браки. 4. Неблагополучное течение беременности. 5. Работа супругов на вредном предприятии. 6. Несовместимость супружеских пар по резус-фактору крови. 7. Возраст женщины старше 35 лет, а мужчины — 40 лет.

Медико-генетическая консультация включает 4 этапа: диагноз, прогноз, заключение и совет. Основой для расчеты генетического риска: • теоретические расчеты с использованием генетического анализf, • на основе таблиц эмпирического риска. (при мультифакториальных болезнях, врожденных пороках развития и при хромосомной патологии).


Генетический риск до 5% считается низким и не является противопоказанием к повторному рождению ребенка в семье. Риск от 6 до 20% принято считать средним. Для планирования семьи рекомендуется всестороннее обследование. Генетический риск свыше 20% принято относить к высокому риску. Деторождение в данной семье не рекомендуется. Вместе с тем, все решения по дальнейшему планированию семьи принимаются только супругами.

Принципы лечения наследственных болезней. 1. Симптоматическое лечение. 2. Патогенетическое лечение. 3. Этиотропное лечение
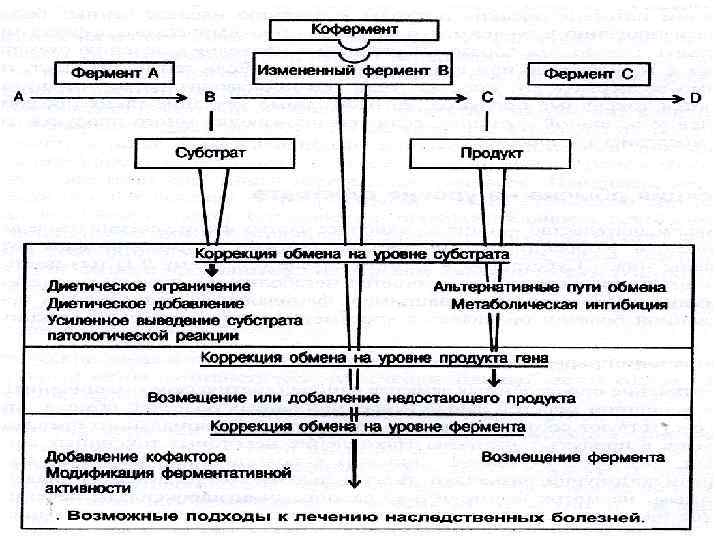

1. Коррекция обмена на уровне продукта гена Получают например инсулин, соматотропин, интерферон. Многие вещества получают от трансгенных животных. А) «сшивки» двух генов, каждый из которых клонирован отдельно. Один ген кодирует нужный белок, другой взят из железы или другого органа, который будет производить этот белок. Б) Гибридная ДНК инъецируется в оплодотворенную яйцеклетку или в эмбрион. В) Яйцеклетки подсаживают в самок, а родившихся животных проверяют на присутствие гибридного гена.


2. Коррекция обмена на уровне ферментов если известен функционально аномальный фермент. Можно вводить кофактор или индуцировать (угнетать) синтез фермента с помощью лекарств, или возмещать недостаток фермента. 3. Этиотропное лечение наследственных болезней достаточно трудная задача может включать: • доставку нормального гена в клетку, • выключение мутантного гена, • обратную мутацию патологического аллеля, • необходимость изменения структуры ДНК во многих функционирующих клетках. Сложности этиотропного лечения очевидны, хотя уже имеются возможности для генной терапи - переноса генетического материала в клетки-мишени индивида.
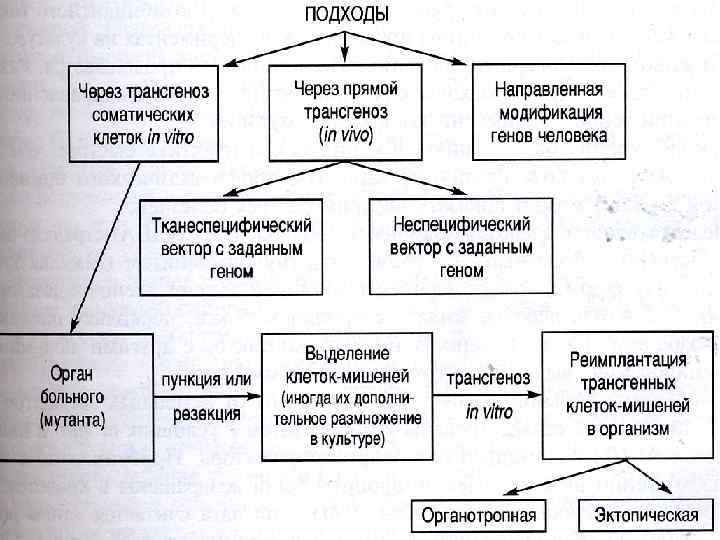

Генная терапия возможна двумя путями: 1. Через трансгеноз изолированных из организма соматических клеток in vitro, затем эти трансгенные клетки-мишени реимплантируют в организм или 2. Через прямой трансгеноз клеток в организме. Прямой Трансгеноз (in vivo) включает создание рекомбинантного генетического вектора с заданным геном, необходимым для лечения. Его вводят в клетки-мишени или в любых клетках происходит трансгеноз с помощью рекомбинантного вектора. Примеры: 1. Девочка 4 лет (США) страдала редкой наследственной болезнью — первичным иммунодефицитом, обусловленным мутацией в гене аденозиндезаминазы (ADA). Т-лимфоциты больной были выделены и стимулированы к росту. Затем in vitro в них был введён ген ADA с помощью ретровирусного вектора и лимфоциты были возвращены в кровоток больной. 14 сентября 1990 г. считается «днём рождения» генной терапии.
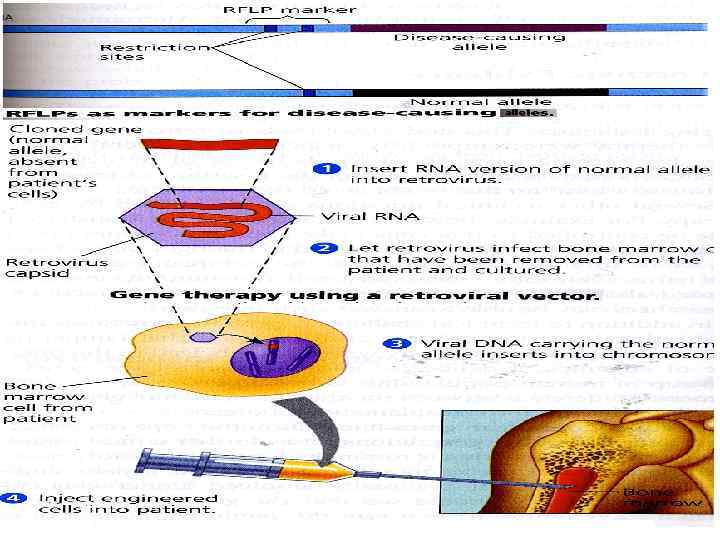

2. Семейная гиперхолестеринемия обусловлена низким уровнем рецепторов ЛПНП (синтезируются в клетках печени), играющих ключевую роль в обмене холестерина. Больной была сделана частичная (около 15%) гепатэктомия. Получили около 6 млн. гепатоцитов. Во время роста в культуре в клетки включали нормальный ген рецептора липопротеидов, используя ретровирусный вектор. Трансгенные гепатоциты были собраны и введены пациентке через катетер в воротную вену. Через несколько месяцев при биопсии печени обнаружили, что новый ген функционирует в некоторых клетках. Содержание ЛПНП в крови пациентки упало на 15— 30%.

3. Рак. Наибольшее число попыток генной терапии злокачественных опухолей связано с введением в клетки резецированной опухоли генов интерлейкина-2 или фактора некроза опухоли. Затем эти клетки вводят подкожно в область бедра. Через 3 нед. удаляют регионарный лимфатический узел (соответственно месту введения смеси трансгенных опухолевых клеток). Культивируют Т-лимфоциты, выделенные из этого узла. Кроме того, размножают лимфоциты из опухолей. Пациенту вводят общую массу лимфоцитов что обеспечивает иммунную реакцию на опухолевые клетки. Так лечили больных злокачественной меланомой, раком почки, запущенным раком разных органов.
09 КОНСУЛЬТИРОВАНИЕ ПРИНЦИПЫ ЛЕЧЕНИЯ.ppt