Основные_законы_массообмена.ppt
- Количество слайдов: 21

Массообменные процессы
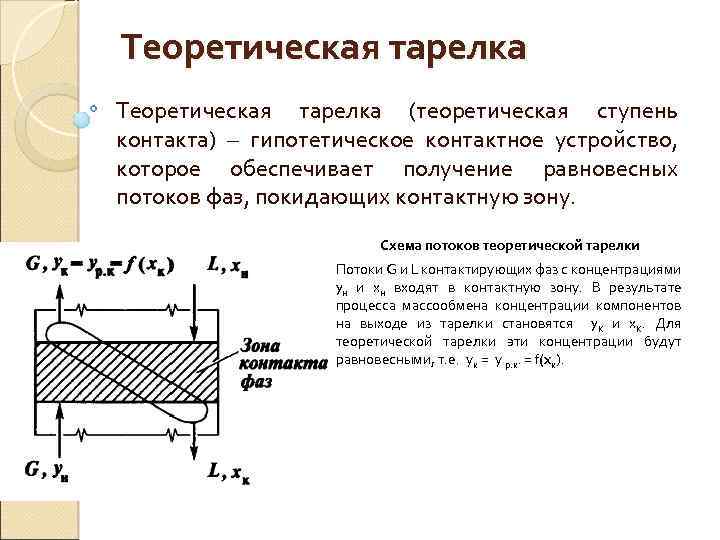
Теоретическая тарелка (теоретическая ступень контакта) – гипотетическое контактное устройство, которое обеспечивает получение равновесных потоков фаз, покидающих контактную зону. Схема потоков теоретической тарелки Потоки G и L контактирующих фаз с концентрациями yн и хн входят в контактную зону. В результате процесса массообмена концентрации компонентов на выходе из тарелки становятся y. К и х. К. Для теоретической тарелки эти концентрации будут равновесными, т. е. ук = у р. к. = f(xк).
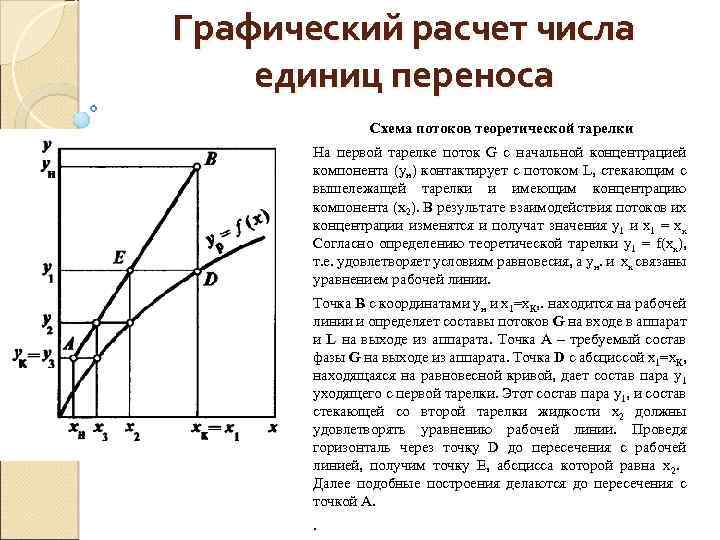
Графический расчет числа единиц переноса Схема потоков теоретической тарелки На первой тарелке поток G с начальной концентрацией компонента (ун) контактирует с потоком L, стекающим с вышележащей тарелки и имеющим концентрацию компонента (х2). В результате взаимодействия потоков их концентрации изменятся и получат значения у1 и х1 = xк Согласно определению теоретической тарелки y 1 = f(хк), т. е. удовлетворяет условиям равновесия, а ун. и хк связаны уравнением рабочей линии. Точка В с координатами ун и х1=х. К, . находится на рабочей линии и определяет составы потоков G на входе в аппарат и L на выходе из аппарата. Точка А – требуемый состав фазы G на выходе из аппарата. Точка D с абсциссой х1=х. К, находящаяся на равновесной кривой, дает состав пара у1 уходящего с первой тарелки. Этот состав пара у1, и состав стекающей со второй тарелки жидкости х2 должны удовлетворять уравнению рабочей линии. Проведя горизонталь через точку D до пересечения с рабочей линией, получим точку Е, абсцисса которой равна х2. Далее подобные построения делаются до пересечения с точкой А. .

Графический расчет числа единиц переноса Число теоретических тарелок зависит от взаимного расположения рабочей и равновесной линий, т. е. от величины движущей силы процесса. При взаимном сближении рабочей и равновесной линии средняя движущая сила процесса уменьшается, а число теоретических тарелок увеличивается. При увеличении расстояния между рабочей и равновесной линиями средняя движущая сила процесса возрастает, что приводит к уменьшению числа теоретических тарелок. Найденное число теоретических тарелок используется для определения высоты контактной зоны аппарата Н или числа реальных тарелок N. В первом случае используют высоту контактной зоны НЭ, эквивалентную одной теоретической тарелке (ВЭТТ) тогда H = HЭNТ. Во втором случае определяют число реальных тарелок NA, используя понятие КПД тарелки: ВЭТТ и КПД тарелки рассчитывают по эмпирическим уравнениям, либо определяют экспериментально

Основные законы массопередачи

Механизмы массопереноса Перенос вещества из одной фазы в другую может происходить по трем механизмам – молекулярной диффузии, турбулентной диффузии и конвективной диффузии. ØПеренос вещества внутри неподвижной фазы осуществляется только путем молекулярной диффузии. ØВ движущейся среде перенос вещества может происходить как молекулярной диффузией, так и конвективным переносом самой средой в направлении ее движения. ØКонвективный перенос вещества под действием турбулентных пульсаций называют турбулентной диффузией.

Уравнение молекулярной диффузии (первый закон Фика) Молекулярная диффузия обусловлена переносом молекул вещества из области с большей его концентрацией в область с меньшей концентрацией и протекает в неподвижной среде или ламинарных пограничных слоях. Перенос вещества при молекулярной диффузии определяется законом Фика: ØКоличество вещества d. M, диффундирующего через слой за время dτ, пропорционально площади слоя d. F, перпендикулярной направлению диффузионного потока, и градиенту концентраций в направлении диффузии dc/dn. или (1) - (минус) указывает, что диффузия протекает в направлении уменьшения концентрации.

Первый закон Фика Молекулярная диффузия обусловлена переносом молекул вещества из области с большей его концентрацией в область с меньшей концентрацией и протекает в неподвижной среде или ламинарных пограничных слоях. Перенос вещества при молекулярной диффузии определяется законом Фика: ØКоличество вещества d. M, диффундирующего через слой за время dτ, пропорционально площади слоя d. F, перпендикулярной направлению диффузионного потока, и градиенту концентраций в направлении диффузии dc/dn. или (1) - (минус) указывает, что диффузия протекает в направлении уменьшения концентрации распределяемого вещества

Первый закон Фика Коэффициент диффузии (коэф-т пропорциональности в законе Фика) Физический смысл коэффициента диффузии – количество вещества, которое диффундирует через единицу поверхности при градиенте концентрации, равном единице. Коэффициент диффузии характеризует способность одного вещества проникать в среду другого. Определяется экспериментально и является справочной величиной. Для газов повышается с ростом температуры и снижается с повышением давления. Для жидкостей пропорционален вязкости жидкости.

Дифференциальное уравнение молекулярной диффузии (второй закон Фика) Выделим в неподвижной среде или ламинарном потоке элементарный параллелепипед с ребрами dx, dy, dz. Рассмотрим перенос вещества вдоль оси Х. Через левую грань площадью dydz входит масса вещества, которая по закону Фика равна через правую грань выходит

Дифференциальное уравнение молекулярной диффузии (второй закон Фика) Приращение массы вещества в объеме параллелепипеда (разность прихода и расхода) для двух других направлений: общее приращение массы вещества в элементарном объеме: (2)

Дифференциальное уравнение молекулярной диффузии (второй закон Фика) С другой стороны это же накопление вещества в объеме может быть выражено через изменение его концентрации во времени (умножение объема на изменение концентрации и на время), т. е. (3) Сопоставляя (2) и (3) получим дифференциальное уравнение молекулярной диффузии В стационарных условиях ( ) получим

Дифференциальное уравнение конвективной диффузии Теория граничного слоя Пусть массообмен между потоками протекает через неподвижную границу раздела фаз. Вещество из ядра потока перемещается к границе раздела фаз непосредственно потоком (конвекцией) и молекулярной диффузией. Поток условно можно разделить на 2 части – ядро потока и граничный диффузионный слой. В ядре потока перенос вещества осуществляется диффузией за счет турбулентности потока и концентрация вещества постоянна. По мере приближения к границе раздела фаз турбулентный перенос затухает, и преобладающим механизмом новится молекулярная диффузия, возникает градиент концентрации. Т. о. пограничный слой – область появления и роста градиента концентраций, т. е. область молекулярной диффузии. При этом конвективный перенос идет в направлении, параллельном движению потока.

Дифференциальное уравнение конвективной диффузии Если рассматривать элементарный концентрации вещества в нем субстанциональную производную: объем фазы, изменение можно записать через общее приращение количества вещества в элементарном объеме: приращение вещества за счет молекулярной диффузии: приравняем левые и правые части, получим дифференциальное уравнение конвективной диффузии.

Массоотдача. Закон Щукарева Для практических расчетов уравнение конвективной диффузии применяют в виде закона массоотдачи Щукарева: Количество вещества d. M, переносимого от поверхности раздела фаз в воспринимающую фазу пропорционально разности концентраций вещества у поверхности раздела фаз (CГ) и в ядре потока воспринимающей среды (CЯ), поверхности фазового контакта (d. F) и времени размерность коэффициента массоотдачи: коэффициент массоотдачи показывает, какое количество вещества передается от поверхности раздела фаз в ядро потока через единицу площади поверхности раздела фаз в единицу времени при разности концентраций, равной 1. Скорость массоотдачи пропорциональна движ. силе – разности концентраций в ядре потока и на границе раздела фаз. β – не физическая константа, а кинетический коэффициент (ρ, μ) зависящий от свойств фазы и гпдродинамических характеристик потока.

Массоотдача. Закон Щукарева Для практических расчетов уравнение конвективной диффузии применяют в виде закона массоотдачи Щукарева: Количество вещества d. M, переносимого от поверхности раздела фаз в воспринимающую фазу пропорционально разности концентраций вещества у поверхности раздела фаз (CГ) и в ядре потока воспринимающей среды (CЯ), поверхности фазового контакта (d. F) и времени размерность коэффициента массоотдачи: коэффициент массоотдачи показывает, какое количество вещества передается от поверхности раздела фаз в ядро потока через единицу площади поверхности раздела фаз в единицу времени при разности концентраций, равной 1. Скорость массоотдачи пропорциональна движ. силе – разности концентраций в ядре потока и на границе раздела фаз. β – не физическая константа, а кинетический коэффициент (ρ, μ) зависящий от свойств фазы и гпдродинамических характеристик потока.

Критериальное уравнение конвективной диффузии Диф. ур. конвективной диффузии описывает процесс перемещения вещества в жидкости конвективной диффузией. Для полного описания этого процесса данное ур-ие необходимо дополнить уравнением, характеризующим условия на границе раздела фаз. Вещество перемещается к границе раздела фаз по механизму конвективной диффузии: У поверхности раздела фаз вещество переходит в другую фазу за счет молекулярной диффузии: поскольку эти уравнения выражают один и тот же поток вещества, то: уравнение характеризует условия на границе раздела фаз. Вместе с уравнением конвективной диффузии является математическим описанием процесса конвективной диффузии.

Критериальное уравнение конвективной диффузии Данная система неразрешима и на практике для описания массообменных процессов пользуются критериальными уравнениями. Выведем основные критерии подобия для массообменных процессов: Уравнение поделим на правую часть. Получим комплекс: вычеркнем символы дифференцирования, направления, разности, получим диффузионный критерий Нуссельта

Критериальное уравнение конвективной диффузии Делим на правую часть Критерий Фурье характеризует скорость диффузионного потока массы во времени. Необходим только для характеристики нестационарных процессов

Критериальное уравнение конвективной диффузии Диффузионный критерий Пекле обычно представляют в виде произведения критериев Рейнольдса и Прандтля: для расчета коэффициентов выражения вида массоотдачи обычно используют
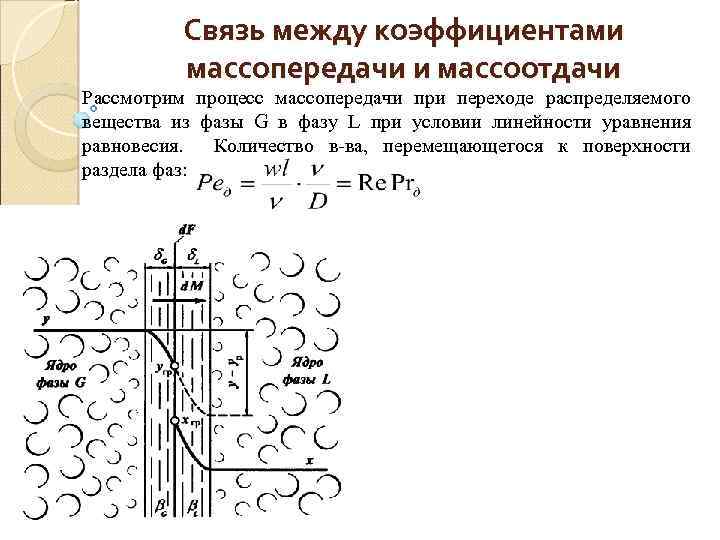
Связь между коэффициентами массопередачи и массоотдачи Рассмотрим процесс массопередачи при переходе распределяемого вещества из фазы G в фазу L при условии линейности уравнения равновесия. Количество в-ва, перемещающегося к поверхности раздела фаз:
Основные_законы_массообмена.ppt