Лекция для курсантов ПДО ОмГМА Микробиология дифтерии и


Лекция для курсантов ПДО ОмГМА Микробиология дифтерии и коклюша

Микробиология дифтерии
Классификация коринебактерий Отдел «Грамположительные» бактерии Подотдел 4: Бактерии с высоким % содержания G+C Порядок Actinomycetales Подпорядок Corynebacterineae Семейство Corynebacteriaceae (коринеформные бактерии) Род Corynebacterium

Род Corynebacterium - Corynebacterium diphtheriae и большая группа близких по морфологическим и биохимическим свойствам МО рода Corynebacterium называют коринеформными бактериями или дифтероидами (Гр+палочки, неподвижные с утолщениями на концах) Составляют 3 экологические группы (патогены Ч и Ж, патогены Р, непатогенные)

Коринебактерии - возбудители дифтерии Дифтерия является острой инфекцией верхних отделов дыхательных путей, преимущественно детского возраста, вызываемой токсинпродуцирующими штаммами Corynebacterium diphtheriae. Значительно реже аналогичное по клинической симптоматике заболевание могут вызывать токсигенные штаммы Corynebacterium ulcerans

Коринебактерии - возбудители дифтерии Эпидемиология. Резервуар – больной человек, реконвалесцент, бактерионоситель. Пути передачи: воздушно-капельный (основной) Контактно-бытовой Сезонность – осенне-зимняя. Устойчивость во внешней среде – хорошо сохраняется при низких температурах, в высушенном состоянии (в слюне,слизи, в пыли)
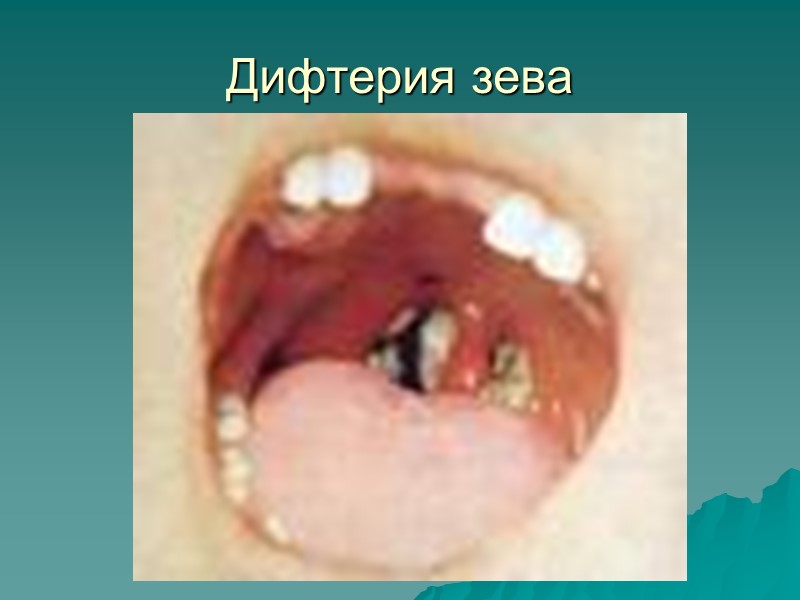
Коринебактерии - возбудители дифтерии Дифтерия – характеризуется: интоксикацией организма дифтерийным токсином фибринозным дифтиридическим воспалением в месте локализации возбудителя (phther – плёнка)

Дифтерия зева

Морфология и тинкториальные свойства Corynebacterium diphtheriae Тонкие полиморфные палочки с булавовидными концами, часто с валютиновыми включениями. Имеют микрокапсулу, фимбрии. Тинкториальные свойства - Гр+палочки. Окраска мазков: - по Граму - по Нейссеру ( хризоидином или везувином) - по Лёффлеру (метиленовым синим)

Культуральные свойства Corynebacterium diphtheriae На простых средах не растут Высоко требовательны к питательным средам с обязательным наличием крови или сыворотки крови. Растут при 37 0 С, в течение 24-48 часов Corynebacterium diphtheriae mitis обладает способностью вызывать гемолиз эритроцитов Среды для культивирования: Кровяно-теллуритовый агар – КТА, Коринебакагар – КБА, Маклеода (теллурит-шоколадный агар) Лёффлера, Ру, 5% КА.

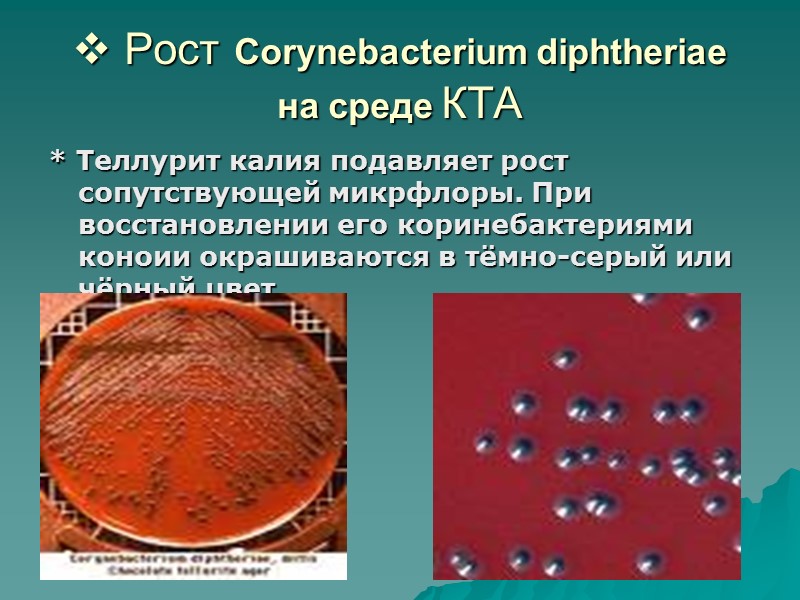
Рост Corynebacterium diphtheriae на среде КТА * Теллурит калия подавляет рост сопутствующей микрфлоры. При восстановлении его коринебактериями коноии окрашиваются в тёмно-серый или чёрный цвет

Рост Corynebacterium diphtheriae на среде КТА

Биотипы Corynebacterium diphtheriae: gravis, mitis, intermedius Биотипы отличаются по морфологии, Аг и б/х свойствам, тяжести заболеваний у человека. Corynebacterium diphtheriae gravis – вызывает более тяжёлое течение заболеваний. На КТ средах растёт в виде колоний R-формы – крупные с неровными краями и радиальной исчерченностью («маргаритка»). Corynebacterium diphtheriae mitis – вызывае преимущественно спорадические лёгкие заболевания. На КТ средах растут в S-форме в виде мелких гладких колоний с ровными краями. Corynebacterium diphtheriae intermedius – средней тяжести заболевания. Рост на средах в виде мелких колоний в S или R- формах.
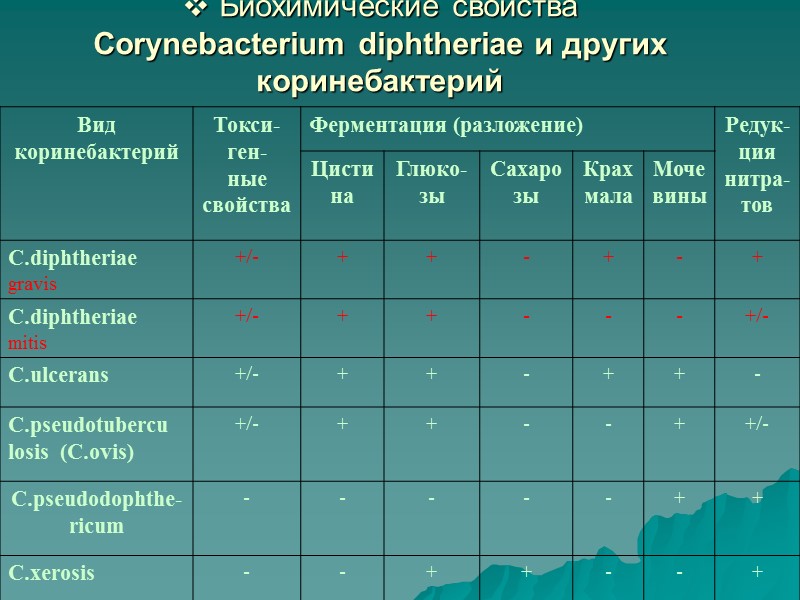
Биохимические свойства Corynebacterium diphtheriae Ферментируют глюкозу (+), мальтозу (+). Не ферментируют сахарозу (-). Не образуют уреазу (проба Заксе на мочевину – отрицательная). Обладают цистиназной активностью (Расщепляют цистин на среде Пизу)

Биохимические свойства Corynebacterium diphtheriae и других коринебактерий

Факторы патогенности Corynebacterium diphtheriae Токсигенные штаммы Corynebacterium diphtheriae продуцируют сильный экзотоксин – термобильный, высокотоксичный иммуногенный белок. Потенциально токсигенными являются C.ulcerans и C.pseudotuberculosis. Токсин вызывает необратимое блокирование удлинения полипептидной цепи, т.е. любого белкового синтеза. Поражаются определённые системы (симпатико-адреналиновая, сердце, кровеносные сосуды, периферические нервы. Отмечаются структурные и функциональные нарушения миокарда, демиелинизация нервных волокон, приводящая к параличам и парезам).

Факторы патогенности Corynebacterium diphtheriae Дифтерийный токсин – результат лизогении b-фагом или другими коринефагами, которые содержат структурный ген (tox-ген) молекулы токсина низкой внеклеточной концентрации железа. Т.е. способность к токсинообразованию проявляют лишь лизогенные штаммы, инфицированные бактериофагом (b-фагом), несущим ген tox, который кодирует структуру токсина, несущего гены умеренного профага в своей хромосоме.

Антигенная структура Corynebacterium diphtheriae Имеют: - межродовой О – Аг (Полисахаридный Аг клеточной стенки). Обуславливает неспецифические перекрёстные реакции с МО данного семейства (с микобактериями, актиномицетами) - видовой К – Аг (Поверхностные капсульные белки). Обладают видовой и иммуногенной специфичностью. Выделено 11 сероваров, из них 1-5 и 7 С.gravis.

Иммунитет и профилактика Иммунитет - стойкий, преимущественно антитоксический. Для количественного определения уровня антитоксического иммунитета ранее применялась проба Шика. Дифтерийный токсин вводился внутрикожно. Профилактика – массовая иммунизация населения различными препаратами, содержащими анатоксин – АКДС, АДС, АДС-М, АД и АД-М.

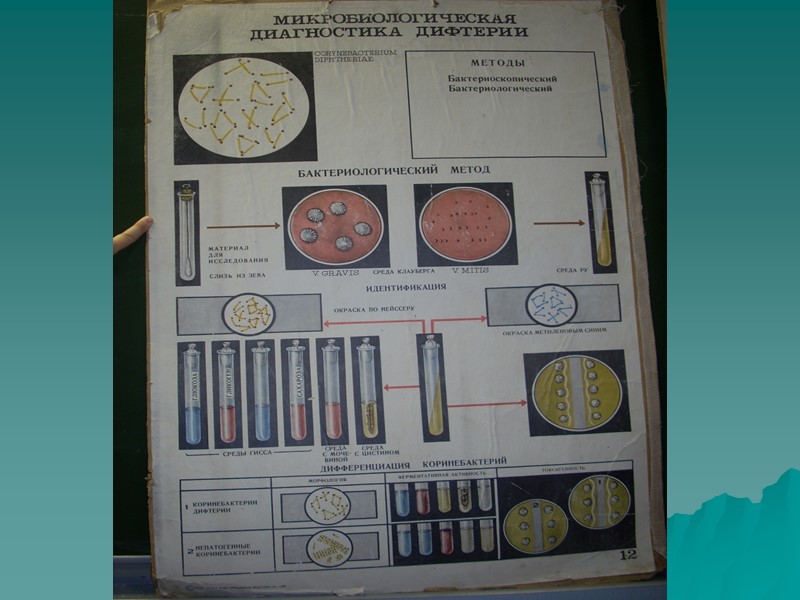
Лабораторная диагностика возбудителей дифтерийной инфекции Основной метод диагностики – бактериологический, применяемый для выявления больных, бактерионосителей, контактных. Материал для исследования: Мазки со слизистой оболочки зева и носа, плёнки с поверхности миндалин и носоглотки. Кровь, сыворотка крови. Секционный материал слизистой оболочки зева и носа, плёнки с поверхности миндалин Материал забирается стерильными тампонами вмонтированными в пробирки; баночки; флаконы.


Методы исследования 1. Бактериоскопические методы для ориентировочного заключения: Окраска по Граму, метиленовой синью, Лёффлеру, Нейссеру; Окраска корифосфином (люммикроскопия)

Окраска по Граму или метиленовым синим Палочки сине-голубые с тёмно-синими включениями в виде булавовидных утолщений, расположены под углом

Окраска зёрен валютина по методу Нейссера: 1. На фиксированные мазок нанести ацетат синьки Нейссера на 2 - 3 мин. 2. Добавить раствор Люголя на 10-30 сек. 3. Промыть водой. 5. Докрасить мазок водным раствором визувина или хризоидина 0,5 - 1 мин. 6. Промыть, высушить, микроскопировать. Зёрна валютина представляют собой включения полифосфатов, имеющих щелочную реакцию, поэтому избирательно воспринимают ацетат синьки, окрашиваясь в тёмно-синий цвет. * (При использовании красителей хризоидина или везувина зёрна валютина окрашиваются в жёлто-коричневый цвет). Цитоплазма клетки, обладающая кислой реакцией, воспринимает щелочной краситель везувина и окрашивается в жёлтый цвет.

Красители хризоидин и синька Нейссера для окраски зёрен валютина по методу Нейссера:
Окраска зёрен валютина Окраска зёрен валютина по методу Лёффлера На фиксированный мазок наливают на 3-10 мин раствор метиленового синего по Лёффлеру. Сливают краску Ополаскивают дистиллированной водой. Просушивают, можно аккуратно промакнуть фильтровальной бумагой. Пропись раствора метиленового синего по Лёффлеру: - Насыщенного спиртового раствора метиленового синего – 30 мл - Дистиллированной воды – 100 мл 1% раствора едкого кали – 1 мл Раствор стойкий. При хранении его красящая способность и свойство давать метахроматическое окрашивание нуклеиновых соединений повышается за счёт образования азуров.

Окраска зёрен валютина по методу Нейссера и Лёффлера : Зёрна валютина тёмно-синего цвета по методу Лёффлера. При использовании красителей хризоидина или везувина по методу Нейссера, зёрна валютина окрашиваются в жёлто-коричневый цвет. Цитоплазма клетки окрашена в жёлтый цвет Палочки находятся под углом друг к другу Окраска по методу Окраска по методу Лёффлера Нейссера

Методы исследования 2. Бактериологический метод. I этап: Первичный посев на элективные среды с теллуритом и 5% КА для накопления коринебактерий и изучения гемолитической активности. II этап: Выделения чистой культуры III этап: 1. Идентификация выделенной чистой культуры (По мазкам, культуральным признакам, по биохимическим признакам). 2. Определение токсигенных свойств (Реакция преципитации в агаре, ИФА). 3. ПЦР с целью обнаружения tox-гена. 4. Определение чувствительности к антибиотикам 5. Фаготипирование для дифференциации штаммов коринебактерий дифтерии

Рост Corynebacterium diphtheriae на КБА

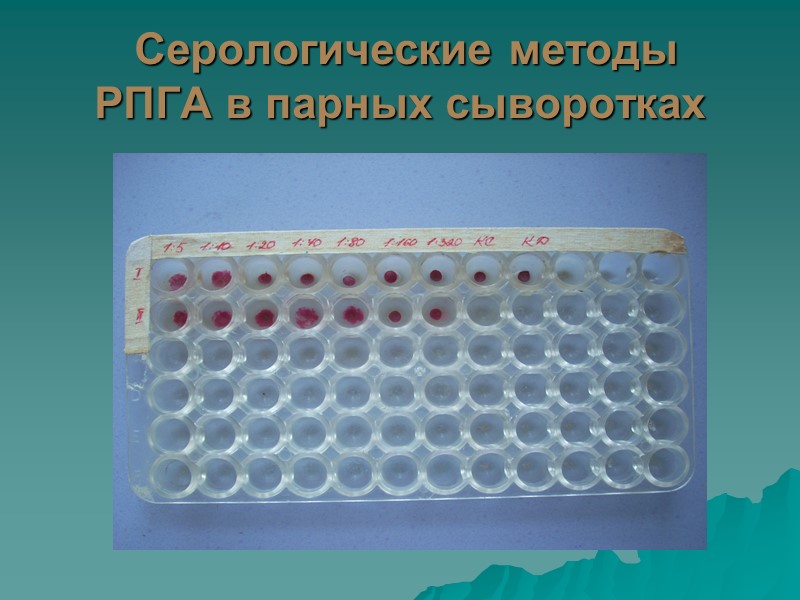
Методы исследования 3. Серологические и иммунологические методы: Определение дифтерийного токсина с помощью РНГА в чистых и смешанных культурах с эритроцитарным дифтерийным антительным диагностикумом. Определения уровня антитоксина в сыворотке больного РПГА с диагностикумами эритроцитарными дифтерийными антигенными сухими. Определение титра Аt к дифтерийному токсину в сыворотке крови в реакции нейтрализации (РН) на культуре клеток. Агглютинация с противодифтерийной сывороткой C.d.gravis и C.d.mitis. Выявление антибактериальных и антитоксических At различных классов (Yg А, М, G) в ИФА.
Серологические методы РПГА РПГА « + » РПГА « - »
Серологические методы РПГА в парных сыворотках
Методы исследования Экспресс-методы: биохимические и молекулярно-билогические – метод генетических зондов и ПЦР для выявления фрагмента А tox-гена. Биологический метод: определение токсигенности на морских свинках.

Тест иммунопреципитации Элека Штаммы способные вызывать заболевания обладают токсигенными свойствами Тест наиболее часто используемый микробиологическими лабораториями всего мира - фенотипический метод определения токсигенности
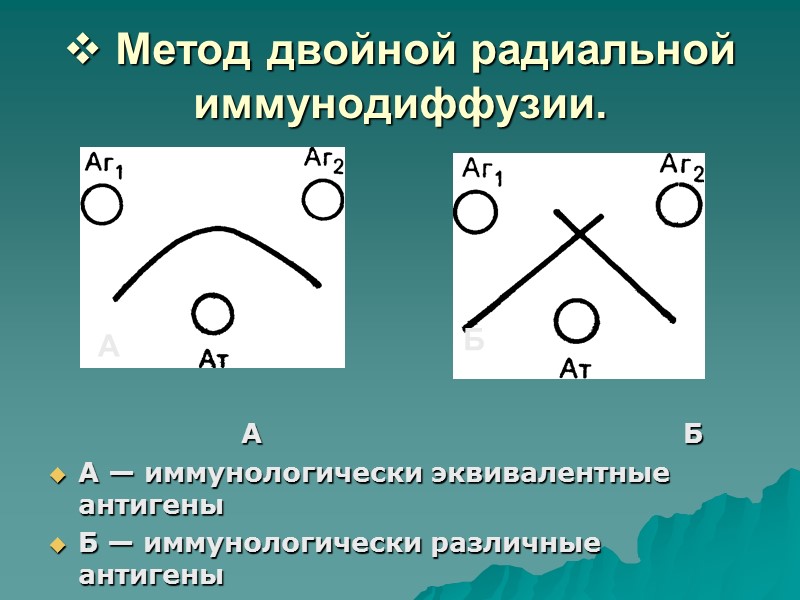
Тест иммунопреципитации Элека

Тест иммунопреципитации Элека (иммунодиффузия) в геле - фенотипический метод определения токсигенности

Тест иммунопреципитации Элека (иммунодиффузия) в геле Образование линий («усов» преципитации - Диски пропитанные антитоксической дифтерийной сывороткой (At) Бляшки испытуемой культуры (Agи ) Контрольные токсигенные штаммы (Agк )

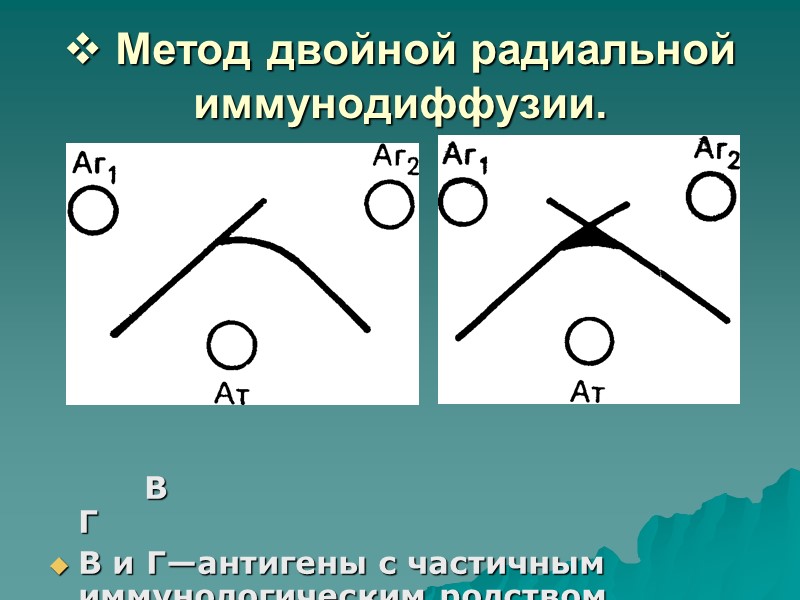
Метод двойной радиальной иммунодиффузии. А Б А — иммунологически эквивалентные антигены Б — иммунологически различные антигены А Б

Метод двойной радиальной иммунодиффузии. В Г В и Г—антигены с частичным иммунологическим родством

Диагностические препараты

Микробиология коклюша и паракоклюша
Основные регламентирующие и методические НД

МР МЗ СССР 1984 «Коклюш и паракоклюш»

МР МЗ СССР 1984 «По бактериологическому и серологическому исследованиям при коклюше и паракоклюше».

СП 3.1.2.1320-03 «Профилактика коклюшной инфекции».

МР «Коклюш у привитых детей, клиническая и лабораторная диагностика» С-Петербург. 2003г.


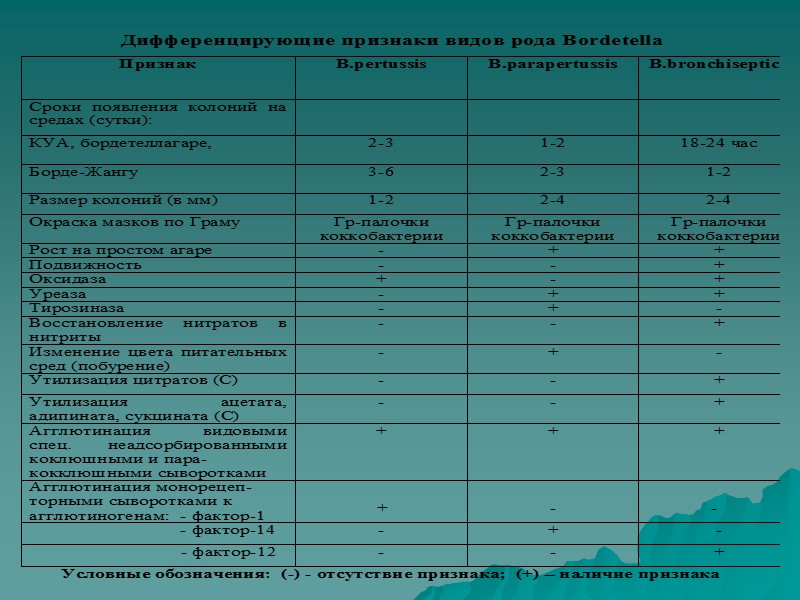
Род Bordetella Семейство Halobacteriaceae Клинический синдром коклюша могут вызвать 3 вида бактерий рода Bordetella: Bordetella pertussis – возбудитель острого инфекционного заболевания коклюша сопровождающегося воспалением гортани, трахеи и бронхов и приступообразным кашлем. Bordetella parapertussis - возбудитель паракоклюша Bordetella bronchoseptica - возбудитель коклюшеподобного заболевания собак, кошек и кроликов. У людей может вызывать заболевания по типу ОРВИ
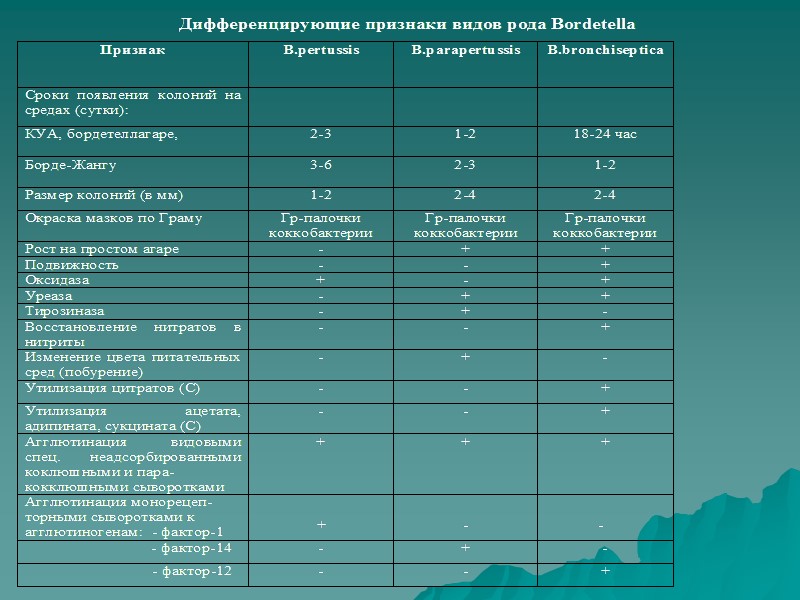
Морфология и тинкториальные свойства: Грам «-» отрицательные мелкие овоидные палочки - коккобациллы (0,2-0,5 мкм х0,5-2,0 мкм). Строгие аэробы B. pertussis и B. parapertussis неподвижные, за исключением B. bronchoseptica (жгутики). У B. pertussis обнаружены пили, принимающие участие в адгезии. B. pertussis имеют капсулу, у B. parapertussis её нет. Спор не образуют Во внешней среде неустойчивы.

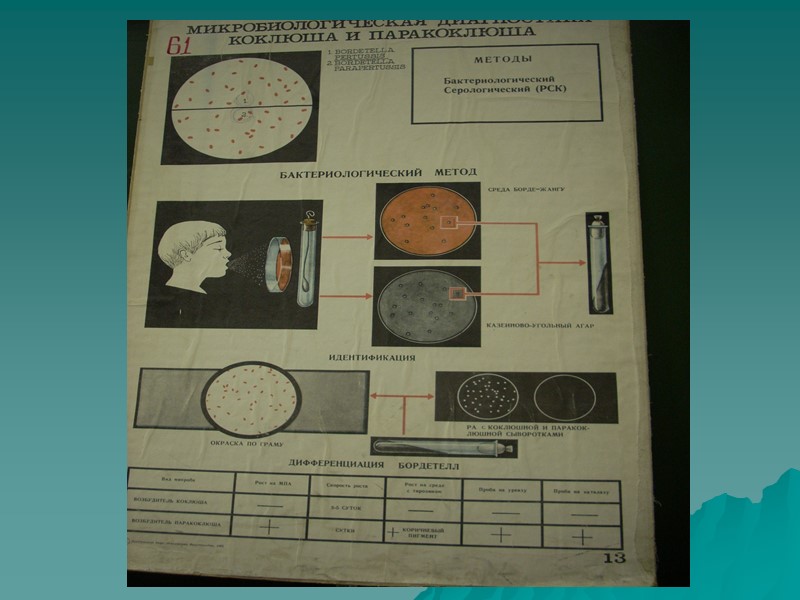
Культуральные свойства Высоко требовательны к питательным средам и условиям роста, особенно возбудитель коклюша. Для первичного выделения гемофильных бордетелл используется: - среда Борде-Жангу (картофельно-глицериновый агар), полусинтетические среды –КУА (казеиново-угольный агар), синтетический – Бордеагар.

Культуральные свойства На перечисленных средах бордетеллы вырастают в виде характерных колоний: Температура выращивания 35-37 0 С. Колонии формируются в разные сроки, более продолжительный срок у B. pertussis (3 сутки): - На среде Борде-Жангу,– выпуклые, гладкие, блестящие, серебрянного цвета, напоминающие капли ртути окружённые зоной гемолиза; - На КУА - выпуклые, гладкие, серого цвета с жемчужным, желтоватым или беловатым оттенком. Колонии маслянистые, легко снимаются петлёй. - B. parapertussis – за счёт образования пигмента вызывает потемнение сред с кровью, образует тёмную подложку. B. parapertussis и B. вronchoseptica менее прихотливы к питательным средам. B. pertussis нуждается в сложных питательных средах B. вronchoseptica способна также расти в фосфатно-солевом буфере и пресной воде.
Биохимические свойства B. pertussis - наименее активна ферментативно – оксидазоположительна. B. parapertussis – вырабатываезы.т ферменты тирозиназу и уреазу и не образует оксидазу. B. Bronchoseptica – вырабатывает уреазу, оксидазу, утилизируют цитраты, восстанавливают нитраты в нитриты.


Антигенные свойства Родовые Видовые – О Аг Факторы патогенности 1.Экзотоксин термолабильный (тропизм к нервным тканям и сосудистой) 2. Эндотоксин термостабильный (токсическое и сенсибилизирующее действие 3. Трахеальный цитотоксин – повреждение мерцательного эпителия
Лабораторная диагностика Материал для исследования: мокрота, слизь из носоглотки Материал для исследования забирается из носоглотки: стерильными мягкими тампонами (сухим и увлажнённым) вмонтированными в пробирки, под контролем шпателя, которым прижимается корень языка; Методом «кашлевых пластинок» после механического раздражения сухим тампоном ребёноку подносят открытую чашку с КУА и держат в течение 6-8 кашлевых толчков.

Методы диагностики Бактериоскопический метод практически не используется. Чаще используется эспресс-метод – иммунофлюоресцентный.
30-difteriya_i_koklyush.ppt
- Количество слайдов: 60

