Лекция 8 Еще не известно, что было бы


Лекция 8 Еще не известно, что было бы с возом, если бы не принципиальность Лебедя, Рака и Щуки. Н. Левицкий Группа веществ, изолируемых из биологического материала экстракцией и сорбцией.
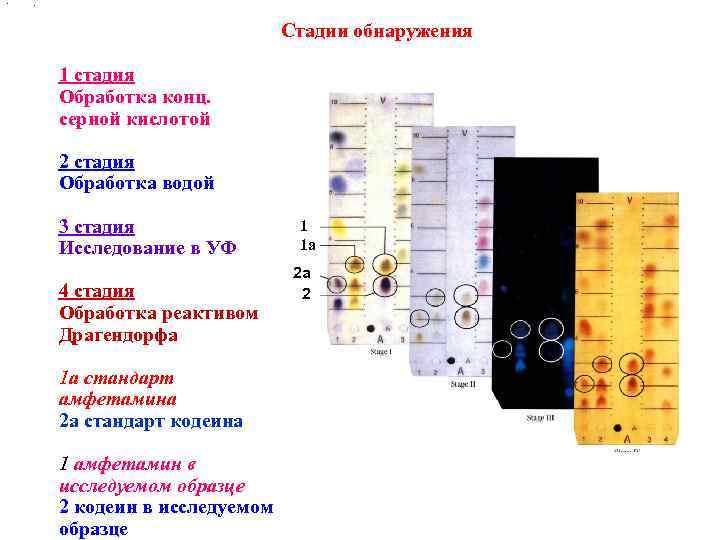
• . Стадии обнаружения 1 стадия Обработка конц. серной кислотой 2 стадия Обработка водой 3 стадия 1 Исследование в УФ 1 а 2 а 4 стадия 2 Обработка реактивом Драгендорфа 1 а стандарт амфетамина 2 а стандарт кодеина 1 амфетамин в исследуемом образце 2 кодеин в исследуемом образце
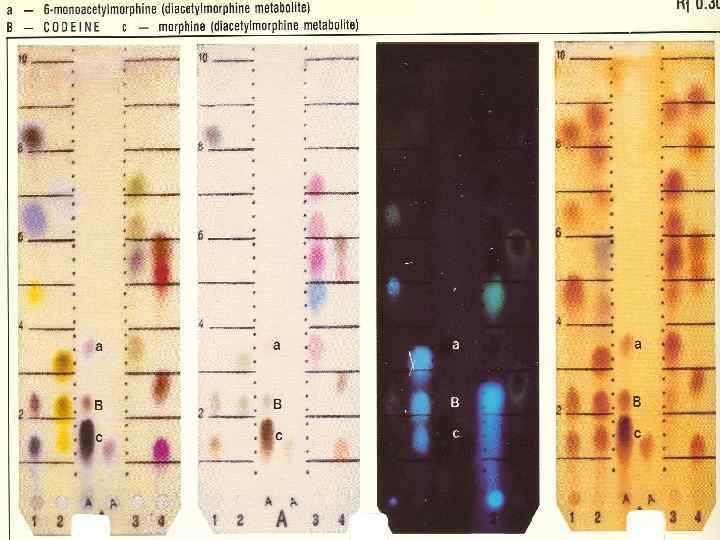
.

• Метод ТСХ получил наиболее широкое распространение из хроматографических методов благодаря своей доступности и простоте выполнения, и в тоже время высокой эффективности, чувствительности, экспрессности, достаточной избирательности (специфичности).

Ионообменная хроматография • Ионообменная хроматография – жидкостная хроматография, основанная на различной способности разделяемых ионов к ионному обмену с фиксированными ионами сорбента, образующимися в результате диссоциации ионногенных групп.

• Для разделения катионов используют катиониты (элюент р-р кислоты); • для разделения анионов – аниониты (элюент – р-р щелочи). • Разделение ионов регулируют подбором оптимальных значений р. Н элюента. • Варьируя р. Н элюента, можно резко изменять степень ионизации компонентов разделяемой смеси (сорбатов) и, следовательно, время их удерживания, добиваясь необходимой селективности разделения.

• Детектирование осуществляют с помощью любого детектора, применяемого в жидкостной хроматографии. Наиболее универсален для ионных соединений кондуктометрический детектор.

• Высокоэффективная ионная хроматография используется для диагностики заболеваний и отравлений, анализируют биологические жидкости (плазма крови, моча, лимфа), смесей нуклеотидов, нуклеозидов, пуриновых и пиримидиновых оснований и их метаболитов. • В препаративных целях используют для выделения индивидуальных алкалоидов, антибиотиков, ферментов и т. д.

Ионит • Ионит можно представить себе состоящим из каркаса или матрицы, молекулы которой способны к ионному обмену. • Матрица несет положительный или отрицательный заряд, который компенсируется зарядом ионов противоположного знака, так что в целом ионит нейтрален.

• . Заряд матрице придают группы атомов, обычно это кислотные или основные остатки молекул, например: │ –SO 3 - или -N+- │ Ионы, компенсирующие заряд матрицы, получили название противоионов. Противоионы обладают в пределах матрицы определенной подвижностью, что и обусловливает способность ионита к обмену.

• Если ионит с провоионами А поместить в раствор, содержащий ионы В, то ионы А покидают ионит, переходят в раствор, а в ионит в строго эквивалентном количестве поступают ионы В из раствора. • Эта модель показывает, что ионный обмен основывается на статистическом распределении противоионов между ионитом и раствором.

• RAn-H+ + Na+ + Cl- ←→ RAn-Na+ + H+ +Cl- катионный обмен • RKt+OH- + Na+ + Cl- ←→ RKt+Cl- + OH- +Na+ анионный обмен • R- матрица ионита; • An-, Kt+ - фиксированные ионы матрицы.

Группа веществ, изолируемых из биологического материала экстракцией и сорбцией. Учение без размышления бесполезно, но и размышление без учения опасно. /Конфуций/

• К этой группе веществ относятся соединения кислотного, нейтрального и основного характера, различные по своему химическому строению. • Наибольшее токсикологическое значение в настоящее время имеют:

Вещества кислотного характера: 1. Органические кислоты: бензойная, салициловая, ацетилсалициловая, пикриновая. 2. Барбитураты: барбитал, барбамил, фенобарбитал, этаминал натрия и др.

Вещества нейтрального характера: 1. Небарбитуровые снотворные: ноксирон, тетридин. 2. Сердечные гликозиды. 3. Многоатомные фенолы: гидрохинон, пирогаллол. 4. Полинитропроизводные: м-динитробензол, динитротолуолы, тринитротолуол.

Вещества основного характера: • Алкалоиды: производные пиридина и пиперидина (жидкие алкалоиды); • тропана (атропин, кокаин и др. ); • хинолина (хинин); • изохинолина (опийные); • индола (стрихнин, бруцин, резерпин); • пурина (кофеин, теобромин, теофиллин); • ациклические (эфедрин) и др.

Синтетические вещества основного характера • производные пиразола (антипирин, анальгин); • производное пиперидина (промедол); • производные аминокислот ароматического ряда (новокаин, новокаин-амид); • производные фенотиазина; • производные бензодиазепина и др.

• Изолирование «нелетучих» ядов из биологического материала основано на различной растворимости их ионизированной и молекулярной форм в воде и органических растворителях и на коэффициенте распределения молекулярной формы между водной и органической фазами. СО КР = ------- СВ • КР – коэффициент распределения молекулярной формы; • С – концентрация вещества в водной и органической фазах

• При исследовании тканевого материала (внутренние органы трупа) изолирование состоит из двух стадий: 1. извлечение яда из твердой фазы (объект) в водную, 2. извлечение яда из водной фазы в органический растворитель. • При исследовании биологических жидкостей (кровь, моча, промывные воды) необходимость в первой стадии изолирования отпадает и сразу проводят экстракцию в органический растворитель.

• На первой стадии на эффективность изолирования вещества влияют такие факторы: 1. растворимость яда в используемом экстрагенте. Поскольку на первой стадии используют полярные растворители (воду), яд должен находится в водорастворимом (ионизированном) состоянии. 2. Значительно влияет природа экстрагента, его количество, время и кратность экстракции.

• К экстрагенту предъявляются следующие основные требования: - способность легко проникать в клетки тканей; - высокая растворяющая способность (по отношению к яду); - селективность (по отношению к анализируемым соединениям), чтобы исключить загрязнение балластными веществами – жирами, белками, пигментами и др.

3. Степень измельченности объекта также играет важную роль, доступ растворителя к искомому веществу должен быть максимальным. Вторая стадия изолирования заключается в выделении из водного извлечения путём экстрагирования органическим растворителем, не смешивающимся с водой, при различных р. Н среды.

• Вещества можно разделить на 2 подгруппы: 1. Вещества, экстрагируемые органическими растворителями из кислого раствора (вещества кислотного, нейтрального и частично слабоосновного характера). 2. Вещества, экстрагируемые из щелочного раствора (вещества основного и частично слабоосновного характера).

• Для веществ нейтрального характера, не способных к ионизации, практически не требуется создания определённого значения р. Н, т. к. они экстрагируются органическим растворителем в молекулярной форме из любой среды.

Общие и частные методы изолирования • Частное исследование – анализ на какое-то определенное вещество или группу веществ. Например: на алкалоиды, на барбитураты или на одно конкретное вещество. При частном исследовании метод изолирования подбирается с учётом физико- химических свойств того соединения (или группы соединений), на которое производится анализ.

Общий анализ включает исследование на несколько групп веществ (3 группы), подлежащих обязательному судебно- химическому исследованию. В этом случае используют общие для всей группы веществ методы изолирования. • К общим методам относятся: 1. Изолирование подкисленным этанолом. 2. Изолирование водой, подкисленной щавелевой кислотой.

Метод Стаса-Отто. - Настаивание в течение суток измельчённого объекта этанолом, подкисленным щавелевой кислотой до р. Н 2 -3. Спирт берётся в количестве, необходимом для покрытия объекта. Спиртовое извлечение сливается и вся операция повторяется трёхкратно;

• упаривание объединенных спиртовых извлечений при температуре 40 -50 0 С до густого остатка, в который по каплям добавляют абсолютный этанол для коагуляции белков. • Осадок отфильтровывают и всю операцию осаждения повторяют по мере необходимости до полного удаления белковых соединений;

Упаривание фильтрата при той же t до густого остатка и разбавляют горячей водой для удаления смолистых веществ, жиров и пигментов. Осадок отфильтровывают. - Экстрагирование веществ кислого, нейтрального и слабоосновного характера из водного фильтрата хлороформом при р. Н=2 (трёхкратная экстракция), отделение органической фазы и концентрирование полученного извлечения упариванием (фракция А, «кислое» извлечение).

Подщелачивание оставшегося после разделения фаз водного слоя до р. Н 9 -10, экстрагирование веществ сильноосновного характера (трёхкратная экстракция) хлороформом, отделение органической фазы и концентрирование упариванием (фракция Б, «щелочное» извлечение).

Достоинства метода: 1. Метод универсален, т. к. этанол является хорошим растворителем для многих веществ этой группы. 2. Метод предусматривает очистку извлечения от балластных веществ, в результате чего получаются чистые хлороформные извлечения, не дающие эмульсий при экстрагировании веществ из водной фазы хлороформом. Метод даёт возможность изолировать до 30 % барбитуратов и 20 -25 % алкалоидов.

Недостатки метода: Длительность (8 -10 дней) и многостадийность. Большое количество операций, значительные потери искомых веществ. 2. Дороговизна метода, на 1 исследование тратится около 500 мл этанола.

Изолирование по методу Васильевой Настаивание измельчённого объекта с водой, подкисленной щавелевой кислотой до р. Н = 2 - 3, в течение двух часов. Вода берётся в количестве 1: 2 по отношению к навеске объекта. Водное извлечение фильтруют;

Экстрагирование веществ кислого, нейтрального и слабоосновного характера из водного фильтрата хлороформом при р. Н=2 (трёхкратная экстракция), отделение органической фазы и концентрирование полученного извлечения упариванием (фракция А, «кислое» извлечение);

подщелачивание оставшегося после разделения фаз водного слоя раствором аммиака до р. Н 9 -10, эктрагирование веществ основного характера трёхкратной экстракцией хлороформом, отделение органической фазы и концентрирование упариванием (фракция Б, «щелочное» извлечение).

Преимущества: 1. Быстрота (анализ можно провести в течение одного дня). 2. Меньшее количество операций, меньше потери искомых веществ (алкалоиды извлекаются на 30 -40 %). 3. Экономичность и дешевизна, т. к. дорогой спирт заменен водой.

Недостатки: Недостатком метода является образование стойких эмульсий при экстрагировании веществ из водной фазы хлороформом, особенно при исследовании гнилостного биоматериала, так как метод не предусматривает очистки извлечений.

Изолирование барбитуратов подщелоченной водой (метод П. Валова) • Измельченный объект в течение 30 минут настаивают с водой, подщелоченной 20 % раствором натрия гидроксида до р. Н=12 и более. • Очистка от белков водного извлечения путём насыщения натрия вольфроматом, раствор фильтруют. • Подкисляют серной кислотой до р. Н =2 и экстрагируют диэтиловым эфиром, эфирное извлечение концентрируют упариванием.

• Выход составляет от 50 % до 90 %, в зависимости от вида барбитурата. Поскольку очищают от белков, метод даёт достаточно чистые извлечения, что повышает качество последующего анализа. • Недостаток – вместе с белками соосаждаются барбитураты, поэтому в последней модификации серная кислота заменена на натрия гидросульфат, что увеличивает выход искомых веществ.

Метод Крамаренко – частный метод изолирования алкалоидов водой подкисленной кислотой серной. • Настаивание измельченного объекта с водой, подкисленной 20 % раствором кислоты серной до р. Н=2 -3, в течение 2 -х часов. • Вода берётся в количестве 1: 2 по отношению к навеске объекта. • Водное извлечение фильтруется. • Операция повторяется двукратно.

• Очистка водного извлечения от белковых соединений путём насыщения его аммония сульфатом, настаивания в течение часа и фильтрования образовавшегося осадка. • Очистка фильтрата от жиров, смол, пигментов путём экстракции эфиром. • Эфирное извлечение отбрасывают.

• Подщелачивание водного извлечения 20 % раствором натрия гидроксида и экстрагирование веществ основного характера хлороформом при р. Н=9 -10 (трёхкратная экстракция), отделение органической фазы и концентрирование полученного извлечения упариванием. • Метод достаточно быстрый. Преимуществом является хорошая очистка извлечений от соэкстрактивных веществ.

Аспирин. Салициловая кислота • Аспирин. Быстро всасывается в желудке и тонком кишечнике; • деацетилируется в плазме крови, с мочой выводится 80 % в течение 24 -48 ч; • биодоступность приеме внутрь составляет 68 %, степень связывания с белками плазмы - 49 %; • смертельная доза 30 -40 г, для детей 10 г; • токсическая концентрация в крови 150 -300 мг/л, смертельная – 500 мг/л.

• Избирательное токсическое действие: психотропное, гемотоксическое. • Клинические признаки и диагностика: возбуждение, эйфория. Головокружение, шум в ушах, ослабление слуха, расстройство зрения. Возможно развитие периферических отеков.

Продукты биотрансформации салициловой кислоты: • 2, 5 -дигидроксибензойная кислота; • 2, 3, 5 -тригидроксибензойная кислота; • глюкурониды салициловой кислоты; • сочетание алициловой кислоты с глицином. Аспирин в организме дает такие же метаболиты.

Предварительная проба на салициловую кислоту в биологических жидкостях • Проводят, применяя реактив Триндлера: к 1 мл мочи прибавляют 2 -3 капли реактива Триндлера, появление пурпурной окраски указывает на наличие салициловой кислоты или аспирина в моче. • Реактив Триндлера: 4 г хлорида ртути (II) при нагревании растворяют в 85 мл воды. Раствор охлаждают, прибавляют 12 мл 1 н раствора НСI и 4 г железа (III) нитрата. После растворения нитрата железа объем жидкости доводят водой до 100 мл.

Качественное определение • Реакция образования трибромфенола (белый осадок). Реакция высокочувствительна, но не специфична и имеет отрицательное судебно-химическое значение. • Реакция с железa (III) хлоридом (сине-фиолетовое окрашивание, не исчезающее от добавления 2 -3 капель этанола); • Реакция образования метилсалицилата (характерный запах метилового эфира кислоты салициловой); • Реакция образования ауринового красителя (красное окрашивание).

• 1

Количественное определение • Титриметрический метод - алкалиметрия (титрование раствором натрия гидроксида в спиртовой среде в присутствии фенолфталеина) или броматометрическое определение. • В 0, 5 моль/л растворе натрия гидроксида к-та салициловая имеет мах поглощения при длине волны 300 нм.

Барбитураты • "Потребитель барбитуратов производит отталкивающее впечатление. У него отсутствует координация, он шатается и падает со стульев в баре, засыпает в середине беседы, пища вываливается у него изо рта. Он застенчив, ворчлив и глуп. " Вильям Бароуз, "Naked Lunch"

• Эта группа веществ подлежит обязательному судебно-химическому исследованию при проведении общего судебно-химического анализа (Приказ МЗ СССР № 1021 от 25. 12. 73 г. ). • В настоящее время синтезировано около 2500 различных веществ этой группы, более 60 из них применялись в медицине. В нашей стране применяется 11 препаратов этого ряда. • Среди пациентов специализированных центров по лечению отравлений 10 -15 % составляют больные с отравлениями барбитуратами. При тяжелых отравлениях с развитием коматозного состояния летальность достигает 10 -15 %.

Токсикологическое значение производных барбитуровой кислоты • Барбитураты обладают высокой фармакологической активностью, поэтому их передозировка может привести к различным осложнениям и даже вызвать смертельный исход. • доступны для населения, т. к. широко используются в медицинской практике в качестве снотворных, седативных, противосудорожных средств, средств для наркоза, оказывая тормозящее действие на ЦНС. • При длительном применении препараты вызывают пристрастие и привыкание (барбитуровою токсикоманию).

Основные симптомы барбитуромании: • отсутствие снотворного действия терапевтических доз, потребность в увеличении снотворной дозы; нарушение сна; • психический дискомфорт вне приема барбитуратов; • потребность в регулярном приеме; утренний, дневной прием барбитуратов; • знакомство с тонизирующим или эйфорическим действием барбитуратов, происходящее при увеличении разовой дозы до 0, 4 -0, 6 г.

• Барбитураты быстро всасываются из ЖКТ. • Смертельная доза – около 10 терапевтических разовых доз каждого препарата. • Частые употребления барбитуратов сопровождается кумуляцией, что создаёт угрозу отравления. Наибольшие концентрации их определяются в печени, почках, селезенке, кро и тканях мозга.

• Производные барбитуровой кислоты по фармакологическому действию делятся на препараты длительного действия (8 -12 ч) – фенобарбитал, барбитал-натрий; барбитураты средней продолжительности действия (6 -8 ч) – барбамил, этаминал- натрий; барбитураты короткого действия (4 -6 ч) – гексобарбитал.

• 1 • З амен а атома се кислородом в позиции 2 и Барбитураты метильной группы в позиции Структура 1 позволили сокра тить барбитуратного кольца длительност ь действия , но повы сили судорожную активность и частоту явлений возбуждения. • Увеличение числа атомов углерода в боковой цепочке в позиции 5 повышает силу агента. • П рямая замена фенильной группы способствует появлению противосудорожной активности.

• Наибольшая концентрация наблюдается в печени, почках, селезенке, крови, мозге. • В настоящее время известно о развитии пристрастия к этой группе препаратов и о синергизме приемах их одновременно с алкоголем, опиатами, алкалоидами белладонны, с психотропными веществами.

Основные пути метаболизма: • окисление заместителей при С 5 атоме углерода с образованием спиртов, фенолов, кетонов и карбоновых кислот с последующим частичным преобразованием их в глюкурониды; • деалкилирование N-алкильных групп; • десульфирование S 2 -группы тиобарбитуратов; • раскрытие барбитурового кольца между N 1 - и С 6 -атомами.

Изолирование • Проводят с использованием общих и частных методов, разработанных для веществ кислотного характера. • Для очистки используют методы: сублимации, экстракции и реэкстракции, хроматографии. • Выделение барбитуратов из слюны, пота и волос.

Таутомерия барбитуратов В зависимости от р. Н среды барбитураты способны существовать в нескольких таутомерных формах: • р. Н=2 – лактамная (имидная); • р. Н=10 – лактимная (моноимидольная); • р. Н=13 – дилактимная (диимидольная).

Химические методы Барбитураты способны образовывать с солями тяжелых металлов окрашенные соединения; • с солями кобальта в аммиачной среде (реакция Пари) образуется комплекс состава Со(NH 3)6 OHBarb 2 красно-фиолетового цвета; • с солями меди в щелочной среде в присутствии пиридина образуется комплекс красно-фиолетового цвета (тиобарбитураты образуют осадок зеленого цвета) – реакция Цвиккера;

• с солями ртути в кислой среде образуется белого цвета осадок комплексной соли. Реакция используется для обнаружения барбитуратов на пластинке методом ТСХ – образуются белые пятна на полупрозрачном фоне. В присутствии дифенилкарбазона (ДФК), барбитураты образуют комплексные соединения, окрашенные в сине-фиолетовый цвет. Реакция широко используется для обнаружения барбитуратов на хроматограмме. Чувствительность ее достигает 0, 5 мкг.

Мурексидная проба • С окислителями в кислой среде производные барбитуровой кислоты образуют смесь производных аллоксана и диалуровой кислоты. От прибавления аммиака к этой смеси образуется мурексид (фиолетовое окрашивание).

Реакция с родамином 6 Ж • При взаимодействии родамина 6 Ж с солями барбитуратов (барбамил, этаминал-натрий) образуются окрашенные ионные ассоциаты, которые экстрагируются четыреххлористым углеродом. При наличии солей барбитуратов слой четыреххлористого углерода приобретает светло-оранжевую или оранжево-красную окраску.

Микрокристаллоскопический анализ • Образование кислотной формы барбитуратов. К сухому остатку добавляется конц. кислота серная, вследствие протонирования атомов азота образуется растворимая в кислоте серной форма барбитуратов. После разбавления кислоты водой образуются кристаллические осадки кислотной формы, характерные для каждого барбитурата.

• Реакция с хлорцинкиодом. Характерные, окрашенные осадки дают: барбитал, этаминал и барбамил. • Реакция с железоиодидной комплексной солью, окрашенные кристаллы специфической формы образуют: фенобарбитал, барбамил и этаминал. • Реакция с медноиодидной комплексной солью. Барбамил и этаминал дают характерные кристаллы.

Хроматография в тонком слое • Частной хроматографической системой для разделения и идентификации барбитуратов служит смесь растворителей хлороформ-н- бутанол-25 % аммиак (70: 40: 5). Детектирование веществ на хроматограмме проводят с помощью растворов ртути сульфата и дифенилкарбазона. Барбитураты обнаруживают по образованию пятен сине- фиолетового цвета.

Спектрофотометрия в УФ-области • Барбитураты в имидной форме (р. Н=2) не поглощают в УФ-области спектра, так как отсутствует система сопряженных двойных связей. • Барбитураты в имидольной форме (р. Н=10) имеют систему сопряжения и обладают характерным поглощением при λмах = 240 нм. • Диимидольная форма барбитуратов также обладает характерным поглощением при λмах = 255 -260 нм.

Количественное определение барбитуратов • К. о. можно проводить спектрофотометрически в УФ-области по полосе поглощения с λmax = 260 нм. Определяют также методами ГЖХ и ВЭЖХ.

Производные пиразола (антипирин, анальгин) • Препараты этого ряда относятся к группе ненаркотических анальгетиков. • В терапевтических дозах оказывают аналгезирующее, противовоспалительное и жаропонижающее действие. • Под влиянием этих препаратов в токсических дозах возбуждаются корковые и подкорковые центры головного мозга, оказывают миелотоксическое действие (в некоторых случаях вызывают апластическую анемию). • В организме при любом пути введения быстро всасываются, следы их обнаруживаются в моче уже через 10 -20 минут после введения.

С и м п т о м ы отравления. • Возбужденное состояние. Судороги. Бессонница. Бред. Кома. Тошнота. Рвота. Высыпание на коже по типу крапивницы. Конъюктивит, ринит, стоматит. Сердечно-сосудистая недостаточность.

Н е о т л о ж н а я п о м о щ ь. • Полный физический и психический покой. Обильное питьё молочных жидкостей. • Промывание желудка большим количеством воды с добавлением активированного угля или магния оксида. • Антидоты: фолиевая кислота, метилурацил, цианокобаламин.

• Для этой группы препаратов характерно поглощение в ИК- и УФ-областях. • УФ-спектры имеют 2 максимума: в интервале от 230 -245 нм и 265 -275 нм, данное свойство используется для идентификации и к. о.

• Производные пиразолона имеют слабо выраженный основный центр – гетероатом во 2 -ом положении. Атом азота в 1 -м положении практически не проявляет основных свойств из-за влияния атома карбонильной группы и фенильного радикала.

Антипирин • Не обладает восстановительными свойствами и не окисляется в отличие от всех производных пиразола. • Благодаря наличию в положении 4 подвижного водорода, вступает в реакции замещения, используемые для качественного и количественного анализа. • Кроме того, антипирин отличает способность к комплексообразованию.

Идентификация антипирина • реакция с раствором железа III хлорида, в результате которой образуется комплексная соль феррипирин (интенсивное красное окрашивание); • образование нитрозоантипирина при взаимодействии с раствором натрия нитрита в кислой среде (стойкое изумрудно-зеленое окрашивание).

• 1

• Основной метаболит антипирина 4 - гидроксиантипирин. • В неизменном виде выделяется около 5 %. Он быстро связывается с глюкуроновой кислотой и в плазме крови не обнаруживается.

Идентификации анальгина • нагревают с минеральными кислотами, выделяется диоксид серы и формальдегид, которые обнаруживают по запаху, если выполняют реакцию в присутствии серной и салициловой кислот, то образуется ауриновый краситель, имеющий интенсивное красное окрашивание за счет выделяющегося формальдегида.

Производные ксантина • В медицинской практике применяют кофеин, теобромин и теофиллин, которые являются алкалоидами. • Кофеин содержится в листьях чая до 5 % и зернах кофе (до 1, 5 %) и некоторых других растениях. В листьях чая содержится также теофиллин, а в бобах какао – теобромин.

• Кофеин избирательно действует на ЦНС, в первую очередь на кору головного мозга. Кумулятивными свойствами не обладает. • Быстро всасываются в желудочно-кишечном тракте, деметилируются в организме, выводятся с мочой в виде метаболитов, 10 % в неизменном виде. Выводятся быстро. • Смертельная доза 20 г с большими индивидуальными различиями,

• Избирательное токсическое действие: психотропное, нейротоксическое (судорожное). • Клинические признаки и диагностика: шум в ушах, головокружение, тошнота, рвота, повышение температуры тела, сердцебиение. При передозировке, особенно при внутривенном введении, возможен приступ клонико-тонических судорог и падение артериального давления.

• Представляют собой бициклическую систему, состоящую из двух колец: пиримидинового (А) и имидазольного (В), в которых 2 атома углерода являются общими. • При нагревании с реактивом Несслера появляется у кофеина красно-бурый осадок. • Для определения кофеина применяют реакцию образования мурексида, реакции группового осаждения алкалоидов, физико-химические методы УФ-, ИК-спектроскопию, хроматографию в тонком слое и т. д. • К. о. весовой или колориметрический методы.

