Лекция_4._Полигенное_наследование.ppt
- Количество слайдов: 40

Лекция 4. ПОЛИГЕННОЕ НАСЛЕДОВАНИЕ. МУЛЬТИФАКТОРИАЛЬНЫЕ ПРИЗНАКИ И ЗАБОЛЕВАНИЯ. ВРОЖДЕННЫЕ БОЛЕЗНИ И ПОРОКИ РАЗВИТИЯ профессор Мутовин Геннадий Романович 1 1

Полигенное наследование генов и признаков (часть 1). 1. Общая характеристика. Наследование многих признаков, для которых очевидна генетическая изменчивость, нельзя объяснить только с помощью моногенного варианта, т. к. нет уверенности, что анализируемый ген - это единственная причина, а один и тот же признак (фенотип) обусловлен разными точковыми мутациями этого гена. Это относится, например, к таких признакам, как необычные рост, масса и пропорции тела, черты и выражение лица, цвет (окраска) кожных покровов, пульс и давление крови, неспецифическая умственная отсталость и высокий интеллект. Кроме того, к таким признакам также были отнесены врожденные пороки развития (ВПР) и хронические заболевания неинфекционной природы. Эти признаки и болезни обусловлены суммарным (аддитивным) действием как генетических факторов, так и факторов среды и поэтому названы мультифакториальными. 2
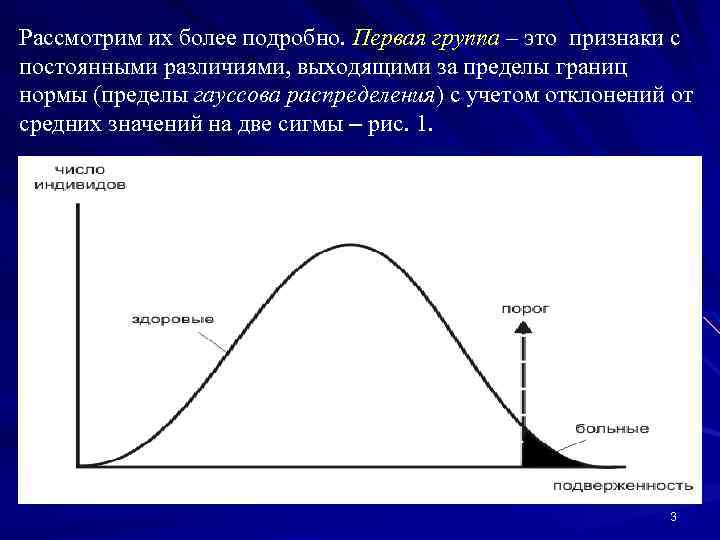
Рассмотрим их более подробно. Первая группа – это признаки с постоянными различиями, выходящими за пределы границ нормы (пределы гауссова распределения) с учетом отклонений от средних значений на две сигмы – рис. 1. 3

Вторая группа - это ВПР с грубыми морфо-функциональными изменениями: аномалад Пьера-Робена, атрезия пищевода, болезнь Гиршпрунга, врожденный пилоростеноз, «заячья губа» и «волчья пасть» , spina bifida и анэнцефалия), врожденные пороки, сердца и магистральных сосудов, вывих бедра, косолапость, плоскостопие, пороки почек, гипоспадия, эписпадия, неклассифицированные комплексы МВПР, синдром Клиппеля. Фейла (аномалии шейных позвонков) и др. Третья группа - это хронические болезни неинфекционной природы, или собственно мультифакториальные заболевания (МФЗ). Сюда относятся: артериальная гипертензия, бронхиальная астма, ишемическая болезнь сердца, многие формы рака, псориаз, ревматизм, сахарный диабет I типа, шизофрения и маниакально- депрессивный психоз, язвенная болезнь желудка и 12 -перстной кишки и др. На их долю приходится 96% всех хронических болезней. 4

Таким образом, в основе любого мультифакториального признака и заболевания лежат несколько причин. При этом индивидуальный вклад каждой причины в проявление болезни может быть незначительным, и только их суммарный вклад ведет к ее развитию. При МФЗ один и тот же патогенетический механизм может быть запущен разными способами: одной, либо сразу несколькими причинами. Одни причины могут быть генетическими (главный ген и/или полигенный комплекс), другие - средовыми (химические аллергены), третьи - поведенческими (пристрастие к определенной пище), четвертые - социальными и/или психологическими (влияние родителей, школы, сослуживцев на работе). Считается, что у человека в большом выборе его белков (до 6 млн. модификаций), формирующих признаки и фенотипы, должна быть возможность существования лиц повышенного риска по неблагоприятному сочетанию наследственных и 5

средовых факторов, обусловливающих развитие МФЗ. Таким образом, эти заболевания имеют генетическую и негенетическую компоненты и, благодаря первой, при них выделяется наследственная предрасположенность или подверженность. Именно по этой причине их называют также болезнями с наследственной предрасположенностью или подверженностью (БНП). 2. Наследственная предрасположенность и ее порог. Наследственная подверженность к МФЗ - это не только генетическая компонента. Прежде всего, это сумма эффектов многих генетических и средовых факторов, обусловливающих для индивида большую или меньшую вероятность заболеть (или не заболеть) конкретным заболеванием. Такая предрасположенность включает в себя индивидуальную и семейную компоненты, что объясняется уникальностью каждого человека (генетической конституцией) и наличием у него общих 6

генов с родственниками. При превышении определенных значений предрасположенности и достижении «порога подверженности» запускается механизм развития МФЗ. Однако физически это понятие не существует, т. к. оно представляет собой некий условный континуум возрастающей восприимчивости к заболеванию, или шкалу подверженности. Подверженность (как гауссова кривая) распределена нормально: она имеет одну вершину (моду) и обусловлена большим числом генов, действующих аддитивно, но при этом каждый из них вносит свой отдельный вклад в общий эффект. При превышении порога подверженности развивается болезнь (рис. 1). И хотя подверженность есть условная величина, существует определенная пороговая область, внутри которой от дополнительных средовых факторов будет зависеть решение вопроса о том: «Заболеет индивид или нет? » . 7

Считается, что большинство людей имеет среднюю степень подверженности, их меньшая часть имеет либо низкую, либо высокую подверженность. В последнем случае это и будут больные лица, у которых подверженность превысила порог. Из этого следует, что индивид даже с необычайно высокой подверженностью к определенному заболеванию может не заболеть им даже при благоприятных условиях среды, но возможна и обратная ситуация. Таким образом, особенностью МФЗ является то, что это всегда результат аддитивного действия множества генных локусов и внешних факторов. 3. Наследуемость МФЗ. Предрасположенность зависит от наследуемости. Это степень, с которой подверженность определяется генетическими факторами в сравнении с факторами среды. Оценка наследуемости состоятельна лишь тогда, когда подверженность к МФЗ определяется большим числом генов. 8

С этой целью еще в 1969 году К. Картером была предложена формула средового отклонения, или основное уравнение: P = G + E, где Р – признак (фенотип), G –генетические факторы и Е – факторы среды. Для расчетов наследуемости тогда же был предложен коэффициент наследуемости: h 2 (Кн) = G / E , где h 2 или Кн коэффициент наследуемости, G и E генетические и средовые факторы соответственно. Этот коэффициент выражается в абсолютных числах (от 0 до 1) или процентах (от 0 до 100%) и отражает аддитивный вклад в фенотип генетических факторов. Если наследуемость включает в себя не относящиеся к генетическим причинам общие семейные факторы, то тогда вероятность развития МФЗ у родственников больного пробанда будет намного выше, чем в общей популяции, т. е. наследуемость будет тем вероятнее, чем чаще больные лица будут иметь со своими родственниками общую среду обитания. 9

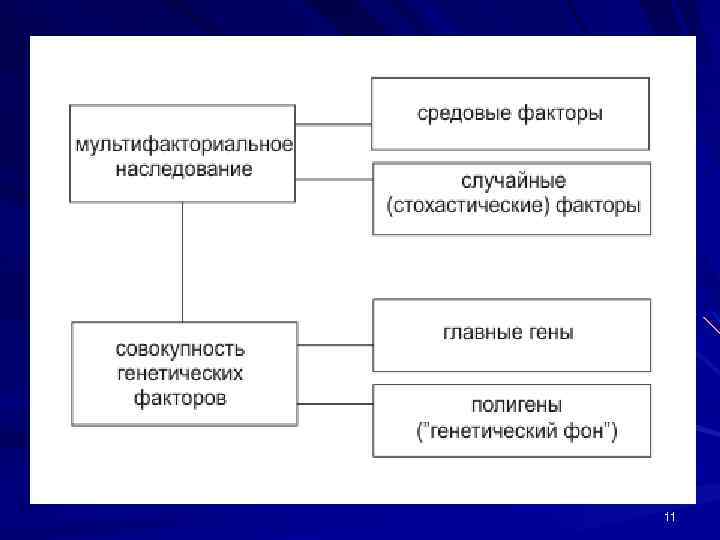
Низкое значение этого коэффициента подразумевает малый вклад аддитивно действующих генов, высокое значение - большой вклад. Итак, наследуемость МФЗ - это популяционно-статистический параметр. Для большинства МФЗ наследуемость выше 60%. 4. Модели полигенного наследования. Моделей полигенного наследования много. Среди них: простая или аддитивная модель (К. Картер, 1969), модель количественной наследственности, модель полигенного компонента с пороговым эффектом, смешанная модель Н. Мортона и К. Мак-Лина (1974), сложная модель с сочетанием действия главных генов, генов полигенного комплекса и факторов среды. В 1990 году Ф. Фогелем и А. Мотульски была предложена концептуальная модель, в которой подчеркивается решающее значение всех генетических факторов (как главных генов, так и генов полигенного комплекса) в развитии МФЗ - рис. 2. 10
11

При этом главные гены не действуют в "вакууме", они экспрессируются на фоне всех генов, модифицирующих их работу. Вместе с тем предположение об участии главного гена в формировании наследственной предрасположенности может быть высказано только в случае обнаружения в этом гене мутаций, не встречающихся у здоровых людей. В большинстве случаев патологический белковый продукт, производимый одним или несколькими главными генами, играет ключевую роль в развитии симптомов болезни. Так, установлен значительный вклад двух главных генов (DRCA 1 и DRCA 2) в предрасположенность к семейным формам рака молочной железы. С помощью модели Ф. Фогеля и А. Мотульски в разных группах больных с МФЗ удалось выделить редкие формы заболеваний с моногенным вариантом наследования: • в группе гиперлипидемий, обусловливающих ишемическую болезнь сердца (ИБС), выделены две моногенные формы - семейная 12

гиперхолестеринемия (ген LDRL локализован на хромосоме 19 р13. 2 -р13. 1) и семейный дефект Аро-В-100 (ген аро-В локализован на хромосоме 2 р23 -р24); • в группе эссенциальной гипертензии выделены: гипертензия, купируемая небольшими дозами глюкокортикоидов (причина неравный кроссинговер между генами альдостерон-синтазы и 11 бета-гидроксилазы; оба гена локализованы в сегменте 8 q 21 - это область гена цитохрома Р 450), синдром Лиддла или псевдоальдостеронизм (причина - 2 гена эпителиального натриевого канала: SCNN 2 и SCNN 3 (оба локализованы в сегментах 16 р13 -р12), синдром Гордона - псевдоальдостеронизм второго типа, синдром избытка минералокортикоидов (ген почечной 11 -бета-гидроксистероид-дегидрогеназы, локализован в 16 р13 -р12); • в группе сахарного диабета I типа выделены 6 MODY-форм, обусловленных генами: HNF 4 A (1), GCK - ген глюкокиназы (2), ядерного фактора гепатоцитов (3), фактора-1 промотора инсулина 13

(4), почечного фактора транскрипции 2 (5), NEURODY (6). Кроме того, роль генетических факторов оказалась значительной при язвенной болезни желудка и двенадцатиперстной кишки, а также при ряде ВПР (дефекты невральной трубки, расщелины верхней губы и нёба, врожденная косолапость и др. ). При этом было показано, что семейное наследование указанных заболеваний отличается от классического моногенного варианта, т. к. в их развитии принимают участие неспецифические гены, действующие совместно с факторами среды. И хотя их действие аддитивно, первичный биологический эффект пока еще не определен (рассматривается как "черный ящик"). 5. Критерии полигенного наследования: Риск развития МФЗ зависит от: 1. Наследуемости. Чем выше коэффициент наследования МФЗ, тем выше риск его развития для здоровых родственников. В таблице 1 приведены значения коэффициентов наследуемости при некоторых МФЗ. 14

Таблица 1 Коэффициенты наследуемости МФЗ ------------------------------------------Название патологии Кн , в % ------------------------------------------Шизофрения: злокачественная форма 85 вялотекущая форма 74 Бронхиальная астма 80 Расщелина губы и нёба 76 Сердечно-сосудистые заболевания 65 Артериальная гипертензия 62 Дефекты невральной трубки 60 Изолированный врожденный порок сердца 35 ------------------------------------------15

2. Числа больных родственников. Чем больше в родословной родственников, имеющих конкретное МФЗ, тем выше риск его развития у потомков (см. таблицу 2). 3. Степени родства с больным пробандом. Чем ближе по степени родства с больным пробандом находится здоровый родственник, тем выше риск развития у него МФЗ. Например, риск псориаза (популяционная частота 0, 75% ) у родственников больного пробанда при первой степени родства (50% общих генов) равен 5, 6%, второй степени (25%) – 3, 5%; третьей степени (12, 5%) – 1, 7%, четвертой степени (6, 25%) – 0, 75%. 4. Степени выраженности (тяжести течения) заболевания. Чем выше степень выраженности (тяжесть течения, или экспрессивность) заболевания у больного пробанда, тем выше риск его развития у потомка. 5. Редко поражаемого пола. Чем чаще проявляется заболевание у одного пола (например, у мужчин), тем выше риск его проявления у противоположного (редко поражаемого) пола. 16

Таблица 2 Риск развития МФЗ и число больных родственников -------------------------------------------Название патологии Число больных и риск 1 2 3 -------------------------------------------Врожденный порок сердца: дефект межжелудочковой перегородки 1: 20 1: 7 1: 2 тетрада Фалло 1: 40 1: 12 1: 4 Дефекты нервной трубки 1: 40 1: 12 1: 4 Эпилепсия 1: 30 1: 10 1: 3 Недифференцированная УМО 1: 20 1: 7 1: 2 Шизофрения 1: 20 1: 4 1: 2 Бронхиальная астма 1: 20 1: 3 1: 2 Инсулинзависимый сахарный диабет 1: 20 1: 7 1: 2 Паховая грыжа 1: 10 1: 4 1: 2 17 -------------------------------------------

Это эффект Картера. Например, врожденный пилоростеноз у новорожденных мальчиков встречается в 2 -5 раз чаще, чем у девочек, т. е. в данном случае девочки - редко поражаемый пол. Однако частота болезни у будущих детей пораженных девочек достигает 10 -20%, тогда как у будущих детей пораженных мальчиков она составляет 2 -6%. Дополнительные критерии: • близнецовый критерий. Если конкордантность монозиготных близнецов по МФЗ в 4 раза выше конкордантности у дизиготных близнецов, то это заболевание наследуется полигенно; • критерий сегрегационного отношения пораженных и непораженных сибсов. Если доля больных сибсов в семьях с одним больным родителем в 2, 5 раза выше, чем доля больных сибсов в семьях с двумя здоровыми родителями, то полигенное наследование предпочтительно, если меньше 2, 5 раз, то оно не исключается. 18

6. Ассоциации и сцепление МФЗ с маркерами. Поиск генетических причин предрасположенности к МФЗ, подразумевает определение их ассоциации с полиморфными маркерами (генами и антигенами) и определение сцепления болезни с ДНК-маркерами. Ассоциация - это наиболее высокая частота полиморфного генамаркера конкретного заболевания. Еще в начале ХХ века были предположения об ассоциации антигенов крови системы АВО с определенными заболеваниями. В дальнейшем это нашло подтверждение только для Rhнесовместимости матери и плода. Попытки описать ассоциации между группами крови и другими заболеваниями, включая онкологические, оказались безуспешными, кроме группы крови О (I), ассоциированной с язвенной болезнью желудка и двенадцатиперстной кишки. Важным шагом для выяснения механизма ассоциации стало 19

установление связи между антигенами системы HLA с: анкилозирующим и псориатическим спондилитом и синдромом Рейтера (сцеплены с В 27), болезнью Адиссона и сахарным диабетом I типа (DR 3) и П типа (DR 4), гемохроматозом (А 3), гнездной алопецией (DQW 7), псориазом (CW 6), ревматоидным артритом (DR 4), рассеянным склерозом (DRВ 1). Вслед за этим была описана ассоциация полиморфизма альфа-1 антитрипсина с хронической эмфиземой легких у взрослых, патогенез которой связан с множественными аллелями локуса РI (23 разных фенотипа), обусловливающими механизмы разрушения легочной ткани при хронической эмфиземе легких в результате инфицирования. При этом было показано, что ассоциация не подразумевает, что ген болезни и маркерный ген расположены в одной хромосоме, например, с HLA-локусами, расположенными на хромосоме 6, Однако, сегодня нет оснований считать, что МФЗ и HLAкомплекс как-то связаны между собой физиологически. 20

К таким заболеваниям, например, относятся аутоиммунные (иммунно-ассоциированные) болезни: Аддисона, детская спру, миастения гравис, множественный склероз, ревматоидный артрит, сахарный диабет I типа, тиреотоксикоз и хронический гепатит. Семейный анализ этих заболеваний выявил сегрегацию у родственников больных пробандов, хотя при этом отсутствовало моногенное наследование. Следовательно, будучи ассоциированными, D/DR-гены HLAкомплекса и гены аутоиммунных заболеваний между собой не сцеплены. Поэтому надо тщательно разграничивать ассоциацию и сцепление, которое относится к двум генам, расположенным в одной хромосоме на определенном расстоянии друг от друга. Для анализа сцепления МФЗ с полиморфными маркерами используются от 300 до 500 ДНК-маркеров, распределенных по всему геному , т. е. ведется их полногеномный скрининг. 21

ВРОЖДЕННЫЕ БОЛЕЗНИ И ПОРОКИ РАЗВИТИЯ (часть 2) 1. Общая характеристика и исторические сведения. Область генетики, изучающая врожденную патологию, называется тератологией (за рубежом – дисморфология). Процесс формирования врожденных болезней и ВПР – это тератогенез, а факторы, обусловливающие такую патологию – это тератогены. Врожденная патология возникает в результате нарушений бластогенеза, эмбриогенеза и фетогенеза (намного реже). Большой удельный вес в ней занимают: врожденные пороки развития (ВПР), или большие аномалии развития (БАР) и малые аномалии развития (МАР). ВПР или БАР - это грубый морфологический дефект органа или большого участка тела с нарушением его функции. В историческом плане такой дефект часто определяли как уродство. В современных условиях этот термин важен лишь в социальном плане, т. к. урод - это «выродок» общества: 22

алкоголик, наркоман, бандит, киллер, мародер и т. п. Очевидно, что такой термин не должен применяться в медицине, где речь идет о больном человеке. В свою очередь МАР и их синонимы (стигма, дисгенезия, диспластическая черта, дисморфологическая черта, микропризнак и т. п. ), хотя и относятся к гистологическим нарушениям (конечные стадии морфогенеза), вместе с тем они не выходят за пределы границ нормы и не сопровождаются функциональными изменениями. Поэтому их медицинское значение менее выражено, чем у БАР. К сожалению, в литературе до сих пор нет однозначного ответа на вопрос: «Какие именно структурные нарушения развития надо рассматривать как микропризнаки? » . Нередко их обозначают как минимальные клинические отклонения (микроформы, микропроявления, микросимптомы). 23

2. Частоты, причины и классификации врожденной патологии. В последние годы установлено, что гены факторов транскрипции в значительной мере представлены среди генов, вызывающих врожденную патологию. Свыше 30% таких генов связаны с врожденными болезнями и пороками развития. Их примеры приведены в таблице 3. Особенно высок удельный вес врожденной патологии , проявляющейся на первом году жизни ребенка, что обусловлено мутациями в генах, кодирующих белки-ферменты (47%). Как правило, это связано с нарушениями гомеостаза в собственном метаболизме у больных детей, т. к. до их рождения метаболизм контролировался через плаценту и соответствовал материнскому гомеостазу. Врачи любой специальности постоянно встречаются с врожденной патологией. 24

Таблица 3 Проявление генов врожденных заболеваний и ВПР ------------------------------------------Название и локализация Врожденное заболевание гена ------------------------------------------MITF (3 p 12) Синдром Ванденбурга, тип 2 KIT (4 q 12) Неполный альбинизм SHH (7 q 36), (7 q 32. 3), Голопрозэнцефалия (2 р21) PTC (9 q 22) Синдром Горлина TBX 5 (12 q 24) Синдром Холт-Орама LIGAM (Хq 28) Гидроцефалия PAX (2 p 25. 2), Аниридия 1 и 2 (11 p 13. 1) 25

В ряде случаев она легко выявляется уже при первом осмотре новорожденного (анэнцефалия, микроцефалия, гидроцефалия, расщелины верхней губы и нёба, укорочение конечностей, черепно- и спиномозговые грыжи). В других случаях это становится возможным только применении синдромологического подхода и клиникоинструментальных методов обследования больного (пороки сердца, почек, органов дыхания, пищеварения и др. ). По данным ВОЗ популяционная частота врожденной патологии составляет 1, 5 -5% (в отдельных странах - от 2, 7 до 16, 3%), а ВПР среди новорожденных в расчете на 1000 рождений выявляются у 25 -35 детей (в среднем 3%). В постнатальном периоде число детей с ВПР достигает 6% - к двухлетнему и 8% - к пятилетнему возрасту. В структуре общей смертности детей на долю ВПР приходится 1520%, а их доля среди причин перинатальной смертности колеблется по данным прозектуры от 4 -7, 7% до 26 -29%. 26

Врожденные пороки чрезвычайно разнообразны, их количество исчисляется сотнями. В большей или меньшей степени они выявляются во всех системах организма, начиная от единичных БАР и МАР и кончая комплексами множественных ВПР (м. ВПР). Среди всех пороков развития на первом месте по их частоте находятся изолированные пороки – они выявляются в одной системе организма (82%). Из них на пороки нервной системы приходится до 30%, включая пороки нервной трубки: 8, 4 -22, 3%. Затем идут пороки развития сердца - 10, 9 -21, 0%, конечностей 7, 4 -24, 5% и гениталий - 2, 4 -7, 5%. Пороки развития, одновременно выявляемые в двух и более системах организма, называются множественными. Их частота колеблется от 7, 9 до 18, 2%. 27

Эта классификация предусматривает деление каждого из двух классов на 6 типов (подклассов) в зависимости от этиологии. (таблица 4). Следует отметить, что различия в показателях частот врожденных болезней и ВПР имеют региональные особенности, зависят от полноты их учета, от самого понятия, что относить к ВПР (? ), а также численного, национального и возрастного состава популяций, исторических, этнических и демографических особенностей, географических и экологических условий, а также от продолжительности мониторирования конкретного региона. За рубежом разработана иная классификация, включающая 4 типа дефектов: мальформация - морфологический дефект в результате действия внутренних причин на аномальный зачаток органа (пороки при хромосомных синдромах и генных мутациях); дизрупция - морфологический дефект в результате 28
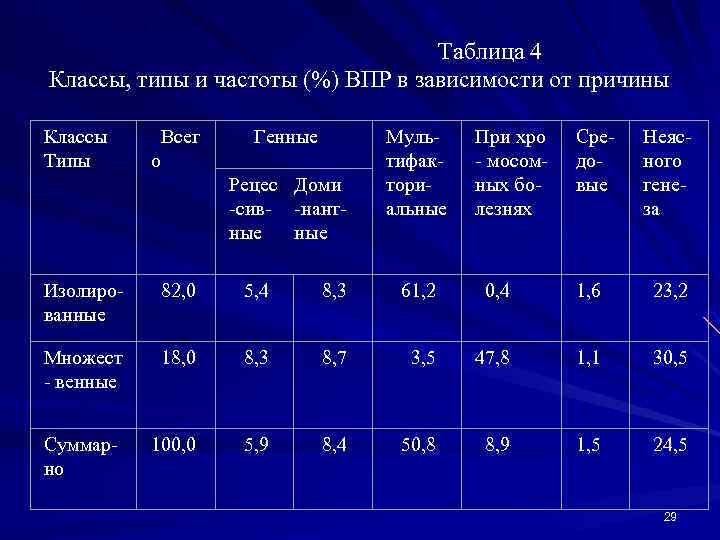
Таблица 4 Классы, типы и частоты (%) ВПР в зависимости от причины Классы Типы Всег Генные о Рецес Доми -сив- -нантные Мультифакториальные При хро - мосомных болезнях Средовые Неясного генеза Изолированные 82, 0 5, 4 8, 3 61, 2 0, 4 1, 6 23, 2 Множест - венные 18, 0 8, 3 8, 7 3, 5 47, 8 1, 1 30, 5 Суммарно 100, 0 5, 9 8, 4 50, 8 8, 9 1, 5 24, 5 29

действия внешних причин на изначально нормальный процесс развития. Это синоним вторичного порока. Например, аплазия Лучевой кости при синдроме Холт-Орама – это первичный порок, а при талидомидном синдроме -это дизрупция); деформация аномальная форма, размер, положение части тела в результате действия внешних механических (недизруптивных) и / или внутренних сил на плод. Например, сдавление уретры и уменьшение размеров и деформация матки при миоме; дисплазияаномальная организация клеток в структуре тканей, либо это аномалия тканевой структуры. Например, синдромы Марфана и Эллерса-Данлоса и несовершенный остеогенез. 3. Патогенез врожденных болезней и ВПР. Во внутриутробном онтогенезе выделены критические периоды перестройки, смысл которых заключается в последовательной 30

смене стадий развития зародыша, эмбриона и плода и в оценке чувствительности (ранимости) растущего организма к повреждающему действию факторов среды. Выделяют тератогенные терминационные периоды (ТТП) и критические периоды внутриутробного онтогенеза. Под понятием ТТП подразумевается предельный (конечный) срок, в течение которого конкретный повреждающий фактор вызывает конкретную БАР и МАР. За пределами этого срока могут развиться другие пороки, но только не данная аномалия. Например, для дефекта межжелудочковой перегородки сердца ТТП ограничен временем воздействия талидомида на 44 день последней менструации, а ТТП для дефекта развития межпредсердной перегородки сердца – на 55 день. Для зародыша характерен I критический период. Это 6 -9 дни беременности, совпадающие во времени с бластогенезом. 31

В это время зародыш реагирует на действие факторов среды по принципу: «все или ничего» , то есть он либо гибнет, либо (в силу большой адаптационной способности) продолжает развиваться, не реагируя. В этом периоде гибнут 35 -50% зародышей, которые элиминируются путем спонтанных абортов. В морфологическом материале погибших зародышей выявляются генные, хромосомные или геномные мутации (в последнем случае до 80% всех мутаций). Эти мутации ведут к нарушениям развития, называемым бластопатиями. К ним относятся: нарушения ориентации эмбриобласта в бластоцисте, пустые зародышевые мешки, гипоплазия или аплазия внезародышевых органов, имплантация зародыша в роге или у внутреннего зева матки, нарушение глубины имплантации, двойниковые пороки (полностью или частично неразделившиеся близнецы), сиреномиелия и циклопия, а также внематочная беременность. 32

Для эмбриона характерен II критический период. Это 3 -6 недели беременности. Развившиеся в это время нарушения называются эмбриопатиями. К ним относятся: очаговые и диффузные нарушения формирования органов, заканчивающиеся гибелью (самопроизвольными выкидышами) 10% эмбрионов или рождением 3% детей с БАР и МАР, т. е. суммарно 13% от всех зарегистрированных беременностей. Сложив (по максимуму) потери беременности путем спонтанного аборта в первом и втором критических периодах (50 + 13), мы получим 63%, т. е. теряются две беременности из трех. На этом основании был сделан вывод, что спонтанный аборт – это защитный природный механизм, избавляющий организм беременной женщины от генетически дефектных зародышей, эмбрионов и плодов! Причинами эмбриопатий служат мутации хроногенов, ведущие к нарушениям клеточной пролиферации и дифференцировки. При ускорении этих процессов развиваются прогероидные симптомы 33

и заболевания (синдромы Вернера, Хатчинсона-Гилфорда и др. ), а при замедлении – гетерогенные тканевые дисплазии мозга, легких или почек. Для эмбриопатий также характерны: высокий удельный вес моногенных и хромосомных болезней у (3% и 1%), несоответствие фенотипа генотипу (фенотип девочки, а генотип мальчика, либо наоборот), а также неполное фенотипическое проявление. В последнем случае речь идет о выявлении у эмбриона с конкретным хромосомным синдромом всего двух трех БАР, тогда как у ребенка с этим же синдромом количество БАР достигает двадцати. В свою очередь нарушения, развившиеся в плодном периоде, называются фетопатиями. В это время критический период беременности отдельно не выделен, т. к. у плода в основном уже завершено структурное формирование органов и систем , но продолжается их функциональное созревание. 34

Например, на 9– 11 неделях. беременности продолжается гистогенез кожной и мышечной тканей, поэтому могут проявиться их структурные дисплазии, а также БАР и МАР. К фетопатиям относятся: • истинные пороки, связанные с функциональной незрелостью мозга, легких, зубов, сердца (баталов проток), половых органов (одно- или двусторонний крипторхизм); • вторичные пороки: гидроуретер и гидронефроз; • ложные пороки в связи с альтеративным и альтеративнопродуктивным воспалением органов (гидроцефалия или порэнцефалия при токсоплазмозе); • наследственные болезни обмена (НБО), реализующиеся на биохимическом уровне (их большинство) или клиническом уровне (ахондрогенез и несовершенный остеогенез). И хотя суммарный вклад генетических причин в патологию плода в 4 -5 раз меньше такового у эмбриона, она достаточно велика по объему. Например, хромосомный дисбаланс у 35

абортусов плодного периода достигает 10 -12%, тогда как у абортусов эмбрионального периода он составляет 50% 4. Задержка внутриутробного развития Наиболее частым нарушением плодного периода является задержка внутриутробного развития (ЗВУР), частота которой по данным ВОЗ от 2, 9% до 39% при средней частоте - 17%, ЗВУР плода – это хроническое расстройство питания с дефицитом массы тела по отношению к длине плода. Дети со ЗВУР рождаются недоношенными в 24% случаев (недоношенный ребенок рождается при сроке 37 недель и сроке гестации менее 36 недель), доношенными – 10, 3 - 22, 0% случаев и переношенными еще реже. Генетические причины ЗВУР связаны с дефектами материнского генома: однородительской изодисомией по хромосомам 11 и 16 (во втором случае выявляется также плацентарный мозаицизм). 36

Выделяют 3 варианта ЗВУР: гипотрофический, гипопластический и диспластический. При первом и втором вариантах - это «маловесный для срока плод» с признаками или без признаков недостаточности питания. Недостаточность питания не сопровождается снижением массы тела плода относительно срока беременности и характеризуется признаками дистрофии: сухость, шелушение и снижение тургора кожи, тонкий подкожный жировой слой. Диспластический вариант ЗВУР – это проявление большого числа генетически детерминированных синдромов (до 200 нозологий) или генерализованных внутриутробных инфекций (чаще вирусных), сочетающихся с БАР и МАР (их частота от 1, 3 до 16, 5%) и нарушениями телосложения. Для этого варианта не характерно нормальное течение онтогенеза, не наблюдается гомеорез, но постоянны нарушения гомеостаза, поражение ЦНС и изменения иммунологической реактивности организма. 37

5. Регистрация, учет и характеристика МАР выделены в 3 группы. Альтернативная группа - это МАР, которые (как и грубые пороки) или есть, или их нет (папилломы, насечки, алопеция, дефекты скальпа и др. ). Измерительная группа - это МАР, определяемые абсолютным или относительным количественным значением (удлинение, укорочение, уменьшение, увеличение, смещение части тела или органа, изменение кривизны поверхности и др. ). В этом случае, принимают во внимание МАР, у которых отклонение от среднего значения не укладывается в 2 сигмы. Описательная группа - это МАР, для которых трудно применимы количественные методы изучения, например, изменения формы мягких тканей, цвета волос, кожи и т. п. В этом случае допустима их балльная оценка: I балл - слабо выраженная МАР, II балла - четко определяемая МАР, III балла - резко выраженная МАР. 38

Характеризуя МАР, следует соблюдать 2 правила. Первое – не существует лиц, у которых нельзя найти хотя бы несколько МАР. Второе – нельзя «устанавливать планку» по нормальному значению количества МАР (менее 5, 10 и т. д. ). 6. Дифференциально-диагностическое значение МАР. В качестве маркеров наследственных заболеваний и синдромов м. ВПР можно рассматривать комплексы из 4, 5 и более МАР, т. е. важно учитывать количество МАР. Например, полидактилия, гипертелоризм глаз и сосков, дополнительные соски - эти МАР предполагают наличие у пациента пороков мочевыводящей системы. Имеет значение и сочетание МАР. Например, при синдроме Варденбурга сочетаются: телекант, гиперхромия радужки, сросшиеся брови, белая прядь волос надо лбом; при синдроме 39

Дауна - косой разрез глазных щелей, эпикант, поперечная ладонная складка, брахидактилия, клинодактилия, сандалевидная щель. И, наконец, важно качество МАР или выделение признаков, которых нет у здоровых пациентов: крыловидные складки шеи (синдромы Шерешевского-Тернера и Нунан), постаксиальная полидактилия (синдром Барде-Бидля), гипоплазия (аплазия) грудного соска на одной стороне грудной клетки (синдром Поланда), вертикальные насечки на мочке уха (синдром Беквита. Видемана). Для большинства МАР характерна стабильность. Для части МАР характерны их изменение и даже полное исчезновение по мере роста ребенка, например: капиллярные гемангиомы шеи и поясничной области, высокое нёбо, седловидная форма носа, гипоплазия большого пальца на стопах, умеренная кожная синдактилия 2 и 3 пальцев ног, эпикант, сандалевидная щель, низко расположенные ушные раковины, пигментация кожи. 40
Лекция_4._Полигенное_наследование.ppt