ГенИнж2.ppt
- Количество слайдов: 79

Лекция 2 Белогуров АА

Емкости векторов разных классов Вектор Емкость (т. п. н. ) Плазмиды 15 Бактериофаг лямбда 25 Применение Библиотеки к. ДНК/экспрессионные вектора Геномные библиотеки Библиотеки к. ДНК Космиды 30 -45 Геномные библиотеки PAC 70 -90 Геномные библиотеки BAC 100 -500 Геномные библиотеки YAC 250 -2000 Геномные библиотеки MAC >2000 Генотерапия

План лекции • Прокариотические предназначенные для клонирования и экспрессионные векторы • Понятие вектора • Требования к вектору • Промотеры • Экспрессия белка и связанные с этим трудности

Какие бывают плазмидные векторы 1. Предназначенные для клонирования 2. Предназначенные для экспрессии

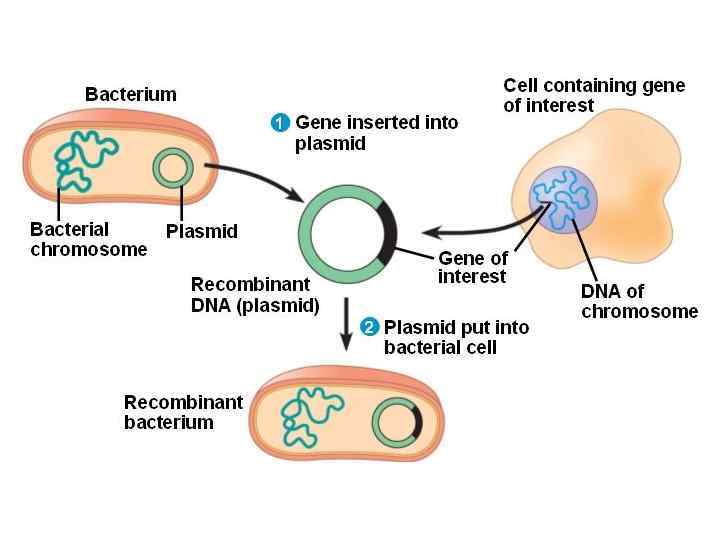
Вектор Основная идея заключается в том, чтобы присоединить исследуемые фрагменты ДНК к молекуле-переносчику, которая могла бы автономно существовать внутри бактериальных клеток в виде одной или нескольких копий и передаваться вместе со встроенным в нее фрагментом ДНК от одной клетки к другой. Такие молекулы-переносчики фрагментов нуклеиновых кислот были созданы, их называют векторами, и они являются одним из важнейших инструментов генной инженерии. Лев Иванович Патрушев

Биологические свойства бактериальных плазмид, используемые в векторах Консервативность размера Минимальный размер определяется элементами внутриклеточной автономии Ограничения на размер вставки чужеродной ДНК Молекулярные эндосимбионты – автономная репликация Негативный контроль числа копий Совместимость разных плазмид в клетке Группы несовместимости Случайная сегрегация в дочерние клетки

Консервативность размера Минимальный размер плазмиды диктуется необходимостью расположения в ее молекуле всех генов и регуляторных последовательностей, необходимых для поддержания ее внутриклеточной автономии. Другое требование, которое необходимо соблюдать при конструировании искусственных плазмид – это близкое друг к другу расположение взаимозависимых регуляторных участков молекулы. Это необходимо для обеспечения высокой вероятности их совместной передачи в дочерние клетки. Повышение размера плазмиды сверх оптимального будет отрицательно сказываться на ее стабильности.
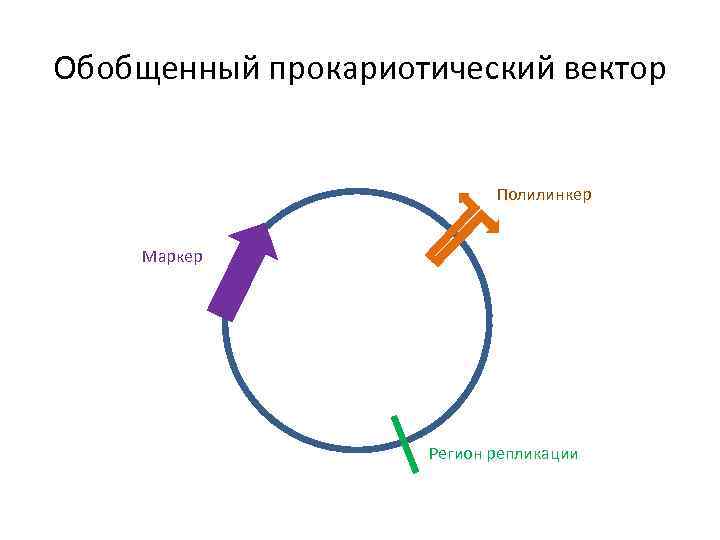
Обобщенный прокариотический вектор Полилинкер Маркер Регион репликации

Требования к Вектору 1. Любой вектор должен длительное время существовать в популяции клеток-хозяев, т. е. реплицироваться автономно или вместе с хромосомами клеток. 2. В любом векторе должны быть биохимические или генетические маркеры, которые позволяли бы обнаруживать его присутствие в клетках. 3. Структура векторной молекулы должна допускать встраивание в нее чужеродной последовательности нуклеотидов без нарушения ее функциональной целостности.

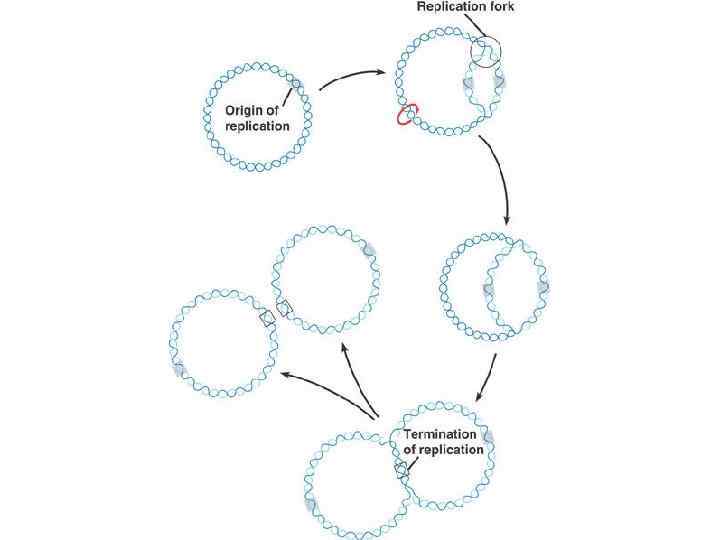
Автономная репликация обеспечивается наличием области начала репликации, на котором происходит сборка макромолекулярного комплекса, осуществляющего инициацию и продолжение синтеза плазмидной ДНК. ori
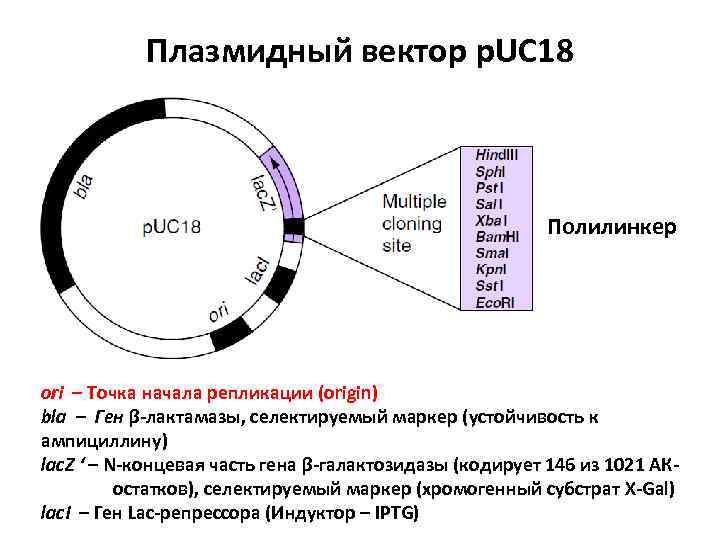
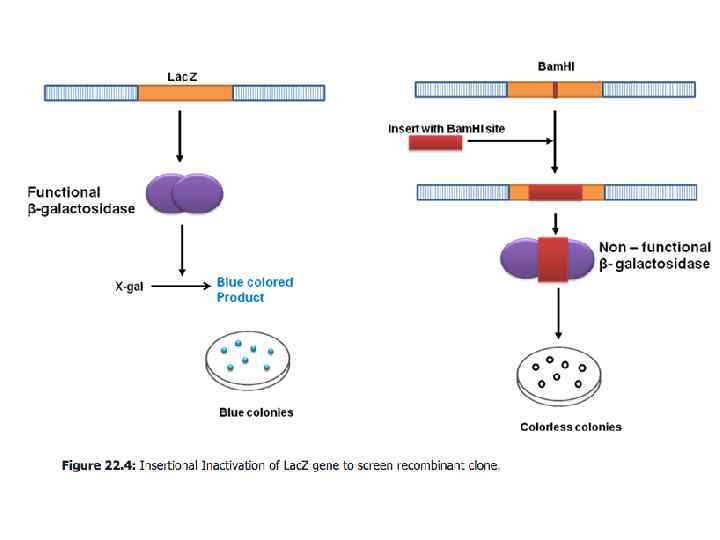
Плазмидный вектор p. UC 18 Полилинкер ori – Точка начала репликации (origin) bla – Ген β-лактамазы, селектируемый маркер (устойчивость к ампициллину) lac. Z ‘ – N-концевая часть гена β-галактозидазы (кодирует 146 из 1021 АКостатков), селектируемый маркер (хромогенный субстрат X-Gal) lac. I – Ген Lac-репрессора (Индуктор – IPTG)

Копийность плазмид Копий на клетку 1 -2 10 100 Низкокопийные Среднекопийные Высококопийные Хлорамфиникол – ингибитор синтеза клеточной, но не плазмидной ДНК

Контроль копийности Все плазмиды осуществляют негативный контроль синтеза ДНК с использованием специфических ингибиторов репликации. 1. Одним из распространенных механизмов негативного контроля является синтез на матрице плазмидной ДНК антисмысловой РНК (контртранскрипта), который может быть комплементарен или м. РНК белка-инициатора репликации Rep, или РНК-праймеру (в том числе, его предшественнику), необходимому для инициации синтеза плазмидной ДНК. 2. итероны, это прямые повторы, расположенные вблизи области начала репликации и гена rep. Итероны конкурируют с областью начала репликации за связывание Rep-белка, присутствующего в клетке в небольшом количестве, и связывают его полностью при достижении числа копий плазмиды определенного уровня, что полностью блокирует инициацию репликации.
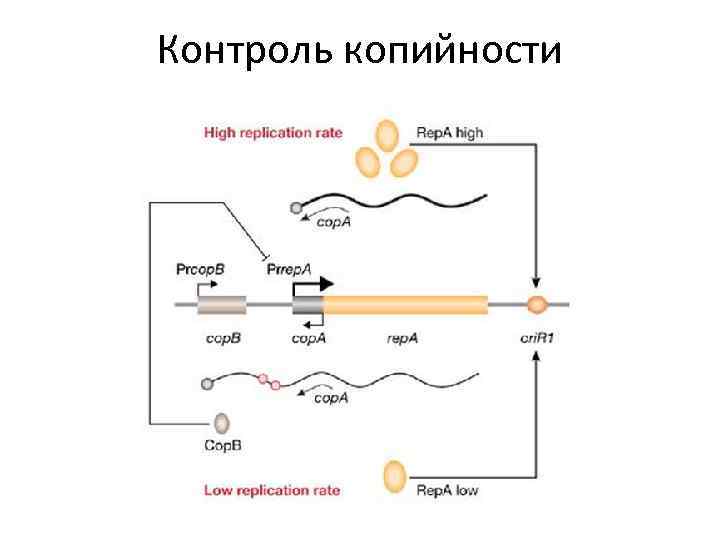
Контроль копийности
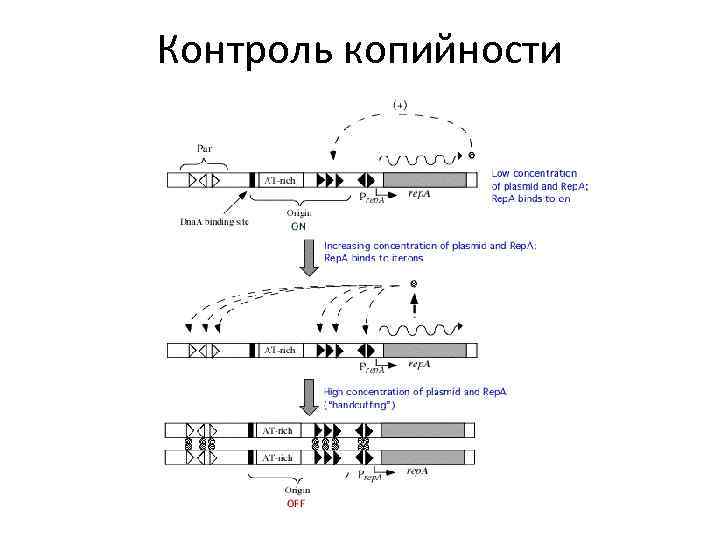
Контроль копийности
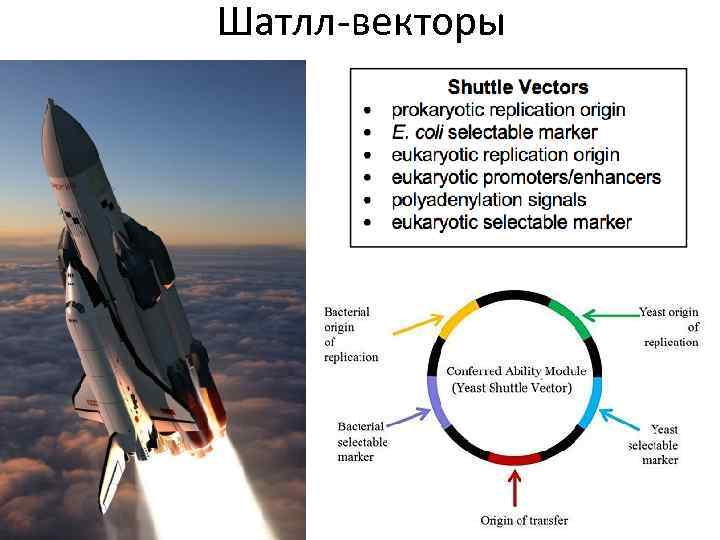
Шатлл-векторы
Обобщенный прокариотический вектор Полилинкер

Плазмидный вектор p. UC 18 Полилинкер ori – Точка начала репликации (origin) bla – Ген β-лактамазы, селектируемый маркер (устойчивость к ампициллину) lac. Z ‘ – N-концевая часть гена β-галактозидазы (кодирует 146 из 1021 АКостатков), селектируемый маркер (хромогенный субстрат X-Gal) lac. I – Ген Lac-репрессора (Индуктор – IPTG)

1. Содержат гены, обеспечивающие устойчивость клеток к токсическим веществам (антибиотикам, ионам тяжелых металлов и т. п. ) 2. Гены, кодируюущие белки (например, колицины), токсичные для клеток, не обладающих такими плазмидами 3. Обеспечивают прикрепление бактериальных клеток к субстрату 4. Гены, которые помогают осваивать клеткам-хозяевам новые источники углерода. Т. е. обеспечивающие преимущество клеток в конкретном окружении - Фенотипические маркеры Т. е. обеспечивающие возможность идентификации клеток носителей
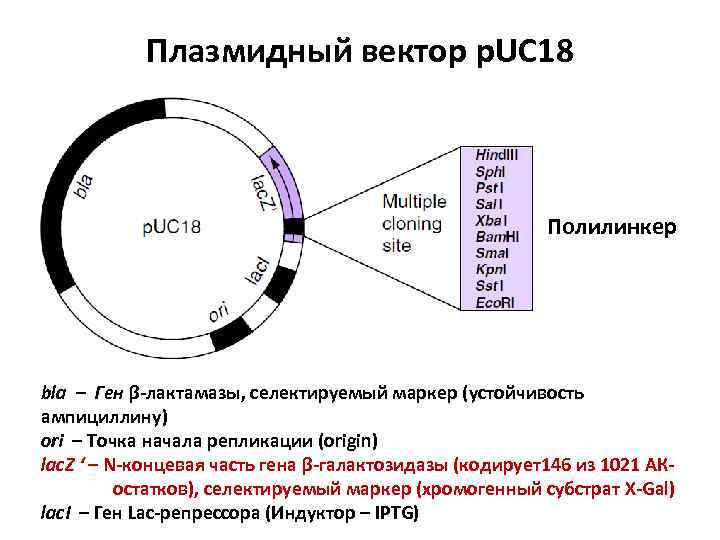
Плазмидный вектор p. UC 18 Полилинкер bla – Ген β-лактамазы, селектируемый маркер (устойчивость ампициллину) ori – Точка начала репликации (origin) lac. Z ‘ – N-концевая часть гена β-галактозидазы (кодирует146 из 1021 АКостатков), селектируемый маркер (хромогенный субстрат X-Gal) lac. I – Ген Lac-репрессора (Индуктор – IPTG)
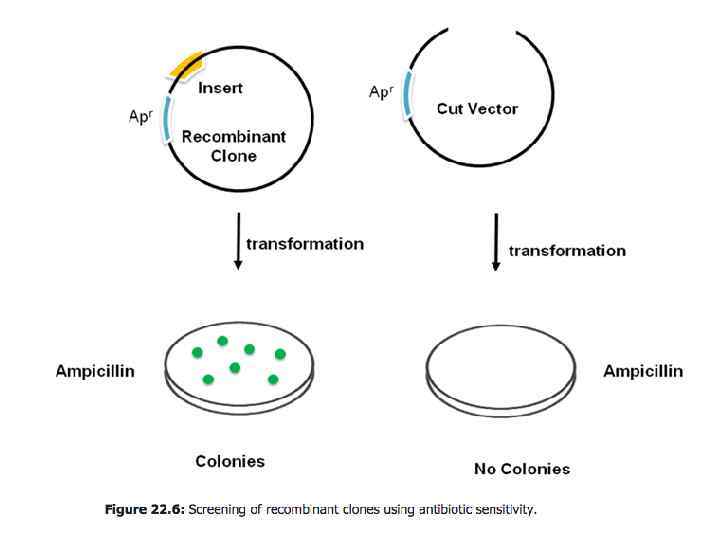

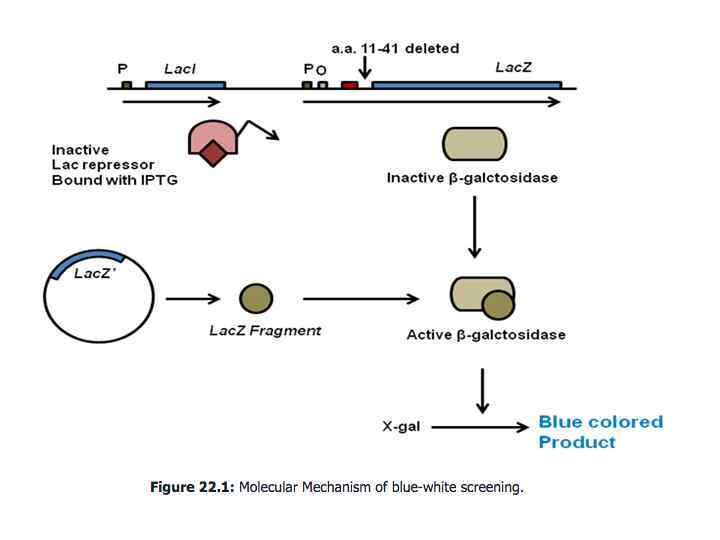
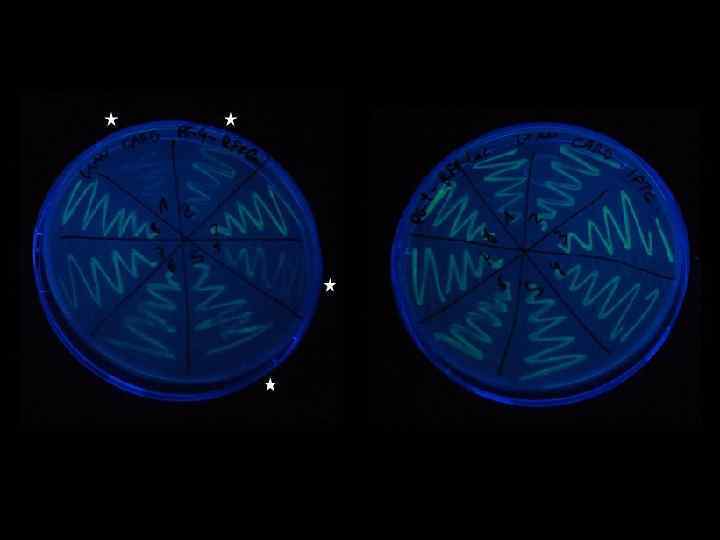
Бело-голубой скрининг
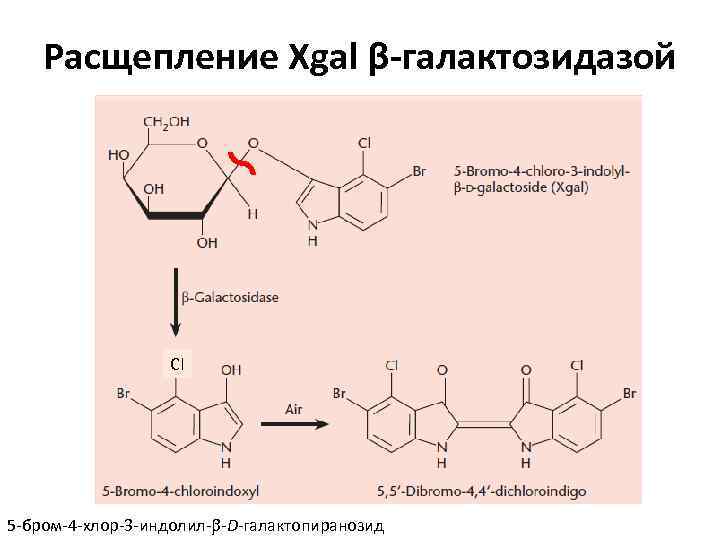
Расщепление Xgal β-галактозидазой Cl 5 -бром-4 -хлор-3 -индолил- -D-галактопиранозид
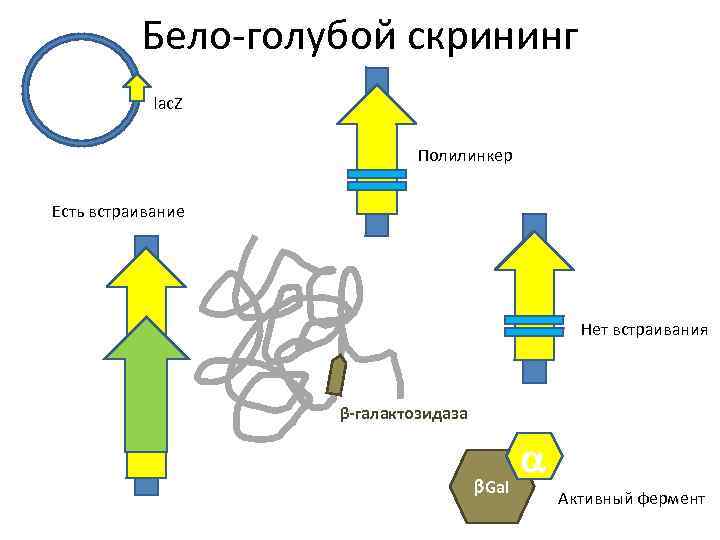
Бело-голубой скрининг lac. Z Полилинкер Есть встраивание Нет встраивания β-галактозидаза b. Gal a Активный фермент
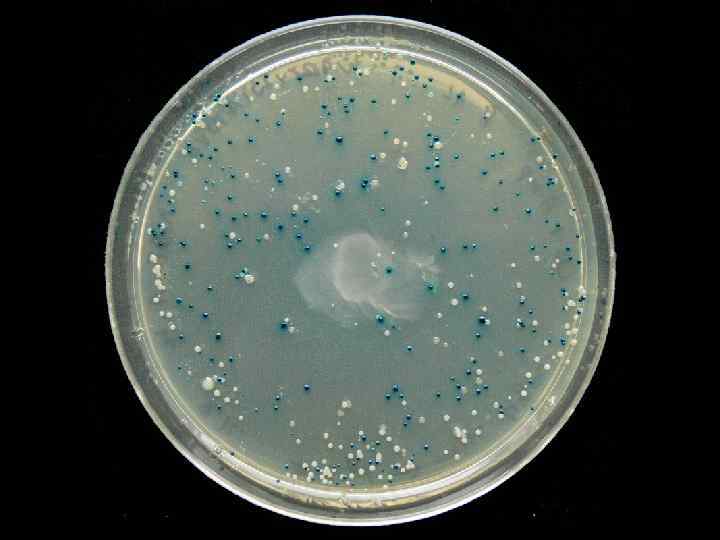


Синтез м-РНК. Промоторы. -35 -10 +1. . . TTGACA. . . . TATAAT. . cat консенсус. . . TTTACA. . . . TATATT. . cat lac-промотор. . . TTGACA. . . . TTAACT. . cat trp-промотор. . . TTGACA. . . . GATACT. . cat PL-промотор фага λ
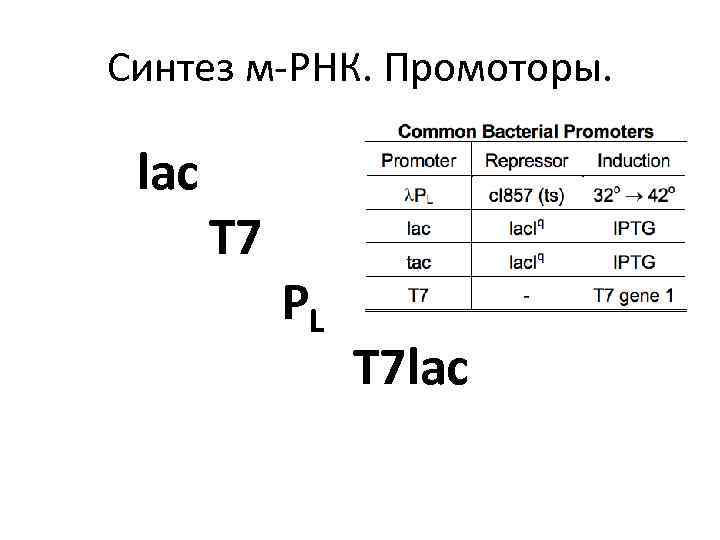
Синтез м-РНК. Промоторы. lac T 7 PL T 7 lac
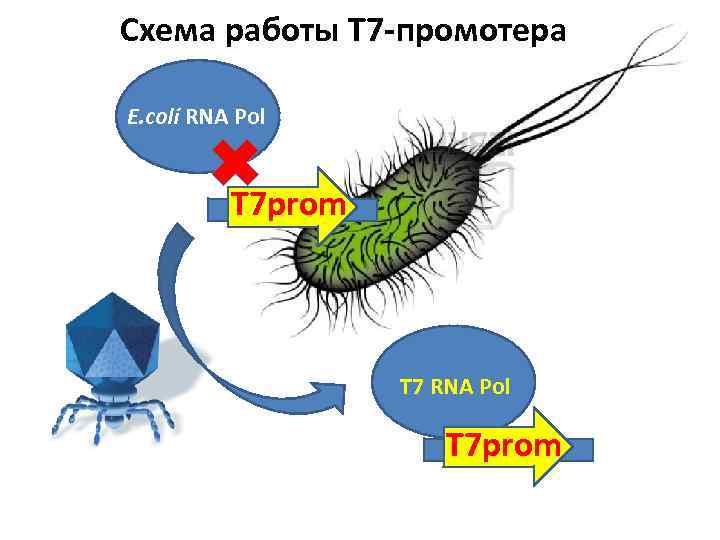
Схема работы Т 7 -промотера E. coli RNA Pol Т 7 prom Т 7 RNA Pol Т 7 prom
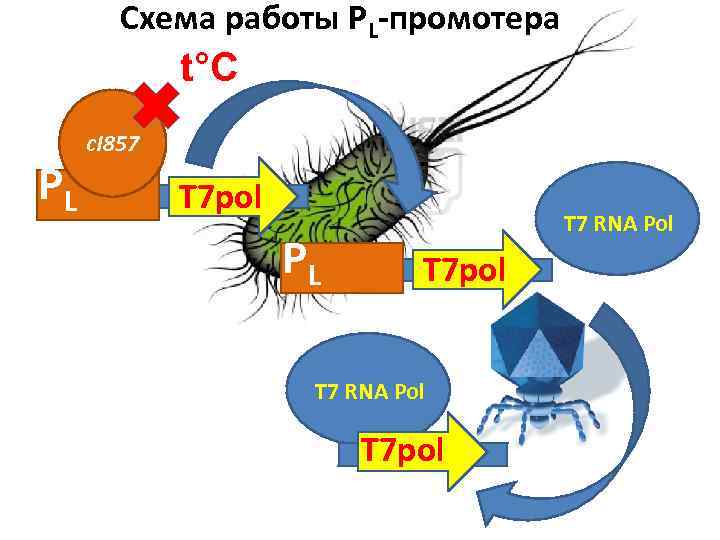
Схема работы PL-промотера t°C PL c. I 857 Т 7 pol PL Т 7 RNA Pol Т 7 pol
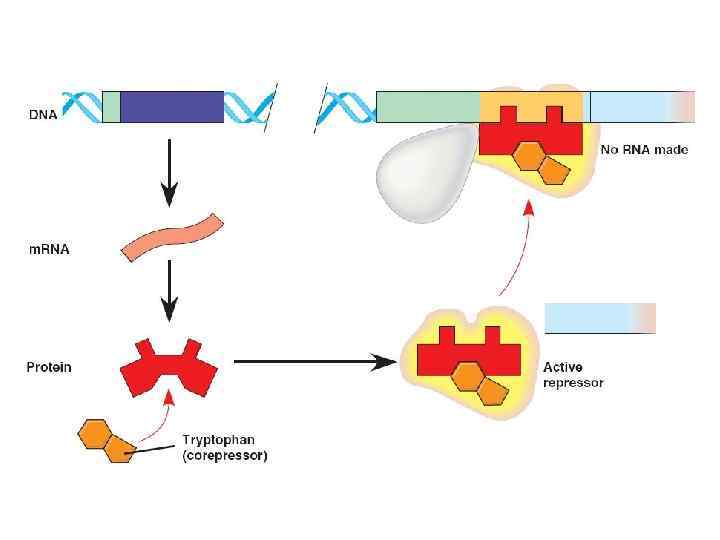
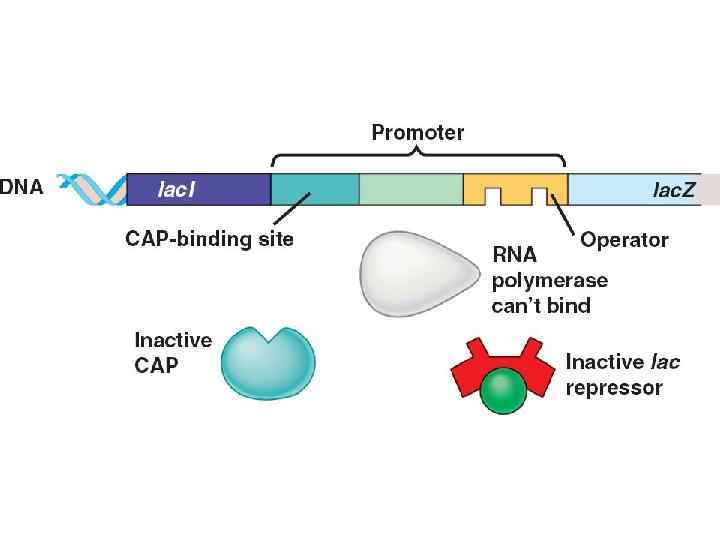
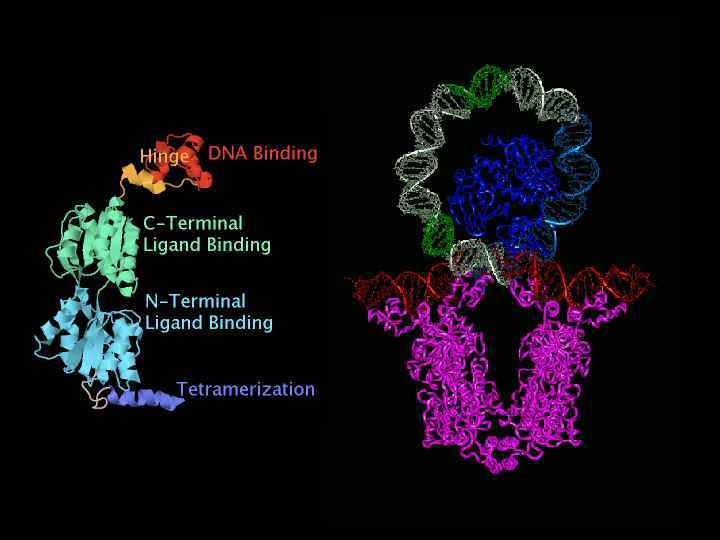
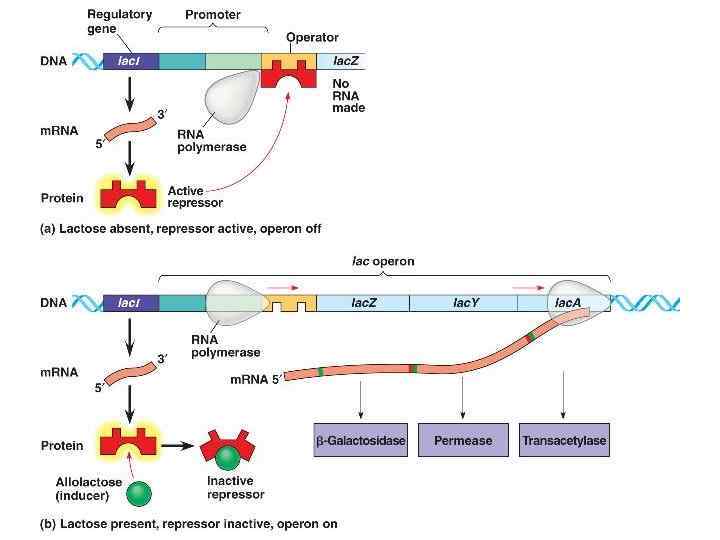
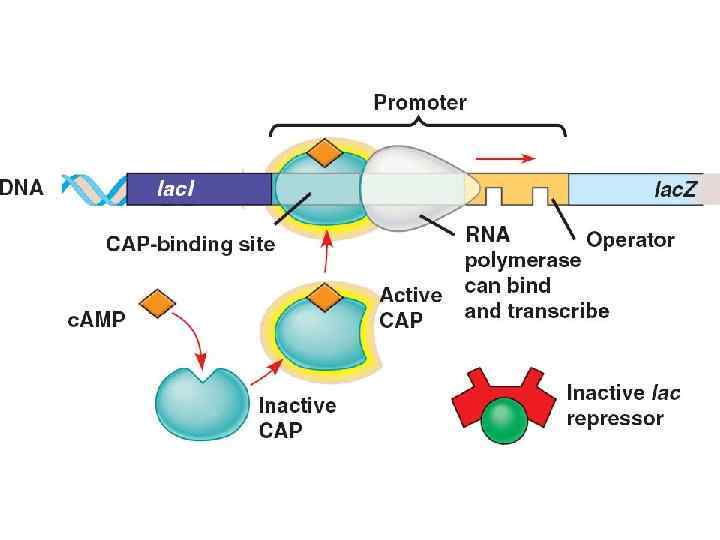
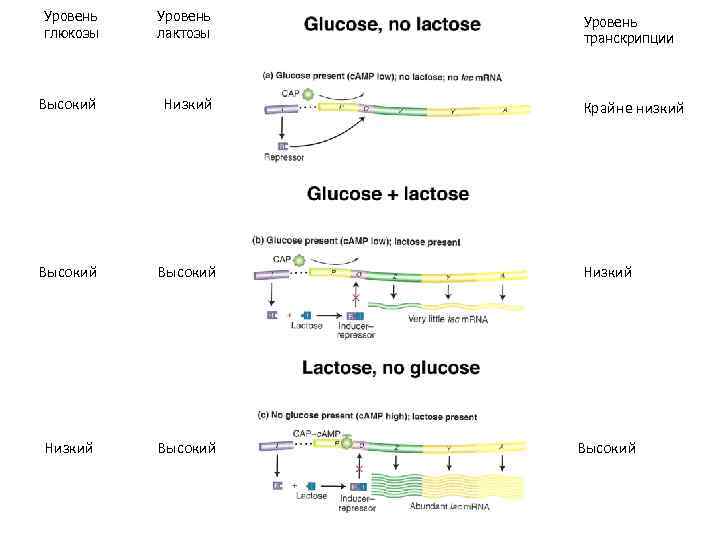
Уровень глюкозы Уровень лактозы Высокий Низкий Высокий Уровень транскрипции Крайне низкий
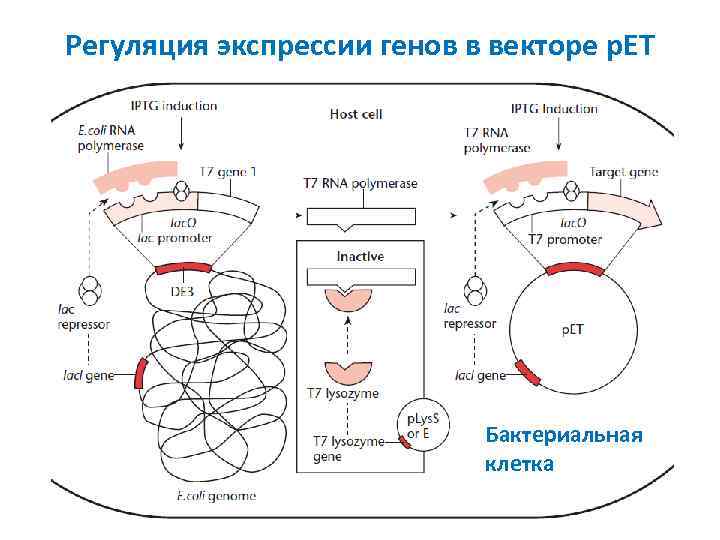
Регуляция экспрессии генов в векторе p. ET Бактериальная клетка

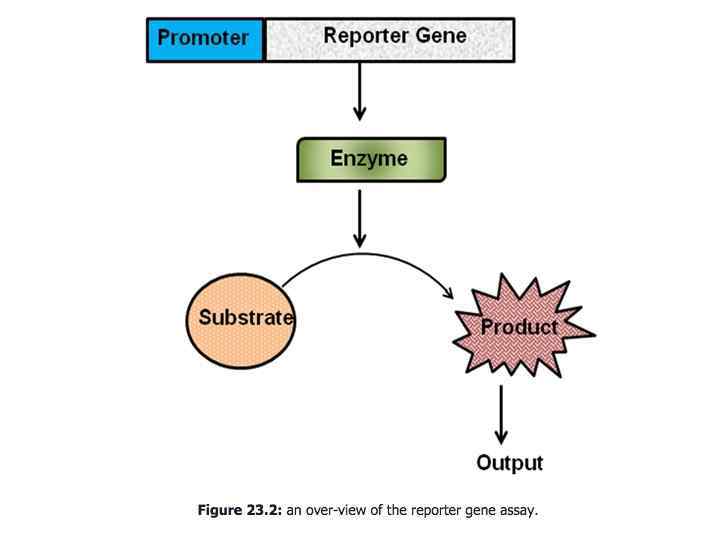
Синтез белка
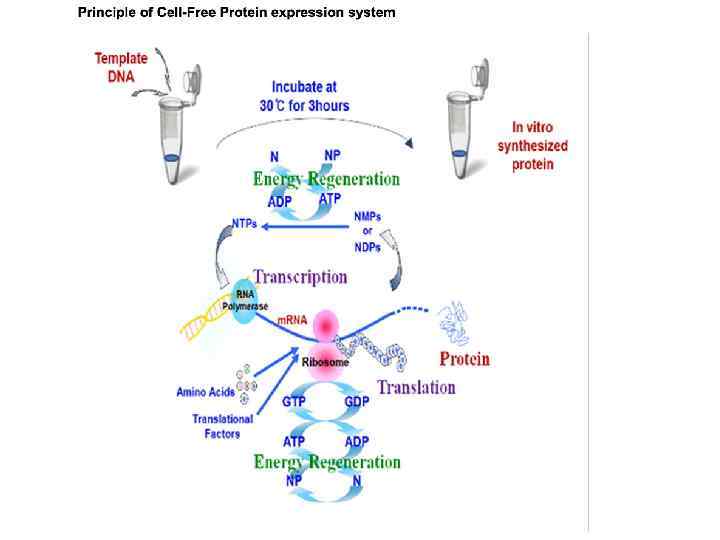
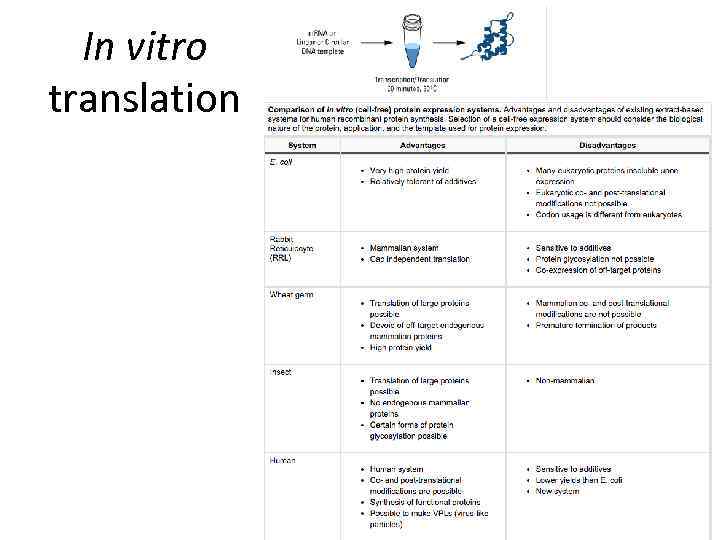
In vitro translation

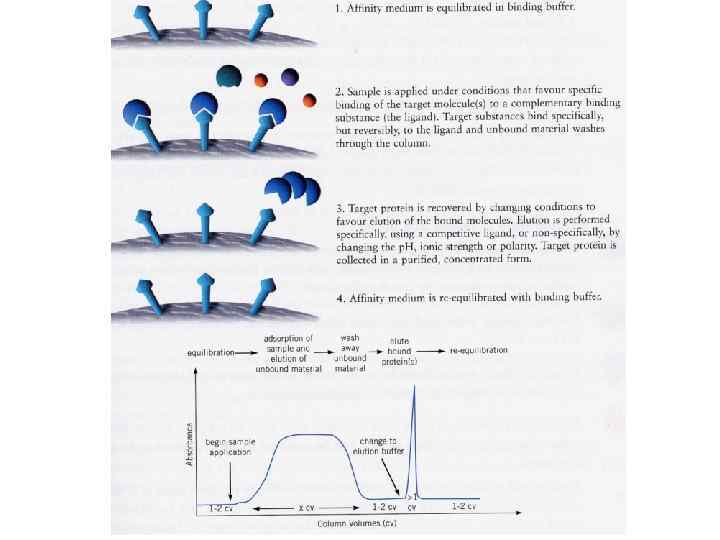
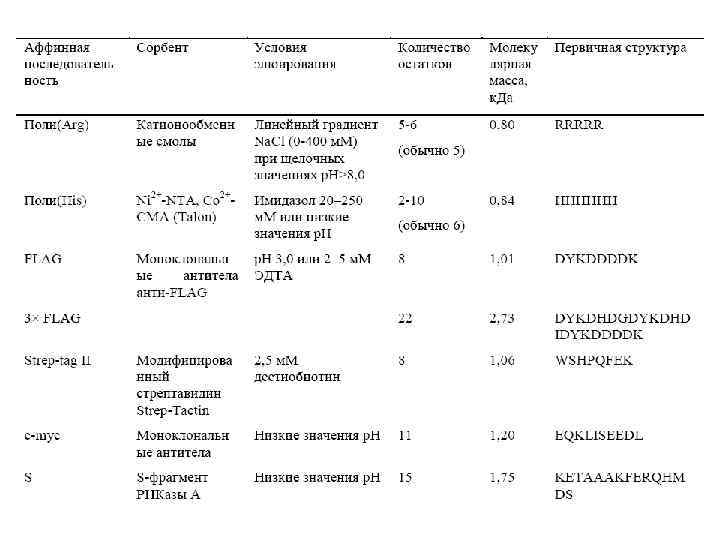
Кластеры (теги) для верификации и очистки рекомбинантных белков
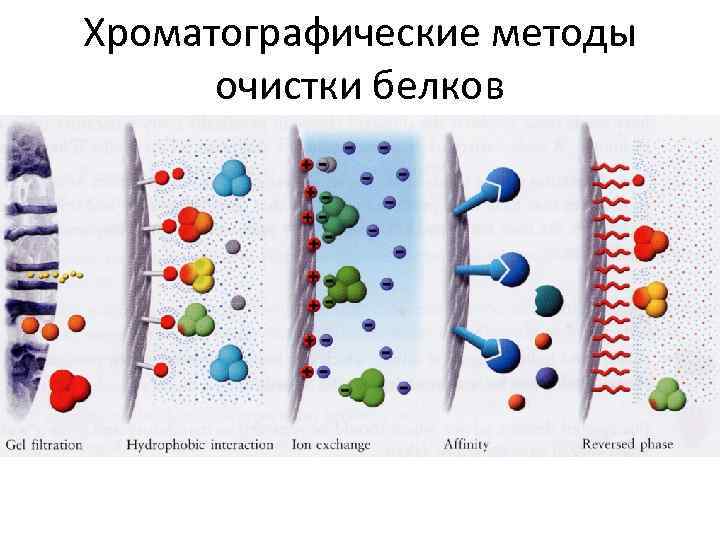
Хроматографические методы очистки белков

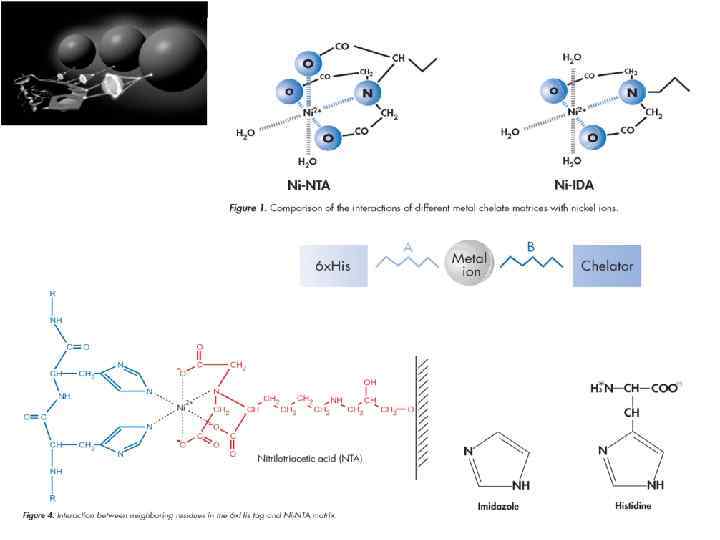

Частота встречаемости кодонов

Влияние концевого остатка На стабильность рекомбинантного белка оказывает заметное влияние природа аминокислотного остатка, непосредственно следующего за инициаторным N-концевым метионином. Этот аминокислотный остаток определяет эффективность удаления остатка формилметионина (f. Met), с которого всегда начинается синтез полипептидных цепей в бактериях. Такой N-концевой процессинг полипептида осуществляется метиониламинопептидазой, которая удаляет f. Met, и с увеличением размера аминокислотного остатка, непосредственно следующего за f. Met, уменьшается эффективность этого процесса. Резкое снижение или полное прекращение процессинга имеет место в том случае, если в этом положении полипептидной цепи находятся остатки His, Gln, Glu, Phe, Met, Lys, Tyr, Trp или Arg.

Влияние концевого остатка Arg, Lys, Phe, Leu, Trp и Tyr, время полужизни белка составляет <2 мин, и оно становится >10 мин при наличии в этом положении всех остальных аминокислотных остатков. Соответствующие аминокислотные остатки являются сигналом для распознавания белков убиквитин-зависимой системой протеолиза.


Проблемы при синтезе белка Вторичные сайты инициации трансляции. Последовательность внутри м. РНК, напоминающая сайт связывания рибосом AAGGAGG, которая расположена за 513 нуклеотидов перед AUG-кодоном, может стать причиной такой ошибочной инициации синтеза белка. Вторичная структура транскрипта рекомбинантного гена. 5’-концевой блок трансляции (5’ translational blockage). Введение редко используемых кодонов в м. РНК вблизи сайта инициации трансляции часто сопровождается подавлением трансляции м. РНК гена-репортера. Влияние терминатора транскрипции вектора. Наличие действенного терминатора транскрипции позади экспрессируемого рекомбинантного гена является еще одним условием эффективной экспрессии рекомбинантного белка. В том случае, если РНК-полимераза не прекращает синтеза РНК на границе рекомбинантного гена, может образоваться полицистронный транскрипт, в котором сайты инициации трансляции векторной плазмиды будут конкурировать за соответствующие участки целевой рекомбинантной м. РНК.

Каким образом можно стабилизировать рекомбинантный белок 1. Слитные белки 1. Периплазматические лидеры
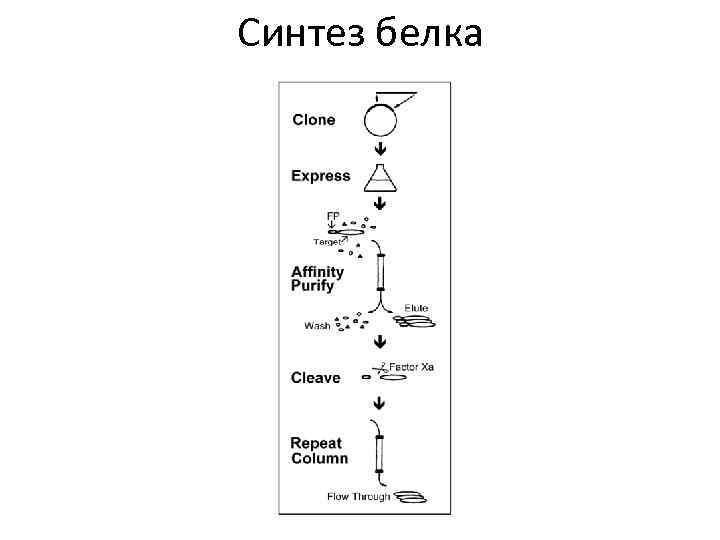
Синтез белка
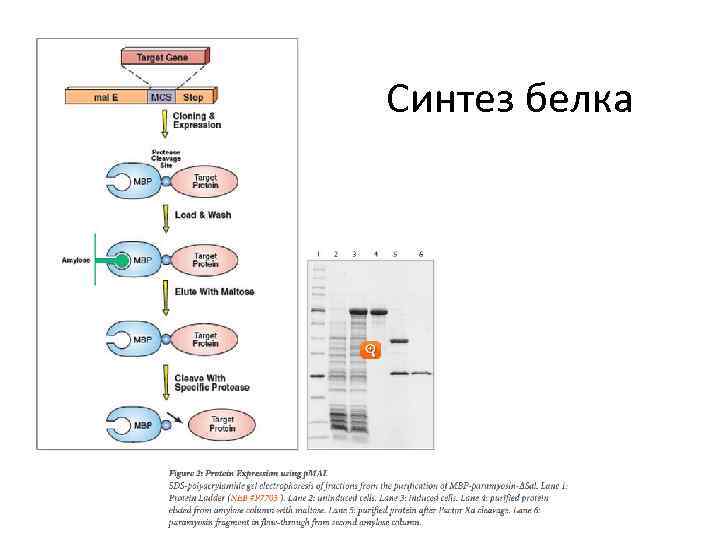
Синтез белка


Создание генетической конструкции, кодирующей каталитический домен ШПТ E. coli
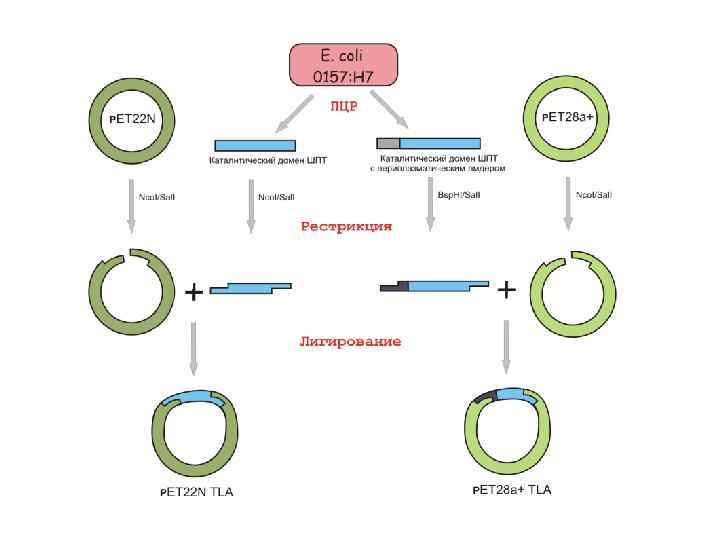
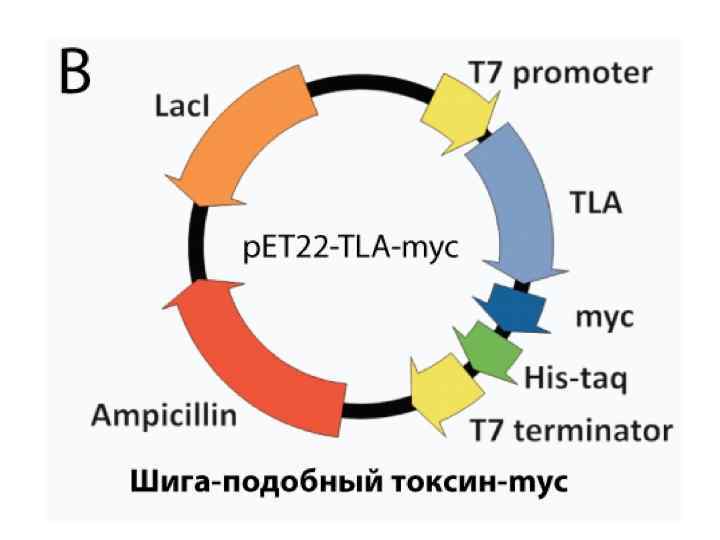

Что клонируем? • • Основной белок миелина человека 18. 3 к. Да Высокая изоэлектрическая точка MASQKRPSQRHGSKYLATASTMDHARHGFLPRH RDTGILDSIGRFFGGDRGAPKRGSGKDSHHPARTA HYGSLPQKSHGRTQDENPVVHFFKNIVTPRTPPPS QGKGRGLSLSRFSWGAEGQRPGFGYGGRASDYKS AHKGFKGVDAQGTLSKIFKLGGRDSRSGSPMARR

Создание генетической конструкции, кодирующей полноразмерный МВР
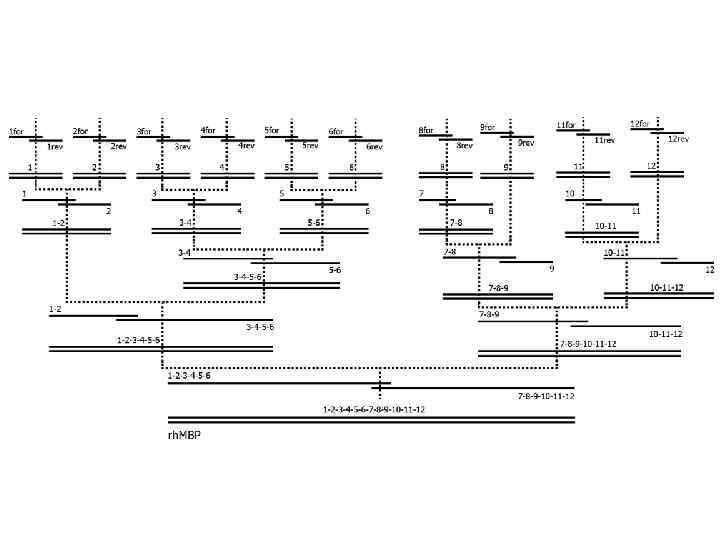
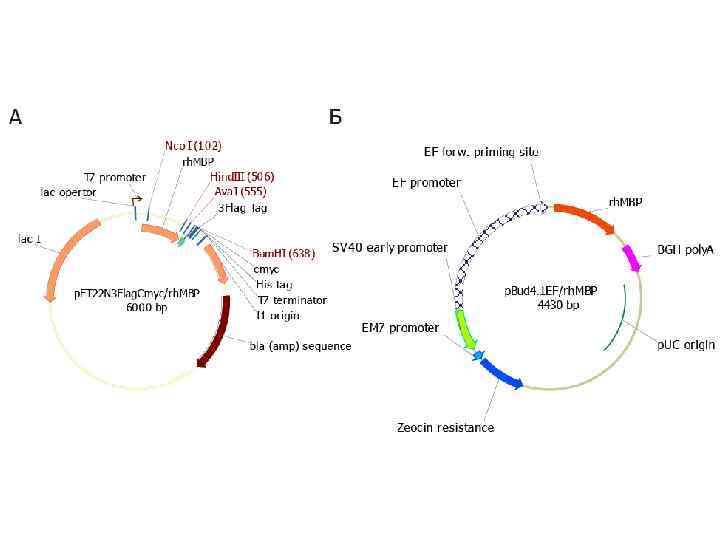
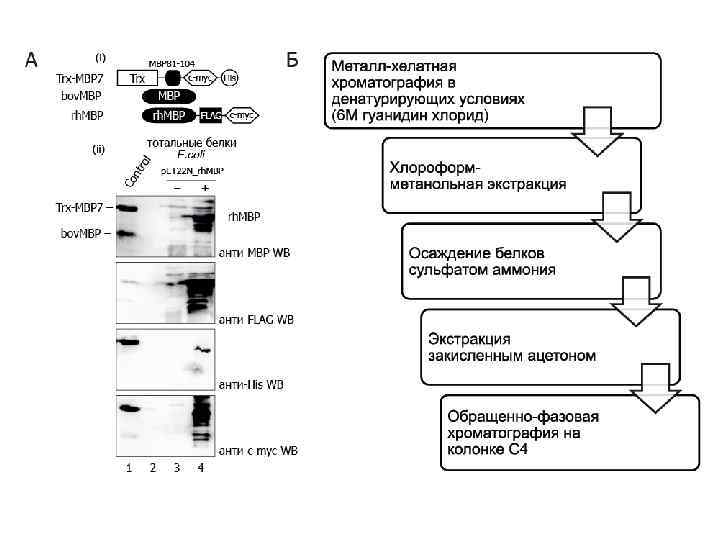
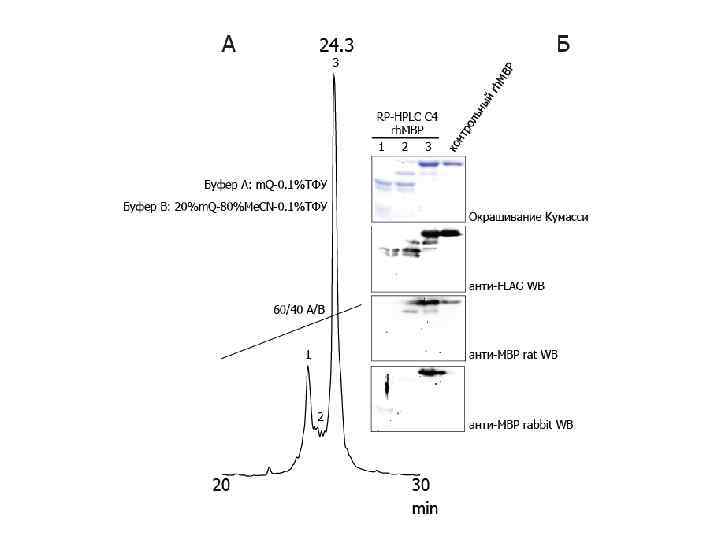

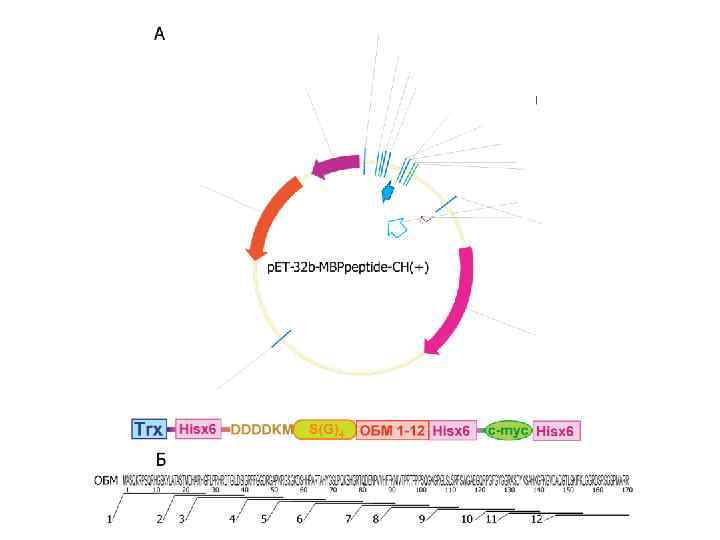
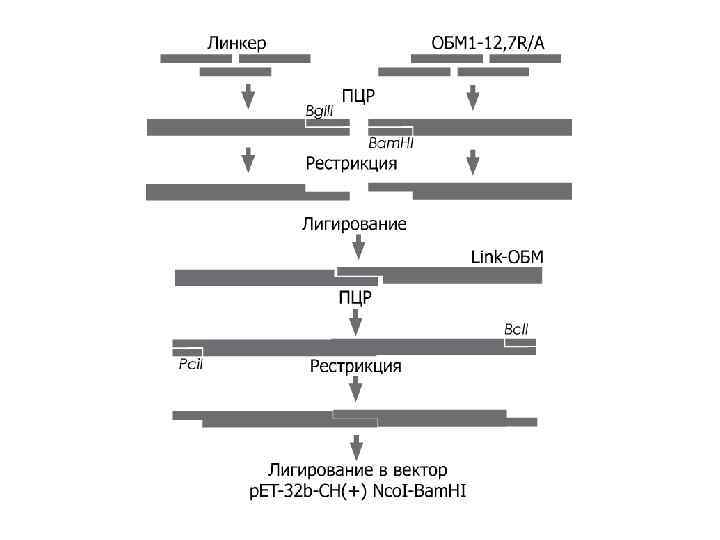
Создание эпитопной библиотеки основного белка миелина

Фрагментация • Белок разделили на 12 перекрывающихся фрагментов размером в среднем 25 аминокислот

Куда клонируем? • Явная необходимость белка-носителя • Необходимо ввести специфические кластеры для очистки и идентификации рекомбинантных белков • Обеспечить корректную презентацию пептидов в растворе

ГенИнж2.ppt