L_7_OVR.ppt
- Количество слайдов: 61
 Лекция 11 Окислительновосстановительные реакции.
Лекция 11 Окислительновосстановительные реакции.
 Типы химических реакций • Реакции протекающие с изменением степени окисления элементов в реагирующих веществах(см. лекцию ОВР) • Реакции, протекающие без изменения степени окисления элементов в реагирующих веществах.
Типы химических реакций • Реакции протекающие с изменением степени окисления элементов в реагирующих веществах(см. лекцию ОВР) • Реакции, протекающие без изменения степени окисления элементов в реагирующих веществах.
 Реакции соединения – реакции в результате которых из 2 -х и более веществ образуется одно • 2 Mg + O 2 2 Mg. O • Ca. O + CO 2 Ca. CO 3
Реакции соединения – реакции в результате которых из 2 -х и более веществ образуется одно • 2 Mg + O 2 2 Mg. O • Ca. O + CO 2 Ca. CO 3
 Реакции разложения – реакции в результате которых из одного вещества образуются два и более веществ • (NH 4)2 Cr 2 O 7 N 2 + Cr 2 O 3 + 4 H 2 O • Cu(OH)2 Cu. O + H 2 O • Условия: нагревание, тепловой или световой импульс, реже самопроизвольно
Реакции разложения – реакции в результате которых из одного вещества образуются два и более веществ • (NH 4)2 Cr 2 O 7 N 2 + Cr 2 O 3 + 4 H 2 O • Cu(OH)2 Cu. O + H 2 O • Условия: нагревание, тепловой или световой импульс, реже самопроизвольно
 Реакции замещения – реакции, в результате которых атомы простого вещества замещают атомы одного из элементов в сложном веществе (всегда ОВР) • Zn + 2 HCl Zn. Cl 2 + H 2 • 2 Al + 3 Cu. SO 4 Al 2(SO 4)3 + 3 Cu
Реакции замещения – реакции, в результате которых атомы простого вещества замещают атомы одного из элементов в сложном веществе (всегда ОВР) • Zn + 2 HCl Zn. Cl 2 + H 2 • 2 Al + 3 Cu. SO 4 Al 2(SO 4)3 + 3 Cu
 Реакции обмена – реакции в результате которых молекулы 2 -х соединений обмениваются своими составными частями (без изменения с. о. ) • Cu. SO 4 + 2 Na. OH Cu(OH)2 + Na 2 SO 4
Реакции обмена – реакции в результате которых молекулы 2 -х соединений обмениваются своими составными частями (без изменения с. о. ) • Cu. SO 4 + 2 Na. OH Cu(OH)2 + Na 2 SO 4
 Эти реакции протекают необратимо если: • Образуется осадок • Выделяется газ • Образуется слабый электролит (вода и др. )
Эти реакции протекают необратимо если: • Образуется осадок • Выделяется газ • Образуется слабый электролит (вода и др. )
 По тепловому эффекту • Экзотермические - протекают с выделением тепла Ca(OH)2+2 HCl Ca. Cl 2+2 H 2 O + Q • Эндотермические - протекают с поглощением тепла Ca. CO 3 Ca. O + CO 2 – Q
По тепловому эффекту • Экзотермические - протекают с выделением тепла Ca(OH)2+2 HCl Ca. Cl 2+2 H 2 O + Q • Эндотермические - протекают с поглощением тепла Ca. CO 3 Ca. O + CO 2 – Q
 Необратимые реакции – реакции, которые при данных условиях протекают практически только в одном направлении. • Обратимые реакции – реакции, которые при данных условиях протекает впрямом и обратном направлениях 2 NO N 2 O 4
Необратимые реакции – реакции, которые при данных условиях протекают практически только в одном направлении. • Обратимые реакции – реакции, которые при данных условиях протекает впрямом и обратном направлениях 2 NO N 2 O 4
 определние Окислительновосстановительные реакции (ОВР) – реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ.
определние Окислительновосстановительные реакции (ОВР) – реакции, протекающие с изменением степени окисления атомов, входящих в состав реагирующих веществ.
 Окисление, восстановитель Окисление – процесс отдачи электронов атомом, молекулой или ионом. Восстановитель – атом, молекула или ион, отдающий электроны.
Окисление, восстановитель Окисление – процесс отдачи электронов атомом, молекулой или ионом. Восстановитель – атом, молекула или ион, отдающий электроны.
 Примеры записи процесса окисления Примеры: Al – 3 e Al 3+ H 20 – 2 e 2 H+ 2 Cl- -2 e Cl 2 Восстановитель окисляется. При этом его степень окисления повышается
Примеры записи процесса окисления Примеры: Al – 3 e Al 3+ H 20 – 2 e 2 H+ 2 Cl- -2 e Cl 2 Восстановитель окисляется. При этом его степень окисления повышается
 Восстановление, окислитель Восстановление – процесс присоединения электронов атомом, молекулой или ионом. Окислитель – атом, молекула или ион, присоединяющий электроны.
Восстановление, окислитель Восстановление – процесс присоединения электронов атомом, молекулой или ионом. Окислитель – атом, молекула или ион, присоединяющий электроны.
 Примеры записи восстановления Примеры: S 0 +2 e S 2 Cl 2 +2 e 2 Cl Окислитель восстанавливается. Его степень окисления понижается
Примеры записи восстановления Примеры: S 0 +2 e S 2 Cl 2 +2 e 2 Cl Окислитель восстанавливается. Его степень окисления понижается
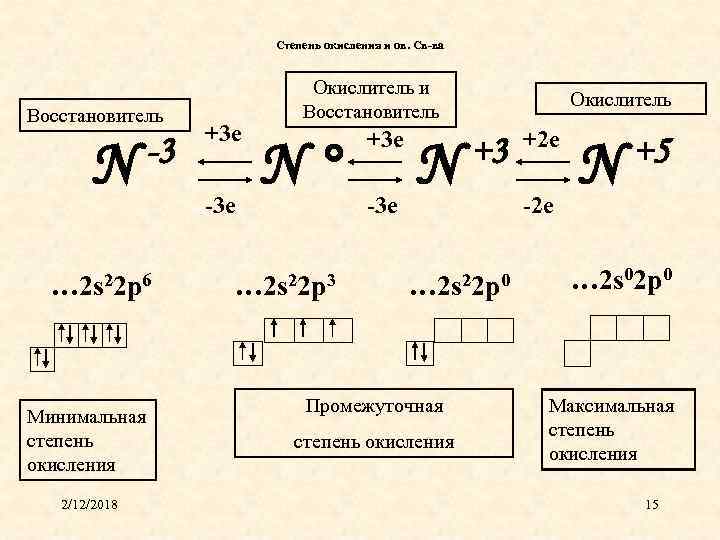 Степень окисления и ов. Св-ва Восстановитель N -3 … 2 s 22 p 6 Минимальная степень окисления 2/12/2018 +3 e -3 e Окислитель и Восстановитель N° … 2 s 22 p 3 +3 e -3 e N Окислитель +3 … 2 s 22 p 0 Промежуточная степень окисления +2 e -2 e N +5 … 2 s 02 p 0 Максимальная степень окисления 15
Степень окисления и ов. Св-ва Восстановитель N -3 … 2 s 22 p 6 Минимальная степень окисления 2/12/2018 +3 e -3 e Окислитель и Восстановитель N° … 2 s 22 p 3 +3 e -3 e N Окислитель +3 … 2 s 22 p 0 Промежуточная степень окисления +2 e -2 e N +5 … 2 s 02 p 0 Максимальная степень окисления 15
 Восстановители. • простые вещества металлы, Н 2, С, Si, Р • ионы в минимальной степени окисления (S 2 -, I-, Br-, Cl-, N 3 -) • некоторые ионы металлов в меньшей из возможных с. о. (Fe 2+, Sn 2+ , Cu+) • органические вещества: спирты, альдегиды, глюкоза
Восстановители. • простые вещества металлы, Н 2, С, Si, Р • ионы в минимальной степени окисления (S 2 -, I-, Br-, Cl-, N 3 -) • некоторые ионы металлов в меньшей из возможных с. о. (Fe 2+, Sn 2+ , Cu+) • органические вещества: спирты, альдегиды, глюкоза
 Окислители • Простые вещества: О 2, О 3, галогены (F 2, Cl 2, Br 2, I 2) • Ионы неметаллов и металлов в высшей с. о. (S+6, N+5, Mn+7, Cr+6) • Оксиды металлов (Cu. O, Pb. O 2, Ag 2 O, Cr. O 3, Mn. O 2)
Окислители • Простые вещества: О 2, О 3, галогены (F 2, Cl 2, Br 2, I 2) • Ионы неметаллов и металлов в высшей с. о. (S+6, N+5, Mn+7, Cr+6) • Оксиды металлов (Cu. O, Pb. O 2, Ag 2 O, Cr. O 3, Mn. O 2)
 Окислительно-восстановительная двойственность Элементы в промежуточной степени окисления могут проявлять как свойства восстановителя, так и свойства окислителя, так как могут и повышать степень окисления (отдают электроны, окисляются), так и понижать (принимают электроны, восстанавливаются).
Окислительно-восстановительная двойственность Элементы в промежуточной степени окисления могут проявлять как свойства восстановителя, так и свойства окислителя, так как могут и повышать степень окисления (отдают электроны, окисляются), так и понижать (принимают электроны, восстанавливаются).
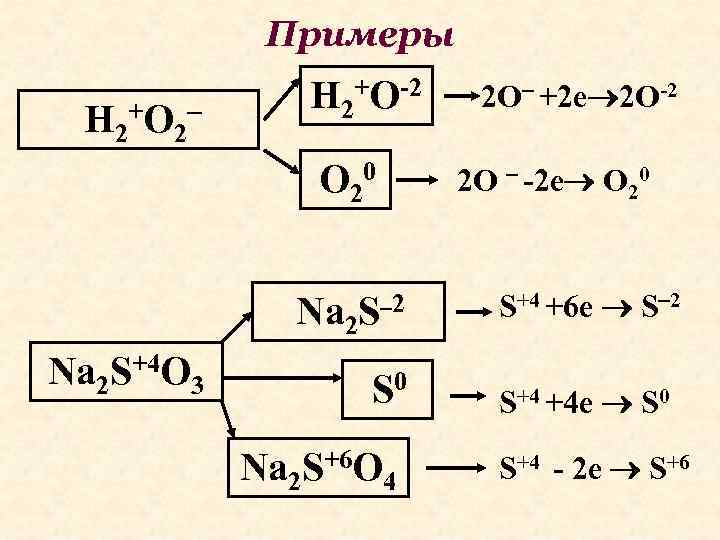 Примеры H 2+O-2 H 2+O 2 О 20 2 О -2 е О 20 2 S+4 +6 e S 2 S 0 S+4 +4 e S 0 Na 2 S+4 O 3 2 О +2 е 2 О-2 Na 2 S+6 O 4 S+4 - 2 e S+6
Примеры H 2+O-2 H 2+O 2 О 20 2 О -2 е О 20 2 S+4 +6 e S 2 S 0 S+4 +4 e S 0 Na 2 S+4 O 3 2 О +2 е 2 О-2 Na 2 S+6 O 4 S+4 - 2 e S+6

 Радиус атома (радиус Слейтера) – расстояние от ядра атома до максимума электронной плотности его валентных электронов Обозначение r. Размерность пм (пикометр – 10 -12 м) или нм (нанометр – 10 -9 м) rан >rат> rкат
Радиус атома (радиус Слейтера) – расстояние от ядра атома до максимума электронной плотности его валентных электронов Обозначение r. Размерность пм (пикометр – 10 -12 м) или нм (нанометр – 10 -9 м) rан >rат> rкат
![Энергия ионизации [к. Дж/моль] • Определяет восстановительную способность атомов элементов • Энергия, необходимая для Энергия ионизации [к. Дж/моль] • Определяет восстановительную способность атомов элементов • Энергия, необходимая для](https://present5.com/presentation/90992014_142242824/image-22.jpg) Энергия ионизации [к. Дж/моль] • Определяет восстановительную способность атомов элементов • Энергия, необходимая для превращения 1 моль атомов в газовой фазе в 1 моль катионов в газовой фазе. • Первая энергия ионизации характеризует способность атома отдавать 1 электрон
Энергия ионизации [к. Дж/моль] • Определяет восстановительную способность атомов элементов • Энергия, необходимая для превращения 1 моль атомов в газовой фазе в 1 моль катионов в газовой фазе. • Первая энергия ионизации характеризует способность атома отдавать 1 электрон
 Энергия сродства к электрону. • Характеризует окислительную способность атомов элементов • Энергия, которая выделяется присоединении 1 моль электронов к 1 моль атомов в газовой фазе
Энергия сродства к электрону. • Характеризует окислительную способность атомов элементов • Энергия, которая выделяется присоединении 1 моль электронов к 1 моль атомов в газовой фазе
 • Также об о-в св-вах можно судить по величине ОЭО и по положению атома элемента в ПС. • Чем выше ОЭО и меньше радиус атома, тем более сильным окислителем является элемент.
• Также об о-в св-вах можно судить по величине ОЭО и по положению атома элемента в ПС. • Чем выше ОЭО и меньше радиус атома, тем более сильным окислителем является элемент.
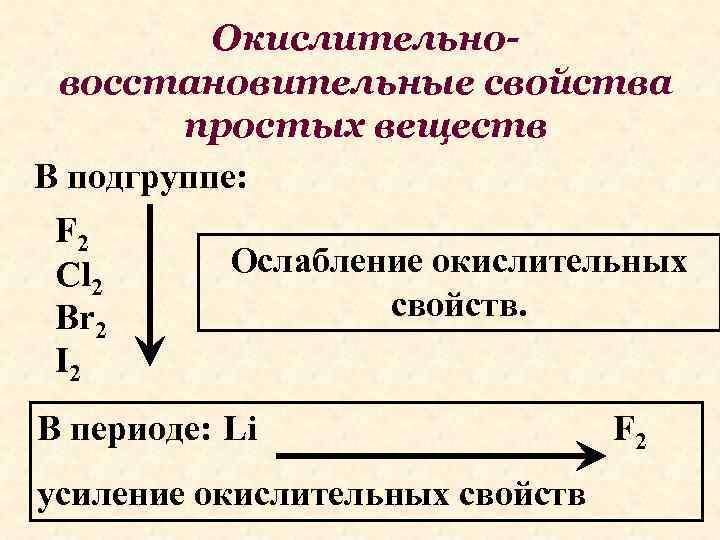 Окислительновосстановительные свойства простых веществ В подгруппе: F 2 Ослабление окислительных Cl 2 свойств. Br 2 I 2 В периоде: Li усиление окислительных свойств F 2
Окислительновосстановительные свойства простых веществ В подгруппе: F 2 Ослабление окислительных Cl 2 свойств. Br 2 I 2 В периоде: Li усиление окислительных свойств F 2
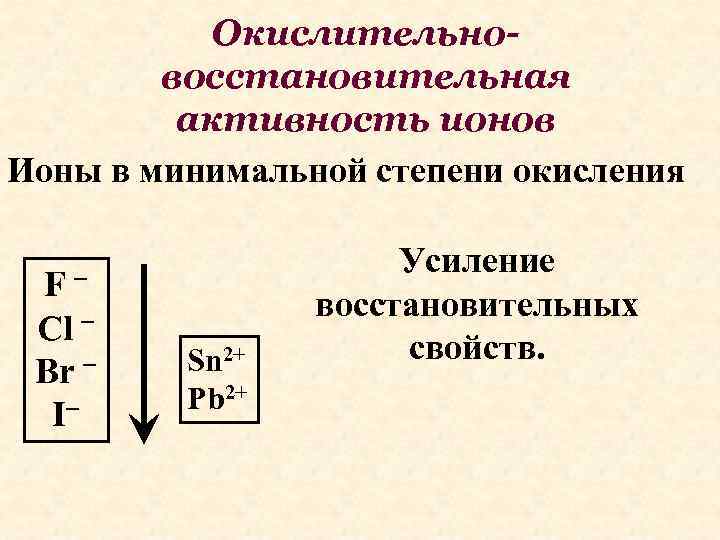 Окислительновосстановительная активность ионов Ионы в минимальной степени окисления F Cl Br I Sn 2+ Pb 2+ Усиление восстановительных свойств.
Окислительновосстановительная активность ионов Ионы в минимальной степени окисления F Cl Br I Sn 2+ Pb 2+ Усиление восстановительных свойств.
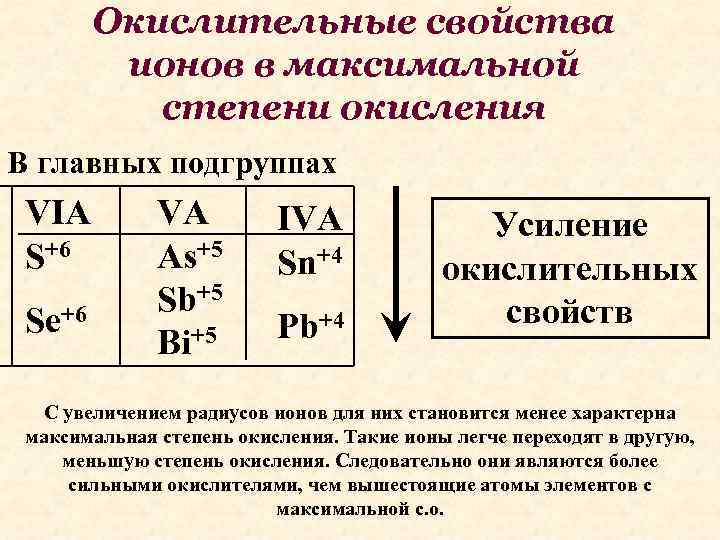 Окислительные свойства ионов в максимальной степени окисления В главных подгруппах VIA S+6 Se+6 VA As+5 Sb+5 Bi+5 IVA Sn+4 Pb+4 Усиление окислительных свойств С увеличением радиусов ионов для них становится менее характерна максимальная степень окисления. Такие ионы легче переходят в другую, меньшую степень окисления. Следовательно они являются более сильными окислителями, чем вышестоящие атомы элементов с максимальной с. о.
Окислительные свойства ионов в максимальной степени окисления В главных подгруппах VIA S+6 Se+6 VA As+5 Sb+5 Bi+5 IVA Sn+4 Pb+4 Усиление окислительных свойств С увеличением радиусов ионов для них становится менее характерна максимальная степень окисления. Такие ионы легче переходят в другую, меньшую степень окисления. Следовательно они являются более сильными окислителями, чем вышестоящие атомы элементов с максимальной с. о.
 Типы ОВР Межмолекулярные ОВР – реакции, в которых окислитель и восстановитель содержатся в молекулах разных веществ. 2 Сu 0 +O 20 2 Cu 2+O 23 H 2 S 2 +H 2 S+6 O 4 4 S 0 + 4 H 2 O 6 KI + 4 H 2 S+6 O 4 3 I 20+S 0 +3 K 2 SO 4+4 H 2 O
Типы ОВР Межмолекулярные ОВР – реакции, в которых окислитель и восстановитель содержатся в молекулах разных веществ. 2 Сu 0 +O 20 2 Cu 2+O 23 H 2 S 2 +H 2 S+6 O 4 4 S 0 + 4 H 2 O 6 KI + 4 H 2 S+6 O 4 3 I 20+S 0 +3 K 2 SO 4+4 H 2 O
 Внутримолекулярные ОВР Реакции, которые идут с изменением степени окисления разных атомов элементов, содержащихся в одной молекуле. Молекула вещества содержит окислитель и восстановитель (N-3 H 4)2 Cr 2+6 O 7 (t 0) N 20 + Cr 2+3 O 3 + 4 H 2 O 2 Na. N+5 O 3 -2 2 Na. N+3 O 2 + O 20 KCl+5 O 3 2 2 KCl + 3 O 20
Внутримолекулярные ОВР Реакции, которые идут с изменением степени окисления разных атомов элементов, содержащихся в одной молекуле. Молекула вещества содержит окислитель и восстановитель (N-3 H 4)2 Cr 2+6 O 7 (t 0) N 20 + Cr 2+3 O 3 + 4 H 2 O 2 Na. N+5 O 3 -2 2 Na. N+3 O 2 + O 20 KCl+5 O 3 2 2 KCl + 3 O 20
 Реакции диспропорционирования (самоокислениясамовосстановления) Это реакции, идущие с изменением степени окисления одного атома элемента в молекуле одного и того же вещества. Атом элемента в промежуточной степени окисления. Он может и понижать и повышать степень окисления. 4 KCl+5 O 3 KCl +3 KCl+7 O 4 Cl 20 + 2 KOH KCl +KCl+1 O +H 2 O 4 Na 2 S+4 O 3 Na 2 S 2 + 3 Na 2 S+6 O 4
Реакции диспропорционирования (самоокислениясамовосстановления) Это реакции, идущие с изменением степени окисления одного атома элемента в молекуле одного и того же вещества. Атом элемента в промежуточной степени окисления. Он может и понижать и повышать степень окисления. 4 KCl+5 O 3 KCl +3 KCl+7 O 4 Cl 20 + 2 KOH KCl +KCl+1 O +H 2 O 4 Na 2 S+4 O 3 Na 2 S 2 + 3 Na 2 S+6 O 4
 Правила составления ОВР 1. Записать схему ОВР. 2. Определить степени окисления элементов в реагирующих веществах. 3. Подчеркнуть символы элементов, изменяющих степени окисления. 4. Составить уравнения электронного баланса, указать окислитель и восстановитель, процессы окисления и восстановления.
Правила составления ОВР 1. Записать схему ОВР. 2. Определить степени окисления элементов в реагирующих веществах. 3. Подчеркнуть символы элементов, изменяющих степени окисления. 4. Составить уравнения электронного баланса, указать окислитель и восстановитель, процессы окисления и восстановления.
 Продолжение 5. Уравнять число отданных и принятых электронов. 6. Расставить коэффициенты при восстановителе и окислителе и проверить количество атомов каждого элемента. Если нужно, уравнять количество атомов других элементов 7. Правильность подбора коэффициентов проверить по водороду и кислороду.
Продолжение 5. Уравнять число отданных и принятых электронов. 6. Расставить коэффициенты при восстановителе и окислителе и проверить количество атомов каждого элемента. Если нужно, уравнять количество атомов других элементов 7. Правильность подбора коэффициентов проверить по водороду и кислороду.
 Примеры 0 +6 +2 -2 4 Mg + H 2 SO 4 (к) Mg. SO 4+H 2 S + H 2 O 4 5 4 Восстановитель Mg 0 -2 е- Mg+2 Окисление Окислитель 8 4 S +6 +8 е- S-2 Восстановле 2 1 4 Mg 0 + S +6 4 Mg+2 + S-2 ние
Примеры 0 +6 +2 -2 4 Mg + H 2 SO 4 (к) Mg. SO 4+H 2 S + H 2 O 4 5 4 Восстановитель Mg 0 -2 е- Mg+2 Окисление Окислитель 8 4 S +6 +8 е- S-2 Восстановле 2 1 4 Mg 0 + S +6 4 Mg+2 + S-2 ние
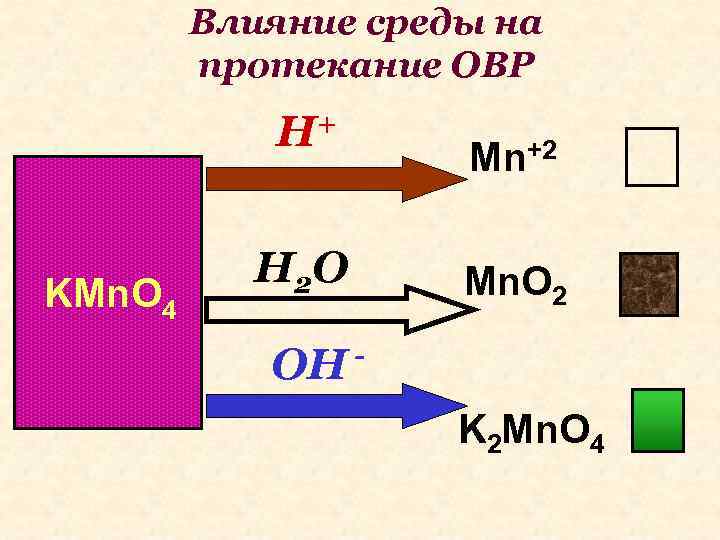 Влияние среды на протекание ОВР H+ KMn. O 4 H 2 O Mn+2 Mn. O 2 OH K 2 Mn. O 4
Влияние среды на протекание ОВР H+ KMn. O 4 H 2 O Mn+2 Mn. O 2 OH K 2 Mn. O 4
 Перманганат в кислой среде + +7 -2 + +4 – 2 + +6 – 2 +2 +6 – 2 + -2 2 KMn. O 4 + 5 Na 2 SO 3+3 H 2 SO 4 = 2 Mn. SO 4+ 5 Na 2 SO 4 + K 2 SO 4 + H 2 O 3 Окислитель Mn+7 +5 e- Mn+2 2 Восстановление Восстановитель S+4 -2 e- S+6 2 Mn+7 + 5 S+4 2 Mn+2 + 5 S+6 5 Окисление
Перманганат в кислой среде + +7 -2 + +4 – 2 + +6 – 2 +2 +6 – 2 + -2 2 KMn. O 4 + 5 Na 2 SO 3+3 H 2 SO 4 = 2 Mn. SO 4+ 5 Na 2 SO 4 + K 2 SO 4 + H 2 O 3 Окислитель Mn+7 +5 e- Mn+2 2 Восстановление Восстановитель S+4 -2 e- S+6 2 Mn+7 + 5 S+4 2 Mn+2 + 5 S+6 5 Окисление
 Перманганат в нейтральной и щелочной среде KMn. O 4 + Na 2 SO 3+ H 2 O = Mn. O 2+ Na 2 SO 4 + KOH KMn. O 4 + Na 2 SO 3+ КOH = K 2 Mn. O 4+ Na 2 SO 4 + H 2 O
Перманганат в нейтральной и щелочной среде KMn. O 4 + Na 2 SO 3+ H 2 O = Mn. O 2+ Na 2 SO 4 + KOH KMn. O 4 + Na 2 SO 3+ КOH = K 2 Mn. O 4+ Na 2 SO 4 + H 2 O
 Электродные потенциалы. Электрохимические процессы в растворах. Возможность и полноту протекания ОВР определяет величина электродного потенциала данной полуреакции. Значение электродных потециалов различных полуреакций при стандартных условиях приводятся в справочных таблицах.
Электродные потенциалы. Электрохимические процессы в растворах. Возможность и полноту протекания ОВР определяет величина электродного потенциала данной полуреакции. Значение электродных потециалов различных полуреакций при стандартных условиях приводятся в справочных таблицах.
 Условие протекания ОВР Обозначение 0. Размерность – В. Условие протекания ОВР 0 окислителя > 0 восстановителя
Условие протекания ОВР Обозначение 0. Размерность – В. Условие протекания ОВР 0 окислителя > 0 восстановителя
 Пример: по какой реакции можно восстановить сульфат железа (III) до сульфата железа (II) Na. Cl + Fe 2(SO 4)3 Fe. SO 4 +Cl 2 + Na 2 SO 4 2 Na. I + Fe 2(SO 4)3 2 Fe. SO 4 +I 2 + Na 2 SO 4
Пример: по какой реакции можно восстановить сульфат железа (III) до сульфата железа (II) Na. Cl + Fe 2(SO 4)3 Fe. SO 4 +Cl 2 + Na 2 SO 4 2 Na. I + Fe 2(SO 4)3 2 Fe. SO 4 +I 2 + Na 2 SO 4
 Решение 1. Составим уравнения электронного баланса и запишем табличные значения потенциалов для каждой полуреакции 2 Na. Cl + Fe 2(SO 4)3 2 Fe. SO 4 +Cl 2 + Na 2 SO 4 Восстанови- Cl e 1/2 Cl 2 тель Fe 3+ +e Fe 2+ окислитель в 0=1, 36 В ок 0=0, 77 В Условие протекания ОВР не выполняется, т. к. в 0 > ок 0.
Решение 1. Составим уравнения электронного баланса и запишем табличные значения потенциалов для каждой полуреакции 2 Na. Cl + Fe 2(SO 4)3 2 Fe. SO 4 +Cl 2 + Na 2 SO 4 Восстанови- Cl e 1/2 Cl 2 тель Fe 3+ +e Fe 2+ окислитель в 0=1, 36 В ок 0=0, 77 В Условие протекания ОВР не выполняется, т. к. в 0 > ок 0.
 Продолжение Аналогично для второй реакции 2 Na. I + Fe 2(SO 4)3 2 Fe. SO 4 +I 2 + Na 2 SO 4 Восстанови- I e 1/2 I 20 тель окислитель Fe 3+ +e Fe 2+ в 0=0, 54 В ок 0=0, 77 В Условие протекания ОВР выполняется, т. к. ок 0 > в 0. Вывод: при стандартных условиях сульфат железа (III) можно восстановить до сульфата железа (II) иодидом натрия.
Продолжение Аналогично для второй реакции 2 Na. I + Fe 2(SO 4)3 2 Fe. SO 4 +I 2 + Na 2 SO 4 Восстанови- I e 1/2 I 20 тель окислитель Fe 3+ +e Fe 2+ в 0=0, 54 В ок 0=0, 77 В Условие протекания ОВР выполняется, т. к. ок 0 > в 0. Вывод: при стандартных условиях сульфат железа (III) можно восстановить до сульфата железа (II) иодидом натрия.
 Электродные потенциалы металлов Электродный потенциал металла– это разность потенциалов между металлом и раствором, в который он погружен. Рассмотрим процессы происходящие при погружении металлической пластины в воду.
Электродные потенциалы металлов Электродный потенциал металла– это разность потенциалов между металлом и раствором, в который он погружен. Рассмотрим процессы происходящие при погружении металлической пластины в воду.
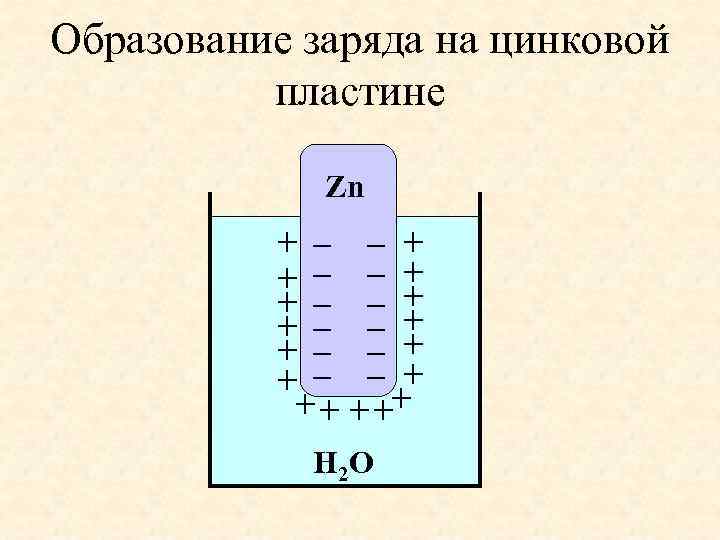 Образование заряда на цинковой пластине Zn + – – + + – – + + + – –+ + + ++ Н 2 О
Образование заряда на цинковой пластине Zn + – – + + – – + + + – –+ + + ++ Н 2 О
 Продолжение При погружении металла в воду, полярные молекулы воды гидратируют ионы металла. Ионы металла переходят в раствор, а его поверхность заряжается отрицательно. Слой воды около поверхности металла заряжается положительно. Устанавливается равновесие: Me + m. H 2 O Me(H 2 O)n+ + ne пластинка раствор пластинка
Продолжение При погружении металла в воду, полярные молекулы воды гидратируют ионы металла. Ионы металла переходят в раствор, а его поверхность заряжается отрицательно. Слой воды около поверхности металла заряжается положительно. Устанавливается равновесие: Me + m. H 2 O Me(H 2 O)n+ + ne пластинка раствор пластинка
 Стандартный электродный потенциал Абсолютное значение электродного потенциала определить невозможно. Поэтому измеряют относительную величину потенциала в стандартных условиях. Стандартный электродный потенциал металла – потенциал металла измеренный относительно водородного электрода при стандартных условиях ( Р=101, 3 к. Па, Т=298 К, содержание соли в растворе 1 моль/л)
Стандартный электродный потенциал Абсолютное значение электродного потенциала определить невозможно. Поэтому измеряют относительную величину потенциала в стандартных условиях. Стандартный электродный потенциал металла – потенциал металла измеренный относительно водородного электрода при стандартных условиях ( Р=101, 3 к. Па, Т=298 К, содержание соли в растворе 1 моль/л)
 Водородный электрод состоит из рыхлой платиновой пластинки, опущенной в раствор серной кислоты с активной концентрацией ионов водорда 1 моль/л, через который пропускают газообразный водород при Р=101, 3 к. Па, Т=298 К (250 С)
Водородный электрод состоит из рыхлой платиновой пластинки, опущенной в раствор серной кислоты с активной концентрацией ионов водорда 1 моль/л, через который пропускают газообразный водород при Р=101, 3 к. Па, Т=298 К (250 С)
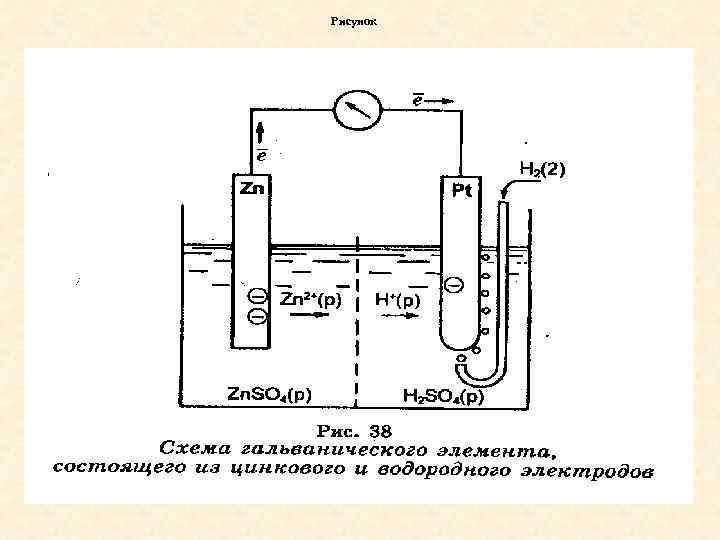 Рисунок
Рисунок
 Ряд напряжений 0 характеризует восстановительную способность металла. Для неактивных металлов 0>0, для активных 0<0. По величине стандартных электродных металлы образуют электрохимичесий ряд напряжений металлов. По ряду напряжений можно определить какие металлы вытесняют водород из растворов кислот, вытесняют другие металлы из растворов их солей.
Ряд напряжений 0 характеризует восстановительную способность металла. Для неактивных металлов 0>0, для активных 0<0. По величине стандартных электродных металлы образуют электрохимичесий ряд напряжений металлов. По ряду напряжений можно определить какие металлы вытесняют водород из растворов кислот, вытесняют другие металлы из растворов их солей.
 Продолжение Каждый левостоящий металл вытесняет правостоящий из раствора его соли. Металлы, стоящие в ряду напряжений до водорода вытесняют его из растворов кислот (кроме азотной и серной концентрированной). Пример. Будут ли реагировать: цинк и раствор сульфата меди; медь и раствор хлорида магния; железо и нитрат серебра.
Продолжение Каждый левостоящий металл вытесняет правостоящий из раствора его соли. Металлы, стоящие в ряду напряжений до водорода вытесняют его из растворов кислот (кроме азотной и серной концентрированной). Пример. Будут ли реагировать: цинк и раствор сульфата меди; медь и раствор хлорида магния; железо и нитрат серебра.
 Гальванический элемент – это устройство, в котром энергия химической реакции превращается в электрическую. Простейший гальванический элемент – элемент Даниэля-Якоби Анод – электрод на котором происходит окисление (более активный металл) Катод – электрод на котором происходит восстановление (менее активный металл)
Гальванический элемент – это устройство, в котром энергия химической реакции превращается в электрическую. Простейший гальванический элемент – элемент Даниэля-Якоби Анод – электрод на котором происходит окисление (более активный металл) Катод – электрод на котором происходит восстановление (менее активный металл)
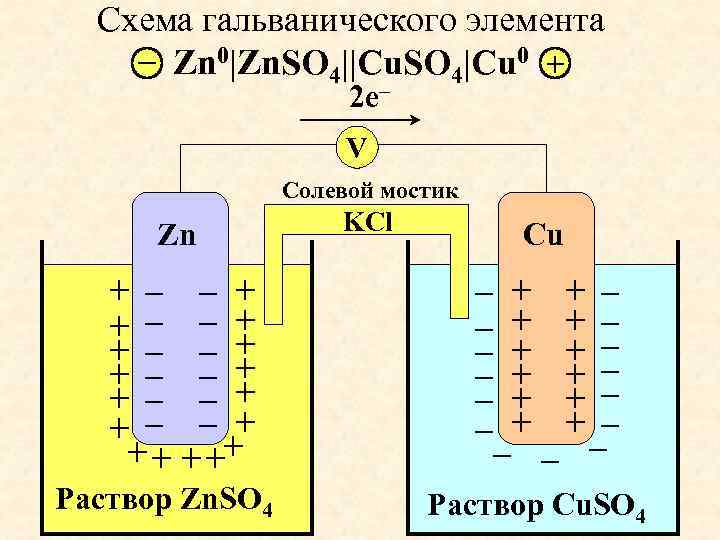 Схема гальванического элемента – Zn 0|Zn. SO 4||Cu. SO 4|Cu 0 + 2 e– V Солевой мостик Zn + – – + + – – + + + – –+ + + ++ Раствор Zn. SO 4 KCl Cu – – – + + + – – – – – Раствор Cu. SO 4
Схема гальванического элемента – Zn 0|Zn. SO 4||Cu. SO 4|Cu 0 + 2 e– V Солевой мостик Zn + – – + + – – + + + – –+ + + ++ Раствор Zn. SO 4 KCl Cu – – – + + + – – – – – Раствор Cu. SO 4
 Процессы на аноде и катоде - Zn 0|Zn. SO 4||Cu. SO 4|Cu 0 + А: Zn 0 – 2 e Zn 2+ 0= 0, 76 окисление K: Cu 2+ + 2 e Cu 0 0 = +0, 34 восстан-ие Zn 0 + Cu 2+ Zn 2+ + Cu 0 Анод заряжен отрицательно, катод положительно
Процессы на аноде и катоде - Zn 0|Zn. SO 4||Cu. SO 4|Cu 0 + А: Zn 0 – 2 e Zn 2+ 0= 0, 76 окисление K: Cu 2+ + 2 e Cu 0 0 = +0, 34 восстан-ие Zn 0 + Cu 2+ Zn 2+ + Cu 0 Анод заряжен отрицательно, катод положительно
 ЭДС Эффективность работы гальванического элемента оценивается величиной электродвижущей силы гальванического элемента. Электродвижущая сила – максимальное напряжение, возникающее при работе гальванического элемента. Обозначение - Е 0. Размерность - В Е 0= 0 К - 0 А Е 0 Cu-Zn= 0, 34 – (-0, 76)=1, 1 В
ЭДС Эффективность работы гальванического элемента оценивается величиной электродвижущей силы гальванического элемента. Электродвижущая сила – максимальное напряжение, возникающее при работе гальванического элемента. Обозначение - Е 0. Размерность - В Е 0= 0 К - 0 А Е 0 Cu-Zn= 0, 34 – (-0, 76)=1, 1 В
 Характеристика элемента по его положению в периодической системе. 1. Положение в п. с. (порядковый номер, период, подгруппа).
Характеристика элемента по его положению в периодической системе. 1. Положение в п. с. (порядковый номер, период, подгруппа).
 ПРОДОЛЖЕНИЕ 2. Характеристика атома элемента: Заряд ядра Z, число протонов Nр, число нейтронов Nn, число электронов Ne. Полная электронная формула. Графическая электронная конфигурация валентных уровней в нормальном и возбужденном состояниях.
ПРОДОЛЖЕНИЕ 2. Характеристика атома элемента: Заряд ядра Z, число протонов Nр, число нейтронов Nn, число электронов Ne. Полная электронная формула. Графическая электронная конфигурация валентных уровней в нормальном и возбужденном состояниях.
 3. Электронное семейство к которому относится элемент, металл или неметалл, формула и характер высшего оксида (основной, амфотерный, кислотный) и соответствующего ему гидрата. Реакции подтверждающие свойства оксида и гидрата.
3. Электронное семейство к которому относится элемент, металл или неметалл, формула и характер высшего оксида (основной, амфотерный, кислотный) и соответствующего ему гидрата. Реакции подтверждающие свойства оксида и гидрата.
 Примеры 1. Дайте характеристику элемента № 56 по положению в п. с. 1)Элемент № 56 – барий 56 Ва. Ва находится в 6 периоде во второй группе главной подгруппы (IIA).
Примеры 1. Дайте характеристику элемента № 56 по положению в п. с. 1)Элемент № 56 – барий 56 Ва. Ва находится в 6 периоде во второй группе главной подгруппы (IIA).
 продолжение 2) Z=+56, A=137 1 p)=56, N(e)=56, N( 1 1 n)=A-N(1 p)=137 -56=81 N( 0 1 Электронная формула: 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 24 d 105 p 6 2 6 s
продолжение 2) Z=+56, A=137 1 p)=56, N(e)=56, N( 1 1 n)=A-N(1 p)=137 -56=81 N( 0 1 Электронная формула: 1 s 22 p 63 s 23 p 64 s 23 d 104 p 65 s 24 d 105 p 6 2 6 s
 Основное состояние: … 6 s 26 р0 В(Ва)=0 В(Ва*)=2 Возбужденное состояние … 6 s 16 р1
Основное состояние: … 6 s 26 р0 В(Ва)=0 В(Ва*)=2 Возбужденное состояние … 6 s 16 р1
 продолжение • 3. Ва – s-элемент, металл, ОЭО=0, 9. • Высший оксид Ва. О – основной. • Гидрат – Ва(ОН)2 -основание • Ва. О+Н 2 О=Ва(ОН)2; Ва. О+СО 2= Ва. СО 3; • Ва. О+2 HCl=Ba. Cl 2+ Н 2 О;
продолжение • 3. Ва – s-элемент, металл, ОЭО=0, 9. • Высший оксид Ва. О – основной. • Гидрат – Ва(ОН)2 -основание • Ва. О+Н 2 О=Ва(ОН)2; Ва. О+СО 2= Ва. СО 3; • Ва. О+2 HCl=Ba. Cl 2+ Н 2 О;
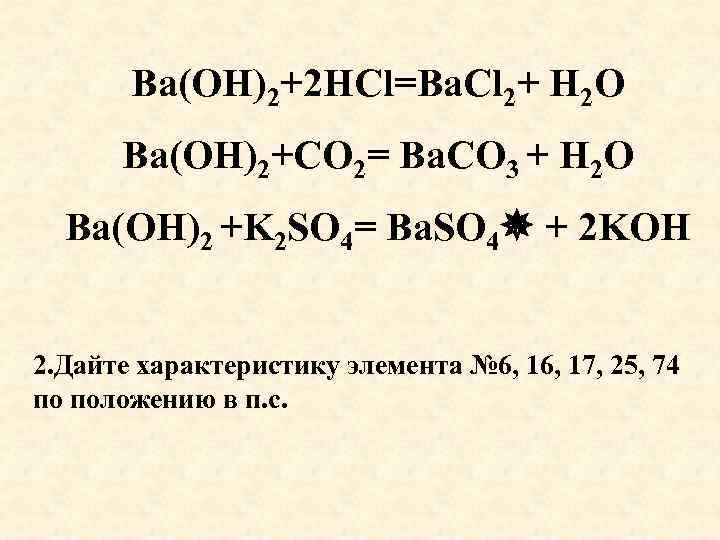 Ba(OH)2+2 HCl=Ba. Cl 2+ Н 2 О Ba(OH)2+CO 2= Ba. CO 3 + Н 2 О Ba(OH)2 +K 2 SO 4= Ba. SO 4 + 2 KOН 2. Дайте характеристику элемента № 6, 17, 25, 74 по положению в п. с.
Ba(OH)2+2 HCl=Ba. Cl 2+ Н 2 О Ba(OH)2+CO 2= Ba. CO 3 + Н 2 О Ba(OH)2 +K 2 SO 4= Ba. SO 4 + 2 KOН 2. Дайте характеристику элемента № 6, 17, 25, 74 по положению в п. с.


