Практика_студентам.ppt
- Количество слайдов: 114

ЛАБОРАТОРНАЯ ДИАГНОСТИКА ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ Практическое занятие

ЛАБОРАТОРНАЯ ДИАГНОСТИКА ИНФЕКЦИОННЫХ ЗАБОЛЕВАНИЙ l Основные группы методов: Прямые методы – определение самого возбудителя. l Косвенные методы – определение реакции организма на инфекцию. l

Прямые методы – определение самого возбудителя l l l Позволяют установить этиологию заболевания. Обнаружение самого возбудителя, получение чистой культуры возбудителя, выявление антигенов, нуклеиновых кислот

Косвенные методы l l l определение реакции организма на инфекцию. Позволяют установить факт контакта с инфекционным агентом. Антитела, б/х маркеры, лейкоциты в общем мазке и т. п. )

Методы специфической диагностики l Микроскопические l Культуральные l Иммунологические l Молекулярно-биологические

МИКРОСКОПИЧЕСКИЕ МЕТОДЫ

Микроскопия (лат. μΙκροσ — мелкий, маленький и σκοποσ — вижу) — изучение объектов с использованием микроскопа. от 0, 2 до 0, 02 х10(-5) мм (с увеличением от нескольких десятков до сотен тысяч раз) l Оптическая (световая) микроскопия l Электронная микроскопия l Рентгеновская микроскопия Микроскопия – прямой метод диагностики!

разновидности микроскопической диагностики l Витальная (прижизненная) l Микроскопия окрашенных препаратов l Микроскопия в темном поле l Флюоресцентная (люминесцентная)

Микроскопические методы в диагностике ИППП Treponema pallidum Сlamidia trachomatis Neiseria gonorrhoeae Trichomonas vaginalis Нативные препараты (в темном поле) Mycoplasma/ Ureaplasma HSV 1, 2 Не используются Окрашенные препараты по Романовскому-Гимзе; прямая иммунофлюоресценция (ПИФ) Окрашенные препараты метиленовым синим, по Граму Нативные препараты, окрашенные препараты (метиленовым синим, по Граму), фазово-контрастная и люминисцентная микроскопия Не используются
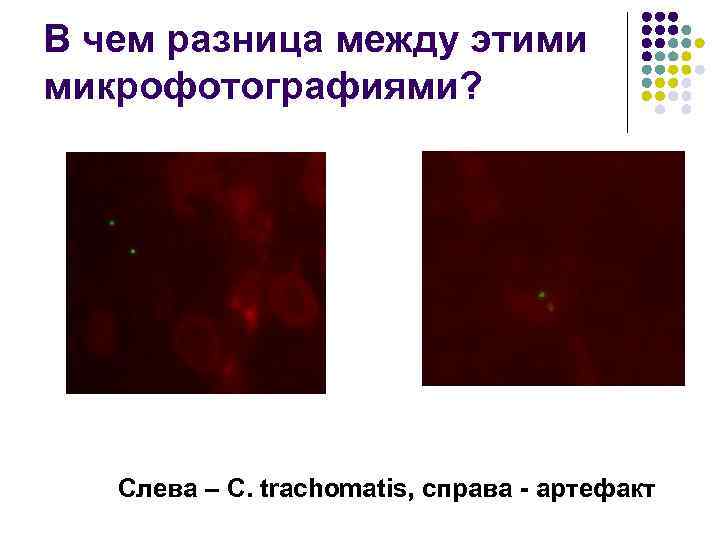
В чем разница между этими микрофотографиями? Слева – C. trachomatis, справа - артефакт
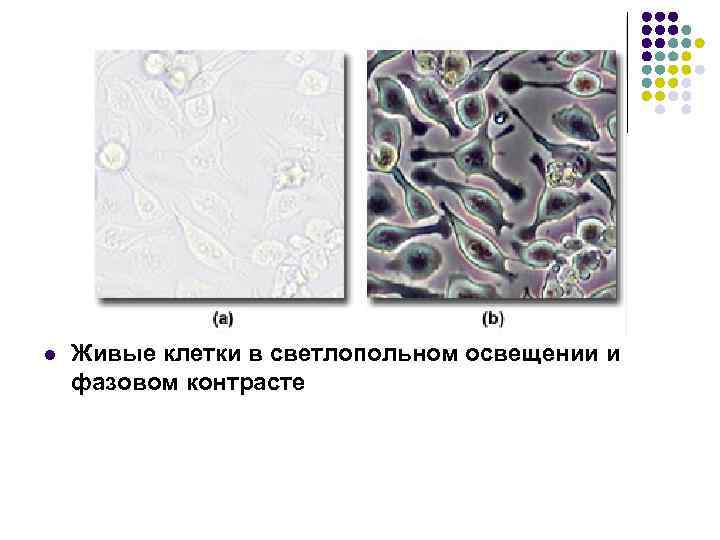
l Живые клетки в светлопольном освещении и фазовом контрасте

Ограничения микроскопии Невысокая чувствительность (от 36% до 82%) l Интерпретации результатов субъективна, зависит от опыта специалиста, качества мазка, соблюдения условий забора материала l Трудности автоматизации l Определяется не вид, а морфотип (например, не гонококки, а внутриклеточные Грам(-) диплококки и т. п. ) l А какие достоинства у микроскопии?
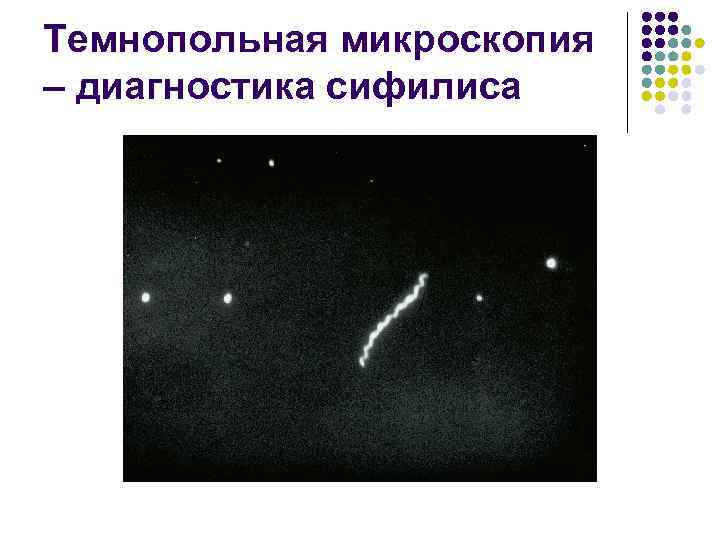
Темнопольная микроскопия – диагностика сифилиса
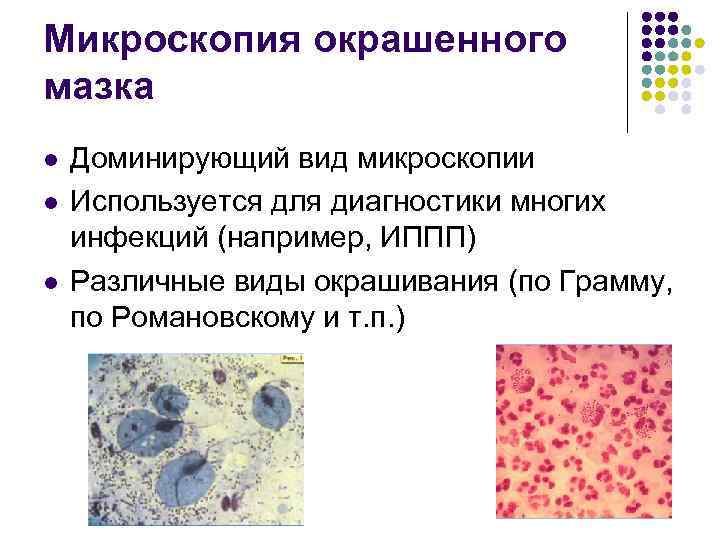
Микроскопия окрашенного мазка l l l Доминирующий вид микроскопии Используется для диагностики многих инфекций (например, ИППП) Различные виды окрашивания (по Грамму, по Романовскому и т. п. )
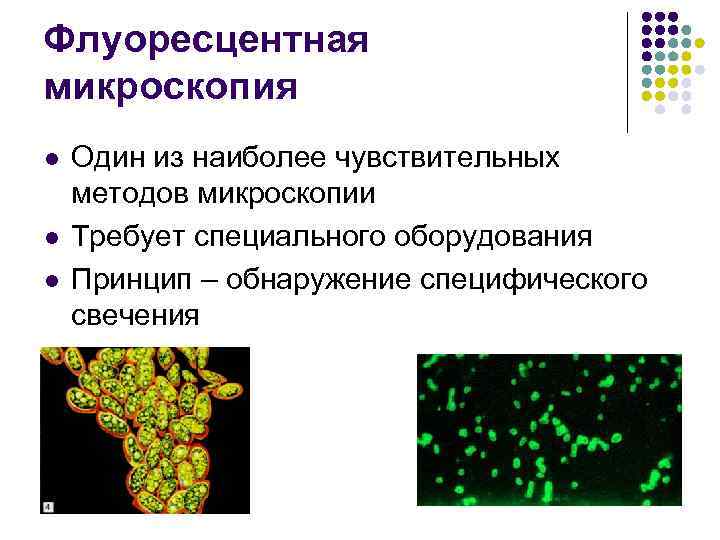
Флуоресцентная микроскопия l l l Один из наиболее чувствительных методов микроскопии Требует специального оборудования Принцип – обнаружение специфического свечения

l ТЕСТЫ 1.

1. Световая микроскопия включает следующие разновидности: фазово-контрастную микроскопию; 2) электронную микроскопию; 3) темнопольную микроскопию; 4) микроскопию в затемнённом поле; 5) эммерсионную микроскопию. Выберите одну комбинацию, в которой учтены все правильные ответы: 1) а) 1, 3, 4, 5 б) 1, 2, 4, 5 в) 2, 3, 4, 5 г) 2, 3, 4 д) 3, 4, 5

1. Световая микроскопия включает следующие разновидности: фазово-контрастную микроскопию; 2) электронную микроскопию; 3) темнопольную микроскопию; 4) микроскопию в затемнённом поле; 5) иммерсионную микроскопию. Выберите одну комбинацию, в которой учтены все правильные ответы: 1) а) 1, 3, 4, 5 б) 1, 2, 4, 5 в) 2, 3, 4, 5 г) 2, 3, 4 д) 3, 4, 5

2. Микроскоп нужен а) для проведения микроскопического анализа б) забивания гвоздей в) рассматривания микробов г) колки орехов

2. Микроскоп нужен а) для проведения микроскопического анализа б) забивания гвоздей в) рассматривания микробов г) колки орехов

3. Темнопольная микроскопия применяется для изучения: а) кишечной палочки б) бледной трепонемы в) стафилококка г) хламидий д) риккетсий

3. Темнопольная микроскопия применяется для изучения: а) кишечной палочки б) бледной трепонемы в) стафилококка г) хламидий д) риккетсий

4. Предел разрешения светового микроскопа: а) 200 мкм б) 0, 01 мкм в) 0, 2 мкм г) 1 -2 мкм д) 10 мкм

4. Предел разрешения светового микроскопа: а) 200 мкм б) 0, 01 мкм в) 0, 2 мкм г) 1 -2 мкм д) 10 мкм

5. В микроскоп смотрят а) глазами б) глазами с увеличительными стеклами в) пальцем г) глазами в очках синего цвета д) не знаю

5. В микроскоп смотрят а) глазами б) глазами с увеличительными стеклами в) пальцем г) глазами в очках синего цвета д) не знаю

6. Достоинства микроскопического метода: а) возможность ускоренной диагностики б) простота и доступность метода в) при некоторых заболеваниях имеет самостоятельное диагностическое значение г) позволяет выявить клинически значимое количество условно-патогенных микроорганизмов д) все вышеперечисленное

6. Достоинства микроскопического метода: а) возможность ускоренной диагностики б) простота и доступность метода в) при некоторых заболеваниях имеет самостоятельное диагностическое значение г) позволяет выявить клинически значимое количество условно-патогенных микроорганизмов д) все вышеперечисленное

7. К числу недостатков микроскопического метода диагностики инфекционных заболеваний относится все, к р о м е: а) использование в ограниченных случаях б)возможность определения только морфотинкториальных свойств микроорганизмов в) зависимость результата от качества микропрепарата г) зависимость результата от исследуемого материала д) простота и доступность метода

8. Тип микроскопии нативных препаратов: а) темнопольная б) электронная в) сканирующая г) невооруженным глазом

8. Тип микроскопии нативных препаратов: а) темнопольная б) электронная в) сканирующая г) невооруженным глазом

9. Микроскопический метод информативен при диагностике: а) дизентерии б) коклюша в) сифилиса г) краснухи д) гонореи

9. Микроскопический метод информативен при диагностике: а) дизентерии б) коклюша в) сифилиса г) краснухи д) гонореи

Культуральный метод заключается в посеве исследуемого материала -на искусственные питательные среды, -культуры клеток или куриные эмбрионы с целью выделения и идентификации чистой культуры возбудителя или возбудителей. Культивирование – прямой метод диагностики.

Культивирование – прямой метод диагностики. Окрашенная культура клеток эпителия На фото кератин (красный) и ДНК (зеленая)

культуральный метод получил название: - в бактериологии бактериологического, - в микологии - микологического, - в протозоологии - протозоологического, -в вирусологии - вирусологического

Принципы культивирования Бактерии/грибы - культивируются на питательных средах Обычные (простые) среды пригодны для культивирования многих видов патогенных и непатогенных бактерий. Дифференциальные среды позволяют различать бактерии разных видов и родов по их культуральным и биохимическим свойствам. Элективные (избирательные) среды и среды обогащения, благоприятствующие размножению бактерий и подавляющие рост других микробов. Специальные среды — наиболее оптимальные для выращивания бактерий, не размножающихся на простых средах.

Принципы культивирования в вирусологии Культуры вирусов выращивают на культурах клеток млекопитающих. Для культивирования вирусов используются живые организмы целиком Методы исследования, применяемые в вирусологии отличаются значительной сложностью, что связано с внутриклеточным паразитизмом вирусов и их Заражение куриных эмбрионов малыми размерами.

Культивирование вирусов путём заражения лабораторных животных Экспериментальные модели для некоторых вирусов Наименование вируса Экспериментальная модель Вирус бешенства Мыши, кролики Вирус Коксаки Мыши-сосунки Вирус полиомиелита Обезьяны, крысы Вирус гриппа Мыши, хорьки Вирус клещевого энцефалита Мыши
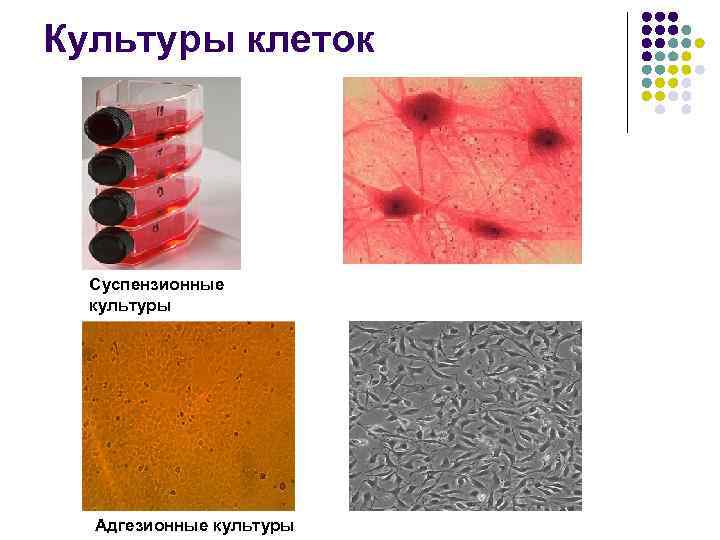
Культуры клеток Суспензионные культуры Адгезионные культуры

Оценка антибиотикорезистентности/ устойчивости к противовирусным препаратам В бактериологии: Метод стандартных дисков Диффузионный метод (Е-тест) Метод серийных разведений В вирусологии: Метод культивирования в планшетах Метод подавления ЦПД- цитопатического действия.
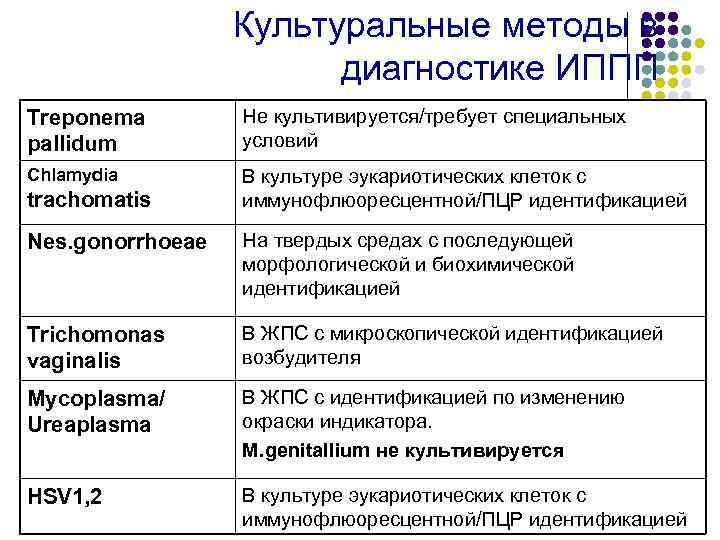
Культуральные методы в диагностике ИППП Treponema pallidum Не культивируется/требует специальных условий Chlamydia В культуре эукариотических клеток с иммунофлюоресцентной/ПЦР идентификацией trachomatis Nes. gonorrhoeae На твердых средах с последующей морфологической и биохимической идентификацией Trichomonas vaginalis В ЖПС с микроскопической идентификацией возбудителя Mycoplasma/ Ureaplasma В ЖПС с идентификацией по изменению окраски индикатора. M. genitallium не культивируется HSV 1, 2 В культуре эукариотических клеток с иммунофлюоресцентной/ПЦР идентификацией

Культуральный метод ПРЕИМУЩЕСТВА высокая точность низкая стоимость широкий спектр микроорганизмов, которые могут быть выявлены возможность автоматизации определение чувствительности к антибиотикам НЕДОСТАТКИ длительность выполнения (7 -10 дней и более) необходим живой организм необходимость присутствия определенной (заражающей) концентрации, микроорганизмов, т. е. ограниченная чувствительность метода Необходимы методы идентификации сложности с исходной количественной оценкой Культивировать можно около 10% микроорганизмов!

Когда эффективен культуральный метод? l l l При острой инфекции (много возбудителя, близость к входным воротам инфекции) Для легкокультивируемых микроорганизмов (M. hominis vs. M. genitalium) Доступность лаборатории – ограничение метода (потеря жизнеспособности м/организмами при транспортировке)

l ТЕСТЫ 2.

10 f Среды, применяемые для выделения и выращивания определенных групп микроорганизмов, которые на обычных средах плохо или совсем не растут: а) обычного назначения б) селективные в) специальные г) дифференциально-диагностические д) элективные

10 f Среды, применяемые для выделения и выращивания определенных групп микроорганизмов, которые на обычных средах плохо или совсем не растут: а) обычного назначения б) селективные в) специальные г) дифференциально диагностические д) элективные Элективные среды (от франц. électif — избранный) специальные питательные среды, создающие более благоприятные условия для роста определённого вида микроорганизмов

10. Вирусов выращивают на культурах: а) клеток млекопитающих б) клеток растений в) клеток бактерий г) все перечисленное верно

10. Вирусов выращивают на культурах: а) клеток млекопитающих б) клеток растений в) клеток бактерий г) все перечисленное верно

11. Инокулят – это: а) смешанная культура б) продукт биотехнологического производства в) посевной материал г) питательная среда д) культуральная жидкость Инокулят (Inoculum) вещество, используемое для инокуляции. (от лат. inoculatio - прививка), введение живых микроорганизмов, инфицированного материала, сыворотки или других веществ в ткани растений, животных или человека (а также в питательные среды).

12. При оценке чувствительности к антибиотику in vitro способом серийных разведений в жидкой среде определяют: а) интенсивность роста культуры б) продукцию пигмента в) диаметр зоны подавления роста г) генетические маркеры резистентности д) верно «в» и «г»

12. При оценке чувствительности к антибиотику in vitro способом серийных разведений в жидкой среде определяют: а) интенсивность роста культуры б) продукцию пигмента в) диаметр зоны подавления роста г) генетические маркеры резистентности д) верно «в» и «г»

13. Какой из методов не применяется в диагностике вирусных инфекций: а) серологический б) вирусологический в) заражение лабораторных животных г) бактериологический д) вирусоскопический

13. Какой из методов не применяется в диагностике вирусных инфекций: а) серологический б) вирусологический в) заражение лабораторных животных г) бактериологический д) вирусоскопический l При вирусоскопическом методе в исследуемом материале обнаруживают с помощью электронной микроскопии вирионы

Иммунологические методы l l l Основа – взаимодействие Аг-Ат Определение Аг – прямой метод диагностики возбудителя Определение Ат – определение реактивности (ответа) иммунной системы организма на инфекцию

Иммунологические методы исследования l методы исследования, основанные на специфическом взаимодействии антигенов и антител для диагностики инфекционных и паразитарных болезней, определения групп крови, тканевых и опухолевых антигенов, видовой принадлежности белка, распознавания аллергии и аутоиммунных болезней, беременности, гормональных нарушений. Они включают серологические исследования, или серологические реакции, к которым относят обычно реакции прямого воздействия антигенов и антител сыворотки крови in vitro.
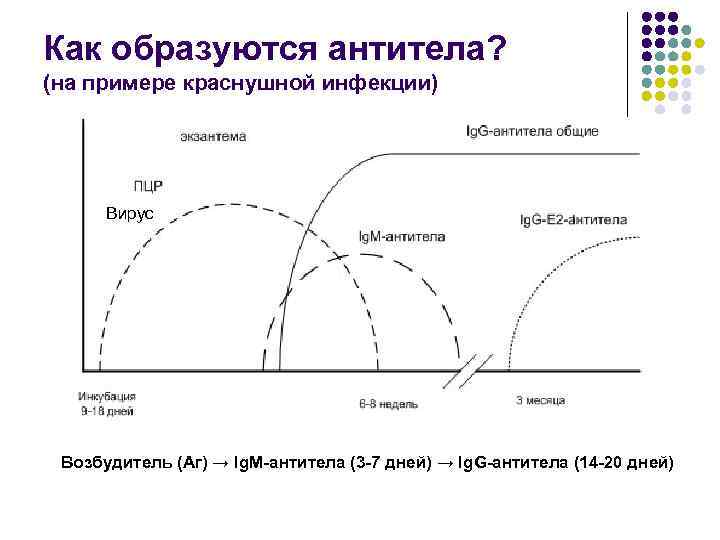
Как образуются антитела? (на примере краснушной инфекции) Вирус Возбудитель (Аг) → Ig. M-антитела (3 -7 дней) → Ig. G-антитела (14 -20 дней)

Чаще всего применяются следующие иммунологические методы: l l Методы агглютинации (РА, РПГА, РНГА, РТГА) Реакции связывания комплемента (РСК) Реакции твердофазного иммуноферментного анализа Иммунный блоттинг
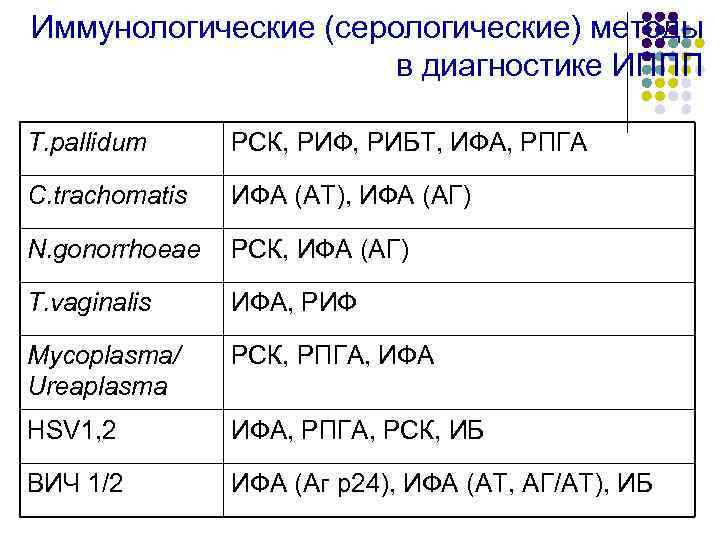
Иммунологические (серологические) методы в диагностике ИППП T. pallidum РСК, РИФ, РИБТ, ИФА, РПГА С. trachomatis ИФА (АТ), ИФА (АГ) N. gonorrhoeae РСК, ИФА (АГ) T. vaginalis ИФА, РИФ Mycoplasma/ Ureaplasma РСК, РПГА, ИФА HSV 1, 2 ИФА, РПГА, РСК, ИБ ВИЧ 1/2 ИФА (Аг р24), ИФА (АТ, АГ/АТ), ИБ
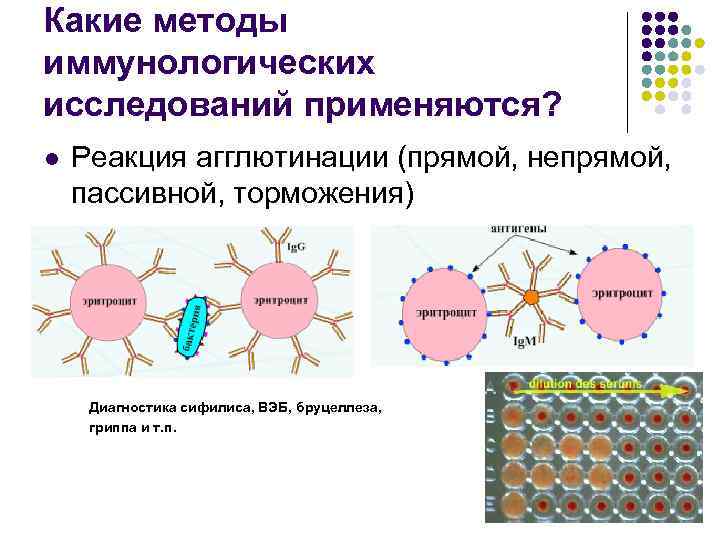
Какие методы иммунологических исследований применяются? l Реакция агглютинации (прямой, непрямой, пассивной, торможения) Диагностика сифилиса, ВЭБ, бруцеллеза, гриппа и т. п.

Что выявляет иммуноферментный анализ (ИФА)? l l Выявление Антигенов и Антител (поликлональных и моноклональных) Раздельное определение Ig. M и Ig. G антител (установление стадии заболевания) Количественное определение Ig. G антител (вакцинальный скрининг, динамика сероконверсии и т. п. ) Определение давности инфицирования
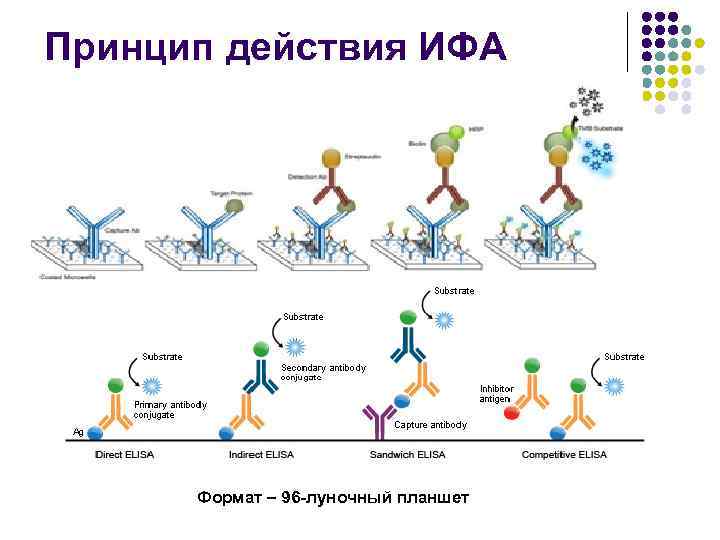
Принцип действия ИФА Формат – 96 -луночный планшет

Иммунный блот – подтверждение диагноза Принцип – раздельное определение антител к различным белкам возбудителя. Наиболее специфический метод иммунологической диагностики, используется для подтверждения диагноза при многих инфекционных заболеваниях (ВИЧ, ВГС, ВПГ, ЦМВИ, ЭБВИ и т. п. ) Недостатки: дорого, трудоемко, трудно автоматизируемо (особенно учет результатов)

ИФА – высокопроизводительный скрининг инфекций l l Развитие ИФА-диагностики идет по пути автоматизации и повышения чувствительности (ИФА→ИХЛА). Два направления – открытые и закрытые платформы

Преимущества и недостатки ИФА Преимущества Недостатки Аппаратный учет Серологическое окно Высокая производительность Неинформативность для целого ряда хронических и латентных инфекций Возможность автоматизации Ложноположительные результаты Ig. M Невысокая стоимость Ложноположительные результаты Ig. G Качественный и количественный формат Возможность алгоритмизации анализа (скрининг и подтверждение)

l ТЕСТЫ 3.

14. Иммунологическая диагностика основана на принципе: 1. Образования антител 2. Комплементарности молекул субстрата и фермента 3. Взаимодействии антиген-антитело 4. Все ответы правильные

14. Иммунологическая диагностика основана на принципе: 1. Образования антител 2. Комплементарности молекул субстрата и фермента 3. Взаимодействии антиген-антитело 4. Все ответы правильные

15. При инфекционном процессе сначала появляется: 1. 2. 3. 4. Ig. M антитела Ig. G и Ig. M антитела Антиген Комплекс антиген-антитело

15. При инфекционном процессе сначала появляется: 1. 2. 3. 4. Ig. M антитела Ig. G и Ig. M антитела Антиген Комплекс антиген-антитело

16. Серологическая диагностика это: 1. 2. 3. 4. Косвенный метод исследования Прямой метод исследования Количественный метод исследования Как прямой, так и косвенный метод исследования

17. Преимуществом иммунологических методов диагностики инфекционных заболеваний является: 1. Возможность автоматизации 2. Качественный или количественный вариант анализа 3. Возможность установить давность инфицирования 4. Невысокая стоимость 5. Все вышеперечисленное

17. Преимуществом иммунологических методов диагностики инфекционных заболеваний является: 1. Возможность автоматизации 2. Качественный или количественный вариант анализа 3. Возможность установить давность инфицирования 4. Невысокая стоимость 5. Все вышеперечисленное

19. Иммунный блот – это метод обнаружения: 1. 2. 3. 4. Антигенов возбудителя Антител к разным белкам возбудителя Антител к белкам и нуклеиновым кислотам возбудителя Доказательство резистентности к лекарственным средствам

19. Иммунный блот – это метод обнаружения: 1. 2. 3. 4. Антигенов возбудителя Антител к разным белкам возбудителя Антител к белкам и нуклеиновым кислотам возбудителя Доказательство резистентности к лекарственным средствам

Молекулярно-биологические методы Наиболее чувствительные и специфические методы диагностики Развиваются с 70 -х – 80 -х гг ХХ века Прорыв – внедрение метода ПЦР в клиническую лабораторную диагностику (1990 г – первый набор для судмедэкспертизы ДНК человека; 1992 г – ПЦР ДНК C. Trachomatis и ПЦР ДНК ВИЧ-1; 1993 г. – ПЦР РНК ВГС)

Центральная догма молекулярной биологии – основа диагностики • ДНК → ДНК (репликация), ДНК → РНК (транскрипция), РНК → белок (трансляция). • РНК → ДНК (обратная транскрипция). • РНК → РНК (репликация РНК).

Генетический материал бактерий и грибов представлен: Бактерии Грибы (от 2 до 28) + B-хромосомами (число непостоянно) Митохондриальными кольцевыми молекулами 3.
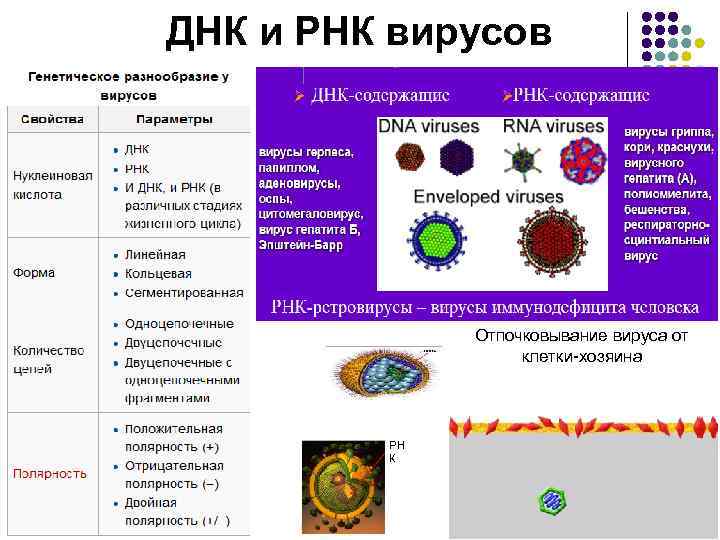
ДНК и РНК вирусов Отпочковывание вируса от клетки-хозяина РН К

Принципы поиска инфекционного агента Усиление сигнала от уникальной мишени Накопление самой мишени 1. 2. 3. 1. Гибридизация нуклеиновых кислот. 2. Изотермическая амплификация нуклеиновых кислот. 3. Метод разветвленных цепей ДНК Полимеразная цепная реакция. Лигазная цепная реакция. Транскрипционная амплификация NASBA в реальном времени.
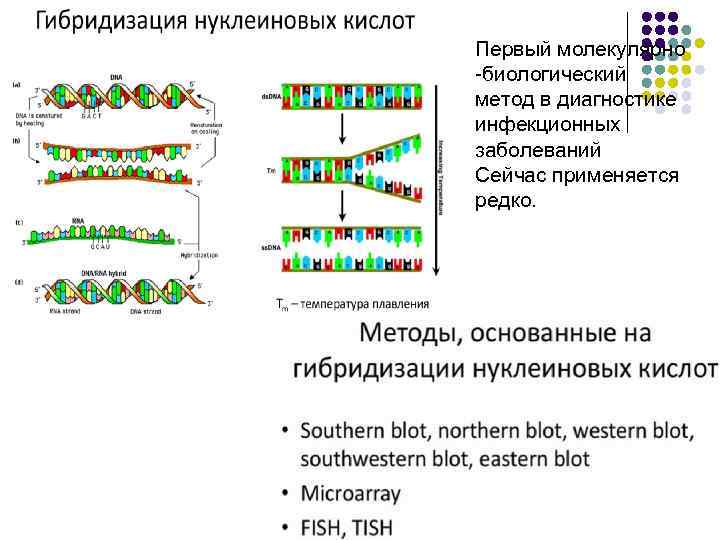
Первый молекулярно -биологический метод в диагностике инфекционных заболеваний Сейчас применяется редко.
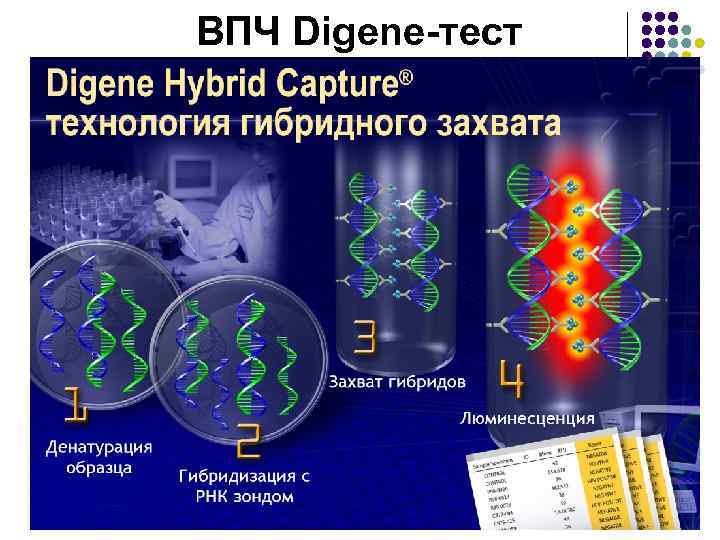
ВПЧ Digene-тест
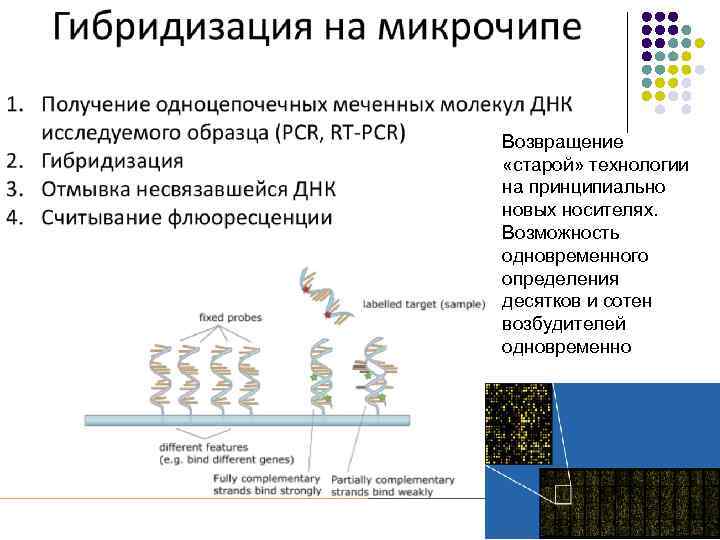
Возвращение «старой» технологии на принципиально новых носителях. Возможность одновременного определения десятков и сотен возбудителей одновременно
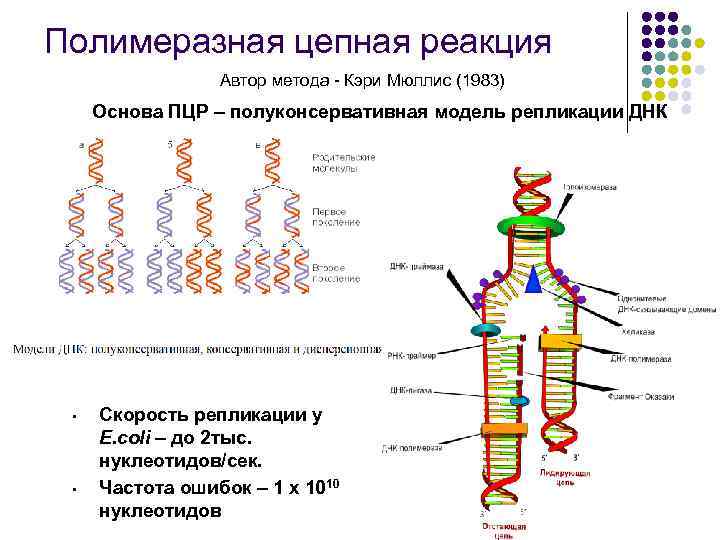
Полимеразная цепная реакция Автор метода - Кэри Мюллис (1983) Основа ПЦР – полуконсервативная модель репликации ДНК • • Скорость репликации у E. coli – до 2 тыс. нуклеотидов/сек. Частота ошибок – 1 х 1010 нуклеотидов


Виды ПЦР-анализа. l Качественный анализ (есть или нет) – установление этиологии l Количественный анализ (сколько возбудителя? ) – прогноз течения инфекции, назначение терапии, сопровождение лечения l Генотипирование (какой вариант возбудителя? ) – определение геноварианта возбудителя, определение резистентности, установление эпидемиологических связей

ПЦР для диагностики. При бессимптомном течении инфекционного процесса, вызванного условнопатогенными и безусловнопатогенными микроорганизмами Chlamydia trachomatis Mycoplasma hominis Mycoplasma genitalium Ureaplasma parvum Ureaplasma urealyticum Neisseria gonorrhoeae HPV Trichomonas vaginalis Gardnerella vaginalis Candida albicans Herpes simplex virus I, II Cytomegalovirus При диагностике особо опасных, социально-значимых инфекций и т. п. Вирус гепатита А Вирус гепатита В Вирус гепатита С Вирус гепатита D ВИЧ ………. Всего более 250 микроорганизмов, в т. ч. некультивируемые

Качественный ПЦР ДНК/РНК возбудителей – самый ранний способ диагностики инфекций l l Чувствительность ПЦР выше чувствительности ИФА АГ в 100 -1000 раз ПЦР раньше всех методов выявляет возбудителя (например РНК ВГС можно выявить на 10 -12 день после инфицирования, Cor. Аг ВГС – 35 -37 день, ВГС АТ – 45 -50 день)
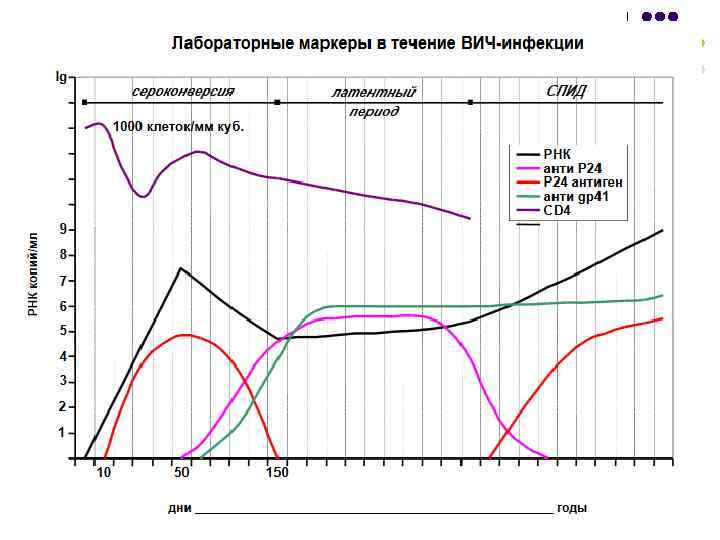
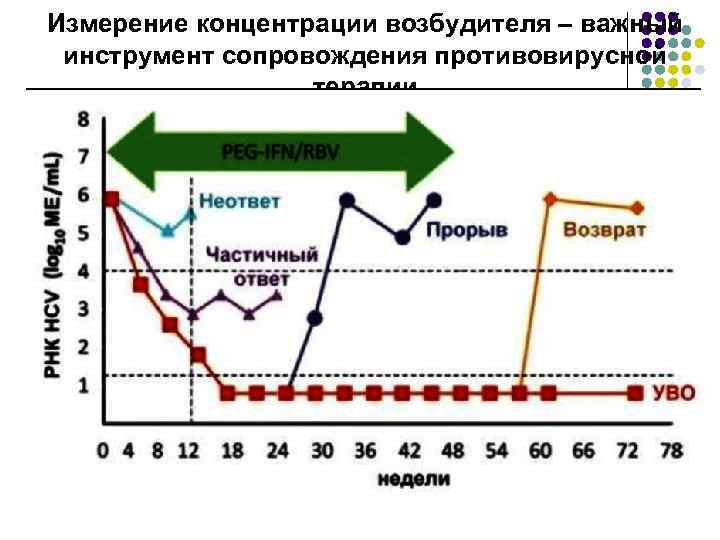
Измерение концентрации возбудителя – важный инструмент сопровождения противовирусной терапии

Количественная оценка – предсказатель прогноза течения заболевания
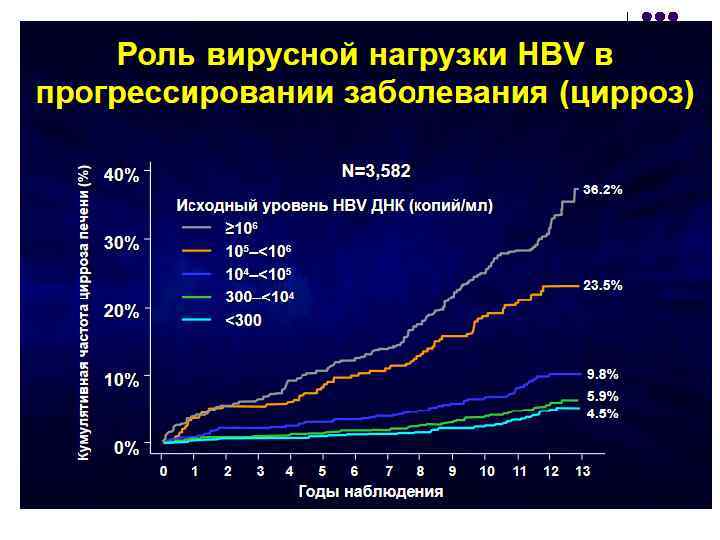
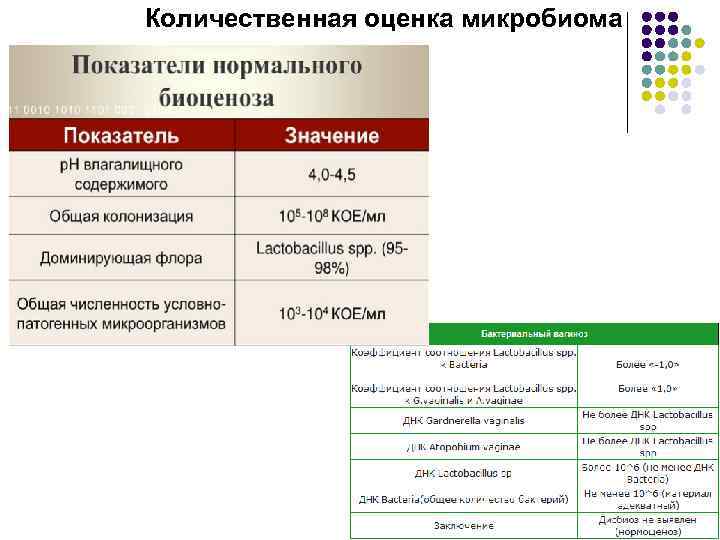
Количественная оценка микробиома
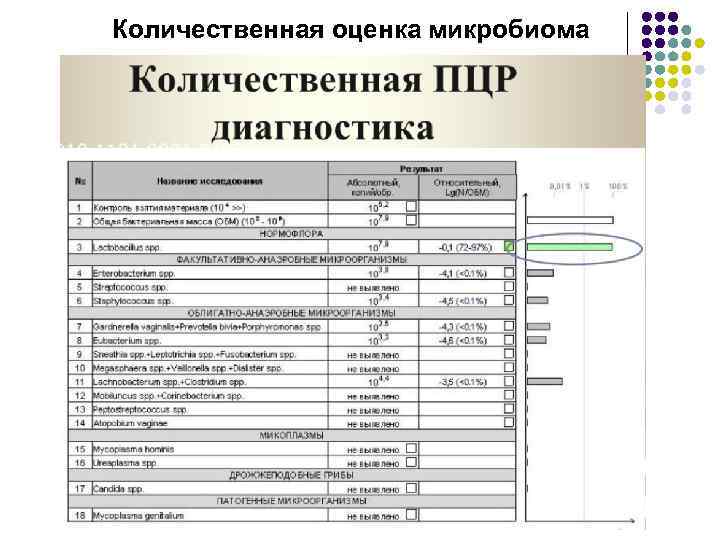
Количественная оценка микробиома
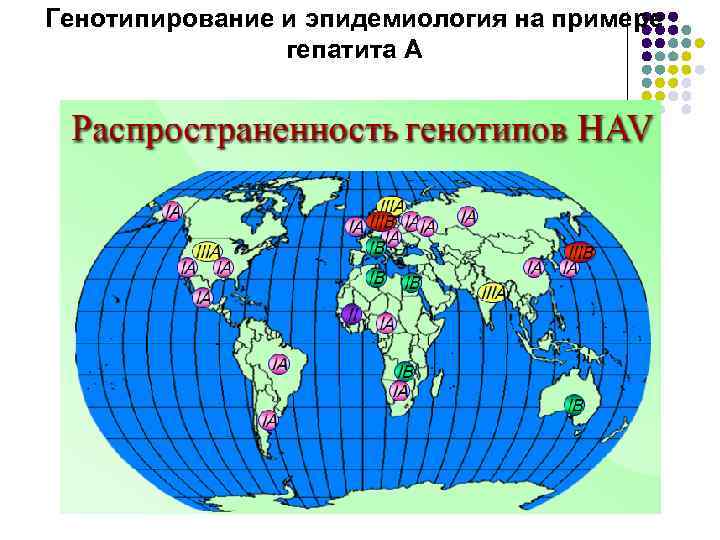
Генотипирование и эпидемиология на примере гепатита А
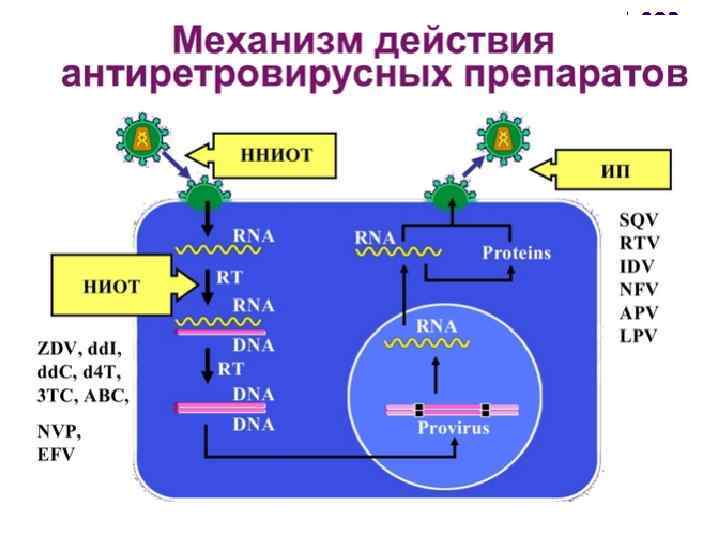
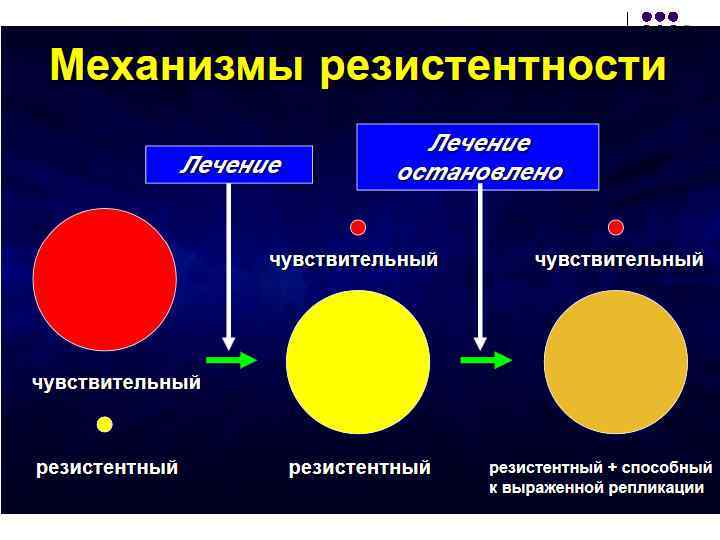


РЕЗИСТЕНТНОСТЬ К АНТИРЕТРОВИРУСНЫМ ПРЕПАРАТАМ В ТЕРАПИИ ВИЧ-ИНФЕКЦИИ

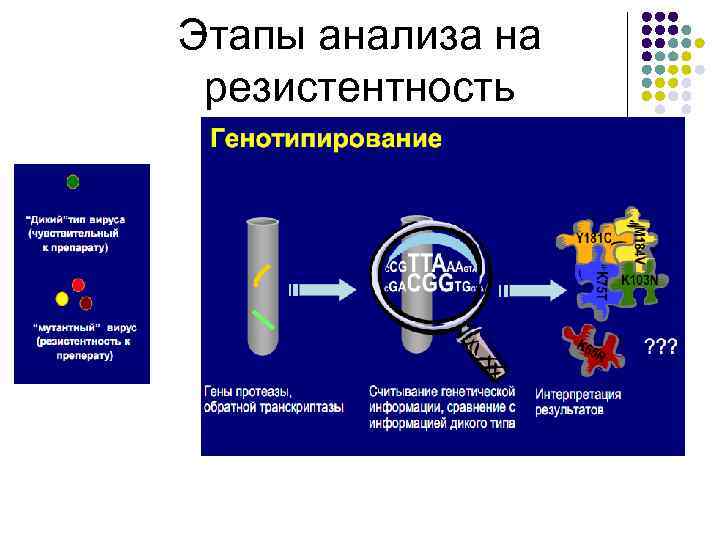
Этапы анализа на резистентность
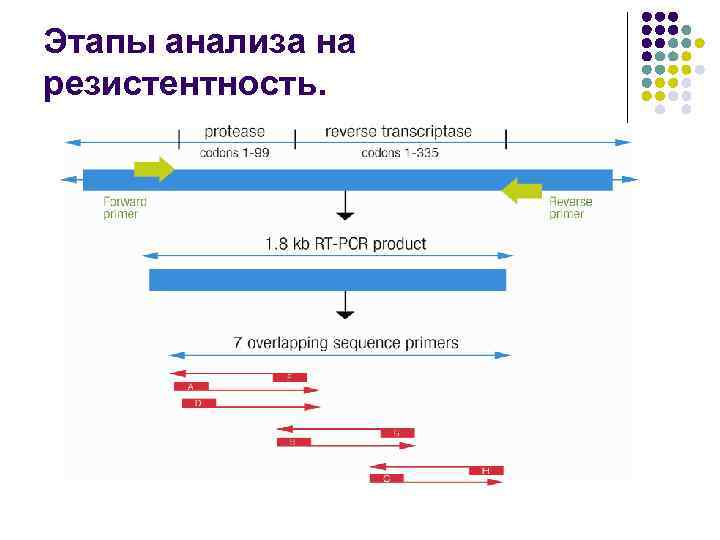
Этапы анализа на резистентность.

Этапы анализа на резистентность 1. Пробоподготовка(Выделение РНК ВИЧ). Использование коммерческих тест - систем ФГУН» Центральный НИИ Эпидемиологии» Роспотребнадзора «Ампли. Сенс® HIV-Resist-Seq» и Viro. Seq. TM HIV-1. 2. 3. 4. 5. 6. 7. 8. 9. Обратная транскрипция и полимеразная цепная реакция Очистка ПЦР-продукта Подсчет количества ДНК Очищенный ПЦР-продукт анализируют методом электрофореза в агарозном геле Циклическое секвенирование Очистка продуктов реакции секвенирования Автоматическая детекция продуктов Интерпретация результатов

Некоторые мутации, ассоциированные с резистентностью

Преимущества метода ПЦР l l l Универсальность (все микроорганизмы содержат РНК или ДНК) Высокая специфичность (можно определить не только вид, но даже штамм) Высокая чувствительность (одна клетка в пробе) Возможность качественной и количественной оценки Минимальный объем биоматериала (множество возбудителей из одной пробы) Скорость получения результатов (в течение 1 рабочего дня)

Недостатки метода ПЦР l l l Высокие требования к лаборатории и квалификации персонала Амплификация ДНК живого и погибшего возбудителя Возможность подтверждения результатов только методом с такой же чувствительностью и специфичностью (другой МАНК)

l ТЕСТЫ 3

19. Определите последовательность этапов полимеразной цепной реакции: 1. Получение и очистка ДНК 2. Амплификация ДНК (увеличение количества) 3. Денатурация нагреванием (разделение на 2 цепочки) 4. Добавление в раствор ДНК-полимеразы 5. Отжиг (добавление искусственных специфических олигопраймеров)

20. Какие возбудители, выявляемые методом ПЦР, могут передаваться при трансфузии крови и ее компонентов: . вирусы гепатитов А, В, Е 2. вирусы гепатитов А и Е 3. вирусы гепатитов В, С, Д 4. вирусы гепатитов В и Д 5. вирусы гепатитов А, В, С, Д, Е 1

21. Какой метод используется для скрининговой лабораторной диагностики ВИЧ-инфекции: 1. иммуноблотинг 2. ИФА 3. ПЦР 4. реакцию нейтрализации 5. РСК

22. Реакции, используемые для видовой идентификации вирусов: 1. Реакция гемадсорбции 2. ПЦР 3. РНГА 4. ИФА

23. Реакции, используемые для обнаружения противовирусных антител: . ИФА 2. Реакция гемагглютинации 3. Реакция биологической нейтрализации 4. ПЦР 1

24. Молекулярно-биологические методы позволяют идентифицировать: 1. 2. 3. 4. Культивируемые организмы Некультивируемые организмы Труднокультивируемые организмы Все перечисленное верно

Практика_студентам.ppt