ПАТОФИЗИОЛОГИЯ КИСЛОТНО-ОСНОВНОГО СОСТОЯНИЯ.ppt
- Количество слайдов: 93

Кустодиев Б. М. Зима 1916 год.

Вся природа стремится к самосохранению. (Марк Туллий Цицерон (лат. Marcus Tullius Cicerо) (3 января 106 до н. э. , Арпинум — 7 декабря 43 до н. э. , Формиа) Древнеримский политик и философ, блестящий оратор ) Немного истории С целью ослабления позиции Антония, он произнес 14 направленных против него речей, Цицерон был убит при попытке к бегству по приказу Антониа. Когда Цицерон заметил догоняющих его убийц, он приказал рабам, несущим его: «Поставьте тут же паланкин» , а потом, высунув голову из-за занавеси, подставил шею под нож убийцы. Его отрубленные голова и правая рука были доставлены Антонию и затем помещены на ораторской трибуне форума


ПАТОФИЗИОЛОГИЯ КИСЛОТНООСНОВНОГО СОСТОЯНИЯ

Определение Кислотно-основное состояние КОС (кислотно-щелочной баланс, кислотно-щелочное равновесие)относительное постоянство реакции внутренней среды организма, количественно характеризующееся концентрацией водородных ионов (протонов).

Для упрощения выражения концентраций u введено понятие р. Н (power hydrogene - сила водорода) , которое соответствует отрицательному десятичному логарифму (- Lg) концентрации водородных ионов.

Кислотно-основное равновесие важнейший физико-химический параметр внутренней среды человека. От соотношения водородных и гидроксильных ионов зависит – -активность ферментов -направленность и интенсивность окислительно-восстановительных процессов -расщепление и синтез белка -гликолиз и окисление углеводов и жиров

-функции органов -чувствительность рецепторов к их медиаторам -проницаемость мембран -способность гемоглобина отдавать и связывать кислород - способность к адсорбции коллоидов клеток и межклеточных структур

Последствия нарушений КОС u Сдвиг р. Н на 0, 1 за нормальные границы приводит к нарушению дыхания, деятельности сердечнососудистой системы. u Снижение р. Н на 0, 3 вызывает ацидотическую кому, а сдвиг на 0, 4 несовместим с жизнью.

Следовательно uу человека и животных существуют сложные механизмы защиты против нарушений кислотно-основного равновесия.

В организме в процессе метаболизма постоянно образуются кислые соединения. При основном обмене постоянно генерируется около 1000020000 ммолей угольной кислоты и 80 ммолей сильных кислот. Но колебания концентрации ионов Н находятся в очень узких пределах: р. Н внеклеточной жидкости : -7, 32 -7, 45; внутри клеток - 6, 9 -7, 0.

Общее количество катионов плазмы 155 ммоль/л, из них - 142 ммоль/л приходится на натрий. Общее количество анионов также 155 ммоль/л, из них - 103 ммоль/л приходится на долю СL- 27 ммоль/л на долю НСО 3 - ВЫВОД - Кровь обладает слабощелочной реакцией.

Постоянство р. Н внутренней среды организма обусловлено совместным действием буферных систем крови и тканей, ряда физиологических механизмов - основном за счет деятельности легких и почек

Быстрое восстановление кислотноосновного равновесия ! - достигается с участием внутри- и внеклеточных буферных систем.

Постоянное поддержание р. Н достигается за счет выведения угольной кислоты легкими и выведением нелетучих кислот почками

Буферная система -сопряженная кислотно-основную пара, состоящая из донора и акцептора водородных ионов (протонов). Кислота- это вещество, отдающее протон Н+ во внеклеточную жидкость, а щелочь - это вещество способное связаться с протоном.

Определение – буферные свойства u способность противодействовать изменениям р. Н раствора при внесении в него кислот или оснований u обладают смеси, состоящие из слабой кислоты и её соли с сильным основанием или слабого основания с солью сильной кислоты.

Буферная емкость определяется - количеством кислоты или щелочи, которое необходимо добавить к буферному раствору, чтобы сместить р. Н на 1, 0.

Источники кислот в организме u Главными источниками образования кислот в организме метаболизм белков, жиров и углеводов. Все кислоты в организме могут быть разделены на летучие и нелетучие. u Летучей кислотой для организма является угольная кислота, которая выделяется через легкие в виде углекислого газа.

Угольная кислота - основной продукт обмена u Количество выделенной угольной кислоты через легкие равно ее метаболической продукции u С помощью легких ее концентрация в крови 1, 2 ммоль/л при Р СО 2 40 мм. рт. ст. в артериальной крови.

Нелетучие кислоты u За сутки в организме образуется около 1 ммоль/кг массы тела нелетучих кислот. Среди основных нелетучих кислот выделяют - серную ( на ее долю приходится 1/3 от всех нелетучих кислот), образуется при катаболизме белков и серосодержащих аминокислот.

- -оксимасляную, ацетоуксусную, молочную кислоту, образующиеся при неполном окислении жиров и углеводов (еще 1/ 3 от общего количества нелетучих кислот) - фосфопротеиы, фосфолипиды, а также пищевые продукты с избыточным содержанием органических катионов

При употреблении пищи, содержащей много мяса и яиц, образуется больше нелетучих кислот, чем при диетах из овощей и фруктов.


Распределение буферных систем u Кровь- гидрокарбонатная, гемоглобиновая, протеиновая, фосфатная. u Внеклеточная жидкостьгидрокарбонатная, фосфатная. u Внутриклеточная жидкость протеиновая, фосфатная, гидрокарбонатная. u Моча- аммонийная, фосфатная.

Гидрокарбонатный буфер Н 2 СО 3 Na. НСО 3 u Угольная кислота (Н 2 СО 3), выполняет роль донора протона, а бикарбонат (НСО 3 -) - роль акцептора протона u В плазме гидрокарбоната в 20 раз больше, чем угольной кислоты

Мощная система внеклеточной жидкости и крови. На долю бикарбонатного буфера приходится 53% всей буферной ёмкости крови и около 92% буферной емкости плазмы и интерстициальной жидкости
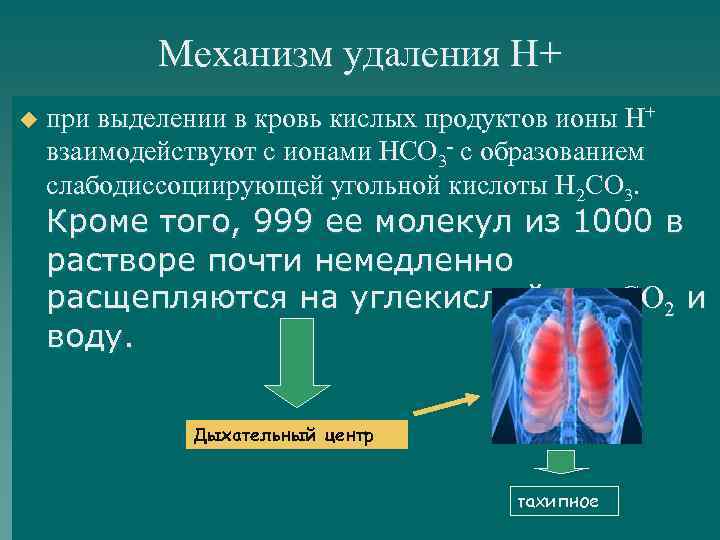
Механизм удаления Н+ u при выделении в кровь кислых продуктов ионы Н+ взаимодействуют с ионами НСО 3 - c образованием слабодиссоциирующей угольной кислоты Н 2 СО 3. Кроме того, 999 ее молекул из 1000 в растворе почти немедленно расщепляются на углекислый газ СО 2 и воду. Дыхательный центр тахипное
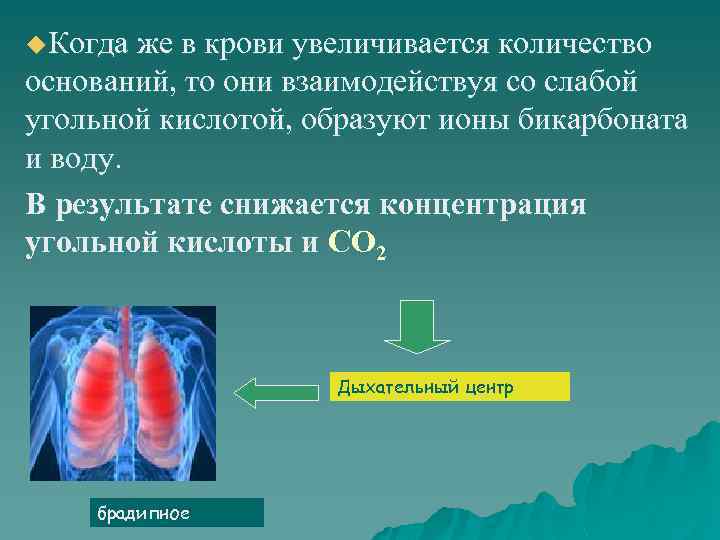
u. Когда же в крови увеличивается количество оснований, то они взаимодействуя со слабой угольной кислотой, образуют ионы бикарбоната и воду. В результате снижается концентрация угольной кислоты и СО 2 Дыхательный центр брадипное

ВЫВОД u гидрокарбонатный буфер можно считать основным буфером организма, так как углекислый газ, образующийся при диссоциации угольной кислоты, быстро удаляется при дыхании u стабильность концентрации НСО 3 достигается работой почек

Гемоглобиновый буфер- Hb. O 2/ Hb - составляет около половины всей буферной ёмкости крови. Гемоглобиновый буфер состоит из кислого компонента — оксигенированного - Нb 02 и основного — неоксигенированного - Нb.
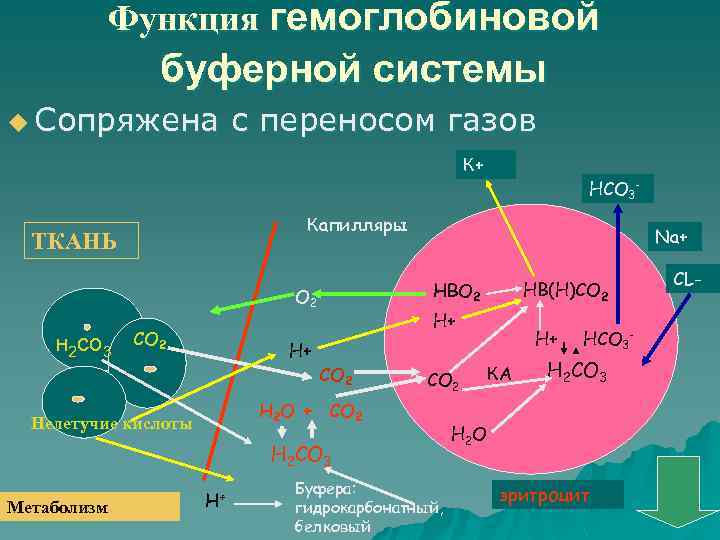
Функция гемоглобиновой буферной системы u Сопряжена с переносом газов К+ Капилляры ТКАНЬ СО 2 H+ Na+ H+ CO 2 H 2 O + CO 2 Нелетучие кислоты H 2 CO 3 Метаболизм H+ HB(Н)CO 2 HBO 2 н 2 со 3 НСО 3 - Буфера: гидрокарбонатный, белковый H+ КА НСО 3 - H 2 CO 3 H 2 O эритроцит CL-

Остающиеся в плазме крови ионы Na+ и вышедший из эритроцитов К+ взаимодействуют с НС 03 - и благодаря этому сохраняют её щелочной резерв Таким образом, В эритроцитах имеется механизм сбережения оснований для организма, известный как эффект Амбурже
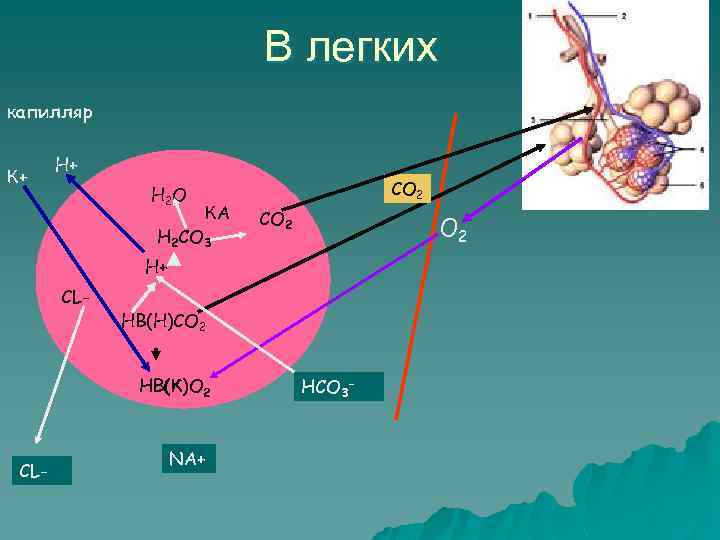
В легких капилляр К+ Н+ Н 2 О КА Н 2 СО 3 CO 2 СО 2 H+ CL- HB(Н)CO 2 HB(К)O 2 CL- NA+ НСО 3 -

Фосфатный буфер – Na. H 2 PO 4/Na 2 HPO 4 u Соотношение основного и кислого компонентов 4: 1. – Основная роль фосфатного буфера - регуляция р. Н внутриклеточной жидкости и тубулярной жидкости почек. В почечных канальцах происходит значительное концентрирование буфера и соответственно увеличение его мощности.

Протеиновая буферная система u основные буферные свойства белков обусловлены их амфотерностью, т. е. белки одновременно обладают свойствами кислот и оснований. Это обусловлено существованием в них карбоксильной группы СООН - кислые свойства и аминогруппы NH 2 – основные свойства.

Аммонийный буфер - NH 3 /NH 4+ u основной компонент аммиак NH 3 образуется нефроцитами из глютамина или глютомата. Роль этого буфера - связывание ионов Н+, секретируемых в просвет канальца, и удержание р. Н тубулярной жидкости не ниже 4, 5.

Кость как буфер. u кость может обеспечить до 40% буферной емкости при острой нагрузке кислотой, за счет освобождения кальция во внеклеточную жидкость.

Итак, общая буферная емкость жидких сред организма 125 мэкв/кг. При истощении функции почек относительно поддержания кислотноосновного равновесия и нормальной продукции сильных кислот буферной емкости хватило бы на 10 -20 дней.

Физиологические системы, поддерживающие кислотно-основное равновесие.

Легкие u Система внешнего дыхания довольно быстро (в течение нескольких минут) способна устранить или уменьшить сдвиги р. Н и предотвратить развитие ацидоза или алкалоза. Углекислого газа через легкие выводится около 850 г в сутки.
Увеличение вентиляции лёгких в 2 раза повышает р. Н крови примерно на 0, 2; снижение вентиляции на 25% может уменьшить р. Н на 0, 3 -0, 4. Если СО 2 в артериальной крови повышается на 10 мм. рт. ст. , то вентиляция увеличивается в 4 раза

Почки- секреция ионов Н+ в мочу клетками канальцевого эпителия; u образование в клетках эпителия канальцев бикарбонатов; u образование и диффузия в мочу аммиака; u реабсорбция бикарбоната профильтровавшегося; u фильтрация в первичную мочу кислых или основных продуктов; u обмен ионов хлора, натрия, калия, фосфатов, сульфатов и 2 х валентных катионов. u

u Некоторые кислоты (молочная, лимонная, однозамещенные кислые фосфаты), анионы сильных кислот выделяются в почках в нативном виде + Н ионов в моче в 800 раз больше, чем в крови; РН мочи 5, 3 -6, 5,

Ионы Н+ , секретируемые эпителием канальцев, замещаются на ионы Na+ которые реабсорбируются в виде бикарбоната. Основное место реабсорбции натрия – проксимальные канальцы – реабсорбируется 70% натрия профильтровавшегося.

Механизм реабсорбции натрия Профильтровавшийся натрий транспортируется из просвета канальца в почечный интерстиций через апикальную мембрану тремя механизмами
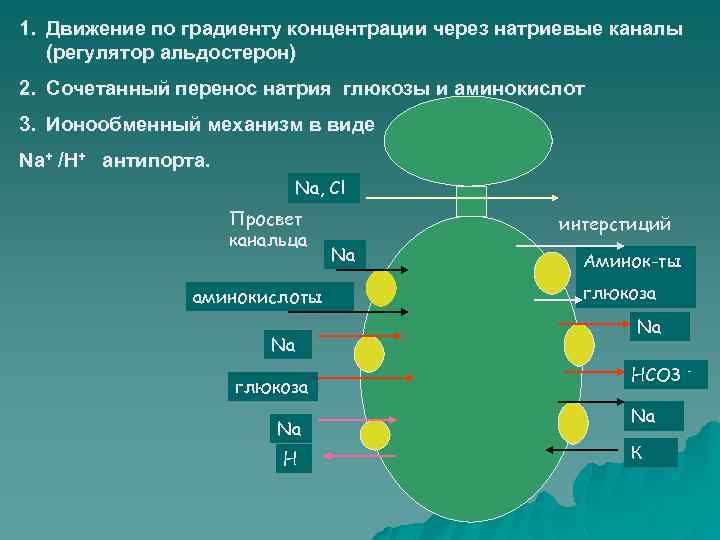
1. Движение по градиенту концентрации через натриевые каналы (регулятор альдостерон) 2. Сочетанный перенос натрия глюкозы и аминокислот 3. Ионообменный механизм в виде Na+ /Н+ антипорта. Na, Cl Просвет канальца аминокислоты Na глюкоза Na H интерстиций Na Аминок-ты глюкоза Na HCO 3 Na К -

Вместе с положительно заряженными ионами натрия реабсорбируются отрицательно заряженные ионы хлора и бикарбоната. За сутки реабсорбируется 20 000 ммоль ионов хлора

Реабсорбция бикарбоната u 1. Профильтровавшийся в первичную мочу бикарбонат в канальцах связывается с ионами Н+ и образуется угольная кислота НСО 3 - + Н+ = Н 2 СО 3 2. Угольная кислота немедленно разлагается карбоангидразой (КА), которая находится на наружной поверхности люминальной мембраны проксимальных почечных канальцев. Образуется вода и углекислый газ.

3. Вода будет реабсорбироваться (85%) в клетках проксимальных канальцев, в них же будет диффундировать СО 2 , который растворим в липидах и легко проходит через мембраны. В клетках эпителия из СО 2 и воды с помощью КА образуется угольная к-та- СО 2+ Н 2 О= Н 2 СО 3 = Н++НСО- 3 4. Ионы водорода выводятся, а ионы натрия взамен поступают в эпителий канальцев. Это активный процесс. Далее ионы натрия с бикарбонатами и уходят в кровь.
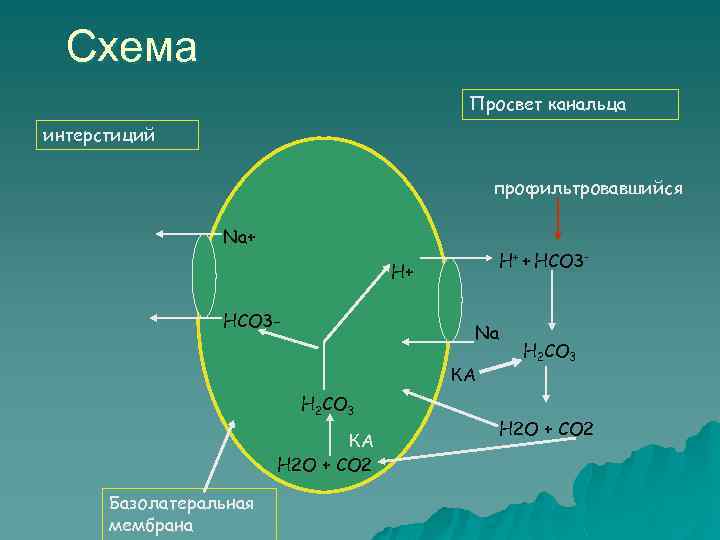
Схема Просвет канальца интерстиций профильтровавшийся Na+ H+ + HCO 3 - H+ HCO 3 - Na КА H 2 CO 3 КА H 2 O + CO 2 Базолатеральная мембрана H 2 CO 3 H 2 O + CO 2
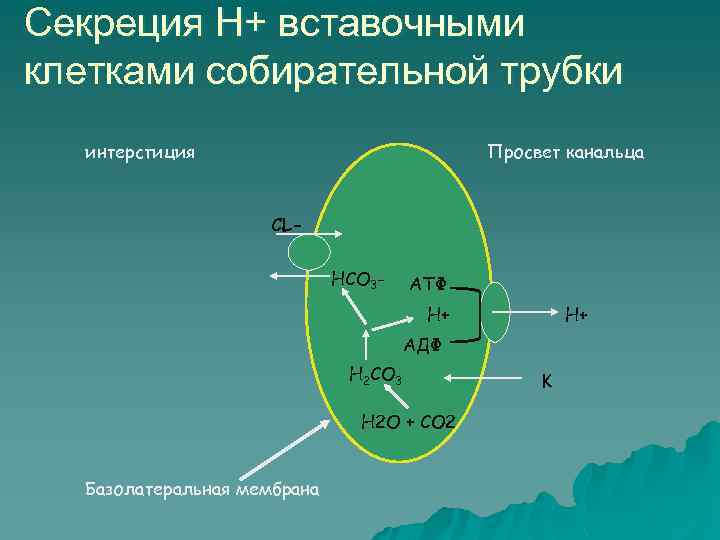
Секреция Н+ вставочными клетками собирательной трубки интерстиция Просвет канальца CLНСО 3 - АТФ Н+ Н+ АДФ Н 2 СО 3 H 2 O + CO 2 Базолатеральная мембрана K

Ионы водорода секретируемые в просвет проксимального канальца взаимодействуют с профильтрованными буферными основаниями. В крови Na 2 H PO 4 в 4 раза больше, чем Na H 2 PO 4 , а в моче Na H 2 PO 4 в 9 раз больше, чем Na 2 H PO 4.

Образование ионов NН 4+ аммониегенез u происходит в дистальных канальцах и собирательных трубках. Сначала образуется в клетках эпителия NН 3 путем дезаминирования глютамата, глютаминовой к-ты, NН 3 свободно проходит через липидный слой мембраны в канальцевую мочу и соединяется с ионами водорода и образуется NН 4+

Печеньu поставщик протеинов, синтез аммиака, мочевины, синтез гликогена из органических кислот, синтез кетоновых тел.

Желудочно-кишечный трактu в желудочном соке содержится натрий-150 - 180, калий 10 -20, хлор – 125, НСО 3 – 45 ммоль/л. u обкладочные клетки секретируют соляную кислоту в очень высокой концентрации. Взамен хлоридов, поступающих из плазмы, в плазму поступает бикарбонат

Определенная часть гидрокарбоната реабсорбируется в кишечнике, реабсорбируется натрий с помощью Na+ / H+- ионообменника. Всасываются двухвалентные ионы, но очень медленно.

Поджелудочная железа u важнейшее место продукции гидрокарбоната, за сутки вырабатывается 1, 5 - 2, 0 л панкреатического сока р. Н 7, 5 -8, 8; источником гидрокарбонатов также является желчь

Основные параметры кислотноосновного состояния. u РН-7, 35 -7, 44 u РСО 2 –парциальное давление углекислого газа в артериальной крови 40 мм. рт. ст. u ВВ-основной (базовый) буферсуммарное содержание всех буферных оснований в крови, 48 ммольл, допустимые колебания- 42 -52 ммоль/л

-АВ- актуальный бикарбонат – содержание акту бикарбонатов в плазме- 24 ммоль/л, колебания 22 -25 ммоль/л - Sb-стандартный бикарбонат – показатель концентрации иона бикарбоната при температуре 380 и полном насыщении кислородом гемоглобина, при р. СО 2 40 мм. рт. ст. В норме 25 -28 ммоль/л. - ИБО (ВЕ) – избыток буферных оснований-отклонение концентрации буферных оснований от нормального уровня. В норме ИБО-0, Допустимые колебания от-2 до+2 - Щелочной резерв - способность крови связать СО 2 при р СО 2 40 мм. рт. ст. Выражается в объемных процентах, в норме 50 -65 об%

Ацидозы, алкалозы Ацидоз – типовая форма нарушения КОС организма, характеризующаяся абсолютным или относительным увеличения содержания кислот (Н+) в плазме крови u Алкалоз типовая форма нарушения КОС организма, характеризующаяся абсолютным или относительным уменьшением содержания кислот (Н+) в плазме крови u

Классификация u - - Ацидозы: газовый негазовый: а. метаболический б. Выделительный в. экзогенный смешанный

Алкалозы - газовый - негазовый а. выделительный б. дегидратационный в. экзогенный - смешанный
По характеру клинического проявления u Острые Хронические Компенсированные Декомпенсированные

Критерием декомпенсации является u сдвиг значений р. Н u Норма 7, 35 -7, 45 u Субкомпенсированный 6 7, 35 -7, 29 ; 7, 45 -7, 56 u Декомпенсированный 7, 3 -6, 8 ; 7, 57 -7, 8

Респираторный (газовый) ацидоз-причины 1. снижение вентиляции, диффузии, перфузии легких (заболевания органов дыхания, нарушение регуляции дыхания, травмы грудной клетки и т. д. ) 2. избыточное поступление экзогенного СО 2 в организм 3. повышенное образование СО 2 не компенсируемое вентиляцией лихорадка, сепсис и т. д.
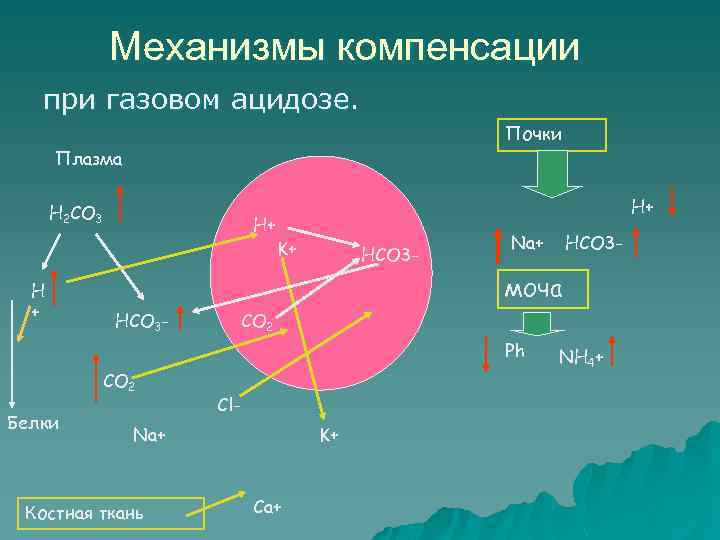
Механизмы компенсации при газовом ацидозе. Почки Плазма H 2 CO 3 H + H+ H+ K+ HCO 3 - Na+ моча HCO 3 - СО 2 Ph CO 2 Белки HCO 3 - Cl- Na+ Костная ткань K+ Ca+ NH 4+

В основе долговременной компенсации газового ацидоза u лежат метаболические изменения. приводящие к возрастанию (выше нормы) u ИБО - избыток буферных оснований u ВВ-основного (базового) буфера, u АВ- актуального бикарбоната u Sb-стандартного бикарбоната

Ацидозuгазовый Н 2 СО 3 Н+= Na. НСО 3 Итак, в стадию компенсации адекватно увеличению угольной кислоты возрастает количество бикарбоната натрия, соотношение 1: 20 сохраняется.

Особенности у детей u. У детей выделяют физиологический ацидоз смешанной формы, респираторного и метаболического характера - с первой минуты жизни и в течении нескольких дней, р. Н в крови – снижен, увеличено содержание молочной кислоты. Причины - незрелость легких, несовершенство деятельности почек в отношении КОС и

Клинико-лабораторные проявления респираторного ацидоза- усиление спазма бронхиол при повышении содержания углекислого газа - спазм артериол в соматических органах - - гиперфункция миокарда - сдвиг кривой диссоциации оксигемоглобина вправо - гипохлоремия - гипоксия тканей

- гиперкалиемия приводит к нарушению деятельности сердца, повышению возбудимости, к фибриляции. - может быть паралитическое расширение мозговых сосудов, гиперпродукция ликвора, повышение внутричерепного давления

Негазовый ацидоз u Причины - нарушена способность организма к выведению нелетучих кислот при их нормальной продукции (заболевания почек) - повышено образование нелетучих кислот. Это имеет место при - ОПН, ХПН, шок, диабетический кетоацидоз, алкогольный кетоацидоз, лактатный ацидоз - отравление экзогенными кислотами, интоксикация

Кроме того, метаболический ацидоз может быть следствием - потери гидрокарбонатов с мочой (проксимальный канальцевый ацидоз 2 типа), - гипоальдостеронизма - снижения способности нефроцитов к секреции ионов Н+ (канальцевый ацидоз 1 типа). - потери гидрокарбонатов с кишечным содержимым.

Механизмы компенсации негазового ацидоза 99% избытка ионов водорода будет реагировать с НСО 3 - из бикарбонатного буфера, результат возрастание угольной кислоты u Эритроциты, задерживая ионы Н+, будут отдавать калий u В обмен ионы хлора из эритроцитов выходят ионы НСО 3 -, которые пойдут на образование угольной кислоты Т. е. из сильных нелетучих для организма кислот образуется слабая летучая кислота – угольная. Результат – усиление дыхания. u

- белки проявляют щелочные свойства - кальций выходит из костной ткани - в почках возрастает секреция ионов водорода, аммиака, - в почках повышается реабсорбция бикарбонатов, натрия, Ph мочи снижается.
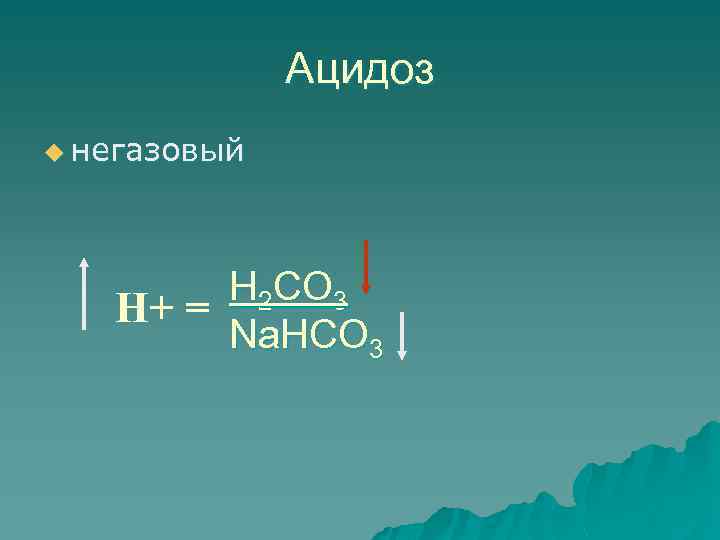
Ацидоз u негазовый Н 2 СО 3 Н+ = Na. НСО 3

Таким образом, метаболический ацидоз сопровождается - снижением НСО 3 - снижением р. СО 2 , как компенсация - снижением показателя ВВ (суммарное содержание буферных оснований), - ИБО (избыток буферных оснований) будет отрицательным

Клинические проявления негазового ацидоза u тахипное, u нарушение деятельности сердца (повышение возбудимости, фибриляция), как следствие гиперкалиемии u из-за снижения р. СО 2 (как компенсация) падение тонуса сосудов, снижение АД, уменьшение МОК, ограничение кровотока в органах (внутриклеточный ацидоз)
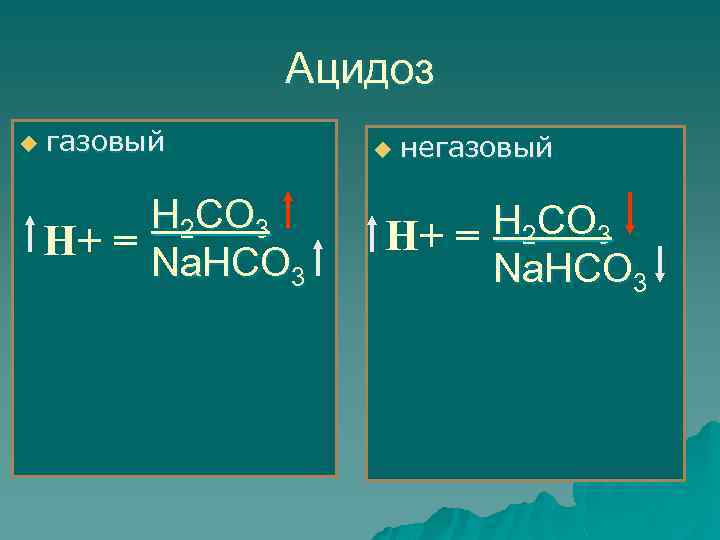
Ацидоз u газовый Н 2 СО 3 Н+ = Na. НСО 3 u негазовый Н 2 СО 3 Н+ = Na. НСО 3
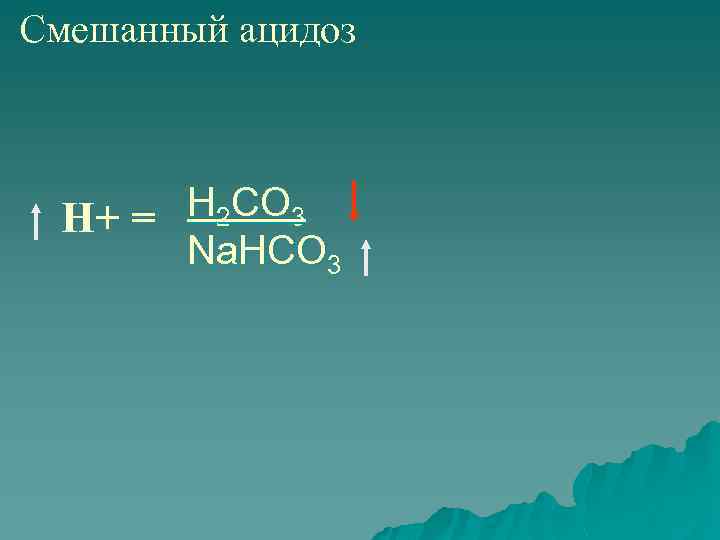
Смешанный ацидоз Н 2 СО 3 Н+ = Na. НСО 3

Респираторный алкалоз следствие увеличения эффективной альвеолярной вентиляции, приводящее к снижению р. СО 2 в крови и следовательно к гипокапнии u Причины-поражение ЦНС ( посттравматические, инфекции, инсульты) -ИВЛ -гипервентиляционые синдромы в психиатрии. - фармакологические препараты (салицилаты, адреналин, прогестагены) u

Механизмы компенсации при респираторном алкалозе понижение возбудимости дыхательного центра и гиповентиляция u из эритроцитов и всех клеток организма начинают выходить в плазму крови ионы водорода Н+ , в обмен на внеклеточные ионы калия и натрия u из эритроцитов и всех клеток организма выходят в плазму крови ионы хлора в обмен на НСО 3 -. u в крови из гидрокарбоната натрия начинается образование угольной кислоты. u

Механизмы компенсации при респираторном алкалозе протеиновый буфер начинает проявлять кислые свойства u костная ткань поглощает кальций u в почках ограничивается секреция ионов водорода, ограничивается реабсорбция натрия и гидрокарбоната u уменьшено выделение аммиака с мочой, р. Н мочи повышается u

Для респираторного алкалоза характерно: u Снижение р СО 2 u Снижение НСО 3 - (как компенсация) u Снижение ВВ-основного (базового) буфера - суммарное содержание буферных оснований u Снижение АВ- актуального бикарбоната, u снижение Sb-стандартного бикарбоната

Клинические проявления респираторного алкалоза u нарушение сосудистого тонуса, падение тонуса периферических сосудов, падение АД u нарушению органного кровотока u гипокалиемия, следствием которой является парез кишечника, судороги, нарушение сердечного ритма,

Негазовый алкалоз может быть результатом: u 1. увеличения концентрации гидрокарбоната при экзогенном его введение, или в результате сокращения объема внеклеточной жидкости. u 2. потери ионов Н+ из организма - неукротимая рвота, либо увеличение их секреции в почках u u задержки или повышения реабсорбция натрия и бикарбонатов, например при избытке минералкортикоидов

Механизмы компенсации негазового алкалоза эритроциты ( и все клетки) отдают в плазму ионы водорода в обмен на ионы калия (из плазмы), натрия, следствие – гипокалиемия u задержка в эритроцитах НСО 3 - и выход ионов хлора u ионы хлора в крови и интерстициальной жидкости реагируют с Na. НСО 3. u Образуется Na. Cl, а при взаимодействии НСО 3 - с ионами водорода – H 2 CO 3

Механизмы компенсации негазового алкалоза Дыхание - гиповентиляция u почки - ограничение секреции ионов водорода u почки – ограничение реабсорбции натрия и гидрокарбонатов u р. Н мочи повышается u

Таким образом, негазовый алкалоз характеризуется u повышением РСО 2 вследствие гиповентиляции, как компенсации u увеличением ВВ (суммарное содержание бикарбонатов) u ИБО-избыток буферных оснований приобретает положительное значение Следует отметить, что в организме нет достаточно эффективных механизмов компенсации метаболического

Клинические проявления связаны с гипокалиемией, как следствие u изменение нервно-мышечной возбудимости u слабость скелетной мускулатуры u уменьшение двигательной активности желудочнокишечного тракта u поражение кардиомиоцитов

Для души И любящие, как во сне, На протяженье многих зим Друг к другу тянутся поспешней, Я помню дни солнцеворота, И на деревьях в вышине И каждый был неповторим Потеют от тепла скворешни. И повторялся вновь без счета. И полусонным стрелкам лень И целая их череда Ворочаться на циферблате, Составилась мало-помалу И дольше века длится день, -Тех дней единственных, когда И не кончается объятье. Нам кажется, что время стало Я помню их наперечет: Зима подходит к середине, Дороги мокнут, с крыш течет И солнце греется на льдине Пастернак Борис Леонидович (1890 - 1960)— русский писатель

ПАТОФИЗИОЛОГИЯ КИСЛОТНО-ОСНОВНОГО СОСТОЯНИЯ.ppt