Климактерический синдром — это симптомокомплекс , который развивается





































6_immunologia_klimaxa_starenia.ppt
- Размер: 2.9 Мб
- Автор:
- Количество слайдов: 38
Описание презентации Климактерический синдром — это симптомокомплекс , который развивается по слайдам

 Климактерический синдром — это симптомокомплекс , который развивается в период возрастного угасания функции репродуктивной системы женщины и характеризуется нейровегетативными, обменно-эндокринными и психо-эмоциональными расстройствами различной степени интенсивности и продолжительности.
Климактерический синдром — это симптомокомплекс , который развивается в период возрастного угасания функции репродуктивной системы женщины и характеризуется нейровегетативными, обменно-эндокринными и психо-эмоциональными расстройствами различной степени интенсивности и продолжительности.
 Клинические проявления климактерического синдрома нередко взаимосвязаны и могут быть обусловлены различными заболеваниями переходного возраста. Общая частота климактерического синдрома варьирует от 40% до 80%.
Клинические проявления климактерического синдрома нередко взаимосвязаны и могут быть обусловлены различными заболеваниями переходного возраста. Общая частота климактерического синдрома варьирует от 40% до 80%.
 К началу климактерического периода происходит «накопление повреждений» , связанное с: — перенесенными заболеваниями, — стрессовыми ситуациями, — оперативными вмешательствами, — особенностями современного образа жизни.
К началу климактерического периода происходит «накопление повреждений» , связанное с: — перенесенными заболеваниями, — стрессовыми ситуациями, — оперативными вмешательствами, — особенностями современного образа жизни.
 Высокая частота, большая интенсивность и продолжительность воздействия неблагоприятных факторов на фоне возрастной перестройки организма обусловливают снижение уровня «ресурсов здоровья» , являясь только пусковым звеном в проявлении уже имеющейся патологии.
Высокая частота, большая интенсивность и продолжительность воздействия неблагоприятных факторов на фоне возрастной перестройки организма обусловливают снижение уровня «ресурсов здоровья» , являясь только пусковым звеном в проявлении уже имеющейся патологии.
 Возникновение климактерического синдрома обусловлено широким комплексом причин , которые связаны с: 1) нарушениями защитно- приспособительных механизмов; 2) нарушениями метаболического равновесия в период возрастной перестройки организма на фоне прогрессирующего угасания функции яичников.
Возникновение климактерического синдрома обусловлено широким комплексом причин , которые связаны с: 1) нарушениями защитно- приспособительных механизмов; 2) нарушениями метаболического равновесия в период возрастной перестройки организма на фоне прогрессирующего угасания функции яичников.
 Развитие климактерического синдрома и его тяжесть во многом определяются гиперактивностью аутоиммунных реакций по отношению к компонентам яичников.
Развитие климактерического синдрома и его тяжесть во многом определяются гиперактивностью аутоиммунных реакций по отношению к компонентам яичников.
 Механизмом поддержания аутоагрессии служит снижение функции Т-супрессоров при умеренной активации В-клеток за счет гиперпродукции Ig. G. Уменьшение активности фагоцитов наблюдается при наличии сопутствующего ожирения.
Механизмом поддержания аутоагрессии служит снижение функции Т-супрессоров при умеренной активации В-клеток за счет гиперпродукции Ig. G. Уменьшение активности фагоцитов наблюдается при наличии сопутствующего ожирения.
 Иммунный статус у больных с климактерическим синдромом имеет некоторые отличия от такового у лиц старшего возраста (более 70 лет).
Иммунный статус у больных с климактерическим синдромом имеет некоторые отличия от такового у лиц старшего возраста (более 70 лет).
 Первые признаки возрастных дисфункций иммунитета иногда выявляются у лиц обоего пола в возрасте старше 50 лет : — гиперпродукция Ig. G — и Ig. A — антител при снижении уровня S-Ig. A и аутоантител ; — снижение функции Т-лимфоцитов ; — увеличение содержания T-клеток (супрессоров, киллеров).
Первые признаки возрастных дисфункций иммунитета иногда выявляются у лиц обоего пола в возрасте старше 50 лет : — гиперпродукция Ig. G — и Ig. A — антител при снижении уровня S-Ig. A и аутоантител ; — снижение функции Т-лимфоцитов ; — увеличение содержания T-клеток (супрессоров, киллеров).
 Снижается в целом «цензорная» функция иммунитета, что обусловливает повышенную частоту онкологических, аутоиммунных и инфекционных заболеваний у людей старшего возраста. Это дает начало аутоагрессии , прежде всего, по отношению к ДНК и клеткам эндокринных желез.
Снижается в целом «цензорная» функция иммунитета, что обусловливает повышенную частоту онкологических, аутоиммунных и инфекционных заболеваний у людей старшего возраста. Это дает начало аутоагрессии , прежде всего, по отношению к ДНК и клеткам эндокринных желез.
 И. И. Мечников утверждал: «Смерть раньше 150 лет — насильственная смерть».
И. И. Мечников утверждал: «Смерть раньше 150 лет — насильственная смерть».
 Проблемы старения становятся все более актуальными и в медицинском, и в социальном аспектах: по данным ВОЗ число лиц пожилого и старческого возраста неуклонно растет. Так как старение ее может ограничивать продолжительность жизни.
Проблемы старения становятся все более актуальными и в медицинском, и в социальном аспектах: по данным ВОЗ число лиц пожилого и старческого возраста неуклонно растет. Так как старение ее может ограничивать продолжительность жизни.
 Одной из основных причин старения считают нарушения в функционировании иммунной системы как в целом, так и в отдельных ее звеньях. С нарушениями работы иммунной системы ассоциируются многие заболевания пожилого и старческого возраста: аутоиммунные заболевания, опухоли, болезни суставов, почек, амилоидоз, патология сердечно-сосудистой системы, инфекционные заболевания.
Одной из основных причин старения считают нарушения в функционировании иммунной системы как в целом, так и в отдельных ее звеньях. С нарушениями работы иммунной системы ассоциируются многие заболевания пожилого и старческого возраста: аутоиммунные заболевания, опухоли, болезни суставов, почек, амилоидоз, патология сердечно-сосудистой системы, инфекционные заболевания.
 Изменения в работе иммунной системы начинаются задолго до каких либо проявлений старения организма. Неясно, какой процесс первичен : болезни вызывают снижение иммунореактивности организма или возрастное ослабление функций иммунной системы способствует развитию болезней.
Изменения в работе иммунной системы начинаются задолго до каких либо проявлений старения организма. Неясно, какой процесс первичен : болезни вызывают снижение иммунореактивности организма или возрастное ослабление функций иммунной системы способствует развитию болезней.
 Структурные изменения затрагивают непосредственно клеточные структуры: 1) появляются изменения в клеточной мембране, органеллах, цитоплазме; 2) снижается плотность клеточных рецепторов у Т- и В-лимфоцитов и появляются новые; 3) ослабевает выработка веществ, подавляющих митозы. Все это предрасполагает к развитию лимфопролиферативных и опухолевых процессов
Структурные изменения затрагивают непосредственно клеточные структуры: 1) появляются изменения в клеточной мембране, органеллах, цитоплазме; 2) снижается плотность клеточных рецепторов у Т- и В-лимфоцитов и появляются новые; 3) ослабевает выработка веществ, подавляющих митозы. Все это предрасполагает к развитию лимфопролиферативных и опухолевых процессов
 Эти причины приводят к гиперпродукции аутоантител , которая является: 1) компенсаторной реакцией (увеличение выведения продуктов распада); 2) нарушением контрольных механизмов иммунной системы в пожилом и старческом возрастах. Отмечается более высокая смертность в группе носителей аутоантител широкой специфичности
Эти причины приводят к гиперпродукции аутоантител , которая является: 1) компенсаторной реакцией (увеличение выведения продуктов распада); 2) нарушением контрольных механизмов иммунной системы в пожилом и старческом возрастах. Отмечается более высокая смертность в группе носителей аутоантител широкой специфичности
 Существует теория о том, что старение есть аутоиммунный процесс Причины увеличения частоты случаев аутоиммунной патологии в старости является: 1) функциональное ослабление иммунологического надзора; 2) накопление мутантных клеток, несущих чуждые организму антигены.
Существует теория о том, что старение есть аутоиммунный процесс Причины увеличения частоты случаев аутоиммунной патологии в старости является: 1) функциональное ослабление иммунологического надзора; 2) накопление мутантных клеток, несущих чуждые организму антигены.
 Иммунный ответ контролируется генами иммунного ответа. Нормальная иммунная реакция и ненарушенная генетическая регуляция иммунореактивности – необходимое условие устойчивости к болезням и старению. Гены системы гистосовместимости участвуют в регуляции иммунореактивности и связаны с патологией.
Иммунный ответ контролируется генами иммунного ответа. Нормальная иммунная реакция и ненарушенная генетическая регуляция иммунореактивности – необходимое условие устойчивости к болезням и старению. Гены системы гистосовместимости участвуют в регуляции иммунореактивности и связаны с патологией.
 Набор антигенов каждого человека строго индивидуален Фенотип человека определяет: 1) особенности функционирования многих органов и систем; 2) общеповеденческую реакцию при взаимодействии с окружающей средой.
Набор антигенов каждого человека строго индивидуален Фенотип человека определяет: 1) особенности функционирования многих органов и систем; 2) общеповеденческую реакцию при взаимодействии с окружающей средой.
 Существует связь комплекса гистосовместимости с чувствительностью к вирусным инфекциям, опухолям и аутоиммуным заболеваниям (н апример, связь комплекса гистосовместимости HLA c рядом патологических состояний) : 1) артропатии, связанные с HLA-В 27 (анкилозирующий спондиллит, реактивный артрит и острый передний увеит);
Существует связь комплекса гистосовместимости с чувствительностью к вирусным инфекциям, опухолям и аутоиммуным заболеваниям (н апример, связь комплекса гистосовместимости HLA c рядом патологических состояний) : 1) артропатии, связанные с HLA-В 27 (анкилозирующий спондиллит, реактивный артрит и острый передний увеит);
 2) иммунопатии, связанные с HLA-В 8 и DR 3 (ювенильный диабет, миастения гравис, целиакия, гипертиформный дерматит, аддисонова болезнь, тиреотоксикоз); 3) заболевания, связанные с фенотипом HLA-В 7, DR 2 (множественный склероз, недостаточность С 4 компонента комплемента). Выявлена связь между маркерами гистосовместимости и продолжительностью жизни
2) иммунопатии, связанные с HLA-В 8 и DR 3 (ювенильный диабет, миастения гравис, целиакия, гипертиформный дерматит, аддисонова болезнь, тиреотоксикоз); 3) заболевания, связанные с фенотипом HLA-В 7, DR 2 (множественный склероз, недостаточность С 4 компонента комплемента). Выявлена связь между маркерами гистосовместимости и продолжительностью жизни
 В различных возрастных группах набор антигенов гистосовместимости отличается за счет редко встречающихся антигенов У представителей старших возрастных групп: 1) гены, ассоциированные с предрасположенностью к пиогенной инфекции , встречались реже ; 2) гены, ассоциированные с аутоиммунными заболеваниями — значительно чаще.
В различных возрастных группах набор антигенов гистосовместимости отличается за счет редко встречающихся антигенов У представителей старших возрастных групп: 1) гены, ассоциированные с предрасположенностью к пиогенной инфекции , встречались реже ; 2) гены, ассоциированные с аутоиммунными заболеваниями — значительно чаще.
 Продолжительность жизни определяется генетически. Различия между максимальной и средней ее продолжительностью в пределах вида в значительной степени отражают влияние окружающей среды.
Продолжительность жизни определяется генетически. Различия между максимальной и средней ее продолжительностью в пределах вида в значительной степени отражают влияние окружающей среды.
 В подтверждение генетической теории старения приводятся исследования монозиготных и дизиготных близнецов из семей с малой и большой продолжительностью жизни родителей.
В подтверждение генетической теории старения приводятся исследования монозиготных и дизиготных близнецов из семей с малой и большой продолжительностью жизни родителей.
 Различие в продолжительности жизни у пары монозиготных близнецов меньше, чем у дизиготных. Средняя продолжительность жизни лиц, родители которых жили долго, была больше, чем у потомков родителей с меньшей продолжительностью жизни Одна и та же причина смерти у монозиготных близнецов встречалась примерно в 2 раза чаще , чем у дизиготных.
Различие в продолжительности жизни у пары монозиготных близнецов меньше, чем у дизиготных. Средняя продолжительность жизни лиц, родители которых жили долго, была больше, чем у потомков родителей с меньшей продолжительностью жизни Одна и та же причина смерти у монозиготных близнецов встречалась примерно в 2 раза чаще , чем у дизиготных.
 На возрастные ослабления функций иммунной системы влияют: 1) Экзогенные факторы; 2) Эндогенные факторы: — изменение клеточного окружения (нарушения нейрогуморального равновесия); — изменения самих клеток иммунной системы.
На возрастные ослабления функций иммунной системы влияют: 1) Экзогенные факторы; 2) Эндогенные факторы: — изменение клеточного окружения (нарушения нейрогуморального равновесия); — изменения самих клеток иммунной системы.
 Старость — Т-иммунодефицит с высоким уровнем иммунологической резистентности (сблансированный Т-иммунодефицит). Характерные для старения изменения в популяции Т-клеток обусловлены возрастной инволюцией тимуса.
Старость — Т-иммунодефицит с высоким уровнем иммунологической резистентности (сблансированный Т-иммунодефицит). Характерные для старения изменения в популяции Т-клеток обусловлены возрастной инволюцией тимуса.
 Инволюция тимуса и снижение активности лизосомальных ферментов макрофагов являются одними из важных причин изменения функциональной активности иммунной системы в пожилом возрасте.
Инволюция тимуса и снижение активности лизосомальных ферментов макрофагов являются одними из важных причин изменения функциональной активности иммунной системы в пожилом возрасте.
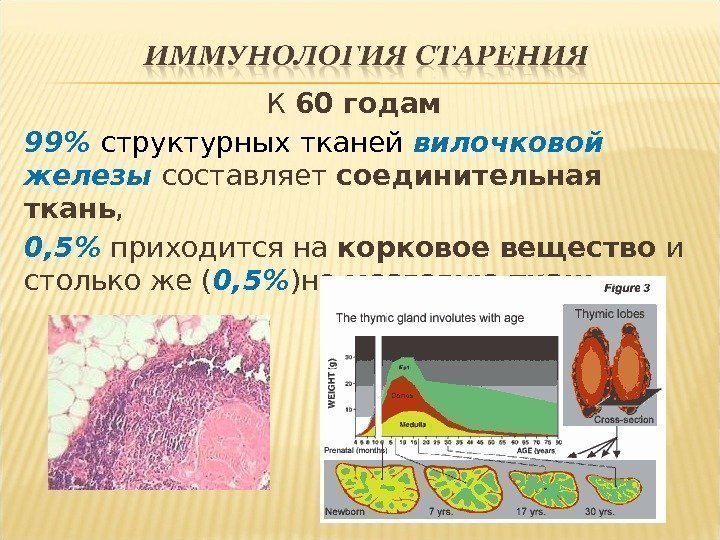
 К 60 годам 99% структурных тканей вилочковой железы составляет соединительная ткань , 0, 5% приходится на корковое вещество и столько же ( 0, 5% )на мозговую ткань.
К 60 годам 99% структурных тканей вилочковой железы составляет соединительная ткань , 0, 5% приходится на корковое вещество и столько же ( 0, 5% )на мозговую ткань.
 Активность лизосомальных ферментов к 60 годам падает в 7 раз, к 70 — в 10 раз. Происходит изменение основных функций: фагоцитоз, опсоно-фагоцитарные реакции, киллерная активность, распознаваемость чужеродных антигенов. Увеличивается: — частота реакций на собственные антигены (растет аутоиммунная патология); — количество В-лимфоцитов (синтезирующих аутоантитела на собственные антигены организма) в сыворотке крови.
Активность лизосомальных ферментов к 60 годам падает в 7 раз, к 70 — в 10 раз. Происходит изменение основных функций: фагоцитоз, опсоно-фагоцитарные реакции, киллерная активность, распознаваемость чужеродных антигенов. Увеличивается: — частота реакций на собственные антигены (растет аутоиммунная патология); — количество В-лимфоцитов (синтезирующих аутоантитела на собственные антигены организма) в сыворотке крови.
 Изменение иммунологической реактивности связано со снижением потенции костного мозга: истощается саморепликация стволовых клеток и уменьшается выработка антител на 20— 50%. Снижение на 60% активности естественных киллеров и дефицит бактериального интерферона влияют на течение бактериальных и вирусных инфекций. При этом снижается также супрессия продукции генома опухолевых вирусов.
Изменение иммунологической реактивности связано со снижением потенции костного мозга: истощается саморепликация стволовых клеток и уменьшается выработка антител на 20— 50%. Снижение на 60% активности естественных киллеров и дефицит бактериального интерферона влияют на течение бактериальных и вирусных инфекций. При этом снижается также супрессия продукции генома опухолевых вирусов.
 Доказательством служат следующие факты : 1) Ослабление Т-зависимых иммунных функций совпадает с началом инволюции тимуса. С этим ослаблением связано повышение восприимчивости к некоторым инфекциям и склонность к аутоиммунным реакциям; 2) Иммунодефицит и аутоиммунитет у мышей, тимэктомированных при рождении, удается предотвратить путем пересадки им тимуса от молодых животных;
Доказательством служат следующие факты : 1) Ослабление Т-зависимых иммунных функций совпадает с началом инволюции тимуса. С этим ослаблением связано повышение восприимчивости к некоторым инфекциям и склонность к аутоиммунным реакциям; 2) Иммунодефицит и аутоиммунитет у мышей, тимэктомированных при рождении, удается предотвратить путем пересадки им тимуса от молодых животных;
 Доказательством служат следующие факты: 3) Больные с первичным иммунодефицитом чаще страдают аутоиммунными заболеваниями , у них чаще возникают злокачественные новообразования ; 4) Способность тимуса влиять на дифференцировку и созревание Т-клеток с возрастом уменьшается
Доказательством служат следующие факты: 3) Больные с первичным иммунодефицитом чаще страдают аутоиммунными заболеваниями , у них чаще возникают злокачественные новообразования ; 4) Способность тимуса влиять на дифференцировку и созревание Т-клеток с возрастом уменьшается
 Для пожилого и старческого возраста характерно снижение: 1) противомикробного иммунитета; 2) противовирусной защиты; 3) противоопухолевой защиты. Это связано непосредственно с реакциями клеточного иммунитета, в которых принимают участие естественные киллеры (ЕК-клетки).
Для пожилого и старческого возраста характерно снижение: 1) противомикробного иммунитета; 2) противовирусной защиты; 3) противоопухолевой защиты. Это связано непосредственно с реакциями клеточного иммунитета, в которых принимают участие естественные киллеры (ЕК-клетки).
 При старении меняется количественное содержание клеток киллеров: — или увеличивается; — или снижается. Функциональная активность после 70 лет , как правило, снижается. У долгожителей отмечается вновь возрастание активности ЕК-клеток , берущих на себя реакции клеточного иммунитета.
При старении меняется количественное содержание клеток киллеров: — или увеличивается; — или снижается. Функциональная активность после 70 лет , как правило, снижается. У долгожителей отмечается вновь возрастание активности ЕК-клеток , берущих на себя реакции клеточного иммунитета.
 Естественное старение — это процесс развития сбалансированного иммунодефицита, увядание всех звеньев иммунной системы.
Естественное старение — это процесс развития сбалансированного иммунодефицита, увядание всех звеньев иммунной системы.
 Болезни в старости усугубляют характерный для пожилых иммунодефицит. Отсрочить начало старения, смягчить проявления болезней пожилого возраста вполне возможно, препятствуя ослаблению нормальных функций иммунитета.
Болезни в старости усугубляют характерный для пожилых иммунодефицит. Отсрочить начало старения, смягчить проявления болезней пожилого возраста вполне возможно, препятствуя ослаблению нормальных функций иммунитета.

