Молекулярная биотехнология 5.ppt
- Количество слайдов: 90
 Клеточная инженерия на уровне яйцеклеток • Операции с яйцеклетками начались в 40 -х-50 -х гг. • Яйцеклетка+сперматозоид = диплоидная зигота • Яйцеклетка с заменой ядра на ядро соматической клетки – имитация диплоидной зиготы
Клеточная инженерия на уровне яйцеклеток • Операции с яйцеклетками начались в 40 -х-50 -х гг. • Яйцеклетка+сперматозоид = диплоидная зигота • Яйцеклетка с заменой ядра на ядро соматической клетки – имитация диплоидной зиготы
 Клонирование организмов • Это получение потомков одной особи без полового процесса. Члены клона генетически идентичны • Клоны вирусов, молекулярные клоны • Клоны бактерий • Клоны клеток в культуре • Клоны растений • КЛОНЫ ЖИВОТНЫХ
Клонирование организмов • Это получение потомков одной особи без полового процесса. Члены клона генетически идентичны • Клоны вирусов, молекулярные клоны • Клоны бактерий • Клоны клеток в культуре • Клоны растений • КЛОНЫ ЖИВОТНЫХ
 Партеногенез – природное клонирование • Партеногенез – размножение без участия мужских половых клеток • Встречается у некоторых видов насекомых и позвоночных (рыб, пресмыкающихся)
Партеногенез – природное клонирование • Партеногенез – размножение без участия мужских половых клеток • Встречается у некоторых видов насекомых и позвоночных (рыб, пресмыкающихся)
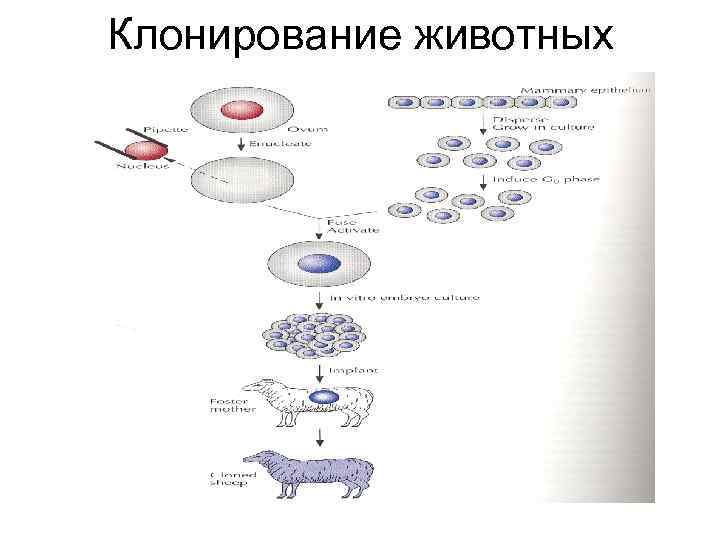 Клонирование животных
Клонирование животных
 Проблема клонирования животных • Клоны генетически идентичны • При клонировании животныхрекордсменов появляется теоретическая возможность получить стада рекордсменов • Возникает теоретическая возможность клонирования человека с вытекающими отсюда последствиями
Проблема клонирования животных • Клоны генетически идентичны • При клонировании животныхрекордсменов появляется теоретическая возможность получить стада рекордсменов • Возникает теоретическая возможность клонирования человека с вытекающими отсюда последствиями
 Трудности в клонировании животных • Технические трудности (низкая эффективность) • Недостаточное знание процессов развития организмов • Фенотипически клоны могут быть неидентичными • Этические проблемы клонирования человека
Трудности в клонировании животных • Технические трудности (низкая эффективность) • Недостаточное знание процессов развития организмов • Фенотипически клоны могут быть неидентичными • Этические проблемы клонирования человека
 Клонированные виды животных • • • Овцы (овечка Долли, 1996) Мыши Кошки Собаки Коровы Приматы (? ? ? )
Клонированные виды животных • • • Овцы (овечка Долли, 1996) Мыши Кошки Собаки Коровы Приматы (? ? ? )
 Стволовые клетки • Это клетки, способные дифференцироваться в клетки различных тканей организма • Стволовые клетки могут быть тотипотентными (все ткани организма), плюрипотентными, или мультипотентными (многие ткани организма), олигопотентными (клетки в пределах одной ткани), клетки-предшественники (один тип дифференцированных клеток)
Стволовые клетки • Это клетки, способные дифференцироваться в клетки различных тканей организма • Стволовые клетки могут быть тотипотентными (все ткани организма), плюрипотентными, или мультипотентными (многие ткани организма), олигопотентными (клетки в пределах одной ткани), клетки-предшественники (один тип дифференцированных клеток)
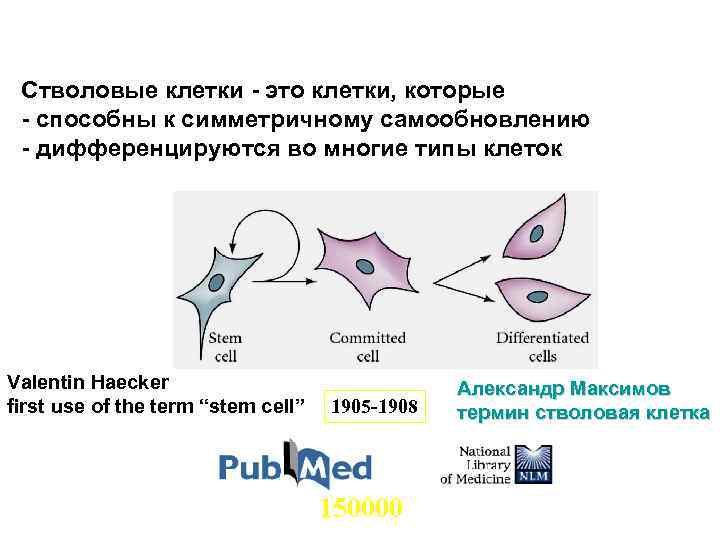 Стволовые клетки - это клетки, которые - способны к симметричному самообновлению - дифференцируются во многие типы клеток Valentin Haecker first use of the term “stem cell” 1905 -1908 150000 Александр Максимов термин стволовая клетка
Стволовые клетки - это клетки, которые - способны к симметричному самообновлению - дифференцируются во многие типы клеток Valentin Haecker first use of the term “stem cell” 1905 -1908 150000 Александр Максимов термин стволовая клетка
 Типы стволовых клеток • Эмбриональные стволовые клетки • Фетальные стволовые клетки • Стволовые клетки из пуповинной крови и плаценты • Взрослые стволовые клетки (из костного мозга и других органов)
Типы стволовых клеток • Эмбриональные стволовые клетки • Фетальные стволовые клетки • Стволовые клетки из пуповинной крови и плаценты • Взрослые стволовые клетки (из костного мозга и других органов)
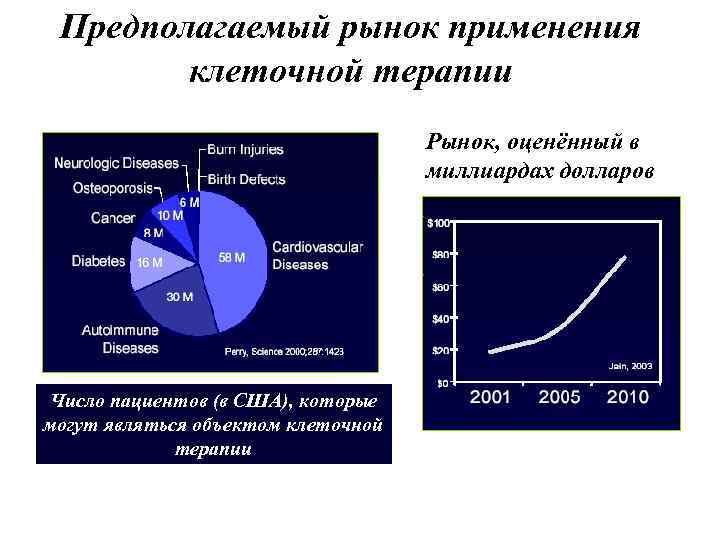 Предполагаемый рынок применения клеточной терапии Рынок, оценённый в миллиардах долларов Число пациентов (в США), которые могут являться объектом клеточной терапии
Предполагаемый рынок применения клеточной терапии Рынок, оценённый в миллиардах долларов Число пациентов (в США), которые могут являться объектом клеточной терапии
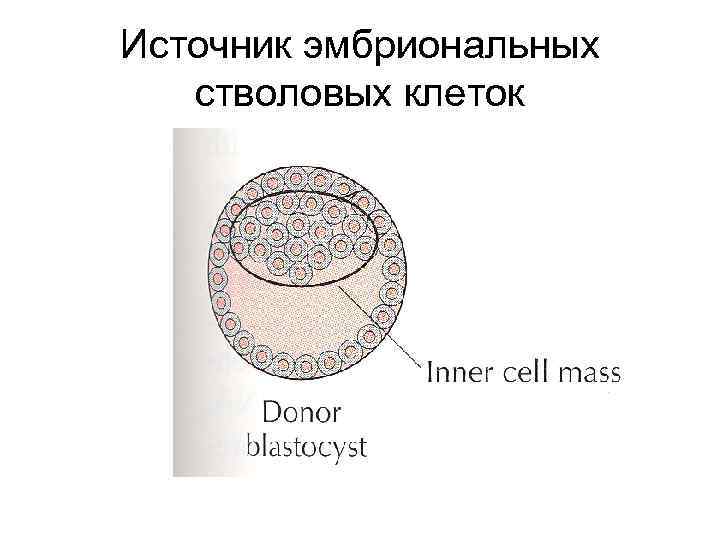 Источник эмбриональных стволовых клеток
Источник эмбриональных стволовых клеток
 ЭМБРИОНАЛЬНЫЕ СТВОЛОВЫЕ КЛЕТКИ МЛЕКОПИТАЮЩИХ • СВОЙСТВА : • произошли из внутренней клеточной массы бластоцисты, • способны к неограниченному числу делений без дифференцировки, • имеют полный (диплоидный) набор хромосом и сохраняют кариотип, • плюрипотентны – способны дифференцироваться в клетки всех трёх зародышевых листков. • 1981 – получены ЭСК мыши • 1995 – получены ЭСК обезьян • 1998 - получены ЭСК человека
ЭМБРИОНАЛЬНЫЕ СТВОЛОВЫЕ КЛЕТКИ МЛЕКОПИТАЮЩИХ • СВОЙСТВА : • произошли из внутренней клеточной массы бластоцисты, • способны к неограниченному числу делений без дифференцировки, • имеют полный (диплоидный) набор хромосом и сохраняют кариотип, • плюрипотентны – способны дифференцироваться в клетки всех трёх зародышевых листков. • 1981 – получены ЭСК мыши • 1995 – получены ЭСК обезьян • 1998 - получены ЭСК человека
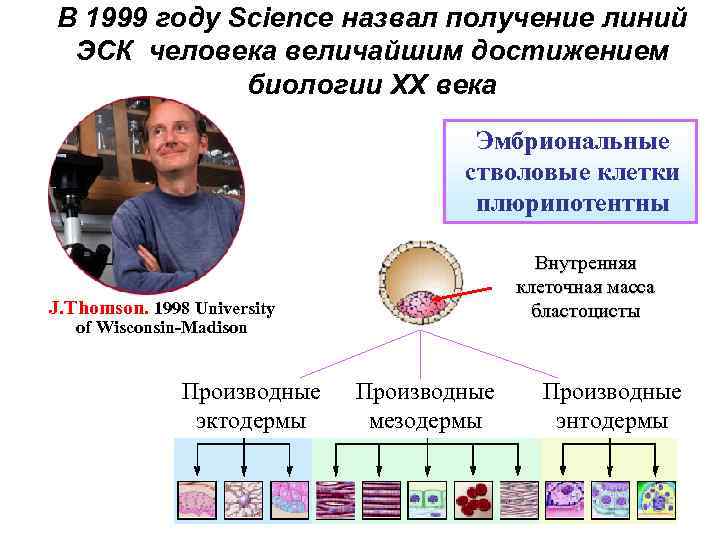 В 1999 году Science назвал получение линий ЭСК человека величайшим достижением биологии ХХ века Эмбриональные стволовые клетки плюрипотентны Внутренняя клеточная масса бластоцисты J. Thomson. 1998 University of Wisconsin-Madison Производные эктодермы Производные мезодермы Производные энтодермы
В 1999 году Science назвал получение линий ЭСК человека величайшим достижением биологии ХХ века Эмбриональные стволовые клетки плюрипотентны Внутренняя клеточная масса бластоцисты J. Thomson. 1998 University of Wisconsin-Madison Производные эктодермы Производные мезодермы Производные энтодермы
 Чем диктуется спрос на клеточные технологии 1. Существование многих хронических заболеваний, которые еще не поддаются эффективному лечению. Возможности существующих методов исчерпаны. 2. Заместительная терапия, трансплантация. 3. Увеличение стареющей популяции. Озабоченность своим здоровьем. СПЕЦИФИКА РОССИИ: Стволовые клетки–это модно, хотя никто не знает, что это такое. Полная бесконтрольность «лечат» всех от всего материалом из неизвестных источников.
Чем диктуется спрос на клеточные технологии 1. Существование многих хронических заболеваний, которые еще не поддаются эффективному лечению. Возможности существующих методов исчерпаны. 2. Заместительная терапия, трансплантация. 3. Увеличение стареющей популяции. Озабоченность своим здоровьем. СПЕЦИФИКА РОССИИ: Стволовые клетки–это модно, хотя никто не знает, что это такое. Полная бесконтрольность «лечат» всех от всего материалом из неизвестных источников.
 Использование стволовых клеток • Научные исследования • Получение трансгенных животных • Терапия различных заболеваний человека (? ) • Банки пуповинной крови
Использование стволовых клеток • Научные исследования • Получение трансгенных животных • Терапия различных заболеваний человека (? ) • Банки пуповинной крови
 Молекулярная биотехнология и инфекционные заболевания
Молекулярная биотехнология и инфекционные заболевания
 Инфекции и инфекционные заболевания • Инфекция – это взаимодействие микрои макроорганизма • Инфекционное заболевание – это один из возможных исходов инфекционного процесса
Инфекции и инфекционные заболевания • Инфекция – это взаимодействие микрои макроорганизма • Инфекционное заболевание – это один из возможных исходов инфекционного процесса
 Два типа иммунитета • Врождённый иммунитет - защищает от многочисленных микроорганизмов, существующих в окружающей среде • Пробретённый (индуцированный, специфический) иммунитет - возникает после перенесённой инфекции или специфической вакцинации
Два типа иммунитета • Врождённый иммунитет - защищает от многочисленных микроорганизмов, существующих в окружающей среде • Пробретённый (индуцированный, специфический) иммунитет - возникает после перенесённой инфекции или специфической вакцинации
 Главные факторы врождённого иммунитета • • Фагоциты (макрофаги, нейтрофилы) Нормальные киллеры (НК) Система комплемента Цитокины – Интерлейкины – Интерфероны (защита от вирусов) – Фактор некроза опухолей • Регуляция врождённого иммунитета через toll- и Nod-подобные рецепторы (ТLR и NLR)
Главные факторы врождённого иммунитета • • Фагоциты (макрофаги, нейтрофилы) Нормальные киллеры (НК) Система комплемента Цитокины – Интерлейкины – Интерфероны (защита от вирусов) – Фактор некроза опухолей • Регуляция врождённого иммунитета через toll- и Nod-подобные рецепторы (ТLR и NLR)
 Главные факторы специфического иммунитета • В-лимфоциты (образование антител, специфический гуморальный иммунитет) • Т-лимфоциты (образование цитотоксических лимфоцитов – ЦТЛ, специфический клеточный иммунитет)
Главные факторы специфического иммунитета • В-лимфоциты (образование антител, специфический гуморальный иммунитет) • Т-лимфоциты (образование цитотоксических лимфоцитов – ЦТЛ, специфический клеточный иммунитет)
 Вакцины • Препараты, предназначенные для индукции активного специфического иммунитета у человека и животных • Первая вакцина (против оспы) была создана Эдвардом Дженнером в 1796 г. • Термин «вакцина» был предложен Луи Пастером (от лат. «vacca» – корова)
Вакцины • Препараты, предназначенные для индукции активного специфического иммунитета у человека и животных • Первая вакцина (против оспы) была создана Эдвардом Дженнером в 1796 г. • Термин «вакцина» был предложен Луи Пастером (от лат. «vacca» – корова)
 Вакцины • Главное свойство вакцины – специфически защищать чувствительный организм от инфекции и заболевания
Вакцины • Главное свойство вакцины – специфически защищать чувствительный организм от инфекции и заболевания
 Протективные антигены • Возбудитель обычно содержит много белков – антигенов • Иммунный ответ на некоторые из них защищает организм от инфекции • Такие антигены называются протективными антигенами • Другие антигены возбудителя могут не влиять на развитие иммунитета
Протективные антигены • Возбудитель обычно содержит много белков – антигенов • Иммунный ответ на некоторые из них защищает организм от инфекции • Такие антигены называются протективными антигенами • Другие антигены возбудителя могут не влиять на развитие иммунитета
 Виды вакцин • Инактивированные вакцины • Субъединичные вакцины • Генноинженерные субъединичные вакцины • Живые вакцины • Генноинженерные живые вакцины • Пептидные вакцины • ДНК-вакцины
Виды вакцин • Инактивированные вакцины • Субъединичные вакцины • Генноинженерные субъединичные вакцины • Живые вакцины • Генноинженерные живые вакцины • Пептидные вакцины • ДНК-вакцины
 Инактивированные вакцины Вакцины, приготовленные из возбудителя заболевания, инактивированного так, чтобы его биологическая активность была устранена, а антигены сохранились. Примеры: вакцина против ящура, инактивированная вакцина против полиомиелита.
Инактивированные вакцины Вакцины, приготовленные из возбудителя заболевания, инактивированного так, чтобы его биологическая активность была устранена, а антигены сохранились. Примеры: вакцина против ящура, инактивированная вакцина против полиомиелита.
 Инактивированная вакцина Солка против полиомиелита • Вирус полиомиелита выращивается в перевиваемой культуре клеток почки зелёной мартышки (линия Vero) • Инактивация проводится с помощью формалина • Вирус сорбируется на гидроокиси алюминия Al(OH)3
Инактивированная вакцина Солка против полиомиелита • Вирус полиомиелита выращивается в перевиваемой культуре клеток почки зелёной мартышки (линия Vero) • Инактивация проводится с помощью формалина • Вирус сорбируется на гидроокиси алюминия Al(OH)3
 Достоинства инактивированных вакцин • Возможность приготовления вакцины при наличии известного и способного культивироваться возбудителя • Относительная стандартность препарата • Отсутствие серьёзных побочных эффектов (по крайней мере, у вирусных вакцин)
Достоинства инактивированных вакцин • Возможность приготовления вакцины при наличии известного и способного культивироваться возбудителя • Относительная стандартность препарата • Отсутствие серьёзных побочных эффектов (по крайней мере, у вирусных вакцин)
 Недостатки инактивированных вакцин • Наличие нежелательных примесей • Необходимость полной инактивации возбудителя • Высокая стоимость
Недостатки инактивированных вакцин • Наличие нежелательных примесей • Необходимость полной инактивации возбудителя • Высокая стоимость
 Субъединичные вакцины • Вакцины, которые приготовлены из изолированных протективных антигенов возбудителя • Отличаются большей чистотой и безопасностью • Имеют высокую стоимость
Субъединичные вакцины • Вакцины, которые приготовлены из изолированных протективных антигенов возбудителя • Отличаются большей чистотой и безопасностью • Имеют высокую стоимость
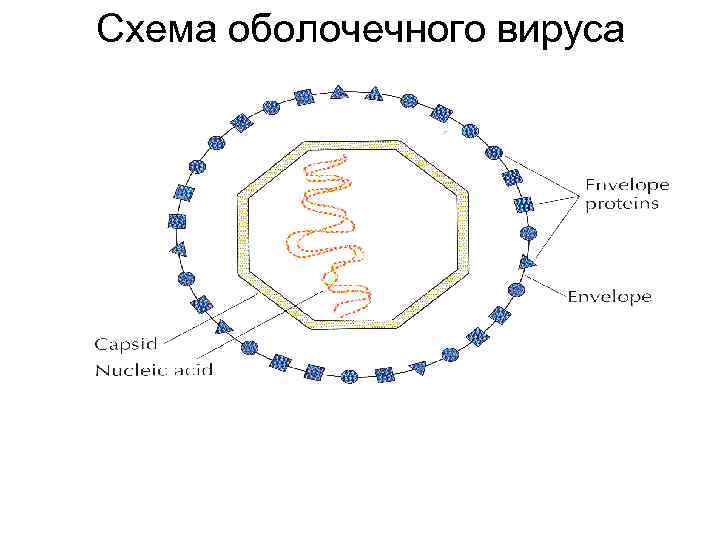 Схема оболочечного вируса
Схема оболочечного вируса
 Генноинженерные субъединичные вакцины • Ген, кодирующий протективный антиген возбудителя, вставляется в плазмиду под контроль сильного промотора • Антиген нарабатывается в соответствующей биологической системе (E. coli, дрожжи или клетки в культуре) • Антиген очищается от примесей, контролируется и используется для иммунизации как субъединичная вакцина
Генноинженерные субъединичные вакцины • Ген, кодирующий протективный антиген возбудителя, вставляется в плазмиду под контроль сильного промотора • Антиген нарабатывается в соответствующей биологической системе (E. coli, дрожжи или клетки в культуре) • Антиген очищается от примесей, контролируется и используется для иммунизации как субъединичная вакцина
 Вакцина против гепатита В – триумф молекулярной биотехнологии • Гепатит В – тяжёлое поражение печени (гепатит, цирроз, рак), вызываемое гепаднавирусом • Протективным антигеном вируса гепатита В (HBV) является поверхностный антиген HBs. Ag • HBV не размножается в культуре клеток
Вакцина против гепатита В – триумф молекулярной биотехнологии • Гепатит В – тяжёлое поражение печени (гепатит, цирроз, рак), вызываемое гепаднавирусом • Протективным антигеном вируса гепатита В (HBV) является поверхностный антиген HBs. Ag • HBV не размножается в культуре клеток
 Генноинженерные подходы к созданию вакцины против гепатита В • Ген HBs. Ag был экспрессирован в E. coli, но полученный антиген не был протективным из-за неправильной сборки • Экспрессия этого гена в дрожжах позволила получить активный антиген • Генноинженерная вакцина против гепатита В используется во всем мире
Генноинженерные подходы к созданию вакцины против гепатита В • Ген HBs. Ag был экспрессирован в E. coli, но полученный антиген не был протективным из-за неправильной сборки • Экспрессия этого гена в дрожжах позволила получить активный антиген • Генноинженерная вакцина против гепатита В используется во всем мире
 Метилотрофные дрожжи • Метилотрофные дрожжи используют метиловый спирт в качестве источника углерода • Они накапливаются в большом количестве • Удобны для наработки рекомбинантных белков под контролем промотора гена алкоголь-оксидазы (АОХ 1)
Метилотрофные дрожжи • Метилотрофные дрожжи используют метиловый спирт в качестве источника углерода • Они накапливаются в большом количестве • Удобны для наработки рекомбинантных белков под контролем промотора гена алкоголь-оксидазы (АОХ 1)
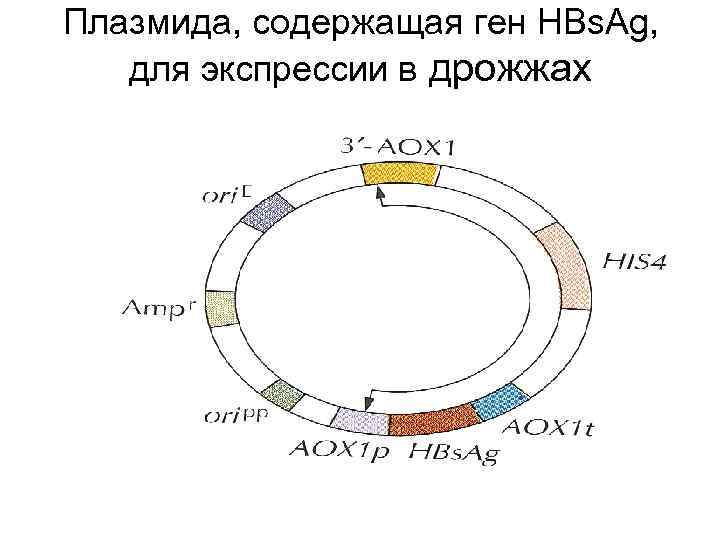 Плазмида, содержащая ген HBs. Ag, для экспрессии в дрожжах
Плазмида, содержащая ген HBs. Ag, для экспрессии в дрожжах
 Живые вакцины • Вакцины из живых возбудителей, утративших свою болезнетворность • Их характеризует максимальная эффективность, удобство применения, низкая стоимость • Недостатки таких вакцин – остаточная вирулентность и возможность загрязнения посторонними вирусами
Живые вакцины • Вакцины из живых возбудителей, утративших свою болезнетворность • Их характеризует максимальная эффективность, удобство применения, низкая стоимость • Недостатки таких вакцин – остаточная вирулентность и возможность загрязнения посторонними вирусами
 Принципы получения аттенуированных (ослабленных) возбудителей • Подбор природных вариантов возбудителя с ослабленной вирулентностью • Культивирование возбудителя в необычных условиях • Сочетание обоих подходов • Направленный мутагенез с помощью методов генетической инженерии
Принципы получения аттенуированных (ослабленных) возбудителей • Подбор природных вариантов возбудителя с ослабленной вирулентностью • Культивирование возбудителя в необычных условиях • Сочетание обоих подходов • Направленный мутагенез с помощью методов генетической инженерии
 Получение аттенуированных возбудителей с помощью генетической инженерии • Изучение молекулярных основ патогенности возбудителей позволяет выявить гены, повреждение которых ведёт к аттенуированному фенотипу • Избирательное удаление или повреждение определённого гена является делом генноинженерной техники • Таким образом, возникает возможность целенаправленно аттенуировать практически любой возбудитель (особенно вирус)
Получение аттенуированных возбудителей с помощью генетической инженерии • Изучение молекулярных основ патогенности возбудителей позволяет выявить гены, повреждение которых ведёт к аттенуированному фенотипу • Избирательное удаление или повреждение определённого гена является делом генноинженерной техники • Таким образом, возникает возможность целенаправленно аттенуировать практически любой возбудитель (особенно вирус)
 Примеры живых вакцин • • • Вакцина против кори Вакцина против полиомиелита Вакцина против оспы Вакцина против болезни Марека кур Вакцина против псевдобешенства свиней
Примеры живых вакцин • • • Вакцина против кори Вакцина против полиомиелита Вакцина против оспы Вакцина против болезни Марека кур Вакцина против псевдобешенства свиней
 Программы ВОЗ по искоренению инфекционных заболеваний • Оспа • Полиомиелит • Корь
Программы ВОЗ по искоренению инфекционных заболеваний • Оспа • Полиомиелит • Корь
 Живая вакцина против полиомиелита • Существуют три типа полиовируса – I, III. • В 50 -е г. г. А. Сэбин создал аттенуированные варианты Сэбин I, Сэбин III • Советские исследователи М. Чумаков и А. Смородинцев внедрили эту вакцину в СССР, затем она была внедрена во всём мире
Живая вакцина против полиомиелита • Существуют три типа полиовируса – I, III. • В 50 -е г. г. А. Сэбин создал аттенуированные варианты Сэбин I, Сэбин III • Советские исследователи М. Чумаков и А. Смородинцев внедрили эту вакцину в СССР, затем она была внедрена во всём мире
 Живая вакцина против полиомиелита • Вакцину готовят из вируса, выращенного в культуре клеток почки зелёной мартышки (линия Vero) • Применяется перорально, защищает кишечник и центральную нервную систему • Тяжёлые осложнения редки (~ 1 на 1000000)
Живая вакцина против полиомиелита • Вакцину готовят из вируса, выращенного в культуре клеток почки зелёной мартышки (линия Vero) • Применяется перорально, защищает кишечник и центральную нервную систему • Тяжёлые осложнения редки (~ 1 на 1000000)
 Программа Всемирной Организации Здравоохранение по глобальной ликвидации полиомиелита Благодаря массивному применению живой вакцины, удалось прекратить циркуляцию диких полиовирусов в мире, за исключением Нигерии и Северной Индии
Программа Всемирной Организации Здравоохранение по глобальной ликвидации полиомиелита Благодаря массивному применению живой вакцины, удалось прекратить циркуляцию диких полиовирусов в мире, за исключением Нигерии и Северной Индии
 Получение вакцин с помощью генноинженерных рекомбинантных вирусов Генноинженерные рекомбинанты вирусов - это вирусы, в геном которых введён чужеродный генетический материал с помощью методов генетической инженерии
Получение вакцин с помощью генноинженерных рекомбинантных вирусов Генноинженерные рекомбинанты вирусов - это вирусы, в геном которых введён чужеродный генетический материал с помощью методов генетической инженерии
 Получение вакцин с помощью генноинженерных рекомбинантных вирусов • Вводя чужеродные протективные гены в аттенуированные вирусы можно получить рекомбинант, способный вакцинировать против возбудителя, из которого получен ген протективного антигена • Хорошим примером этого подхода является вирус осповакцины и его генноинженерные рекомбинанты
Получение вакцин с помощью генноинженерных рекомбинантных вирусов • Вводя чужеродные протективные гены в аттенуированные вирусы можно получить рекомбинант, способный вакцинировать против возбудителя, из которого получен ген протективного антигена • Хорошим примером этого подхода является вирус осповакцины и его генноинженерные рекомбинанты
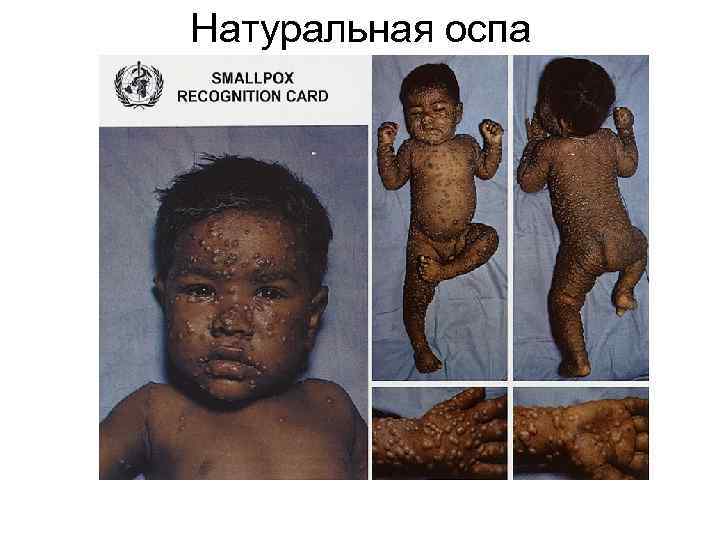 Натуральная оспа
Натуральная оспа
 Вирион
Вирион
 Программа ВОЗ по искоренению натуральной оспы • С помощью живой вакцины против оспы вирус натуральной оспы в 1977 г. прекратил существование, сохранившись только в лабораториях
Программа ВОЗ по искоренению натуральной оспы • С помощью живой вакцины против оспы вирус натуральной оспы в 1977 г. прекратил существование, сохранившись только в лабораториях
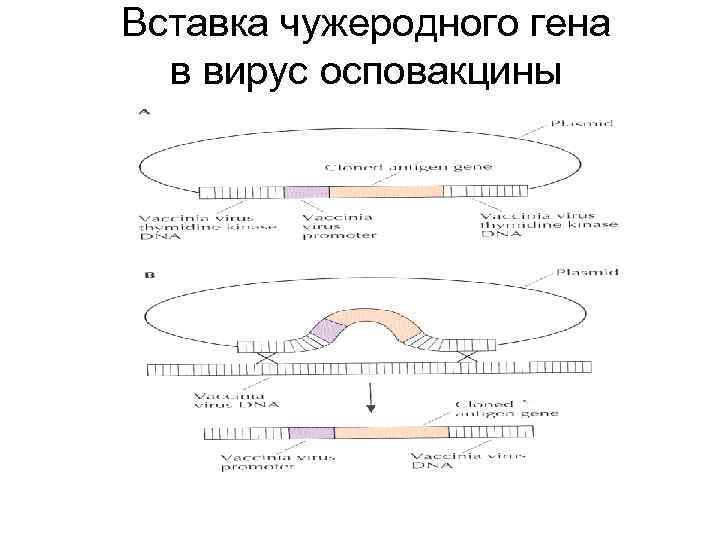 Вставка чужеродного гена в вирус осповакцины
Вставка чужеродного гена в вирус осповакцины
 Селекция рекомбинантов вируса осповакцины • Встройка чужеродного гена в ген тимидинкиназы меняет фенотип вируса от tk+ к tk • tk- вирус образует бляшки в tk- клетках в присутствии 5 -бром-2’-дезоксиуридина • Такие бляшки можно отобрать и определить встройку чужеродного гена различными методами (дот-гибридизация, блотгибридизация по Саузерну, ПЦР, обнаружение продуктов экспрессии встроенного гена)
Селекция рекомбинантов вируса осповакцины • Встройка чужеродного гена в ген тимидинкиназы меняет фенотип вируса от tk+ к tk • tk- вирус образует бляшки в tk- клетках в присутствии 5 -бром-2’-дезоксиуридина • Такие бляшки можно отобрать и определить встройку чужеродного гена различными методами (дот-гибридизация, блотгибридизация по Саузерну, ПЦР, обнаружение продуктов экспрессии встроенного гена)
 Протективные гены, вставленные в вирус осповакцины • Ген HBs. Ag вируса гепатита В • Ген оболочечного антигена вируса бычьего лейкоза • Протективные гены вируса гриппа • Ген белка оболочки вируса бешенства • Ген белка оболочки вируса лейкоза кошек • Многие другие
Протективные гены, вставленные в вирус осповакцины • Ген HBs. Ag вируса гепатита В • Ген оболочечного антигена вируса бычьего лейкоза • Протективные гены вируса гриппа • Ген белка оболочки вируса бешенства • Ген белка оболочки вируса лейкоза кошек • Многие другие
 Пептидные вакцины • Иммунногенным действием обладает не весь белок, а его определённые участки – антигенные детерминанты • Антигенные детерминанты бывают секвенальными и конформационными • Секвенальные детерминанты можно синтезировать из аминокислот с помощью автоматических синтезаторов
Пептидные вакцины • Иммунногенным действием обладает не весь белок, а его определённые участки – антигенные детерминанты • Антигенные детерминанты бывают секвенальными и конформационными • Секвенальные детерминанты можно синтезировать из аминокислот с помощью автоматических синтезаторов
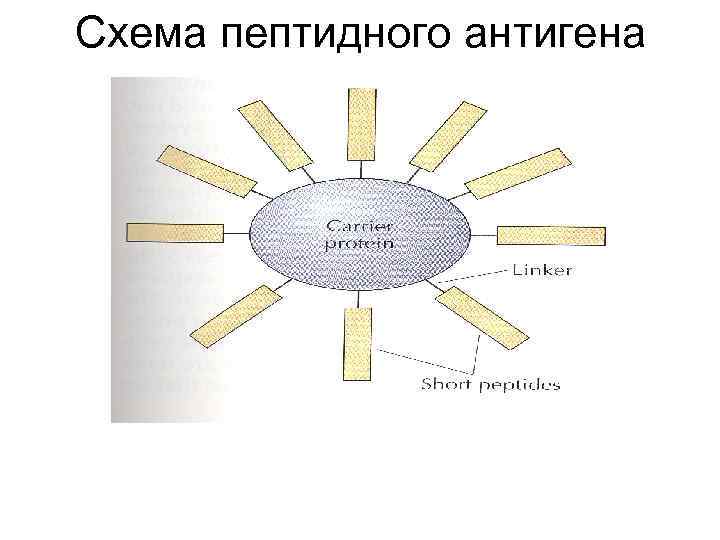 Схема пептидного антигена
Схема пептидного антигена
 ДНК-вакцинация • Вакцинация с помощью плазмиды, несущей протективный ген под контролем эукариотического промотора • При внутримышечном введении такой плазмиды происходит экспрессия гена, образуется белок, на который развивается иммунный ответ как Вклеточный (антитела), так и особенно Тклеточный (ЦТЛ)
ДНК-вакцинация • Вакцинация с помощью плазмиды, несущей протективный ген под контролем эукариотического промотора • При внутримышечном введении такой плазмиды происходит экспрессия гена, образуется белок, на который развивается иммунный ответ как Вклеточный (антитела), так и особенно Тклеточный (ЦТЛ)
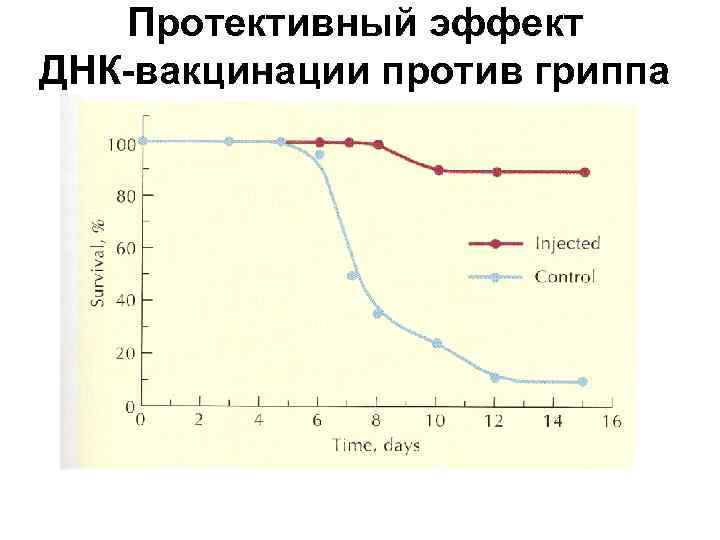 Протективный эффект ДНК-вакцинации против гриппа
Протективный эффект ДНК-вакцинации против гриппа
 Диагностика инфекционных заболеваний Для диагностики широко используют возможности молекулярной биотехнологии: • Антигены, полученные методами генетической инженерии • Моноклональные антитела, полученные методами клеточной инженерии • Полимеразную цепную реакцию (ПЦР)
Диагностика инфекционных заболеваний Для диагностики широко используют возможности молекулярной биотехнологии: • Антигены, полученные методами генетической инженерии • Моноклональные антитела, полученные методами клеточной инженерии • Полимеразную цепную реакцию (ПЦР)
 Диагностика ВИЧ–ифекции • Выявление антител к ВИЧ с использованием рекомбинантных антигенов иммуноферментным методом и вестерн-блотом • ПЦР для обнаружения ДНК-провируса ВИЧ
Диагностика ВИЧ–ифекции • Выявление антител к ВИЧ с использованием рекомбинантных антигенов иммуноферментным методом и вестерн-блотом • ПЦР для обнаружения ДНК-провируса ВИЧ
 Молекулярная биотехнология и проблема биобезопасности
Молекулярная биотехнология и проблема биобезопасности

 Основной подход молекулярной биотехнологии – вмешательство в генетическую систему организмов
Основной подход молекулярной биотехнологии – вмешательство в генетическую систему организмов
 1973 г. – Стэнли Коэн и Герберт Бойер с сотрудниками описали стратегию встраивания чужеродной ДНК в плазмиду. Это сделало возможным получение организмов, несущих чужеродные для себя гены.
1973 г. – Стэнли Коэн и Герберт Бойер с сотрудниками описали стратегию встраивания чужеродной ДНК в плазмиду. Это сделало возможным получение организмов, несущих чужеродные для себя гены.
 ВОЗМОЖНОСТИ МОЛЕКУЛЯРНОЙ БИОТЕХНОЛОГИИ - Резкая стимуляция научных исследований. Создание микроорганизмов, продуцирующих различные химические соединения, антибиотики, полимеры, биологически активные вещества (БАВ), ферменты и др. Получение вакцин и диагностикумов. Создание новых методов диагностики, профилактики и лечения инфекционных и генетических заболеваний. Повышение урожайности с/х культур путём создания растений, устойчивых к вредителям, инфекционным агентам и вредным воздействиям окружающей среды. Создание пород с/х и других животных с улучшенными показателями продуктивности, устойчивых к инфекционным заболеваниям. Получение пищи. Переработка отходов, загрязняющих окружающую среду.
ВОЗМОЖНОСТИ МОЛЕКУЛЯРНОЙ БИОТЕХНОЛОГИИ - Резкая стимуляция научных исследований. Создание микроорганизмов, продуцирующих различные химические соединения, антибиотики, полимеры, биологически активные вещества (БАВ), ферменты и др. Получение вакцин и диагностикумов. Создание новых методов диагностики, профилактики и лечения инфекционных и генетических заболеваний. Повышение урожайности с/х культур путём создания растений, устойчивых к вредителям, инфекционным агентам и вредным воздействиям окружающей среды. Создание пород с/х и других животных с улучшенными показателями продуктивности, устойчивых к инфекционным заболеваниям. Получение пищи. Переработка отходов, загрязняющих окружающую среду.
 Генотерапия • Устранение патологических генетических дефектов у человека путём введения генетических конструкций (применение рекомбинантных вирусов и стволовых клеток) • Вмешательство в генетику человека на ранних этапах развития организма
Генотерапия • Устранение патологических генетических дефектов у человека путём введения генетических конструкций (применение рекомбинантных вирусов и стволовых клеток) • Вмешательство в генетику человека на ранних этапах развития организма
 Последствия достижений молекулярной биотехнологии • • Биомедицинские Экономические Социальные Этические
Последствия достижений молекулярной биотехнологии • • Биомедицинские Экономические Социальные Этические
 Биобезопасность – защищённость людей, с/х животных и растений, окружающей среды от вредного воздействия, опасного для их жизни и здоровья, не допускающая неблагоприятных экологических последствий при эффективном использовании достижений генетической инженерии и биотехнологии.
Биобезопасность – защищённость людей, с/х животных и растений, окружающей среды от вредного воздействия, опасного для их жизни и здоровья, не допускающая неблагоприятных экологических последствий при эффективном использовании достижений генетической инженерии и биотехнологии.
 1975 г. - Первая попытка оценки риска от экспериментов с рекомбинантными ДНК и разработка мер безопасности проведении лабораторных исследований (Асиломарская конференция в Калифорнии). 1976 г. - Национальные институты здравоохранения США (National Institutes of Health, NIH) разработали директиву, регламентирующую проведение всех экспериментов с рекомбинантной ДНК, и ввели мораторий на работы, включающие использование патогенных микроорганизмов.
1975 г. - Первая попытка оценки риска от экспериментов с рекомбинантными ДНК и разработка мер безопасности проведении лабораторных исследований (Асиломарская конференция в Калифорнии). 1976 г. - Национальные институты здравоохранения США (National Institutes of Health, NIH) разработали директиву, регламентирующую проведение всех экспериментов с рекомбинантной ДНК, и ввели мораторий на работы, включающие использование патогенных микроорганизмов.
 1980 г. - Смягчение первоначальных директив. - Появление патогенного микроорганизма было признано маловероятным, если использованный для клонирования ген не отвечает за патогенные свойства того организма, из которого он был выделен. -Были добавлены специальные правила, предотвращающие выброс ГМО в окружающую среду. 1992 г. – 193 государства-члена ООН подписали Конвенцию по биоразнообразию о намерениях принимать меры по исключению вредного влияния современной биотехнологии на здоровье человека и окружающую среду (конференция в Рио-де. Жанейро).
1980 г. - Смягчение первоначальных директив. - Появление патогенного микроорганизма было признано маловероятным, если использованный для клонирования ген не отвечает за патогенные свойства того организма, из которого он был выделен. -Были добавлены специальные правила, предотвращающие выброс ГМО в окружающую среду. 1992 г. – 193 государства-члена ООН подписали Конвенцию по биоразнообразию о намерениях принимать меры по исключению вредного влияния современной биотехнологии на здоровье человека и окружающую среду (конференция в Рио-де. Жанейро).
 2002 г. – Был принят «Картахенский протокол» международное соглашение о регулировании трансграничного перемещения живых модифицированных организмов. Цель протокола - обеспечение надлежащего уровня защиты в области безопасной передачи, обработки и использования живых изменённых организмов (ЖИО), являющихся результатом применения современной биотехнологии и способных оказать неблагоприятное воздействие на сохранение и устойчивое использование биоразнообразия, с учётом рисков для здоровья человека (ст. 1 протокола).
2002 г. – Был принят «Картахенский протокол» международное соглашение о регулировании трансграничного перемещения живых модифицированных организмов. Цель протокола - обеспечение надлежащего уровня защиты в области безопасной передачи, обработки и использования живых изменённых организмов (ЖИО), являющихся результатом применения современной биотехнологии и способных оказать неблагоприятное воздействие на сохранение и устойчивое использование биоразнообразия, с учётом рисков для здоровья человека (ст. 1 протокола).
 Подходы к проблеме биобезопасности 1. Молекулярная биотехнология не несёт никакой опасности. 2. Молекулярная биотехнология настолько опасна, что должна быть запрещена. 3. Молекулярная биотехнология необходима человечеству, но может нести риск неблагоприятного воздействия на человека и на природу и нуждается в определённой регламентации.
Подходы к проблеме биобезопасности 1. Молекулярная биотехнология не несёт никакой опасности. 2. Молекулярная биотехнология настолько опасна, что должна быть запрещена. 3. Молекулярная биотехнология необходима человечеству, но может нести риск неблагоприятного воздействия на человека и на природу и нуждается в определённой регламентации.
 ОСНОВНЫЕ РИСКИ ДЛЯ ЧЕЛОВЕКА • Неблагоприятное воздействие генноинженерных продуктов (рекомбинантные белки, вакцины, лекарственные препараты) на организм человека при длительном применении: - токсичность, - онкогенез, - тератогенез, - нарушения иммунитета, - генетические нарушения • Неэффективность лечения многих заболеваний антибиотиками вследствие заимствования бактериями кишечника человека фрагментов ДНК из клеток генетически модифицированной пищи.
ОСНОВНЫЕ РИСКИ ДЛЯ ЧЕЛОВЕКА • Неблагоприятное воздействие генноинженерных продуктов (рекомбинантные белки, вакцины, лекарственные препараты) на организм человека при длительном применении: - токсичность, - онкогенез, - тератогенез, - нарушения иммунитета, - генетические нарушения • Неэффективность лечения многих заболеваний антибиотиками вследствие заимствования бактериями кишечника человека фрагментов ДНК из клеток генетически модифицированной пищи.
 ПРОБЛЕМА ИСПОЛЬЗОВАНИЯ РЕКОМБИНАНТНЫХ БЕЛКОВ • • • Интерфероны (α, β, γ) Инсулин HBs. Ag Тканевой активатор плазминогена Урокиназа Гормон роста
ПРОБЛЕМА ИСПОЛЬЗОВАНИЯ РЕКОМБИНАНТНЫХ БЕЛКОВ • • • Интерфероны (α, β, γ) Инсулин HBs. Ag Тканевой активатор плазминогена Урокиназа Гормон роста
 Тесты • • • Острая токсичность Хроническая токсичность Онкогенез Тератогенез Клинические исследования
Тесты • • • Острая токсичность Хроническая токсичность Онкогенез Тератогенез Клинические исследования
 История с триптофаном • Генноинженерный триптофан вызвал у потребителей синдром эозинофилиимиалгии (1989 -1990 гг. ) • Причиной оказалась примесь [этиленбистриптофан (EBT)], не удалявшаяся из-за изменения метода очистки
История с триптофаном • Генноинженерный триптофан вызвал у потребителей синдром эозинофилиимиалгии (1989 -1990 гг. ) • Причиной оказалась примесь [этиленбистриптофан (EBT)], не удалявшаяся из-за изменения метода очистки
 История с бычьим соматотропином (гормоном роста) • Введение этого гормона коровам повышает надои молока на 20 -25% • Возражение: у коров повысится частота маститов, их будут лечить антибиотиками, которые попадут в молоко (не подтвердилось) • Повышение надоев приведёт к разорению мелких ферм
История с бычьим соматотропином (гормоном роста) • Введение этого гормона коровам повышает надои молока на 20 -25% • Возражение: у коров повысится частота маститов, их будут лечить антибиотиками, которые попадут в молоко (не подтвердилось) • Повышение надоев приведёт к разорению мелких ферм
 НАРУШЕНИЕ БИОРАЗНООБРАЗИЯ • Вытеснение обычных видов растений, животных и микроорганизмов генетически модифицированными. • Растения, устойчивые к вредителям, могут представлять опасность для полезных насекомых. • Неконтролируемая передача трансгенов может привести к возникновению новых организмов с опасными для человека и окружающей среды свойствами (в частности, к появлению сорняков, устойчивых к гербицидам и насекомым). • Уменьшение сортового и видового разнообразия с/х культур вследствие внедрения более урожайных и более рентабельных сортов трансгенных растений.
НАРУШЕНИЕ БИОРАЗНООБРАЗИЯ • Вытеснение обычных видов растений, животных и микроорганизмов генетически модифицированными. • Растения, устойчивые к вредителям, могут представлять опасность для полезных насекомых. • Неконтролируемая передача трансгенов может привести к возникновению новых организмов с опасными для человека и окружающей среды свойствами (в частности, к появлению сорняков, устойчивых к гербицидам и насекомым). • Уменьшение сортового и видового разнообразия с/х культур вследствие внедрения более урожайных и более рентабельных сортов трансгенных растений.
 Возможно ли изменение патогенности и вирулентности генетически модифицированных микроорганизмов (ГММ)? • Чаще всего вирулентность ГММ снижается • Однако описаны случаи повышения вирулентности ГММ
Возможно ли изменение патогенности и вирулентности генетически модифицированных микроорганизмов (ГММ)? • Чаще всего вирулентность ГММ снижается • Однако описаны случаи повышения вирулентности ГММ
 Намеренное освобождение трансгенных организмов в окружающую среду • Живые вакцины • Посевы трансгенных растений • Бактериальные и вирусные пестициды (B. thuringiensis, бакуловирусы) • Бактерии, уничтожающие загрязнение окружающей среды нефтью, фенолом и др.
Намеренное освобождение трансгенных организмов в окружающую среду • Живые вакцины • Посевы трансгенных растений • Бактериальные и вирусные пестициды (B. thuringiensis, бакуловирусы) • Бактерии, уничтожающие загрязнение окружающей среды нефтью, фенолом и др.
 Неконтролируемая передача устойчивости к антибиотикам • Удаление маркерных генов из рекомбинантных организмов (трансгенных вирусов, животных, растений) генетическими методами
Неконтролируемая передача устойчивости к антибиотикам • Удаление маркерных генов из рекомбинантных организмов (трансгенных вирусов, животных, растений) генетическими методами
 Штамм Е. coli K 12 • • • Это мутант кишечной палочки Не имеет патогенных свойств Не способен выжить в окружающей среде Не способен заразить человека Хорошо охарактеризован генетически
Штамм Е. coli K 12 • • • Это мутант кишечной палочки Не имеет патогенных свойств Не способен выжить в окружающей среде Не способен заразить человека Хорошо охарактеризован генетически
 ТРАНСГЕННЫЕ ЖИВОТНЫЕ • Мыши, чувствительные к вирусу полиомиелита, должны тщательно оберегаться от случайного ухода в окружающую среду, чтобы не создать природный очаг для полиовирусной инфекции
ТРАНСГЕННЫЕ ЖИВОТНЫЕ • Мыши, чувствительные к вирусу полиомиелита, должны тщательно оберегаться от случайного ухода в окружающую среду, чтобы не создать природный очаг для полиовирусной инфекции
 ТРАНСГЕННЫЕ РАСТЕНИЯ • Устойчивость к пестицидам, гербицидам, вирусам, грибам, бактериям, стрессам и другие свойства • Экономическая целесообразность ГМ растений
ТРАНСГЕННЫЕ РАСТЕНИЯ • Устойчивость к пестицидам, гербицидам, вирусам, грибам, бактериям, стрессам и другие свойства • Экономическая целесообразность ГМ растений
 Страны, выращивающие трансгенные растения • • • США Китай Бразилия Аргентина Ряд других стран
Страны, выращивающие трансгенные растения • • • США Китай Бразилия Аргентина Ряд других стран
 Пища Франкенштейна? ? ? • Гены пищевого сырья не изменяют генетическую природу человека и животных, потребляющих соответствующую пищу • Пища на основе трансгенных растений практически не отличается от пищи на основе растений, полученных в результате селекции • Вопрос об употреблении в пищу трансгенных продуктов является исключительно экономическим, а возражения имеют, в основном, психологическую и экономическую основу
Пища Франкенштейна? ? ? • Гены пищевого сырья не изменяют генетическую природу человека и животных, потребляющих соответствующую пищу • Пища на основе трансгенных растений практически не отличается от пищи на основе растений, полученных в результате селекции • Вопрос об употреблении в пищу трансгенных продуктов является исключительно экономическим, а возражения имеют, в основном, психологическую и экономическую основу
 Отношение к пище, содержащей трансгенные ингредиенты • В США не требуется маркировка и использование трансгенных продуктов не ограничивается • В большинстве стран требуется маркировка с указанием содержания трансгенного компонента
Отношение к пище, содержащей трансгенные ингредиенты • В США не требуется маркировка и использование трансгенных продуктов не ограничивается • В большинстве стран требуется маркировка с указанием содержания трансгенного компонента
 Ситуация в России • Обязательной является маркировка продуктов, содержащих генетически модифицированные ингредиенты (ГМИ) • Ведется активная компания против ГМИ в печати и рекламе • ГМИ используются по экономическим соображениям • Ведётся контроль за содержанием ГМИ в продуктах
Ситуация в России • Обязательной является маркировка продуктов, содержащих генетически модифицированные ингредиенты (ГМИ) • Ведется активная компания против ГМИ в печати и рекламе • ГМИ используются по экономическим соображениям • Ведётся контроль за содержанием ГМИ в продуктах
 ОБЕСПЕЧЕНИЕ БИОБЕЗОПАСНОСТИ 1. 2. 3. Использование природных генов, участвующих в процессах рекомбинации в течение длительного времени и обеспечивающих устойчивый характер репарации процессов биосинтеза белков. Разработка и использование эффективных методов мониторинга качества получаемых трансгенных организмов, свойств белковых и других компонентов вновь созданных генотипов. Это позволяет выявить опасные для человека и окружающей среды генотипы на раннем этапе исследований и не допустить их выхода в биосферу. Отбор и использование проверенных регуляторных генетических структур и создание на их основе векторов, обеспечивающих получение трансгенов с заданными свойствами.
ОБЕСПЕЧЕНИЕ БИОБЕЗОПАСНОСТИ 1. 2. 3. Использование природных генов, участвующих в процессах рекомбинации в течение длительного времени и обеспечивающих устойчивый характер репарации процессов биосинтеза белков. Разработка и использование эффективных методов мониторинга качества получаемых трансгенных организмов, свойств белковых и других компонентов вновь созданных генотипов. Это позволяет выявить опасные для человека и окружающей среды генотипы на раннем этапе исследований и не допустить их выхода в биосферу. Отбор и использование проверенных регуляторных генетических структур и создание на их основе векторов, обеспечивающих получение трансгенов с заданными свойствами.
 Контроль трансгенности и свойств трансгенной пищи • Контроль на наличие трансгенов - ПЦР (выявление промотора 35 S гена вируса мозаики цветной капусты и терминатора nos гена Тi-плазмиды) • Методы контроля токсичности и питательности пищи – длительные опыты на мышах и крысах
Контроль трансгенности и свойств трансгенной пищи • Контроль на наличие трансгенов - ПЦР (выявление промотора 35 S гена вируса мозаики цветной капусты и терминатора nos гена Тi-плазмиды) • Методы контроля токсичности и питательности пищи – длительные опыты на мышах и крысах
 • Регламентация генноинженерной деятельности и внедрения в практику рекомбинантных белков, трансгенных животных и растений, а также пищевых продуктов из них
• Регламентация генноинженерной деятельности и внедрения в практику рекомбинантных белков, трансгенных животных и растений, а также пищевых продуктов из них
 Контроль за внедрением рекомбинантных продуктов Система сан- и ветнадзора в России Федеральный Центр Сан. Эпид. Надзора Федеральная Служба фитосанитарного и ветеринарного надзора Комиссия по генноинженерной деятельности Институт питания РАМН
Контроль за внедрением рекомбинантных продуктов Система сан- и ветнадзора в России Федеральный Центр Сан. Эпид. Надзора Федеральная Служба фитосанитарного и ветеринарного надзора Комиссия по генноинженерной деятельности Институт питания РАМН


