Кислоты шерстобоева.ppt
- Количество слайдов: 35

КИСЛОТЫ Выполнила: Ученица 11 А класса Шерстобоева Екатерина

Что такое кислоты? • Сложные вещества, состоящие из атомов водорода, соединенных с кислотным остатком • Электролиты, диссоциирующие с образованием катионов водорода и анионов кислотного остатка

Классификация кислот Признаки классификации Группы кислот Примеры Наличие кислорода в кислотном остатке А) кислородные; Б) бескислородные А) H 3 PO 4, H 2 SO 4; , Б) HBr, H 2 S Основность А) одноосновные; Б) многоосновные А) HNO 3, HCl; Б) H 2 SO 4, H 3 PO 4 Растворимость в воде А) растворимые; Б) нерастворимые А) HNO 3, HCl; Б) H 2 Si. O 3 Летучесть А) летучие; Б) нелетучие А) H 2 S, HNO 3 Б) H 2 SO 4, H 3 PO 4 Степень диссоциации А) сильные; Б) слабые А) HNO 3, HCl; Б) H 2 SO 3, H 2 CO 3 Стабильность А) стабильные; Б) нестабильные А) H 2 SO 4, HCl Б) H 2 SO 3, H 2 CO 3
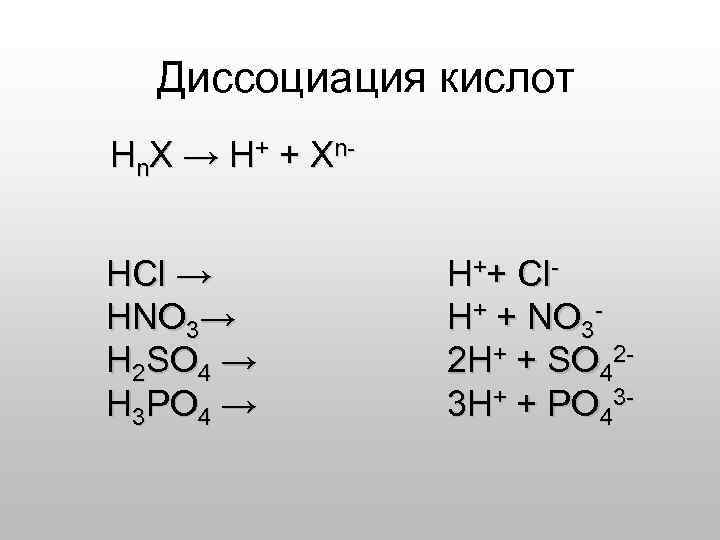
Диссоциация кислот Н n. X → Н + + X n. HCl → HNO 3→ H 2 SO 4 → H 3 PO 4 → H++ Cl. H+ + NO 32 H+ + SO 423 H+ + PO 43 -

Взаимодействие с индикаторами Индикатор Нейтральная Кислая среда Лакмус Фиолетовый Красный Фенолфталеи Бесцветный н Бесцветный Метиловый оранжевый Розовый Оранжевый Помни! Нерастворимые кислоты не меняют окраску индикаторов.

Взаимодействие с металлами Ме + Нn. X → Меn. Xm+ Н 2 металл + кислота→соль + водород 2 Al + 3 H 2 SO 4 → Al 2(SO 4)3 + 3 H 2 Реакция возможна, если: 1. Металл находится в ряду активности до водорода; 2. В результате реакции получается растворимая соль; 3. Кислота растворима
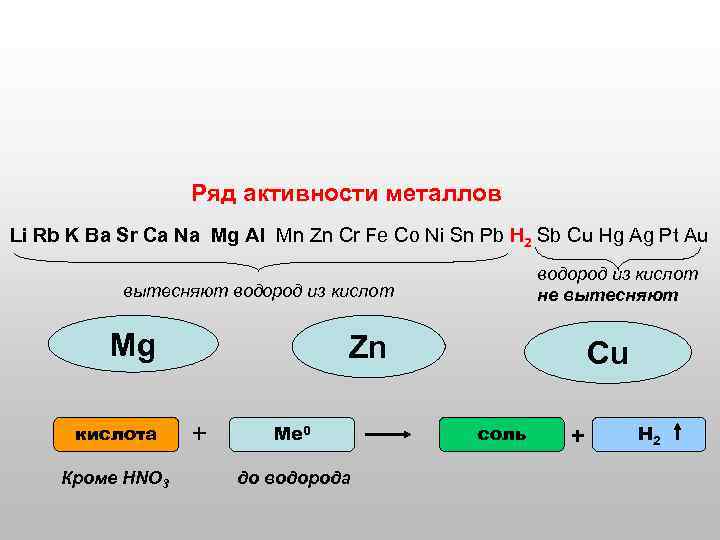
Ряд активности металлов Li Rb K Ba Sr Ca Na Mg Al Mn Zn Cr Fe Co Ni Sn Pb H 2 Sb Cu Hg Ag Pt Au водород из кислот не вытесняют водород из кислот Mg кислота Кроме HNO 3 Zn + Ме 0 до водорода Сu соль + Н 2

Взаимодействие с основными оксидами Меx. Oy + Hn. X → Меn. Xy + H 2 O Основный оксид + кислота → соль + вода Mg. O + 2 HCl → Mg. Cl 2 + H 2 O Mg. O + 2 H+ + 2 Cl- → Mg 2+ + 2 Cl- + H 2 O Mg. O + 2 H+ → Mg 2+ + H 2 O Реакция возможна, если в результате получается растворимая соль

Взаимодействие с основаниями Ме(ОН)m + Нn. X → Men. Xm + H 2 O Основание + кислота → соль + вода 3 Na. OH + H 3 PO 4→ Na 3 PO 4 + 3 H 2 O 3 Na+ + 3 OH- + 3 H+ + PO 43 - → 3 Na+ + PO 43 - + 3 H 2 O H+ + OH- → H 2 O Реакция между щелочью и кислотой с образованием соли и воды называется реакцией нейтрализации.

Взаимодействие с солями Меx. Xy + Hn. X → Hх. X + Меn. Xy Соль + кислота → новая кислота + новая соль 3 Li 2 CO 3 + 2 H 3 PO 4 → 2 Li 3 PO 4 + 3 H 2 O + 3 CO 2 6 Li+ + 3 CO 32 - + 6 H+ + PO 43 - → 6 Li+ + 2 PO 43 - + 3 H 2 O + 3 CO 2 2 H+ + CO 32 - → H 2 O + CO 2 Реакция возможна, если в результате образуется осадок, газ или слабый электролит Обратно ко всем свойствам
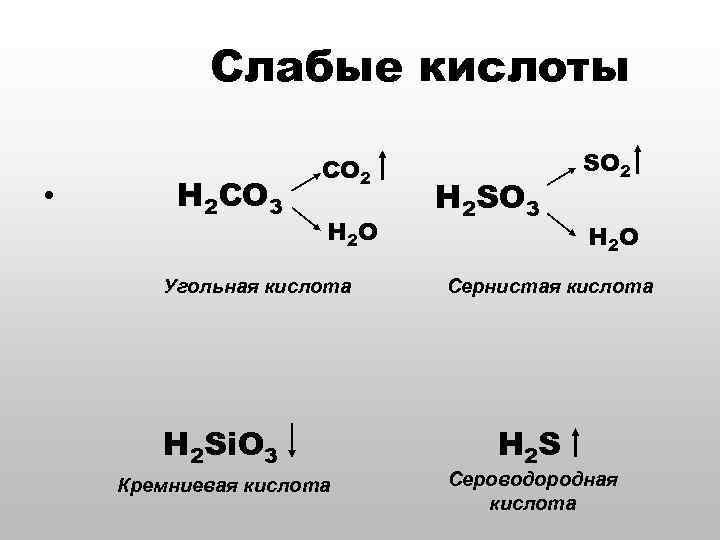
Слабые кислоты • H 2 CO 3 CO 2 H 2 O Угольная кислота H 2 Si. O 3 Кремниевая кислота H 2 SO 3 SO 2 H 2 O Сернистая кислота H 2 S Сероводородная кислота

Получение кислот Бескислородные кислоты • H 2 + Cl 2 = 2 HCl • Взаимодействие простых веществ. Кислородсодержащие кислоты • SO 3 + H 2 O = H 2 SO 4 • Взаимодействие кислотного оксида и воды. Na. Cl(тв. ) + H 2 SO 4 (конц. ) Na 2 SO 4 + 2 HCl Летучие кислоты могут быть вытеснены из солей менее летучими кислотами.

Пищевые кислоты • • Лимонная кислота содержится в лимонах. Яблочная- в яблоках. Щавелевая - в листьях щавеля. Муравьиная содержится в выделениях муравьев, пчелином яде и в жгучих волосках крапивы. Уксусная кислота образуется при скисании виноградного вина. Молочная – при скисании молока, квашении капусты и силосовании кормов для скота. Аскорбиновая( витамин С) - в черной смородине, малине, лимонах, апельсинах, томатах. Недостаток его в пище вызывает заболевание цынгу.

Технические кислоты Формула HCL H 2 S HBr HNO 3 HNO 2 H 2 SO 4 H 2 SO 3 H 2 CO 3 H 2 Si. O 3 H 3 PO 4 HF Название Хлороводородная (соляная) Сероводородная Бромоводородная Азотистая Сернистая Угольная Кремниевая Фосфорная Фтороводородная (плавиковая)

Представители кислот • Серная кислота Н 2 SО 4 • бесцветная вязкая жидкость, без запаха , вдвое тяжелее воды, поглощает влагу из воздуха и других газов, обугливает древесину, кожу, ткани, бумагу. • Для приготовления растворов запомните правило: • Сначала вода, потом кислота, Иначе случится большая беда! • По объему производства серной кислоты можно судить о развитии химической промышленности страны. • Серную кислоту называют «Хлебом» химической промышленности, ее используют практически во всех отраслях народного хозяйства.

Соляная кислота • Бесцветная, дымящаяся на воздухе жидкость, имеет специфический запах, несколько тяжелее воды. • Содержится в желудке и выполняет две функции: 1) Уничтожает микробов, которые попадают в желудок вместе с пищей. • 2) Помогает перевариванию пищи, так как входит в состав желудочного сока.

Карбоновые кислоты — класс органических соединений, молекулы которого содержат карбоксильную группу - COOH. Состав предельных одноосновных карбоновых кислот соответствует общей формуле О R–C OH.
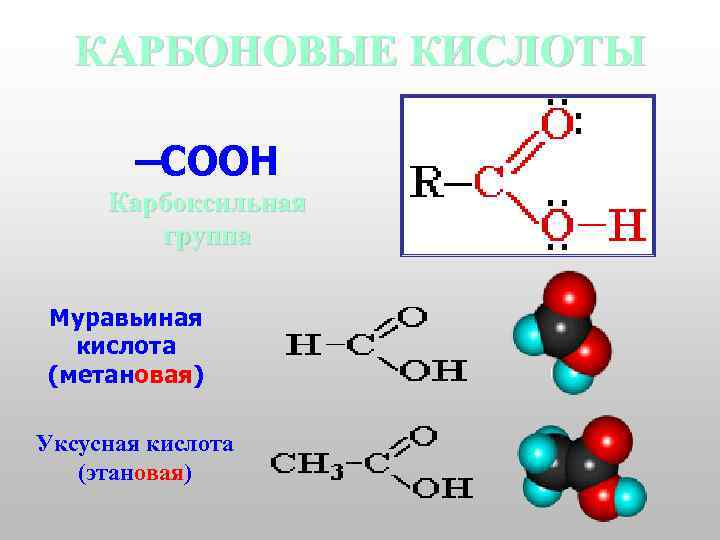
КАРБОНОВЫЕ КИСЛОТЫ –COOH Карбоксильная группа Муравьиная кислота (метановая) Уксусная кислота (этановая)
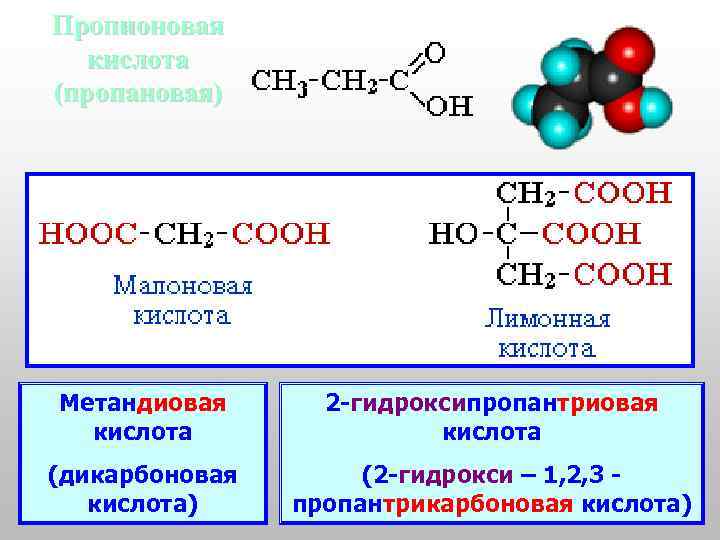
Пропионовая кислота (пропановая) Метандиовая кислота 2 -гидроксипропантриовая кислота (дикарбоновая кислота) (2 -гидрокси – 1, 2, 3 пропантрикарбоновая кислота)

Классификация По числу карбоксильных групп карбоновые кислоты делятся на: • монокарбоновые или одноосновные (уксусная кислота) • дикарбоновые или двухосновные (щавелевая кислота) В зависимости от строения углеводородного радикала, с которым связана карбоксильная группа, карбоновые кислоты делятся на: • алифатические ( уксусная или акриловая) • алициклические (циклогексанкарбоновая) • ароматические (бензойная, фталевая)
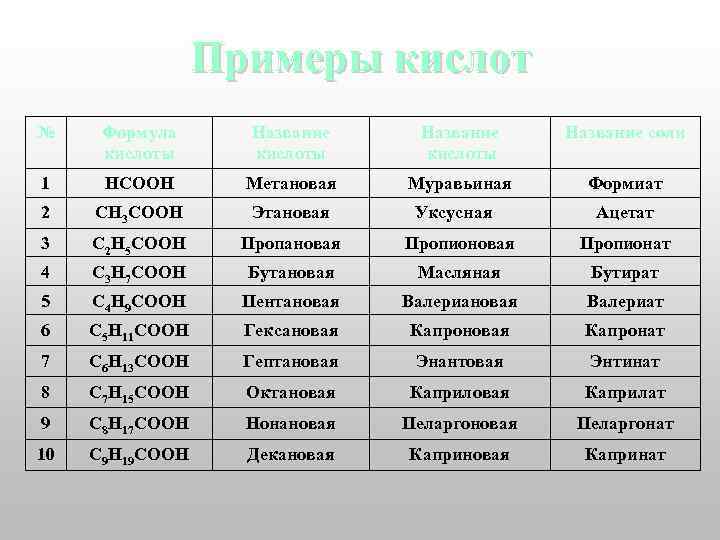
Примеры кислот № Формула кислоты Название соли 1 HCOOH Метановая Муравьиная Формиат 2 CH 3 COOH Этановая 3 C 2 H 5 COOH Пропановая Пропионат 4 C 3 H 7 COOH Бутановая Масляная Бутират 5 C 4 H 9 COOH Пентановая Валериат 6 C 5 H 11 COOH Гексановая Капронат 7 C 6 H 13 COOH Гептановая Энантовая Энтинат 8 C 7 H 15 COOH Октановая Каприлат 9 C 8 H 17 COOH Нонановая Пеларгонат 10 C 9 H 19 COOH Декановая Капринат Уксусная Ацетат
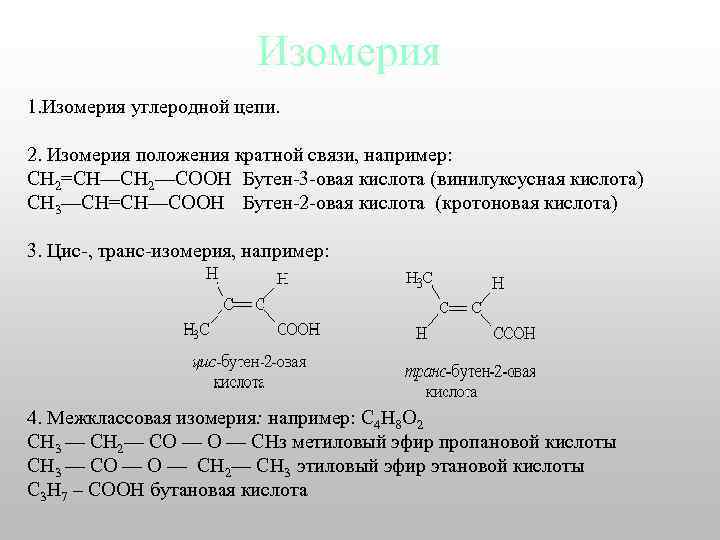
Изомерия 1. Изомерия углеродной цепи. 2. Изомерия положения кратной связи, например: СН 2=СН—СН 2—СООН Бутен-3 -овая кислота (винилуксусная кислота) СН 3—СН=СН—СООН Бутен-2 -овая кислота (кротоновая кислота) 3. Цис-, транс-изомерия, например: 4. Межклассовая изомерия: например: С 4 Н 8 О 2 СН 3 — СН 2— СО — СНз метиловый эфир пропановой кислоты СН 3 — СО — CH 2— СН 3 этиловый эфир этановой кислоты С 3 Н 7 – СООН бутановая кислота

Строение • Карбоксильная группа СООН состоит из карбонильной группы С=О и гидроксильной группы ОН. • В группе СО атом углерода несет частичный положительный заряд и притягивает к себе электронную пару атома кислорода в группе ОН. При этом электронная плотность на атоме кислорода уменьшается, и связь О-Н ослабляется: • В свою очередь, группа ОН "гасит" положительный заряд на группе СО.

Физические и химические свойства Низшие карбоновые кислоты — жидкости с острым запахом, хорошо растворимые в воде. С повышением относительной молекулярной массы растворимость кислот в воде уменьшается, а температура кипения повышается. Высшие кислоты, начиная с пеларгоновой С 8 Н 17 СООН — твердые вещества, без запаха, нерастворимые в воде. Наиболее важные химические свойства, характерные для большинства карбоновых кислот: 1) Взаимодействие с активными металлами: 2 CH 3 COOH + Mg (CH 2 COO)2 Mg + H 2 2) Взаимодействие с оксидами металлов: 2 СН 3 СООН + Са. О (СН 3 СОО)2 Са + Н 2 О
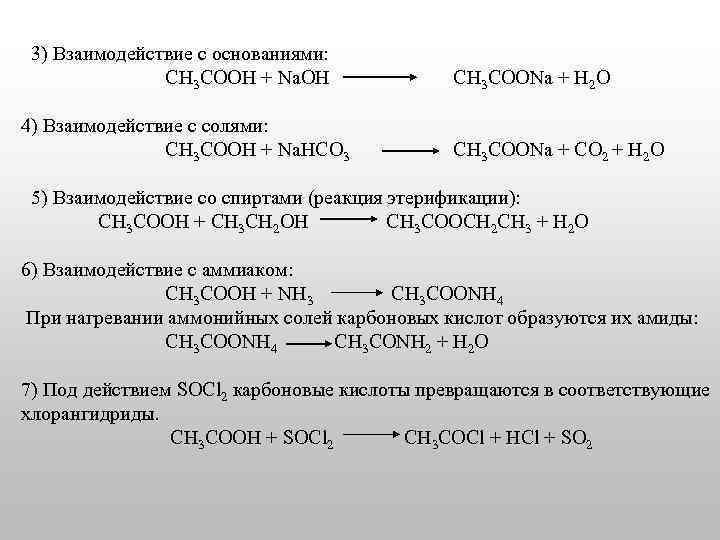
3) Взаимодействие с основаниями: CH 3 COOH + Na. OH 4) Взаимодействие с солями: CH 3 COOH + Na. HCO 3 CH 3 COONa + H 2 O CH 3 COONa + СО 2 + Н 2 О 5) Взаимодействие со спиртами (реакция этерификации): CH 3 COOH + СН 3 СН 2 ОН CH 3 COOСН 2 СН 3 + H 2 O 6) Взаимодействие с аммиаком: CH 3 COOH + NH 3 CH 3 COONH 4 При нагревании аммонийных солей карбоновых кислот образуются их амиды: CH 3 COONH 4 CH 3 CONH 2 + H 2 O 7) Под действием SOCl 2 карбоновые кислоты превращаются в соответствующие хлорангидриды. CH 3 COOH + SOCl 2 CH 3 COCl + HCl + SO 2
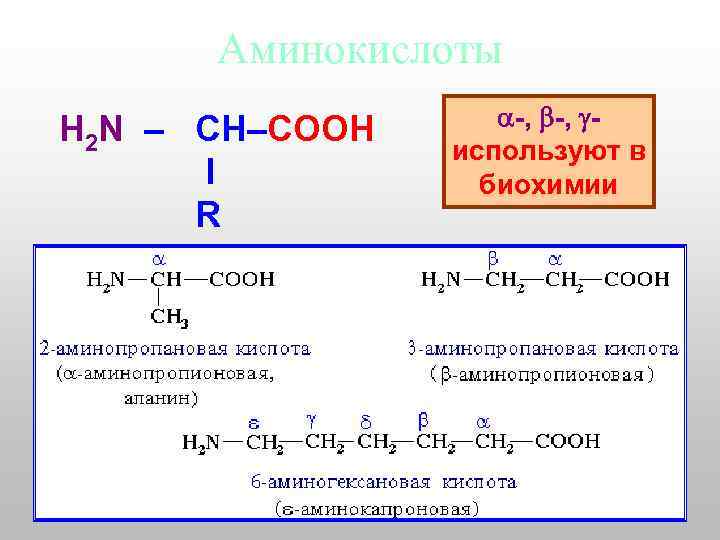
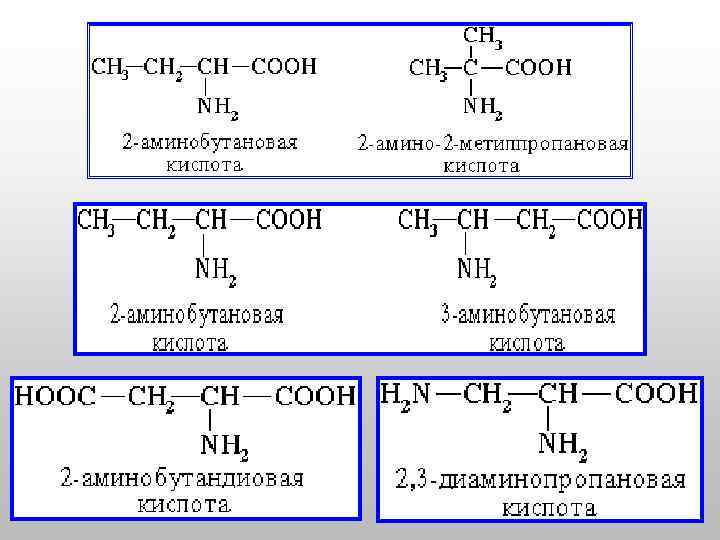
Аминокислоты H 2 N – CH–COOH I R a-, b-, g- используют в биохимии

Способы получения 1. Окисление альдегидов и первичных спиртов — общий способ получения карбоновых кислот: 2. Другой общий способ — гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода: -3 Na. Cl 3. Взаимодействие реактива Гриньяра с СО 2:

4. Гидролиз сложных эфиров: 5. Гидролиз ангидридов кислот:
O H C O H H C H H
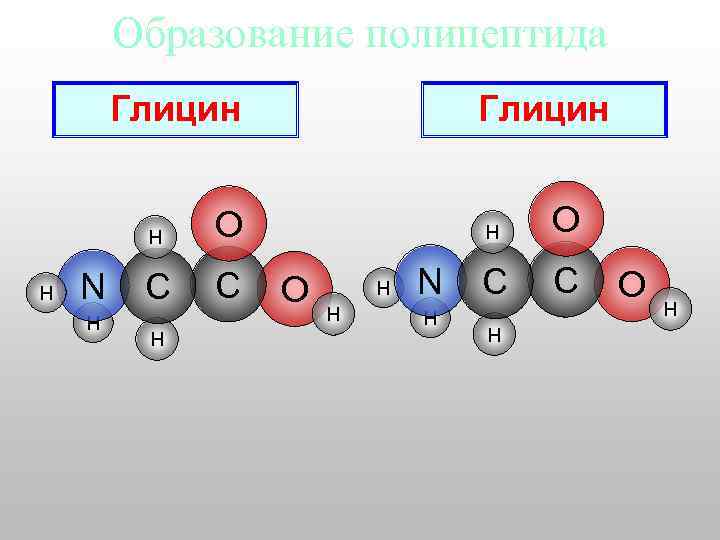
Образование полипептида Глицин H H N H C H O C Глицин H O H H N H O C C H O H
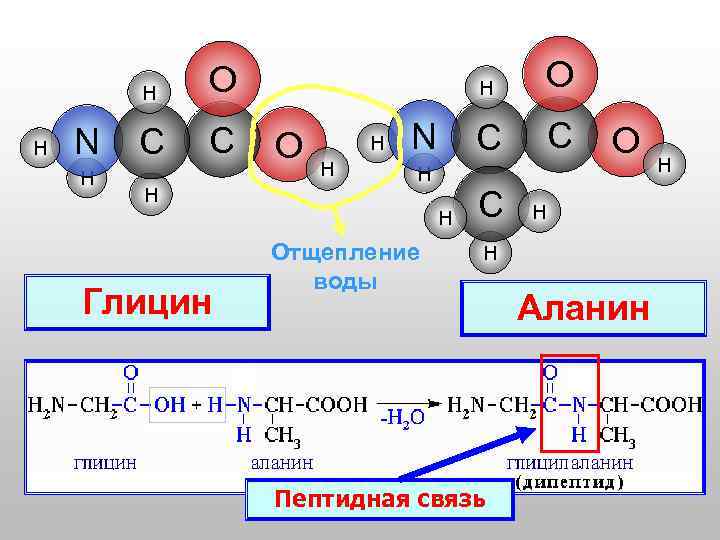
H H N H C C H H O H H N H H Глицин Отщепление воды O C C O H H H Пептидная связь Аланин
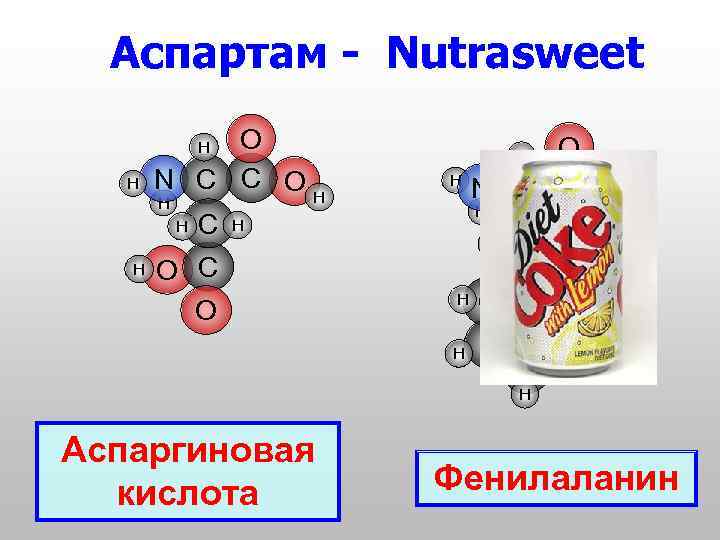
Аспартам - Nutrasweet O N C C OH H H C H H O C O O N C C O H H C C H H C CH H Аспаргиновая кислота Фенилаланин

Специфические способы получения Для отдельных кислот существуют специфические способы получения: Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия: Уксусную кислоту получают в промышленных масштабах каталитическим окислением бутана кислородом воздуха: Муравьиную кислоту получают нагреванием оксида углерода (II) с порошкообразным гидроксидом натрия под давлением и обработкой полученного формиата натрия сильной кислотой:
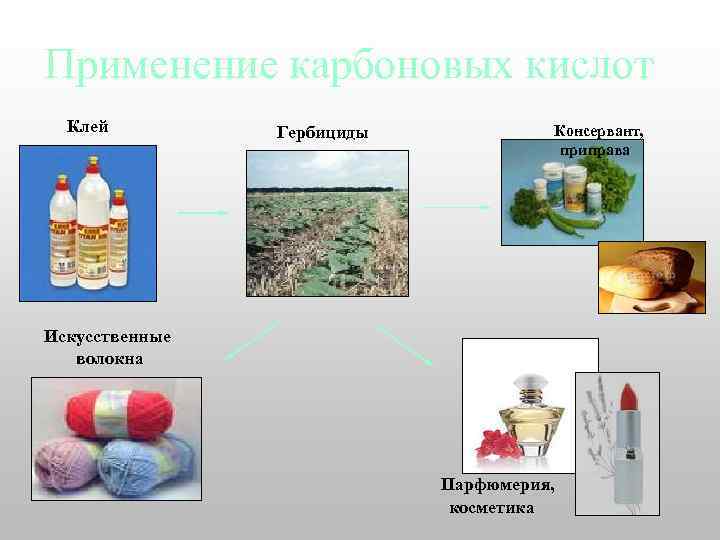
Применение карбоновых кислот Клей Гербициды Консервант, приправа Искусственные волокна Парфюмерия, косметика
Кислоты шерстобоева.ppt