Кислородные соединения азота Азотная кислота ПРОВЕРКА ЗНАНИЙ
















azotnaya_kislota.ppt
- Размер: 899.0 Кб
- Автор: Юлия Гнездилова
- Количество слайдов: 19
Описание презентации Кислородные соединения азота Азотная кислота ПРОВЕРКА ЗНАНИЙ по слайдам
 Кислородные соединения азота Азотная кислота
Кислородные соединения азота Азотная кислота
 ПРОВЕРКА ЗНАНИЙ
ПРОВЕРКА ЗНАНИЙ
 1. Определите, о каком веществе идёт речь I вариант Бесцветный газ, плохо растворим в воде, легко соединяется с кислородом воздуха, образуя бурый газ. II вариант Бесцветный газ с характерным резким запахом, хорошо растворим в воде, легче воздуха.
1. Определите, о каком веществе идёт речь I вариант Бесцветный газ, плохо растворим в воде, легко соединяется с кислородом воздуха, образуя бурый газ. II вариант Бесцветный газ с характерным резким запахом, хорошо растворим в воде, легче воздуха.
 I вариант NO – оксид азота ( II ) II вариант NH 3 — аммиак
I вариант NO – оксид азота ( II ) II вариант NH 3 — аммиак
 2. Расположите соединения азота в порядке возрастания степеней окисления I вариант N 2 , NH 3 , KNO 3 , NO, HNO 2 II вариант NO 2 , N 2 O, HNO 3 , NH 4 Cl, N 2 O
2. Расположите соединения азота в порядке возрастания степеней окисления I вариант N 2 , NH 3 , KNO 3 , NO, HNO 2 II вариант NO 2 , N 2 O, HNO 3 , NH 4 Cl, N 2 O
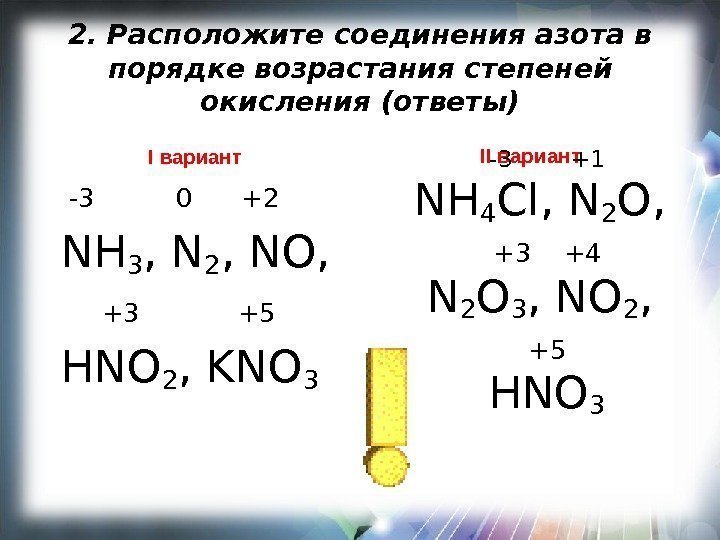
 2. Расположите соединения азота в порядке возрастания степеней окисления (ответы) I вариант -3 0 +2 NH 3 , N 2 , NO, +3 +5 HNO 2 , KNO 3 II вариант -3 +1 NH 4 Cl, N 2 O, + 3 + 4 N 2 O 3 , NO 2 , +5 HNO
2. Расположите соединения азота в порядке возрастания степеней окисления (ответы) I вариант -3 0 +2 NH 3 , N 2 , NO, +3 +5 HNO 2 , KNO 3 II вариант -3 +1 NH 4 Cl, N 2 O, + 3 + 4 N 2 O 3 , NO 2 , +5 HNO
 3. Составьте уравнения реакций по схеме. Назовите вещество Х I вариант N 2 → X → NH 4 Cl II вариант NO 2 → X → NH 4 NO
3. Составьте уравнения реакций по схеме. Назовите вещество Х I вариант N 2 → X → NH 4 Cl II вариант NO 2 → X → NH 4 NO
 3. Составьте уравнения реакций по схеме. Назовите вещество Х (ответы) I вариант X – NH 3 ( аммиак ) 1. N 2 + 3 H 2 =2 NH 3 2. NH 3 + HCl = NH 4 Cl II вариант X – HNO 3 ( азотная кислота ) 1. 4 NO 2 +2 H 2 O+O 2 =4 HNO 3 2. HNO 3 + NH 3 =NH 4 NO
3. Составьте уравнения реакций по схеме. Назовите вещество Х (ответы) I вариант X – NH 3 ( аммиак ) 1. N 2 + 3 H 2 =2 NH 3 2. NH 3 + HCl = NH 4 Cl II вариант X – HNO 3 ( азотная кислота ) 1. 4 NO 2 +2 H 2 O+O 2 =4 HNO 3 2. HNO 3 + NH 3 =NH 4 NO
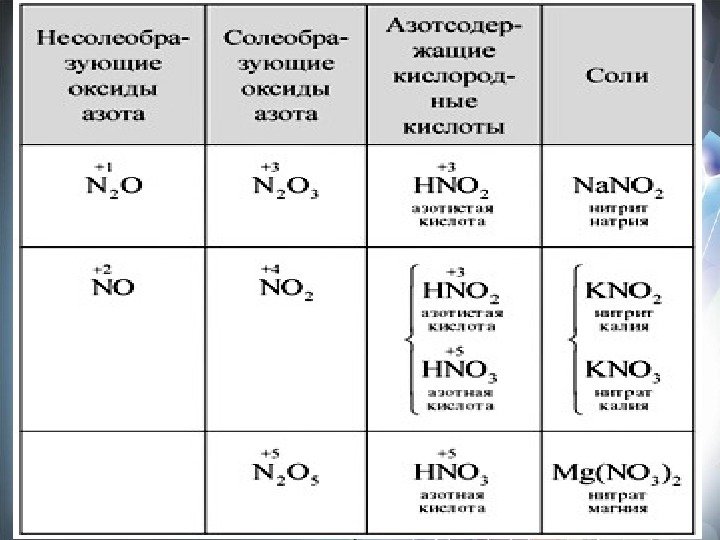
 Кислородные соединения азота. Азотная кислота План изучения: I. Оксиды азота. Физические свойства азотной кислоты; II. Характеристика кислоты; III. Химические свойства ; IV. Применение азотной кислоты.
Кислородные соединения азота. Азотная кислота План изучения: I. Оксиды азота. Физические свойства азотной кислоты; II. Характеристика кислоты; III. Химические свойства ; IV. Применение азотной кислоты.

 I. Физические свойства азотной кислоты • Агрегатное состояние – жидкость ; • Цвет – отсутствует; • Запах – едкий, кислотный; • Растворимость в воде – хорошая; • «Дымит» на воздухе; • «Особые приметы» : при хранении на свету разлагается , приобретая желтоватый оттенок: 4 HNO 3 =4 NO 2 ↑ + 2 H 2 O
I. Физические свойства азотной кислоты • Агрегатное состояние – жидкость ; • Цвет – отсутствует; • Запах – едкий, кислотный; • Растворимость в воде – хорошая; • «Дымит» на воздухе; • «Особые приметы» : при хранении на свету разлагается , приобретая желтоватый оттенок: 4 HNO 3 =4 NO 2 ↑ + 2 H 2 O
 II. Характеристика HNO 3 1. По основности: одноосновная 2. По содержанию «О» : кислородсодержащая 3. По растворимости в воде: растворимая 4. По стабильности: нестабильная 5. По летучести: летучая 6. По степени диссоциации: сильная
II. Характеристика HNO 3 1. По основности: одноосновная 2. По содержанию «О» : кислородсодержащая 3. По растворимости в воде: растворимая 4. По стабильности: нестабильная 5. По летучести: летучая 6. По степени диссоциации: сильная
 III. Химические свойства HNO 3 1. Свойства HNO 3 как электролита Диссоциация: HNO 3 = H+ + NO 3 – Взаимодействует А) с оксидами металлов: Cu. O + 2 HNO 3 = Cu(NO 3 )2 + H 2 O Cu. O + 2 H + = Cu 2+ + H 2 O Б) с основаниями: Cu(OH) 2 + 2 HNO 3 = Cu(NO 3 )2 + 2 H 2 O Cu(OH) 2 + 2 H+ = Cu 2+ + 2 H 2 O В) с солями: Na 2 CO 3 + 2 HNO 3 = 2 Na. NO 3 + CO 2 ↑ + H 2 O CO 32 — + 2 H+ = CO 2 + H 2 O
III. Химические свойства HNO 3 1. Свойства HNO 3 как электролита Диссоциация: HNO 3 = H+ + NO 3 – Взаимодействует А) с оксидами металлов: Cu. O + 2 HNO 3 = Cu(NO 3 )2 + H 2 O Cu. O + 2 H + = Cu 2+ + H 2 O Б) с основаниями: Cu(OH) 2 + 2 HNO 3 = Cu(NO 3 )2 + 2 H 2 O Cu(OH) 2 + 2 H+ = Cu 2+ + 2 H 2 O В) с солями: Na 2 CO 3 + 2 HNO 3 = 2 Na. NO 3 + CO 2 ↑ + H 2 O CO 32 — + 2 H+ = CO 2 + H 2 O
 III. Химические свойства HNO 3 2. Окислительные свойства Взаимодействует с металлами: K Ca Na Mg Al Zn Cr Fe Pb H 2 Cu Hg Ag Au Ме + HNO 3 → Me(NO 3 ) n + H 2 O + N x O y Cu + 4 HNO 3 ( конц) = Cu(NO 3 ) 2 + 2 H 2 O + 2 NO 2 ↑ 3 Cu + 8 HNO 3 ( разб) = 3 Cu(NO 3 ) 2 + 4 H 2 O + 2 NO ↑ Me + HNO 3 = Me(NO 3 ) 2 + H 2 ↑
III. Химические свойства HNO 3 2. Окислительные свойства Взаимодействует с металлами: K Ca Na Mg Al Zn Cr Fe Pb H 2 Cu Hg Ag Au Ме + HNO 3 → Me(NO 3 ) n + H 2 O + N x O y Cu + 4 HNO 3 ( конц) = Cu(NO 3 ) 2 + 2 H 2 O + 2 NO 2 ↑ 3 Cu + 8 HNO 3 ( разб) = 3 Cu(NO 3 ) 2 + 4 H 2 O + 2 NO ↑ Me + HNO 3 = Me(NO 3 ) 2 + H 2 ↑
 III. Химические свойства HNO 3 2. Окислительные свойства Взаимодействует с неметаллами: (S, P, C) C + 4 HNO 3 → CO 2 + 2 H 2 O + 4 NO 2 Взаимодействует с органическими веществами (скипидар)
III. Химические свойства HNO 3 2. Окислительные свойства Взаимодействует с неметаллами: (S, P, C) C + 4 HNO 3 → CO 2 + 2 H 2 O + 4 NO 2 Взаимодействует с органическими веществами (скипидар)
 Металл Концентри рованная (> 60%) Разбавлен ная (5 -60%) Очень разбавлен ная (<5 %) до Fe NO NO, N 2 O, N 2 NH 3 (NH 4 NO 3 ) Pb — Ag NO 2 NO NO не действует Fe, Cr, Al, Au, Pt , Ir , Ta (на холоде) с Al при t 0 → NO Fe, Cr, Al, Au, Pt , Ir , Ta
Металл Концентри рованная (> 60%) Разбавлен ная (5 -60%) Очень разбавлен ная (<5 %) до Fe NO NO, N 2 O, N 2 NH 3 (NH 4 NO 3 ) Pb — Ag NO 2 NO NO не действует Fe, Cr, Al, Au, Pt , Ir , Ta (на холоде) с Al при t 0 → NO Fe, Cr, Al, Au, Pt , Ir , Ta
 IV. Применение азотной кислоты HNO
IV. Применение азотной кислоты HNO
 Вопросы на закрепление I. Назовите вещества, с которыми может реагировать азотная кислота как электролит: SO 2 H 2 Zn. O Ca(OH) 2 HCl Na 2 Si. O 3 Ag II. Азотную кислоту применяют для определения примесей в золотых изделиях. Объясните, чем в ряде случаев обуславливается появление бурого газа и голубого раствора при обработке золота кислотой?
Вопросы на закрепление I. Назовите вещества, с которыми может реагировать азотная кислота как электролит: SO 2 H 2 Zn. O Ca(OH) 2 HCl Na 2 Si. O 3 Ag II. Азотную кислоту применяют для определения примесей в золотых изделиях. Объясните, чем в ряде случаев обуславливается появление бурого газа и голубого раствора при обработке золота кислотой?
 Домашнее задание § 27, упр. 5,
Домашнее задание § 27, упр. 5,

