карбоновые кислоты, омыляемые липиды.ppt
- Количество слайдов: 36

Карбоновые кислоты. Омыляемые липиды.

Карбоновые кислоты – производные углеводородов, содержащие –COOH группу. • Классификация кислот: • По количеству групп –COOH: одно- и многоосновные. • По характеру радикала: предельные, непредельные, ароматические, циклические. • По наличию дополнительных функциональных групп: • - гидроксикислоты ( ‑OH) • ‑ оксокислоты • ‑ аминокислоты ( ‑NH 2)

Предельные одноосновные кислоты HCOOH – Метановая (муравьиная) CH 3 COOH – Этановая (уксусная) CH 3 -CH 2 -COOH – Пропановая (пропионовая) CH 3 -(CH 2)2 -COOH – Бутановая (масляная) – – – C 15 H 31 COOH – Пальмитиновая C 17 H 35 COOH – Стеариновая
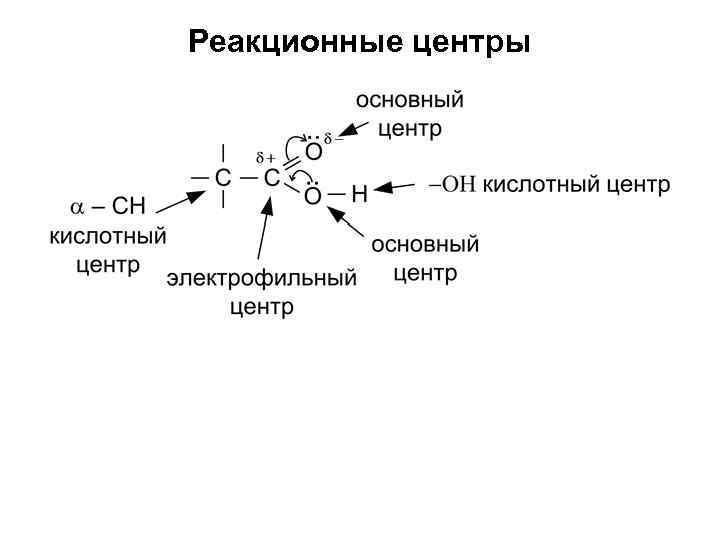
Реакционные центры

Вследствие р – π сопряжения происходит равномерное распределение электронной плотности между двумя атомами кислорода, увеличивается стабильность аниона, оказывается влияние на реакционную способность. 1. ↓δ+ на атоме углерода по сравнению с оксосоединениями. Для кислот характерны реакции SN, а не AN и группа ‑ОН уходит легче, чем в спиртах. 2. ↑ основность оксониевого центра группы (взаимодействие с Н+ катализатором в реакциях SN) 3. ↑ активность –OH кислотного центра по сравнению со спиртами. Карбоновые кислоты реагируют с Ме. О, Ме(ОН)2, с солями активных металлов. 4. –СООН группа проявляет: ‑I, ‑M (ЭА), поэтому усиливается a ‑CH кислотный центр и a водородные атомы замещаются по механизму SR.
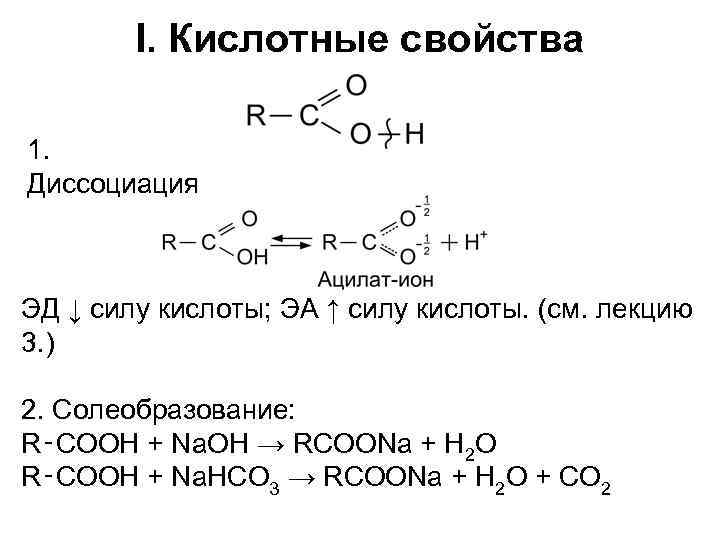
I. Кислотные свойства 1. Диссоциация ЭД ↓ силу кислоты; ЭА ↑ силу кислоты. (см. лекцию 3. ) 2. Солеобразование: R‑COOH + Na. OH → RCOONa + H 2 O R‑COOH + Na. HCO 3 → RCOONa + H 2 O + CO 2
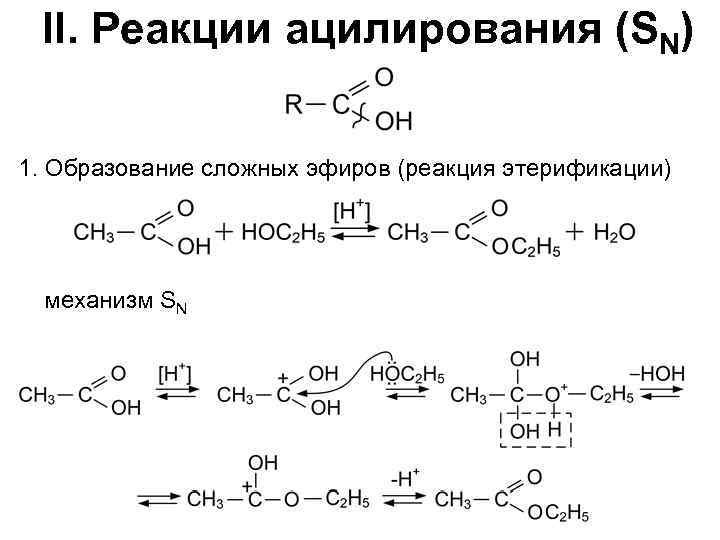
II. Реакции ацилирования (SN) 1. Образование сложных эфиров (реакция этерификации) механизм SN
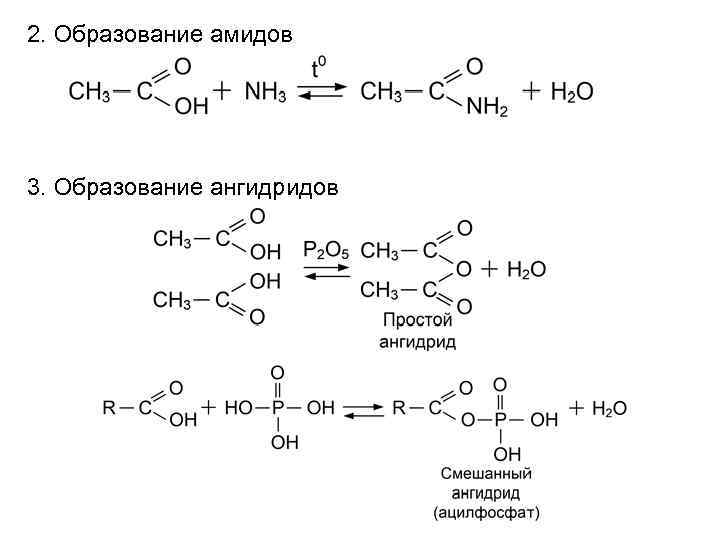
2. Образование амидов 3. Образование ангидридов
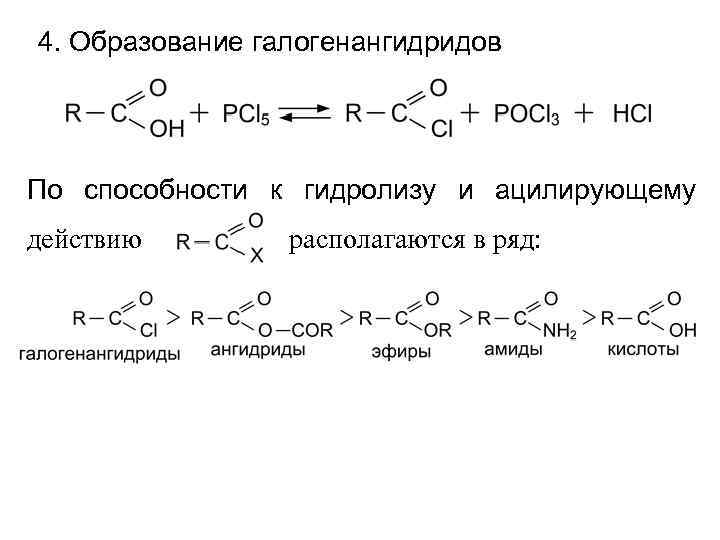
4. Образование галогенангидридов По способности к гидролизу и ацилирующему действию располагаются в ряд:
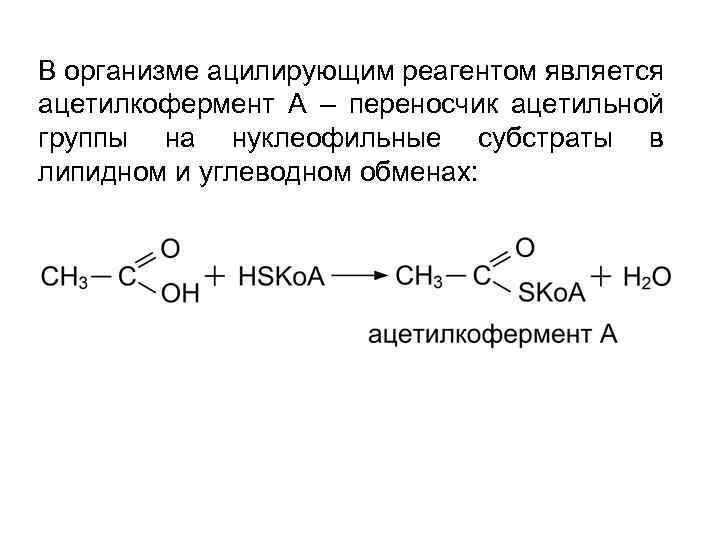
В организме ацилирующим реагентом является ацетилкофермент А – переносчик ацетильной группы на нуклеофильные субстраты в липидном и углеводном обменах:
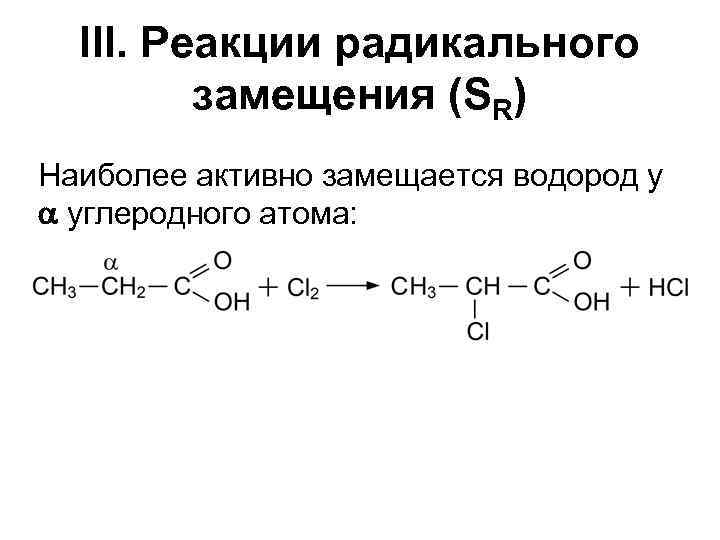
III. Реакции радикального замещения (SR) Наиболее активно замещается водород у a углеродного атома:
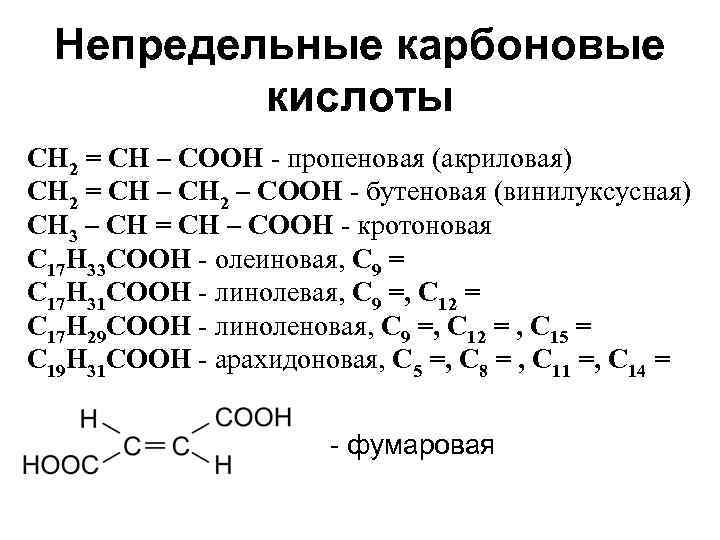
Непредельные карбоновые кислоты СН 2 = СН – СООН - пропеновая (акриловая) СН 2 = СН – СН 2 – СООН - бутеновая (винилуксусная) СН 3 – СН = СН – СООН - кротоновая С 17 Н 33 СООН - олеиновая, С 9 = С 17 Н 31 СООН - линолевая, С 9 =, С 12 = С 17 Н 29 СООН - линоленовая, С 9 =, С 12 = , С 15 = С 19 Н 31 СООН - арахидоновая, С 5 =, С 8 = , С 11 =, С 14 = - фумаровая
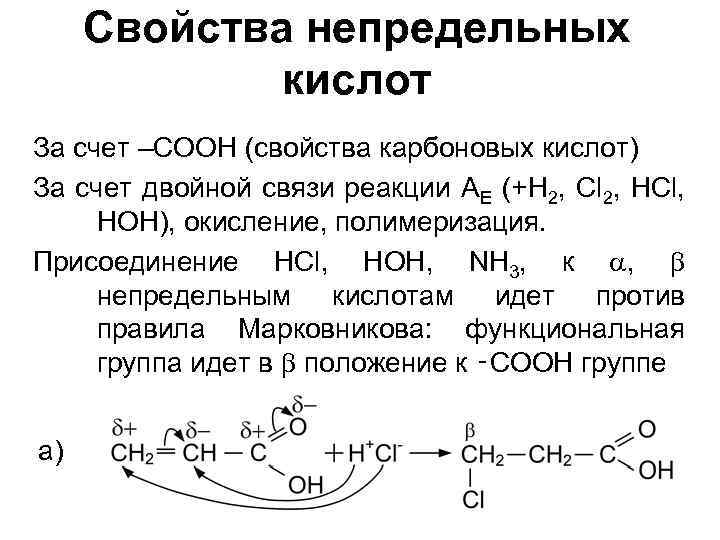
Свойства непредельных кислот За счет –СООН (свойства карбоновых кислот) За счет двойной связи реакции AE (+H 2, Cl 2, HCl, HOH), окисление, полимеризация. Присоединение HCl, HOH, NH 3, к a, b непредельным кислотам идет против правила Марковникова: функциональная группа идет в b положение к ‑СООН группе а)
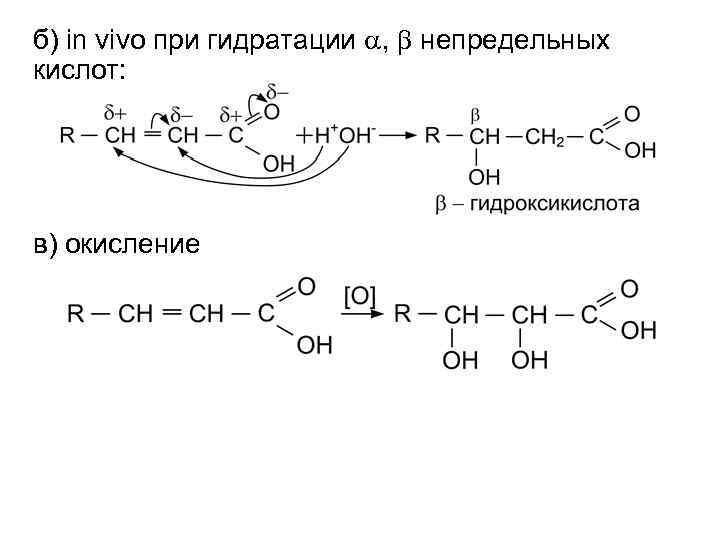
б) in vivo при гидратации a, b непредельных кислот: в) окисление
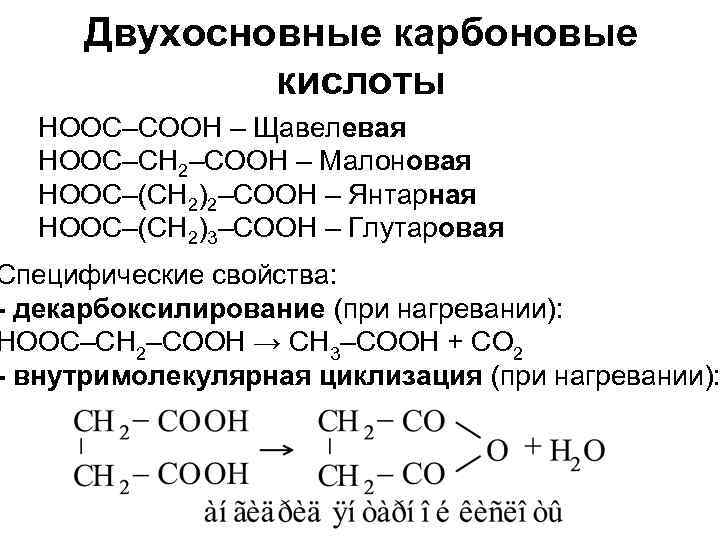
Двухосновные карбоновые кислоты HOOC–COOH – Щавелевая HOOC–CH 2–COOH – Малоновая HOOC–(CH 2)2–COOH – Янтарная HOOC–(CH 2)3–COOH – Глутаровая Специфические свойства: - декарбоксилирование (при нагревании): HOOC–CH 2–COOH → CH 3–COOH + CO 2 - внутримолекулярная циклизация (при нагревании):
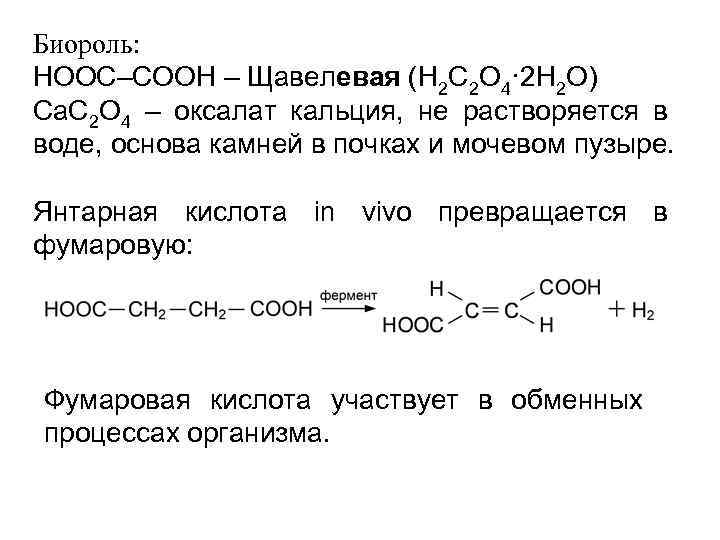
Биороль: HOOC–COOH – Щавелевая (H 2 C 2 O 4· 2 H 2 O) Ca. C 2 O 4 – оксалат кальция, не растворяется в воде, основа камней в почках и мочевом пузыре. Янтарная кислота in vivo превращается в фумаровую: Фумаровая кислота участвует в обменных процессах организма.

Угольная кислота и ее производные H+ + HCO 3‑ ↔ H 2 CO 3 ↔ H 2 O + CO 2 Входит в состав буферных систем организма для поддержания p. H = const.
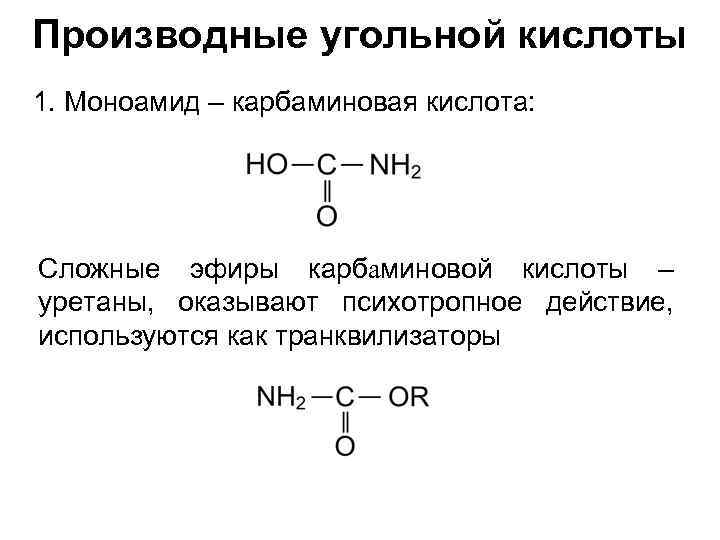
Производные угольной кислоты 1. Моноамид – карбаминовая кислота: Сложные эфиры карбаминовой кислоты – уретаны, оказывают психотропное действие, используются как транквилизаторы
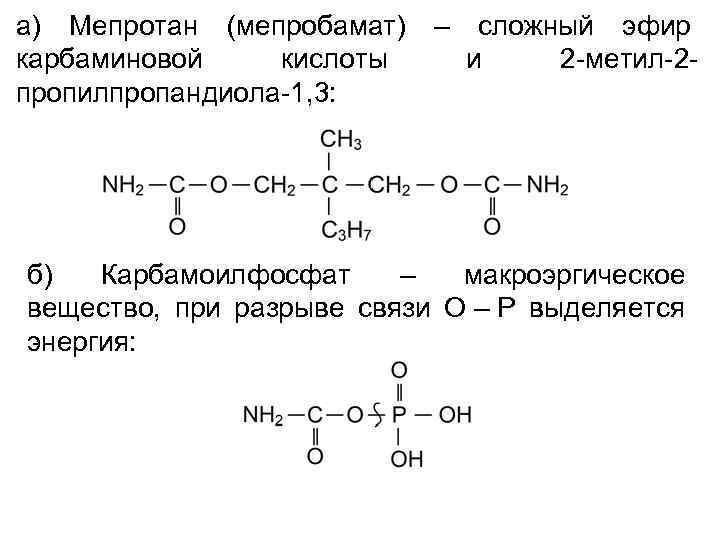
а) Мепротан (мепробамат) – сложный эфир карбаминовой кислоты и 2 -метил-2 пропилпропандиола-1, 3: б) Карбамоилфосфат – макроэргическое вещество, при разрыве связи О – Р выделяется энергия:
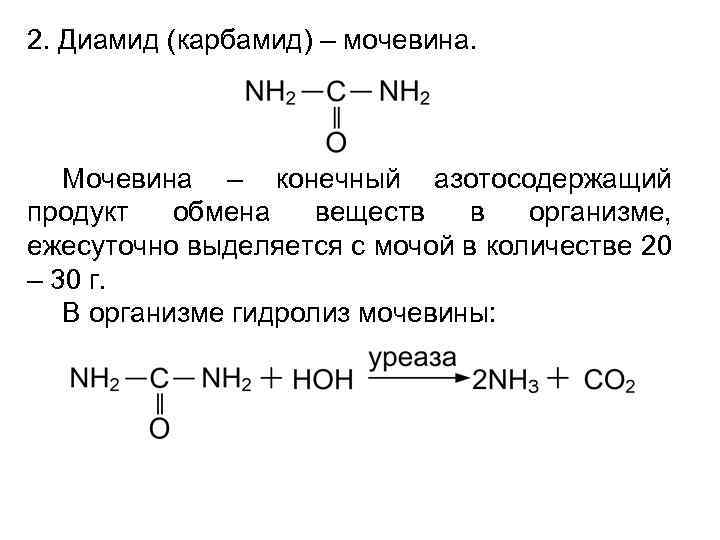
2. Диамид (карбамид) – мочевина. Мочевина – конечный азотосодержащий продукт обмена веществ в организме, ежесуточно выделяется с мочой в количестве 20 – 30 г. В организме гидролиз мочевины:
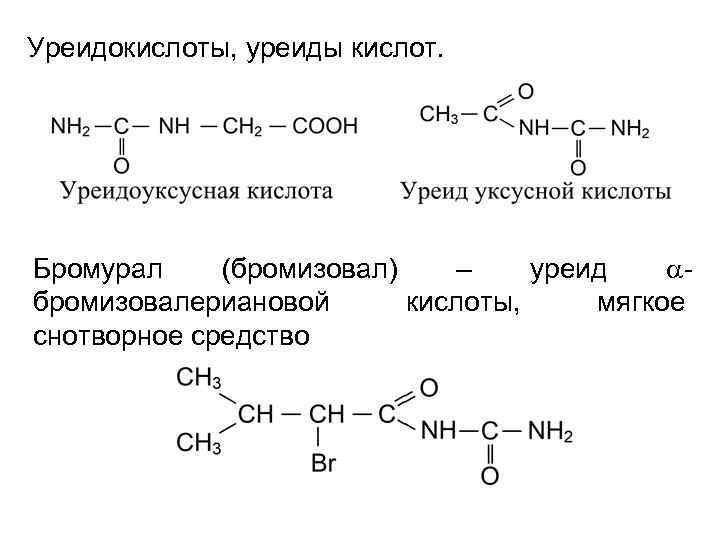
Уреидокислоты, уреиды кислот. Бромурал (бромизовал) – уреид aбромизовалериановой кислоты, мягкое снотворное средство
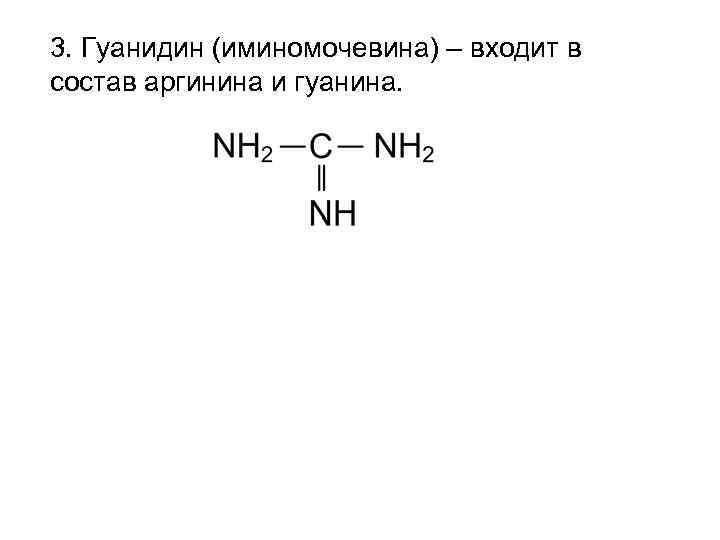
3. Гуанидин (иминомочевина) – входит в состав аргинина и гуанина.

Липиды – сложные эфиры высших карбоновых кислот и спиртов содержатся в животных и растительных тканях, не растворимы в воде, а растворимы в малополярных растворителях (эфире, бензоле). Функции липидов: - Структурная (компонент клеточных мембран). - Защитная (кожа). - Энергетическая (форма в виде которой запасается и транспортируется энергетическое топливо). Энергетическая ценность липидов в два раза больше, чем у белков и углеводов.

Классификация липидов По отношению к гидролизу липиды: а) омыляемые, т. е. в присутствии щелочей образуют соли высших жирных кислот (мыла); б) неомыляемые (терпены, стероиды).
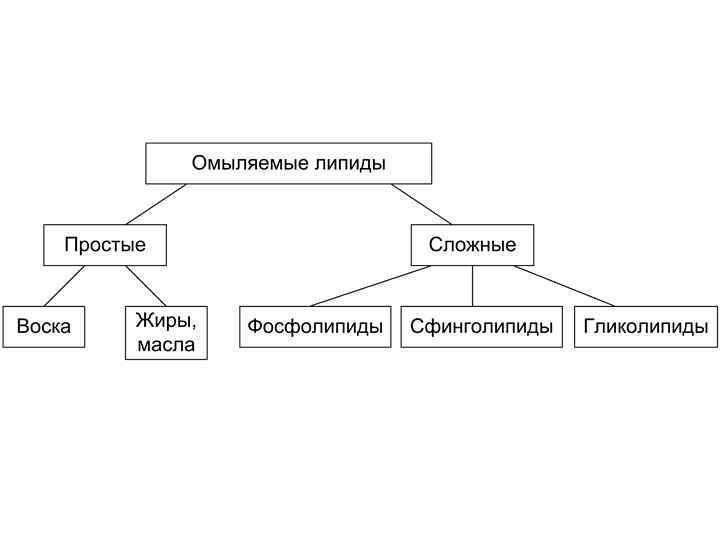

Высшие жирные кислоты, входящие в состав липидов

Синтез простого липида (жира)

Свойства липидов 1. Гидролиз. Кислотный гидролиз (при нагревании в присутствии кислоты) приводит к образованию глицерина и высших карбоновых кислот, входящих в состав липида. При щелочном гидролизе образуется глицерин и соли высших карбоновых кислот (мыла):

2. Реакции присоединения. Гидрирование жиров, содержащих ненасыщенных кислот: остатки

Йодное число – мера ненасыщенности: количество граммов йода, которое может присоединиться к 100 г. вещества (жира).
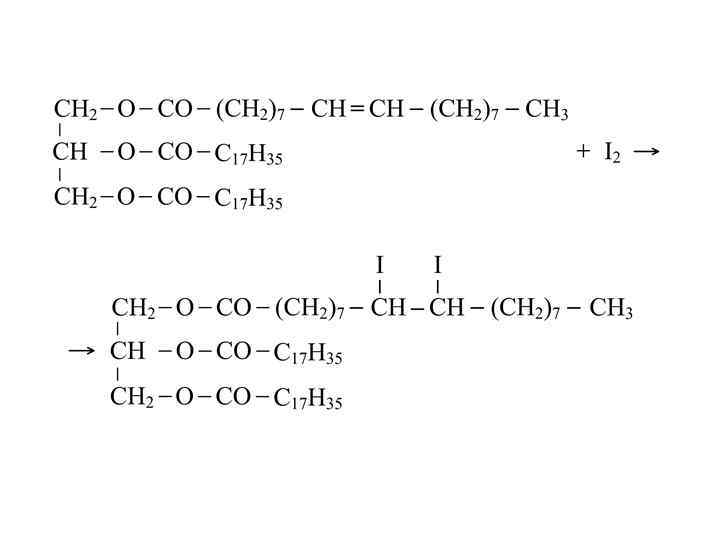

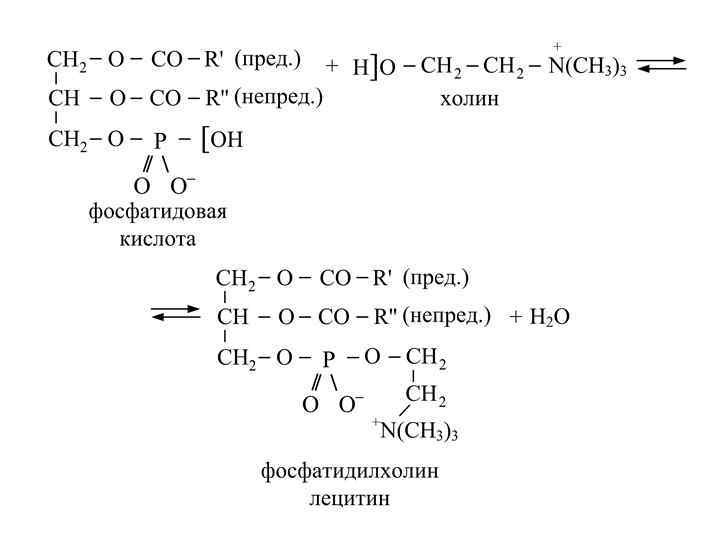
Сложные липиды. Фосфолипиды В состав сложных глицерофосфолипидов входят: остатки трехатомного спирта глицерина, высших предельных и непредельных кислот, фосфорной кислоты и аминоспиртов. Фосфолипиды являются главными компонентами клеточных мембран. Они сопутствуют жирам в пище и служат источником фосфорной кислоты, необходимой для жизни человека.


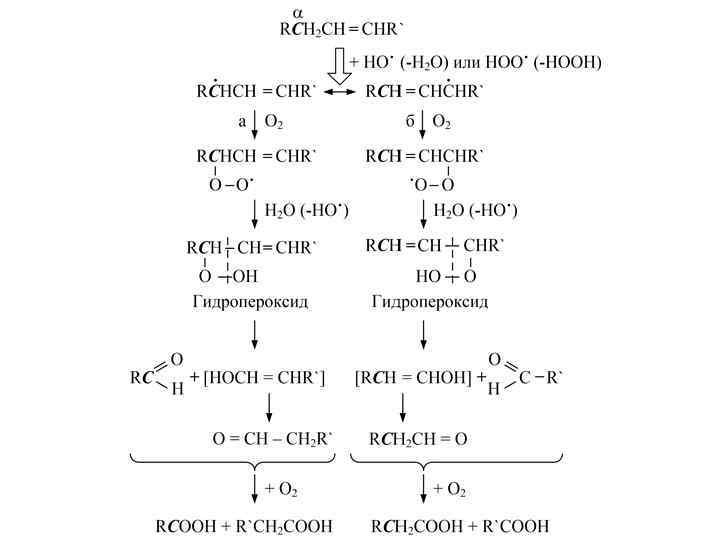
3. Реакции окисления. Пероксидное окисление липидов является основной причиной повреждения клеточных мембран, например, при лучевой болезни. В организме цепи инициируются радикалами HO˙ или HOO˙, образующимися при окислении кислородом ионов железа Fe 2+ в водной среде. Радикал действует на CH 2 группу липида, соседнюю с двойной связью.
карбоновые кислоты, омыляемые липиды.ppt