Карбоновые кислоты.ppt
- Количество слайдов: 22

КАРБОНОВЫЕ КИСЛОТЫ

Карбоновые кислоты, класс органических соединений, содержащих карбоксильную группу (карбоксил). В зависимости от природы радикала, связанного с группой — COOH. Карбоновые кислоты могут принадлежать к алифатическому (жирному), алициклическому, ароматическому или гетероциклическому ряду. По числу карбоксильных групп в молекуле различают одно-, двух и многоосновные (соответственно моно-, ди и поликарбоновые) кислоты. Кроме того, карбоновые кислоты могут быть насыщенными (предельными) и ненасыщенными (непредельными), содержащими в молекулах двойные или тройные связи. Большинство карбоновых кислот имеет тривиальные названия, многие из которых связаны с их нахождением в природе, например муравьиная, яблочная, валериановая, лимонная кислоты.

По Женевской номенклатуре наименования карбоновых кислот производят от названий углеводородов с тем же числом атомов углерода, прибавляя окончание «овая» и слово «кислота» , например метановая кислота (муравьиная), этановая кислота (уксусная) и т. д. Нередко карбоновые кислоты рассматривают как производные углеводородов; например, кислоту строения HCС — COOH называют ацетиленкарбоновой кислотой. Кислотные свойства обусловлены способностью карбоновых кислот к диссоциации в водном растворе: RCOOH = RCOO- + H+. Как правило, карбоновые кислоты слабее минеральных. Константы диссоциации одноосновных насыщенных кислот жирного ряда при 25°С изменяются от 1, 7× 10 -4(муравьиная кислота) до 1, 3. 10 -5 (высшие гомологи). Сила карбоновых кислот существенно зависит также от электрофильности радикала, связанного с карбоксилом.

Введение электроотрицательных заместителей (например, NO 2, CN, Cl) в положение, соседнее с карбоксильной группой, резко повышает кислотность, например циануксусная кислота CNCH 2 COOH примерно в 200 раз сильнее уксусной кислоты CH 3 COOH. По мере удаления от карбоксила влияние заместителей ослабевает. Дикарбоновые кислоты сильнее монокарбоновых, причём влияние одного карбоксила на другой тем больше, чем они ближе расположены друг к другу. Так, в ряду кислот щавелевая кислота HOOC—COOH сильнее малоновой кислоты HOOCCH 2 COOH, которая, в свою очередь, сильнее янтарной HOOC (CH 2)2 COOH, и т. д. Кислотность непредельных кислот выше, чем предельных; влияние двойной связи тем сильнее, чем она ближе расположена к карбоксилу. Так, акриловая кислота CH 2=CH—СООН в 4 раза сильнее пропионовой CH 3—CH 2—COOH. Ароматические кислоты сильнее предельных алифатических (например, константа диссоциации бензойной кислоты 6, 5. 10 -5).

КАРБОНОВЫЕ КИСЛОТЫ жидкие (например, низшие жирные кислоты) или твёрдые (например, высшие жирные и ароматические кислоты) вещества (см. табл. ). Низшие члены насыщенных карбоновых кислот жирного ряда хорошо растворимы в воде, средние члены (C 4 — C 10), а также ароматические кислоты — ограниченно, высшие жирные кислоты в воде не растворимы; как и ароматические кислоты, они хорошо растворяются в спирте, эфире, бензоле.
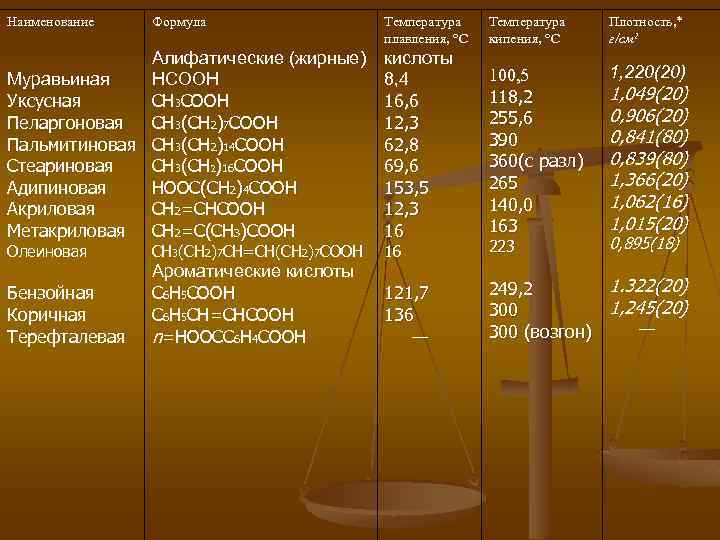
Наименование Формула Алифатические (жирные) НСООН Муравьиная СН 3 СООН Уксусная Пеларгоновая СН 3(СН 2)7 СООН Пальмитиновая СН 3(СН 2)14 СООН Стеариновая СН 3(СН 2)16 СООН Адипиновая НООС(СН 2)4 СООН Акриловая СН 2=СНСООН Метакриловая СН 2=С(СНЗ)СООН Олеиновая СН 3(СН 2)7 СН=СН(СН 2)7 СООН Бензойная Коричная Терефталевая Ароматические кислоты С 6 Н 5 СООН С 6 Н 5 СН=СНСООН n=НООСС 6 Н 4 СООН Температура плавления, °С Температура кипения, °С Плотность, * г/см 2 кислоты 8, 4 16, 6 12, 3 62, 8 69, 6 153, 5 12, 3 16 100, 5 118, 2 255, 6 390 360(с разл) 265 140, 0 163 1, 220(20) 16 223 121, 7 136 — 1. 322(20) 249, 2 1, 245(20) 300 — 300 (возгон) 1, 049(20) 0, 906(20) 0, 841(80) 0, 839(80) 1, 366(20) 1, 062(16) 1, 015(20) 0, 895(18)

ИЗОМЕРЫ И ГОМОЛОГИ n Одноосновные предельные карбоновые кислоты R—COOH являются изомерами сложных эфиров (сокращенно R'—COOR'') с тем же числом атомов углерода. Общая формула и тех, и других Cn. H 2 n. O 2.

АЛГОРИТМ СОСТАВЛЕНИЯ НАЗВАНИЙ КАРБОНОВЫХ КИСЛОТ Найдите главную углеродную цепь - это самая длинная цепь атомов углерода, включающая атом углерода карбоксильной группы. n Пронумеруйте атомы углерода в главной цепи, начиная с атома углерода карбоксильной группы. n Назовите соединение по алгоритму для углеводородов. n В конце названия допишите суффикс "-ов", окончание "-ая" и слово "кислота". В молекулах карбоновых кислот p-электроны атомов кислорода гидроксильной группы взаимодействуют с электронами -связи карбонильной группы, в результате чего возрастает полярность связи O—H, упрочняется -связь в карбонильной группе, уменьшается частичный заряд (+) на атоме углерода и увеличивается частичный заряд (+) на атоме водорода. n

n Последнее способствует образованию прочных водородных связей между молекулами карбоновых кислот. Физические свойства предельных одноосновных карбоновых кислот в значительной степени обусловлены наличием между молекулами прочных водородных связей (более прочных, чем между молекулами спиртов). Поэтому температуры кипения и растворимость в воде у кислот больше, чем у соответствующих спиртов.

ХИМИЧЕСКИЕ СВОЙСТВА КИСЛОТ Упрочнение -связи в карбонильной группе приводит к тому, что реакции присоединения для карбоновых кислот нехарактерны n Горение: CH 3 COOH + 2 O 2 = 2 CO 2 + 2 H 2 O n Синтетическая пищевая уксусная кислота - бесцветная, прозрачная, легковоспламеняющаяся жидкость с резким запахом уксуса. Синтетическую пищевую уксусную кислоту получают из метанола и окиси углерода на родиевом катализаторе. Синтетическая пищевая уксусная кислота применяется в химической, фармацевтической и легкой промышленности, а также в пищевой промышленности в качестве консерванта. Формула СН 3 СООН. Синтетическая пищевая уксусная кислота выпускается концентрированной (99. 7 %) и в виде водного раствора (80 %). n Кислотные свойства В кислотах кислород карбонильной группы , обладая большой электроотрицательностью, вызывает смещение электронного облака соседнего атома углерода к себе. Атом углерода, приобретая вследствие этого некоторый положительный заряд, притягивает к себе электронное облако от атома кислорода гидроксильной группы, наконец, атом кислорода активно отнимает электрон от соседнего атома водорода, вследствие этого водород отщепляется в виде протона-наступает диссоциация. n

n n n HCOOH = HCOO- + H+ (точнее HCOOH + H 2 O = HCOO- + H 3 O+) В свободных кислотах водород каброксила, способный к диссоциации в виде положительного иона, связан с остатком кислоты электростатическими силами притяжения. В анионе диссоциированной кислоты нет истинной карбонильнойгруппы. Все карбоновые кислоты - слабые электролиты. С увеличением числа атомов углерода сила кислот убывает (из-за снижения полярности связи O-H); напротив, введение атомов галогена в углеводородный радикал приводит к возрастанию силы кислоты. Так, в ряду HCOOH - CH 3 COOH - C 2 H 5 COOH сила кислот снижается, а в ряду CH 3 COOH CH 2 Cl. COOH CHCl 2 COOH CCl 3 COOH уксусная монохлоруксусная дихлоруксусная трихлоруксусная - возрастает

n n n Введение электроотрицательных заместителей (например, NO 2, CN, Cl) в положение, соседнее с карбоксильной группой, резко повышает кислотность, например циануксусная кислота CNCH 2 COOH примерно в 200 раз сильнее уксусной кислоты CH 3 COOH. По мере удаления от карбоксила влияние заместителей ослабевает. Дикарбоновые кислоты сильнее монокарбоновых, причём влияние одного карбоксила на другой тем больше, чем они ближе расположены друг к другу. Так, в ряду кислот щавелевая кислота HOOC—COOH сильнее малоновой кислоты HOOCCH 2 COOH, которая, в свою очередь, сильнее янтарной HOOC (CH 2)2 COOH, и т. д. Кислотность непредельных кислот выше, чем предельных; влияние двойной связи тем сильнее, чем она ближе расположена к карбоксилу. Так, акриловая кислота CH 2=CH—СООН в 4 раза сильнее пропионовой CH 3—CH 2—COOH. Ароматические кислоты сильнее предельных алифатических (например, константа диссоциации бензойной кислоты 6, 5. 10 -5). Карбоновые кислоты проявляют все свойства, присущие слабым кислотам: Mg + 2 CH 3 COOH = (CH 3 COO)2 Mg + H 2 Ca. O + 2 CH 3 COOH = (CH 3 COO)2 Ca + H 2 O Na. OH + CH 3 COOH = CH 3 COONa + H 2 O K 2 CO 3 + 2 CH 3 COOH = 2 CH 3 COOK + H 2 O + CO 2

n n Этерификация Реакция нуклеофильного замещения при взаимодействии со спиртами (в присутствии концентрированной H 2 SO 4) образуются сложные эфиры. Образование сложных эфиров при взаимодействии кислоты и спирта в присутствии минеральных кислот называется реакцией этерификации (eter с латинского "эфир"): + Н 2 О муравьиная кислота этанол этиловый эфир муравьиной кислоты Как видно, процесс этерификации обратимый поэтому при наступлении химического равновесия в реакционной смеси будут находиться как исходные, так и конечные вещества. Катализатор (ионы водорода) – одинаково ускоряют прямую и обратную реакции, то есть достижение равновесия. Чтобы сдвинуть равновесие в сторону образования эфира, следует брать в избытке исходные кислоту или спирт, или удалять один из продуктов реакции из сферы взаимодействия – например, отгоняя эфир или связывая воду водоотнимающими средствами.

n n Методом "меченых атомов" с помощью тяжёлого изотопа кислорода доказано, что вода при этерификации образуется за счёт атома водорода спирта и гидроксила кислоты: В природных водах в небольших количествах муравьиная кислота образуется в процессах жизнедеятельности и посмертного разложения водных организмов и биохимической трансформации содержащихся в воде органических веществ. Ее повышенная концентрация связана с поступлением в водные объекты сточных вод предприятий, производящих формальдегид и пластические массы наегооснове. Муравьиная кислота мигрирует главным образом в растворенном состоянии, в виде ионов и недиссоциированных молекул, количественное соотношение между которыми определяется константой ионизации К 25°С = 2. 4. 10 -4 и значениями р. Н. При поступлении муравьиной кислоты в водные объекты она разрушается главным образом под влиянием биохимических процессов. Особенность муравьиной кислоты HCOOH состоит в том, что это вещество - двуфункциональное соединение, оно одновременно является и карбоновой кислотой, и альдегидом. Поэтому муравьиная кислота кроме всего прочего реагирует и с аммиачным раствором оксида серебра (реакция серебряного зеркала; качественная реакция): HCOOH + Ag 2 O(аммиачный раствор) = CO 2 + H 2 O + 2 Ag

n В реакцию этерификации могут вступать и многоатомные спирты, например, глицерин. Сложные эфиры, образованные глицерином и высшими карбоновыми кислотами (жирными кислотами) - это жиры. +3 Н О 2 Глицерин n n карбоновые кислоты триглицерид Жиры представляют собой смеси триглицеридов. Предельные жирные кислоты (пальмитиновая C 15 H 31 COOH, стеариновая C 17 H 35 COOH) образуют твердые жиры животного происхождения, а непредельные (олеиновая C 17 H 33 COOH, линолевая C 17 H 31 COOH и др. ) - жидкие жиры (масла) растительного происхождения. Замещение в углеводородном радикале: CH 3—CH 2—COOH+ Cl 2 = CH 3—CHCl—COOH+ HCl пропионовая кислота - хлорпропионовая кислота

n n n n n Наиболее важные химические свойства карбоновых кислот — способность превращаться в производные. При взаимодействии с основаниями Карбоновые кислоты дают соли: RCOOH + Na. OH = RCOONa + H 2 O. Схема получения хлораангидрида CH 3–СО–OH + PCl 5 = CH 3–СО–Cl + POCl 3 + HCl Схема получения ангидридов уксусной кислоты, пропаномида, бензойной кислоты CH 3–СО–OH + H–O–СО–CH 3 = CH 3–СО–O–СО–CH 3 + H 2 O Декарбоксилирование-одна из наиболее важных реакций. Незамещенные карбоновые кислоты декарбоксилируются чрезвычайно трудно. Реакция протекает легче при наличии у альфауглеродного атома электроноакцепторной группы, поляризующей C-COOH связь этого атома с карбоксильной группой. HOOC-COOH = CO 2 +HCOOH Галогенирование карбоновых кислот и их производных идет в жестких условиях. Бромирование кислот обычно проводят в присутствии фосфора(реакция Гелля-Фольгарда-Зелинского. Атом галогена в альфа-галоген-карбонильных соединениях достаточно подвижен и легко замещается под действием различных нуклеофильных реагентов(Na. OН, NH 3 и т. д. ). Однако все же его подвижность гораздо ниже, чем в галогенангидридов кислот.

n n n CH 3 CH 2 COOH+Cl 2 = CHCl 2 CH 2 COOH R-CH=CH-COOH+Cl 2 = R-CHCl-COOH Величина эффективногог положительного заряда на карбонильном атоме углерода в функциональных производных карбоновых кислот увеличивается с ростом I-эффекта заместителя. X и уменьшается с увеличениемего +Mэффекта. В результате действия этих эффектов величина заряда, и способность подвергаться нуклиофильной атаке увеличивается. В кислой среде активность карбонильной группы увеличивается, поскольку вследствие протонирования кислорода на атоме углерода возникает полный положительный заряд.
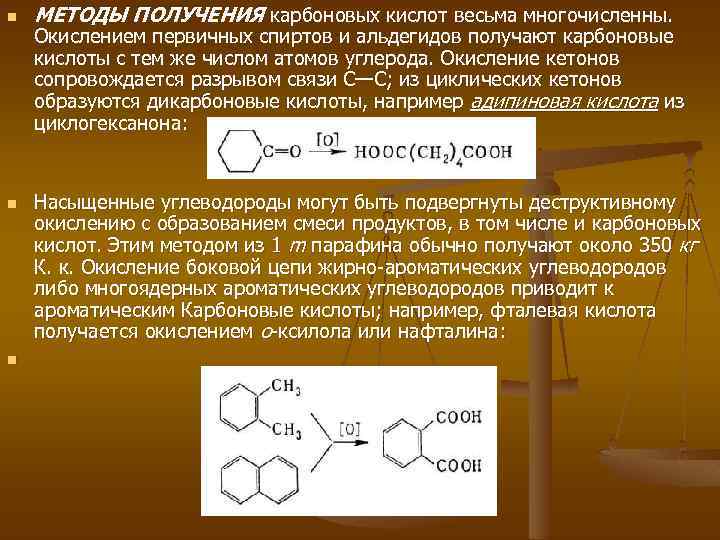
n n n МЕТОДЫ ПОЛУЧЕНИЯ карбоновых кислот весьма многочисленны. Окислением первичных спиртов и альдегидов получают карбоновые кислоты с тем же числом атомов углерода. Окисление кетонов сопровождается разрывом связи С—С; из циклических кетонов образуются дикарбоновые кислоты, например адипиновая кислота из циклогексанона: Насыщенные углеводороды могут быть подвергнуты деструктивному окислению с образованием смеси продуктов, в том числе и карбоновых кислот. Этим методом из 1 m парафина обычно получают около 350 кг К. к. Окисление боковой цепи жирно-ароматических углеводородов либо многоядерных ароматических углеводородов приводит к ароматическим Карбоновые кислоты; например, фталевая кислота получается окислением о-ксилола или нафталина:

n Ненасыщенные углеводороды окисляются по месту двойной связи: . n Важный метод синтеза карбоновых кислот — гидролиз их нитрилов, n n n легко получаемых взаимодействием галогенопроизводных углеводородов с цианистым натрием: RCI + Na. CN ® RCOOH. В настоящее время промышленное значение приобрёл метод синтеза карбоновых кислот карбонилированием, т. е. введением группы CO в органические соединения: Окисление первичных спиртов и альдегидов (кислородом на катализаторе; KMn. O 4; K 2 Cr 2 O 7): R-CH 2 OH = R-COOH Ароматические кислоты синтезируют окислением гомологов бензола : 5 + 6 KMn. O 4 + 9 H 2 SO 4 = 5 + K 2 SO 4 + 6 Mn. SO 4 +14 H 2 O

n n n n Гидролиз функциональных производных (сложных эфиров, ангидридов, галогенангидридов, амидов). R-CОХ + Н 2 О = R-СООН + НХ из галогенпроизводных R-Cl + KCN = R-CN + 2 H 2 O = R-COOH из непредельные кислоты получают окислением непредельных альдегидов H 2 C=CH-CH 2 OH + [O] = H 2 С=СH-COH + [O] = H 2 С=СH-СOOH Схема получения бензойной кислоты +[O] = + 2 H 2 O схема получения щавелевой кислоты n HO-CH 2 -OH + [O] = HOC-COH + [O] = HOOC-COOH

n n Некоторые карбоновые кислоты получают из природных продуктов. Так, щелочным гидролизом (омылением) жиров получают соли высших жирных кислот (мыла) и глицерин. Лимонную кислоту получают из ботвы хлопчатника и из стеблей махорки (после выделения из них никотина). Многие Карбоновые кислоты получают сбраживанием углеводов в присутствии бактерий определённого вида (маслянокислое, молочнокислое, лимоннокислое и др. виды брожения). Гидролиз (омыление) в кислой или в щелочной среде, или под действием ферментов:

Благодарю за внимание
Карбоновые кислоты.ppt