Л. 11 Карбонильные соед..ppt
- Количество слайдов: 22

Карбонильные соединения - это производные УВ, содержащие функциональную группу >С=О. В зависимости от строения молекулы среди карбонильных соединений различают альдегиды и кетоны.

Альдегиды – органические соединения, в молекулах которых атом углерода карбонильной группы (карбонильный углерод) связан с атомом водорода и углеводородным радикалом. Общая формула: Сn. H 2 n+1 CН=O или , где R = H, алкил, арил Функциональная группа – СН=О называется альдегидной. Номенклатура n n Систематические названия альдегидов строят по названию соответствующего углеводорода с добавлением суффикса -аль. Нумерацию цепи начинают с карбонильного атома углерода. Тривиальные названия производят от тривиальных названий тех кислот, в которые альдегиды превращаются при окислении.
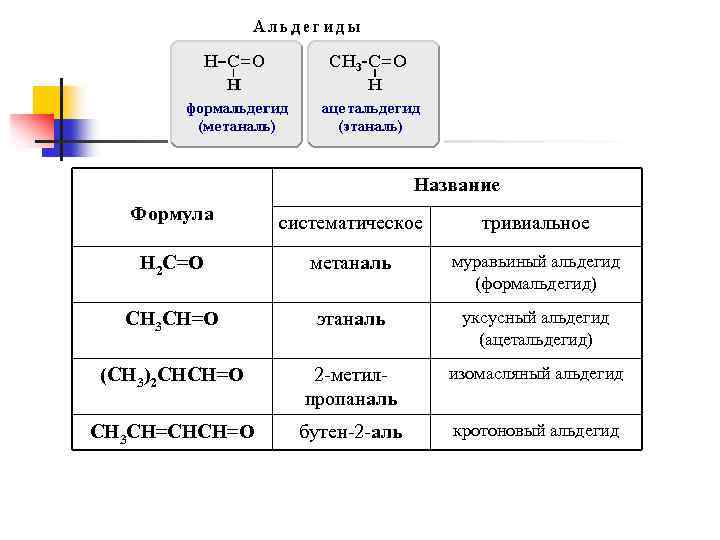
Название Формула систематическое тривиальное H 2 C=O метаналь муравьиный альдегид (формальдегид) CH 3 CH=O этаналь уксусный альдегид (ацетальдегид) (CH 3)2 CHCH=O 2 -метилпропаналь изомасляный альдегид CH 3 CH=CHCH=O бутен-2 -аль кротоновый альдегид

Кетоны – органические вещества, молекулы которых содержат карбонильную группу, соединенную с двумя углеводородными радикалами. Общие формулы: R 2 C=O, R–CO–R' или R, R' = алкил, арил Номенклатура n n По систематической номенклатуре название кетона строится по названию соответствующего алкана с добавлением суффикса –он и указанием номера атома С, с которым связан карбонильный кислород; нумерацию цепи начинают от конца цепи, ближайшего к карбонильной группе. По рациональной номенклатуре к названиям радикалов, связанных с карбонильной группой и перечисленных в порядке их усложнения, прибавляют слово кетон.
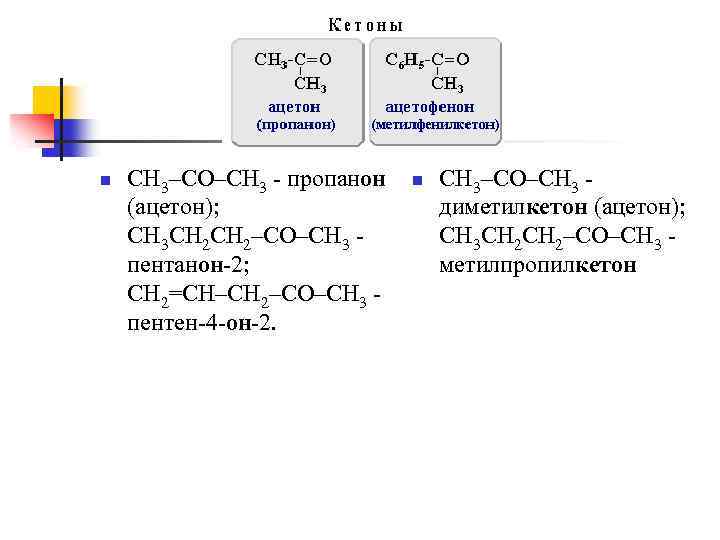
n CH 3–CO–CH 3 - пропанон (ацетон); CH 3 CH 2–CO–CH 3 - пентанон-2; CH 2=CH–CH 2–CO–CH 3 - пентен-4 -он-2. n CH 3–CO–CH 3 - диметилкетон (ацетон); CH 3 CH 2–CO–CH 3 - метилпропилкетон

Изомерия альдегидов и кетонов Изомерия углеродного скелета Изомерия положения карбонильного кислорода (только для кетонов) Альдегиды и кетоны – структурные изомеры одного класса Межклассовая изомерия С 3 Н 6 О
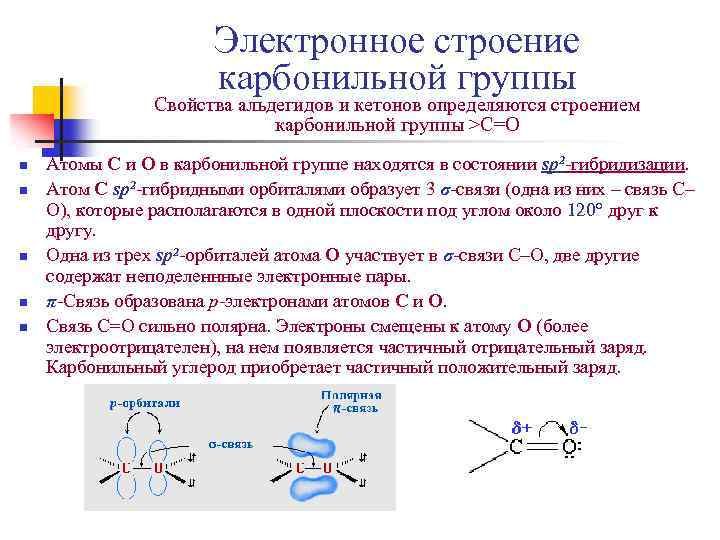
Электронное строение карбонильной группы Свойства альдегидов и кетонов определяются строением карбонильной группы >C=O n n n Атомы С и О в карбонильной группе находятся в состоянии sp 2 -гибридизации. Атом С sp 2 -гибридными орбиталями образует 3 σ-связи (одна из них – связь С– О), которые располагаются в одной плоскости под углом около 120° друг к другу. Одна из трех sp 2 -орбиталей атома О участвует в σ-связи С–О, две другие содержат неподеленнные электронные пары. π-Связь образована р-электронами атомов С и О. Связь С=О сильно полярна. Электроны смещены к атому О (более электроотрицателен), на нем появляется частичный отрицательный заряд. Карбонильный углерод приобретает частичный положительный заряд.

Физические свойства карбонильных соединений Молекулы карбонильных соединений не ассоциированы. В них отсутствуют атомы водорода, способные к образованию водородных связей. Вследствие этого: n Их температуры кипения ниже, чем у соответствующих спиртов. Метаналь (формальдегид) – газ, альдегиды С 2 -C 5 и кетоны С 3 -С 4 – жидкости, высшие – твердые вещества. Однако: n Низшие гомологи растворимы в воде, благодаря образованию водородных связей между атомами водорода молекул воды и карбонильными атомами кислорода. С увеличением углеводородного радикала растворимость в воде падает. n Альдегиды, как правило раздражают слизистые оболочки глаз и дыхательных путей, вредно влияют на нервную систему.

Для карбонильных соединений характерны реакции различных типов: присоединение по карбонильной группе; n полимеризация; n конденсация; n восстановление и окисление. Реакционная способность уменьшается от альдегидов к кетонам: n Это объясняется, главным образом, двумя факторами: n углеводородные радикалы у группы С=О увеличивают пространственные препятствия присоединению к карбонильному атому С новых атомов или атомных групп; n углеводородные радикалы уменьшают положительный заряд на карбонильном атоме С, что затрудняет реакции присоединения.

Реакции присоединения по карбонильной группе Присоединение большинства реагентов по двойной связи С=О происходит как ионная реакция n Присоединение спиртов с образованием полуацеталей (в присутствии кислоты или основания как катализатора): Полуацетали - соединения, в которых атом углерода связан с гидроксильной и алкоксильной (-OR) группами. n Взаимодействие полуацеталя с еще одной молекулой спирта приводит к замещению полуацетального гидроксила на алкоксильную группу OR' и образованию ацеталя:

§ Присоединение циановодородной (синильной) кислоты HCN: Эта реакция используется для удлинения углеродной цепи. n Гидрирование (восстановление) альдегидов и кетонов: Альдегиды при взаимодействии с водородом в присутствии Niкатализатора образуют первичные спирты, кетоны - вторичные:

Реакции окисления альдегидов и кетонов Альдегиды легко окисляются в соответствующие карбоновые кислоты под действием мягких окислителей: оксид серебра и гидроксид меди (II). Это качественные реакции на альдегиды. 1. Реакция "серебрянного зеркала" – окисление аммиачным раствором оксида серебра (реактив Толленса): R–CH=O + 2[Ag(NH 3)2]OH → RCOOH + 2 Ag↓ + 4 NH 3 + H 2 O 2. Реакция "медного зеркала" - окисление свежеприготовленным осадком гидроксида меди (II) при нагревании: R-CH=О + 2 Cu(OH)2 → RCOOH + Cu 2 O↓ + H 2 О Образуется красно-кирпичный осадок оксида меди (I) или металлическая медь (реакция "медного зеркала", более характерная для формальдегида).

Кетоны не вступают в эти реакции, окисляются с трудом при действии более сильных окислителей и повышенной температуре. Происходит разрыв С–С-связей, соседних с карбонилом и образование смеси карбоновых кислот меньшей молекулярной массы. n На воздухе карбонильные соединения сгорают с образованием оксида углерода(IV) и воды: НСНО + О 2 → СО 2 + Н 2 О

Реакции полимеризации Полимеризация - частный случай реакций присоединения - характерна в основном для альдегидов. Например, при стоянии 40% водного раствора формальдегида (формалина), в виде белого осадка образуется полимер формальдегида с невысокой молекулярной массой - параформ: n H 2 C=O + H 2 O → HOCH 2– (OCH 2)n-2– OCH 2 OH ( n = 7, 8 ) Реакция происходит за счет разрыва π-связи

Реакции поликонденсации Процессы образования полимеров из низкомолекулярных веществ, сопровождающиеся выделением побочных низкомолекулярных веществ: воды, хлороводорода, аммиака. n n Конденсация с фенолами. Практическое значение имеет реакция формальдегида с фенолом (катализаторы - кислоты или основания): Дальнейшее взаимодействие с другими молекулами формальдегида и фенола приводит к образованию фенолформальдегидных смол.

Получение карбонильных соединений 1. Окисление спиртов n Первичные спирты при окислении образуют альдегиды, которые затем легко окисляются до карбоновых кислот. Чтобы предотвратить превращение альдегида в кислоту, его отгоняют в ходе реакции (т. кип. альдегида, не образующего межмолекулярные водородные связи, ниже т. кип. спирта и кислоты). n При окислении вторичных спиртов образуются кетоны.

В промышлености альдегиды и кетоны получают дегидрированием спиртов, пропуская пары спирта над нагретым катализатором (Cu, соединения Ag, Cr или Zn). 2. Гидратация алкинов (реакция Кучерова) Присоединение воды к ацетилену в присутствии солей ртути (II) приводит к образованию ацетальдегида: Кетоны получают при гидратации других гомологов ряда алкинов:

3. Щелочной гидролиз дигалогеналканов (атомы галогена при одном атоме углерода): H │ +2 Na. OH │ CH 3 - C - Cl → [ CH 3 – C - ОH ] → CH 3 – CH = O + H 2 O │ -2 Na. Cl │ Cl OH неустойчивое соединение (геминальный диол)

4. Окисление углеводородов кислородом воздуха в присутствии катализаторов. n Окисление алканов (получение формальдегида при t = 5000 C в присутствии меди или серебра): CH 4 + O 2 → HCH=O + H 2 O Каталитическое окисление алкенов: t, kat 2 R-CH=CH 2 + O 2 → 2 R-CH 2 - CH=O 100, Pd. Cl 2, Cu. Cl 2 2 CH 2=CH 2 + O 2 → 2 CH 3 -CH=O n

Кумольный способ получения ацетона (наряду с фенолом).
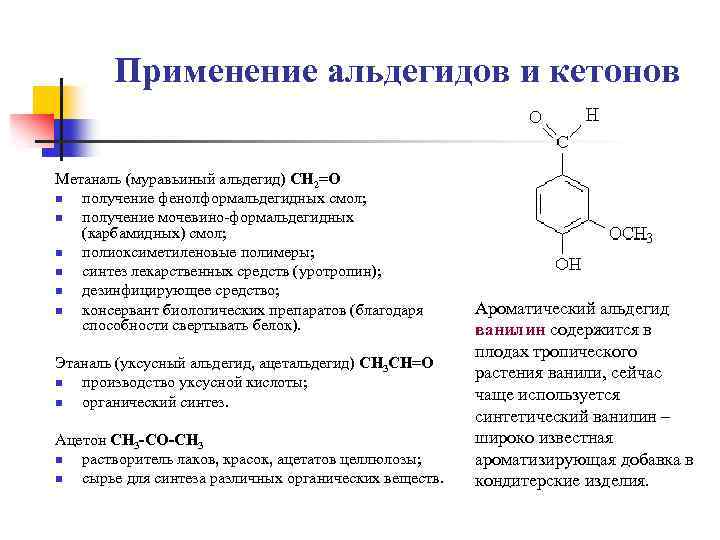
Применение альдегидов и кетонов Метаналь (муравьиный альдегид) CH 2=O n получение фенолформальдегидных смол; n получение мочевино-формальдегидных (карбамидных) смол; n полиоксиметиленовые полимеры; n синтез лекарственных средств (уротропин); n дезинфицирующее средство; n консервант биологических препаратов (благодаря способности свертывать белок). Этаналь (уксусный альдегид, ацетальдегид) СН 3 СН=О n производство уксусной кислоты; n органический синтез. Ацетон СН 3 -СО-СН 3 n растворитель лаков, красок, ацетатов целлюлозы; n сырье для синтеза различных органических веществ. Ароматический альдегид ванилин содержится в плодах тропического растения ванили, сейчас чаще используется синтетический ванилин – широко известная ароматизирующая добавка в кондитерские изделия.

Домашнее задание по теме «Карбонильные соединения» 1. 2. Электронный учебник: часть -IV ; раздел - 3; Учебник Скворцов А. В. : глава 11 (стр. 16 -20); устно – вопросы 11. 1 - 11. 7; письменно – 11. 8 – 11. 11, стр. 21.
Л. 11 Карбонильные соед..ppt