Кафедра молекулярной фармакологии и радиобиологии МБФ ГОУ ВПО

Кафедра молекулярной фармакологии и радиобиологии МБФ ГОУ ВПО РГМУ Росздрава Эффекты малых доз радиации Цикл из двух лекций ст. преподавателя В.Г. Шепелёва

Малые дозы радиации Лекция 1 Определение малой дозы Адаптивный ответ Радиационный гормезис

Рассмотрение закономерностей и особенностей действия ионизирующей радиации в малых дозах обусловливается несколькими причинами: обнаружением биологических эффектов ненаблю-даемых, или которые невозможно наблюдать при воздействии радиации в больших дозах; необходимостью оценить последствия для здоровья человека облучения в малых дозах в связи с тем, что в небольших дозах подверглись или продолжают подвергаться целые субпопуляции людей; важностью выработать научно обоснованные нормы допустимых доз облучения для работников радиоактивных производств и населения

ЧТО ТАКОЕ МАЛАЯ ДОЗА ОБЛУЧЕНИЯ. Единого мнения по этому вопросу у радиобиологов до настоящего времени нет, хотя все согласны с тем, что это дозы, не вызывающие опасных детермини-рованных последствий для здоровья. Как известно, количественное проявление большин-ства биологических эффектов воздействия излучений, в основном редкоионизирующих, не строго пропорцио-нально дозе излучения (как правило, в области низкого диапазона доз выход повреждений на единицу дозы снижается), т. е. кривые доза-эффект многих типов повреждений, носящие нелинейный характер, хорошо описываются линейно-квадратичной зависимостью: I(D)=aD+bD2

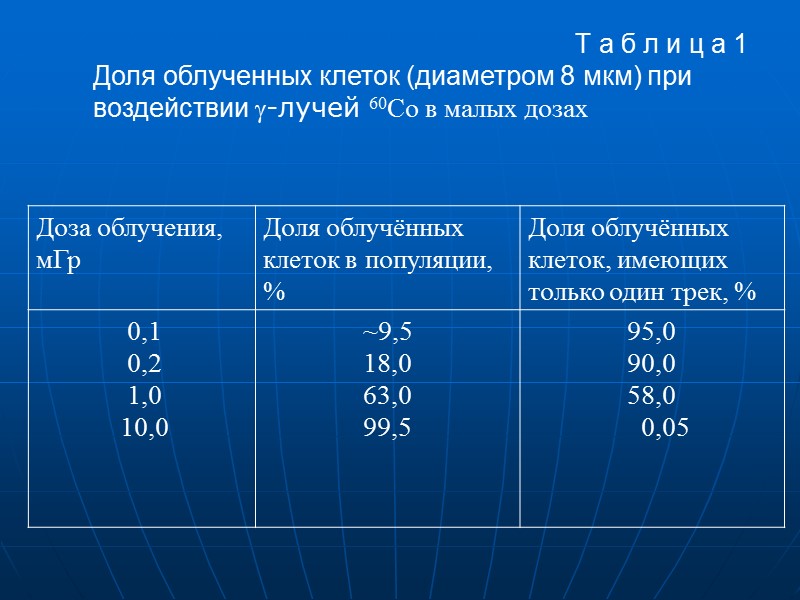
Взаимодействие ионизирующих излучений с биологическими объектами (мишенями) - клетками, клеточными ядрами и молекулами ДНК - происходит дискретно. Исходя из принципов радиационной биофизики при воздействии любого типа излучения границей для выделения диапазона малых доз была предложена такая доза, при которой в среднем на одну клетку (мишень) приходится один трек от прохождения ионизирующей частицы (кванта). Поскольку взаимодействие ионизирующих частиц с мишенями происходит случайным образом, число треков в разных клетках при облучении в указанном диапазоне доз может довольно сильно отличаться.

Т а б л и ц а 1 Доля облученных клеток (диаметром 8 мкм) при воздействии -лучей 60Со в малых дозах

Несмотря на существенные различия в индивидуаль-ной радиочувствительности человека при остром воздействии редкоионизирующей радиации в дозах 200 мГр и ниже не отмечено случаев развития детерминированных последствий (лучевой болезни) облучения. Более того, при обследовании небольшого контингента лиц (меньших нескольких сотен тысяч), облученных в дозах ниже 200 мГр, не удается выявить увеличе-ния числа злокачественных опухолей (стохасти-ческие события). Эти результаты получены в ходе эпидемиологических наблюдений за лицами, облученными при взрывах атомных бомб. Поэтому НКДАР предложил считать дозы в 200 мГр и ниже малыми. За малую мощность излучений предложено считать воздействие редкоионизирующей радиации с интенсивностью в 0,1 мГр/мин и ниже.
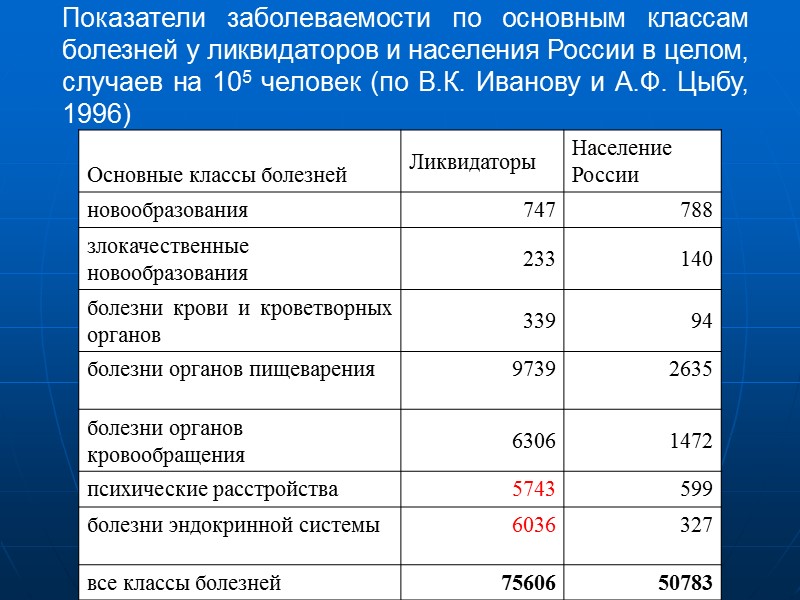
Показатели заболеваемости по основным классам болезней у ликвидаторов и населения России в целом, случаев на 105 человек (по В.К. Иванову и А.Ф. Цыбу, 1996)

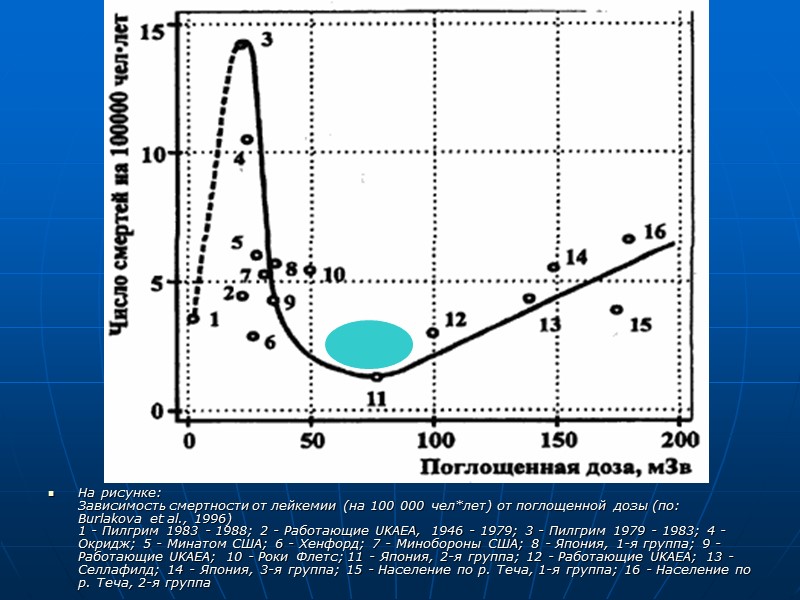
На рисунке: Зависимость смертности от лейкемии (на 100 000 чел*лет) от поглощенной дозы (по: Burlakova et al., 1996) 1 - Пилгрим 1983 - 1988; 2 - Работающие UKAEA, 1946 - 1979; 3 - Пилгрим 1979 - 1983; 4 - Окридж; 5 - Минатом США; 6 - Хенфорд; 7 - Минобороны США; 8 - Япония, 1-я группа; 9 - Работающие UKAEA; 10 - Роки Флетс; 11 - Япония, 2-я группа; 12 - Работающие UKAEA; 13 - Селлафилд; 14 - Япония, 3-я группа; 15 - Население по р. Теча, 1-я группа; 16 - Население по р. Теча, 2-я группа


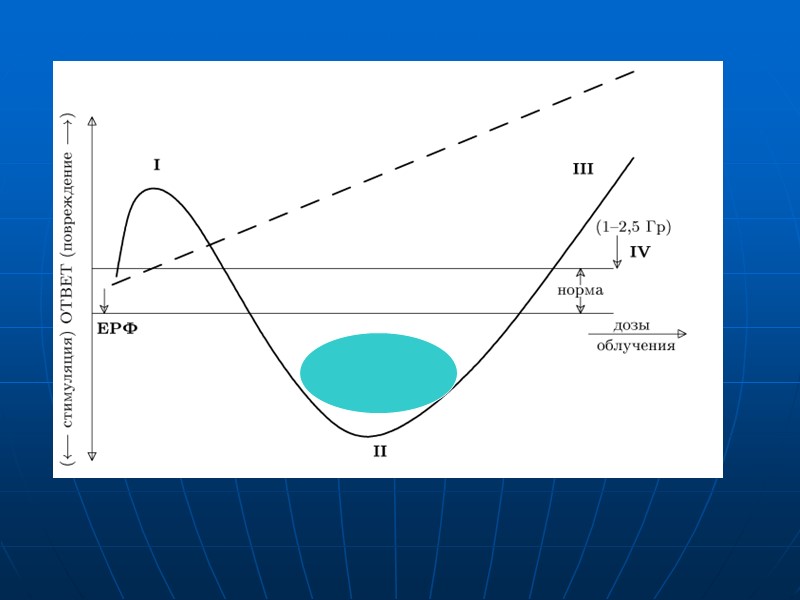
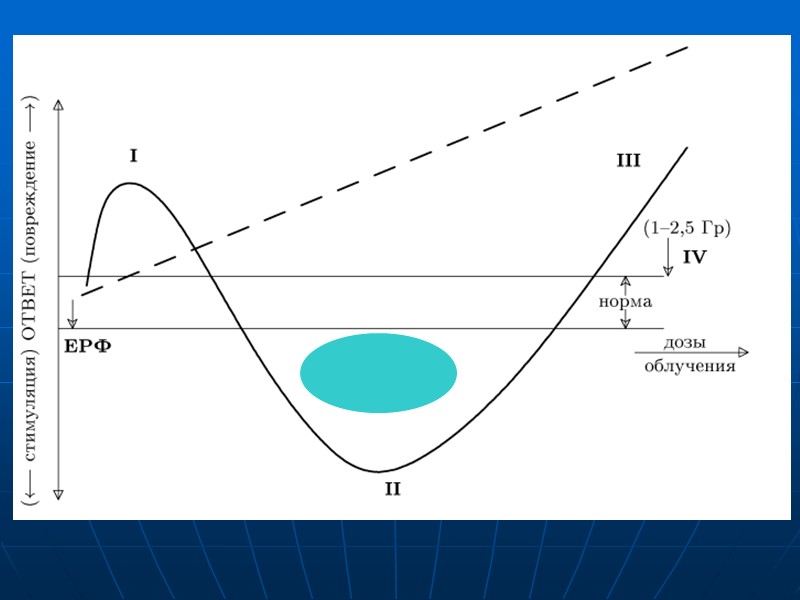
Как видно из схемы, для наиболее высоких значений сублеталъных доз (участок III) существует прямая зависимость ответа (размера повреждения) от величины дозы облучения. Немонотонная часть кривой, относится к малым дозам. Она имеет два противоположно направленных максимума: собственно малые дозы (участок II), вызывающие «гормезис» - стимуляцию жизненных процессов (табл. VII.1), и «сверхмалые» дозы - всплеск повреждений, соот-ветствующий эффекту гиперрадиочувствительности - эффект Петко(участок I). Естественный радиационный фон (ЕРФ) изображен на схеме в качестве начальной точки отсчета радиобиологических изменений.

АДАПТИВНЫЙ ОТВЕТ Адаптивный ответ - радиобиологический феномен, заключающийся в увеличении радиоустойчивости биологических объектов к большим, повреждающим дозам облучения после предварительного воздействия ионизирующей радиации в малых, неповреждающих дозах облучения.

АДАПТИВНЫЙ ОТВЕТ Радиобиологический феномен, заключающийся в увеличении радиоустойчивости биологических объектов к большим, повреждающим дозам облучения после предварительного воздействия ионизирующей радиации в малых, неповреждающих дозах облучения.

В 1984 г. итальянские исследователи во главе с доктором Оливиери (Oliviery) описали феномен увеличения радиорезистентности лимфоцитов человека in vitro после воздействия радиации в малых дозах. Первоначально было обнаружено, что в культуре лимфоцитов после добавления меченного тритием тимидина увеличивается устойчивость клеток к последующему действию редкоионизирующей радиации в больших, повреждающих дозах. В таких клетках образование структурных аберраций (в основном хроматидных) на единицу дозы значительно снижалось. Важно, что содержание радиоактивного тимидина оказалось таким, что за время эксперимента количество распадов атомов трития было сопоставимо с числом клеток в культуре, т. е. предварительное облучение было в малой дозе. Эксперименты, выполненные с большой тщательностью, исключали возможность влияния других, кроме облучения в малой дозе, факторов на исследуемые клетки. Результаты были подтверждены и в опытах с предварительным внешним рентгеновским облучением.

При этом эффект наблюдался только при предварительном действии редкоионизирующего излучения в малых дозах 10 - 200 мГр и не обнаруживался при облучении в дозах от 500 мГр и выше! Важно, что этот феномен был воспроизведен в десятках лабораторий во многих странах, и поэтому с конца 1980-х годов прошлого столетия вопрос о том, вызывает ли облучение в малых дозах характерные реакции биологических объектов, перестал вызывать сомнение. Феномен получил название адаптивного ответа, предварительную малую дозу облучения называют адаптирующей или предварительной, а большую повреждающую дозу - разрешающей или повреждающей.

Свое название феномен получил по аналогии проведенным еще в древности наблюдением о повышении устойчивости (адаптации) биологических объектов к многим ядам (химическим агентам) при предварительной обработке клеток или многоклеточных организмов, в том числе человека, этими же ядами в малых нетоксичных концентрациях. Тщательные исследования адаптивного ответа, предпринятые после опубликования работ группы Оливиери и других радиобиологов, позволили установить многие закономерности проявления этого феномена и выявить ряд молекулярных механизмов, приводящих к повышению радиоустойчивости клеток и многоклеточных организмов после действия радиации в малых дозах. Было показано, что адаптивный ответ наблюдается и у бактерий, и у дрожжевых клеток, и у клеток различных растений и животных.
Проявление адаптивного ответа регистрируется при использовании всех общепринятых тестов, характеризующих радиочувствительность клеток, таких как определение хромосомных и хроматидных аберраций, микроядер, генных мутаций, образование колоний (выживаемости клеток). Повышенная радиорезистентность наблюдается после облучения в малых дозах у многоклеточных организмов - разнообразных растений и животных. Адаптивный ответ проявляется не сразу после воздействия предварительной дозы: необходимо время для его формирования. Для большинства исследованных объектов максимальный эффект наблюдался спустя 6 ч после подведения адаптирующей дозы. Состояние повышенной устойчивости культивируемых клеток сохраняется не менее 24 часов, а у лимфоцитов человека in vitro - около 72 часов. При облучении животных адаптивный ответ наблюдался в течение недель и месяцев.
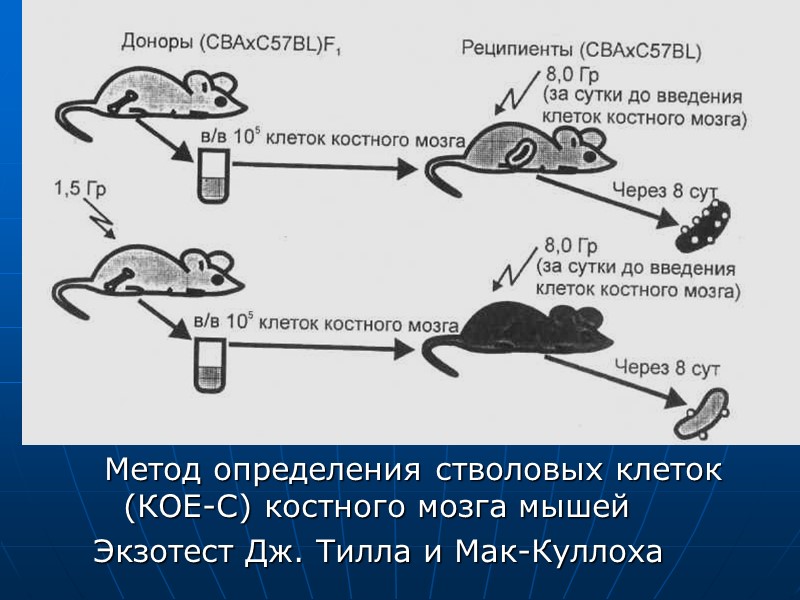
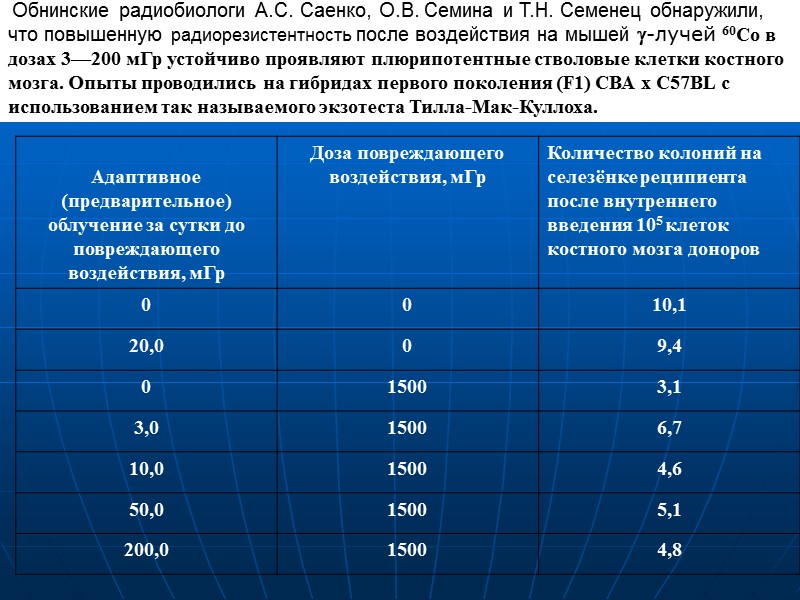
Обнинские радиобиологи А.С. Саенко, О.В. Семина и Т.Н. Семенец обнаружили, что повышенную радиорезистентность после воздействия на мышей -лучей 60Со в дозах 3—200 мГр устойчиво проявляют плюрипотентные стволовые клетки костного мозга. Опыты проводились на гибридах первого поколения (F1) СВА х C57BL с использованием так называемого экзотеста Тилла-Мак-Куллоха.

Метод определения стволовых клеток (КОЕ-С) костного мозга мышей Экзотест Дж. Тилла и Мак-Куллоха

В описанном эксперименте выявлены не только плюрипотентные стволовые клетки, способные после многократных делений в конечном итоге образовывать зрелые клетки любых кроветворных ростков, но и частично дифференцированные, «полустволовые» клетки. Такие клетки способны образовывать многоклеточные селезеночные колонии определенного типа клеток, например эритроидных или мегакариоцитарных, поэтому клетки, размножающиеся в селезенке с образованием колоний, называют колониеобразующими единицами КОЕ-С. Последняя буква обозначает «селезеночные». Она введена для указания на то, в каком органе указанные клетки (КОЕ) размножаются с образованием колоний, поскольку в дальнейших исследованиях выяснилось, что КОЕ могут образовывать колонии клеток и в других органах, например в легких.

Установлено, что проявление адаптивного ответа зависит от генетических особенностей разных линий клеток и животных. Например, он хорошо проявляется у мышей линии C57BL и практически отсутствует у животных линии СВА. При исследовании лимфоцитов человека выявлено, что клетки одних людей форми-руют выраженный ответ на предварительное воз-действие редкоионизирующих излучений в малых дозах, в то время как лимфоциты других не проявляют такой реакции. Таким образом, выраженность адаптивного ответа лимфоцитов людей носит индивидуальный характер.

Молекулярные механизмы адаптивного ответа так же, как и клеточного стресса постоянно изучаются. В опытах in vitro и in vivo установлено, что повышение радиорезис-тентности связано с усилением процессов репарации ДНК, активацией систем антио-ксидантной защиты и других установленных и еще не выявленных факторов. В формирова-нии адаптивного ответа участвуют АДФ-фосфорибозилтрансфераза, белки теплового шока, различные тирозинкиназы и многие другие компоненты сигнальной системы клетки.

Можно говорить о двух возможных способах реализации адаптирующих воздействий: 1)включение новой генетической программы, 2)индуцированные радиацией синтез белков и мобилизация антиокислителей, т. е. эндогенных защитных ресурсов клетки, в количествах, способных поддерживать состояние готовности к адаптивному ответу в течение нескольких клеточных поколений. Так, было обнаружено, что через 4-6 часов после воздействия -излучения в адаптирующих дозах в лимфоцитах человека появляются вновь синтезирован-ные белки, которые могут быть кандидатами на роль адаптивных белков. Известно также, что уже вскоре после действия ионизирующих излучений в адаптирующих дозах в клетке происходит накопление антиокислителей-адаптогенов, выполняющих функцию противолучевых средств.

Радиоадаптивный ответ обнаружен при облучении растительных и животных организмов, а также в опытах на лимфоцитах человека, мыши и кролика, фибробластах китайского хомячка, клетках костного мозга и сперматоцитах мышей. При адаптивном ответе можно достичь 50 - 60% снижения количества генных, хромосомных мутаций или других нарушений генома, а также иных проявлений повреждения биологических объектов. Наиболее общим, интегральным критерием адаптивного ответа в опытах на животных является изменение их выживаемости после повторного, проявляющего воздействия рентгеновского или -излучения.

Способность ионизирующих излучений к формированию адаптивного ответа зависит не только от величины дозы облучения, но и от ее мощности. При сравнительно больших дозах необходима невысокая ее мощность, и наоборот. Так, для многих типов клеток установлена связь между адаптирующей дозой D1 и ее мощностью D1/dt: D1*dD1/dt=const
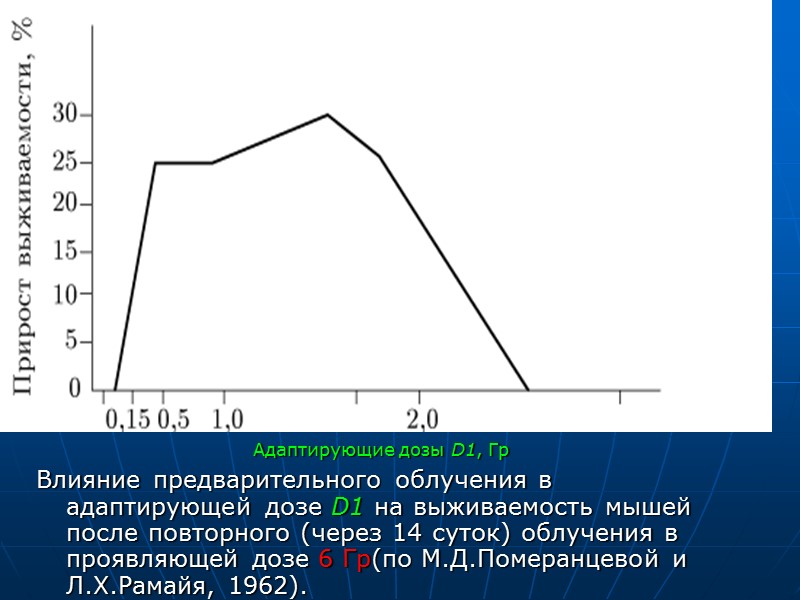
Адаптирующие дозы D1, Гр Влияние предварительного облучения в адаптирующей дозе D1 на выживаемость мышей после повторного (через 14 суток) облучения в проявляющей дозе 6 Гр(по М.Д.Померанцевой и Л.Х.Рамайя, 1962).

Таким образом, только при воздействии излучений в малых дозах (обычно в диапазоне до 200,0 мГр) наблюдается характерная реакция - адаптивный ответ, проявляющийся в последующем повышении радиоустойчивости клеток и макроорганизмов. При остром подведении больших доз эффект не регистрируется. Адаптивный ответ возникает в основном при действии в малых дозах редкоионизирующей радиации. При воздействии плотноионизирующих излучений в большинстве случаев эффект не наблюдается, хотя из теоретических соображений адаптивный ответ и при действии ряда корпускулярных излучений может быть индуцирован. Однако в этих случаях он, как правило, будет слабо выражен и будет проявляться в очень узком диапазоне доз, когда только часть клеток в популяции будет облучена, т. е. в условиях проявления эффекта «свидетеля», роль которого в формировании адаптивного эффекта еще не изучена.

Радиационный гормезис Еще в конце XIX века было известно, что ряд химических соединений оказывает стимули-рующий эффект на рост и развитие микроорга-низмов, грибов, водорослей, растений. Впоследствии это явление было обнаружено на самых разнообразных биологических объектах. Термин «гормезис» впервые появился в науч-ных публикациях в 1942 г. при описании стимуляции клеточного деления и роста грибка под влиянием антибиотика в малых концент-рациях, тогда как в больших концентрациях антибиотик оказывал угнетающее действие

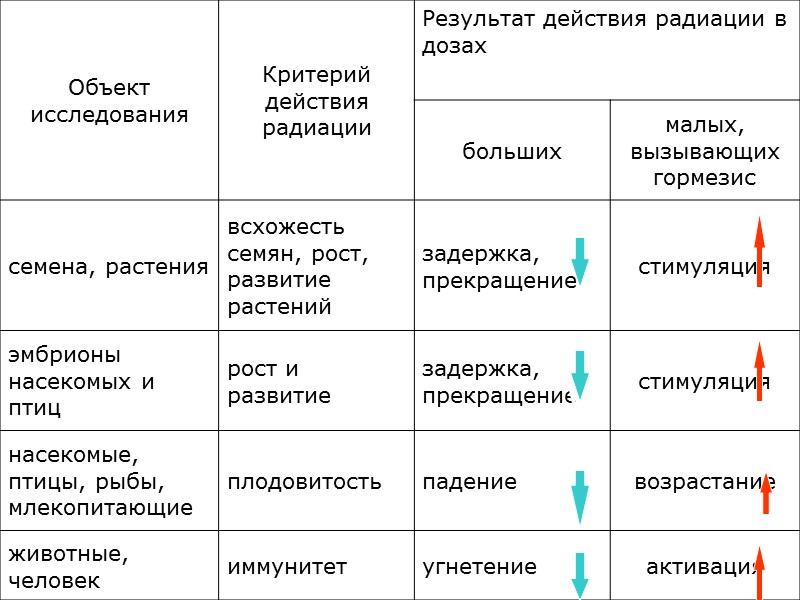
Таким образом, гормезис - это неспецифический эффект воздействий на живые организмы в малых дозах (концентрациях), вызывающих измене-ния, диаметрально противоположные повреждающим эффектам при воздей-ствии в больших дозах, то есть стимулирующим.

Вскоре после открытия Рентгеном ионизирую-щего излучения стали появляться отдельные сообщения, в которых наряду с поражающим действием больших доз радиации иногда обна-руживались и стимулирующие эффекты при облучении биологических объектов в малых дозах. Однако эти сообщения были немного-численны, и основное внимание радиобио-логических работ было приковано к поражаю-щему действию ионизирующих излучений. Беспороговая линейная концепция, предпола-гающая опасность любого, даже самого малого превышения естественного радиационного фона, была положена в основу рекомендаций МКРЗ. Мы уже отмечали, что эта парадигма не выдержала проверки временем.

В 1980 г. вышла монография Т. Д. Люкки, в которой автор обобщил данные литературы и привел собст-венные эксперименты о биологическом эффекте иони-зирующих излучений в малых дозах, которые в отли-чие от воздействия в больших, повреждающих дозах оказывают диаметрально противоположное, «благо-приятное», стимулирующее действие на рост, развитие и жизнедеятельность клеток и многоклеточных орга-низмов. Такие ответные реакции на облучение в малых дозах были объединены автором под названием «радиационный гормезис». Стало очевидным, что гормезисные эффекты, произво-димые радиацией в малых дозах, характеризуются теми же свойствами и теми же характеристическими параметрами описывающих их графиков, что и при химическом гормезисе.

Указанные наблюдения послужили основой для разработки ряда технологий использования облучения для практических целей: предпосадочного облучения семян, луковиц, клубней, черенков для увеличения урожаев. Однократное и хроническое облучение яиц, цыплят и кур приводит к снижению падежа и увели-чению яйценоскости, воздействие на молодняк различных сельскохозяйственных животных уве-личивает скорость прироста биомассы животных. Существует ряд и других наблюдений, указывающих на перспективность использования облучения для увеличения продуктивности сельскохозяйственных растений и животных. Однако несмотря на, казалось бы, очевидную полезность применения и относительную легкость организации использования облучения, эти методы почти не получили распространения

Широкое внедрение в практику достижений в изучении закономерностей радиационного гормезиса не происходит, очевидно, в большинстве случаев потому, что до сих пор не проведены долгосрочные исследования влияния такого облучения на потомство в поколениях облученных растений и животных. Кроме того, нет надежных данных об отсутствии вредного влияния продуктов, полученных из плодов, выращен-ных из облученных семян и клубней, на здоровье животных и людей при их систематическом использо-вании. В настоящее время в связи с развитием генно-инженерных и клеточных технологий повышения продуктивности растениеводства и животноводства, имеющих значительно более высокую эффективность по сравнению с радиационными, такие длительные исследования, необходимые для обоснования безопасности широкого использования феномена гормезиса в практике, вряд ли будут проведены.

В отношении полезности облучения в малых дозах для здоровья приводятся в основном положительные резу-льтаты использования радоновых ванн, пребывания на высокогорных курортах в качестве оздоровительных мероприятий. При использовании радоновых ванн получены экспериментальные результаты, указываю-щие, что их полезность зависит от концентрации радона в воде: существует оптимум его содержания, ниже и выше которого эффект оздоровления снижа-ется. За время лечебного курса (15 - 20 ванн) больной облучается в дозе около 3,0 мЗв. Если учесть, что в среднем при прохождении -частицы через клетку она облучается в дозе около 400 - 500 мЗв и подавляющая часть энергии поглощается отмершими или отмираю-щими клетками эпидермиса, то живых делящихся клеток кожи, получивших хотя бы один проход -частицы за время принятия ванны, чрезвычайно мало и сопоставимо с количеством клеток кожи, облучаемых в течение суток за счет естественного фона.

Поэтому доказательность приводимых сведений о полезности (гормезисе) для здоровья облучения организма в малых дозах сомнительна, тем более что эксперименты с радоновыми ваннами проведены практически в единичных количествах и не воспроизведены в других учреждениях. Однако полностью отрицать отсутствие реакции на облучение во время принятия радоновых ванн исключить пока нельзя. Полезность отдыха для здоровья в перечисленных условиях несомненно, однако при этом наряду с радиационным воздействием не учитываются другие, способствующие восстановлению и укреплению здоровья условия пребывания на отдыхе.

Таким образом, облучение в малых дозах разных биологических объектов в ряде случаев может привести к полезному эффекту. Этот эффект называется радиационным гормезисом, и его существование, в частности, в виде адаптивного ответа и повышения продуктивности растениеводства и животно-водства не вызывает сомнения. Существование радиационного гормезиса в отношении здоровья людей (лечебный, оздоровительный эффект) в настоящее время не является доказанным и требует дальнейшего изучения. Спасибо за внимание!

Малые дозы радиации Лекция 2 Эффект Петко Эффект свидетеля Нестабильность генома Канцерогенез

1. Гиперрадиочувствительность В конце прошлого столетия появились сообщения о том, что однократное облучение клеток млекопитающих в сверхмалых дозах - от исходной «нулевой» отметки ЕРФ до ~ 5-20 сГр, вызывает у них так называемый эффект гиперрадиочувствительности (рис. 1, I), оцениваемой по биохимическим (нарушение окислительно-восстановительного гомеостаза) и цитогенетическим показателям (аберрации хромосом, выход клеток с микроядрами, злокачественная трансформация и др. прецизионные показатели), имеющим при больших дозах облучения связь с выживаемостью клеток.

Впервые такой эффект обнаружил канадский ученый А. Петко в 1972 году, который обнаружил, что одна и та же доза подведенная хронически, т.е. растянутой по времени, вызывает большие изменения проницаемости БМ, чем острая, кратковременная. При мощности дозы 26 рад/мин проницаемость БМ менялась при дозе 3,5 тысяч рад, а при мощности дозы 10-3 рад/мин достаточно было дозы 0,7 рад, то есть в 5 тысяч меньше

Этот феномен обратной зависимости от мощности дозы при облучении клеток в незначительной по величине дозе и их гиперчувствительности по некоторым критериям при облучении в сверхмалых дозах получил впоследствии название «эффект Петко» (Р. Грейбс, 1996).


Обнаруженное изменение получило название эффекта сверхмалых доз или «эффекта колокола». Показано, что в основе его лежат нарушения конкурент-ных отношений между про- и антиоксидантами в окислительно-восстановительном гомеостазе, возни-кающие при облучении в сверхмалых дозах в клетках и тканях животных и растений, одиночных клетках и биологических мембранах. Эти изме-нения наблюдаются как при кратко-временном, так и пролонгированном облучении в сверхмалых дозах.
Так, у мышей после общего хронического внешнего воздействия -излучения (мощность дозы 0,6 мГр/сут) установлены статистически достоверные изменения уровня содержания в надпочечниках адреналина и кортико-стероидов: возрастание на 1/3 при дозе 0,6 мГр, возвращение к норме после облучения в дозе 1,2 мГр и начало падения ниже нормы уже при воздействии в дозах 2,4 - 5,4 мГр (Е. Н. Гончаренко и соавт., 2000).

В последние годы появились работы, позволяющие более полно характеризовать природу «эффекта колокола» в организмах, облученных в сверхмалых дозах: наблюдаемые изменения уровней содержания АФК, ППОЛ и АО у животных, облученных в сверхмалых дозах, характерны для неспецифических реакций живых систем на слабые воздействия

Таким образом, изменения внутри-клеточных структур, наблюдающиеся после облучения в очень незначительных по величине дозах отражают асинхронностъ конкурентных процессов повреждения и репарации, окисления и восстановления. Другими словами уровень сигнала повреждающего воздействия облучения на клетку настолько низок, что системы репарации не запускаются.

В качестве одного из примеров гиперрадиочувствительности, проявляющейся в тканях облученных организмов, можно привести данные из работ Е. Б. Бурлаковой. Автором этих исследований обнаружено, что уже при незначительном (на 1-3 порядка) превышении ЕРФ при общем однократном облучении в диапазоне сверхмалых доз наблюдается характерный «колоколообразный» по форме кривой всплеск оксидативных изменений в липидах.

4. Эффект свидетеля «Эффект свидетеля» в радиобиологии – это феномен, заключающийся в проявлении «лучевых» повреждений в необлученных клетках, находящихся вблизи от облученных клеток в момент воздействия ионизирующей радиации, т. е. необлученные в данной ситуации клетки являются «свидетелями» нанесения лучевых повреждений другим клеткам.

Опосредованное повреждающее действие облученных клеток на необлученные может осуществляться, например, воздействием на нор-мальные клетки средой, в которой культивировались облученные клетки, или биологическими жидкостями облу-ченного макроорганизма. Широкое толкование эффекта свидетеля пред-ложено известным радиобиологом Б. Джорджевичем в 2000 г.

В отличие от адаптивного ответа эффект свидетеля проявляется не только и не столько при действии радиации в малых дозах, но и в больших, вызывающих значительную гибель клеток. В области малых доз проявление эффекта свидетеля более характерно для воздействия плотноионизирующих, а не редкоионизирующих излучений. Для адаптивного ответа наблюдается обратная картина.

Наиболее важные результаты по изучению закономерностей и механизмов проявления эффекта свидетеля в области малых доз получены при использовании трёх экспериментальных подходов:

Путём воздействия -излу-чения в очень низких дозах, при которых непосредственно повреждается небольшая часть клеток, а остальные остаются необлучёнными, т. е. не име-ющими ни одного трека от прохождения -частицы;

Облучением клеток микропучками (в основном -частиц), площадь которых значительно меньше размеров ядра клетки, в резуль тате этого можно воздействовать на отдельные участки клетки, например на участок ядра или цитоплазмы, не затраги- вая другие;

Путём использования защитных микрорешеток, которые позволя-ют экранировать большую или меньшую часть клеток, растущих слоем на поверхности в момент воздействия радиации в малых или больших дозах.

Одними из первых проявление эффекта свидетеля наблюдали в своих экспериментах X. Нагасава и Дж. Литтл (1992). Было отмечено, что воздействие альфа-излучения в малой дозе (менее 1 % непосредственно поражённых ра-диацией ядер клеток) приводило к сестринским хроматидным обменам почти в трети клеток, при-сутствовавших при облучении.

В дальнейшем с помощью указанных подходов было показано, что в необлученных клетках-свидетелях увеличивается число хромосомных и хроматидных аберраций, микроядер, генных мутаций, повышается число трансформированных клеток. При использовании микропучков -частиц установлено более сильно выраженное проявление эффекта свидетеля при воздействии малых доз.

В экспериментах вместо клеток-свидетелей использовали в качестве свидетелей клеточные ядра, так как лучевому воздействию подвергалась только цитоплазма клеток. Было выявлено, что при прохождении через цитоплазму клетки одной a-частицы число генетических повреждений (генных мутаций) в таких клетках увеличивается вдвое. Однако, чтобы добиться троекратного увеличения мутаций, необходимо воздействие в среднем четырёх частиц.

Результаты экспериментов свиде-тельствуют о том, что при воздействии радиации в малых дозах выход повреждений на единицу дозы в связи с существованием эффекта свидетеля может быть большим, чем при облучении в больших дозах. Этот вывод, полученный при изучении воздействия радиации на цитоплазму, был подтвержден и в опытах Г. Жу и соавторов (2001) на конфлюентной (покоящейся) культуре гибридных фибробластов с облучением ядер.

При воздействии плотно- и редкоионизирующей радиации в низких, в том числе малых дозах, на всю клетку интенсивность проявления эффекта присутствия мало зависит от дозы облучения. Исследования механизма повреждающего воздействия облученных клеток на необлучённые клетки-свидетели выявили три независимых способа оказания такого влияния.

Первый из них хорошо известен как непрямое действие, связанное с образованием активных форм кислорода и, вероятно, других радикалов. Действительно, добавление анти-оксидантов перед облучением части клеток снимает в значительной мере проявление эффекта свидетеля — уменьшает количество повреждений в необлученных клетках. Однако молекулярные изменения в мутировавших генах были похожи на изменения, возникающие при спонтанных мутациях, но не тех, которые возникают в облученных клетках.

Второй механизм используется только при тесном контакте облученных и необлученных клеток. Сигнал на повреждение передается через клеточные контакты. В конфлюентных сливных клеточных культурах, где передача сигнала через клеточные контакты заблокирована, клетки-свидетели повреждаются или испы-тывают злокачественную трансформацию в значительно меньшей степени. Молекулярные механизмы этого процесса неизвестны.

Третий механизм, напоминающий первый, заключается в передаче сигнала неповреждённым клеткам через культуральную среду, в которой находились облученные клетки. Перенесение необлученных клеток из нормальной питательной среды в среду, в которой росли облученные клетки, приводило к гибели части нормальных клеток путем апоптоза. Повреждающих факторов в облученной среде в отсутствие клеток обнаружено не было. Следовательно, токсические факторы выделяются в среду облучёнными клетками. Выделяемые в питательную среду вещества, которые вызывают гибель необлучённых клеток, обнаружены К. Мазерсилл (2000) только после подведения довольно значительных доз фотонных излучений - 0,5 Гр и выше, и их образование было связано с биохимическими процессами гликолиза.
Однако оказалось, что не все облучённые клетки выделяют токсические факторы и не все необлучённые клетки чувствительны к их воздействию. Природа повреждающих агентов не выяснена. Известно также, что помимо факторов, индуцирующих апоптоз, облученные клетки выделяет и кластогенные, индуцирующие в необлучённых клетках хромосомные аберрации. Однако наличие кластогенных факторов уверенно проде-монстрировано только в опытах in vivo. В опытах in vitro кластогенные факторы только начинают изучаться. Они были обнаружены и после облучения сывороток крови и плазмы людей in vitro.

Повышенное содержание кластогенных факторов обнаружено в сыворотках людей и животных, подвергнутых действию радиации в малых дозах, например у ликвидаторов аварии на ЧАЭС. У некоторых облучённых в малых дозах лиц высокое содержание кластогенных факторов обнаруживается даже через 30 лет после воздействия. Однако кластогенные факторы обна-руживаются не у всех облучённых и необлучённых людей.

Подтверждением выделения облучён-ными клетками макроорганизма факторов, вызывающих нарушения в необлученных клетках, служит факт нахождения повреждённых клеток в тканях вне зоны облучения у больных, подвергнутых локальному лучевому лечению. Например, локальное облу-чение тканей, находящихся ниже диафрагмы, вызывает повреждения в клетках и тканях, расположенных выше диафрагмы.

Этот феномен получил название «Abscopal effects». Показано также, что введение облучённых клеток костного мозга необлучённым животным вызывает хромосомные аберрации в клетках костного мозга животного-реципиента. Природа образующихся или синтезирующихся повреждающих фак-торов в облучённых донорских клетках не известна.

Эффект «свидетеля» у мышей или крыс (по Б.П. Суринову и др., 1998)

1 2 2 1 2 2 2 2 2 1

Проявление эффекта свидетеля может осуществляться и на популяционном уровне у животных. Б.П. Суринов с сотрудниками (2001) из Медицинского радиологического научного центра РАМН показали, что при помещении облучённой мыши в клетку к необлучённым животным через сутки у интактных животных наблюдались изменения в крови и в иммунном статусе, сходные с обнаруженными у облучённых особей. Оказалось, что повреждающие агенты, выделяющиеся облучёнными мышами с мочой, достаточно летучи и действуют на обонятельный анализатор необлучённых животных, вызывая изменения в физиологических показателях .

Таким образом, обнаружение эффекта свидетеля в радио-биологических экспериментах показало, что поражающее действие радиации может быть связано не только с прямым действием неё на клетки, но и с повреждающим действием облу-чённых клеток на необлучённые.

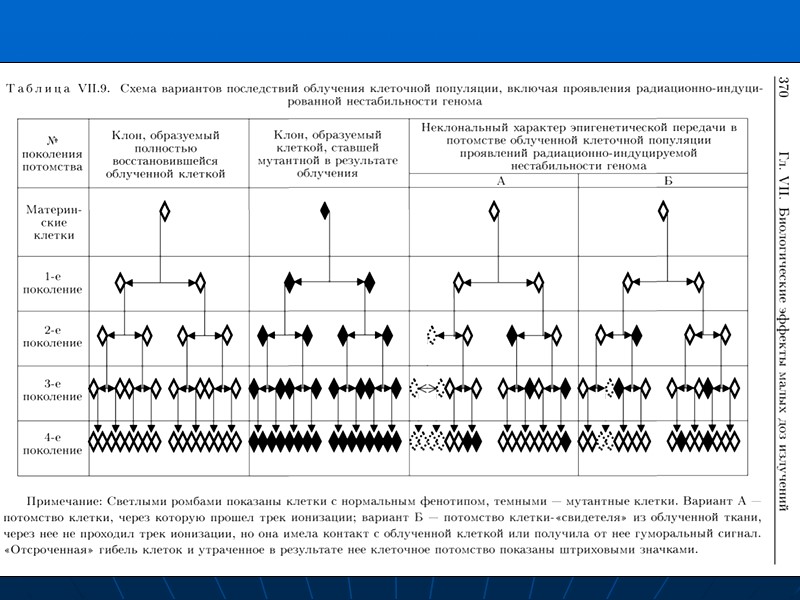
5. Нестабильность генома Радиационно-индуцированная неста-бильность генома - это явление повышенной частоты образования генетических нарушений у потомков облученных клеток. Феномен заклю-чается в образовании de novo множественного появления геномных, хромосомных, хроматидных и генных мутаций неклонального характера, т. е. возникающих в геноме потомков облученных клеток случайным образом, а не передающихся по наследству.
Нестабильность может проявляться в отдалённые сроки после облучения через много циклов деления (иногда сотен), и в некоторых генерациях число клеток со структурными мутациями in vitro может достигать 10 % и более от всей популяции клеток, при этом наблюдается массовая гибель клеток.

У многоклеточных организмов нестабильность генома проявляется в увеличении числа (частоты) соматических мутантных клеток. Состояние нестабильности генома может сохраняться регулярно и на протяжении десятков поколений клеток. Это явление обнаружено после облучения клеток и животных в больших дозах. Одними из первых учёных, описавших в 70 - 80-х годах прошлого столетия такое явление, были отечественные исследователи И.Б. Бычковская, И.И. Пелевина и др. Результаты их исследований и ряда зарубежных лабораторий показали, что нестабильность генома может проявляться и у потомков клеток, облученных в малых дозах.

Установлено, что нестабильность генома проявляется после действия как плотно-ионизирующих, так и редкоионизирующих излучений. Однако у ряда культивируемых объектов in vitro при действии фотонного излучения повышенного образования генетических нарушений у потомков облученных клеток на хромосомном уровне не удаётся обнаружить, хотя после воздействия -частиц нестабильность генома, проявляющаяся в повышенном образовании хромосомных и хроматидных поломок, легко выявляется.

Одновременное исследование генных и хромосомных мутаций в потомках стволовых клеток костного мозга после воздействия излучений с разной ЛПЭ показало, что в отличие от хромосомных генные мутации возникают с повышенной частотой как при действии -излучения, так и при воздействии рентгеновского излучения.

Следовательно, вывод об отсутствии проявления нестабильности генома в потомках облучённых клеток в тех исследованиях, где в качестве показателя нестабильности используются структурные мутации, не является окончательным. В этих случаях, особенно при воздействии редко-ионизирующей радиации, для такого заключения требуется провести определение частоты генных мутаций.

Таким образом, механизмы форми-рования генетической нестабильности на хромосомном и генном уровнях отличаются, вероятно, лишь частично, что подтверждают наблюдения, выполненные в МРНЦ РАМН под руководством И.А. Замулаевой и А.В. Севанькаева. Ими отмечено: у части лиц, подвергшихся облучению в малых дозах на атомных производствах или проживающих на загрязненных территориях, в отдалённые сроки после воздействия наблюдается увеличение генных и хромосомных мутаций в лимфоцитах периферической крови.

Увеличение числа клеток с генетическими нарушениями у таких лиц, вероятно, связано с проявлением феномена генетической нестабильности. Оказалось, что практически у всех лиц с повышенными частотами структурных мутаций увеличено число клеток с генными мутациями, но у лиц с повышенной частотой генных мутаций приблизительно в половине случаев повышение числа хромосомных нарушений не обнаружено.

Другое важное наблюдение законо-мерностей проявления нестабильности генома - малая зависимость (или ее отсутствие) от дозы облучения в большом диапазоне доз. Увеличение числа клеток-потомков с генетическими изменениями было приблизительно одинаковым и при использовании воздействия в малой дозе, и при подведении большой дозы. Не наблюдалось отличий в количественном проявлении нестабильности генома по тесту генных мутаций при подведении больших доз рентгеновского излучения в диапазоне от 2,0 до 12,0 Гр.

При клонировании in vitro потомков облученных клеток, т. е. получении и исследовании популяций клеток, полученных в результате размножения индивидуальных клеток-потомков, установлено, что они не все проявляют генетическую нестабильность, а генетически нестабильные клетки могут восстанавливать стабильность генома, сохранять тот же уровень нестабильности или «становиться» еще более нестабильными.

Молекулярные изменения, происходящие в генетическом материале при возникновении генных мутаций у «нестабильных» потомков облученных клеток, сходны с молекулярными изменениями, происходящими при спонтанном мутировании нормальных интактных клеток, и следовательно, отличаются по спектру изменений в молекулах ДНК у непо-средственно облучённых клеток. Спектр структурных мутаций, наблюдаемых в отдалённые сроки у людей, облучённых в малых дозах в результате аварии на ЧАЭС, также отличается от спектра мутаций в облучённых клетках.

Так, на хромосомном уровне в отдалённые сроки преобладают одиночные и парные фрагменты, а в непосредственно облучённых клетках наблюдается значительное число дицентриков и кольцевых центрических хромосом. Повышенные частоты соматических мутаций обнаруживаются и у детей облучённых в больших и малых дозах родителей. Однако вопрос о проявлении нестабильности генома у детей облучённых родителей еще очень мало изучен и поэтому здесь не рассмотрен.

Механизм возникновения и поддержания нестабильности генома у потомков облученных клеток изучен недостаточно. Имеющиеся экспери-ментальные данные и эпидемио-логические наблюдения позволяют полагать, что существует несколько механизмов, участвующих в формиро-вании генетической нестабильности.

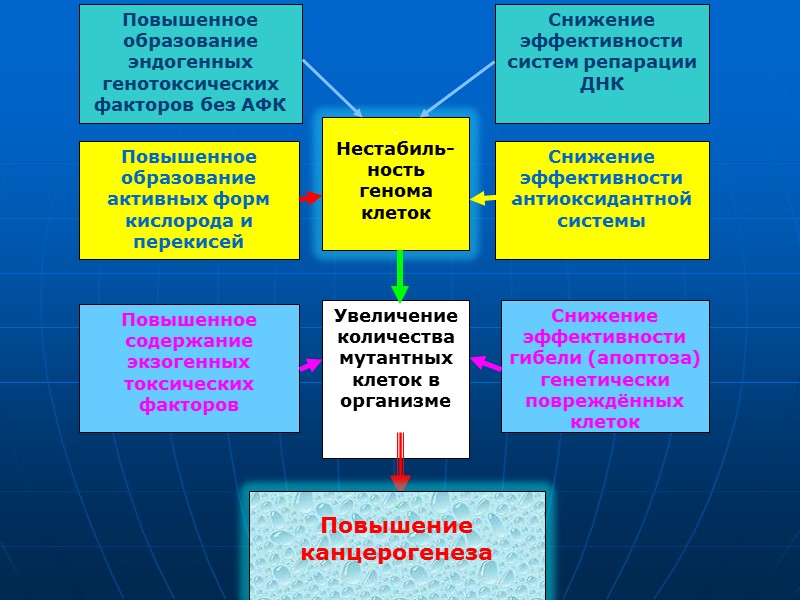
Большая часть исследователей считает, что облучение вызывает долговременное измене-ние клеточной системы поддержания системы окислительно-восстановительного гомеостаза, выражающееся в усилении продукции актив-ных форм кислорода. Повышенное обра-зование активных форм кислорода приводит к увеличению оксидативных повреждений в молекулах ДНК и, как следствие, к увеличению количества мутаций. Это предположение основывается на повышенном содержании перекисных радикалов в культуральных средах, в которых растут потомки облученных клеток. В таких средах, как было сказано выше, имеются и другие активные вещества, например кластогенные факторы.
Другим возможным механизмом создания и поддержания генетической нестабильности является нарушение системы контроля клеточного цикла. Прохож-дение клетки по клеточному циклу — это цепь последовательных событий, основными участниками которой являются компоненты системы передачи и анализа внешних и внутренних сигналов, определяющих судьбу клетки. Упрощенно это звучит так - в результате работы этой системы решается вопрос, что будет с клеткой в ближайшем будущем:

-Будет ли она делиться (давать потомство себе подобных дочерних клеток, так как для этого имеются потребности и условия); -Выполнять уже приобретенные функции, не участвуя в увеличении численности популяции (выход из клеточного цикла путем перехода в фазу Go); -Приобретать новые функции путём дальнейшей дифференцировки, созрева-ния (в результате которого, например, поддерживается необходимая численность специализированных зрелых клеток в той или иной ткани у животных и человека); -Включать программу собственной гибели в основном путем апоптоза.


В ходе прохождения клеточного цикла клетка проходит два важнейших контрольных пункта: на границе перехода из фазы G1 в фазу синтеза ДНК - S-фазу и фазу G2, т. е. непосредственно перед делением. В этих контрольных пунктах клетки с возникшими дефектами в генетическом материале задерживаются, в результате чего создаются условия для ликвидации нарушений до их фиксации, превращения в стабильные изменения - мутации. В настоящее время имеются веские экспериментальные аргументы, свидетельствующие о причастности этой системы контроля в поддержании генетической стабильности клеток на молекулярном уровне.

В результате функционирования «сигнальной» системы поддерживается генетическая стабильность клеточной популяции и на клеточном уровне: поврежденным (например, с нарушениями в структуре ДНК) или ненужным организму (такие условия создаются, например, в эмбриогенезе) клеткам дается команда на самоуничтожение - апоптоз. Ключевая роль в поддержании генетической стабильности клеток и клеточных популяций принадлежит белку р53.

Данные, полученные в ходе изучения генетической нестабильности клеток многоклеточного организма, в том числе и у человека, путем определения количества (частоты) клеток с генными и структурными мутациями, дают основание говорить о том, что повышенный уровень мутантных клеток может быть следствием либо увеличения интенсивности мутагенеза, либо снижения эффективности ликвидации мутантных клеток путём апоптоза - программированной клеточной гибели.

Повышение частоты мутагенеза (нестабильность генома) может быть обусловлено не только увеличением интенсивности внесения повреждений в молекулы ДНК, но и снижением эффективности функционирования систем ликвидации таких повреждений - систем репарации ДНК. В ряде экс-периментов выявлено снижение эффективности репарации ДНК при проявлении радиационно-индуциро-ванной генетической нестабильности.

Однако роль этого механизма в поддержании нестабильности генома у потомков облучённых клеток до конца еще не выяснена. Косвенным указанием на снижение активности систем репарации ДНК у потомков облучённых клеток и причиной нестабильности генома служит существование другого феномена, проявляющегося при действии радиации в малых дозах - повышенной чувствительности к действию радиации и других токсических для клеток факторов.
Нарушение процесса репарации ДНК может являться не единственной причиной такого «обратного» адаптив-ного ответа. Повышение радио-чувствительности может быть связано с ухудшением защитных механизмов, например системы антиоксидантной защиты, и(или) нарушением контроля клеточного цикла. В любом случае повышение чувствительности к действию генотоксических факторов эндогенного и экзогенного происхождения будет сопровождаться увеличением мутагенеза в соматических клетках.

Таким образом, после действия радиации как в малых, так и в больших дозах у необлученных потомков облученных родительских клеток проявляется нестабильность генома, т. е. происходит повышенное образование структурных и генных мутаций. Феномен нестабильности генома прослеживается в десятках и сотнях поколений клеток in vitro, а в организме животных и человека проявляется в отдаленные после облучения сроки в виде увеличения количества, частоты клеток с генетическими нарушениями, представ-ляющими собой геномные, хроматидные, хромосомные, генные мутации и микроядра.

Нестабильность генома в потомках про-является после действия на родитель-ские клетки как редкоионизирующих, так и плотноионизирующих излучений. Последние более стабильно индуцируют генетическую нестабильность, прояв-ляющуюся на хромосомном уровне. У потомков клеток после воздействия редкоионизирующей радиации неста-бильность на хромосомном уровне возникает не всегда. Интенсивность проявления нестабильности не зависит от дозы облучения родительских клеток в большом диапазоне доз.
Важнейший вывод, следующий из результатов проведенных иссле-дований по изучению нестабиль-ности генома, а также эффекта свидетеля, заключается в том, что часть этого эффекта не является следствием непосредственного дей-ствия радиации на клетки, а может быть индуцирована сигналами от облученных клеток, т. е. с помощью эпигенетических механизмов.

Проявление генетической нестаби-льности у потомков облучённых клеток в связи с первостепенной ролью генных и хромосомных мутаций в индукции злока-чественных опухолей ставит вопрос о значении этого феномена в радиационном канцерогенезе, особенно при воздействии ионизирующего излучения в малых дозах.

При воздействии в малых дозах риск развития злокачественной трансформации и возникновения опухолей в отдалённые сроки после воздействия радиации на единицу дозы за счет развития неста-бильности генома у потомков облучённых и необлучённых, но получивших сигналы от облучённых клеток, может быть значительно выше, чем при воздействии в больших дозах.


Изучение радиационного канцерогенеза имеет достаточно долгую историю. Впервые пагубные явления рентгеновских лучей были обнаружены вскоре после их открытия в 1895 Рентгеном. Первыми наблюдаемыми эффектами были покраснение и образование пузырей на коже в течение часов или дней после воздействия радиации. После 1902 года становится очевидным, что рак является одним из замедленных эффектов воздействия радиации.

По данным исследований эпидемиологов воздействие в течении жизни 1мЗв радиации на 100000 населения приводит к возникновению 65 случаев лейкоза и 495 случаев других форм злокачественных опухолей. На основании этих расчетов ученые пришли к выводам, что 4-5% всех злокачественных опухолей человека связаны с ионизирующей радиацией.

Многочисленными работами показано, что ионизирующее излучение вызывает практически все формы злокачественных новообразований, кроме лимфобластного лейкоза, лимфогранулематоза, рака шейки матки и простаты. Наиболее распространенными опухолями при радиационном канцерогенезе являются лейкемия, рак кожи, лимфомы, опухоли мозга.

Оценки латентного периода 7-10 лет для лейкемии, 10-15 лет для остеосаркомы, 27 лет опухоли головного мозга, 25 лет для рака легкого, 24 года для рака кожи.

Помимо активации чекпойнтов и задержки клеточного цикла, при действии радиации происходит индукция целого ряда генов. Среди них можно назвать гены раннего ответа c-jun и Egr-1; гены позднего ответа фактор некроза опухолей (TNF-α) и PDGF-α; активация интерлейкина IL-1 и онкогенов c-myc и K-ras. Будучи активированными, эти гены запускают события, которые приводят к канцерогенезу.

Р53, часто называемый «стражем генома», играет неоспоримую роль в регуляции процессов канцерогенеза. P53 способен переводить клетку в состояние остановки клеточного цикла, апоптоза, старения, защищая ее, таким образом, от трансформации в раковую клетку.
16-effekty_malyh_doz_radiacii1.pptx
- Количество слайдов: 107

