иммуноглобулины Одной из форм реагирования иммунной

































zanyatie_9._immunoglobuliny.ppt
- Размер: 1.9 Мб
- Автор: Георгий Филин
- Количество слайдов: 38
Описание презентации иммуноглобулины Одной из форм реагирования иммунной по слайдам
 иммуноглобулины
иммуноглобулины
 Одной из форм реагирования иммунной системы в ответ на внедрение в организм антигена является биосинтез антител — белков, специфически реагирующих с антигенами. Антитела, также как и фагоцитоз, — это одна из наиболее филогенетически древних форм иммунной защиты. Антительный ответ обнаруживается уже у некоторых видов рыб
Одной из форм реагирования иммунной системы в ответ на внедрение в организм антигена является биосинтез антител — белков, специфически реагирующих с антигенами. Антитела, также как и фагоцитоз, — это одна из наиболее филогенетически древних форм иммунной защиты. Антительный ответ обнаруживается уже у некоторых видов рыб
 Антитела относятся к γ-глобулиновой фракции белков сыворотки крови. На долю γ-глобулинов приходится 15 -25 % белкового содержания сыворотки крови, что составляет примерно 10 -20 г/л. Поэтому антитела получили название иммуноглобулинов , и их обозначают символом I g.
Антитела относятся к γ-глобулиновой фракции белков сыворотки крови. На долю γ-глобулинов приходится 15 -25 % белкового содержания сыворотки крови, что составляет примерно 10 -20 г/л. Поэтому антитела получили название иммуноглобулинов , и их обозначают символом I g.
 Антитела – это γ-глобулины, вырабатываемые в ответ на введение антигена, способные специфически связываться с антигеном и участвовать во многих иммунологических реакциях. Антитела синтезируются В-лимфоцитами и их потомками – плазматическими клетками.
Антитела – это γ-глобулины, вырабатываемые в ответ на введение антигена, способные специфически связываться с антигеном и участвовать во многих иммунологических реакциях. Антитела синтезируются В-лимфоцитами и их потомками – плазматическими клетками.
 Иммуноглобулины существуют в циркулирующей форме , в виде рецепторных молекул на иммунокомпетентных клетках миеломных белков. Циркулирующие антитела подразделяются на сывороточные и секреторные. К антителам могут быть также отнесены белки Бенс-Джонса , которые являются фрагментами молекулы Ig (его легкая цепь) и синтезируются в избытке при миеломной болезни.
Иммуноглобулины существуют в циркулирующей форме , в виде рецепторных молекул на иммунокомпетентных клетках миеломных белков. Циркулирующие антитела подразделяются на сывороточные и секреторные. К антителам могут быть также отнесены белки Бенс-Джонса , которые являются фрагментами молекулы Ig (его легкая цепь) и синтезируются в избытке при миеломной болезни.
 Иммуноглобулины являются гликопротеидами. Мономеры иммуноглобулинов состоят из двух тяжелых (Н-цепи) и двух легких ( L -цепи) полипептидных цепей, связанных дисульфидной связью. Между тяжелыми цепями также есть дисульфидная связь. Это так называемый «шарнирный участок » . Такой тип межпептидного соединения придает структуре молекулы динамичность — он позволяет легко менять конформацию в зависимости от окружающих условий и состояния.
Иммуноглобулины являются гликопротеидами. Мономеры иммуноглобулинов состоят из двух тяжелых (Н-цепи) и двух легких ( L -цепи) полипептидных цепей, связанных дисульфидной связью. Между тяжелыми цепями также есть дисульфидная связь. Это так называемый «шарнирный участок » . Такой тип межпептидного соединения придает структуре молекулы динамичность — он позволяет легко менять конформацию в зависимости от окружающих условий и состояния.
 Легкие цепи бывают 2 типов : κ и λ (каппа и лямбда). Тяжелых цепей известно 5 типов : α, γ, μ, ε и δ (альфа, гамма, мю, эпсилон и дельта), — которые имеют также и внутреннее подразделение. Среди многообразия цепей α-типа выделяют α l — и α 2 — подтипы, а μ-цепей— μ 1 — и μ 2 -. Для γ-цепи известны 4 подтипа: γl -, γ 2 -, γ 3 — и γ 4 -.
Легкие цепи бывают 2 типов : κ и λ (каппа и лямбда). Тяжелых цепей известно 5 типов : α, γ, μ, ε и δ (альфа, гамма, мю, эпсилон и дельта), — которые имеют также и внутреннее подразделение. Среди многообразия цепей α-типа выделяют α l — и α 2 — подтипы, а μ-цепей— μ 1 — и μ 2 -. Для γ-цепи известны 4 подтипа: γl -, γ 2 -, γ 3 — и γ 4 -.
 Папаин расщепляет молекулу иммуноглобулина на два одинаковых антигенсвязывающих фрагмента — Fab (Fragment antigen binding) и Fc (Fragment cristallizable). Антигенсвязывающий участок (активный центр антител) Fab -фрагмента иммуноглобулина, образован гипервариабельными участками Н- и L -цепей; он связывает эпитопы антигена. В активном центре имеются специфичные комплементарные участки к определенным антигенным эпитопам. Fc -фрагмент связывает комплемент (при образовании комплекса антиген-антитело), взаимодействует с мембранами клеток и участвует в переносе Ig. G через плаценту.
Папаин расщепляет молекулу иммуноглобулина на два одинаковых антигенсвязывающих фрагмента — Fab (Fragment antigen binding) и Fc (Fragment cristallizable). Антигенсвязывающий участок (активный центр антител) Fab -фрагмента иммуноглобулина, образован гипервариабельными участками Н- и L -цепей; он связывает эпитопы антигена. В активном центре имеются специфичные комплементарные участки к определенным антигенным эпитопам. Fc -фрагмент связывает комплемент (при образовании комплекса антиген-антитело), взаимодействует с мембранами клеток и участвует в переносе Ig. G через плаценту.
 Компактные структуры антител, скрепленные дисульфидной связью называются доменами. Так, в Ig. G различают: вариабельные V -домены легких ( VL ) и тяжелых ( VH ) цепей, расположенные в N -концевой части Fab -фрагмента; С-домены константных участков легких цепей ( CL ); С-домены константных участков тяжелых цепей ( CHI , CH 2, СНЗ). В СН 2 -домене находится комплементсвязывающий участок.
Компактные структуры антител, скрепленные дисульфидной связью называются доменами. Так, в Ig. G различают: вариабельные V -домены легких ( VL ) и тяжелых ( VH ) цепей, расположенные в N -концевой части Fab -фрагмента; С-домены константных участков легких цепей ( CL ); С-домены константных участков тяжелых цепей ( CHI , CH 2, СНЗ). В СН 2 -домене находится комплементсвязывающий участок.
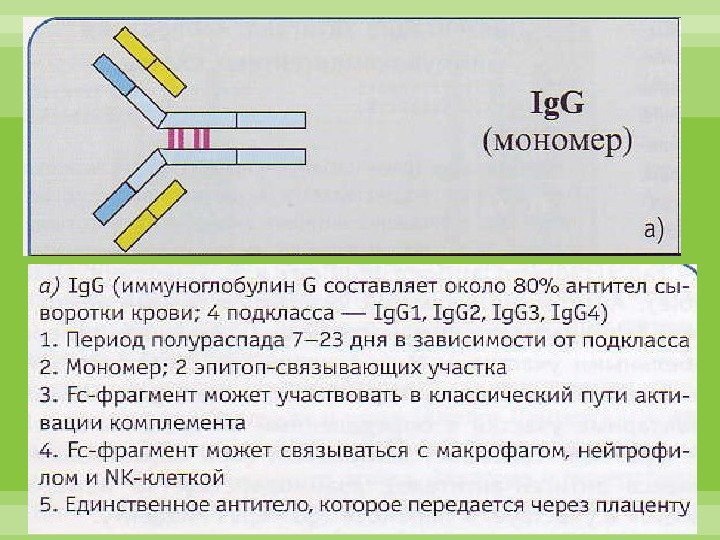
 В зависимости от особенностей молекулярного строения тяжелой цепи (т. е. наличия изотопических, или групповых антигенных детерминант) различают 5 классов, или изотипов Ig. Молекулы, содержащие тяжелую цепь α-типа, относят к изотипу А (сокращенно Ig. A); Ig. D обладает δ -цепью, Ig. E — ε-цепью, Ig. G — γ-цепью Ig. M — μ-цепью. Соответственно особенностям строения подтипов тяжелых цепей различают и подклассы Ig.
В зависимости от особенностей молекулярного строения тяжелой цепи (т. е. наличия изотопических, или групповых антигенных детерминант) различают 5 классов, или изотипов Ig. Молекулы, содержащие тяжелую цепь α-типа, относят к изотипу А (сокращенно Ig. A); Ig. D обладает δ -цепью, Ig. E — ε-цепью, Ig. G — γ-цепью Ig. M — μ-цепью. Соответственно особенностям строения подтипов тяжелых цепей различают и подклассы Ig.

 Ig. G обеспечивает нейтрализацию, опсонизацию и маркирование антигена осуществляет запуск комплементопосредованного цитолиза И антителозависимой клеточно-опосредованной цитотоксичности.
Ig. G обеспечивает нейтрализацию, опсонизацию и маркирование антигена осуществляет запуск комплементопосредованного цитолиза И антителозависимой клеточно-опосредованной цитотоксичности.

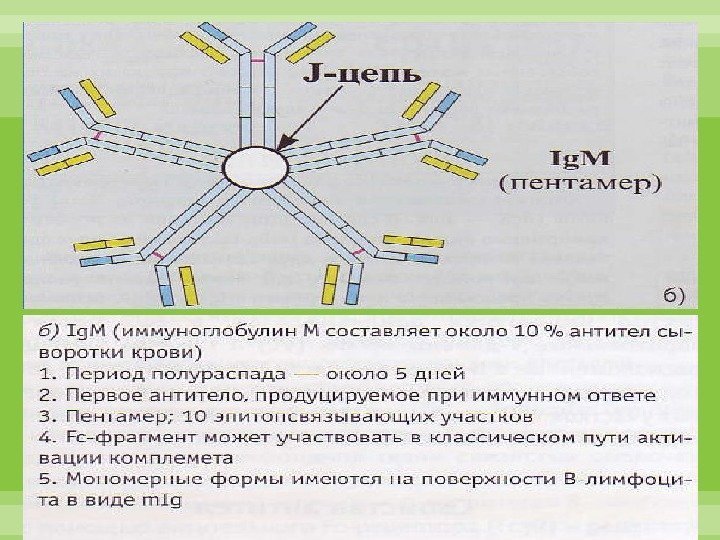
 Ig. M не проходит через плаценту. Обнаружение специфических антител изотипа М в сыворотке крови новорожденного указывает на бывшую внутриутробную инфекцию или дефект плаценты. Ig. M обеспечивает нейтрализацию, опсонизацию и маркирование антигена, осуществляет запуск комплемент-опосредованного цитолиза и антителозависимой клеточноопосредованной цитотоксичности.
Ig. M не проходит через плаценту. Обнаружение специфических антител изотипа М в сыворотке крови новорожденного указывает на бывшую внутриутробную инфекцию или дефект плаценты. Ig. M обеспечивает нейтрализацию, опсонизацию и маркирование антигена, осуществляет запуск комплемент-опосредованного цитолиза и антителозависимой клеточноопосредованной цитотоксичности.

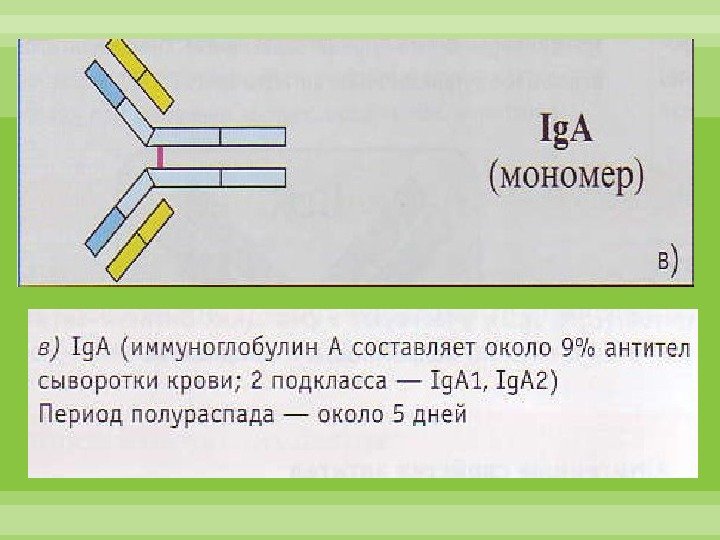
 Различают подтипы А 1 и А 2 Ig. A. Синтезируется зрелыми В-лимфоцитами (Вα ) и плазматическими клетками. Хорошо определяется в сыворотке крови на пике первичного и при вторичном иммунном ответе. Обладает высокой аффинностью. Может быть неполным антителом. Не связывает комплемент. Не проходит через плацентарный барьер. Ig. A обеспечивает нейтрализацию, опсонизацию и маркирование антигена, осуществляет запуск антителозависимой клеточно-опосредованной цитотоксичности.
Различают подтипы А 1 и А 2 Ig. A. Синтезируется зрелыми В-лимфоцитами (Вα ) и плазматическими клетками. Хорошо определяется в сыворотке крови на пике первичного и при вторичном иммунном ответе. Обладает высокой аффинностью. Может быть неполным антителом. Не связывает комплемент. Не проходит через плацентарный барьер. Ig. A обеспечивает нейтрализацию, опсонизацию и маркирование антигена, осуществляет запуск антителозависимой клеточно-опосредованной цитотоксичности.

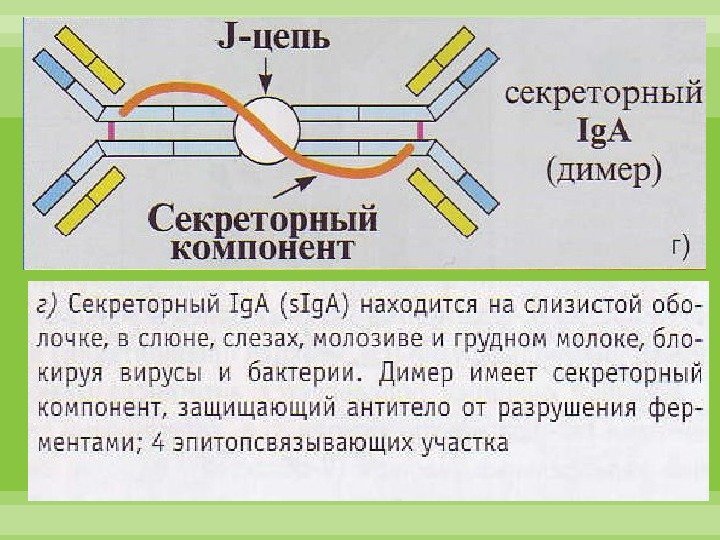
 Секреторная форма Ig. A — основной фактор специфического гуморального местного иммунитета слизистых оболочек желудочно-кишечного тракта, мочеполовой системы и респираторного тракта. Благодаря S -цепи он устойчив к действию протеаз. Ig. A не активирует комплемент, но эффективно связывается с антигенами и нейтрализует их. Он препятствует адгезии микробов на эпителиальных клетках и генерализации инфекции в пределах слизистых.
Секреторная форма Ig. A — основной фактор специфического гуморального местного иммунитета слизистых оболочек желудочно-кишечного тракта, мочеполовой системы и респираторного тракта. Благодаря S -цепи он устойчив к действию протеаз. Ig. A не активирует комплемент, но эффективно связывается с антигенами и нейтрализует их. Он препятствует адгезии микробов на эпителиальных клетках и генерализации инфекции в пределах слизистых.

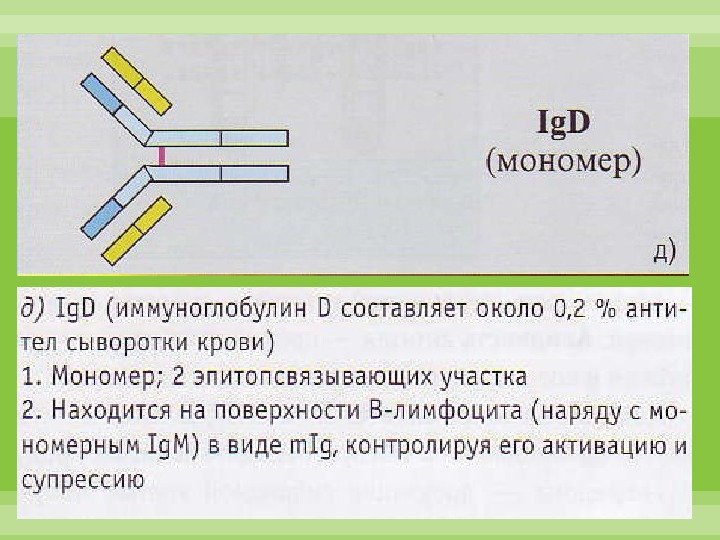
 Ig. D не связывает комплемент. Не проходит через плацентарный барьер. Является рецептором предшественников В-лимфоцитов.
Ig. D не связывает комплемент. Не проходит через плацентарный барьер. Является рецептором предшественников В-лимфоцитов.

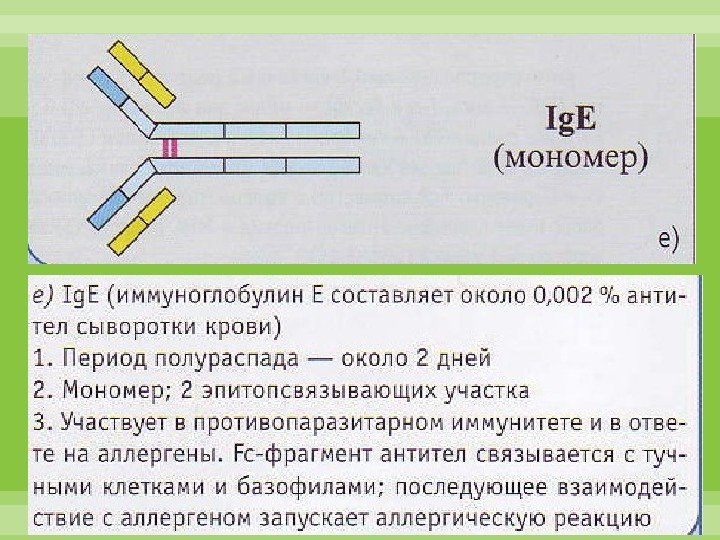
 Ig Е синтезируется зрелыми В-лимфоцитами (Вε ) и плазматическими клетками преимущественно в лимфоидной ткани бронхолегочного дерева и ЖКТ. Не связывает комплемент. Не проходит через плацентарный барьер. Обладает выраженной цитофильностью — тропностью к тучным клеткам и базофилам. Участвует в развитии гиперчувствительности немедленного типа — реакция I типа
Ig Е синтезируется зрелыми В-лимфоцитами (Вε ) и плазматическими клетками преимущественно в лимфоидной ткани бронхолегочного дерева и ЖКТ. Не связывает комплемент. Не проходит через плацентарный барьер. Обладает выраженной цитофильностью — тропностью к тучным клеткам и базофилам. Участвует в развитии гиперчувствительности немедленного типа — реакция I типа
 Рецепторные, или мембраные Ig , локализуются на цитоплазматической мембране В-лимфоцитов. Выполняют функции антигенспецифических рецепторов. Рецепторные Ig имеют те же изотип и специфичность, что и синтезируемые в межклеточную среду антитела. Структурное отличие от секретируемых антител заключается в особом, дополнительном М-пептиде, благодаря которому молекула рецепторного Ig фиксируется в цитоплазматической мембране иммунокомпетентной клетки.
Рецепторные, или мембраные Ig , локализуются на цитоплазматической мембране В-лимфоцитов. Выполняют функции антигенспецифических рецепторов. Рецепторные Ig имеют те же изотип и специфичность, что и синтезируемые в межклеточную среду антитела. Структурное отличие от секретируемых антител заключается в особом, дополнительном М-пептиде, благодаря которому молекула рецепторного Ig фиксируется в цитоплазматической мембране иммунокомпетентной клетки.
 Иммуноглобулин, как и всякий белок, обладает антигеностью и выраженной иммуногенностью. В молекуле Ig различают 4 типа атигенных детерминант: видовые, изотипические, идиотипические, аллотипические.
Иммуноглобулин, как и всякий белок, обладает антигеностью и выраженной иммуногенностью. В молекуле Ig различают 4 типа атигенных детерминант: видовые, изотипические, идиотипические, аллотипические.
 Видовые антигенные детерминанты характерны для Ig всех особей данного вида (например, кролика, собаки, человека). Они определяются строением легкой и тяжелой цепи. По этим детерминантам можно идентифицировать видовую принадлежность антител.
Видовые антигенные детерминанты характерны для Ig всех особей данного вида (например, кролика, собаки, человека). Они определяются строением легкой и тяжелой цепи. По этим детерминантам можно идентифицировать видовую принадлежность антител.
 Изотипические антигенные детерминанты являются групповыми. Они локализуются в тяжелой цепи и служат для дифференцировки семейства Ig на 5 изотипов (классов) и множество подклассов
Изотипические антигенные детерминанты являются групповыми. Они локализуются в тяжелой цепи и служат для дифференцировки семейства Ig на 5 изотипов (классов) и множество подклассов
 Аллотипические антигенные детерминанты являются индивидуальными, т. е. присущими конкретному организму. Они располагаются в легкой и тяжелой полипептидных цепях. На основании строения аллотипических детерминант можно различать особи внутри одного вида.
Аллотипические антигенные детерминанты являются индивидуальными, т. е. присущими конкретному организму. Они располагаются в легкой и тяжелой полипептидных цепях. На основании строения аллотипических детерминант можно различать особи внутри одного вида.
 Идиотипические антигеннные детерминанты отражают особенности строения антигенсвязывающего центра самой молекулы Ig. Они образованы V -доменами легкой и тяжелой цепи молекулы Ig. Обнаружение идиотипических антигенных детерминант послужило основанием для создания теории «идиотип-антиидиотипической» регуляции биосинтеза антител.
Идиотипические антигеннные детерминанты отражают особенности строения антигенсвязывающего центра самой молекулы Ig. Они образованы V -доменами легкой и тяжелой цепи молекулы Ig. Обнаружение идиотипических антигенных детерминант послужило основанием для создания теории «идиотип-антиидиотипической» регуляции биосинтеза антител.
 В процессе взаимодействия с антигеном принимает участие не вся молекула Ig , а лишь ее ограниченный участок — антигенсвязывающий центр, или паратоп , который локализован в Fab -фрагменте молекулы Ig. Co своей стороны, антитело взаимодействует не со всей молекулой антигена сразу, а лишь с ее антигенной детерминантой.
В процессе взаимодействия с антигеном принимает участие не вся молекула Ig , а лишь ее ограниченный участок — антигенсвязывающий центр, или паратоп , который локализован в Fab -фрагменте молекулы Ig. Co своей стороны, антитело взаимодействует не со всей молекулой антигена сразу, а лишь с ее антигенной детерминантой.
 Антитела отличает специфичность взаимодействия , т. е. способность связываться со строго определенной антигенной детерминантой. Наиболее доступные для взаимодействия эпитопы располагаются на поверхности молекулы антигена.
Антитела отличает специфичность взаимодействия , т. е. способность связываться со строго определенной антигенной детерминантой. Наиболее доступные для взаимодействия эпитопы располагаются на поверхности молекулы антигена.
 Связь антигена с антителом осуществляется за счет слабых взаимодействий (Ван-дер-ваальсовы силы, водородные связи, электростатические взаимодействия) в пределах антигенсвязывающего центра. Такая связь отличается неустойчивостью — образовавшийся иммунный комплекс (ИК) может легко диссоциировать на составляющие его компоненты. Поэтому взаимодействие антигена и антитела может быть представлено в виде уравнения: [ A Г] + [ AT ] [ИК].
Связь антигена с антителом осуществляется за счет слабых взаимодействий (Ван-дер-ваальсовы силы, водородные связи, электростатические взаимодействия) в пределах антигенсвязывающего центра. Такая связь отличается неустойчивостью — образовавшийся иммунный комплекс (ИК) может легко диссоциировать на составляющие его компоненты. Поэтому взаимодействие антигена и антитела может быть представлено в виде уравнения: [ A Г] + [ AT ] [ИК].
 Продолжительность существования иммунного комплекса определяется целым рядом факторов. При этом важное значение имеют особенности антитела, антигена и условия, в которых происходит их взаимодействие. К особенностям антитела следует отнести его аффинность и авидность.
Продолжительность существования иммунного комплекса определяется целым рядом факторов. При этом важное значение имеют особенности антитела, антигена и условия, в которых происходит их взаимодействие. К особенностям антитела следует отнести его аффинность и авидность.
 Аффинность — сила специфического взаимодействия антитела с антигеном (или энергия их связи). Эта характеристика зависит от степени стерического, или пространственного, соответствия (комплементарности) структуры антигенсвязывающего центра и антигенной детерминанты. Чем выше их комплементарность, т. е. чем больше они подходят другу, тем больше образуется межмолекулярных связей и тем выше будет устойчивость и продолжительность жизни образовавшегося иммунного комплекса.
Аффинность — сила специфического взаимодействия антитела с антигеном (или энергия их связи). Эта характеристика зависит от степени стерического, или пространственного, соответствия (комплементарности) структуры антигенсвязывающего центра и антигенной детерминанты. Чем выше их комплементарность, т. е. чем больше они подходят другу, тем больше образуется межмолекулярных связей и тем выше будет устойчивость и продолжительность жизни образовавшегося иммунного комплекса.
 Структурные несоответствия антигенсвязывающего центра и антигенной детерминанты существенно снижают число образующихся связей и прочность взаимодействия антитела с антигеном. Иммунный комплекс, образованный низкоаффинными антителами, чрезвычайно неустойчив, имеет малую продолжительность существования и быстро распадается на исходные компоненты.
Структурные несоответствия антигенсвязывающего центра и антигенной детерминанты существенно снижают число образующихся связей и прочность взаимодействия антитела с антигеном. Иммунный комплекс, образованный низкоаффинными антителами, чрезвычайно неустойчив, имеет малую продолжительность существования и быстро распадается на исходные компоненты.
 Под термином «авидность» понимают прочность связывания антитела и антигена. Эта характеристика определяется аффинностью Ig и числом антигенсвязывающих центров. При равной степени аффинности наибольшей авидностью обладают антитела класса М , так как они имеют 10 антигенсвязывающих центров.
Под термином «авидность» понимают прочность связывания антитела и антигена. Эта характеристика определяется аффинностью Ig и числом антигенсвязывающих центров. При равной степени аффинности наибольшей авидностью обладают антитела класса М , так как они имеют 10 антигенсвязывающих центров.
 Особенности антигена также влияют на эффективность его взаимодействия с антителом. Важное значение имеют стерическая (пространственная) доступность антигенной детерминанты для антигенсвязывающего центра молекулы Ig и число эпитопов в составе молекулы антигена.
Особенности антигена также влияют на эффективность его взаимодействия с антителом. Важное значение имеют стерическая (пространственная) доступность антигенной детерминанты для антигенсвязывающего центра молекулы Ig и число эпитопов в составе молекулы антигена.
 Эффективность взаимодействия антитела с антигеном существенно зависит от условий, в которых происходит реакция, и прежде всего от р. Н среды, осмотической плотности, солевого состава и температуры среды. Оптимальными для реакции антиген—антитело являются физиологические условия внутренней среды макроорганизма: близкая к нейтральной реакция среды, присутствие фосфат-, карбонат-, хлорид- и ацетат-ионов, осмолярность физиологического раствора (концентрация раствора 0, 15 М), а также температура (36— 37 °С).
Эффективность взаимодействия антитела с антигеном существенно зависит от условий, в которых происходит реакция, и прежде всего от р. Н среды, осмотической плотности, солевого состава и температуры среды. Оптимальными для реакции антиген—антитело являются физиологические условия внутренней среды макроорганизма: близкая к нейтральной реакция среды, присутствие фосфат-, карбонат-, хлорид- и ацетат-ионов, осмолярность физиологического раствора (концентрация раствора 0, 15 М), а также температура (36— 37 °С).


